Биология внутренних вод, 2019, № 1, стр. 100-104
Нарушение синхронного развития ооцитов леща Abramis brama L. Рыбинского водохранилища
А. В. Герман *
Институт биологии внутренних вод им. И.Д. Папанина РАН
152742 Ярославская обл., Некоузский р-н, пос. Борок, Россия
* E-mail: gera@ibiw.yaroslavl.ru
Поступила в редакцию 28.04.2017
После доработки 07.12.2017
Принята к публикации 19.07.2017
Аннотация
Изучена сезонная динамика размеров ооцитов леща. У части особей в выборке асинхронность развития ооцитов приводит к формированию второй порции икры. Динамика формирования второй порции ооцитов, сильная вариабельность их количества и доли от общего числа ооцитов, резорбция после вымета первой порции икры отличаются от типичного асинхронного развития ооцитов у видов с порционным икрометанием. Повторный нерест леща в настоящее время маловероятен.
Изменение типа икрометания в зависимости от условий существования популяций служит одним из наиболее интересных примеров адаптации рыб. Для популяции леща Abramis brama L. южных водоемов характерно асинхронное развитие ооцитов и порционное икрометание. В Рыбинском водохранилище этот вид нерестится единовременно. Вместе с тем, потенциальная способность леща к формированию двух порций икры сохранилась. В 1950-е годы XX в. отмечено наличие у некоторых особей в преднерестовый период двух порций ооцитов [4, 5]. В середине 1970-х годов XX в. самки с признаками порционного икрометания в нерестовом стаде леща отсутствовали [1, 2]. В 1991 г. В.В. Халько и М.Г. Таликина [7] наблюдали в преднерестовый период наличие в гонадах ооцитов, отстающих в росте. Доля рыб с ооцитами в фазе вакуолизации и первоначального накопления желтка была в среднем 52% от общего количества исследованных рыб. Показано [3], что увеличение плодовитости леща в 2011–2014 гг. сопровождалось не только повышением темпа роста рыб, но и увеличением доли самок с асинхронным развитием ооцитов до 80% от их общего числа.
Цель работы – исследовать динамику диаметра ооцитов леща Рыбинского водохранилища в период трофоплазматического роста и оценить вероятность изменения типа икрометания в условиях продолжающегося потепления климата.
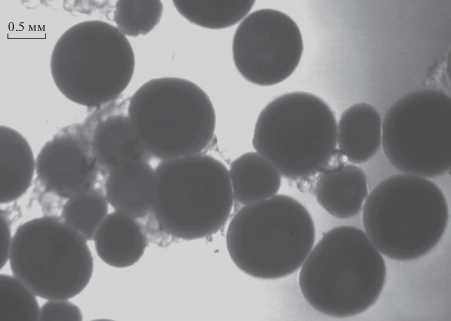
Материал собирали в 2011–2014 гг. в Волжском плесе Рыбинского водохранилища. Оогенез леща изучали в июне–августе 2012 г., сентябре–ноябре 2011–2012 гг., декабре–феврале 2013–2014 гг. и марте–мае 2011–2014 гг. Фрагменты свежих гонад препарировали в физиологическом растворе. Тотальные препараты помещали под бинокуляр и фотографировали. Диаметр ооцита определяли по фотографиям тотальных препаратов как среднее между наибольшим и наименьшим диаметром с помощью программы Image Tool. Средний диаметр и коэффициент асимметрии (КА) для вариационных рядов вычисляли на основе измерений ≥50 ооцитов каждой особи, с помощью пакета программ Statistica. Усредненные данные для нескольких рыб из выборки до разделения ооцитов на порции (июль–сентябрь) и после обособления ооцитов, отстающих в росте (октябрь–май), приведены в табл. 1. Всего сделано 749 фотографий, измерено 6995 ооцитов. Долю отстающих в росте ооцитов от их общего числа определяли одновременно с плодовитостью [3]. Исследованы гонады 210 рыб с длиной тела 300–491 мм.
Таблица 1.
Диаметр ооцитов леща Рыбинского водохранилища в период трофоплазматического роста (2011–2014 гг.)
| Месяц | Тип развития ооцитов | Число рыб | n | Диаметр ооцитов, мм | |
|---|---|---|---|---|---|
| 1-я порция | 2-я порция | ||||
| Июль | Синхронный | 3 | 329 | $\frac{{0.34{\kern 1pt} - {\kern 1pt} 0.82}}{{0.51 \pm 0.08}}$ | – |
| Август | Синхронный | 5 | 553 | $\frac{{0.38{\kern 1pt} - {\kern 1pt} 1.00}}{{0.80 \pm 0.12}}$ | – |
| Сентябрь | Синхронный | 7 | 902 | $\frac{{0.44{\kern 1pt} - {\kern 1pt} 1.24}}{{0.92 \pm 0.11}}$ | – |
| Октябрь | Синхронный | 2 | 207 | $\frac{{0.89{\kern 1pt} - {\kern 1pt} 1.23}}{{1.10 \pm 0.06}}$ | – |
| Асинхронный | 3 | 509 | $\frac{{0.98{\kern 1pt} - {\kern 1pt} 1.26}}{{1.12 \pm 0.05}}$ | $\frac{{0.40{\kern 1pt} - {\kern 1pt} 0.97}}{{0.75 \pm 0.12}}$ | |
| Декабрь | Синхронный | 8 | 638 | $\frac{{0.92{\kern 1pt} - {\kern 1pt} 1.25}}{{1.12 \pm 0.06}}$ | – |
| Асинхронный | 7 | 608 | $\frac{{0.90{\kern 1pt} - {\kern 1pt} 1.35}}{{1.08 \pm 0.08}}$ | $\frac{{0.53{\kern 1pt} - {\kern 1pt} 0.89}}{{0.69 \pm 0.08}}$ | |
| Январь | Асинхронный | 8 | 689 | $\frac{{1.05{\kern 1pt} - {\kern 1pt} 1.36}}{{1.19 \pm 0.05}}$ | $\frac{{0.43{\kern 1pt} - {\kern 1pt} 0.88}}{{0.73 \pm 0.08}}$ |
| Февраль | Синхронный | 4 | 313 | $\frac{{0.97{\kern 1pt} - {\kern 1pt} 1.59}}{{1.15 \pm 0.08}}$ | – |
| Асинхронный | 7 | 579 | $\frac{{0.98{\kern 1pt} - {\kern 1pt} 1.78}}{{1.18 \pm 0.06}}$ | $\frac{{0.49{\kern 1pt} - {\kern 1pt} 0.89}}{{0.73 \pm 0.07}}$ | |
| Апрель | Синхронный | 6 | 379 | $\frac{{1.05{\kern 1pt} - {\kern 1pt} 1.42}}{{1.23 \pm 0.06}}$ | – |
| Асинхронный | 4 | 304 | $\frac{{1.10{\kern 1pt} - {\kern 1pt} 1.49}}{{1.27 \pm 0.06}}$ | $\frac{{0.50{\kern 1pt} - {\kern 1pt} 0.88}}{{0.72 \pm 0.08}}$ | |
| Май | Синхронный | 4 | 254 | $\frac{{1.20{\kern 1pt} - {\kern 1pt} 1.50}}{{1.32 \pm 0.04}}$ | – |
| Асинхронный | 7 | 493 | $\frac{{1.11{\kern 1pt} - {\kern 1pt} 1.50}}{{1.29 \pm 0.09}}$ | $\frac{{0.46{\kern 1pt} - {\kern 1pt} 1.08}}{{0.69 \pm 0.07}}$ | |
| Синхронный, овуляция | 1 | 58 | $\frac{{1.47{\kern 1pt} --{\kern 1pt} 1.68}}{{1.56 \pm 0.05}}$ | – | |
| Асинхронный, овуляция | 1 | 74 | $\frac{{1.42{\kern 1pt} --{\kern 1pt} 1.71}}{{1.53 \pm 0.07}}$ | $\frac{{0.62{\kern 1pt} --{\kern 1pt} 1.04}}{{0.89 \pm 0.09}}$ | |
| Асинхронный, VI–II стадии | 2 | 106 | – | $\frac{{0.69{\kern 1pt} --{\kern 1pt} 1.11}}{{0.94 \pm 0.07}}$ | |
Начало трофоплазматического периода роста ооцитов у леща приходилось на июль. К третьей декаде месяца средний диаметр ооцитов колебался от 0.34 до 0.82 мм (см. табл. 1). Различия в диаметре обусловлены неодновременным переходом протоплазматических ооцитов в фазу вакуолизации, вследствие чего наименьшие ооциты лишь незначительно превышали размер ооцитов фазы VI протоплазматического роста по А.М. Андреевой [1]. КА варьировал от –0.37 до –0.76. В конце августа различия по диаметру ооцитов увеличивались более чем в 2 раза, КА варьировал от –1.39 до –2.1. Часть ооцитов перешла в фазу первичного накопления желтка, а отстающие в росте ооциты находились в фазе вакуолизации. В сентябре КА варьировал от –0.4 до –2.86. Минимальный и максимальный диаметры ооцитов отдельных особей различались на 0.22–0.64 мм. На фоне роста среднего диаметра ооцитов выделялась группа рыб, у которой вариабельность размеров ооцитов уменьшалась, отрицательная асимметрия вариационной кривой ослабевала. В декабре различия между минимальным и максимальным диаметром ооцитов у рыб из этой группы были 0.15–0.27 мм, КА варьировал ‒1.03…‒ 0.32. В феврале верхняя граница диаметра ооцитов превышала таковую в апреле. Возможно, небольшая часть ооцитов в этот период переходила в V стадию зрелости, что приводило к увеличению коэффициента асимметрии до 2.46. В дальнейшем такие “перезревшие” ооциты резорбировались. В апреле–мае КА колебался от –0.41 до 0.36. В период нереста созревшие ооциты выметывались полностью, в гонадах отнерестившихся рыб присутствовали ооциты в различных фазах протоплазматического роста и единичные гидратированные ооциты. Таким образом, по характеру изменения вариационной кривой распределения диаметра ооцитов в период трофоплазматического роста и по посленерестовому состоянию гонад эта группа рыб полностью соответствовала рыбам с синхронным развитием ооцитов и единовременным икрометанием.
Часть рыб составила группу, у которой в сентябре увеличение среднего диаметра ооцитов не сопровождалось снижением вариабельности размеров ооцитов, отрицательная асимметрия вариационной кривой сохранялась высокой. В октябре вариационная кривая распределения приобрела двухвершинный характер. К декабрю между отстающими в росте ооцитами и их основным количеством образовался устойчивый хиатус (рис. 1). Различия между минимальным и максимальным диаметром ооцитов были 0.50–0.69 мм, КА ооцитов первой порции варьировал от –0.51 до 0.52 (рис. 2). В течение зимы происходило дозревание ооцитов первой порции, их диаметр увеличивался в среднем от 1.08 до 1.18 мм, в то время как ооциты второй порции не развивались. Во время нереста ооциты, достигшие размеров >1.3 мм, выметывались. Ооциты второй порции оставались в гонадах. Их диаметр увеличивался в среднем до 0.96 мм, что указывало на вступление в фазу первичного накопления желтка. В течение нескольких суток после нереста развитие этих ооцитов останавливалось, и они подвергались резорбции. Таким образом, формирование второй порции икры происходило из ооцитов, перешедших в июле в фазу вакуолизации. Задержка развития части ооцитов на III стадии трофоплазматического роста характерна для видов с асинхронным развитием ооцитов и потенциально порционным икрометанием. У видов с синхронным развитием, например, у плотвы Rutilus rutilus (L.), ооциты на III и IV стадиях развития одновременно присутствуют в гонадах относительно небольшой период времени (конец августа–начало сентября).
Рис. 2.
Гистограмма распределения ооцитов леща (%) по их диаметру (Рыбинское водохранилище, декабрь 2014 г.).
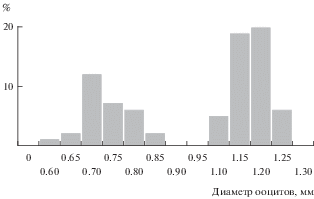
Вместе с тем, обособление двух порций ооцитов у леща происходит уже в октябре–декабре, в то время как у густеры Blicca bjoerkna (L.), всегда формирующего несколько порций икры, хиатус в вариационной кривой распределения появляется только на заключительной стадии созревания в апреле–мае.
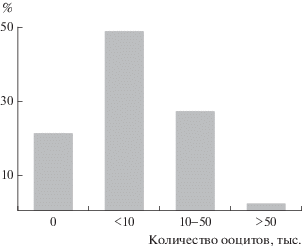
Другим существенным отличием от типичного асинхронного развития служит наличие доли ооцитов второй порции от общего числа ооцитов. У леща из р. Дон, нерестившегося порционно, эта доля составила ≥30% [6], однако, у леща из Рыбинского водохранилища доля второй порции ооцитов не превышала 20% у особей с максимально выраженной асинхронностью и, как правило, была значительно меньше. Количество ооцитов второй порции лишь у 2% всех исследованных самок превышает 50 тыс. (рис. 3), в то время как у донского леща с порционным типом метания икры этот показатель достигает 60 тыс. [6].
Рис. 3.
Гистограмма распределения рыб с разным количеством ооцитов второй порции икры (декабрь–май, 2011–2014 гг.).
Полученные данные не позволяют в настоящее время подтвердить ни предположение Л.А. Леви [4] об асинхронном развитии ооцитов как свидетельстве перехода леща от единовременного икрометания к порционному, ни заключение В.В. Халько и М.Г. Таликиной [7] о дозревании отстающих в росте ооцитов на заключительной стадии оогенеза. Динамика формирования второй порции ооцитов, сильная вариабельность их количества и доли от общего числа ооцитов, резорбция после вымета первой порции икры отражают, по мнению автора, различную степень нарушения синхронного развития ооцитов у леща Рыбинского водохранилища. Потепление климата, по-видимому, усиливает нарушение синхронного развития ооцитов, вызванное первоначально изменением гидрологического режима при создании водохранилища. Аналогичные нарушения, хотя и у значительно меньшего количества особей, встречаются, по наблюдениям автора, у плотвы из Рыбинского водохранилища.
Выводы. Развитие ооцитов леща в период трофоплазматического роста у значительной части особей происходит асинхронно. Наблюдаются признаки формирования второй порции икры и ее неполного созревания и резорбции. Повторный нерест леща в настоящее время маловероятен.
Работа выполнена в рамках государственного задания по теме № г/р АААА-А18-118012690104-3.
Список литературы
Андреева А.М. Оогенез леща Abramis brama (L.) (Cyprinidae) Рыбинского водохранилища // Вопр. ихтиологии. 1983. Т. 23. Вып. 2. С. 257–261.
Володин В.М. Плодовитость леща Abramis brama (L.) (Cyprinidae) Рыбинского водохранилища // Вопр. ихтиологии. 1982. Т. 22. Вып. 2. С. 246–252.
Герман А.В. Темп полового созревания и плодовитость леща Abramis brama Волжского плеса Рыбинского водохранилища // Рыбоводство и рыб. хоз-во. 2016. № 8. С. 17–23.
Леви Л.А. О некоторых особенностях полового цикла леща Рыбинского водохранилища // Изв. Всесоюз. НИИ озер. и реч. рыб. хоз-ва. 1953. Т. 33. С. 62–71.
Сергеев Р.С., Пермитин Ю.Е., Ястребков А.А. О плодовитости рыб Рыбинского водохранилища // Тр. биол. ст. Борок. 1955. Вып. 2. С. 278–300.
Сыроватская Н.И. О типе икрометания донского леща // Докл. АН СССР. 1949. Т. 66. № 5. С. 1001–1004.
Халько В.В., Таликина М.Г. Сравнительная характеристика преднерестового состояния гонад репродуктивных изолятов фитофильных рыб Рыбинского водохранилища // Вопр. ихтиологии. 1993. Т. 33. № 2. С. 241–247.
Дополнительные материалы отсутствуют.
Инструменты
Биология внутренних вод