Доклады Российской академии наук. Химия, науки о материалах , 2020, T. 492-493, № 1, стр. 138-142
Текстурные характеристики органических и углеродных аэрогелей, полученных при различных параметрах синтеза резорцин-формальдегидных гелей-прекурсоров
И. В. Эльманович 1, *, М. С. Рубина 2, С. С. Абрамчук 2
1 Институт элементоорганических соединений
им. А.Н. Несмеянова Российской академии наук
Москва, Россия
2 Московский государственный университет
имени М.В. Ломоносова, физический факультет
Москва, Россия
* E-mail: elmanovich@polly.phys.msu.ru
Поступила в редакцию 14.04.2020
После доработки 25.05.2020
Принята к публикации 11.06.2020
Аннотация
В работе исследован классический подход к получению углеродных аэрогелей путем пиролиза органических резорцин-формальдегидных аэрогелей. Получены органические аэрогели с плотностью до 0.17 г/см3 и удельной поверхностью до 632 м2/г. Соответствующие углеродные аэрогели имели плотность до 0.20 г/см3, при этом их удельная поверхность достигала 757 м2/г. Продемонстрировано влияние важных синтетических параметров – концентрации катализатора и времени созревания геля-прекурсора – на особенности пористой структуры и значение удельной поверхности. Впервые детально исследовано такое влияние на распределение по размерам мезо- и микропор.
Углеродные аэрогели (УА) представляют собой трехмерную монолитную пористую структуру, сформированную, полностью или частично, углеродной фазой. Уникальные свойства, присущие всем аэрогелям как классу материалов, такие как высокая пористость, большие значения удельной поверхности, низкая плотность и т.д., сочетаются в УА с электропроводностью и механической устойчивостью, что значительно расширяет сферу их возможного применения. УА рассматриваются как потенциально эффективные адсорбенты, термоизоляционные среды, материалы для электрических и электрохимических приложений [1, 2].
Впервые УА были получены пиролизом органических аэрогелей, сформированных по методике, предложенной в научной группе профессора Pekala [3, 4]. В основе методики получения органического геля лежит реакция поликонденсации резорцина с формальдегидом в щелочной среде, которую создают добавлением катализатора – карбоната натрия. Взаимодействие между компонентами происходит в два основных этапа: нуклеофильное присоединение формальдегида в ароматическое кольцо с образованием метилольных производных резорцина и последующая конденсация этих производных с образованием, преимущественно, метиленовых мостиков [5]. В результате целого каскада реакций образуются разветвленные резорцин-формальдегидные олигомеры, которые дают начало пространственной сетке органогеля. Нагревание реакционной смеси способствует процессам отверждения.
Замена растворителя и сверхкритическая сушка органогеля приводят к формированию органического аэрогеля (ОА), который затем трансформируется в УА в результате пиролиза в инертной атмосфере. Полученный таким образом УА состоит из переплетенных наноструктур аморфного углерода, которые образуют мезо- и микропористую архитектуру материала.
Несмотря на то, что значительная часть современных исследований посвящена поиску путей синтеза углеродных аэрогелей на основе других аллотропных форм углерода – главным образом графена [6] и углеродных нанотрубок [7], – представленная профессором Pekala схема синтеза УА остается актуальной и на сегодняшний день [8–10].
В настоящей работе предлагается исследование некоторых морфологических особенностей и текстурных свойств органических и углеродных аэрогелей, полученных при разных параметрах синтеза резорцин-формальдегидных гелей-прекурсоров. Для достижения цели в работе была синтезирована серия ОА по методике, основанной на классической работе [3], в которой исследовали аэрогели, полученные при разных значениях загрузки катализатора и времени созревания органического геля в маточном растворе. При выборе времен созревания ориентировались на границы диапазона этого параметра, используемого в большинстве работ по получению аэрогелей. Для концентрации (при выборе количества) катализатора использовали значения, близкие к крайним точкам, приведенным в оригинальной работе Pekala [3]. Условия синтеза всех типов полученных органических аэрогелей приведены в табл. 1.
Таблица 1.
Данные о загрузках реагентов и времени созревания для образцов гелей, полученных в настоящей работе
| Тип аэрогеля | Соотношения компонентов, ммоль | Время созревания | ||
|---|---|---|---|---|
| Резорцин | Формальдегид | Карбонат натрия | ||
| OA_5_1 | 15 | 29 | 0.12 | 2 суток |
| OA_5_1_w | 15 | 29 | 0.12 | 1 неделя |
| OA_5_3 | 15 | 29 | 0.06 | 2 суток |
| OA_5_3_w | 15 | 29 | 0.06 | 1 неделя |
Все представленные в таблице типы аэрогелей были пиролизованы в высоком вакууме (давление менее 1 × 10–4 мбар) при температуре 800°С с образованием углеродных аэрогелей (в соответствующих шифрах образцов для углеродных аэрогелей буквы OA заменены на УA).
ОА представляли собой монолитные цилиндры темно-красного цвета, опалесцирующие по краям. УА представляли собой черные монолитные цилиндры. Цилиндрическая форма повторяла форму сосуда, в котором проводился процесс гелеобразования. Ни на одном из этапов приготовления аэрогелей не наблюдалось коллапса исходной трехмерной структуры геля. После проведения процедуры сверхкритической сушки наибольшим объемом (и, соответственно, наименьшей степенью усадки) обладал органический аэрогель, полученный с использованием наименьшего количества катализатора и с большим временем созревания, а также полученный его пиролизом углеродный аэрогель. Плотность такого ОА составляла около 0.17 г/см3, соответствующего УА – 0.20 г/см3.
Особенности микроструктуры полученных гелей были исследованы методом ПЭМ. Изображения образцов OA_5_1, OA_5_1_w, УA_5_1, УA_5_1_w, отличающихся различным временем созревания органического геля, представлены на рис. 1. Для всех перечисленных образцов материал представлял собой агломераты частиц с размерами от 5 до 8 нм. На ПЭМ изображениях не прослеживается ярко выраженных изменений при сравнении ОА, полученных из органических гелей с разным временем созревания. При переходе от ОА к УА наблюдается некоторое изменение морфологии агрегатов в сторону более пористой, “рыхлой” структуры.
Рис. 1.
Типичные ПЭМ изображения органических аэрогелей, сформированных при разных временах созревания и углеродных аэрогелей, полученных в результате пиролиза.

Более существенной оказывается разница в микроструктуре материала при сравнении аэрогелей, полученных с разными загрузками катализатора. На рис. 2 приведены соответствующие микрофотографии ПЭМ. Видно, что в случае большей концентрации катализатора (левое изображение на рис. 3) повышается склонность частиц аэрогеля к агломерации (представленные на рисунках типичные изображения репрезентативны и отражают тенденцию, наблюдаемую для набранной статистики подобных микрофотографий). Напротив, для аэрогеля, сформированного при меньшей загрузке катализатора, характерным оказывается более разряженная пористая микроструктура, в которой отдельные частицы образуют “нити”, или “тяжи” (правое изображение на рис. 2).
Рис. 3.
Изотермы низкотемпературной адсорбции азота для резорцин-формальдегидных УА и ОА. Слева – количество катализатора 0.12 ммоль; справа – количество катализатора 0.06 ммоль.
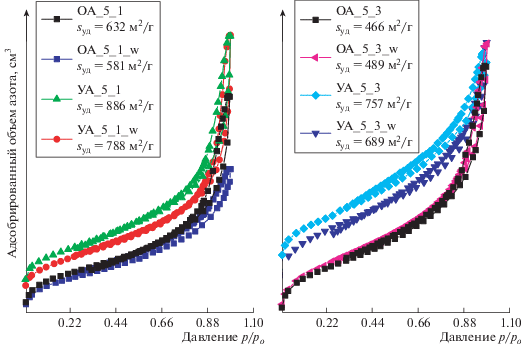
Текстурные свойства полученных органических и углеродных резорцин-формальдегидных аэрогелей были исследованы методом низкотемпературной адсорбции азота (соответствующие изотермы представлены на рис. 3). Вид изотерм адсорбции для всех исследованных образцов указывает на мезопористый характер структуры как ОА, так и УА. Наличие изгиба на начальном участке изотерм говорит о наличии микропор в материалах.
Согласно модели БЭТ была рассчитана удельная площадь поверхности, которая составила более 500 м2/г для ОА и более 700 м2/г для УА (для сравнения, удельная поверхность активированного угля, как правило, колеблется в диапазоне от 500 до 1500 м2/г [11]). Видно, что при переходе от ОА к УА наблюдается рост значения удельной поверхности для всех четырех исследованных образцов. Помимо этого, для УА значения удельной площади поверхности уменьшаются при увеличении времени созревания. Наконец, уже отмеченная нами разница в микроструктуре образцов ОА_5_1 и ОА_5_3 сопровождается соответству- ющим изменением удельной поверхности – она составляет 632 м2/г и 466 м2/г соответственно.
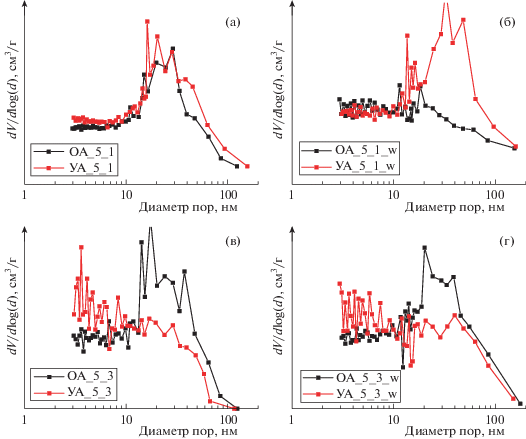
Согласно модели БДХ были рассчитаны распределения пор по размерам в материалах. Для аэрогелей, полученных при меньшей загрузке катализатора, общий вид распределения пор по размерам оказывается схожим для ОА и УА при меньших временах созревания (рис. 4а) и различается для случая с большим временем созревания (рис. 4б). При переходе от ОА к УА для случая с большей концентрацией катализатора наблюдаются существенные изменения для распределения пор по размерам (рис. 4в, 4г) – при переходе от ОА к УА значительно увеличивается количество пор с размерами до 10 нм, средний размер пор для УА в этом случае составляет около 2–3 нм. При созревании в маточном растворе наблюдается общая тенденция к уменьшению доли крупных пор и возрастанию доли мелких пор независимо от концентрации катализатора.
Рис. 4.
Сравнение распределения пор по размерам для УА и ОА, полученных при разном времени созревания органического геля (а и б, в и г) и при разной загрузке катализатора (а и в, б и г).
Таким образом, в работе проведено исследование некоторых морфологических особенностей и текстурных свойств органических и углеродных резорцин-формальдегидных аэрогелей, полученных при разной загрузке катализатора и времени созревания. Впервые обнаружено, что для случая низкой загрузки катализатора в реакции гелеобразования время созревания геля оказывает существенное влияние на распределение пор по размерам в ОА: увеличение времени созревания приводит к уменьшению среднего размера пор. Более ярко зависимость распределения пор по размерам выражена для УА в случае увеличения концентрации катализатора: средний размер пор смещается от значений 10–100 нм к 2–3 нм.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы. В работе использовали резорцин (чистота ≥98%) фирмы Acros Organics, водный раствор формальдегида (м. д. 37%, стабилизированный метанолом) фирмы Fisher Chemical, моногидрат карбоната натрия (чистота ≥99.5%) фирмы Merck.
Методика получения резорцин-формальдегидных органогелей. Резорцин (1.62 г) и карбонат натрия (8 или 15 мг) растворяли в 47.5 мл деионизованной воды при перемешивании в течение 10 мин; перемешивали до полного растворения компонентов смеси. В полученный раствор добавляли по каплям из шприца раствор формальдегида массой 881 мг и реакционную смесь перемешивали в течение часа. Далее раствор разливали в цилиндрические формы (шприцы объемом 10 мл) и термостатировали при температуре 70°С в течение 2 суток или недели. По прошествии времени созревания для каждого образца, указанного в табл. 1, была проведена замена растворителя на ацетон. Для этого гели помещали в избыток ацетона, причем эту операцию проводили несколько раз подряд для обеспечения полноты замены растворителя.
Методика сверхкритической экстракции растворителя. После проведения замены растворителя полученные органогели (гели в органическом растворителе) высушивали в сверхкритическом СО2. Сверхкритическую сушку проводили при давлении 200 атм., температуре 40°С, со скоростью потока СО2 через проточный реактор высокого давления, в который помещали органогели, 2 мл/мин. Сброс давления после 4 ч работы установки в проточном режиме проводили со скоростью 1 атм./мин. В результате были сформированы соответствующие резорцин-формальдегидные гели.
Методика получения углеродных аэрогелей. Все полученные в работе аэрогели были пиролизованы в вакумной печи Carbolite HTV 12/80/700 (Великобритания) при остаточном давлении в печи менее 1 × 10–4 мбар и температуре 800°С с образованием углеродных аэрогелей.
Методы. Исследования ПЭМ проводили на электронном микроскопе LEO 912 AB OMEGA (Carl Zeiss, Германия). Исследования пористой структуры методом анализа изотерм адсорбции/десорбции азота проводили с помощью прибора Quantochrome Nova Station A (США) при 77 K.
Список литературы
Chandrasekaran S., et al. Carbon aerogel evolution: Allotrope, graphene-inspired, and 3D-printed aerogels // J. Mater. Res. 2017. V. 32. № 22. P. 4166–4185.
Gan G., et al. Carbon Aerogels for Environmental Clean-Up // Eur. J. Inorg. Chem. 2019. V. 2019. № 27. P. 3126–3141.
Pekala R.W. Organic aerogels from the polycondensation of resorcinol with formaldehyde // J. Mater. Sci. 1989. V. 24. № 9. P. 3221–3227.
Fung A.W.P., et al. Characterization of carbon aerogels by transport measurements // J. Mater. Res. 1993. V. 8. № 8. P. 1875–1885.
Pekala R.W., Schaefer D.W. Structure of Organic Aerogels. 1. Morphology and Scaling // Macromolecules. 1993. V. 26. P. 5487–5493.
Kashyap S., Kabra S., Kandasubramanian B. Graphene aerogel-based phase changing composites for thermal energy storage systems // J. Mater. Sci. 2020. V. 55. № 10. P. 4127–4156.
Kharissova O.V., et al. All-Carbon Hybrid Aerogels: Synthesis, Properties, and Applications // Ind. Eng. Chem. Res. 2019. V. 58. № 36. P. 16258–16286.
Bong S., Han D. Mesopore-Controllable Carbon Aerogel and their Highly Loaded PtRu Anode Electrocatalyst for DMFC Applications // Electroanalysis. 2019. V. 32. № 1. P. 104–111.
Rodríguez N., et al. Effect of starch as binder in carbon aerogel and carbon xerogel preparation // J. Non. Cryst. Solids. 2019. V. 522. P. 119554.
Aghabararpour M., et al. Fabrication of binder-free electrode using reinforced resorcinol formaldehyde-based carbon aerogels // J. Nanopart. Res. 2019. V. 21. article no. 178.
Yin C.Y., Aroua M.K., Daud W.M.A.W. Review of modifications of activated carbon for enhancing contaminant uptakes from aqueous solutions // Sep. Purif. Technol. 2007. V. 52. № 3. P. 403–415.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах



