Доклады Российской академии наук. Химия, науки о материалах , 2020, T. 492-493, № 1, стр. 13-17
Экстракционные системы на основе N-винилформамида для извлечения и разделения циклических аминокислот
Н. Я. Мокшина 1, *, В. М. Шкинев 2, Г. В. Шаталов 3, О. А. Пахомова 4, член-корреспондент РАН Б. Я. Спиваков 2
1 Военно-воздушная академия им. проф. Н.Е. Жуковского и Ю.А. Гагарина
Воронеж, Россия
2 Институт геохимии и аналитической химии
им. В.И. Вернадского Российской академии наук
Москва, Россия
3 Воронежский государственный университет
Воронеж, Россия
4 Елецкий государственный университет
им. И.А. Бунина
Елец, Россия
* E-mail: moksnad@mail.ru
Поступила в редакцию 18.04.2020
После доработки 25.05.2020
Принята к публикации 10.06.2020
Аннотация
Для эффективного извлечения циклических аминокислот предложено использовать полимеры на основе N-винилформамида. В работе впервые приведены результаты экстракции фенилаланина, тирозина, гистидина и пролина в двухфазных системах на основе поли-N-винилформамида и сополимера N-винилформамида с N-винилимидазолом. Найдены системы с максимальной степенью извлечения индивидуальных аминокислот. Предложен механизм межмолекулярных взаимодействий в системах полимер–аминокислота. Приведены результаты экстракции смеси фенилаланина и тирозина сополимером N-винилформамида с N-винил-имидазолом. Предложен электрофоретический способ определения аминокислот в экстрактах.
Циклические аминокислоты играют важную роль в жизни человека и животных, поэтому требуется контроль их количественного содержания в окружающей среде, продуктах питания, в фармацевтических препаратах и других продуктах, используемых в медицине. Для их концентрирования, при малом содержании в объектах анализа, часто используются системы на основе водорастворимых полимеров, например, поли-N-пирролидоны [1], полиэтиленгликоли [2]. В последнее время для увеличения эффективности таких систем в них вводят ионные жидкости [3–5]. Однако, это усложняет и удорожает методы разделения и очистки аминокислот.
Альтернативой для данных систем могут быть новые водорастворимые и нетоксичные гомо- и сополимеры N-виниламидов, и прежде всего такие как поли-N-винилпирролидон, поли-N-винилкапролактам и некоторые другие, которые представляют значительный интерес благодаря возможности их применения в медицине, биотехнологии и в процессах экстракции [6–8]. Менее исследованными в качестве экстрагентов в ряду рассматриваемых полимеров являются продукты полимеризации простейшего представителя N-виниламидов N-винилформамида (ВФ), некоторые из которых проявляют иммуностимулирующее действие. Наличие в макроцепи таких полимеров звеньев ВФ, способных к гидролизу с образованием NH2-групп, позволяет получать монодисперсные субмикронные частицы с многофункциональной поверхностью. В результате этого становится возможным увеличить эффективность взаимодействия макромолекул с веществами [8]. Имеющиеся данные о свойствах полимеров ВФ указывают на возможность их использования для создания высокоэффективных экстракционных систем с целью извлечения биологически активных веществ.
В работе впервые систематически изучена экстракция циклических аминокислот (фенилаланин, тирозин, гистидин, пролин) в двухфазных системах на основе поли-N-винилформамида (ПВФ) и сополимера N-винилформамида с N-винилимидазолом (ВФ-ВИ) с применением в качестве высаливателя сульфата аммония с концентрацией 20 мас. %: рН в таких системах составлял 4.2 ± 0.1. Основываясь на результатах ранее проведенных исследований по применению N-винилформамида для экстракции аминокислот [6, 8], нами целенаправленно использован ПВФ со средневязкостной молекулярной массой М = 25 × 103 г/моль и величиной характеристической вязкости [η] = 0.40 дл/г в 0.2 М растворе хлорида натрия при 20°C. Сополимер ВФ-ВИ получали радикальной полимеризацией в диоксане с применением в качестве инициатора азодиизобутиронитрила с концентрацией 1 мас. % в течение 8 ч при 65°С [9]. Сополимер ВФ-ВИ синтезировали при молярном соотношении сомономеров 9 : 1 с получением сополимера, содержащего 0.49 мол. дол. звеньев ВФ. Характеристическая вязкость ВФ в сополимере составила 0.52 дл/г.
Растворы экстрагировали на вибросмесителе в течение 10 мин при температуре 20 ± 1°С. Для установления межфазного равновесия и полного расслаивания системы экстракционную систему центрифугировали при 10 000 об./мин в течение 15 мин. Измеряли соотношение равновесных объемов водной и органической фаз (r). Водно-солевую фазу отделяли от органической и анализировали методом капиллярного электрофореза [10]. Рассчитаны коэффициенты распределения (D) и степень извлечения аминокислот (R, %) при их межфазном распределении и различных соотношениях исходных объемов фаз (табл. 1).
Таблица 1.
Результаты экстракции циклических аминокислот (n = 3; Р = 0.95)*
| Аминокислота | С, моль/дм3 | Соотношение объемов фаз r | Коэффициент распределения D | Степень извлечения R, % |
|---|---|---|---|---|
| Экстрагент–ПВФ | ||||
| Фенилаланин | 3.5 × 10–4 | 10:3 | 32 ± 3 | 91 ± 4 |
| 4.0 × 10–4 | 62 ± 6 | 95 ± 5 | ||
| 4.5 × 10–4 | 39 ± 4 | 93 ± 4 | ||
| Тирозин | 3.0 × 10–4 | 10:2 | 256 ± 4 | 98 ± 1 |
| 3.2 × 10–4 | 260 ± 12 | 98 ± 6 | ||
| 3.5 × 10–4 | 234 ± 9 | 98 ± 5 | ||
| Гистидин | 2.2 × 10–4 | 10:2 | 83 ± 7 | 94 ± 4 |
| 2.5 × 10–4 | 86 ± 6 | 95 ± 3 | ||
| 3.0 × 10–4 | 81 ± 5 | 94 ± 4 | ||
| Пролин | 5.0 × 10–4 | 10:4 | 58 ± 5 | 94 ± 4 |
| 5.5 × 10–4 | 56 ± 6 | 93 ± 4 | ||
| 6.0 × 10–4 | 51 ± 4 | 93 ± 3 | ||
| Экстрагент–ВФ-ВИ | ||||
| Фенилаланин | 3.5 × 10–4 | 10:2 | 99 ± 5 | 95 ± 3 |
| 4.0 × 10–4 | 112 ± 11 | 96 ± 5 | ||
| 4.5 × 10–4 | 100 ± 13 | 95 ± 4 | ||
| Тирозин | 3.8 × 10–4 | 10:2 | 79 ± 5 | 97 ± 6 |
| 4.0 × 10–4 | 72 ± 4 | 96 ± 5 | ||
| 4.5 × 10–4 | 67 ± 6 | 95 ± 4 | ||
| Гистидин | 2.2 × 10–4 | 10:2 | 90 ± 11 | 90 ± 3 |
| 2.5 × 10–4 | 103 ± 12 | 99 ± 5 | ||
| 3.0 × 10–4 | 96 ± 10 | 91 ± 3 | ||
| Пролин | 5.0 × 10–4 | 10:4 | 67 ± 5 | 95 ± 3 |
| 5.5 × 10–4 | 75 ± 8 | 96 ± 5 | ||
| 6.0 × 10–4 | 69 ± 7 | 96 ± 4 | ||
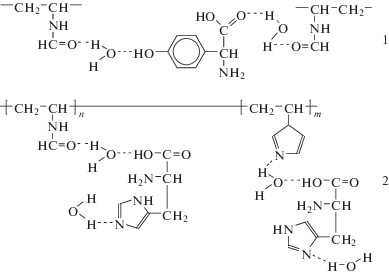
Установлено, что тирозин извлекается лучше других аминокислот в системах с ПВФ в качестве экстрагента, а гистидин экстрагируется более эффективно в системах ВФ-ВИ (обе аминокислоты извлекаются более, чем на 98%) при соотношении объемов фаз 10 : 2. На основании полученных экстракционных характеристик предложен механизм межмолекулярных взаимодействий в системах полимер–аминокислота (рис. 1).
Тирозин – гораздо более полярная молекула, чем фенилаланин, а молекула пролина содержит циклическую структуру в алифатической боковой цепи, что удерживает пролин в жесткой конформации [11]. Поэтому результаты экстракции фенилаланина и пролина в системах с ПВФ несколько ниже, чем тирозина и гистидина. Можно предположить, что наличие в структуре тирозина гидроксильной группы и азота в пятичленном цикле гистидина обусловливает их большую способность к комплексообразованию, что способствует их лучшему перераспределению в фазу гомо- или сополимера в процессе экстракции по сравнению с фенилаланином и пролином. Введение в систему компонента со звеньями ВИ приводит к образованию внутримолекулярных связей между полярными группами аминокислот и N-атомами пиридинового типа в имидазольном цикле. Такой характер взаимодействия способствует более сильному сжатию макромолекул, находящихся в конформации клубка, что отражается на результатах экстракции. Это объясняется тем, что в макроцепи сополимеров появляются звенья, проявляющие комплексообразующую способность и характеризующиеся неравномерным распределением электронной плотности и наличием нуклеофильных центров [9].
Учитывая результаты экстракции индивидуальных аминокислот, нами предложены оптимальные системы для разделения и селективного определения двухкомпонентных растворов аналитов при r = 10 : 2 (табл. 2). В качестве примера приводим результаты экстракции смеси фенилаланин–тирозин, так как раздельное определение этих аминокислот имеет существенное значение: лечение фенилкетонурии заключается в соблюдении специальной диеты, при которой белок замещается смесью аминокислот с низким содержанием фенилаланина и высоким содержанием тирозина.
Таблица 2.
Результаты экстракции смеси фенилаланина (1) и тирозина (2) сополимером ВФ-ВИ (n = 3; Р = 0.95).
| С, моль/дм3 | Результаты экстракции | ||||
|---|---|---|---|---|---|
| Фенилаланин | Тирозин | D1 | R1, % | D2 | R2, % |
| 3.0 × 10–4 | 2.5 × 10–4 | 77 ± 4 | 94 ± 3 | 85 ± 5 | 94 ± 2 |
| 3.5 × 10–4 | 3.0 × 10–4 | 85 ± 5 | 94 ± 3 | 88 ± 6 | 94 ± 1 |
| 3.8 × 10–4 | 3.5 × 10–4 | 83 ± 4 | 95 ± 2 | 86 ± 5 | 95 ± 3 |
| 4.0 × 10–4 | 3.8 × 10–4 | 124 ± 11 | 96 ± 3 | 88 ± 8 | 96 ± 3 |
| 5.0 × 10–4 | 4.5 × 10–4 | 99 ± 9 | 95 ± 2 | 80 ± 7 | 94 ± 2 |
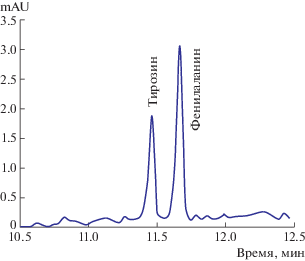
Для идентификации и раздельного определения аминокислот нами применен электрофоретический метод. Электрофоретический анализ проводили на приборе “Капель-105 М” (производитель “Люмэкс”, Россия). Определение проводили при условиях: ввод пробы при давлении 300 мбар в течение 5 с, длина волны – 254 нм, напряжение +25 кВ, температура 30°С, время ввода пробы 7 мин, ведущий электролит – фосфатный буферный раствор с рН 7.8 ± 0.2 с добавкой β-циклодекстрина. Регистрировали электрофореграммы, проверяли правильность автоматической разметки пиков, с помощью программного обеспечения “Эльфоран” идентифицировали компоненты. Для исключения влияния буферного раствора и экстрагента предварительно были получены их электрофореграммы.
На электрофореграмме отчетливо проявляются пики фенилаланина и тирозина, имеющие хорошее разрешение (рис. 2). Использование поли-N-винилформамида позволяет провести экстракционно-электрофоретическое определение аминокислот в таблетированных фармацевтических препаратах “Гистидин” (“ОЗОН”, Россия) и “Пролин” (“Vitaline”, США). Производителями заявляется содержание гистидина 500 мг на одну таблетку, нами найдено 487 ± 6 мг; содержание пролина заявляется 25 мг, найдено 24.6 ± 0.2 мг.
В результате проведенного исследования установлена высокая экстрагирующая способность гомо- и сополимеров на основе N-винилформамида. Максимальная эффективность экстракции индивидуальных аминокислот достигается при использовании в качестве экстрагента поли-N-винилформамида и соотношении объемов фаз 10 : 2; в этих условиях степени извлечения аминокислот достигают 93–98%. Впервые проведенное экстракционное разделение двухкомпонентной смеси аминокислот наиболее эффективно в системах на основе сополимера ВФ-ВИ. Разработаны условия электрофоретического определения аминокислот после их экстракции растворами полимеров. Полученные результаты экстракции и определения циклических аминокислот позволяют рекомендовать предложенные методики при анализе объектов окружающей среды, пищевых и фармацевтических продуктов, содержащих циклические аминокислоты.
Список литературы
Шкинев В.М., Мокшина Н.Я., Хохлов В.Ю., Спиваков Б.Я. // ДАН. 2013. Т. 448. № 4. С. 427–429. https://doi.org/10.7868/S0869565213040166
Salabat A., Abnosi M.H., Motahari A. // J. Chem. Eng. Data. 2008. V. 53. № 9. P. 2018–2021.
Hatti-Kaul R. // Mol. Biotechnol. 2001. V. 19. № 3. P. 269–277. https://doi.org/10.1385/MB:19:3:269
McQueen L., Lai D. // Front. Chem. 2019. V. 7. P. 135. https://doi.org/10.3389/fchem.2019.00135
Pereira J.F.B., Lima Á.S., Freire M.G., Coutinho J.A.P. // Green Chem. 2010. V. 12. № 9. P. 1661–1669. https://doi.org/10.1039/C003578E
Мокшина Н.Я., Быковский Д.В., Шаталов Г.В., Пахомова О.А. // Журнал аналитической химии. 2016. Т. 71. № 2. С 208–211. https://doi.org/10.1134/S1061934816020106
Шаталов Г.В., Лавлинская М.С., Мокшина Н.Я., Пахомова О.А., Кузнецов В.А. // Журнал прикладной химии. 2016. Т. 89. № 1. С. 112–118. https://doi.org/10.1134/S1070427216010225
Мокшина Н.Я., Пахомова О.А., Шаталов Г.В., Косинова И.И. // Известия вузов. Сер. Химия и хим. технология. 2019. Т. 62. № 1. С. 4–10. https://doi.org/10.6060/ivkkt.20196201.5763
Kuznetsov V.A., Lavlinskaya M.S., Ostankova I.V., Shatalov G.V., Shikhaliev Kh.S., Ryzhkova E.A. // Polym. Bull. 2018. V. 75. № 3. C. 1237–1251. https://doi.org/10.1007/s00289-017-2091-2
Карцова Л.А. Проблемы аналитической химии. Т. 18 / Капиллярный электрофорез. Москва: Наука, 2014. 438 с.
Нельсон Д., Кокс М. Основы биохимии Ленинджера: в 3 т. Москва: БИНОМ. Лаборатория знаний. 2011. Т. 1. 694 с.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах