Доклады Российской академии наук. Химия, науки о материалах , 2020, T. 492-493, № 1, стр. 18-22
Водорастворимые полимерные лиганды для связывания ионов тербия
Т. Н. Некрасова 1, *, О. Н. Журавская 1, М. А. Безрукова 1, А. В. Добродумов 1, член-корреспондент РАН Е. Ф. Панарин 1, 2
1 Институт высокомолекулярных соединений Российской академии наук
Санкт-Петербург, Россия
2 Санкт-Петербургский политехнический университет им. Петра Великого
Санкт-Петербург, Россия
* E-mail: polar@imc.macro.ru
Поступила в редакцию 28.02.2020
После доработки 05.06.2020
Принята к публикации 11.06.2020
Аннотация
Методом радикальной сополимеризации синтезированы тройные водорастворимые сополимеры 2-деокси-N-метакрилоиламидоглюкозы, метакрилоилацетона и метакриловой кислоты. Показано, что в водных растворах они образуют люминесцирующие комплексы с ионами тербия, интенсивность люминесценции которых зависит от соотношения компонентов и остается постоянной в присутствии солей CaCl2 и NaCl. Сополимеры, связывающие ионы тербия, могут быть основой при создании как люминесцирующих зондов, так и радиоактивных фармпрепаратов при использовании коротко живущего γ-излучателя 161Tb в радиотерапии онкологических заболеваний.
Широкое использование ионов Ln3+ в качестве люминесцирующих зондов связано с рядом особенностей их свечения по сравнению с органическими люминофорами [1–4]. Использование полимерных комплексов лантанидов в биомедицине позволяет пролонгировать их действие, в связи с чем актуальным является получение металлокомплексов на основе водорастворимых биосовместимых полимеров, содержащих хелатные звенья.
Особый интерес представляют сополимеры, содержащие лигандные звенья, способные обеспечивать внутримолекулярный перенос энергии с триплетного уровня лиганда на резонансные уровни иона лантанидов. При этом надо иметь в виду, что эффективность переноса энергии зависит не только от энергии триплетного уровня лиганда, но и от природы заместителей в нем и их взаимодействия с окружением [5].
Помимо применения полимерных лигандов при разработке люминесцирующих маркеров значительный интерес представляет их использование для получения комплексов с радионуклидами 161Tb3+ (период полураспада 6.906 суток), перспективных в ядерной медицине, в терапии онкологических заболеваний [6, 7].
Макромолекулярные комплексы (ММК) лантанидов для медико-биологических исследований должны обладать биосовместимостью, высокой растворимостью и устойчивостью в водных растворах. При высоком содержании хелатных групп в сополимере из-за стерических ограничений формируются координационно ненасыщенные ММК, что влияет на их фотофизические свойства [2]. Поэтому представляет интерес исследовать комплексы с невысоким содержанием (до 10 мол. %) хелатирующих звеньев.
Перспективным классом веществ, которые используются в качестве лигандов, являются карбоцепные полимеры с хелатирующими функциональными группами, в частности, (со)полимеры карбоновых кислот (акриловой, метакриловой, салициловой, аминобензойной, малеиновой) с нейтральными сомономерами, такими как алкилметакрилаты, стирол [8–10]. Карбоксильные группы (лиганды) прочно связывают ион лантанида, а сенсибилизирующий лиганд обеспечивает эффективность процесса переноса энергии электронного возбуждения (ЭЭВ) с триплетного уровня лиганда на резонансный уровень лантанида (антенный эффект).
В данной работе синтезированы водорастворимые сополимеры метакрилоиламидоглюкозы (2-деокси-N-метакрилоиламидоглюкоза) (МАГ) с содержанием хелатных групп метакрилоилацетона (МАЦ) (2-метил-1-гексен-3,5-дион) от 0.5 до 3.4 мол. %, метакриловой кислоты (МАК) – 10 мол. %, и исследованы условия формирования и фотолюминесценция их комплексов с ионами тербия; проведена оценка стабильности люминесценции комплексов в присутствии неорганических солей. Применение люминесцентных методов для исследования комплексообразования в растворе позволяет изучать процессы формирования комплексов без их выделения из раствора [11] при низких концентрациях, близких к тем, которые используют в ядерной медицине и биологических тестах [6, 7].
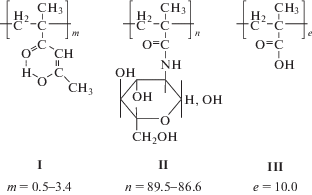
Сополимеры МАЦ (I) (2-метил-1-гексен-3,5-дион), МАГ (II) и МАК (III)
были получены радикальной сополимеризацией соответствующих мономеров в 30%-ном растворе ДМФА в присутствии ДАК (динитрил азобисизомасляной кислоты) при 65°С, реакцию вели в течение 24 ч [12, 13].Строение и состав сополимеров подтвержден данными ЯМР-спектроскопии, УФ-спектроскопии и кондуктометрическим титрованием 0.1 N раствором NaOH. Синтезированные сополимеры содержали 0.5–3.4 мол. % МАЦ и 10 мол. % МАК, хорошо растворимы в воде. ММ сополимеров составляли 1.0 × 105. Спектры возбуждения и люминесценции растворов сополимеров в присутствии ионов Tb3+ записывали на спектрофлуориметре LS-100 (фирма PTI, Канада). Концентрацию звеньев МАЦ в растворе варьировали от 2 × 10–5 до 5.8 × 10–4 моль/л.
На рис. 1 приведены спектры поглощения (а) и возбуждения (б) ионов тербия в растворах сополимера МАГ–МАЦ–МАК при различных концентрациях сополимера Cпол и Tb3+.
Рис. 1.
Спектры поглощения водного раствора сополимера (1), содержащего 3.4 мол. % МАЦ, и в присутствии ионов тербия (2), β = [Tb3+]/[МАЦ] = 0.04 (а). Спектры возбуждения водного раствора сополимера в присутствии ионов тербия: Спол = 0.078, 0.15, 0.23 и 0.26 мас. % (спектры 1, 2, 3, 4 соответственно), β = [Tb3+]/[МАЦ] = 0.04, λнабл = 545 Нм, соответствующая переходу 5D4 → 7F5 (б).
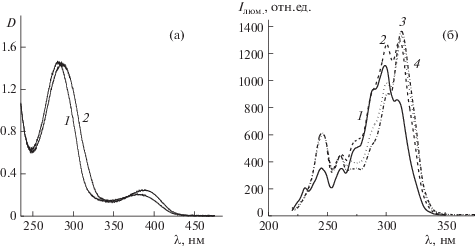
Смещение полос в спектрах поглощения сополимера при добавлении ионов Tb3+ подтверждает факт образования его комплекса со звеньями МАЦ (рис. 1а). Из рис. 1б, на котором приведены спектры возбуждения комплексов тербия с сополимером, видно, что с увеличением концентрации комплекса интенсивность полосы при 298 нм уменьшается, но растет интенсивность полосы с максимумом при 311 нм и при Спол ≥ 0.2 мас. % спектры меняются незначительно. При Спол ≥ ≥ 0.2 мас. % полоса с λмакс = 298 нм присутствует в виде плеча (рис. 1б, кривая 4), в то время как при β = [Tb3+]/[МАЦ] = 0.1 основной является полоса λвозб = 295 ± 3 нм, а полоса λвозб = 310 нм присутствует в виде плеча при всех Спол. Зависимость формы спектров возбуждения как от Спол, так и от β = [Tb3+]/[МАЦ] свидетельствует о том, что центры возбуждения, то есть окружение иона тербия, имеют разную структуру. Меняется состав координационной сферы в полимерном комплексе и эффективность передачи ЭЭВ со звена МАЦ на ион тербия. Поэтому было исследовано влияние концентрации сополимера, ионов тербия и их соотношения в растворе, а также состава сополимера на фотофизические параметры люминесценции ионов тербия.
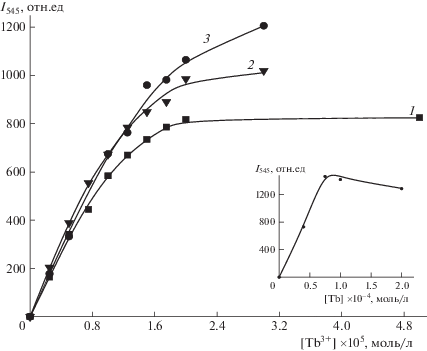
На рис. 2 приведены зависимости I545 (положение основного максимума в спектре люминесценции тербия) от содержания ионов тербия в растворе сополимеров с различным содержанием звеньев МАЦ. Из рисунка видно, что в присутствии всех синтезированных сополимеров ионы Tb3+ люминесцируют. При концентрации ${{C}_{{{\text{T}}{{{\text{b}}}^{{{\text{3 + }}}}}}}}$ ≤ ≤ 1 × 10–5 мол/л I545 линейно растет с увеличением содержания тербия в растворе для сополимеров всех составов. Для сополимера, содержащего 0.5 мол. % МАЦ, зависимость выходит на плато. Выход на плато I545 указывает на то, что все места, доступные для связывания, заняты. Можно предположить, что в этих условиях комплекс имеет постоянный состав: 1 ион тербия связан с 2 звеньями МАЦ. Для сополимеров с более высоким содержанием МАЦ I545 медленно растет, достигая насыщения при ${{C}_{{{\text{T}}{{{\text{b}}}^{{{\text{3 + }}}}}}}}$ ≤ 1 × 10–4 моль/л. Возможно это связано с тем, что образуются комплексы с разной стехиометрией, меняется соотношение звеньев МАЦ, метакриловой кислоты и молекул воды в координационной сфере, что оказывает заметное влияние на эффективность передачи ЭЭВ с триплета органического лиганда на резонансный уровень тербия и интенсивности люминесценции.
Рис. 2.
Зависимость I545 от концентрации ионов Tb3+ для сополимеров разного состава. Кривые 1, 2, 3 (0.5, 2 и 3.4 мол. % соответственно) Спол = 0.2 мас. %. На врезке: зависимость I545 от концентрации ионов Tb3+ в интервале 0–2 × 10–4 М.
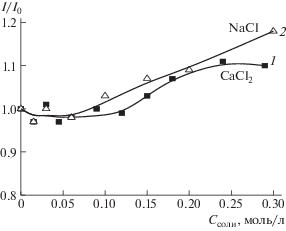
Перспективы применения комплексов в биомедицине требуют исследования стабильности люминесценции в условиях, приближающихся к физиологическим, по крайней мере, в присутствии ионов Na+, Ca2+. На рис. 3 приведено относительное изменение интенсивности люминесценции ионов тербия I/I0 в комплексе с сополимером при добавлении NaCl или CaCl2. Добавление соли практически не влияет на I545 вплоть до концентраций 0.1–0.12 М, что свидетельствует о достаточно высокой стабильности сформированных комплексов в растворе. Компактизация макромолекулярного клубка, содержащего группы СОО–, при добавлении солей уменьшает его гидратацию, что обеспечивает стабильность комплекса в этих условиях [10, 14].
Рис. 3.
Изменение интенсивности люминесценции I/I0 раствора комплекса сополимера, содержащего 2.3 мол. % МАЦ с Tb3+ при добавлении NaCl (кривая 1) или CaCl2 (кривая 2); Спол = 1 мг/мл, ${{C}_{{{\text{T}}{{{\text{b}}}^{{{\text{3 + }}}}}}}}$ = 5 × 10–5 М.
Таким образом, синтезированные водорастворимые сополимеры МАГ, содержащие 0.5–3.4 мол. % МАЦ, при взаимодействии с ионами тербия (1 × 10–5 М) в разбавленных водных растворах (Спол ≤ 0.1 мас. %) образуют люминесцирующие комплексы, стабильные в водно-солевых (0.15 М) растворах NaCl или CaCl2. Использование полимерных лигандов для связывания радионуклидов тербия открывает перспективы создания полифункциональных препаратов для одновременной визуализации и терапии поврежденных опухолями органов.
Список литературы
Bünzli J.-C.G. Lanthanide light for biology and medical diagnosis // J. Lumin. 2016. V. 170. P. 866–878. https://doi.org/10.1016/j.jlumin.2015.07.033
Карасев В.Е., Петроченкова Н.В. Лантанидсодержащие полимеры. Владивосток: Дальнаука, 2005. 194 с.
Bünzli J.-C.G. Review: Lanthanide coordination chemistry: from old concepts to coordination polymers // J. Coord. Chem. 2014. V. 67. № 23–24. P. 3706–3733. https://doi.org/10.1080/00958972.2014.957201
Bochkarev M.N., Pushkarev A.P. Synthesis and luminescence of some rare earth metal complexes // Org. Photonics Photovolt. 2016. V. 4. P. 60–67. https://doi.org/10.1515/oph-2016-0007
Уточникова В.В., Кузьмина Н.П. Фотолюминесценция ароматических карбоксилатов лантанидов // Коорд. химия. 2016. Т. 42. № 10. С. 640–656. https://doi.org/10.7868/S013234
Zimmermann R. La Medecine nucleaire La radioactivite au service du diagnostic et de la therapie / EDP Sci. 2006. 192 p.
Панарин Е.Ф., Лавров Н.А., Соловский М.В., и др. Полимеры-носители биологически активных веществ. СПб: ЦОП “Профессия”, 2014. 304 с.
Qi X., Wang Z., Ma S., et al. Complexation Behavior of Poly(acrylic acid) and Lanthanide Ions // Polymer. 2014. V. 55. № 5. P. 1183–1189. https://doi.org/10.1016/j.polymer.2014.01.051
Gao B., Fang L., Men J. Studies on preparation, structure and fluorescence emission of polymer-rare earth complexes composed of aryl carboxylic acid-functionalized polystyrene and Tb(III) ion // Polymer. 2012. V. 53. № 21. P. 4709–4717. https://doi.org/10.1016/j.polymer.2012.07.059
Okamoto S., Vyprachticky D., Furuya H., et al. Ion binding properties of polycarboxylates using terbium(III) as a fluorescent probe: viscosities and coordinated water molecules in polycarboxylate-terbium(III) complexes in aqueous solutions // Macromolecules. 1996. V. 29. № 10. P. 3511–3514. https://doi.org/10.1021/ma960251I
Utochnikova V.V. The use of luminescent spectroscopy to obtain information about the composition and the structure of lanthanide coordination compounds // Coord. Chem. Rev. 2019. V. 398. P. 113006. https://doi.org/10.1016/j.ccr.2019.07.003
Korzhikov V.A., Diederichs S., Nazarova O.V., et al. Water-soluble aldehyde bearing polymers of 2-deoxy-2-methacrylamido-D-glucose for bone tissue engineering // J. Appl. Polym. Sci. 2008. V. 108. № 4. P. 2386–2397. https://doi.org/10.1002/app.27292
Teyssiee Ph., Smets G. Synthesis and polymerization of methacroylacetone // Makromol. Chem. 1958. V. 26. № 1. P. 245–251. https://doi.org/10.1002/macp.1958.020260122
Kido J., Brittain H.G., Okamoto Y. Investigation of ion binding properties of synthetic polyelectrolytes using a terbium(III) probe: elucidation of the number of coordinated water molecules on metal polyelectrolyte complexes // Macromolecules. 1988. V. 21. № 6. P. 1872–1875. https://doi.org/10.1021/ma00184a058
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах