Доклады Российской академии наук. Химия, науки о материалах , 2020, T. 494, № 1, стр. 55-61
научно-технологические основы повышения ресурсоэффективности электрофлотационных процессов извлечения труднорастворимых неорганических соединений (оксиды, карбиды, гидроксиды) из водных растворов электролитов
А. В. Колесников 1, *, академик РАН В. П. Мешалкин 1, 2, Т. В. Давыдкова 1, В. А. Колесников 1
1 Российский химико-технологический университет имени Д.И. Менделеева
Москва, Россия
2 Институт общей и неорганической химии
имени Н.С. Курнакова Российской академии наук
Москва, Россия
* E-mail: artkoles@list.ru
Поступила в редакцию 07.07.2020
После доработки 09.08.2020
Принята к публикации 01.09.2020
Аннотация
Установлено, что для систем H2О–TiO2, H2О–Ti3N4, H2О–SiC, порошки углеродных материалов–H2О и ряда других степень извлечения не превышает 10–20% за 30 мин флотации в электролитах NaCl и Na2SO4 в широком диапазоне рН, что связано с малым размером дисперсной фазы и гидрофильными свойствами поверхности порошков. Введение в систему коагулянтов FeCl3, AlCl3 и композиций с поверхностно-активными веществами интенсифицирует процесс флотации и приводит к росту степени извлечения для отмеченных выше систем до 90–96%. Впервые рассчитаны константы скорости K электрофлотационных процессов для типовых зависимостей α = f(τ). С учетом величин K и степени извлечения определены критерии эффективности электрофлотационных процессов по пяти основным группам. Результаты исследований важны при выборе технологии обезвреживания жидких техногенных отходов, содержащих соединения титана.
ВВЕДЕНИЕ
Электрофлотационный процесс (ЭФП) привлекает внимание исследователей и находит все большее применение в первую очередь для процессов водоочистки [1–3].
Теоретические исследования электрофлотационного процесса с целью описания кинетики извлечения, механизма взаимодействия частиц и пузырьков опубликованы в ряде обзоров и монографий российских и зарубежных специалистов [4–7]. В современных подходах авторы обращают внимание на коалесценцию и полидисперсность газовых пузырьков и дисперсной фазы, электростатическое взаимодействие пузырьков Н2 и О2 с частицами малых размеров в процессах электрофлотационного извлечения (ЭФ).
Наиболее интересна в настоящее время модель, учитывающая многостадийность процесса флотации, возможность коагуляции и седиментации частиц, предложенная профессором Б.С. Ксе- нофонтовым [2] и актуальная с практической точки зрения [8–11].
Электрофлотационному процессу извлечения дисперсной фазы различной природы из водных растворов электролитов посвящен ряд статей [1, 5, 7, 9, 12], в том числе с растворимыми железными и алюминиевыми анодами [13, 14]. Положительное влияние поверхностно-активных веществ (ПАВ) на повышение эффективности электрофлотационного процесса извлечения гидроксидов меди, никеля и цинка представлено в работе [15]. Особенности электрофлотационного процесса извлечения порошков углеродных материалов опубликованы в статьях [16, 17].
ЭКСПЕРИМЕНТАЛЬНЫЕ РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Анализ различных моделей формирования флотокомплексов в различных установках позволил определить факторы интенсификации и повышения эффективности процесса извлечения загрязнений. Степени извлечения гидрофильно-гидрофобных частиц для напорной флотации составили 50–70%, гидрофобных 90–95%. Электрофлотационный процесс обеспечивает более высокие степени извлечения гидрофильно-гидрофобных частиц (85–95%), гидрофобных ‒ до 98% [18]. Нами было рассмотрено формирование флотокомплекса в электрофлотационном процессе и основные подходы к повышению эффективности извлечения дисперсной фазы различной природы из водных растворов и сточных вод.
На рис. 1 показано формирование флотокомплекса в условиях электрофлотационного процесса.
Рис. 1.
Формирование флотокомплекса в электрофлотационном процессе. Обозначения: А – частицы и пузырек в исходном состоянии; В – флотокомплекс “частица‒пузырек H2”; С – флотокомплекс “частица‒пузырек О2”; D – частица в пенном слое.
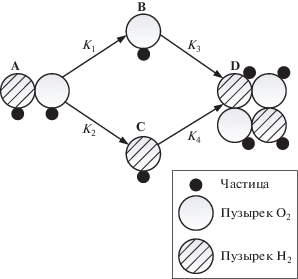
На практике для анализа кинетики электрофлотационного процесса часто используют уравнение
где α – степень извлечения дисперсной фазы, %; τ – время, мин; K – константа скорости перехода дисперсной фазы в пенный продукт.Величина K связана с многостадийностью процесса согласно следующей зависимости:
где:K1 – вероятность образования флотокомплекса “частица‒пузырек H2”;
K2 – вероятность образования флотокомплекса “частица‒пузырек О2”;
K3 – всплытие флотокомплекса “частица‒пузырек H2”;
K4 – всплытие флотокомплекса “частица‒пузырек О2”.
Константа скорости перехода дисперсной фазы в пенный продукт связана с газонасыщением (Iv), размером пузырьков (Dпуз), размером частиц (Dчаст), полидисперсностью частицы и пузырька ($K_{0}^{'}$) и может быть рассчитана по формуле:
(3)
$K = \frac{{E{{I}_{{\text{v}}}}{{D}_{{{\text{част}}}}}{{K}_{0}}}}{{{{D}_{{{\text{пуз}}}}}{{K}_{0}}}}.$В то же время величина Е – эффективность захвата комплекса “частица–пузырек” ‒ трудно определяется экспериментально, так как зависит от большого количества факторов: гидрофобности поверхности, заряда дисперсной фазы, структуры осадка и природы дисперсной фазы, адсорбции ПАВ и т.д.
Анализ показывает, что вероятность столкновения мелких частиц размером меньше 10 мкм с пузырьками размером 40–60 мкм невелика и близка к нулю, степень извлечения составляет 1–5%.
Вероятности K1 и K2, которые зависят от химических свойств поверхности, структуры поверхностных слоев, гидрофобности или гидрофильности поверхности, заряда поверхности и заряда пузырьков адсорбции анионов и катионов ПАВ, флокуляции частиц и пузырьков, гетерокоагуляции “частица–коагулянт”, краевого угла смачивания “пузырек–частица” и других факторов, фактически определяют эффективность процесса и степень извлечения.
Вероятности K3 и K4 имеют бóльшие значения для мелких пузырьков, характерных для электрофлотации, в отличие от других флотационных процессов, в первую очередь, в присутствии ПАВ, которые стабилизируют пузырьки в ЭФ аппарате на уровне среднего размера 25–30 мкм.
Величина K имеет бóльшие значения для гидрофобных частиц, которые эффективно флотируются в пенный продукт, степень извлечения достигает 90–95%.
Предложены основные подходы для повышения эффективности электрофлотационного процесса извлечения труднорастворимых соединений металлов и углеродных материалов, а именно:
1) гидрофобизация поверхности дисперсной фазы (H2O ↔ ПАВ);
2) создание нового флотокомплекса:
− дисперсная фаза–флокулянт, ПАВ;
− дисперсная фаза–коагулянт (Fe, Al, Ti);
− дисперсная фаза–композиция (коагулянт–ПАВа), где композиция – это система коагулянт–ПАВ;
3) увеличение размера частиц (30–100 мкм) (флокулянт, pH, ζ -потенциал, концентрация, коагулянт);
4) изменение электрокинетического потенциала, ζ → 0 (pH, ПАВ, катионы – Ca2+, Mg2+, анионы – SO$_{4}^{{2 - }}$, PO$_{4}^{{3 - }}$);
5) изменение природы и структуры дисперсной фазы (аморфная, рыхлая) (гидроксиды, фосфаты, сульфиды, карбонаты).
Лабораторные эксперименты в установках непроточного типа дают общую информацию о протекании процесса электрофлотационного извлечения, в первую очередь, о влиянии на степень извлечения таких факторов, как размер и заряд частиц, изменение рН, адсорбция ионов электролита, присутствие флокулянтов и ПАВ различной природы, природа коагулянта, концентрация дисперсной фазы и газонасыщение раствора электролитическими газами.
Проанализировано большое количество экспериментальных зависимостей кинетики процесса извлечения дисперсной фазы на лабораторной установке согласно методике исследования, опубликованной в работах [18–20]. На рис. 2 представлены зависимости α = f(τ) для случаев, где флотация протекает с очень высокой (кривая 5) и с очень низкой (кривая 1) эффективностью.
Рис. 2.
Зависимость степени извлечения дисперсной фазы в электрофлотационном процессе от времени в различных системах: 1 – очень низкая; 2 – низкая; 3 – средняя; 4 – высокая; 5 – очень высокая.
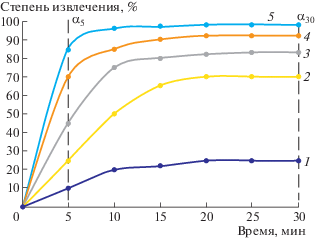
На основании анализа уравнения (1) рассчитаны величины K. На основании анализа экспериментальных величин α5 и α30 (степени извлечения через 5 и 30 мин в процессе электрофлотации) и расчетной величины K предложен подход к оценке эффективности протекания ЭФ процесса на лабораторной установке непроточного типа. Результаты анализа представлены в табл. 1.
Таблица 1.
Базовые параметры электрофлотационного процесса
| Параметр | Эффективность процесса | ||||
|---|---|---|---|---|---|
| очень высокая | высокая | средняя | низкая | очень низкая | |
| K | 0.2–0.3 | 0.1–0.2 | 0.01–0.1 | менее 1 × 10‒2 | менее 1 × 10‒3 |
| α5, % | 80–95 | 60–75 | 40–555 | 20‒25 | 5‒10 |
| α30, % | 98 | 92 | 83 | 70 | 25 |
Величина степени извлечения α5 в течение 5 мин характеризует качественно формирование флотокомплекса “частица–пузырек” и способность всплытия на границу “раствор–воздух”.
Величина α5 коррелирует с высокими значениями K. Величина α30 характеризует эффективность ЭФ процесса в целом, стабильность пенного продукта, возможные процессы разрушения пены, приводящие к снижению величины α30.
В зависимости от значения величин α5, α30, и K предложено разделить исследуемые системы на 5 групп.
На основании лабораторных исследований для групп (4) и (5) можно рекомендовать опытно-промышленные и промышленные испытания; для групп (1) и (2), где значения α5, α30, K имеют низкие значения, необходимы дополнительные исследования и поиск технологических приемов интенсификации и повышения эффективности электрофлотационного процесса.
Указанный подход удобен для тестирования реальных объектов, например, сточных вод промышленных предприятий. При поставке в лабораторию 10 л сточной воды удается протестировать систему 8‒10 раз в различных условиях с добавлением необходимых реагентов: флокулянтов, ПАВ, коагулянтов.
В электрофлотационном процессе, особенно для электрофлотации частиц малых размеров (до 10 мкм), формирование флотокомплекса связано с электростатическим притяжением частиц и пузырьков, имеющих за счет формирования двойного электрического слоя различные заряды поверхности.
Экспериментально установлено, что низкая эффективность электрофлотационного процесса наблюдается для частиц отрицательно заряженных, как правило, в растворах при рН > 7 в присутствии анионов (S2–, PO$_{4}^{{3 - }}$, СО$_{3}^{{2 - }}$, H2PO$_{4}^{ - }$). Низкая эффективность в этом случае связана со сложностью формирования флотокомплекса “отрицательно заряженная частица–пузырьки H2–дисперсная фаза”. При рН 9–10 пузырьки O2 в объеме раствора, вероятнее всего, заряжены так же отрицательно.
Низкие степени извлечения 10–15% определены для электрофлотационного процесса извлечения порошков TiO2, SiC, углеродных материалов марок ОУ-А, ОУ-Б (Россия) в первую очередь из-за малых размеров и высоких отрицательных ζ-потенциалов. Величина электрокинетического потенциала (ζ, мВ), измеренная экспериментально, дает необходимую информацию об объектах флотации.
Как показали исследования, эффективность ЭФ процесса значительно увеличивается в присутствии ПАВ в растворе, т.к. ПАВ оказывают влияние вследствие адсорбции на поверхности дисперсной фазы и способствуют формированию на поверхности гидрофильных осадков (гидроксиды металлов) гидрофобно-гидрофильных частиц. Наиболее сильное влияние оказывает анионный ПАВ на ЭФ процесс извлечения коагулянтов Fe(OH)3, Al(OH)3, Al(OH)2Cl, что было использовано для интенсификации ЭФ процесса извлечения порошков TiO2, SiC, Ti3N4, древесных порошкообразных активированных углей марок ОУ-А и ОУ-Б (Россия).
Схема формирования флотокомплекса “частица–пузырек–коагулянт–ПАВ” представлена на рис. 3.
Рис. 3.
Схема формирования флотокомплекса “частица–пузырек–коагулянт–ПАВ”. Вариант А ‒ электрофлотация гидрофильных осадков, вариант Б – электрофлотация гидрофильно-гидрофобных осадков.
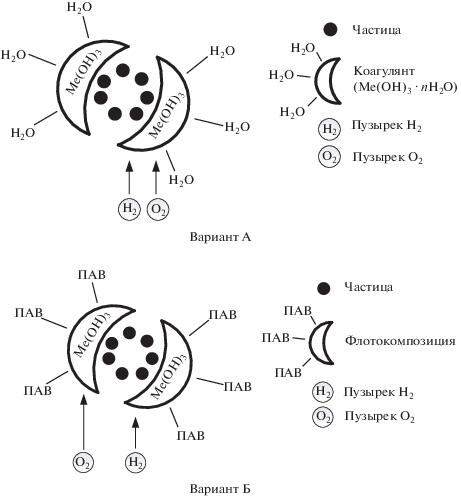
Экспериментально доказана высокая эффективность электрофлотации по варианту Б вследствие адсорбции ПАВ на гидроксидах железа и алюминия [21].
В табл. 2 представлены экспериментальные данные по ЭФ извлечению различных порошков оксидов, нитридов и карбидов титана, а также порошков активированных углей марок ОУ-А, ОУ-Б, гидроксидов хрома и алюминия. Степень извлечения указанных объектов без ПАВ и коагулянтов не превышает 10–15%.
Таблица 2.
Объекты с высокой эффективностью электрофлотационного процесса извлечения дисперсной фазы (α30 = 93–98%)a
| Объект | Технологический прием | α5 | α30 |
|---|---|---|---|
| TiO2 | Fe3+ | 32 | 74 |
| Al3+ | 24 | 64 | |
| Fe + ПАВа* | 85 | 96 (98) | |
| Al + ПАВа | 80 | 90‒95 | |
| Ti3N4 | Fe3+ | 70 | 85 |
| Al3+ | 74 | 90 | |
| Fe + ПАВа | 78 | 93 | |
| Al + ПАВа | 85 | 93–98 | |
| TiC | Fe3+ | 75 | 82 |
| Al3+ | 40 | 45 | |
| Fe + ПАВа | 88 | 95 | |
| Al + ПАВа | 90 | 98 | |
| ОУ-А | Fe–NaCl | 31 | 96 |
| Fe–ПАВа (NaCl) | 92 | 96 | |
| ОУ-Б | Fe–Na2SO4 | 75 | 98 |
| Al–Na2SO4 | 70 | 97 | |
| Fe + ПАВк (Na2SO4)** | 71 | 98 | |
| Al + ПАВа (NaCl) | 81 | 90 | |
| Al(OH)3 – x · (SO4)x | + ПАВа (NaDDS***, NaDBS****) | 75 | 93‒95 |
| Cr(OH)3 – x · (SO4)x | + ПАВа (NaDDS, NaDBS) | 68 | 90‒93 |
Примечание: a условия эксперимента ‒ с (взвешенных веществ) ≤ 100 мг/л, с (Na2SO4) = 1 г/л, с (коагулянт) = 5–10 мг/л, с (ПАВ) = 5–10 мг/л, объемная плотность тока Jv = 0.2–0.4 А/л, рН 7 ± 0.5. * ПАВа – анионный ПАВ, ** ПАВк – катионный ПАВ дидецилдиметиламмоний хлорид,*** NaDDS – додецилсульфат натрия, **** NaDBS – додецибензолсульфонат натрия.
Высокие степени извлечения наблюдаются в присутствии флокулирующей композиции “коагулянт‒гидроксид железа, алюминия‒ПАВ”. Положительное влияние анионного ПАВ (ПАВа) отмечается и при электрофлотации гидроксидных осадков Fe(OH)3, Cr(OH)3, Al(OH)3, Cu(OH)2, Zn(OH)2, Ni(OH)2.
Исследования, проведенные с другими объектами, в частности, с оксидами металлов, сульфидами и фосфатами Cu, Ni, Zn, при добавлении композиции Me(OH)3–ПАВ в соотношении концентраций 100 : (5‒10), показали высокие значения степени извлечения. Композиция “коагулянт Al(OH)2Cl–ПАВа–флокулянт Superfloc” показала высокую эффективность при извлечении взвешенных веществ, снижая их концентрацию с 1500 мг/л до 100–150 мг/л из фильтратов полигонов твердых бытовых отходов.
Таким образом, проведенные исследования показали, что электрофлотационный процесс извлечения дисперсной фазы из водных растворов можно интенсифицировать и повысить степень извлечения за счет добавления ПАВ, коагулянтов (Fe3+, Al3+) и композиций “коагулянт–ПАВ”.
ЗАКЛЮЧЕНИЕ
В результате исследования выявлен ряд несомненных преимуществ электрофлотационного метода, основными из которых являются:
• короткое время процесса (5‒10 мин) и высокая степень извлечения (до 99%), небольшие энергозатраты (0.5 кВт ч/м3) при обработке исследуемых растворов;
• возможность одновременного извлечения примесей, имеющих различный фазово-дисперсный состав с размером частиц от 10 до 100 мкм;
• образование мелкодисперсных газовых пузырьков, обладающих высокой адгезионной способностью к извлекаемым гидрофильным, гидрофобным и гидрофильно-гидрофобным примесям, и их эффективное извлечение;
• благоприятное влияние электрического поля на изменение физико-химических свойств извлекаемой дисперсной системы, интенсифицирующее процесс флокуляции;
• возможность извлечения дисперсной фазы, эмульсии и ПАВ одновременно.
Отмеченные достоинства важны при очистке сточных вод сложного состава.
Перечисленные выше преимущества объясняют то внимание, которое уделяется разработке и совершенствованию электрофлотационного процесса во многих странах мира, в том числе и в России.
Список литературы
Колесников В.А., Ильин В.И., Бродский В.А., Колесников А.В. Электрофлотация в процессах водоочистки и извлечения ценных компонентов из жидких техногенных отходов. Обзор. Ч. 1 // Теоретические основы химической технологии. 2017. Т. 51. № 4. С. 361–375.
Ксенофонтов Б.С., Антонова Е.С., Бондаренко, Капитонова С.Н., Юрьева О.А. Моделирование очистки сточных вод электрофлотацией // Экология пром. производства. 2015. Т. 89. № 1. С. 36.
Kolesnikov V.A., Brodsky V.A., Perfileva A.V., Kolesni-kov A.V. Electroflotation extraction of sparingly soluble compounds of non-ferrous and rare-earth metals from liquid technological waste // Pur. Appl. Chem. 2017. V. 89. № 10. P. 1535‒1541. https://doi.org/10.1515/pac-2016-1113
Kolesnikov A.V., Milyutina A.D., Desyatov A.V., Kolesnikov V.A. Electroflotation recovery of highly dispersed carbon materials from aqueous solutions of electrolyte // Sep. Purif. Technol. 2019. V. 209. P. 73‒78. https://doi.org/10.1016/j.seppur.2018.07.014
Chen G. Hung Y.T. Electrochemical Wastewater Treatment Processes / Wang L.K., Hung Y.T., Shammas N.K., eds. Advanced Physicochemical Treatment Technologies. Handbook of Environmental Engineering, V. 5. Totowa, NJ: Humana Press Inc.; 2007. P. 57‒106.
Шуленина З.М., Багров В.В., Десятов А.В. Вода техногенная. Проблемы, технологии, ресурсная ценность / Монография. М.: Издательство МГТУ им. Н. Баумана, 2015. 401 с.
Matis K.A., Peleka E.N. // Sep. Sci. Technol. 2010. V. 45. № 16. P. 2465.
Sillanpää M., Shestakova M. Electrochemical water treatment methods: fundamentals, methods and full scale applications / 1st ed.; Butterworth-Heinemann: 2017. V. 1. P. 310.
Sarkar S.K., Machniewski P.M., Evans G.M. Modelling and measurement of bubble formation and growth in electroflotation processes // Chemical and Process Engineering – Inzynieria Chemiczna i Procesowa. 2013. V. 34. № 3. P. 327‒336.
Binquan J., Jin L. The mathematical model of bubble size based on the bubble nucleation theory in the process of air-flotation // Res. J. Chem. Environ. 2011. V. 15. № 1. P. 59.
Chen X., Chen G. Electroflotation Electrochemistry for the Environment. New York, Dordrecht, Heidelberg, London: Springer; 2010. 263 p.
Matis K.A. Flotation as a separation process / in: Lehr J.H., Keeley J., eds., Water Encyclopedia. V. 1. Wiley & Sons. 2015. P. 684–688.
Martínez-Huitle C.A., Rodrigo M.A., Scialdone O. Electrochemical water and wastewater treatment. Oxford: Butterworth-Heinemann, an imprint of Elsevier, 2018. P. 556.
Ксенофонтов Б.С. Очистка сточных вод: кинетика флотации и флотокомбайны. ИД “Форум”, ИНФРА-М. 2020. 256 с.
Козодаев А.С., Таранов Р.А., Ксенофонтов Б.С., Воропаева А.А., Виноградов М.С. Петрова Е.В., Иванов М.В. Флотокомбайны – перспективная техника для очистки сточных вод // Научное обозрение. 2015. № 24. С. 128‒138.
Attour, A., Touati, M., Tlili, M., Ben Amor M., Lapicque F., Leclerc J.-P. Influence of operating parameters on phosphate removal from water by electrocoagulation using aluminum electrodes // Sep. Purif. Technol. 2014. V. 123. P. 124–129.
Garcia-Segura S.G, Eiband M.M.S.G., de Melo J.V., Martínez-Huitle C.A. Electrocoagulation and advanced electrocoagulation processes: A general review about the fundamentals, emerging applications and its association with other technologies // J. Electroanal. Chem. 2017. V. 801. P. 267–299.
Мешалкин В.П., Колесников А.В., Савельев Д.С. Колесников В.А., Белозерский А.Ю., Меньшова И.И., Маслянникова Д.В., Сычева О.В. Анализ физико-химической эффективности электрофлотационного процесса извлечения продуктов гидролиза четыреххлористого титана из техногенных стоков // ДАН. 2019. Т. 486. № 6. С. 680–684. https://doi.org/10.31857/S0869-56524866680-684
Мешалкин В.П., Колесников В.А., Десятов А.В., Милютина А.Д, Колесников А.В. Физико-химическая эффективность процесса электрофлотации высокодисперсного углеродного наноматериала из водных растворов с поверхностно-активными веществами // ДАН. 2017. Т. 476. № 2. С. 166–169. https://doi.org/10.7868/S0869565217260103
Мешалкин В.П., Колесников А.В., Милютина А.Д., Десятов А.В., Колесников В.А. Экспериментальные исследования межфазных явлений на инновационных углеродных наноматериалах в водных растворах электролитов // ДАН. 2017. Т. 474. № 5. С. 585–588. https://doi.org/10.7868/S0869565217050139
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах


