Доклады Российской академии наук. Химия, науки о материалах , 2020, T. 495, № 1, стр. 46-53
Метод получения графена, допированного атомами азота, с высокой удельной поверхностью
В. В. Чесноков 1, А. С. Чичкань 1, *, Д. А. Свинцицкий 1, Е. Ю. Герасимов 1, академик РАН В. Н. Пармон 1
1 Институт катализа им. Г.К. Борескова
Сибирского отделения Российской академии наук
Новосибирск, Россия
* E-mail: AlexCsh@yandex.ru
Поступила в редакцию 24.07.2020
После доработки 15.09.2020
Принята к публикации 30.10.2020
Аннотация
Разработан метод получения графена, допированного атомами азота (N-графен), с высокой удельной поверхностью. Метод состоит в использовании в качестве темплата оксида магния, на котором происходит отложение углеродного слоя, модифицированного атомами азота. Синтезирована серия азот–углерод-минеральных композитов N–С/MgO с содержанием углерода, модифицированного азотом, от 5 до 27 мас. %. После вытравливания оксида магния впервые был получен N-графен с удельной поверхностью 1300–1400 м2 г–1. Получение N-графена подтверждено методами электронной микроскопии, рентгеновской дифракции и рентгеновской фотоэлектронной спектроскопии.
ВВЕДЕНИЕ
Графен представляет собой двумерный кристалл, состоящий из гексагонально-связанных атомов углерода [1]. Графен обладает уникальными как электропроводящими, так и механическими свойствами. Разработка подобных материалов и развитие методов их получения очень важны в связи с большим потенциалом их использования в электрохимических процессах и катализе [2, 3]. Потенциал применения графена может быть расширен за счет модифицирования его атомами азота. По сравнению с атомами углерода атомы азота, встроенные в углеродную сетку графена, обладают способностью образовывать более прочные связи с атомами нанесенных металлов (Pd, Pt, Ni). Эта особенность N-графена открывает возможности синтеза высокодисперсных, вплоть до атомарных, частиц металлов [4, 5].
В принципе, в качестве исходного оксида, на котором формируется N-графен, можно использовать оксиды: SiO2, γ-Al2O3 и MgO. Однако силикагель (SiO2) обладает узкими порами, и очень сложно эти поры равномерно покрыть тонким слоем модифицированного углерода. При использовании γ-Al2O3 в качестве темплата нам удалось равномерно зауглеродить внутреннюю поверхность пор оксида тонким слоем углерода. Однако не удалось вытравить оксид алюминия из такого синтезированного углерод-минерального композита [6].
В работе [7] было показано, что использование оксида магния в качестве подложки позволяет получить равномерное распределение графеновых слоев.
Получение графена, модифицированного атомами азота, возможно двумя методами. Первый метод представляет собой прямой синтез N-графена с использованием смеси метана и аммиака [8, 9]. Синтез N-графена проводился на поликристаллической металлической (никелевой или медной) фольге методом химического газофазного осаждения (CVD).
Второй метод состоит в постсинтезной обработке образцов графена с использованием плазменной обработки [10, 11] или химических реакций [12, 13].
В работе [14] был осуществлен синтез графена, недопированного и допированного азотом, на отдельном полированном кристалле MgO с ориентацией (100). Кристалл имел размеры 10 × 5 × 0.5 мм. В качестве прекурсоров использовали бензол и пиридин. Синтезированный допированный графен имел небольшое количество монослоев (от двух до пяти) и высокое содержание азота. По-видимому, этот метод может найти применение в микроэлектронике.
В работе [15] предложен метод получения графена из азотсодержащего предшественника ацетонитрила на микрогранулах MgO. В статье содержание азота в синтезированном графене не указано. Синтезированный углеродный материал имеет низкую удельную поверхность – 175 м2 г–1, поэтому должен быть [10–15] многослойным. Такой углеродный материал можно отнести скорее к графиту. Анализ литературных данных показывает, что имеющиеся методы [16] не позволяют получать N-графен с высокой удельной поверхностью и малым (от 2 до 5) количеством графеновых слоев.
Цель этой работы – разработка метода синтеза графена, модифицированного атомами азота, с высокой удельной поверхностью.
МЕТОДЫ ИССЛЕДОВАНИЯ
В качестве подложки, на которую осаждали графен, использовали оксид магния с удельной поверхностью 70 м2 г–1 (ч. д. а., ГОСТ 4526-75, ОАО “Вектон”, Россия), а газовая смесь состава 40% NH3–1% C2H2–C2H4 была выбрана в качестве источника каталитического углерода.
Исследование структуры и микроструктуры образцов осуществляли методом просвечивающей электронной микроскопии высокого разрешения на электронном микроскопе ThemisZ (Thermo Fisher Scientific, США) c ускоряющим напряжением 200 кВ и предельным разрешением по решетке 0.07 нм. Запись изображений осуществлялась с помощью ПЗС матрицы Ceta 16 (Thermo Fisher Scientific, США).
Удельную поверхность и пористость получаемых образцов исследовали методом Баррета–Джойнера–Халенды [17, 18] с помощью анализатора удельной поверхности ASAP-2400 (Micromeritics, США).
Методика изучения образцов методом рентгеновской фотоэлектронной спектроскопии (РФЭС) представлена в работе [19]. Для определения качественного химического состава и наличия примесей были сняты обзорные спектры в диапазоне энергий связи 0–1200 эВ и с шагом 1 эВ. Определение количественного химического состава и состояния индивидуальных элементов проводили по основным фотоэлектронным спектрам элементов, снятым с шагом по энергии связи 0.1 эВ. Давление остаточных газов в камере во время съемки не превышало 1 × 10–7 Торр. Основными фоновыми газами являлись CO, CO2, H2. Соотношение концентраций отдельных компонентов в пробе определяли по площади соответствующих линий спектров РФЭС элементов с помощью эмпирических факторов атомной чувствительности (ASF) после регистрации узких районов соответствующих атомных уровней [20].
Оксид магния нагревали в потоке аргона до заданной температуры 650–700°С, затем перекрывали аргон и подавали реакционную смесь. Зауглероживали оксид магния смесью, состоящей из 40 об. % аммиака, 1 об. % ацетилена и 59 об. % этилена (40% NH3–1% C2H2–C2H4), в проточном кварцевом реакторе с весами Мак-Бена, что позволяло непосредственно в ходе опыта контролировать изменение массы образца. Дополнительно количество отложившегося углерода, модифицированного атомами азота, контролировали по его количеству, оставшемуся после травления оксида магния в растворе соляной кислоты.
Способ удаления оксида магния из композита N–С/MgO с помощью раствора соляной кислоты аналогичен ранее использованному в работе [7].
После травления полученный образец N-графена отфильтровывали и на фильтре промывали дистиллированной водой до нейтрального значения рH промывных вод. Синтезированный образец N-графена сушили в муфельной печи при температуре 150°С в течение часа.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В качестве источника каталитического углерода выбран азотсодержащий прекурсор (смесь 40% NH3–1% C2H2–C2H4), так как компоненты этой смеси склонны к образованию углеродных отложений по консекутивному механизму [18], т.е. через реакции полимеризации и конденсации. При использовании газообразной смеси 40% NH3–1% C2H2–C2H4 аммиак может встраиваться в виде азотсодержащих групп в углеродные цепочки промежуточных продуктов в ходе образования углеродных отложений. Таким образом, происходит модификация формирующегося углеродного материала атомами азота.
Результаты исследования влияния времени реакции зауглероживания на количество углерода, модифицированного азотом, отлагающегося на оксиде магния, удельную площадь поверхности и общий объем пор при температуре 650°С представлены в табл. 1. Как видно из табл. 1, увеличение времени реакции зауглероживания оксида магния приводит к увеличению количества отложившегося углерода, модифицированного азотом, что в свою очередь приводит к уменьшению удельной площади поверхности образцов N-графена с 1400 до 1200 м2 г–1.
Таблица 1.
Зависимость характеристик N-графена от времени реакции зауглероживания оксида магния при температуре 650°С
| Образец | Время реакции, мин | Количество углерода, модифи-цированного азотом, мас. % | Sуд, м2 г–1 |
|---|---|---|---|
| N-графен 650-60 | 60 | 5.0 | 1400 |
| N-графен 650-90 | 90 | 6.2 | 1300 |
| N-графен 650-120 | 120 | 9.6 | 1200 |
Проведено исследование пористой структуры исходного MgO и композита N–С/MgO, и на рис. 1 представлены зависимости распределения пор по размерам.
Из рис. 1 следует, что после отложения углерода, модифицированного азотом, на оксиде магния распределение пор по размерам изменяется незначительно, лишь несколько снижается высота пика. Полученные данные свидетельствуют об отсутствии блокировки пор углеродом и его равномерном распределении по поверхности оксида магния. На рис. 2 представлено распределение пор по размерам для N-графена.
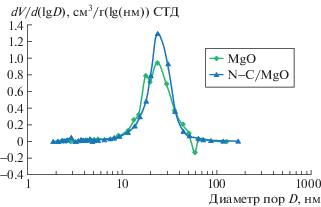
Рис. 2.
Распределение объема пор по размерам, определенное методом Баррета–Джойнера–Халенды (адсорбционная ветвь).
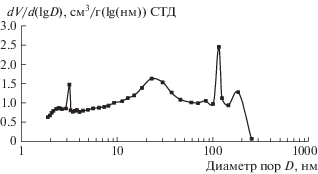
Видно, что N-графен содержит микропоры размером 2–3 нм и мезопоры размером 20–50 нм. Оценка количества микропор показала, что их вклад в удельную поверхность N-графена может достигать 25%. Так как удельная поверхность идеального монослоя атомов углерода может достигать 2675 м2 г–1 [21], то удельная поверхность без учета микропор составляет максимум 975 и 1050 м2 г–1 для образцов N-графена 650-90 и N-графена 650-60 соответственно; толщина N-графена составляет около 3 монослоев.
Повышение температуры реакции зауглероживания до 700°С приводит к увеличению скорости отложения углерода, модифицированного азотом, на оксиде магния из смеси 40% NH3–1% C2H2–C2H4. При этой температуре была получена вторая серия N–C/MgO материалов. Варьируя время реакции от 30 до 120 мин, получили следующие образцы: N–C/MgO 700-30, N–C/MgO 700-60, N–С/MgO 700-90, N–С/MgO 700-120. После удаления из вышеперечисленных композиционных N-С/MgO материалов оксида магния была получена серия образцов N-графена 700.
Установлено, что повышение температуры реакции приводит к уменьшению удельной поверхности N-графена (табл. 2), что, вероятно, связано с менее однородным отложением углерода, модифицированного азотом, на поверхности оксида магния.
Таблица 2.
Зависимость характеристик N-графена от времени реакции зауглероживания оксида магния при температуре 700°С
| Образец | Время реакции, мин | Количество углерода, модифи-цированного азотом, мас. % | Sуд, м2 г–1 |
|---|---|---|---|
| N-графен 700-30 | 30 | 5.8 | 1300 |
| N-графен 700-60 | 60 | 13 | 900 |
| N-графен 700-90 | 90 | 20 | 650 |
| N-графен 700-120 | 120 | 27 | 550 |
Фазовый состав композитов N–C/MgO и N-графена
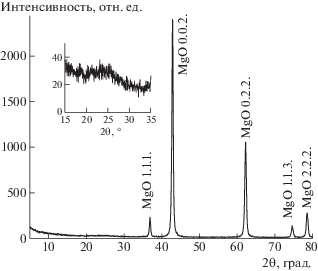
Дифрактограмма образца композита N–С/MgO представлена на рис. 3. На дифрактограмме видны пики, соответствующие оксиду магния (№ ICSD 26958, кубическая сингония, а = 4.22 Å). Размеры области когерентного рассеяния (ОКР) оксида магния 30–50 нм в разных направлениях. При увеличении дифрактограммы (см. вставку к рис. 3) заметен широкий максимум при 2θ = 25°, который, скорее всего, принадлежит турбостратному углероду.
Рис. 3.
Дифрактограмма образца композита N–С/MgO. На вставке – увеличенный фрагмент дифрактограммы с максимумом, относящимся к углеродсодержащей фазе.
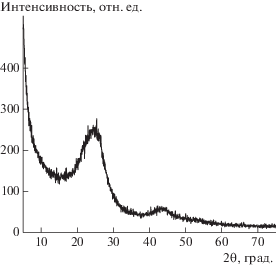
После удаления оксида магния из композита N–С/MgO оставшийся углеродный материал, модифицированный азотом, был также исследован методом рентгеновской дифракции (рис. 4).
Графитоподобная фаза в травленом образце представлена широкими гало в областях 2θ 15°–30° и 40°–48°. Степень разупорядоченности N-графена 650-90 высокая. Размеры ОКР турбостратного углерода в образце N-графен 650-90 – 1.4 нм (рис. 4).
Исследование методом РФЭС образцов N-графена
Методом РФЭС проведено исследование двух серий образцов N-графена, полученных после обработки в смеси 40% NH3–1% C2H2–C2H4 при температурах 650 и 700°C. Для всех синтезированных образцов N-графена были сняты обзорные спектры. Анализ линий на обзорных спектрах позволил установить присутствие на поверхности всех образцов таких элементов, как углерод (C1s), кислород (O1s), азот (N1s) и хлор (Cl2p). Присутствие хлора в составе всех образцов можно объяснить остаточными количествами после травления в растворе соляной кислоты.
Количественный анализ элементов, обнаруженных на поверхности синтезированного N-графена, представлен в табл. 3 и 4. Отметим, что концентрация азота на поверхности была выше для образцов, полученных при температуре 650°C по сравнению с температурой роста, равной 700°C. Максимальная концентрация азота была найдена на поверхности образца N-графена 650-90. Такие же зависимости наблюдались для кислорода.
Таблица 3.
Массовые концентрации элементов на поверхности образцов N-графена, полученных по данным метода РФЭС, в зависимости от времени синтеза. Температура 650°C
| Образец | C, % | N, % | O, % | Cl, % |
|---|---|---|---|---|
| N-графен 650-60 | 88.2 | 4.1 | 7.0 | 0.70 |
| N-графен 650-90 | 88.5 | 5.0 | 6.0 | 0.50 |
| N-графен 650-120 | 89.2 | 3.6 | 6.5 | 0.70 |
Таблица 4.
Массовые концентрации элементов на поверхности образцов N-графена по данным метода РФЭС в зависимости от времени синтеза. Температура 700°C
| Образец | C, % | N, % | O, % | Cl, % |
|---|---|---|---|---|
| N-графен 700-30 | 91.1 | 3.4 | 5.1 | 0.40 |
| N-графен 700-60 | 91.0 | 2.9 | 5.8 | 0.30 |
| N-графен 700-90 | 92.1 | 2.3 | 5.3 | 0.30 |
| N-графен 700-120 | 92.2 | 1.9 | 5.6 | 0.30 |
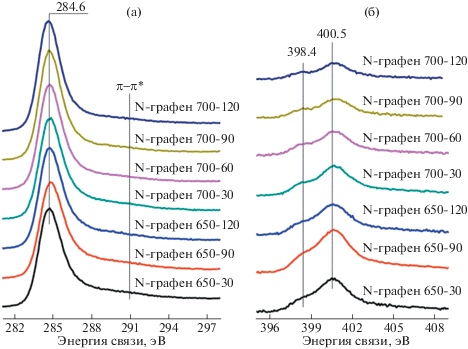
Нормированные спектральные регионы C1s и N1s для изученных углеродных образцов представлены на рис. 5.
Основной C1s-пик для всех образцов характеризуется типичным положением для sp2-гибридизованного углерода 284.6 эВ, что дополнительно подтверждалось характерным сателлитом в области ~291 эВ, обусловленным π → π* переходом. В целом формы спектральной линии N1s для всех образцов были подобны, что указывает на близкий набор состояний азота на их поверхности.
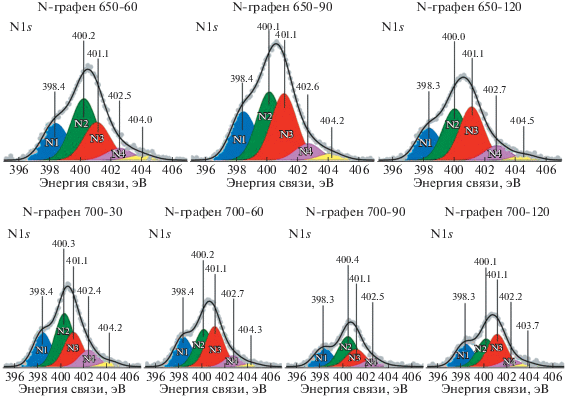
На рис. 6 представлены разложенные на компоненты спектры N1s для всех изученных углеродных образцов N-графена. Для разложения этих спектральных регионов использовали пять компонент с энергиями связи пика ~398.4 (N1), ~400.2 (N2), ~401.1 (N3), ~402.2–402.7 (N4) и 403.7–404.5 (N5) эВ.
В соответствии с литературными данными [21, 24] компоненты N1 и N3 могут быть отнесены к пиридино- и графито-подобной азотным формам. Компоненту N2, характеризующуюся промежуточной между N1 и N3 энергией связи, относят к пиррольным или аминогруппам на поверхности углеродных материалов. Компонента N4 типично относится к слабо окисленным азотным формам в виде, например, оксида пиридина. В качестве интерпретации компоненты N5 c энергией связи >403 эВ можно рассматривать глубоко окисленные формы NOx (например, нитриты). Количественные данные о распределении различных форм азота на поверхности всех образцов представлены в табл. 5.
Таблица 5.
Доли различных форм азота на поверхности N-графена
| Образец | N1, % | N2, % | N3, % | N4, % | N5, % |
|---|---|---|---|---|---|
| N-графен 650-60 | 24 | 40 | 25 | 8 | 3 |
| N-графен 650-90 | 23 | 34 | 32 | 8 | 3 |
| N-графен 650-120 | 21 | 33 | 34 | 9 | 3 |
| N-графен 700-30 | 24 | 37 | 24 | 11 | 4 |
| N-графен 700-60 | 25 | 31 | 33 | 9 | 2 |
| N-графен 700-90 | 25 | 37 | 27 | 10 | 1 |
| N-графен 700-120 | 24 | 30 | 34 | 8 | 4 |
Следует отметить, что основными формами азота в составе углеродных материалов N-графена являются компоненты N1–N4, в то время как компонента N5 с концентрацией не выше 4% является примесной.
Электронно-микроскопическое исследование N-графена
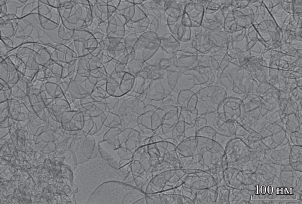
Структура синтезированных образцов N-графена изучена с помощью электронной микроскопии. На рис. 7 представлен электронно-микроскопический снимок N-графена, полученного при температуре 650°C.
Видно, что частицы N-графена 650-90 имеют сферическую форму. Размер сфер 20–100 нм соответствует размерам кристаллов оксида магния в композите N–C/MgO. Полученная структура отражает темплатный метод синтеза N-графена. На рис. 8 представлен электронно-микроскопический снимок N-графена 650-90, полученный с бóльшим увеличением.
На рис. 8 видны отдельные слои N-графена. Толщина стенок сфер N-графена составляет 2–4 монослоя, что согласуется с оценкой толщины графена, полученной на основании измерения удельной поверхности и пористости.ЗАКЛЮЧЕНИЕ
Разработан метод получения графена, модифицированного атомами азота. Метод состоит в синтезе композита N–C/MgO в результате обработки оксида магния в смеси 40% NH3–1% С2Н2–C2H4 при температурах 650 и 700°С. Количество отложившегося углерода и, соответственно, толщину N-графенового слоя возможно контролировать временем зауглероживания оксида магния. Оксид магния из композита N–C/MgO удаляли обработкой раствором соляной кислоты.
Впервые получен N-графен с удельной площадью поверхности 1400 м2 г–1 и толщиной 2–4 монослоя. Максимальное содержание атомарного азота в N-графене составило 5 мас. %. Повышение температуры обработки оксида магния в смеси 40% NH3–1% С2Н2–C2H4 с 650 до 700°С приводит к уменьшению как удельной поверхности N-графена, так и содержания в нем азота.
Увеличение содержания азота и высокая удельная поверхность материала N-графена позволят повысить количество металлических центров (Pt, Pd) на поверхности графена, что в свою очередь должно привести к увеличению активности катализаторов в реакциях селективного гидрирования органических соединений с тройной связью.
Таким образом, синтезированный в настоящей работе N-графен значительно превосходит по качеству имеющиеся материалы, данные о которых представлены в литературе [8–15].
Список литературы
Novoselov K.S., Geim A.K., Morozov S.V., Jiang D., Zhang Y., Dubonos S.V., Grigorieva I.V., Firsov A.A. // Science. 2004. V. 306. № 5696. P. 666–669. https://doi.org/10.1126/science.1102896
Ning G., Fan Z., Wang G., Gao J., Qian W., Wei F. // Chem. Comm. 2011. V. 47. № 21. P. 5976–5978. https://doi.org/10.1039/c1cc11159k
Bulushev D.A., Zacharska M., Shlyakhova E.V., Chuvilin A.L., Guo Y., Beloshapkin S., Okotrub A.V., Bulusheva L.G. // ACS Catal. 2016. V. 6. № 2. P. 681–691. https://doi.org/10.1021/acscatal.5b02381
Чесноков В.В., Кривенцов В.В., Малыхин С.Е., Чичкань А.С., Подъячева О.Ю. // Журнал структурной химии. 2018. Т. 59. № 4. С. 876–882. https://doi.org/10.26902/jsc20180412
Chesnokov V.V., Kriventsov V.V., Malykhin S.E., Svintsitskiy D.A., Podyacheva O.Y., Lisitsyn A.S., Ri-chards R.M. // Diamond and Related Materials. 2018. V. 89. P. 67–73. https://doi.org/10.1016/j.diamond.2018.08.007
Chesnokov V.V., Chichkan A.S., Bedilo A.F., Shuvarakova E.I. // Fullerenes Nanotubes and Carbon Nanostructures. 2020. V. 28. № 5. P. 402–406. https://doi.org/10.1080/1536383x.2019.1695249
Chesnokov V.V., Chichkan A.S., Bedilo A.F., Shuvarakova E.I., Parmon V.N. // Dokl. Phys. Chem. 2019. V. 488. P. 154–157. https://doi.org/10.1134/S0012501619100038
Qu L., Liu Y., Baek J.-B., Dai L. // ACS Nano. 2010. V. 4. № 3. 1321–1326. https://doi.org/10.1021/nn901850u
Zhao L., He R., Rim K.T., Schiros T., Kim K.S., Zhou H., Gutiérrez Ch., Chockalingam S.P., Arguello C.J., Pálová L., Nordlund D., Hybertsen M.S., Reichman D.R., Heinz T.F., Kim Ph., Pinczuk A., Flynn G.W., Pasupathy A.N. // Science. 2011. V. 333. № 6045. P. 999–1003. https://doi.org/10.1126/science.1208759
Moon J., An J., Sim U., Cho S.-P., Kang J.H., Chung C., Seo J.-H., Lee J., Nam K.T., Hong B.H. // Adv. Mater. 2014. V. 26. P. 3501–3505. https://doi.org/10.1002/adma.201306287
Rybin M., Pereyaslavtsev A., Vasilieva T., Myasnikov V., Sokolov I., Pavlova A., Obraztsova E., Khomich A., Ralchenko V., Obraztsova E. // Carbon. 2016. V. 96. P. 196–202. https://doi.org/10.1016/j.carbon.2015.09.056
Deng D., Pan X., Yu L., Cui Y., Jiang Y., Qi J., Li W.-X., Fu Q., Ma X., Xue Q., Sun G., Bao X. // Chem. Mater. 2011. V. 23. № 5. P. 1188–1193. https://doi.org/10.1021/cm102666r
Reddy A.L.M., Srivastava A., Gowda S.R., Gullapalli H., Dubey M., Ajayan P.M. // ACS Nano. 2010. V. 4. № 11. P. 6337–6342. https://doi.org/10.1021/nn101926g
Zhao J., Zhu G., Huang W., He Z., Feng X., Ma Y., Dong X., Fan Q., Wang L., Hu Z., Lu Y., Huang W. // J. Mater. Chem. 2012. V. 22. № 37. P. 19679–19683. https://doi.org/10.1039/c2jm33209d
Wang H., Maiyalagan T., Wang X. // ACS Catal. 2012. V. 2. № 5. P. 781–794. https://doi.org/10.1021/cs200652y
Jin Z., Yao J., Kittrell C., Tour J. M. // ACS Nano. 2011. V. 5. № 5. P. 4112–4117. https://doi.org/10.1021/nn200766e
Pan W., He M., Zhang L., Hou Y., Chen C. // Nanomaterials. 2019. V. 9. № 5. P. 798. https://doi.org/10.3390/nano9050798
Буянов Р.А. Закоксование катализаторов / М., Наука, 1983. 207 с.
Gor G.Yu., Thommes M., Cychosz K.A., Neimark A.V. // Carbon. 2012. V. 50. P. 1583–1590. https://doi.org/10.1016/j.carbon.2011.11.037
Thommes M., Kaneko K., Neimark A.V., Olivier J.P., Rodriguez-Reinoso F., Rouquerol J., Sing K.S.W. // Pure Appl. Chem. 2015. V. 87. P. 1051–1069. https://doi.org/10.1515/pac-2014-1117
Чесноков В.В., Чичкань А.С., Паукштис Е.А., Свинцицкий Д.А., Исмагилов З.Р., Пармон В.Н. // ДАН. 2017. Т. 476. № 5. С. 535–538. https://doi.org/10.7868/S0869565217290126
Moulder J.F., Stickle W.F., Sobol P.E., Bomben K.D. Handbook of X-Ray Photoelectron Spectroscopy / Perkin-Elmer Corp, Eden Prairie, Minnesota, USA, 1992.
Yang H., Kannappan S., Pandian A.S., Jang J-H., Lee Y.S., Lu W. // J. Power Sources. 2015. V. 284. P. 146–153. https://doi.org/10.1016/j.jpowsour.2015.03.015
Arrigo R., Schuster M.E., Xie Z., Yi Y., Wowsnick G., Sun L.L., Hermann K.E., Friedrich M., Kast P., Häve-cker M., Knop-Gericke A., Schlögl R. // ACS Catal. 2015. V. 5. P. 2740–2753. https://doi.org/10.1021/acscatal.5b00094
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах