Доклады Российской академии наук. Химия, науки о материалах , 2020, T. 495, № 1, стр. 5-8
Электронное состояние наночастиц серебра при их фотохимическом образовании в деаэрированном водном растворе
В. А. Ершов 1, 2, член-корреспондент РАН Н. П. Тарасова 1, *, член-корреспондент РАН Б. Г. Ершов 2
1 Российский химико-технологический университет им. Д.И. Менделеева
Москва, Россия
2 Институт физической химии и электрохимии
им. А.Н. Фрумкина Российской академии наук
Москва, Россия
* E-mail: tarasnp@muctr.ru
Поступила в редакцию 30.07.2020
После доработки 30.08.2020
Принята к публикации 29.09.2020
Аннотация
Впервые обнаружен и обоснован эффект увеличения электронной плотности в наночастицах серебра в процессе их образования при фотохимическом восстановлении ионов Ag+ в присутствии оксалата. Эффект вызывает смещение полосы локализованного поверхностного плазмонного резонанса и уменьшение ее ширины от 402 до 383 нм. Выявлена количественная взаимосвязь между величиной сдвига полосы и плотностью электронов. Наблюдаемый сдвиг на 19 нм соответствует увеличению концентрации электронов в наночастицах примерно на 10%. Обнаруженный эффект, возможно, является общим и для других металлов и влияет на эффективность протекания разнообразных каталитических реакций с участием металлов в наноразмерном состоянии.
ВВЕДЕНИЕ
Коллоидные растворы металлов поглощают свет в УФ- и видимой областях спектра [1–4]. Поглощение обусловлено возбуждением поверхностных плазмонов ультрамалых частиц металлов и межзонными электронными переходами. В случае сферических наночастиц (НЧ) серебра малого размера (4–20 нм) полоса локализованного поверхностного плазмонного резонанса (ЛППР) находится в области 370–430 нм, а нижняя граница межзонного электронного перехода (МЗЭП) 4d → 5sp начинается примерно при 320 нм и продолжается в сторону меньших длин волн. Поглощение ЛППР в случае гидрозолей золота и серебра очень чувствительно к состоянию поверхности наночастиц. Спектрофотометрический анализ дает возможность получить полезную информацию о состоянии частицы и ее стабилизирующего слоя, сорбции молекул с донорными и акцепторными свойствами и о других факторах, вызывающих изменение электронного состояния частицы. В результате адсорбции и десорбции молекул и ионов изменяется плотность электронов проводимости в металле, что приводит к сдвигу полосы поглощения. Адсорбция молекул и ионов с донорными свойствами вызывает смещение полосы ЛППР в сторону коротких длин волн и, напротив, адсорбция молекул и ионов с акцепторными свойствами – в сторону длинных волн [5–8]. В отличие от ЛППР, МЗЭП вызваны возбуждением внутренних валентных электронов металла (4d → 5sp). Внешние “слабые” воздействия, связанные с хемосорбцией и другими процессами на поверхности, заметно не отражаются на поглощении МЗЭП, в отличие от поглощения ЛППР. Для наночастиц малого размера поглощение МЗЭП пропорционально концентрации атомов металла.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Использовались моногидрат перхлората серебра (AgClO4 · H2O, 99%, “Sigma Aldrich”) и оксалат калия (K2C2O4, 99.9% “ос. ч.”, Reakhim). Приготовление “чистого” гидрозоля серебра, содержащего наночастицы серебра и стабилизирующие их карбонат-ионы, проводилось путем восстановления ионов серебра оксалат-ионами под воздействием импульсного УФ-излучения [9]. Раствор предварительно деаэрировался вакуумированием. Облучение проводилось в стеклянном сосуде, снабженном кварцевой кюветой (объем кюветы 2 или 4 мл) с длиной оптического пути 5 или 10 мм. Растворы облучали светом импульсной ксеноновой лампы с суммарной интенсивностью потока излучения IUV = 6.0 × 1020 квант с–1.
Оптические спектры измеряли на спектрофотометре Cary 100 Scan (Varian Inc., США), снабженным термостатической ячейкой Пельтье, при температуре 293 К. Гидродинамический размер (d) и ζ-потенциал НЧ серебра определяли методом динамического рассеяния света (ДРС) на приборе Delsa Nano C (Beckman Coulter, Inc., США). Длина волны рассеянного лазерного излучения λ = 658 нм. Размеры и полидисперсность НЧ определяли методом просвечивающей электронной микроскопии (ПЭМ) на приборе JEM-2100 (TEM) (JEOL, Япония), работающего при ускоряющем напряжении 200 кВ.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В согласии с данными работы [9], УФ-облучение деаэрированного раствора, содержащего ионы Ag+ с концентрацией (1–3) × 10–4 моль л–1 и оксалат-ионы с концентрацией (2–5) × 10–4 моль л–1, инициирует образование устойчивого гидрозоля серебра. Процесс обусловлен фотохимическим разложением оксалат-ионов и образованием ион-радикалов ${\text{CO}}_{2}^{{ - .}}$, которые восстанавливают ионы Ag+ до атомов Ag0 с последующей их агломерацией до НЧ металла. Ионы ${\text{НСО}}_{3}^{ - }$ и ${\text{СО}}_{3}^{{2 - }}$ обеспечивают электростатическую стабилизацию гидрозоля металла [10].
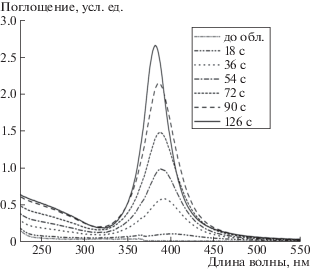
В оптическом спектре гидрозоля (рис. 1) интенсивность полос ЛППР и МЗЭП в процессе фотохимического восстановления ионов Ag+ возрастает.
Рис. 1.
Спектры оптического поглощения гидрозоля серебра в процессе восстановления ионов Ag+ (толщина оптической ячейки 5 мм). Раствор: 3 × 10–4 моль л–1 ионов Ag+ и 5 × 10–4 моль л–1 ионов ${{{\text{С}}}_{{\text{2}}}}{\text{О}}_{4}^{{2 - }}$.
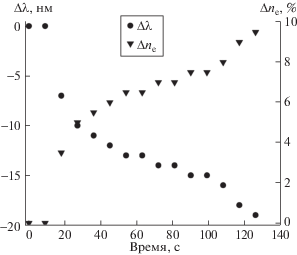
На рис. 2 показана зависимость смещения максимума поглощения полосы ЛППР Δλ от времени УФ-воздействия.
Здесь Δλ = λt – λt0, где λt и λt0 – положения максимумов полосы поглощения ЛППР на текущий и начальный момент УФ-воздействия. Сдвиг в синюю область спектра при полном восстановлении серебра составляет 19 нм (от 402 до 383 нм), а ширина изменяется примерно от 80 до 40 нм. В отличие от ЛППР, поглощение МЗЭП увеличивается в процессе фотохимического восстановления серебра без изменения положения и формы полосы. Интенсивность поглощения пропорциональна концентрации НЧ серебра.
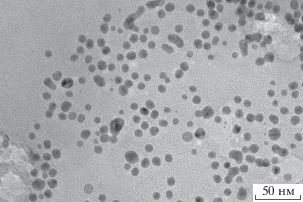
Данные ПЭМ (рис. 3) указывают на образование сферических НЧ серебра со средним размером 10.4 нм.
Рис. 3.
Изображение ПЭМ наночастиц серебра. Раствор: 3 × 10–4 моль л–1 ионов Ag+ и 5 × 10–4 моль л–1 ионов ${{{\text{С}}}_{{\text{2}}}}{\text{О}}_{4}^{{2 - }}$.
Размер мицеллы, которая, помимо металлического ядра, включает также и лигандное окружение, измеренный методом ДРС, составил 12.5 нм. В процессе формирования гидрозоля было сделано несколько измерений методом ДРС, значения составили 11–13 нм, т.е. заметного увеличения размера при последующем фотохимическом восстановлении ионов Ag+ не происходило. По-видимому, это является следствием того, что ион-радикалы ${\text{CO}}_{2}^{{ - \cdot }}$ восстанавливают ионы Ag+ до атомов Ag0 в объеме раствора, чему благоприятствует соотношение потенциалов: E0(CO2/${\text{CO}}_{2}^{{ - .}}$) = –1.9 В [11] и E0(Ag+/Ag0) = –1.8 В [12]. Соответствующая реакция (1) протекает с очень высокой скоростью [14]:
(1)
$\begin{gathered} {\text{A}}{{{\text{g}}}^{ + }} + {\text{CO}}_{2}^{{ - .}} \to {\text{A}}{{{\text{g}}}^{0}} + {\text{C}}{{{\text{O}}}_{2}} \\ k = 4 \times {{10}^{9}}\;{\text{л}}\;{\text{мол}}{{{\text{ь}}}^{{--1}}}\;{{{\text{с}}}^{{--1}}}. \\ \end{gathered} $В дальнейшем возникают короткоживущие кластеры серебра (${\text{Ag}}_{2}^{ + }$, ${\text{Ag}}_{3}^{{2 + }}$, ${\text{Ag}}_{4}^{{2 + }}$, ${\text{Ag}}_{8}^{{2 + }}$ и др.), агломерация которых, независимо от уже имеющейся фазы металла, завершается образованием НЧ [13]. По-видимому, импульсное воздействие УФ-света преимущественно увеличивает число НЧ в объеме раствора, но заметно не влияет на их размеры. Это отличает фотохимический метод генерации частиц серебра от других, где применяются реагенты с меньшим восстановительным потенциалом, чем у анион-радикала ${\text{CO}}_{2}^{{ - .}}$. Поэтому при их применении реализуется автокаталитический механизм восстановления ионов Ag+ на поверхности возникающих НЧ, приводящий к увеличению их размера.
Согласно теории Ми–Друде [14, 15] исходные и финальные положения полос ЛППР (${\lambda }_{{{\text{max}}}}^{i}$ и ${\lambda }_{{{\text{max}}}}^{f}$) НЧ малого размера связаны с относительными концентрациями электронов в них (${\text{N}}_{{\text{e}}}^{i}$ и ${\text{N}}_{{\text{e}}}^{f}$) следующим уравнением:
(2)
$\frac{{{\text{N}}_{e}^{f}}}{{{\text{N}}_{e}^{i}}} = {{\left( {\frac{{\lambda _{{\max }}^{i}}}{{\lambda _{{\max }}^{f}}}} \right)}^{2}}.$Уравнение позволяет оценить изменение относительной концентрации электронов в металле по сдвигу полосы ЛППР. В работе [8] для выявления характера аналитической зависимости смещения полосы ЛППР Δλ от изменения электронной плотности Δne это уравнение было преобразовано к виду (3):
(3)
$\Delta {{n}_{{\text{e}}}} \approx \frac{{\lambda _{{\max }}^{f}}}{{\lambda _{{\max }}^{i}}}\Delta \lambda .$Полученное уравнение устанавливает зависимость изменения относительной концентрации электронов в наночастице ∆nе от смещения полосы ЛППР ∆λ. Чем больше смещение в синюю область (–Δλ), тем больше концентрация электронов в металле (рис. 1).
Видно, что смещение на 19 нм в синюю область спектра вызвано увеличением плотности свободных электронов в них примерно на 10%. Ионы Ag+, адсорбированные на поверхности наночастиц, проявляют свойства акцептора, оттягивая на себя электроны проводимости в металле. В процессе фотохимического восстановления их концентрация в растворе уменьшается, что влечет за собой снижение концентрации адсорбированных ионов Ag+ вследствие сдвига равновесия (4) вправо:
ЗАКЛЮЧЕНИЕ
Впервые установлено, что с уменьшением концентрации ионов Ag+, адсорбированных на НЧ серебра, концентрация электронов проводимости в НЧ увеличивается. Структура двойного электрического слоя в процессе формирования НЧ непрерывно изменяется. Это прослеживается по постепенному смещению полосы ЛППР, вызванному изменением заряда наночастицы, что, в свою очередь, обусловлено изменением состава раствора – снижением плотности потенциал-образующих ионов Ag+ на поверхности, уменьшением концентрации расходуемых при фотолизе ионов С2О$_{4}^{{2 - }}$ и образованием стабилизирующих карбонат-ионов. Обнаруженный на примере серебра эффект изменения электронной плотности наночастиц в процессе их окислительно-восстановительного образования, возможно, является общим и для других металлов. Это обстоятельство представляется нам важным, поскольку предполагает возможность влияния этого фактора (электронной зарядки-разрядки наночастиц) на эффективность протекания разнообразных каталитических реакций с участием металлов в наноразмерном состоянии.
Список литературы
Mie G. // Ann. Phys. 1908. V. 330. № 3. P. 377–445. https://doi.org/10.1002/andp.19083300302
Van de Hulst H.C. Light scattering by small particles. New York: John Wiley and Sons, London: Chapman and Hall, 1957. https://doi.org/10.1002/qj.49708436025
Kerker M. The Scattering of Light and Other Electromagnetic Radiation. New York: Academic Press, 1969.
Creighton J.A., Eadon D.G. // J. Chem. Soc., Faraday Trans. 1991. V. 24. P. 3881–3891. https://doi.org/10.1039/FT9918703881
Herne T.M., Ahern A.M., Garrell R.L. // J. Am. Chem. Soc. 1991. V. 113. P. 846–854. https://doi.org/10.1021/ja00003a018
Henglein A. // J. Phys. Chem. 1993. V. 97. P. 5457–5471. https://doi.org/10.1021/j100123a004
Ershov B.G., Abkhalimov E.V., Roldughin V. I., Rudoy V.M., Dement’eva O.V., Solovov R.D. // Phys. Chem. Chem. Phys. 2015. V. 17. № 28. P. 18431–18436. https://doi.org/10.1039/C5CP02326B
Ershov B.G., Abkhalimov E.V., Solovov R. D., Roldu-ghin V.I. // Phys. Chem. Chem. Phys. 2016. V. 18. P. 13459–13466. https://doi.org/10.1039/C6CP01996J
Abkhalimov E.V., Ershov V.A., Ershov B.G. // J. Nanopart. Res. 2019. V. 21. P. 93. https://doi.org/10.1007/s11051-019-4538-x
Abkhalimov E.V., Parsaev A.A., Ershov B.G. // Colloid J. 2011. V. 73. P. 1–5. https://doi.org/10.1134/S1061933X11010029
Wardman P. // J. Phys. Chem. Ref. Data. 1989. V. 18. P. 1637–1755. https://doi.org/10.1063/1.555843
Henglein A. // Ber. Bunsen-Ges. Phys. Chem. 1990. V. 94. P. 600–603. https://doi.org/10.1002/bbpc.19900940513
Ershov B.G., Janata E., Henglein A. // J. Phys. Chem. 1993. V. 97. P. 339–343. https://doi.org/10.1021/j100104a013
Boronina T., Klabunde K.J., Sergeev G. // Environ. Sci. Technol. 1995. V. 29. P. 1511–1517. https://doi.org/10.1021/es00006a012
Doremus R.H. // J. Chem. Phys. 1965. V. 42. № 1. P. 414–417. https://doi.org/10.1063/1.1695709
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах