Доклады Российской академии наук. Химия, науки о материалах , 2020, T. 495, № 1, стр. 30-34
Термодинамические аспекты взаимодействия полихлорбифенилов с метоксидом натрия в среде этанола и диметилсульфоксида
А. В. Майорова 1, 2, *, Т. В. Куликова 1, 2, Т. И. Горбунова 3, М. Г. Первова 3, К. Ю. Шуняев 1, 2, Академик РАН Л. И. Леонтьев 1
1 Институт металлургии Уральского отделения Российской академии наук
Екатеринбург, Россия
2 Уральский федеральный университет имени первого Президента России Б.Н. Ельцина
Екатеринбург, Россия
3 Институт органического синтеза им. И.Я. Постовского Уральского отделения
Российской академии наук
Екатеринбург, Россия
* E-mail: imeturoran@mail.ru
Поступила в редакцию 12.05.2020
После доработки 18.09.2020
Принята к публикации 26.09.2020
Аннотация
Впервые методом термодинамического моделирования исследовано взаимодействие технической смеси полихлорбифенилов “Совол” с метоксидом натрия в среде диметилсульфоксида и этанола. Установлено, что добавление к диметилсульфоксиду сорастворителя этанола приводит к возникновению и протеканию процесса сольволиза. Найдены оптимальные условия процесса нуклеофильного замещения. С их использованием синтезированы производные полихлорбифенилов со сниженным содержанием хлора. Достигнута высокая степень конверсии исходных конгенеров смеси полихлорбифенилов “Совол”. Изученное взаимодействие может служить стадией предподготовки токсичных полихлорбифенилов для их уничтожения термическими методами.
В настоящее время обезвреживание полихлорбифенилов (ПХБ) остается важной и актуальной задачей [1, 2]. Только применение междисциплинарных подходов позволит достичь прогресса в разработке эффективных схем утилизации этих токсичных хлорсодержащих отходов.
Для предотвращения образования газообразных экотоксикантов (полихлорированных дибензо-п-диоксинов и дибензофуранов (ПХДД и ПХДФ) [3, 4]) при термической утилизации технических смесей ПХБ необходимо предварительно максимально полно удалить хлор из структуры конгенеров (получить предпродукты). Для этого можно использовать реакцию нуклеофильного замещения SN. Известные на данный момент методики удаления хлора из технических смесей ПХБ характеризуются низкой степенью конверсии исходных соединений [5, 6], из-за многокомпонентности состава смеси осуществление полной химической функционализации конгенеров является сложной задачей.
Термодинамическое моделирование (ТДМ) [7] является эффективным инструментом для поиска условий химического взаимодействия, приводящих к полной конверсии конгенеров смесей ПХБ. Метод применялся ранее при оптимизации взаимодействия смеси ПХБ “Совол” в реакции с метоксидом натрия (MeONa) в среде диметилсульфоксида (ДМСО) [8]. При синтезе с использованием условий, предложенных ТДМ, степень конверсии исходных конгенеров значительно увеличивается, но, так как в этих условиях образуются ПХДФ, такая процедура экологически небезопасна.
Избежать образования ПХДФ удалось путем добавления к ДМСО сорастворителя метанола и последующего подбора условий синтеза с помощью ТДМ [9, 10]. Продукты такого взаимодействия представляли собой смесь метокси-, гидрокси- и метоксигидроксипроизводных ПХБ. Полученные предпродукты являлись менее термостабильными соединениями по сравнению с исходными конгенерами смеси “Совол” и при термолизе претерпевали не только стадии испарения, но и процессы разложения до простейших летучих веществ [11].
Установлено, что при проведении реакции нуклеофильного замещения увеличение температуры процесса положительно влияет на степень конверсии исходных конгенеров смесей ПХБ [8, 10]. Поэтому мы предложили использовать смесь с мольным соотношением ДМСО : EtOH = 1 : 3 (Ткип = 145°С) вместо смеси ДМСО : MeOH = 1 : 3 (Ткип = 115°С). Термодеструкция предпродуктов со сниженным содержанием хлора, полученных вследствие большей степени конверсии исходных конгенеров ПХБ, потенциально приведет к снижению уровня выброса газообразных и летучих хлорсодержащих экотоксикантов (ПХДФ, ПХДД, оксидов хлора и фосгена).
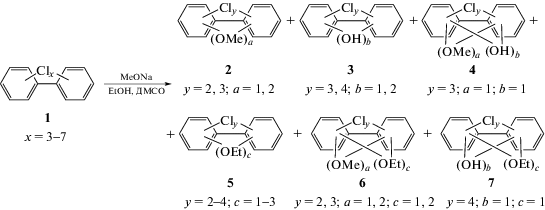
В настоящей работе впервые проведено ТДМ с целью оптимизации взаимодействия смеси ПХБ “Совол” 1 с MeONa в среде ДМСО и EtOH. Мы предположили и затем экспериментально подтвердили, что результатом такого взаимодействия является смесь продуктов шести видов – соединения 2–7 (схема 1).
Подробный алгоритм расчета термохимических свойств соединений представлен в работе [12]. Термохимические свойства для метокси-, гидрокси- и метоксигидроксипроизводных ПХБ (соединения 2–4 соответственно) рассчитаны нами ранее и представлены в работах [8, 10, 12]. Данные по этокси- 5, этокcиметокси- 6 и этоксигидроксипроизводным 7 в литературе отсутствуют. Учитывая все типы функциональных групп в соединениях 5–7 (атомы хлора, гидрокси-, метокси- и этокси-группы) и их количество, перечень всех гипотетически возможных соединений 5–7 насчитывает 125 структур. Рассчитанные свойства для этих 125 производных соединений 5–7 введены в базу данных программного комплекса “HSC Chemistry”, расчеты в котором основаны на принципе минимизации энергии Гиббса системы. В качестве примера в табл. 1 представлены рассчитанные термохимические свойства для трех возможных производных соединений 5–7, выбранные в случайном порядке.
Таблица 1.
Рассчитанные термохимические свойства производных ПХБ 5–7
| Соединение | C12H7Cl2(OC2H5) 5 |
C12H6Cl2(OC2H5)OCH3 6 |
C12H3(OC2H5)3(OH)4 7 |
|
|---|---|---|---|---|
| $\Delta H_{{298}}^{^\circ }$, кДж/моль | –57 | –222 | –1082 | |
| $S_{{298}}^{^\circ }$, Дж/моль K | 542 | 586 | 758 | |
| $\Delta G_{{298}}^{^\circ }$, кДж/моль | 134 | 28 | –637 | |
| $H_{{298}}^{^\circ }$ – $H_{0}^{^\circ }$, кДж/моль | 38 | 44 | 63 | |
| Ср = a + b × 10–3Т + + c × 105Т–2 + d × 10–6Т 2, Дж/моль K | a | 49 | 65 | 117 |
| b | 818 | 883 | 1213 | |
| c | –6.9 | 15.1 | –12.7 | |
| d | –339 | –624 | –513 | |
Проведено моделирование взаимодействия смеси ПХБ “Совол” 1 (0.01 моль) с МеОNa (0.01–0.06 моль) в среде ДМСО (0.26 моль) в отсутствие и в присутствии сорастворителя EtОН (0.087 моль). С помощью программного комплекса CEMCAD установлено и затем экспериментально подтверждено, что температура кипения смеси растворителей ДМСО и EtОН, взятых в указанном мольном соотношении, составляет примерно 130–150°С. ТДМ проводили в расширенном диапазоне температур от 50 до 200°С. Расчет равновесных составов систем, полученных при моделировании взаимодействия конгенеров ПХБ марки “Совол” 1 с МеОNa в среде ДМСО и EtOH, проведен для мольных соотношений от 1 : 1 до 1 : 6.
На рис. 1 в качестве примера представлены результаты ТДМ равновесного состава для мольного соотношения 1 : 4 в отсутствие и в присутствии сорастворителя EtОН.
Рис. 1.
Зависимость равновесного состава конгенеров и производных ПХБ от температуры. Исходный состав: (а) 0.01 моль смесь ПХБ “Совол” 1, 0.04 моль МеОNa, 0.26 моль ДМСО; (б) 0.01 моль смесь ПХБ “Совол” 1, 0.1 моль МеОNa, 0.26 моль ДМСО, 0.087 моль EtОН. Т = 50–200°С, P = 1 атм. Сумма мольных долей всех конгенеров и производных ПХБ равна 1. (а) C12H4(OCH3)6 (кривая 1), C12H7Cl3 (кривая 2), C12H5(OCH3)5 (кривая 3), C12H6(OCH3)4 (кривая 4), C12H7(OCH3)3 (кривая 5), C12H3Cl(OCH3)6 (кривая 6); (б) C12H4Cl2(OCH3)4 (кривая 1), C12H7(OH)3 (кривая 2), C12H5(OC2H5)5 (кривая 3), C12H7(OCH3)3 (кривая 4), C12H5Cl2(OCH3)3 (кривая 5).
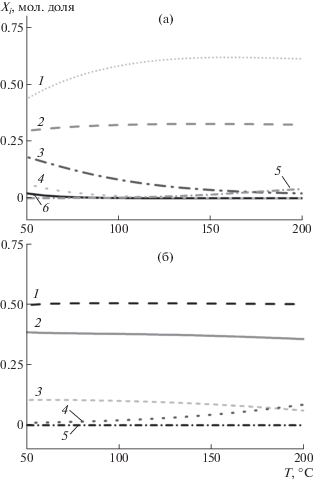
Из рис. 1а видно, что при взаимодействии смеси ПХБ “Совол” 1 с МеONa без добавления EtОН в составе продуктов реакции наибольшую концентрацию из непрореагировавших конгенеров имеет трихлорбифенил (C12H7Cl3). В продуктах реакции с увеличением температуры процесса зафиксированы снижение концентрации C12H7Cl3 и увеличение вклада метоксипроизводных ПХБ 2. Содержание гидроксипроизводных ПХБ 3 в составе продуктов минимально и составило менее 1 × 10–5 мол. долей. Использование смеси растворителей ДМСО/EtОН привело к обнаружению в результирующих продуктах не только метокси-, а также этокси- и гидроксипроизводных ПХБ 2, 5, 3 соответственно (рис. 1б). При этом исходные конгенеры ПХБ отсутствовали. Концентрация “интермедиатов” 4, 6, 7 составляет менее 1 × 10–10 мол. долей. Возможно, в ходе реакции замещения они трансформировались из производных ПХБ 4, 6 в соединения 3, а из производных ПХБ 7 – в соединения 2, которые являются более термодинамически устойчивыми (имеют бóльшие отрицательные значения стандартной энергии Гиббса). Обнаружение в продуктах реакции этоксипроизводных ПХБ 5 связано с протеканием процесса сольволиза, когда растворитель выступает одновременно нуклеофильным агентом. Этим объясняется снижение количества MeONa, необходимого для полной конверсии конгенеров смеси “Совол” 1 (рис. 1б). Однако, как установлено в ходе данного исследования, последующее бесконтрольное увеличение массы сорастворителя невозможно. EtОН является протонным растворителем и экспериментально установлено, что его избыток приводит к ингибированию реакций замещения с МеONa. Оптимальное мольное соотношение, при котором не происходит ингибирования взаимодействия, ДМСО : EtОН = 1 : 3. Это соотношение использовалось в дальнейших исследованиях.
Экспериментальные условия проведения реакции соответствовали оптимальным данным, полученным по результатам ТДМ (мольное соотношение смеси ПХБ 1 : МеОNa = 1 : 4, 0.087 моль EtОН, 0.26 моль ДМСО, Ткип = 145°С). Состав продуктов изучаемого химического взаимодействия конгенеров смеси “Совол” 1 c МеОNa только в ДМСО [8] и в смеси растворителей ДМСО/EtОН сравнивали после проведения реакции в течение 10 ч. По результатам анализа продуктов реакции методом ГХ-МС установлено образование более 80 новых производных. Их среднее относительное содержание по результатам трех экспериментов представлено в табл. 2, среднеквадратическое отклонение составило не более 3%.
Таблица 2.
Данные по продуктам взаимодействия смеси ПХБ “Совол” 1 с MeONa в среде ДМСО и EtOH при Т = 145°С, время реакции 10 ч
| № соед. согласно схеме 1 | Брутто-формула | Молекулярный ион, m/z | Число изомеров | Относительное содержание, % |
|---|---|---|---|---|
| 1 | C12H8Cl2 | 222 | 2 | 0.05 |
| 1 | C12H7Cl3 | 256 | 2 | 0.10 |
| 1 | C12H6Cl4 | 290 | 1 | 0.14 |
| 2 | C12H7Cl2(OCH3) | 252 | 1 | 0.11 |
| 2 | C12H6Cl3(OCH3) | 286 | 2 | 1.34 |
| 2 | C12H5Cl3(OCH3)2 | 316 | 2 | 0.97 |
| 3 | C12H6Cl3(OH) | 272 | 4 | 1.43 |
| 3 | C12H5Cl4(OH) | 306 | 10 | 26.65 |
| 3 | C12H4Cl3(OH)2 | 322 | 2 | 1.31 |
| 4 | C12H5Cl3(OCH3)(OH) | 302 | 1 | 0.27 |
| 3 | C12H7Cl2(OC2H5) | 266 | 2 | 0.48 |
| 5 | C12H6Cl3(OC2H5) | 300 | 7 | 9.88 |
| 5 | C12H5Cl4(OC2H5) | 334 | 7 | 11.24 |
| 5 | C12H6Cl2(OC2H5)2 | 310 | 3 | 3.49 |
| 5 | C12H5Cl3(OC2H5)2 | 344 | 14 | 19.16 |
| 5 | C12H4Cl4(OC2H5)2 | 378 | 2 | 0.16 |
| 5 | C12H5Cl2(OC2H5)3 | 354 | 5 | 6.01 |
| 5 | C12H4Cl3(OC2H5)3 | 388 | 3 | 0.21 |
| 6 | C12H6Cl2(OC2H5)(OCH3) | 296 | 3 | 2.82 |
| 6 | C12H5Cl3(OC2H5)(OCH3) | 330 | 5 | 4.21 |
| 6 | C12H5Cl2(OC2H5)2(OCH3) | 340 | 2 | 1.30 |
| 6 | C12H4Cl3(OC2H5)(OCH3)2 | 360 | 2 | 2.13 |
| 7 | C12H4Cl4(OC2H5)(OH) | 350 | 7 | 6.55 |
| Итого: | 99.72 | |||
Полученные данные показали, что в ходе взаимодействия смеси ПХБ 1 с MeONa в смеси ДМСО/EtOH одновременно или последовательно может протекать образование производных ПХБ 2–7. Причем содержание в продуктах реакций производных 4, 6, 7 незначительно по сравнению с содержанием соответствующих исходных производных 2, 3, 5. Полученные результаты совпадают с данными ТДМ, согласно которым основными производными также являются продукты замещения 2, 3, 5, а “интермедиаты” 4, 6, 7 представляют собой термодинамически нестабильные соединения.
Конверсия исходных конгенеров смеси ПХБ “Совол” 1 в реакции с MeONa в присутствии ДМСО и ДМСО/EtOH составила 100 [8] и 99.7% (табл. 2) соответственно. При проведении реакции в присутствии этанола образование ПХДФ не зафиксировано, а количество необходимого MeONa ниже стехиометрического.
Согласно данным элементного анализа содержание хлора в полученных результирующих продуктах синтеза 2–7 в 1.6 раза ниже, чем в исходной смеси ПХБ “Совол” 1.
Таким образом, впервые по результатам теоретических расчетов подобраны условия проведения реакции нуклеофильного замещения конгенеров смеси “Совол” 1 при взаимодействии с MeONa в среде ДМСО/EtOH. Такой подход позволил экспериментально безопасно получить предпродукты 2–7, так как содержание хлора в них снижено в 1.6 раза. Полученные производные ПХБ 2–7 являются менее токсичными для дальнейших исследований в процессах их термической утилизации.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве исходных объектов в настоящей работе использована техническая смесь ПХБ “Совол” (ОСТ 6-01-24-75), металлический натрий, свежевысушенные и перегнанные МеОН ($d_{{20}}^{4}$ 0.7918), EtOH ($d_{{20}}^{4}$ 0.7917) и ДМСО ($d_{{20}}^{4}$ 1.1004).
Методика взаимодействия смеси “Совол” 1 с МеОNa в среде ДМСО и EtОН аналогична методике проведения реакции с МеОNa в среде ДМСО и MeОН, описанной в работе [14].
Для идентификации и количественной оценки продуктов реакций использовали газовый хроматограф-масс-спектрометр “Agilent GC 7890A MSD 5975C inert XL EI/CI” (США) с кварцевой капиллярной колонкой НР-5MS и квадрупольным масс-спектрометрическим детектором (ГХ-МС). Сканирование по полному ионному току осуществляли в диапазоне масс 20–1000 Да в режиме электронной ионизации с энергией излучения 70 эВ.
Список литературы
Porta M., Zumeta E. // Occup. Environ. Med. V. 59. P. 651–652. https://doi.org/10.1136/oem.59.10.651
Gomes H.I., Dias-Ferreira C., Ribeiro A.B. // Science Total Environ. 2013. V. 445–446. P. 237–260. https://doi.org/10.1016/j.scitotenv.2012.11.098
Kawamoto K., Mabuchi K. // J. Mater. Cycles Waste Manag. 2001. V. 3. P. 38–47. https://doi.org/10.1007/s10163-000-0039-2
Vermeulen I., Caneghem J.V., Vandecasteele C. // J. Mater. Cycles Waste Manag. 2014. V. 16. P. 167–171. https://doi.org/10.1007/s10163-013-0160-7
Kamarehie B., Jafari A.J., Mahabadi H.A. // J. Mater. Cycles Waste Manag. 2014. V. 16. P. 711–720. https://doi.org/10.1007/s10163-013-0185-y
Gorbunova T.I., Subbotina J.O., Saloutin V.I., Chupa-khin O.N. // J. Hazard. Mater. 2014. V. 278. P. 491–499. https://doi.org/10.1016/j.jhazmat.2014.06.035
Метод, универсальный алгоритм и программа термодинамического расчета многокомпонентных гетерогенных систем. Труды МВТУ/Под ред. Г.Б. Синярева. М.: МВТУ, 1978. 56 с.
Kulikova T.V., Maiorova A.V., Bykov V.A., Shunyaev K.Y., Gorbunova T.I., Pervova M.G., Plotnikova K.A. // Intern. J. Environ. Sci. Technol. 2019. V. 16. № 7. P. 3265–3274. https://doi.org/10.1007/s13762-018-2022-2
Плотникова К.А., Первова М.Г., Горбунова Т.И., Хайбулова Т.Ш., Боярский В.П., Салоутин В.И., Чупахин О.Н. // ДАН. 2017. Т. 476. № 1. С. 45–50. https://doi.org/10.1134/S0012500817090038
Майорова А.В., Куликова Т.В., Шуняев К.Ю., Горбунова Т.И., Первова М.Г. // ЖОХ. 2019. Т. 89. № 9. С. 1439–1447. https://doi.org/10.1134/S1070363219090184
Куликова Т.В., Майорова А.В., Сафронов А.П., Горбунова Т.И., Первова М.Г., Шуняев К.Ю., Леонтьев Л.И. // ДАН. 2019. Т. 487. № 6. С. 630–635. https://doi.org/10.1134/S0012500819080068
Куликова Т.В., Майорова А.В., Шуняев К.Ю., Горбунова Т.И., Салоутин В.И., Чупахин О.Н. // ЖОХ. 2013. Т. 83. № 5. С. 754–762. https://doi.org/10.1134/S1070363213050034
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах