Доклады Российской академии наук. Химия, науки о материалах , 2021, T. 497, № 1, стр. 3-8
Водорастворимые люминесцирующие комплексы лантаноидов на основе сополимеров 2-метакрилоилоксиэтилениминодиуксусной кислоты
Т. Н. Некрасова 1, М. В. Соловский 1, М. С. Борисенко 1, *, А. И. Фишер 1, 2, член-корреспондент РАН Е. Ф. Панарин 1
1 Институт высокомолекулярных соединений Российской академии наук
199004 Санкт-Петербург, Россия
2 Санкт-Петербургский государственный технологический институт (технический университет)
190013 Санкт-Петербург, Россия
* E-mail: aarghm@hq.macro.ru
Поступила в редакцию 27.10.2020
После доработки 29.12.2020
Принята к публикации 25.01.2021
Аннотация
Синтезирована 2-метакрилоилоксиэтилениминодиуксусная кислота и ее новые водорастворимые сополимеры с N-винилпирролидоном. Исследовано взаимодействие сополимеров в разбавленных водных растворах с ионами лантаноидов; установлено усиление люминесценции Eu3+ в 25 раз в полимерном комплексе по сравнению с низкомолекулярным аналогом при формировании гетеролигандных комплексов как с теноилтрифторацетоном, так и в гетерометаллических (биметаллических) комплексах Eu3+ и Gd3+.
В связи с широким применением люминесцентных методов исследования в различных областях биохимии, медицинской диагностики, большое внимание уделяется люминесцирующим координационным комплексам ионов лантаноидов (Ln3+). Лантаноиды оказались в центре внимания исследователей благодаря своим уникальным оптическим свойствам [1, 4]: квазимонохроматичность излучения (полуширина полос люминесценции 5–10 нм, в то время как для органических хромофоров более 100 нм), стабильность свечения во времени, независимость положения полос люминесценции от природы лиганда и растворителя, большой стоксовский сдвиг в спектрах, высокие значения времени жизни возбужденного состояния (≈1000 мкс). Кроме того, имеет место независимость формы спектра от природы лиганда, за исключением штарковского расщепления f-уровней, вызываемого изменением кристаллического поля лигандов [1–3].
В полимерных комплексах лантаноидов сохраняются уникальные оптические свойства ионов [5]. Использование полимерных комплексов Ln3+ в биомедицине позволяет пролонгировать действие зонда по сравнению с низкомолекулярными аналогами, что важно при проведении длительных исследований. Полимерные комплексы с короткоживущими радионуклидами Ln3+ могут быть использованы для получения механически прочных и стабильных материалов в виде пленок, гелей, покрытий при лечении онкологических заболеваний. Применение комплексов в биологии и биомедицинских исследованиях предъявляет к лиганду особые требования, такие как растворимость в воде, биосовместимость, отсутствие токсичности и т.д. Получение новых полимерных комплексонов, удовлетворяющих этим условиям, требует разработки методов синтеза мономеров, содержащих хелатные группы, способных вступать в реакции сополимеризации с гидрофильными виниловыми мономерами различной природы, и поэтому является актуальным.
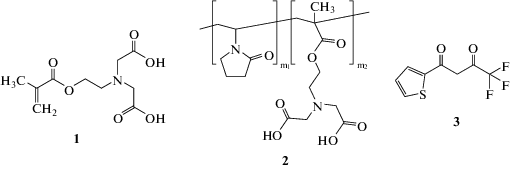
В данной работе синтезирован новый мономер – 2‑метакрилоилоксиэтилениминодиуксусная кислота (2-МОЭИДУК) 1. Методом радикальной сополимеризации получены его водорастворимые сополимеры 2 с N-винилпирролидоном (ВП). Люминесцентными методами исследовано их взаимодействие с ионами лантаноидов Eu3+ и Gd3+ в разбавленных водных растворах.
Мономер 1 был получен алкилированием гидрохлорида 2-аминоэтилметакрилата, синтезированного
по методу [6], монохлоруксусной кислотой. Вспектрах 1H ЯМР 2-МОЭИДУК в D2O присутствует характерный для протонов группы (СH2) остатков монохлоруксусной кислоты сигнал 3.55 м. д., сигналы протонов карбоксильных
групп: 7.85 м. д. 13С ЯМР, D2O, δ, м. д.: 17.64 (CH3), 41.58 (CH2–N), 59.32 (N–CH2), 69.44 (CH2–O), 121.09 (СН2), 138.97 (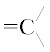 ); 171.95 (C=O); 176.26 (COOH).
); 171.95 (C=O); 176.26 (COOH).
Сополимеризацию 2-МОЭИДУК с N-винилпирролидоном (при молярном соотношении 20 : 80) проводили в этаноле с инициатором – динитрилом азоизомасляной кислоты (4.5 мас. %) в запаянных ампулах в атмосфере аргона при 60°С в течение 48 ч. Содержание 2‑иминодиуксусной кислоты (ИДУК) в полученном сополимере с ВП (ВП–ИДУК), определенное потенциометрическим титрованием, составило 20.2 мол. %, выход 50.0%. Сополимер хорошо растворим в воде. Молекулярная масса полученного сополимера, определенная методами седиментации и диффузии, составила 58 кДа.
Для приготовления комплексов 2 с ионами лантаноидов использовали водные растворы солей EuCl3 · 6H2O, GdCl3 · 6H2O (“Aldrich”), с = 1 × × 10–4 моль л–1. Навеску сополимера растворяли в дистиллированной воде и 0.1 н раствором NaOH доводили рН раствора сополимера до 7.5–8.0. Затем растворы разбавляли до спол = 0.02 мг мл–1 (что соответствует концентрации 5.75 × 10–5 моль л–1 групп СОО–) и добавляли рассчитанное количество раствора соли лантаноида, задаваемое соотношением [Ln3+] : [СОО–]. Гетеролигандные и гетерометаллические комплексы получали добавлением варьируемого количества теноилтрифторацетона (ТТА) 3 (раствор в этаноле, с0 = 5.3 × 10–3 моль л–1) или GdCl3 соответственно.
Спектры поглощения регистрировали на спектрофотометре СФ-256 УВИ (ЛОМО ФОТОНИКА, Россия). Спектры возбуждения и фотолюминесценции записывали на спектрофлуориметре LS-100 (PTI, Канада), измерения проводились с использованием кварцевой кюветы с длиной оптического пути 1 см в термостатируемой ячейке при 25°С. Сополимеры, содержащие фрагменты иминодиуксусной кислоты, полученные реакцией модификации цепей [7], образуют стабильные комплексы с ионами поливалентных металлов, логарифм константы образования которых находится в интервале 7–8.
Карбоксильные группы алифатических кислот только координируют Ln3+, но не обеспечивают эффективный перенос энергии из-за очень слабого поглощения в ультрафиолетовой области, поэтому для усиления люминесценции комплексов использовали соединение 3, образующее комплексы с ионами лантаноидов и обеспечивающее перенос энергии электронного возбуждения с триплетного уровня соединения 3 на резонансный уровень иона Eu3+ [4].
УФ-спектры поглощения растворов приведены на рис. 1.
Рис. 1.
УФ-спектры поглощения водно-этанольных растворов ВП–ИДУК (кривая 1), ТТА (кривая 2), смеси ВП–ИДУК с ТТА (кривая 3), смеси ВП–ИДУК, ТТА и Eu(NO3)3 (кривая 4), смеси Eu(NO3)3 с ТТА (кривая 5). Концентрации [ВП–ИДУК] = 0.95 г л–1, [ТТА] = 1.13 × 10–4 моль л–1, [Eu3+] = 4.5 × 10–5 моль л–1; [Eu3+] : [ТТА] = 0.40; во всех растворах содержание этанола 5.0 об. %.
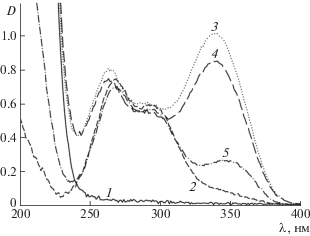
Наличие в спектрах поглощения полосы с λмакс 340 нм, отсутствующей у исходных компонентов, указывает на образование комплекса [Eu3+] : : [ВП–ИДУК : ТТА].
Спектры возбуждения и фотолюминесценции растворов [ВП–ИДУК + Eu3+ + ТТА] при изменении концентрации ТТА приведены на рис. 2. Спектры возбуждения регистрировали при наблюдении в полосе люминесценции европия λнабл = = 614 нм.
Рис. 2.
Спектры возбуждения (λнабл = 614 нм) (а) и фотолюминесценции (λвозб = 375 нм) (б) растворов [ВП–ИДУК + + Eu3+ + ТТА] при изменении концентрации ТТА. [ТТА] : [Eu3+] = 3.2 (кривая 1), 6.4 (кривая 2), 9.6 (кривая 3) при постоянном соотношении [Eu3+] : [СОО–] = 0.3. На врезке (а) кривые 1 и 2 даны при увеличении.
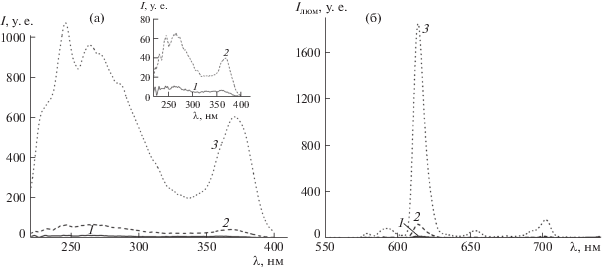
Появление в спектрах возбуждения растворов [ВП–ИДУК + Eu3+ + ТТА] новой полосы, по сравнению со спектрами свободного Eu3+, указывает на то, что происходит процесс передачи энергии, поглощенной ТТА, с его триплетного уровня (Е = 20 500 см–1)на резонансный уровень иона Eu3+ (E(5D0) = 17 200 см–1). Величина энергетического зазора между триплетным уровнем лиганда и резонансным уровнем Eu3+ составляет 3200 cм–1, и лежит в области значений 2500–3500 cм–1, необходимых для эффективной передачи энергии [8]. В спектрах люминесценции присутствуют полосы в области 580, 595, 614, 655 и 702 нм, характерные для иона Eu3+ и относимые к переходам из состояния 5D0 на уровни 7Fi(0–5). Изменение формы спектров возбуждения в растворе является признаком изменения состава координационной сферы комплекса по мере включения в нее ТТА с ростом его концентрации [9].
Зависимость интенсивности полосы люминесценции λ = 614 нм (I614) растворов EuCl3 и [EuCl3 + ВП–ИДУК] при добавлении ТТА от соотношения [ТТА] : [Eu3+] приведена на рис. 3.
Рис. 3.
Зависимость I614 растворов EuCl3 (кривая 1) и [EuCl3 + ВП–ИДУК] (кривая 2); [Eu3+] : [СОО–] = 0.3; спол = = 0.02 мг мл–1 от концентрации ТТА. Для сравнения значений I614 на кривых 1 и 2 при одном и том же усилении ФЭУ значения I614 для кривой 2 нужно разделить на 6.5.
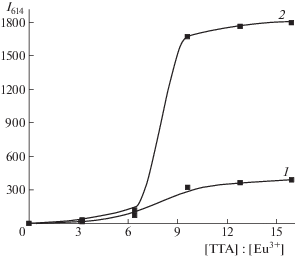
Из рисунка видно, что интенсивность люминесценции растворов комплекса [ВП–ИДУК : : Eu3+ : ТТА], по сравнению с таковой растворов [2-МОЭИДУК + Eu3+ + ТТА] при одинаковых соотношениях компонентов, в 25 раз выше. Наблюдаемый рост интенсивности люминесценции вызван “полимерным эффектом”, который возникает в результате гидрофобизации макромолекулярного клубкапри замене молекул воды в сольватной оболочке СОО– групп на ионы Eu3+. Известно, что молекулы воды являются эффективными тушителями люминесценции Ln3+ [1] за счет безызлучательной потери энергии на колебаниях связи О–Н.
Из рис. 3 видно, что изменение I614 с ростом соотношения [ТТА] : [Eu3+] происходит немонотонно. По-видимому, сначала при соотношении [ТТА] : [Eu3+ ] < 3 молекула ТТА взаимодействует с атомом третичного азота ИДУК, а затем с Eu3+, включенным в комплекс [–RСОО– : Eu3+]. То есть формирование комплекса [ВП–ИДУК : Eu3+ : ТТА] происходит в условиях конкурентного взаимодействия молекул ТТА с атомом третичного азота в боковом радикале ИДУК и ионами Eu3+, так как константа образования комплекса [Eu3+ : TTA] в воде невелика (lg Kуст = –3.4) [10]. При взаимодействии с полимерными лигандами образование связи комплексон–металл происходит как между близко расположенными, так и удаленными вдоль цепи карбоксилатными группами. Этовызывает усиление стерических препятствий в макромолекулярном клубке и приводит к формированию “координационно ненасыщенных” комплексов типа (–RСОО–)(3 – n)Eu3+, где n = 1 или 2 [5]. Возможные варианты строения гетеролигандных комплексов Eu3+ с полимерным лигандом ВП–ИДУК и ТТА представлены на рис. 4.
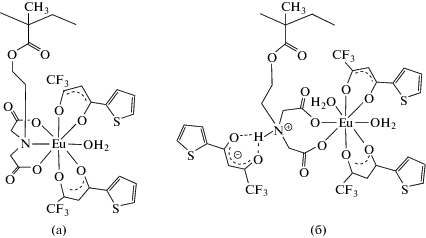
Рис. 4.
Предполагаемое строение гетеролигандных комплексов Eu3+ с полимерным лигандом ВП–ИДУК и ТТА: звено полимерного лиганда ВП–ИДУК занимает три координационных места во внутренней сфере Eu3+ (а); третичный атом азота протонирован и взаимодействует с енолятным анионом ТТА, звено лиганда ВП–ИДУК занимает два координационных места во внутренней сфере металла (б).
Еще одним возможным способом усиления люминесценции ионов лантаноидов является формирование биметаллических комплексов с ионами других f-элементов (колюминесценция), так как появляется дополнительная ступень для передачи энергии [4, 11]. Нами исследовано влияние ионов Gd3+ на интенсивность люминесценции Eu3+ в комплексе [ВП–ИДУК : Eu3+ : ТТА] при различном соотношении [TTA] : [Eu3+]. При добавлении GdCl3 (табл. 1) наблюдается усиление люминесценции в 1.5–2 раза, которое зависит как от соотношения [TTA] : [Eu3+], так и от соотношения [Gd3+] : [Eu3+].
Таблица 1.
Изменение относительной интенсивности люминесценции (I/I0) ионов Eu3+ при добавлении GdCl3 к раствору [ВП–ИДУК : Eu3+ : ТТА] при различных значениях [TTA] : [Eu3+], [Eu3+] : [COO–] = const = 0.3
| [Gd3+] : [Eu3+] | I/I0 | ||||
|---|---|---|---|---|---|
| [TTA] : [Eu3+] | |||||
| 4.7 | 7.6 | 9.5 | 18.9 | 28 | |
| 0 | 1 | 1 | 1 | 1 | 1 |
| 0.96 | 1.2 | 1.57 | 1.55 | 1.47 | 1.43 |
| 1.9 | 1 | 1.57 | 1.55 | 1.49 | 1.42 |
| 3.8 | 1 | 1.64 | 1.62 | 1.74 | 1.99 |
| 5.7 | не иссл. | 1.54 | 1.69 | 1.96 | 1.83 |
| 7.6 | не иссл. | не иссл. | 1.49 | 2.02 | 1.8 |
Наблюдаемое изменение люминесценции указывает на эффективность внутрисистемного переноса энергии Gd3+ → Eu3+, способствующего росту интенсивности люминесценции Eu3+.
Таким образом, впервые синтезированные водорастворимые сополимеры 2-метакрилоилоксиэтилениминодиуксусной кислоты с N‑винилпирролидоном образуют в воде комплексы с ионами лантаноидов. Формирование на основе синтезированных сополимеров гетеролигандных комплексов с ТТА позволило повысить интенсивность люминесценции Eu3+ в 25 раз по сравнению с интенсивностью Eu3+ в присутствии ТТА при тех же соотношениях. Добавление ионов Gd3+ привело дополнительно к двукратному росту интенсивности люминесценции. Формирование комплексов Eu3+ и Gd3+ на основе синтезированных сополимеров позволило управлять интенсивностью люминесценции путем варьирования соотношения взаимодействующих компонентов. Полученные результаты могут быть основой для создания водорастворимых бифункциональных люминесцирующих полимерных комплексов, сочетающих одновременно оптические и магнитные свойства ионов лантаноидов.
Список литературы
Bünzli J.-C.G. Lanthanide light for biology and medical diagnosis // J. Lumin. 2016. V. 170. № 3. P. 866–878. https://doi.org/10.1016/j.jlumin.2015.07.033
Bünzli J.-C.G., Review: Lanthanide coordination chemistry: from old concepts to coordination polymers // J. Coord. Chem. 2014. V. 67. № 23–24. P. 3706–3733. https://doi.org/10.1080/00958972.2014.957201
Bochkarev M.N., Pushkarev A.P. Synthesis and luminescence of some rare earth metal complexes // Org. Photonics Photovolt. 2016. V. 4. P. 60–67. https://doi.org/10.1515/oph-2016-0007
Уточникова В.В., Кузьмина Н.П. Фотолюминесценция ароматических карбоксилатов лантаноидов // Коорд. химия. 2016. Т. 42. № 10. С. 640–656. https://doi.org/10.7868/S0132344X16090073
Карасев В.Е., Петроченкова Н.В. Лантанидсодержащие полимеры / Владивосток: Дальнаука. 2005. 194 с.
Коршунов М.А., Михлин В.С. Синтез гидрохлорида 2-аминоэтилметакрилата // ЖОрХ. 1969. Т. 5. № 2. С. 254–256.
Тихонова Л.И. Комплексообразование Ca2+, Sr2+, Y3+, и Ce3+ с поливинилпирролидонполивинилиминодиуксусными кислотами // Журн. физ. химии. 1974. Т. 48. № 4. С. 823–827.
Latva M., Takalo H., Mukkala V.-M., Matachescuc C., Rodriguez-Ubisd J.C., Kankarea J. Correlation between the lowest triplet state energy level of the ligand and lanthanide(III) luminescence quantum yield // J. Lumin. 1997. V. 75. № 2. P. 149. https://doi.org/10.1016/S0022-2313(97)00113-0
Utochnikova V.V. The use of luminescent spectroscopy to obtain information about the composition and the structure of lanthanide coordination compounds // Coord. Chem Rev. 2019. V. 398. 113006. https://doi.org/10.1016/j.ccr.2019.07.003
Arnaud N., Georges J. Comprehensive study of the luminescent properties and lifetimes of Eu3+ and Tb3+ chelated with various ligands in aqueous solutions: influence of the synergic agent, the surfactant and the energy level of the ligand triplet // Spectrochim. Acta, Part A. 2003. V. 59. № 8. P. 1829–1840. https://doi.org/10.1016/S1386-1425(02)00414-6
Ермолаев В.Л., Свешникова Е.Б. Колюминесценция ионов и молекул в наночастицах комплексов металлов // Усп. химии. 2012. Т. 81. № 9. С. 769–789.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах