Доклады Российской академии наук. Науки о Земле, 2022, T. 503, № 2, стр. 126-130
Оценка механизмов вхождения примеси титана в состав MgSiO3 бриджманита
Член-корреспондент РАН Н. Н. Еремин 1, *, А. В. Бобров 1, 2, 3, **
1 Московский государственный университет
имени М.В. Ломоносова
Москва, Россия
2 Институт геохимии и аналитической химии
имени В.И. Вернадского Российской академии наук
Москва, Россия
3 Институт экспериментальной минералогии
имени Д.С. Коржинского Российской академии наук
Черноголовка, Московская область, Россия
* E-mail: neremin@mail.ru
** E-mail: archi@geol.msu.ru
Поступила в редакцию 08.12.2021
После доработки 20.12.2021
Принята к публикации 21.12.2021
- EDN: AMLBMP
- DOI: 10.31857/S2686739722040053
Аннотация
Методом атомистического моделирования проведено тестирование механизмов образования твердых растворов титанистого бриджманита в системе MgSiO3–MgTiO3. Полученные данные сопоставлены с результатами экспериментов. Показано, что изоморфная емкость бриджманита по титану при PT-параметрах холодной зоны субдукции систематически выше, чем для условий мантийной геотермы, и заметно повышается с глубиной.
Бриджманит (Al-(Mg,Fe)SiO3 со структурой перовскита) является главной фазой нижней мантии Земли, его содержание составляет примерно 70% от ее общего объема [1]. С учетом огромной протяженности нижней мантии, бриджманит можно рассматривать как самый распространенный минерал Земли в целом. Характерно, что бриджманит количественно преобладает и в ассоциации фаз, образующихся при погружении базальтов на глубины нижней мантии, где его доля может достигать 50 объемных % [2]. Свое название и, соответственно, статус минерала бриджманит получил только в 2014 г., когда в составе прожилков из метеорита, упавшего в Австралии в 1879 г., было впервые структурно подтверждено присутствие (Mg,Fe)SiO3-перовскита [3].
К числу природных находок бриджманита можно отнести включения в так называемых сверхглубинных природных алмазах. В этих алмазах бриджманит ассоциирует с дейвмаоитом (CaSiO3 со структурой перовскита, недавно получившим статус минерала [4]), ферропериклазом и стишовитом, а также в редких случаях с джеффбенитом (ТАРР), эллинаитом (Ca–Cr оксидом с перовскитовой структурой), Mg–Cr–Fe и другими оксидами с ромбической структурой, титанитом, мервинитом и некоторыми другими минералами [5]. Несмотря на то что (Mg,Fe)SiO3 c перовскитовой структурой не был подтвержден ни в одном включении в алмазе, допущение о возможном присутствии бриджманита определяется ассоциацией с ферропериклазом, так как этот парагенезис однозначно характеризует термодинамические условия нижней мантии. В условиях переходной зоны и верхней мантии парагенезис фаз аналогичного состава (Mg,Fe)SiO3 + (Mg,Fe)O считается “запрещенным” и уступает место (Mg,Fe)2SiO4 (оливину/вадслеиту/рингвудиту).
В большинстве случаев примесь TiO2 в бриджманите не превышает 0.2 мас %, что соответствует средним концентрациям титана в мантии Земли. Тем не менее некоторые богатые титаном комбинированные включения в алмазах были интерпретированы как продукты декомпрессионного разложения бриджманита. Рассчитанный состав первичного бриджманита характеризуется более высокими содержаниями титана, которые изменяются в диапазоне от 4 до 7 мас % TiO2 [6]. Считается, что такие разности этого минерала образуются в условиях погружающихся литосферных плит.
В экспериментах, проведенных в модельной системе MgSiO3–MgTiO3 при 21–24 ГПа и 1600°С, был установлен широкий диапазон вхождения титана в состав бриджманита (5–13 мас % TiO2), причем более высокая концентрация TiO2 отмечается в отсутствии других фаз [6]. Одновременно наблюдается довольно четкая отрицательная корреляция между содержаниями титана и кремния, свидетельствующая о преобладании механизма вхождения титана в бриджманит VITi4+ = VISi4+, при реализации которого содержание магния в минерале практически не изменяется.
Целью настоящего исследования явились получение количественной оценки изоморфной емкости бриджманита по примесному титану при различных мантийных давлениях и температурах с помощью методов атомистического моделирования и сопоставление полученных результатов с экспериментальными данными, представленными в вышеуказанных публикациях.
Для расчетов свойств смешения в системе MgSiO3–MgTiO3 использовалась оптимизированная частично ионная модель межатомных парных потенциалов [8], хорошо зарекомендовавшая себя при моделировании кристаллических структур, упругих и термодинамических свойств разнообразных силикатов. Ранее эта модель использовалась нами для оценки вхождения примесных ионов в состав некоторых мантийных фаз – Cr3+ в бриджманит и CaSiO3 со структурой перовскита [9] и Ti4+ в гранат [10].
Расчеты изоморфного вхождения ионов Ti4+ осуществлялись методом межатомных потенциалов с использованием программы GULP [11] в сверхструктурных ячейках бриджманита размером 3 × 3 × 3 со снятой нетрансляционной симметрией, содержащих 540 атомов (рис. 1). Расчеты осуществлялись в диапазоне давлений и температур 6.5–30 ГПа и 850–2200 К.
Рис. 1.
Суперъячейка 3 × 3 × 3 структурного типа бриджманита, использованная для расчетов свойств смешения в системе MgSiO3–MgTiO3.
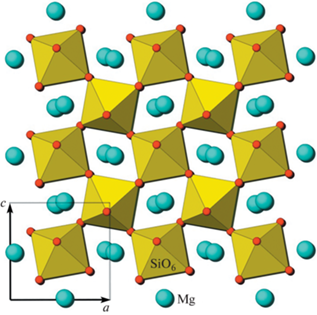
Для оценок изоморфной емкости был сконструирован гипотетический минал состава MgTiO3, изоструктурный бриджманиту. Некоторые структурные, физические и термодинамические характеристики этой виртуальной фазы при различных PT-параметрах, отвечающих мантийной геотерме [12], приведены в табл. 1.
Таблица 1.
Характеристики виртуальной фазы MgTiO3, изоструктурной бриджманиту при различных температурах и давлениях
| MgTiO3 (6.5 ГПа) | MgTiO3 (15 ГПа) | MgTiO3 (25 ГПа) | MgTiO3 (30 ГПа) | |
|---|---|---|---|---|
| a, Å | 5.24 | 5.19 | 5.13 | 5.11 |
| b, Å | 7.40 | 7.31 | 7.21 | 7.18 |
| c, Å | 5.03 | 4.96 | 4.90 | 4.87 |
| V, Å3 | 195.10 | 188.21 | 181.49 | 178.57 |
| d (VITi–O), Å | 2 × 1.915 | 2 × 1.897 | 2 × 1.879 | 2 × 1.871 |
| 2 × 1.917 | 2 × 1.899 | 2 × 1.881 | 2 × 1.873 | |
| 2 × 1.959 | 2 × 1.939 | 2 × 1.918 | 2 × 1.909 | |
| K, ГПа | 214.9 | 250.6 | 290.3 | 309.6 |
| СV, Дж/моль К | 123.2 | 123.2 | 123.4 | 123.4 |
| (1800 K) | (1900 K) | (2150 K) | (2200 K) | |
| S, Дж/моль К | 272.8 | 272.7 | 281.4 | 281.3 |
| (1800 K) | (1900 K) | (2150 K) | (2200 K) |
Для оценки энергии дефектов и изоморфной емкости титана в исследуемых структурах использовались две теоретические модели: расчет в сверхструктурных ячейках и в пределе бесконечно разбавленной примеси. Использовались ячейки размером 3 × 3 × 3 по отношению к базовой перовскитовой для 16 различных соотношений катионов Ti и Si по октаэдрическим позициям. Для расчетов выбиралось несколько “оптимальных” атомных конфигураций, наилучшим образом имитирующих статистическое распределение атомов в разупорядоченном твердом растворе по методике, изложенной в [13].
Результаты расчетов параметров взаимодействия (энергии смешения) и энтальпии смешения приведены в табл. 2 и на рис. 2. Как видно из таблицы, полученные значения параметра взаимодействия для состава MgSiO3 (Q1) оказались большими, чем для состава MgTiO3 (Q2) в полном соответствии с правилом полярности изоморфизма. Также обратим внимание, что расчеты в пределе бесконечного разбавления и суперъячейках дают в рамках одной модели межатомных потенциалов хорошо согласующиеся между собой значения, что фиксировалось нами ранее и в других системах [14].
Таблица 2.
Расчет параметров взаимодействия и энтальпии смешения (КДж) в системе MgSiO3–MgTiO3 при различных температурах и давлениях, отвечающих геотерме мантии Земли [12] и холодной зоне субдукции [15]
| Р, ГПа | Т, K | Q1 | Q2 | ΔH (0.1 MgTiO3) | ΔH (0.2 MgTiO3) | VTi4+, % |
|---|---|---|---|---|---|---|
| Условия мантии Земли | ||||||
| 6.5 | 1800 | 42.62 | 11.95 | 3.56 | 6.82 | 3–5 |
| 15 | 1900 | 41.51 | 11.76 | 3.47 | 6.66 | 3–5 |
| 20 | 2000 | 42.08 | 10.55 | 3.50 | 6.58 | 4–6 |
| 25 | 2150 | 42.18 | 9.92 | 3.51 | 6.51 | 5–7 |
| 30 | 2200 | 41.77 | 9.85 | 3.47 | 6.45 | 5–7 |
| Условия холодной зоны субдукции | ||||||
| 6.5 | 850 | 30.96 | 23.62 | 2.72 | 4.72 | 3–5 |
| 15 | 1250 | 33.96 | 19.37 | 2.92 | 4.96 | 5–7 |
| 20 | 1420 | 34.07 | 17.76 | 2.92 | 4.93 | 7–9 |
| 25 | 1570 | 35.67 | 16.42 | 3.03 | 5.09 | 9–11 |
| 30 | 1670 | 35.93 | 15.70 | 3.05 | 5.10 | 10–12 |
Рис. 2.
Изменение энтальпии смешения в системе MgSiO3 (бриджманит) – MgTiO3 в условии температур и давлений, соответствующих геотерме мантии Земли. Сплошные линии – расчет в приближении бесконечно разбавленного дефекта при PT-условиях из табл. 1. Квадратами показаны усредненные расчетные значения энтальпии смешения для различных атомных конфигураций в 3 × 3 × 3 сверхъячейке для составов: 4, 7, 15 и 24% MgTiO3 для P = 30 ГПа и T = = 2200 К; кружками – для P = 30 ГПа и T = 1670 К соответственно.
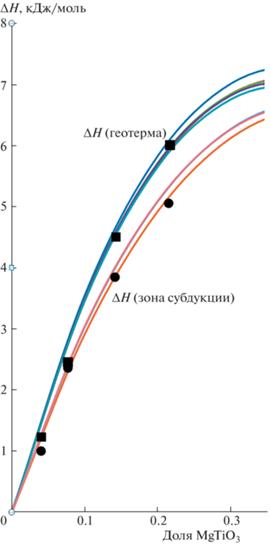
Отметим, что при изменении термодинамических условий по геотерме мантии Земли или в условиях холодной зоны субдукции [15] значение энтальпии смешения меняется незначительно, особенно в областях малых концентраций титана в бриджманите. Это связано с конкурирующим действием двух факторов – температуры (повышающей колебательный вклад энтропии смешения) и давления (подавляющего изоморфное замещение по правилу депрессии для извовалентного изоморфизма). Как следует из полученных результатов, значения энтальпии смешения в холодной зоне субдукции оказываются систематически ниже, чем при условиях мантийной геотермы.
Учитывая, что энтропийный фактор при повышении температуры способствует росту смесимости в этой системе, можно сделать вывод, что при повышении давления от 6.5 до 30 ГПа изоморфная емкость бриджманита по титану будет систематически и существенно возрастать.
Оценка изоморфной емкости проводилась путем построения концентрационных зависимостей энергии Гиббса. Равновесные составы фаз определялись согласно [16] как абсциссы точек касания общей касательной к кривой концентрационной зависимости $\Delta G(х)$. Расчеты осуществлялись в 3 × 3 × 3 суперъячейках для 16 различных составов твердого раствора с расчетом колебательного спектра кристалла и последующего определения колебательного вклада в энтропию смешения при заданных температурах и давлениях. Конфигурационная энтропия кристалла SКОНФ рассчитывалась с помощью статистико-термодинамических моделей для однопозиционной бинарной смеси по формуле (1):
(1)
${{S}_{{{\text{КОНФ}}}}} = - kN\left[ {x\ln x + \left( {1 - x} \right)\ln \left( {1 - x} \right)} \right].$Колебательный вклад SКОЛ в общую энтропию смешения Sсм рассчитывался по формуле (2):
где S(x) – энтропия твердого раствора заданного состава, а S1 и S2 – энтропии MgSiO3 и MgTiO3 соответственно. Расчеты показали, что основной вклад (от 75 до 85%) в общую энтропию смешения при изучаемых температурах для данных систем дает конфигурационная составляющая, а колебательная энтропия составляет не более 25% от общей энтропии.Расчеты, представленные в табл. 2, показали, что изоморфная емкость бриджманита по титану (VTi4+, %) в зоне субдукции систематически выше, чем для условий мантийной геотермы, и заметно повышается с глубиной. В связи с тем, что корово-мантийное взаимодействие при субдукции океанической коры на различные мантийные глубины является главным механизмом обеспечения высоких содержаний TiO2 в локальных участках мантии Земли, установленная в настоящей работе максимальная емкость бриджманита по примесному титану при параметрах холодной субдукции может служить объяснением высоких концентраций титана (до 7 мас % TiO2) в некоторых природных бриджманитах из включений в алмазе. Такие богатые титаном включения являются геохимическими индикаторами корового субстрата в веществе нижней мантии Земли.
В заключение следует отметить, что в экспериментальной работе [7] в ассоциации с титансодержащим бриджманитом при давлении более 20 ГПа была получена еще одна фаза с перовскитовой структурой, также относящаяся к ряду твердых растворов MgSiO3–MgTiO3, но имеющая гораздо более высокое содержание титана (до 51 мас % TiO2). При этом стабильность фазы простирается в область пониженного давления вплоть до 17 ГПа. Кроме того, при 20 ГПа и 1600°С c добавлением алюминия к данной системе была впервые получена фаза состава [Mg5/6Al1/6][Si1/2Ti1/3Al1/6]O3, представляющая собой троекратно увеличенную сверхструктуру идеального MgSiO3-бриджманита, появление которой связано с упорядочением Ti в одной из октаэдрических позиций в структуре минерала [17]. Оценка механизмов вхождения титана в такие фазы представляет собой отдельную задачу для будущих исследований.
Список литературы
Andrault D. Properties of Lower-mantle Al-(Mg,Fe)SiO3 Perovskite // Geological Society of America. Special Papers. 2007. V. 421. P. 15–36.
Irifune T., Ringwood A.E. Phase Transformations in Subducted Oceanic Crust and Buoyancy Relationships at Depths of 600–800 km in the Mantle // Earth and Planetary Science Letters. 1993. V. 117. № 1–2. P. 101–110.
Tschauner O., Ma C., Beckett J.R., Prescher C., Prakapenka V.B., Rossman G.R. Discovery of Bridgmanite, the Most Abundant Mineral in Earth, in a Shocked Meteorite // Science. 2013. V. 346. Iss. 6213. P. 1100–1102.
Tschauner O., Huang S., Yang S., Humayun M., Liu W., Gilbert Corder S.N., Bechtel H.A., Tischler J., Rossman G.R. Discovery of Davemaoite, CaSiO3-perovskite, as a Mineral from the Lower Mantle // Science. 2021. V. 374. № 6569. P. 891–894.
Kaminsky F.V. The Earth’s Lower Mantle: Composition and Structure. Springer, 2017. 331 p.
Walter M.J., Kohn S.C., Araujo D., Bulanova G.P., Smith C.B., Gaillou E., Wang J., Steele A., Shirey S.B. Deep Mantle Cycling of Oceanic Crust: Evidence from Diamonds and Their Mineral Inclusions // Science. 2011. V. 334. P. 54–57.
Matrosova E.A., Bobrov A.V., Bindi L., Pushcharovsky D.Yu., Irifune T. Titanium-rich Phases in the Earth’s Transition Zone and Lower Mantle: Evidence from Experiments in the System MgO–SiO2–TiO2(±Al2O3) at 10–24 GPa and 1600 °C // Lithos. 2020. V. 366–367. № 105539.
Pedone A., Malavasi G., Menziani M.C., Cormack A.N., Serge A. A New Self-Consistent Empirical Interatomic Potential Model for Oxides, Silicates, and Silica-Based Glasses // J. Phys. Chem. B. 2006. V. 110. P. 11780–11795.
Марченко Е.И., Бобров А.В., Еремин Н.Н. Оценка механизма вхождения примеси хрома в CaSiO3 и MgSiO3 фазы нижней мантии Земли при давлениях 18–25 ГПа // ДАН. 2019. Т. 488. № 5. С. 530–533.
Еремин Н.Н., Гостищева Н.Д., Бобров А.В., Бенделиани А.А., Бурова А.И. Оценка вхождения ионов Ti4+ в состав мантийных гранатов: результаты атомистического моделирования // Кристаллография. 2021. Т. 66. № 1. С. 48–51.
Gale J.D., Rohl A.L. // Mol. Simulation. 2003. V. 29. № 5. P. 291–341.
Brown J.M., Shankland T.J. Thermodynamic Parameters in the Earth as Determined from Seismic Profiles // Geophys. J. R. Astr. Soc. 1981. V. 66. P. 579–596.
Eremin N.N., Deyanov R.Z., Urusov V.S. Choice of the Supercell with the Optimum Atomic Configuration in Simulation of Disordered Solid Solutions // Glass Physics and Chemistry. 2008. V. 34. № 1. P. 9–18.
Eremin N.N., Marchenko E.I., Petrov V.G., Mitrofa- nov A.A., Ulanova A.S. Solid Solutions of Monazites and Xenotimes of Lanthanides and Plutonium: Atomistic Model of Crystal Structures, Point Defects and Mixing Properties // Computational Materials Science. 2019. V. 157. P. 43–50.
Komabayashi T., Omori S., Maruyama S. Petrogenetic Grid in the System MgO–SiO2–H2O up to 30 GPa, 1600°C: Applications to Hydrous Peridotite Subducting into the Earth’s Deep Interior // J. Geophys. Res. 2004. V. 109. B03206.
Хачатурян А.Г. Теория фазовых превращений и структура твердых растворов. М.: Наука, 1974. 384 с.
Bindi L., Sirotkina E.A., Bobrov A.V., Walter M.J., Pushcharovsky D.Yu., Irifune T. Bridgmanite-like Crystal Structure in the Novel Ti-rich Phase Synthesized at Transition Zone Condition // American Mineralogist. 2017. V. 102. No. 1. P. 227–230.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Науки о Земле


