Доклады Российской академии наук. Науки о Земле, 2022, T. 505, № 1, стр. 120-124
О коррозионной устойчивости Nd–Ti-матрицы актинидов
Член-корреспондент РАН С. В. Юдинцев 1, *, С. С. Данилов 2, А. А. Ширяев 3, И. М. Мельникова 4
1 Институт геологии рудных месторождений, петрографии, минералогии и геохимии Российской академии наук
Москва, Россия
2 Институт геохимии и аналитической химии
им. В.И. Вернадского Российской академии наук
Москва, Россия
3 Институт физической химии и электрохимии
им. А.Н. Фрумкина Российской академии наук
Москва, Россия
4 Ведущий научно-исследовательский институт химической технологии Государственной корпорации “Росатом”
Москва, Россия
* E-mail: yudintsevsv@gmail.com
Поступила в редакцию 22.03.2022
После доработки 06.04.2022
Принята к публикации 07.04.2022
- EDN: EIEGPG
- DOI: 10.31857/S2686739722070192
Аннотация
Исследовано выщелачивание Np и Pu водой из образцов, сложенных двумя титанатными фазами: Nd2Ti3O9 (75%) и Nd2Ti2O7 (25%). Скорости выщелачивания из них актинидов при Т = 90°С снижаются со временем взаимодействия и на 28-е сутки эксперимента равны 10–8 г/(см2 сутки) для Pu и 7 × 10–7 г/(см2 сутки) для Np. Более высокое значение у нептуния связано, вероятно, с тем, что он находится в образцах в валентных состояниях IV и V, а плутоний – в состояниях III и IV. Показано, что на скорость выщелачивания существенное влияние оказывает кислотность раствора. В близнейтральных условиях, характерных для глубоких хранилищ, матрицы для иммобилизации актинидов на основе титанатов РЗЭ можно считать коррозионно-стойкими. Рассмотрены причины образования перовскитоподобной фазы состава Nd2Ti3O9. Они могут быть связаны как с высокой температурой, так и восстановительными условиями процесса синтеза.
Обращение с высокорадиоактивными отходами (ВАО) – это важная проблема, от которой зависит устойчивое и безопасное функционирование ядерной энергетики. Один из путей ее решения связан с выделением из жидких ВАО групп элементов для размещения в глубоких хранилищах в форме устойчивых в водах матриц [1]. Главную радиэкологическую угрозу в долгосрочном плане представляют трансурановые актиниды (Np, Pu, Am, Cm). Известны [1–3] способы фракционирования отходов переработки облученного ядерного топлива (ОЯТ) с выделением редкоземельных элементов (РЗЭ) и малых актинидов, МА (Am, Cm). Часть этих приемов уже проверена на реальных отходах и имеет уровень готовности, необходимый для внедрения. В составе РЗЭ–МА-фракции преобладают стабильные легкие РЗЭ группы церия, доля малых актинидов (Am241,243 и Cm244,245) составляет от 5 до 10 мас %. Доли отдельных РЗЭ в их общем количестве для ОЯТ с выгоранием 45 ГВт в сутки/т после 5 лет хранения равны [3], отн. %: 41% Nd, 24% Ce, 12% La, 11% Pr, 8% Sm, еще 4% приходится на Y, Gd, Eu.
Для иммобилизации ВАО предложены кристаллические фазы с высокой емкостью и устойчивые в воде [1, 4–10]. При поиске оптимальных типов матриц используют стабильные имитаторы, выбор которых основан на близости кристаллохимических свойств (заряда и ионных радиусов) этих элементов и актинидов. Для РЗЭ–МА-фракции имитатором служит Nd [1, 6], поэтому титанаты неодима интересны как матрицы для РЗЭ-актинидной фракции. Исследования их свойств касаются, в основном, поведения при облучении [6, 7], немногие работы [8–11] посвящены устойчивости в растворе и только в одной статье [12] изучалось выщелачивание из Nd–Ti-керамики реальных актинидов (244Cm). Скорости выщелачивания Nd из Nd2Ti2O7 и Nd4Ti9O24 в воде при 90°С или рассоле (200°С) равны 10–7–10–9 г/(см2 в сутки), что близко к значениям для матриц на основе цирконолита, пирохлора, бритолита в сходных условиях [6]. В наиболее экстремальных условиях (200–240°С, вода, хлоридный рассол) скорости выщелачивания Nd из образца керамики, содержащей Nd4Ti9O24, в опытах длительностью от 28 до 42 сут меняются от 10–7 до 10–8 г / (см2 в сутки). В предположении равномерности процесса это соответствует скорости растворения в первые микроны за год. Полученные данные позволяют определить титанаты Nd как высокоустойчивые к коррозии.
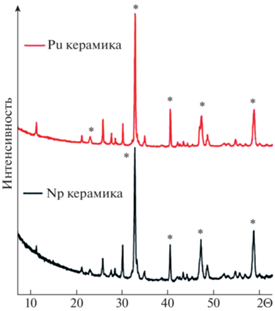
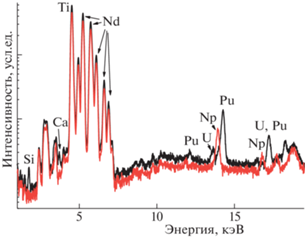
Наряду с РЗЭ и МА в составе фракции могут быть небольшие количества U, Np и Pu [2]. Кроме того, распад Am241,243 и Cm244,245 приведет со временем к накоплению изотопов Np237 и Pu239–241. Поэтому нами изучена гидролитическая устойчивость Nd–Ti-матриц с 0.06 мас. % 239Pu или 237Np. Их синтез проводили прессованием при 25°С оксидной шихты с мольным отношением TiO2 : Nd2O3, равным 3, последующей пропиткой таблеток раствором 239Pu или 237Np и спеканием 8 ч при 1350°С. Рентгено-флюоресцентный анализ (рис. 1) показал, что главные элементы в образцах – это Ti и Nd; обнаружены Pu или Np и U, Na, Al и Si (доли мас. %). В образце с Np примесей меньше, т.е. они в основном были в реактиве Pu. По данным рентгенофазового анализа (рис. 2) оба образца сложены фазами Nd2Ti3O9 (пр. гр. I4/mmm) и Nd2Ti2O7 (P21) в весовом отношении 75%: 25%, которые обладают структурой перовскитового типа. Имеется небольшое количество не идентифицированной фазы (или фаз), возможно оксидов неодима или титана.
Рис. 1.
Рентгено-флюоресцентные спектры керамик (черное – образец с Pu, красное – с Np). Ось интенсивностей приведена в логарифмическом масштабе. Имеется примесь Ca, Si и U.
Исследования по выщелачиванию Np и Pu из керамик проводили в соответствии с ГОСТ Р 52126-2003. Монолитные образцы и дистиллированную воду помещали в автоклав с тефлоновыми вставками и выдерживали в электропечи при 90°С с периодической заменой раствора. Площадь поверхности образцов рассчитывали из их геометрических размеров, соотношение поверхности и объема раствора составляло 10 м–1. Замену раствора проводили на 1, 7, 14, 21-е сутки, через 28 сут эксперимент завершали. Содержания Np и Pu в растворах после опыта определяли на α-спектрометре (“Analyst” Canberra). В диапазоне энергий 3.5–6.2 МэВ значение фона равно 5 × 10–5 имп/сек. Дифференциальную скорость выщелачивания i-ого элемента за n-й интервал времени $R_{n}^{i}$, г/(см2·сут), вычисляли по формуле (1):
где $m_{n}^{i}$ – масса элемента, выщелоченная за n-й интервал времени, г; $М_{{0,n}}^{i}$ – массовая концентрация элемента в образце в начале n-го периода г/г; S – площадь поверхности образца, см2; $\Delta {{t}_{n}}$ – длительность n-го периода выщелачивания между сменами раствора, сутки.Интегральную скорость выщелачивания i-го элемента за k-й интервал времени $V_{k}^{i}$, г/(см2 сут), вычисляли по формуле (2):
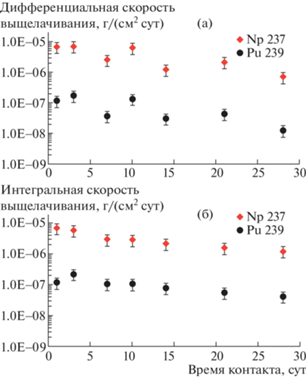
где $m_{k}^{i}$ – масса элемента, выщелоченная за k-й интервал времени, г; $M_{0}^{i}$ – массовая концентрация элемента в образце, г/г; S – площадь поверхности образца, контактирующая с водой, см2; ${{t}_{k}}$ – продолжительность k-го периода выщелачивания от начала опыта, сутки.Скорости выщелачивания Np и Pu из образцов, как и в большинстве других случаев, снижаются со временем (рис. 3). Причиной тому считается образование на поверхности образца при контакте с раствором тонкого защитного слоя, обогащенного титаном [4–6]. Дифференциальная скорость выщелачивания Pu при 90°С на 28-е сутки составила 10–8 г/(см2 сутки), а для Np она почти на 2 порядка выше и равна 7 × 10–7 г/(см2 сутки). Это, скорее всего, обусловлено различной степенью их окисления: IV и V у Np, III и IV у Pu [4], из-за чего нептуний хуже удерживается в структурах титанатов. Ранее установлено [12], что скорость выщелачивания Cm (вода, 90°С) из фазы состава (Nd,Cm)2Ti3O9 с 2 мас. % 244Cm составила 10–5 г/(см2 сутки). Это на один (Np) или три (Pu) порядка выше, чем из изученной керамики, состоящей из фаз Nd2Ti3O9 и Nd2Ti2O7. Возможное объяснение такого различия состоит в увеличении кислотности раствора в опытах с кюриевым образцом из-за радиолиза до рН 4.
Рис. 3.
Дифференциальная (а) и интегральная (б) скорости выщелачивания Pu и Np водой из керамик фазового состава Nd2Ti3O9 (75 мас. %) – Nd2Ti2O7 (25 мас. %) при 90°С. Точность определения значений скорости выщелачивания показана вертикальными отрезками.
Свойства титанатных керамик с искусственными актинидами, включая устойчивость в воде и водных растворах, анализировались в работах [5, 6, 12–17]. Основная часть этих исследований выполнена в связи с поиском матриц для избыточного оружейного плутония. Опыты проводили в статических и динамических условиях при 90°С и рН раствора от 2 до 12 с цирконолитом состава Ca(Zr,Pu)(Ti,Hf)2O7 и пирохлорами состава (Gd,Pu)2Ti2O7 или (Ca,Gd,Hf,U,Pu)2(Ti,Hf)2O7. Скорость выщелачивания Pu водой составила 10–8 г/(см2 сутки) в начале взаимодействия и снизилась до 10–9 г/(см2 сутки) через 300 сут, для цирконолита ее значение в 2–3 раза ниже, чем для пирохлора. Близкие значения получены в динамических условиях при низкой скорости обновления раствора, при быстром просачивании скорости выщелачивания Pu возрастают до 10–7 г/(см2 сутки). После аморфизации структуры фаз из-за распада актинидов скорость выщелачивания Pu растет в 10 раз для цирконолита и в 20–50 раз для пирохлора, но остается на 1–2 порядка ниже, чем у стеклообразных матриц ВАО [16].
Сильное влияние рН раствора на выщелачивание церия из фазы Ce2Ti2O7 (табл. 1) установлено в работе [8]. Скорость выщелачивания Nd из керамики состава Nd2Ti2O7 в опытах с заменяемым каждые сутки раствором HNO3 (рН = 1) составила около 10–4 г (см2 в сутки) при 90°С [11]. Это доказывает ускорение коррозии матрицы актинидов в случае повышения кислотности раствора. В реальном хранилище радиолитическое подкисление воды будет выражено в меньшей степени, если вообще проявлено. Это связано с тем, что содержание короткоживущего 244Cm (период полураспада равен 18 лет) в матрице с РЗЭ–МА-фракцией равно 0.2 мас. %, что на порядок меньше, чем в работе [12]. Кроме того, контейнер и упаковка ВАО должны обеспечить физическую изоляцию матрицы от подземных вод на срок порядка 500 лет, за который 244Cm полностью распадется до 240Pu (6537 лет). Периоды полураспада других актинидов РЗЭ–МА-фракции и их дочерних элементов варьируются от 433 лет (241Am) до 2.14 млн лет (237Np). Радиолитическое изменение рН подземных вод в хранилище ВАО будет подавляться их реакцией с металлическим контейнером и буфером на основе бентонита, что обеспечит их значения рН, близкие к нейтральным. Несомненно, что в таких условиях коррозионная устойчивость матрицы РЗЭ–МА окажется существенно выше.
Таблица 1.
Содержание элементов в растворе после контакта с Ce2Ti2O7 при 25 и 50°С [8]
| Состав раствора и температура в экспериментах | Ce (ppm) | Ti (ppm) | |
|---|---|---|---|
| рассол, г/л: 42 Na+, 30 K+, 35 Mg2+, 0.6 Ca2+, 190 Cl–, 3.5 SO$_{4}^{{2 - }}$, 1.3 BO$_{3}^{{3 - }}$ | 25°С | <10* | <0.1* |
| 50°С | <10* | <0.1* | |
| 0.1 M NaCl | 25°С | <2* | <3* |
| 50°С | <2* | <3* | |
| 0.1 M HCl | 25°С | 301 ± 32 (0.2*) | 1 (0.002*) |
| 50°С | 305 ± 133 (0.2*) | <0.002* | |
В работе [18] изучены керамики, содержащие до 50 мас. % Nd2O3 и состоящие из Zn2TiO4, NdPO4 (монацит) и двух перовскитоподобных фаз – Nd2Ti2O7 и (Ca0.4Nd0.6)1.54Ti2O6. Скорость выщелачивания Nd из них определена методом PCT-B (90°С, вода, смена раствора, 28 сут). Она максимальна в первые сутки, затем снижается и уже через 7 сут становится постоянной, примерно 10–10 г/(см2 сутки). Устойчивость перовскитоподобных фаз Nd2Ti2O7 и (Ca0.4Nd0.6)1.54Ti2O6 в растворе выше, чем у монацита, NdPO4. Эти испытания показали, что данные фазы способны надежно иммобилизовать Nd (имитатор РЗЭ-актинидной фракции).
Рассмотрим влияние состава шихты и условий синтеза на строение Nd–Ti-керамик. В системе Nd2O3–TiO2 образуются [19]: Nd2TiO5 (кратко NT), Nd2Ti2O7 (NT2), Nd2Ti4O11 (NT4), Nd4Ti9O24 (N2T9). При мольном отношении TiO2 : Nd2O3, равном 3, должна доминировать фаза N2T9, но изученные нами образцы состоят из фаз NT3 (главная) и NT2 (второстепенная). Та же ситуация наблюдалась при синтезе керамики с Cm [12]: вместо N2T9 образовалась фаза NT3 со структурой перовскитового типа. Причиной этого мы считали восстановительные условия с протеканием реакции (Nd,Cm)4Ti9O24 = 2(Nd,Cm)2Ti3O9 + Ti3O5 с появлением оксида титана, в котором часть Ti находится в виде Ti3+. Изучение системы Nd2O3 –TiO2 [20] показало, что фаза NT3 образуется выше 1200°С по реакции: 0.2N2T9 + 0.6NT2 = NT3. Таким образом, образование фазы NT3 вместо N2T9 могут вызывать высокая температура и восстановительные условия. По данным работы [20], фаза N2T9 стабилизируется при избытке TiO2 в шихте относительно ее формулы, что обеспечит формирование керамики, состоящей из Nd4Ti9O24 и рутила (TiO2), как это, например, показано в нашей предыдущей работе [9].
Таким образом, скорости выщелачивания Pu в воде из керамик на основе фаз Nd2Ti3O9 и Nd2Ti2O7 со структурой перовскитового типа составили около 10–8 г/(см2 сутки). Это близко к значениям у титанатных матриц на основе цирконолита Ca(Zr,Pu)(Ti,Hf)2O7 и пирохлоров (Gd,Pu)2Ti2O7, (Ca,Gd,Hf,U,Pu)2(Ti,Hf)2O7. Таких же или даже еще меньших величин можно ожидать для скорости выщелачивания Nd3+, аналога трехвалентных малых актинидов (Am и Cm). Значения для Np почти на 2 порядка выше, чем у Pu, что, вероятнее всего, вызвано его нахождением в пятивалентном состоянии с более высокой способностью к выщелачиванию.
Список литературы
Юдинцев С.В. Изоляция фракционированных отходов ядерной энергетики // Радиохимия. 2021. Т. 63. № 5. С. 403–430.
Копырин А.А., Карелин А.И., Карелин В.А. Технология производства и радиохимической переработки ядерного топлива. М.: Атомэнергоиздат, 2006. 576 с.
Spent Nuclear Fuel Reprocessing Flowsheet. Paris: OECD NEA, 2012. 120 p.
Ewing R.C. Actinides and Radiation Effects: Impact on the Back-end of the Nuclear Fuel Cycle // Mineralogical Magazine. 2011. V. 75 (4). P. 2359–2377.
Lumpkin G.R., Smith K.L., Giere R., Williams C.T. Geochemical Behaviour of Host Phases for Actinides and Fission Products in Crystalline Ceramic Nuclear Waste Forms / In: Energy, Waste, and the Environment: a Geochemical Perspective. R. Giere, P. Stille (Eds). London, UK: Geol. Soc., 2004. V. 236. P. 89–111.
Lumpkin G.R. Ceramic Host Phases for Nuclear Waste Remediation / In: Experimental and Theoretical Approaches to Actinide Chemistry. J.K. Gibson, W.A. de Jong (Eds.). John Wiley & Sons Ltd. 2018. Ch. 7. P. 333–377.
Whittle K.R., Lumpkin G.R., Blackford M.G., Aughterson R.D., Smith K.L., Zaluzec N.J. Ion-beam Irradiation of Lanthanum Compounds in the Systems La2O3–Al2O3 and La2O3–TiO2 // Journal of Solid-State Chemistry. 2010. V. 183. P. 2416–2420.
Shoup S.S. Synthesis and Characterization of Novel Lanthanide- and Actinide-containing Titanates and Zircono-titanates; Relevance to Nuclear Waste Disposal / PhD dissertation. Knoxville, USA: The Unniversity of Tennessee, 1995. 131 p.
Юдинцев С.В., Александрова Е.В., Лившиц Т.С., Мальковский В.И., Бычкова Я.В., Тагиров Б.Р. Коррозионная стойкость в воде кристаллических матриц для иммобилизации актинидов // ДАН. 2014. Т. 458. № 5. С. 598–601.
Юдинцев С.В., Мальковский В.И., Никольский М.С., Никонов Б.С. Взаимодействие матриц актинидов с рассолом // ДАН. 2019. Т. 485. № 2. С. 87–91.
Yang K., Lei P., Yao T., Gong B., Wang Y., Li M., Wang J., Lian J. A Systematic Study of Lanthanide Titanates (A2Ti2O7) Chemical Durability: Corrosion Mechanisms and Control Parameters // Corrosion Science. 2021. V. 185. Paper ID 109394.
Юдинцев С.В., Лизин А.А., Томилин С.В. Синтез и изучение неодим-титанатной керамики с кюрием // Доклады Российской академии наук. Науки о Земле. 2022. Т. 503. № 1. С. 71–76.
Weber W.J., Ewing R.C., Catlow C.R.A., Diaz de la Rubia T., Hobbs L.W., Kinoshita C., Matzke Hj., Motta A.T., Nastasi M., Salje E.K.H., Vance E.R., Zinkle S.J. Radiation Effects in Crystalline Ceramics for the Immobilization of High-level Nuclear Waste and Plutonium // J. Mater. Res. 1998. V. 13 (6). P. 1434–1484.
Strachan D.M., Scheele R.D., Buck E.C., Icenhower J.P., Kozelisky A.E., Sell R.L., Elovich R.J., Buchmiller W.C. Radiation Damage Effects in Candidate Titanates for Pu Disposition: Pyrochlore // J. Nucl. Mater. 2005. V. 345. P. 109–135.
Strachan D.M., Scheele R.D., Buck E.C., Kozelisky A.E., Sell R.L., Elovich R.J., Buchmiller W.C. Radiation Damage Effects in Candidate Titanates for Pu Disposition: Zirconolite // J. Nucl. Mater. 2008. V. 372. P. 16–31.
Ewing R.C., Weber W.J. Actinide Waste Forms and Radiation Effects / In: The Chemistry of the Actinide and Transactinide Elements. Morss L.R., Edelstein N.M., Fuger J. (eds). Dordrecht: Springer. 2010. V. 6. Ch. 35. P. 3813–3887.
Burakov B.E., Ojovan M.I., Lee W.E. Crystalline Materials for Actinide Immobilization. London: Imperial College Press, 2011. 197 p.
Ren F., An C., Yan Y., Smolenski V., Novoselova A., Xue Y., Ma F., Zhang M. Synthesis of ZIT Composite Material and Immobilization of Nd2O3 // Ceramics Intern. 2022 (in press). https://doi.org/10.1016/j.ceramint.2022.02.088
Shoup S.S., Bamberger C.E., Tyree J.L., Anovitz L. Lanthanide-containing Zircon-titanate Solid Solutions // Journal of Solid-State Chemistry. 1996. V. 127. P. 231–239.
Gong W., Zhang R. Phase Relationship in the TiO2– Nd2O3 Pseudo-binary System // J. Alloys and Compd. 2013. V. 548. P. 216–221.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Науки о Земле