Экология, 2019, № 6, стр. 456-462
Потоки энергии и круговорот фосфора в экосистеме мелководного водохранилища в условиях антропогенного стресса
С. М. Голубков a, *, В. П. Беляков b, М. С. Голубков a, Л. Ф. Литвинчук a, В. А. Петухов a, Ю. И. Губелит a
a Зоологический институт РАН
199034 Санкт-Петербург, Университетская наб., 1, Россия
b Институт озероведения РАН
196105 Санкт-Петербург, ул. Севастьянова, 9, Россия
* E-mail: golubkov@zin.ru
Поступила в редакцию 12.01.2019
После доработки 06.05.2019
Принята к публикации 23.05.2019
Аннотация
Исследовали величины потоков энергии и интенсивности круговорота фосфора в сообществах планктона и зообентоса в мелководном сильно эвтрофированном водохранилище. Показано, что из-за высокой степени эвтрофирования водоема поток энергии через зоопланктон значительно превышал поток энергии через зообентос. Роль биоты в круговороте фосфора оказалась очень высока. За вегетационный сезон организмами планктона регенерировалось в 1.5 раза больше фосфора, чем внешняя нагрузка за год, и в 5 раз больше, чем внутренняя нагрузка этим элементом. В год с наибольшей скоростью оборота фосфора наблюдалась максимальная величина первичной продукции планктона.
Согласно современным представлениям [1], в основе функционирования экологических систем водоемов лежит динамическое взаимодействие потоков энергии, вещества и информации, обеспечивающее стабильность экосистемы в конкретных условиях среды. Выяснение величин этих потоков относится к приоритетным задачам современной экологии.
Важным инструментом исследований потоков энергии, позволяющим выяснить закономерности их динамики и устойчивость к факторам среды, является составление биотического баланса водной экосистемы [1], к основным характеристикам которого относится соотношение потока энергии через планктонные и донные сообщества организмов. Это соотношение в значительной степени определяет качество воды в водоеме, его способность к самоочищению и биоресурсный потенциал экосистемы, т.е. способность к созданию полезной для человека продукции, например рыбопродуктивность [1, 2]. К факторам среды, влияющим на баланс энергии в водоеме и соотношение величин потоков энергии через сообщества планктонных и донных организмов, относятся средняя глубина водоема, прозрачность, соленость воды, содержание в воде биогенных элементов и многие другие характеристики [1–4]. Например, показано [1], что в глубоководных водоемах основной поток энергии часто проходит через планктонные сообщества, а в мелководных – через донные.
Потоки вещества, и в первую очередь потоки биогенных веществ в водных экосистемах, исследованы в меньшей степени, чем потоки энергии. В частности, это относится к оценкам скорости оборота фосфора – основного биогенного элемента в большинстве континентальных водоемов, определяющего их первичную продуктивность. Большинство исследователей ограничивается определением внешней и внутренней нагрузки фосфором на водную экосистему водоема. При этом под внутренней нагрузкой понимается выделение фосфора из донных отложений, происходящего в основном за счет геохимических процессов на границе “донные отложения–вода”. Между тем немногочисленные данные указывают на то, что потоки фосфора внутри экосистемы могут составлять весьма значительную величину [2].
Цель настоящей работы состояла в оценке величин потоков энергии и круговорота фосфора в экосистеме мелководного водохранилища Сестрорецкий Разлив, расположенного в пределах г. Санкт-Петербурга и подвергающегося интенсивному антропогенному воздействию. Мы проверяли следующие гипотезы: 1) что эвтрофирование водоема влияет на соотношение потоков энергии через зоопланктон и зообентос и 2) величины регенерации фосфора внутри экосистемы за счет жизнедеятельности организмов могут превышать его внутреннюю и внешнюю нагрузку на экосистему водоема.
МАТЕРИАЛ И МЕТОДЫ
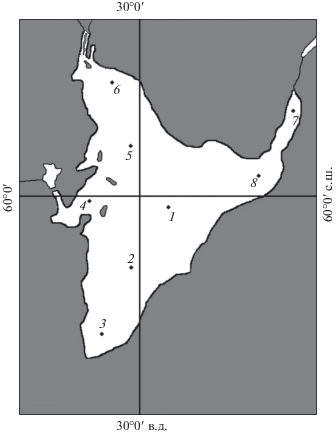
Водохранилище Сестрорецкий Разлив расположено на северо-западе России в черте г. Санкт-Петербурга (рис. 1 ). Площадь водохранилища составляет 10.3 км2, средняя многолетняя глубина – около 2 м, дно ровное и на основной части акватории глубины не превышают 1.5–2.5 м. Водосбор водохранилища занимает площадь 566 км2 и дренируется реками Сестра и Черная. Коэффициент условного водообмена равен 10.
Исследования проводили в августе, октябре и декабре 2015 г., в мае, августе и октябре 2016 г., а также в мае и августе 2018 г. На восьми станциях (см. рис. 1 ) с помощью гидробиологического зонда С-6 Multi-Sensor Platform фирмы TurnerDesignes (США) в столбе воды от поверхности до дна измеряли температуру и содержание хлорофилла а. Содержание в воде взвешенного вещества определяли стандартным гравиметрическим методом, содержание взвешенного органического вещества – методом бихроматного окисления, содержание общего фосфора – стандартным методом сжигания нефильтрованной пробы воды с последующим определением содержания минерального фосфора молибдатным методом с использованием аскорбиновой кислоты в качестве восстановителя [5]. Первичную продукцию и скорость деструкции органического вещества планктоном измеряли методом темных и светлых склянок в кислородной модификации [1]. Пробы фитопланктона изучали с помощью светового микроскопа БИМАМ Р-13-1, используя камеру Нажотта объемом 0.05 мл. Пробы зоопланктона собирали с помощью планктонной сети Джеди с размером ячеи 125 мкм, при этом делали 2–4 протяжки от дна до поверхности воды, пробы макрозообентоса – с помощью дночерпателя Ван-Вина с площадью захвата 0.025 м2. Пробы мейозообентоса собирали почвенным стаканчиком с площадью захвата 1/500 м2 из дночерпателя Ван-Вина по 2 пробы на каждой станции.
Продукцию зоопланктона (Рzp) определяли физиологическим методом [1] с использованием коэффициента К2, который для коловраток, кладоцер и копепод принимали равным 0.4, 0.3 и 0.2 соответственно [6]. При этом затраты на метаболизм рассчитывали по уравнениям, взятым из [1], а продукцию макро- и мейозообентоса – по величинам удельной продукции животных с использованием литературных источников [1, 7–9]. Скорость регенерации фосфора зоопланктоном и зообентосом рассчитывали по уравнениям зависимости удельной скорости экскреции фосфора от массы тела животных [10, 11]. Для расчета скорости регенерации фосфора всем планктонным сообществом скорость деструкции органического вещества планктоном делили на отношение Редфилда: среднее отношение углерода и фосфора в теле гидробионтов 41 : 1 (в весовых единицах) [12].
РЕЗУЛЬТАТЫ
Концентрация общего фосфора в воде водохранилища Сестрорецкий Разлив в 2015–2016 и 2018 гг. значительно превышала 100 мг/м3, а концентрация хлорофилла – 70 мг/м3 (табл. 1), что характерно для эвтрофно-гиперэвтрофных водоемов [3]. Наибольшее содержание хлорофилла в воде в годы исследований наблюдались летом 2018 г.
Таблица 1.
Средняя температура (Т), прозрачность (S), содержание общего фосфора (Р), взвешенного сухого (SDM) и органического (SOM) вещества и хлорофилла а (Chl) в воде водохранилища Сестрорецкий Разлив в 2015–2016 и 2018 гг.
| Дата | Т, °C | S, м | P, мг/м3 | SDM, г/м3 | SOM, г/м3 | Chl, мг/м3 |
|---|---|---|---|---|---|---|
| 04.08.2015 | 18.8 ± 0.1 | 0.27 ± 0.02 | 337 ± 33 | 50.0 ± 6.6 | 22.4 ± 2.7 | 124 ± 14 |
| 20.10.2015 | 5.1 ± 0.1 | 0.76 ± 0.05 | 133 ± 7 | 8.0 ± 1.3 | 4.9 ± 0.8 | 24 ± 3 |
| 01.12.2015 | 0.8 ± 0.1 | 0.58 ± 0.02 | 118 ± 3 | 10.3 ± 0.6 | 5.7 ± 0.6 | 10 ± 2 |
| 16.05.2016 | 16.0 ± 0.1 | 0.51 ± 0.05 | 99 ± 14 | 12.9 ± 2.2 | 6.1 ± 0.3 | 56 ± 4 |
| 10.08.2016 | 20.1 ± 0.3 | 0.32 ± 0.02 | 281 ± 5 | 14.3 ± 2.4 | 9.6 ± 0.8 | 74 ± 11 |
| 17.10.2016 | 5.8 ± 0.1 | 0.48 ± 0.04 | 255 ± 7 | 11.6 ± 0.7 | 3.7 ± 0.3 | 12 ± 1 |
| 15.05.2018 | 19.6 ± 0.6 | 0.54 ± 0.05 | 46 ± 7 | 4.3 ± 0.5 | – | 62 ± 5 |
| 07.08.2018 | 20.8 ± 0.1 | 0.37 ± 0.02 | 153 ± 11 | 34.6 ± 3.3 | – | 212 ± 25 |
Среди фитопланктона по биомассе наибольшую роль в летний период играли крупные диатомовые Aulacoseira muzzanensis (F. Meister) Krammer и цианобактерии Microcystis wesenbergei Kom.: в целом на долю диатомовых приходилось около 80%, а на долю цианобактерий – 18% биомассы фитопланктона. Осенью в фитопланктоне доминировали цианобактерии Planktothrix agardhii (Gomont) Anagnostidis et Komárek и криптофитовые. Зимой доминировали криптофитовые Cryptomonas obovata Skuja, составлявшие около 40% биомассы фитопланктона. Весной в планктоне резко доминировали диатомовые A. muzzanensis, на долю которых приходилось около 50% биомассы фитопланктона.
В 2015–2018 гг. в зоопланктоне водохранилища было обнаружено 67 видов, в том числе 29 видов коловраток (Rotifera), 22 – ветвистоусых (Cladocera) и 16 – веслоногих ракообразных (Copepoda). Средняя численность зоопланктона за все годы исследований составляла 152 ± 51 тыс. экз/м2 (табл. 2). Наиболее многочисленными были мелкие панцирные коловратки Keratella cochlearis (Gosse) и Kellicottia longispina (Kellicott), ветвистоусые ракообразные Bosmina coregoni thersites Poppe и Daphnia cristata Sars. Средняя биомасса зоопланктона составляла 1.77 ± 0.67 г/м3. В состав доминирующего комплекса на разных станциях входили B. coregoni thersites, D. cristata, а также молодь копепод.
Таблица 2.
Численность (N) и биомасса (B) зоопланктона и макрозообентоса в водохранилище Сестрорецкий Разлив в 2015–2016 и 2018 гг.
| Дата | Зоопланктон | Макрозообентос | ||
|---|---|---|---|---|
| N, тыс. экз/м3 | B, г/м3 | N, экз/м2 | B, г/м2 | |
| 04.08.2015 | 428 ± 84 | 3.95 ± 0.74 | 783 ± 425 | 2.27 ± 0.73 |
| 20.10.2015 | 164 ± 33 | 1.48 ± 0.52 | 2474 ± 628 | 4.05 ± 1.53 |
| 01.12.2015 | 85 ± 26 | 0.14 ± 0.05 | 2926 ± 749 | 3.50 ± 0.99 |
| 16.05.2016 | 304 ± 90 | 5.29 ± 1.86 | 1950 ± 536 | 3.00 ± 1.29 |
| 10.08.2016 | 130 ± 37 | 1.87 ± 0.66 | 641 ± 220 | 1.01 ± 0.37 |
| 17.10.2016 | 25 ± 7 | 0.23 ± 0.08 | 1123 ± 301 | 1.98 ± 0.85 |
| 15.05.2018 | 50 ± 11 | 0.42 ± 0.15 | 700 ± 121 | 0.65 ± 0.29 |
| 07.08.2018 | 35 ± 8 | 0.77 ± 0.27 | 910 ± 237 | 0.46 ± 0.13 |
Средняя численность макрозообентоса в водохранилище за все годы исследований составила 1438 ± 313 экз./м2, а средняя биомасса – 2.12 ± ± 0.47 г/м2. Всего в макрозообентосе обнаружено 116 видов и форм донных животных, из которых 55 видов относились к двукрылым насекомым сем. Chironomidae, 34 – к малощетинковым червям (Oligochaeta) и 14 – к ручейникам. Среди последних обычными были личинки Molanna angustata Curt. и Polycentropus flavimaculatus F.J. Pictet. Немногочисленными в зообентосе были пиявки Helobdella stagnalis (L.), двустворчатые моллюски Anodonta subcircularis Clessin, Unio pictorum (L.), Sphaerium sp. и Euglesa sp., водные клещи, водные клопы, личинки поденок и двукрылых насекомых сем. Ceratopoganidae и Chaoborus crystallinus De Geer (Chaoboridae).
Основную роль в зообентосе играли личинки хирономид: они составляли 55% от общей численности и 51% от общей биомассы донных животных. К доминирующим видам относились Chironomus plumosus (L.) и Procladius ferrugineus (Kieffer). Вместе с ними практически во всех биотопах водохранилища встречались Pr. choreus (Meigen), Einfeldia carbonaria (Meigen), Tanytarsus veralli Goetghebuer и часто являлись субдоминантными видами. Кроме хирономид, повсеместно были распространены олигохеты – в среднем за 2015–2016 гг. на них приходилось 43% от численности и 22% от биомассы донных животных. Доминировали Limnodrilus hoffmeisteri Clap. и Potamothrix hammoniensis (Michaelsen).
Биомасса мейозообентоса была низкой и в среднем за сезон 2016 г. составила лишь 0.017 г/м2 при средней численности 400 экз/м2. В пробах были обнаружены только копеподы Thermocyclops oithonoides (Sars), которые также встречались в планктоне.
Наибольшие количественные показатели зоопланктона наблюдались весной и летом, по окончании вегетационного сезона (в декабре 2015 г.) они значительно снизились (см. табл. 2). При этом количественные показатели зообентоса остались достаточно высокими, что связано с более длительным жизненным циклом донных животных. Численность и биомасса как планктонных, так и донных животных в мае и августе 2018 г. оказались намного ниже, чем в те же месяцы 2015–2016 гг.
Первичная продукция планктона весной и летом достигала величин, соответствующих эвтрофно-гиперэвтрофным водам, и была выше, чем скорость минерализации органического вещества планктоном (табл. 3). Максимальная величина первичной продукции измерена летом 2018 г.
Таблица 3.
Первичная продукция планктона (А), минерализация органических веществ (M), отношения скорости регенерации фосфора зоопланктоном (Ez) и макрозообентосом (Ezb) к скорости его регенерация всем планктоном (Epl) в водохранилище Сестрорецкий Разлив
| Дата | А, гС/(м2сут) | D, гС/(м2 сут) | Ez/Epl, % | Eb/Epl, % | Epl, мг Р/(м2 сут) |
|---|---|---|---|---|---|
| 04.08.2015 | 1.10 ± 0.09 | 0.69 ± 0.16 | 25.5 | 1.1 | 16.92 |
| 20.10.2015 | 0.82 ± 0.14 | 0.54 ± 0.05 | 10.0 | 1.0 | 13.17 |
| 01.12.2015 | 0.15 ± 0.05 | 0.42 ± 0.03 | 2.7 | 1.0 | 10.24 |
| 16.05.2016 | 0.68 ± 0.03 | 0.35 ± 0.03 | 45.0 | 3.1 | 8.54 |
| 10.08.2016 | 0.60 ± 0.10 | 0.46 ± 0.08 | 14.0 | 1.1 | 11.28 |
| 17.10.2016 | 0.11 ± 0.02 | 0.12 ± 0.02 | 7.9 | 2.6 | 3.01 |
| 15.05.2018 | 0.27 ± 0.03 | 0.33 ± 0.04 | 4.9 | 0.6 | 7.99 |
| 07.08.2018 | 2.89 ± 0.23 | 2.59 ± 0.25 | 0.8 | 0.2 | 63.26 |
Величины скорости продукции, затраты энергии на метаболизм, рацион и скорость экскреции (регенерации) фосфора зоопланктоном и макрозообентосом были наибольшими в весеннее и летнее время 2015–2016 гг. (табл. 4). В 2018 г. эти величины значительно снизились. Еще больше снизилась доля участия беспозвоночных животных в регенерации фосфора. Если в 2015–2016 гг. доля экскреции этого биогенного элемента зоопланктоном в весенние и летние месяцы составляла от 14 до 45% от скорости его регенерации всем планктоном, то в 2018 г. она составила всего лишь 0.8–4.9% (см. табл. 3). Также заметно уменьшилась скорость экскреции фосфора зообентосом: если весной и летом 2015–2016 гг. она составляла от 1 до 3% от скорости его регенерации всем планктоном, то в 2018 г. она составила 0.2–0.6% (см. табл. 3). С учетом концентрации фосфора в воде время оборота фосфора в экосистеме за счет жизнедеятельности всего планктона и зообентоса в весенне-летнее время 2016 г. составило около 33 сут. В 2018 г. оно снизилось до 9 сут.
Таблица 4.
Скорость продукции (Р), затраты энергии на метаболизм (R), рацион (С) и скорость экскреции (регенерации) фосфора (Е) нехищным и хищным зоопланктоном и макрозообентосом в водохранилище Сестрорецкий Разлив в 2015–2016 и 2018 гг.
| Показатели | Авг. 2015 | Окт. 2015 | Дек. 2015 | Май 2016 | Авг. 2016 | Окт. 2016 | Май 2018 | Авг. 2018 |
|---|---|---|---|---|---|---|---|---|
| Нехищный зоопланктон | ||||||||
| P, кал/(м2 сут) | 604 | 49 | 4 | 296 | 217 | 12 | 38 | 79 |
| R, кал/(м2 сут) | 1517 | 119 | 11 | 767 | 449 | 30 | 129 | 176 |
| C, кал/(м2 сут) | 3510 | 267 | 22 | 1419 | 1097 | 69 | 244 | 424 |
| Е, мкг Р/(м2 сут) | 4087 | 1255 | 276 | 3734 | 1500 | 222 | 368 | 454 |
| Хищный зоопланктон | ||||||||
| P, кал/(м2 сут) | 38 | 6 | 1 | 31 | 20 | 1 | 3 | 9 |
| R, кал/(м2 сут) | 114 | 10 | 1 | 53 | 42 | 2 | 12 | 17 |
| C, кал/(м2 сут) | 228 | 25 | 2 | 139 | 103 | 5 | 22 | 42 |
| Е, мкг Р/(м2 сут) | 232 | 58 | 2 | 110 | 78 | 13 | 25 | 28 |
| Нехищный макрозообентос | ||||||||
| P, кал/(м2 сут) | 65 | 27 | 6 | 70 | 30 | 15 | 20 | 16 |
| R, кал/(м2 сут) | 69 | 51 | 41 | 95 | 40 | 29 | 33 | 31 |
| C, кал/(м2 сут) | 229 | 131 | 78 | 280 | 117 | 74 | 90 | 78 |
| Е, мкг Р/(м2 сут) | 174 | 127 | 101 | 229 | 109 | 75 | 42 | 98 |
| Хищный макрозообентос | ||||||||
| P, кал/(м2 сут) | 7.0 | 4 | 1 | 20 | 4 | 1 | 2 | 1 |
| R, кал/(м2 сут) | 7.2 | 4 | 2 | 27 | 5 | 2 | 2 | 1 |
| C, кал/(м2 сут) | 17.4 | 10 | 4 | 72 | 11 | 4 | 4 | 4 |
| Е, мкг Р/(м2 сут) | 17.2 | 11 | 6 | 38 | 10 | 4 | 4 | 4 |
В целом в мелководном водохранилище Сестрорецкий Разлив роль зоопланктона в потоке энергии от первичных продуцентов к консументам и его роль в регенерации фосфора была значительно выше, чем зообентоса. Так, суммарная величина продукции нехищного зоопланктона за вегетационный сезон 2016 г. составила 34.3 ккал/м2 (табл. 5), или 3.7% от первичной продукции планктона, тогда как продукция нехищного зообентоса составила лишь 6.7 ккал/м2, или 0.7% от первичной продукции планктона. Роль мейозообентоса в потоке энергии через донные сообщества была незначительной: его продукция за сезон 2016 г. оказалась равной лишь 0.064 ккал/м2, а затраты на метаболизм – 0.064 ккал/м2. Доля зоопланктона в регенерации фосфора всем планктоном в 2016 г. составила 21.5%, при этом зоопланктон за вегетационный сезон регенерировал в 12.5 раза больше фосфора, чем зообентос (см. табл. 5).
Таблица 5.
Биотический баланс энергии экосистемы водохранилища Сестрорецкий Разлив за вегетационный сезон 2016 г. (Р – продукция, R – затраты на метаболизм, С – рацион, Е – экскреция фосфора)
| Сообщество | P | R | C | E, мг Р/м2 |
|---|---|---|---|---|
| ккал/м2 | ||||
| Планктон | 916.8 | 637.1 | 1563.0 | |
| Зоопланктон: | ||||
| нехищный | 34.3 | 78.6 | 170.1 | 323.5 |
| хищный | 3.3 | 6.4 | 16.2 | 12.9 |
| Макрозообентос: | ||||
| нехищный | 6.7 | 9.4 | 27.2 | 24.1 |
| хищный | 1.4 | 1.8 | 4.6 | 2.9 |
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Как было показано ранее [1], в озерах, как правило, основные потоки энергии проходят через сообщества планктона, а в водохранилищах – через сообщества зообентоса. Это связано с относительной мелководностью водохранилищ по сравнению с озерами и осаждением в них аллохтонных взвешенных органических веществ, приносимых речными водами и служащих пищей для зообентоса.
Для экосистемы водохранилища Сестрорецкий Разлив такой закономерности не наблюдалось. За все время исследований, за исключением декабря 2015 г. и октября 2016 г., продукция и рацион зообентоса были ниже, чем у зоопланктона (см. табл. 4). Соотношение между продукцией фитопланктона и нехищного зообентоса было в 5 раз ниже, чем между продукцией фитопланктона и нехищного зоопланктона. По-видимому, это было вызвано экологическим стрессом экосистемы водохранилища из-за высокой степени эвтрофирования водоема. В летние месяцы содержание общего фосфора и хлорофилла а в столбе воды соответствовало эвтрофному-гиперэвтрофному статусу [3]. На высокую степень эвтрофирования водохранилища указывал и состав населяющих его гидробионтов: в фитопланктоне большую роль играли цианобактерии, в зообентосе – виды, характерные для загрязненных вод: личинки комаров Ch. plumosus, а также олигохеты L. hoffmeisteri и P. hammoniensis.
Быстрое эвтрофирование водохранилища произошло в конце прошлого века. В начале 1980-х годов его трофический статус оценивали как мезотрофный, а в начале 2000-х уже как гиперэвтрофный. Биомасса фитопланктона за этот период увеличилась в 6–7 раз, возросла роль цианобактерий [13].
Несмотря на мелководность и отсутствие стратификации, на некоторых станциях в 2015–2016 и 2018 гг. встречались черные илы – признак гипоксии в донных отложениях, характерной для эвтрофных водоемов. На периодическую гипоксию у дна также указывает значительное повышение содержания общего фосфора в столбе воды в летние месяцы по сравнению с остальными периодами (см. табл. 1). Такое повышение содержания фосфора летом обычно происходит при восстановительных условиях (аноксии) в донных отложениях, при которых депонированный в них фосфор выделяется в толщу воды [3, 12].
Периодическая гипоксия у дна оказывает повреждающее влияние на сообщества зообентоса, снижая численность и биомассу донных животных [14]. Особенно сильно от гипоксии страдает мейозообентос: в эвтрофных озерах его биомасса обычно составляет лишь несколько процентов от биомассы макрозообентоса [15]. Этим, по-видимому, объясняется крайне низкая биомасса мейозообентоса в водохранилище Сестрорецкий Разлив. Следовательно, низкая эффективность передачи энергии от первичных продуцентов к донным консументам может быть вызвана высокой степенью эвтрофирования водохранилища. Такое снижение эффективности передачи энергии от продуцентов к донным консументам при высокой первичной продукции планктона ранее была отмечена в мелководных озерах Крыма [4].
Еще более значимой была роль зоопланктона в регенерации фосфора: скорость его регенерации во много раз превышала скорость регенерации фосфора зообентосом (см. табл. 5). В целом роль биоты в круговороте этого биогенного элемента оказалась очень высока. Внешняя нагрузка фосфором с водосбора на водохранилище в 2016 г. составила 11 т Р, или 1068 мг Р/м2 в год, а внутренняя нагрузка (геохимическое выделение Р из донных отложений) – 3.2 т Р, или 311 мг Р/м2 в год [16]. По нашим данным, только за вегетационный сезон организмами планктона регенерировалось в 1.5 раза больше фосфора (1563 мг Р/м2 за сезон – табл. 5), чем внешняя нагрузка за год, и в 5 раз больше, чем внутренняя нагрузка этим элементом. Существенная роль в данном процессе принадлежала организмам зоопланктона: величина регенерации фосфора зоопланктоном (323 мг Р/м2 за сезон) была выше, чем внутренняя биогенная нагрузка.
В течение вегетационного сезона 2016 г. время оборота фосфора в толще воды водохранилища за счет жизнедеятельности организмов составляло около месяца, а с усилением степени эвтрофирования этого водоема в 2018 г. оно сократилось более чем в 3 раза. При этом если в 2016 г. значительную роль в регенерации фосфора играли животные зоопланктона и зообентоса, то в более продуктивном 2018 г. их доля в его регенерации была невелика, а основная роль, по-видимому, принадлежала организмам “микробиальной петли”: бактериопланктону и простейшим.
Важно принимать во внимание, что повышение скорости оборота фосфора стимулирует первичную продукцию водоема, поэтому ускорение круговорота этого элемента за счет снижения роли беспозвоночных животных и повышения роли в его регенерации бактериопланктона и протозойного зоопланктона, обладающих благодаря малым размерам гораздо более высокой скоростью оборота фосфора в своей биомассе, должно формировать положительную обратную связь, повышающую первичную продукцию и степень эвтрофирования водоема. Например, несмотря на более низкое содержание фосфора в воде первичная продукция летом 2018 г. была выше, чем летом 2016 г. (см. табл. 1, 3), что, по-видимому, объясняется в 3 раза более высокой скоростью его оборота в воде водохранилища в 2018 г. по сравнению с 2016 г. Таким образом, чем выше роль беспозвоночных животных в круговороте фосфора в водоеме по сравнению с микроорганизмами, тем ниже первичная продукция водоема. Ранее [2] уже указывалось на необходимость учитывать структуру сообществ гидробионтов при выяснении причин эвтрофирования водоемов. Важная роль зообентоса в регенерации фосфора была отмечена в озерах разного типа и трофического статуса [17–19].
Таким образом, проведенные исследования показали, что эвтрофирование водоема отрицательно влияет на поток энергии через сообщества донных животных. Даже в таком мелководном водохранилище, как Сестрорецкий Разлив, поток энергии через зоопланктон значительно превышал поток энергии через зообентос. Особенно низкие величины продукции и деструкции органического вещества зообентосом оказались в год, когда показатели эвтрофирования были самыми высокими. В тот же год наблюдалась наиболее высокая скорость круговорота фосфора за счет жизнедеятельности организмов микропланктона. В целом суммарная скорость регенерации фосфора планктоном и зообентосом значительно превосходила величины как внутренней, так и внешней нагрузки этим биогенным элементом на экосистему водохранилища, что указывает на необходимость учитывать эти процессы при выяснении причин эвтрофирования водоемов.
Работа выполнена и подготовлена к публикации в рамках государственных тем № АААА-А17-117021310121-0 и АААА-А19-119020690091-0 и при поддержке Программы Президиума Российской академии наук № 41 “Биоразнообразие природных систем и биологические ресурсы России” (проект № AAAA-A18-118042390186-9).
Список литературы
Алимов А.Ф., Богатов В.В., Голубков С.М. Продукционная гидробиология. СПб.: Наука, 2013. 343 с.
Алимов А.Ф., Голубков М.С. Эвтрофирование водоемов и структура сообщества гидробионтов // Биол. внутр. вод. 2014. № 3. С. 5–11.
Rast W., Thornton J.A. The phosphorus loading concept and the OECD eutrophication programme: origin, application and capabilities // The Lake Handbook. V. 1. Limnology and Limnetic Ecology. Oxford: Blackwell Publishing, 2004. P. 354–385.
Голубков С.М., Шадрин Н.В., Голубков М.С. и др. Пищевые цепи и их динамика в экосистемах мелководных озер с различной соленостью воды // Экология. 2018. № 5. С. 391–398. [Golubkov S.M., Shadrin N.V., Golubkov M.S. et al. Food chains and their dynamics in ecosystems of shallow lakes with different water salinities // Rus. J. of Ecology. 2018. V. 49. № 5. P. 442–448. doi 10.1134/S1067413618050053]
Wetzel R.G., Likens G. Limnological Analyses. New York: Springer-Verlag, 2000. 429 p.
Салазкин А.А., Иванова М.Б., Огородникова В.А. Методические рекомендации по сбору и обработке материалов при гидробиологических исследованиях на пресноводных водоемах. Зоопланктон и его продукция. Л.: ГосНИОРХ, 1984. 33 с.
Балушкина Е.В. Функциональное значение личинок хирономид в континентальных водоемах. Л.: Наука, 1987. 179 с. (Труды ЗИН АН СССР. Т. 142).
Голубков С.М. Функциональная экология личинок амфибиотических насекомых // Труды Зоол. ин-та РАН. 2000. Т. 284. 294 с.
Курашов Е.А. Методы и подходы для количественного изучения пресноводного мейобентоса // Актуальные вопросы изучения микро-, мейо-, зообентоса и фауны зарослей пресноводных водоемов. Нижний Новгород: Вектор ТиС, 2007. С. 5–35.
Голубков С.М., Березина Н.А. Экскреция фосфора донными беспозвоночными континентальных водоемов // Докл. РАН. 2012. Т. 444. № 5. С. 580–582.
Голубков С.М. Масса тела и экскреция фосфора водными беспозвоночными // Изв. РАН. Серия биологич. 2014. № 1. С. 86–91.
Wetzel G.R. Limnology. Lake and river ecosystems. San Diego: Academic Press, 2001. 1006 p.
Трифонова И.С., Павлова О.А., Афанасьева А.Л., Станиславская Е.В. Летний фитопланктон водохранилища Сестрорецкий Разлив по многолетним наблюдениям // Изв. Самар. науч. центра РАН. 2015. Т. 17. №5(2). С. 522–527.
Berezina N.A., Golubkov S.M. Effect of drifting macroalgae Cladophora glomerata on benthic community dynamics in the easternmost Baltic Sea // J. of Marine Systems. Supplement. 2008. V. 74. P. S80–S85.
Курашов Е.А. Мейобентос в пресноводных экосистемах. Его роль и перспективы исследования // Актуальные вопросы изучения микро-, мейо-, зообентоса и фауны зарослей пресноводных водоемов. Нижний Новгород: Вектор ТиС, 2007. С. 36–71.
Кондратьев С. А., Игнатьева Н.В., Каретников С.Г. Внешняя и внутренняя фосфорная нагрузка на водоем на примере водохранилища Сестрорецкий Разлив // Региональная экология. 2016. № 4. С. 59–70.
Berezina N.A., Maximov A.A., Umnova L.P. et al. Excretion by benthic invertebrates as important source of phosphorus in oligotrophic ecosystem (Lake Krivoe, Northern Russia) // J. of Siberian Federal University. Biology. 2017. V. 10. № 4. P. 485–501.
Ji L., Berezina N.A., Golubkov S.M. et al. Phosphorus flux by bottom macroinvertebrates in a shallow eutrophic Lake Donghu // Knowledge and Management of Aquatic Ecosystems. 2011. V. 402. № 11. https://doi.org/10.1051/kmae/2011073
Драбкова В.Г., Стравинская Е.А. (ред.) Трансформация органического и биогенных веществ при антропогенном эвтрофировании озер. Л.: Наука, 1989. 268 с.
Дополнительные материалы отсутствуют.