Электрохимия, 2019, T. 55, № 2, стр. 171-181
V2O5 с чешуйчатой структурой: морфология, схема образования и свойства суперконденсатора
Б. Сараванакумар a, *, К. К. Пурушотаман b, Г. Мумалидхаран c
a Физический факультет, Инженерно-технологический колледж им. д-ра Махалингама
642003 Поллачи, Индия
b Физический факультет, Инженерно-технологический колледж ССМ
Тамил Наду, Диндугул, Индия
c Физический факультет, Гандиграмский сельскохозяйственный институт
Тамил Наду, Гандиграм, Индия
* E-mail: saravanakumar123@gmail.com
Поступила в редакцию 10.02.2017
После доработки 11.06.2017
Принята к публикации 10.04.2018
Аннотация
В последнее десятилетие электроды на основе оксида ванадия(V) (V2O5) для аккумулирующих энергию устройств вызывают значительный интерес благодаря своим привлекательным физико-химическим характеристикам. В настоящей работе V2O5 с чешуйчатой структурой получали, используя одностадийный гидротермический метод. Результаты аналитических исследований хорошо согласуются с предложенной схемой образования. Чешуйчатая морфология V2O5 упрощает дополнительные пути переноса электронов и эффективный доступ ионов. При использовании в качестве электрода суперконденсатора в нейтральном электролите электрод на основе чешуйчатого V2O5 демонстрирует удельную емкость 472 Ф г–1. Кроме того, он сохраняет максимальную емкость при повышенной плотности тока, подтверждая свои хорошие эксплуатационные характеристики. Суперконденсатор асимметричного типа с использованием чешуйчатого V2O5 в качестве положительного электрода и активированного угля в качестве отрицательного электрода проявляет удельную емкость 69 Ф г–1. Данное устройство демонстрирует плотность энергии 10 Вт ч кг–1 в пределах рабочего диапазона 1 В.
ВВЕДЕНИЕ
Быстрое развитие исследований наноматериалов вызывает значительные инновации в области аккумулирующих энергию электрохимических систем (EES). Устройства EES находят разнообразные приложения в портативных электронных устройствах, гибридных электромобилях и промышленных системах управления энергоснабжением [1–3]. Среди различных систем EES суперконденсаторы (SC) завоевали повышенный интерес благодаря своей способности дополнения или замещения аккумуляторов [4, 5]. Как правило, SC разделяют на категории электрохимических двойнослойных конденсаторов (EDLC) и псевдоконденсаторов в зависимости от процесса аккумулирования заряда. В EDLC использована адсорбция ионов электролита на границе раздела электрод/электролит (использованы электродные материалы на основе углерода). С другой стороны, псевдоконденсаторы аккумулируют заряд посредством обратимой окислительно-восстановительной реакции на поверхности электрода (используются электроды на основе оксидов металлов и проводящих полимеров) [6].
В составе SC инновационный электродный материал, рассматриваемый в качестве основного компонента, определяет суммарную эффективность. Благодаря привлекательным физико-химическим свойствам и простым методикам получения наноструктурированные оксиды переходных металлов (TMO) часто используют в качестве материала электродов для SC [7–10]. Среди различных TMO наноструктуры оксида ванадия(V) (V2O5) пользуются огромным интересом благодаря своим замечательным структурным и электрохимическим свойствам. В нем сочетаются множество степеней окисления, распространенность в природе, слоистая структура и высокая теоретическая удельная емкость [11, 12]. Однако требуется дальнейшее улучшение электрохимических свойств V2O5 в целях его промышленного применения [13].
Для решения этих важных проблем используются различные стратегии. Например, уменьшение размеров от крупных до наночастиц способствует сокращению диффузионных путей, обеспечивая ускоренный доступ ионов. Кроме того, подробно описано, что при введении в V2O5 материалы на основе углерода (углеродные нанотрубки (CNT), наноуглерод, графен), проводящие полимеры (полипиррол (PPy), полианилин (PANI)) и металлы (Na, Cr, Nb) могут выступать в качестве усилителей проводимости и способствовать улучшению электрохимических характеристик. Здесь важно отметить, что для введения инородного элемента в чистый V2O5 требуются дополнительные усилия и использование усложненного лабораторного оборудования, дорогостоящие химические реагенты, сложные экспериментальные процедуры и время [14, 15]. Наноструктуры V2O5 проявляют относительно высокие электрохимические характеристики, гибридный нанокомпозит на основе V2O5 является привлекательным в отношении простоты получения и экономичности.
Разнообразные наноструктуры на основе V2O5, включая нанотрубки, нановолокна, нанопористые сетки, нанопроволоки, наносферы получают, используя различные методики синтеза [16‒20]. Среди различных наноструктур наночешуйчатая морфология является высокопривлекательной благодаря присутствию многочисленных микрометровых и нанометровых каналов, которые выступают в качестве дополнительных путей для диффузии ионов. Кроме того, гидротермический подход представляет собой тонкий инструмент для получения высококачественных наноструктур благодаря своей простоте и легкости регулирования реакционной среды посредством внешних параметров.
Как известно, распространенность лития в земной коре является весьма ограниченной. В связи с этим имеет большое значение нахождение альтернативного рабочего иона, заменяющего Li+. Кроме того, важна проверка возможности реализации аккумулирующих энергию систем, использующих альтернативные рабочие ионы, такие как ионы натрия Na+ и калия K+. В некоторых из побуждающих к действию опубликованных работ продемонстрирована концепция обратимого введения–выведения ионов K+ на примере решетки твердого V2O5 [21, 22]. Меньший радиус гидратированного иона (0.33 нм) и более высокая ионная проводимость (72.2 см2/(Ом моль)) ионов K+ обеспечивают большое преимущество в отношении достижения высоких эксплуатационных характеристик SC [23, 24]. Кроме того, применение нейтральных водных электролитов обеспечивает низкую стоимость, а также безопасность. Благодаря этим полезным свойствам предполагается, что применение водного электролита на основе K2SO4 с V2O5 обеспечит улучшенные электрохимические характеристики.
С учетом всех этих важных обстоятельств в настоящей работе представлен синтез имеющего чешуйчатую структуру V2O5 с применением одностадийного гидротермического подхода без использования дорогостоящих исходных веществ и сложных приборов. Структурные и морфологические исследования подтверждают присутствие чешуеобразной морфологии полученного образца. Далее электрохимические свойства данного материала были систематически исследованы в целях применения в качестве электродов для SC. Этот материал проявляет полезные электрохимические характеристики, такие как повышенная удельная емкость, номинальная мощность и пониженное значение сопротивления переносу заряда, по сравнению с другими гибридными наноструктурами на основе V2O5.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы и реагенты
Оксид ванадия(V) (V2O5), додецилсульфат натрия (SDS) и сульфат калия (K2SO4) получены от компании Sigma Aldrich (Индия). Раствор 30% пероксида водорода (H2O2) приобретен у компании Merck. Химические реагенты имели квалификацию ч. д. а. и были использованы без дополнительной очистки.
Метод получения
Наночешуйки V2O5 получали, используя гидротермическую методику с применением поверхностно-активного вещества. В типичном синтезе 0.72 г товарного V2O5 смешивали с 50 мл деионизированной воды. Полученную смесь перемешивали в течение 15 мин, и в раствор медленно добавляли 10 мл 30% H2O2. Добавление H2O2 инициировало одновременные химические реакции, и полученная желтая суспензия интенсивно закипела и изменила свой цвет на оранжевый. Присутствие H2O2 (30%) инициировало процесс гелеобразования в течение нескольких минут. Во избежание этого в качестве поверхностно-активного вещества добавляли 0.072 г додецилсульфата натрия при интенсивном перемешивании с помощью магнитной мешалки. Раствор перешивали в течение 6 ч с образованием гомогенного раствора. Затем смешанный раствор переносили в имеющий тефлоновое покрытие автоклав из нержавеющей стали и выдерживали при 140°C в течение 20 ч. Полученный в результате материал тщательно извлекали из автоклава и промывали с использованием деионизированной воды. Конечный продукт высушивали при 80°C в течение 10 ч, и он получал наименование VNF.
Методы исследования
Фазовый состав и чистоту образцов анализировали, используя дифрактометр Panalytical X’Pert PRO с источником излучения CuKα (λ = 1.5406 Å). Морфологические данные образца получали методами сканирующей электронной микроскопии, используя микроскоп TESCAN VEGA 3 LMU, и просвечивающей электронной микроскопии, используя микроскоп Philips JEOL JEM 2100. Исследования методами циклической вольтамперометрии (CV), гальваностатического заряда–разряда (GCD) и спектроскопии электрохимического импеданса (EIS) осуществляли, используя электрохимическую рабочую станцию CHI 660 D от компании CH Instruments.
Электрохимические измерения
Электрохимические измерения осуществляли в трехэлектродной ячейке, используя V2O5 в составе рабочего электрода, Ag/AgCl в качестве электрода сравнения и платиновую проволоку как противоэлектрод. Активный материал электрода состоял из 85 мас. % V2O5, 10 мас. % активированного угля и 5 мас. % политетрафторэтилена (Sigma-Aldrich) в качестве связующего материала. Эту суспензию в форме пасты наносили на пеноникелевый токоприемник (1 см2) и сушили при 80°C в течение 4 ч. Раствор 0.5 M K2SO4 служил фоновым электролитом. Все измерения проводили при комнатной температуре. Значения удельной емкости, плотности энергии и плотности мощности определяли на основании массы активного материала в электроде. Формулы, используемые для вычисления электрохимических характеристик, представлены ниже [25, 26]. По измерениям CV удельную емкость получали из следующего уравнения:
(1)
${{C}_{{\text{s}}}} = \frac{1}{{mv({{v}_{{\text{c}}}} - {{v}_{{\text{a}}}})}}\int\limits_{{{v}_{{\text{a}}}}}^{{{v}_{{\text{c}}}}} I ,$Из разрядной части кривых заряда–разряда удельную емкость оценивали из уравнения:
где I (мА), Δt (с), Δv (В) и m (мг) представляют собой плотность тока, время разряда, диапазон потенциала и массу активного материала, соответственно.Следующие соотношения были приняты для оценки плотности энергии и мощности:
где CCell (Ф г–1), Δv (В), E (Вт ч кг–1), P (Вт кг–1) и t (с) представляют собой удельную емкость, диапазон потенциала, плотность энергии, плотность мощности и время, соответственно.РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
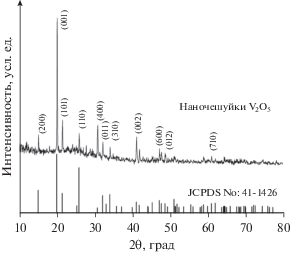
Данные в отношении структуры и фазового состава наночешуек V2O5 (VNF) получены из рентгеновских дифрактограмм, представленных на рис. 1. Существование выраженных резких характеристических пиков при 15.34°, 20.30° и 26.15°, соответствующих плоскостям (200), (001) и (110), четко доказывает кристаллическую природу и орторомбическую фазу V2O5 (карта Объединенного комитета порошковых дифракционных стандартов (JCPDS) № 41-1426). Индицирование произведено в системе щербианита для пространственной группы Pmmn (59). Параметры элементарной ячейки представляют собой a = 0.1151 нм, b = 0.3565 нм, c = 0.4372 нм. Отсутствие пиков других фаз подтверждает фазовую чистоту образцов.
Сканирующая электронная микроскопия (SEM) и просвечивающая электронная микроскопия (TEM) использованы для анализа морфологии свежеприготовленного образца. Рисунок 2a–2в представляют изображения SEM образца V2O5 с различными степенями увеличения, свидетельствующие о морфологии типа наночешуек. Кроме того, SEM-микрофотографии демонстрируют наличие дополнительных пустот между чешуйками. Изображения TEM повышенного разрешения для VNF также представлены на рис. 2в–2д. Они дополнительно подтверждают чешуйчатую морфологию и позволяют оценить межплоскостное расстояние, равное приблизительно 0.56 нм, которое соответствует V2O5 [27]. Чешуйчатая морфология образца предположительно должна улучшить его электрохимические характеристики. Каналы, присутствующие в данной морфологии, обеспечивают дополнительные пути для быстрого проникновения электролита, что, вероятно, может улучшать кинетику электродных процессов.
Рис. 2.
Изображения SEM наночешуек V2O5 при различных степенях увеличения (а–в). Изображения TEM наночешуек V2O5 (г–е).

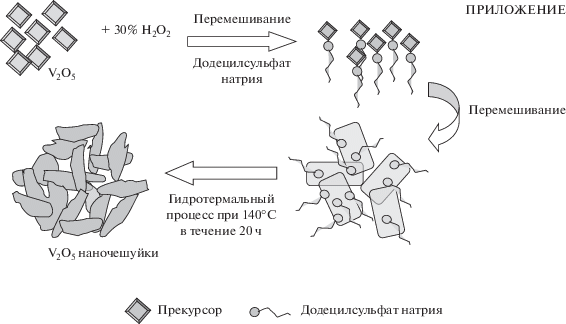
Авторы сделали попытку объяснения механизма образования VNF с помощью схемы, которая представлена на рис. S1 (дополнительные данные). Исходный товарный порошок V2O5 растворяли, добавляя воду и раствор H2O2. Присутствие H2O2 в смешанном растворе инициировало одновременные химические реакции, в ходе которых желтый цвет раствора превращался в рубиново-красный цвет (экзотермическая реакция). Изменение цвета обусловлено присутствием аниона дипероксованадата [VO(O2)2(OH2)]−, а рубиново-красный цвет показывает образование катиона монопероксованадата [VO(O2)2]+ [11, 28]. SDS представляет собой анионное поверхностно-активное вещество, которое использовано во многих недавних работах в качестве модифицирующего-структурирующего поверхность компонента для синтеза разнообразных наноструктур [29, 30]. В частности, SDS может выступать в качестве структурирующего поверхность агента и фиксировать размер наноструктур, предотвращая дальнейшую агломерацию [31]. В раствор V2O5 добавляли SDS в процессе перемешивания магнитной мешалкой. Как правило, температура и продолжительность реакции в гидротермических условиях играют важную роль в образовании наноструктур [32]. Данный раствор выдерживали в гидротермических условиях, используя автоклав. SDS и отрицательно заряженные ионы $\left( {{\text{SO}}_{{\text{4}}}^{{{\text{2}} - }}} \right)$ в растворе образовывали мицеллы, которые начинали окружать ванадиевые зародыши [33]. Агрегацию частиц задерживают алкильные функциональные группы с длинными цепями от SDS, которые создают отталкивание, противодействующее силе Ван-дер-Ваальса [34–36]. Это окружение может предотвращать дальнейший доступ ионов ванадия и вызывает расширение центров зародышеобразования. Свежий оксид ванадия начинал рост на наружных краях мицеллы, и этот боковой рост образует чешуеобразную морфологию, как представлено на рис. S1.
Чтобы выявить возможности VNF для применения в электродах суперконденсаторов, его электрохимические свойства исследовали методом циклической вольтамперометрии (CV). Рисунок 3a представляет кривые CV для электрода VNF при скорости развертки потенциала 5 мВ с–1 (отн. Ag/AgCl). Кривая CV имеет пару окислительно-восстановительных пиков, подтверждая возникновение емкости в результате быстрых фарадеевских реакций на границе раздела электрод/электролит. Согласно оценке из CV, удельная емкость составляет 616 Ф г–1. Это повышенное значение удельной емкости обусловлено присутствием чешуйчатой морфологии образца с наноканалами, открывающими путь для эффективного проникновения ионов, что и повышает удельную емкость. Рисунок 3б представляет кривые CV электрода VNF при различных скоростях развертки потенциала. Он показывает, что площадь под кривой увеличивается при увеличении скорости развертки потенциала, подтверждая улучшенные емкостные свойства электрода [37, 38].
Рис. 3.
Кривые CV при скорости развертки потенциала 5 мВ с–1 для электрода VNF (а), кривые CV электрода VNF при различных скоростях развертки потенциала (б). Изменение удельной емкости в зависимости от скорости развертки потенциала (в). Профили GCD электрода VNF при плотности тока 0.5 А г–1 (г). Профили GCD электрода VNF при различных плотностях тока (д). Изменение удельной емкости в зависимости от плотности тока (е).
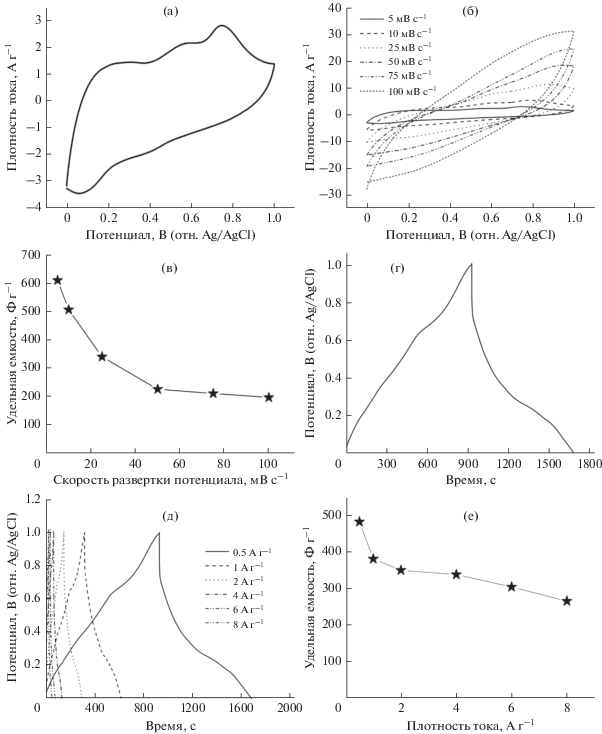
На рис. 3в представлено изменение удельной емкости в зависимости от скорости развертки потенциала (от 5 до 100 мВ с–1). Следует отметить, что удельная емкость уменьшается при увеличении скорости развертки потенциала. Это обычный эффект, обусловленный ограничениями массопереноса ионов электролита, ибо при повышенных скоростях развертки потенциала отсутствует доступ ионов электролита к части активного материала электрода [25, 39–41].
Интересно, что электрод VNF сохраняет удельную емкость 349 Ф г–1 (57%) и 201 Ф г–1 (33%) при скорости развертки потенциала, составляющей 25 и 100 мВ с–1, соответственно. Это подтверждает высокую устойчивость электрода VNF при повышенных скоростях развертки потенциала.
Гальваностатические измерения заряда–разряда (GCD) проводили для электрода VNF в целях получения информации о разрядной емкости, номинальной характеристике и устойчивости. Рисунок 3г представляет профили GCD электрода VNF при плотности тока 0.5 A г–1. Линейная кривая свидетельствует о псевдоемкостной природе процесса заряда–разряда. Разрядная удельная емкость, оцениваемая по кривой GCD, оказалась равной 471 Ф г–1 для электрода VNF. Рисунок S2, представляющий увеличенное изображение кривой GCD электрода VNF, снятой при 0.5 A г–1, подтверждает очень низкое омическое падение напряжения (0.013 В), что также приводит к повышенной емкости электрода VNF.
Хорошая номинальная емкость электрода VNF представляет собой преимущество для осуществления заряда–разряда при повышенных плотностях тока. Профили GCD при различных плотностях тока от 0.5 до 8 А г–1 представлены на рис. 3д. Рисунок 3е представляет график изменения удельной емкости в зависимости от плотности тока. Электрод VNF сохраняет удельную емкость 339 Ф г–1 (70%) и 260 Ф г–1 (54%) при повышенных плотностях тока, составляющих 4 и 8 А г–1, подтверждая превосходные номинальные характеристики данного электродного материала. Номинальные характеристики полученного нами чистого V2O5 выше, чем в недавно опубликованных работах: Ananthakumar et al. (сохраняется только 50% при 1 А г–1 для V2O5/восстановленный оксид графена), Wu et al., (сохраняется 53% при 5 А г–1 для V2O5/графеновый аэрогель) [13, 42]. Циклическая устойчивость представляет собой определяющую электрохимическую характеристику активного материала электрода в целях его промышленного применения. Авторы провели испытание устойчивости при циклическом заряде–разряде электрода VNF в течение вплоть до 1000 циклов при токе10 А г–1, и соответствующий график представлен на рис. S3a. Электрод VNF сохраняет 73% своей первоначальной емкости.
Для дополнительного исследования резистивных характеристик электрода VNF проведены исследования методом спектроскопии электрохимического импеданса (EIS) в диапазоне частот от 0.01 до 100 кГц. Примерная диаграмма Найквиста для электрода VNF представлена на рис. S3b. Модельная эквивалентная схема, используемая для фитинга данных импеданса, представлена в дополнительных материалах (рис. S4). Эта модельная схема включает сопротивление раствора (Rs), сопротивление переносу заряда (RCT), массовую емкость (CL), емкость двойного слоя CDL и сопротивление Варбурга (W). Значение RCT, полученное из диаграммы, составляет 3.9 Ом, что ниже, чем значения, приведенные в других работах. Например, в работе Perera et al. [43] приведено значение 7.6 Ом для электродов, содержащих нанопроволоку оксида ванадия/графеновую бумагу. В работе Zhu et al. [11] приведено значение RCT, составляющее 10 Ом для электрода на основе нанолиста V2O5. Меньшее значение RCT для электрода VNF также говорит о его преимуществе для применения в устройствах.
Чтобы оценить характеристики электрода VNF в работе полной ячейки, авторы изготовили суперконденсатор асимметричного типа, используя VNF и активированный уголь в качестве электродов. Как правило, суперконденсатор асимметричного типа состоит из положительного электрода на основе оксида металла и отрицательного электрода на основе углерода, что, согласно предположениям, должно обеспечивать повышение плотностей энергии и мощности. Схема изготовления данного асимметричного устройства (VNF//AC) на основе VNF представлена на рис. S5. Кривые CV асимметричного устройства VNF//AC при различных скоростях развертки потенциала от 5 до 40 мВ с–1 представлены на рис. 4a.
Рис. 4.
Электрохимические исследования асимметричного суперконденсатора VNF//AC. Кривые CV при различных скоростях развертки потенциала (а). Профили GCD при различных плотностях тока (б). Испытание циклической устойчивости при плотности тока 5 А г–1 (в). Диаграмма Найквиста (г).

Вычисленная по измерениям CV удельная емкость составляет 66, 54, 37, 30, 26 Ф г–1 при 5, 10, 20, 30 и 40 мВ с–1, соответственно. Рисунок 4б представляет профили GCD асимметричного устройства VNF//AC при различных плотностях тока от 1 до 4 А г–1. Близкая к треугольной форма этих профилей GCD обеспечивает улучшенную обратимость заряда–разряда и емкостную характеристику [44]. Определенная по измерениям GCD удельная емкость составляет 69, 50, 34, 20 Ф г–1 при плотности тока 1, 2, 3 и 4 А г–1, соответственно. Недавно Ananthakumar et al. [13] изготовили суперконденсатор, используя нанокомпозит V2O5/rGO, который проявляет удельную емкость 35 Ф г–1 при плотности тока 0.1 А г–1. Кроме того, в предшествующей работе этих авторов был изготовлен суперконденсатор на основе нанокомпозита V2O5/rGO, с удельной емкостью 53 Ф г–1 при 0.5 А г–1 [26]. По сравнению с вышеупомянутыми работами асимметричное устройство VNF//AC проявляет более высокую удельную емкость. Отметим, что вычисление плотности энергии и плотности мощности с использованием двухэлектродных систем является более подходящим и показательным по сравнению с трехэлектродной системой. Плотность энергии и плотность мощности асимметричного устройства суперконденсатора VNF//AC по измерениям GCD составляют 10 Вт ч кг–1 и 314 Вт кг–1, соответственно. Для исследования циклических характеристик данного устройства проводили вплоть до 100 циклов заряда–разряда при повышенной плотности тока 10 А г–1, и соответствующий график представлен на рис. 4c. Асимметричное устройство VNF//AC сохраняет 78% исходной емкости после 100 циклов. Это уменьшение циклической устойчивости устройства обусловлено комбинированным механическим напряжением, создаваемым от обоих электродов в процессе интеркаляции ионов. Рисунок 4г представляет диаграмму Найквиста по результатам измерений EIS для симметричного устройства VNF//AC. Найденное значение RCT устройства составляет 135 Ом.
ВЫВОДЫ
Имеющий чешуйчатую структуру V2O5 синтезирован с применением гидротермальной методики, используя SDS в качестве структурообразующего агента. Морфологические исследования подтвердили чешуйчатую морфологию материала. При испытании в качестве материала электрода суперконденсатора данный материал проявляет максимальную удельную емкость 472 Ф г–1 при пониженном сопротивлении переносу заряда (3.9 Ом). Кроме того, асимметричное устройство на основе данного чешуйчатого V2O5 проявляет удельную емкость 69 Ф г–1 при постоянном удельном токе 1 А г–1. Электрохимические характеристики синтезированных чистых наночешуек V2O5 сопоставимы с характеристиками гибридного нанокомпозита на основе V2O5.
Список литературы
Chen, T. and Dai, L., Carbon nanomaterials for high-performance supercapacitors, Mat. Today, 2013, vol. 16, p. 272.
Yuan, L., Lu, X. H., Xiao, X., Zhai, T., Dai, J. Zhang, F., Hu, B., Wang, X., Gong, I., Chen, J., Hu, C., Tong, Y., Zhou, J., and Wang, Z.L., Flexible solid-state supercapacitors based on carbon nanoparticles/MnO2 nanorods hybrid structure, ACS Nano, 2012, vol. 6(1), p. 656.
Jiang, Y., Wang, P., Zang, X., Yang, Y., Kozinda, A., and Lin, L., Uniformly embedded metal oxide nanoparticles in vertically aligned carbon nanotube forests as pseudocapacitor electrodes for enhanced energy storage, Nano Lett, 2013, vol. 13, p. 3524.
Sarkar, D., Khan, G.G., Singh, A.K., and Mandal, K., High-performance pseudocapacitor electrodes based on α-Fe2O3/MnO2 core–shell nanowire heterostructure arrays, J. Phys. Chem. C, 2013, vol. 117, p. 15523.
Guan, Q., Cheng, J., Wang, B., Ni, W., Gu, G., Li, X., Huang, L., Yang, G., and Nie, F., Needle-like Co3O4 Anchored on the Graphene with Enhanced Electrochemical Performance for Aqueous Supercapacitors, ACS Appl. Mater. Interfaces, 2014, vol. 6(10), p. 7626.
Wang, Y., Song, Y., and Xia, Y., Electrochemical capacitors: mechanism, materials, systems, characterization and applications, Chem. Soc. Rev., 2016, vol. 45, p. 5925.
Zhang, X., Shi, W., Zhu, J., Zhao, W., Ma, J., Mhaisalkar, S., Maria, T.L., Yang, Y., Zhang, H., Hng, H.H., and Yan, Q., Synthesis of porous NiO nanocrystals with controllable surface area and their application as supercapacitor electrodes, Nano Res., 2010, vol. 3(9), p. 643.
Cheng, H., Lu, Z.G., Deng, J.Q., Chung, C.Y., Zhang, K., and Li, Y.Y., A facile method to improve the high rate capability of Co3O4 nanowire array electrodes, Nano Res, 2010, vol. 3(12), p. 895.
Jagadale, A. J., Kumbhar, V.S., Dhawale, D.S., and Lokhande, C.D., Performance evaluation of symmetric supercapacitor based on cobalt hydroxide [Co(OH)2] thin film electrodes, Electrochim Acta, 2013, vol. 98, p. 32.
Yang, H., Jiang, J., Zhou, W., Lai, L., Xi, L., Lam, Y.M., Shen, Z., Khezri, B., and Yu, T., Influences of graphene oxide support on the electrochemical performances of graphene oxide-MnO2 nanocomposites, Nanoscale Res Lett., 2011, vol. 6, p. 531.
Zhu, J., Cao, L., Wu, Y., Gong, Y., Liu, Z., Hoster, H.E., Zhang, Y., Zhang, S., Yang, S.,Yan, Q., Ajayan, P.M., and Vajtai, R., Building 3D Structures of Vanadium Pentoxide Nanosheets and Application as Electrodes in Supercapacitors, Nano Lett., 2013, vol. 13, p. 5408.
Saravanakumar, B., Purushothaman, K.K., and Muralidharan, G., Interconnected V2O5 nanoporous network for high-performance supercapacitors, ACS Appl. Mater. Interfaces, 2012, vol. 4, p. 4484.
Ramadoss, A., Saravanakumar, B., and Kim, S.J., Vanadium Pentoxide/Reduced Graphene Oxide Composite as an Efficient Electrode Material for High-Performance Supercapacitors and Self-Powered Systems, Energy Technol., 2015, vol. 3, p. 913.
Daubert, J.S., Lewis, N.P., Gotsch, H.N., Mundy, J.Z., Monroe, D.N., Dickey, E.C., Losego, M.D., and Parsons, G.N., Effect of Meso-and Micro-Porosity in Carbon Electrodes on Atomic Layer Deposition of Pseudocapacitive V2O5 for High Performance Supercapacitors, Chem. Mater., 2015, vol. 27(19), p. 6524.
Ye, G., Gong, Y., Keyshar, K., Husain, A.M., Brunetto, G., Yang, S., Vajtai, R., and Ajayan, P.M., 3D Reduced Graphene Oxide Coated V2O5 Nanoribbon Scaffolds for High-Capacity Supercapacitor Electrodes, Part. Part. Syst. Charact., 2015, vol. 32, p. 817.
Perera, S, D., Patel, B., Bonso, J., Grunewald, M., Ferraris, J.P., and Balkus, K.J., Jr., Vanadium oxide nanotube spherical clusters prepared on carbon fabrics for energy storage applications, ACS Appl. Mater. Interfaces, 2011, vol. 3(11), p. 4512.
Aravindan, V., Cheah, Y.L., Mak, W.F., Wee, G., Chowdari, B.V.R., and Madhavi, S., Fabrication of High Energy-Density Hybrid Supercapacitors Using Electrospun V2O5 Nanofibers with a Self-Supported Carbon Nanotube Network, ChemPlusChem., 2012, vol. 77, p. 570.
Li, L., Peng, S., Wu, H.B., Yu, L., Madhavi, S., and Lou, X.W., Adv. Energy Mater, 2015, vol. 5, p. 1500753.
Liang, K., Tang, X., Hu, W., and Yang, Y., ChemElectroChem. 2016, vol. 3, p. 704.
Sun, B., Huang, K., Qi, X., Wei, X., and Zhong, J., Adv. Funct. Mater, 2015, vol. 25, p. 5716.
Qu, Q.T., Liu, L.L., Wu, Y.P., and Holze, R., Electrochemical behavior of V2O5 · 0.6H2O nanoribbons in neutral aqueous electrolyte solution, Electrochim. Acta, 2013, vol. 96, p. 8.
Shao, J., Li, X., Qu, Q., and Wu, Y., Study on different power and cycling performance of crystalline KMnO2 · nH2O as cathode material for supercapacitors in Li2SO4, Na2SO4, and K2SO4 aqueous electrolytes, J. Power Sources, 2013, vol. 223, p. 56.
Qu, Q.T., Zhang, P., Wang, B., Chen, Y., Tian, S., Wu, Y., and Holze, R., Electrochemical performance of MnO2 nanorods in neutral aqueous electrolytes as a cathode for asymmetric supercapacitors, J. Phys. Chem. C, 2009, vol. 113(31), p. 14020.
Liu, Y., Clark, M., Zhang, Q., Yu, D., Liu, D., Liu, J., and Cao, G., V2O5 nano-electrodes with high power and energy densities for thin film Li-Ion batteries, Adv. Energy Mater., 2011, vol. 1, p. 194.
Nagamuthu, S., Vijayakumar, S., and Ryu, K.S., Synthesis of Ag Anchored Ag3VO4 Stacked Nanosheets: Toward a Negative Electrode Material for High-Performance Asymmetric Supercapacitor Devices, J. Phys. Chem. C, 2016, vol. 120, p. 18963.
Saravanakumar, B., Purushothaman, K.K., and Muralidharan, G., Fabrication of two-dimensional reduced graphene oxide supported V2O5 networks and their application in supercapacitors, Mat. Chem. Phy. 2016, vol. 170, p. 266.
Saravanakumar, B., Purushothaman, K.K., and Muralidharan, G., MnO2 grafted V2O5 nanostructures: formation mechanism, morphology and supercapacitive features, Cryst Eng Comm., 2014, vol. 16, p. 10711.
Livage, J., Vanadium Pentoxide Gels, Chem. Mater., 1991, vol. 3, 1991, p. 578.
Fu, H., Xie, H., Yang, X., An, X., Jiang, X., and Yu, A., Hydrothermal synthesis of silver vanadium oxide (Ag0.35V2O5) nanobelts for sensing amines, Nanoscale Res Lett., 2015, vol. 10, p. 411.
Derazkola, S.M., Ajabshir, S.Z., and Niasari, M.S., New sodium dodecyl sulfate-assisted preparation of Nd2O3 nanostructures via a simple route, RSC Adv., 2015, vol. 5, p. 56666.
Wang, J., Chen, J., Yu, Y., Yu, W., Meng, X., Chen, J., and Li, D., One-step SDS-assisted hydrothermal synthesis and photoelectrochemical study of Ag4V2O7 nanorods decorated with Ag nanoparticles, CrystEngComm., 2015, vol. 17, p. 6661.
Purushothaman, K.K., Manohara Babu, I., Sethuraman, B., and Muralidharan, G., Nanosheet-assembled NiO microstructures for high-performance supercapacitors, ACS Appl. Mater. Interfaces., 2013, vol. 5, p. 10767.
Mazloom, F.,Arani, M.M., Arani, M.G., and Niasari, M.S., Novel sodium dodecyl sulfate-assisted synthesis of Zn3V2O8 nanostructures via a simple route, J. Molecular Liquids, 2016, vol. 214, p. 46.
Miao, R., Zeng, W., and Gao, Q., SDS-assisted hydrothermal synthesis of NiO flake-flower architectures with enhanced gas-sensing properties, Applied Surface Science, 2016, vol. 384, p. 304.
Jiang, L.Q., Gao, L., and Sun, J., Production of aqueous colloidal dispersions of carbon nanotubes, J. Colloid Interface Sci., 2003, vol. 260, p. 89.
Zhao, Y., Tan, X., Yu, T., and Wang, S.C., SDS-assisted solvothermal synthesis of BiOBr microspheres with highly visible-light photocatalytic activity, Mater. Lett., 2016, vol. 164, p. 243.
Jagadale, A.D., Guan, G., Li, X., Du, X., Ma, X., Hao, X., and Abudula, A., Ultrathin nanoflakes of cobalt–manganese layered double hydroxide with high reversibility for asymmetric supercapacitor, J. Power Sources, 2016, vol. 306, p. 526.
Hsu, C.T., Hu, C.C., Wu, T.H., Chen, J.C., and Rajkumar, M., How the electrochemical reversibility of a battery-type material affects the charge balance and performances of asymmetric supercapacitors, Electrochim. Acta, 2014, vol. 146, p. 759.
Meher, S.K ., Justin, P., and Rao, R., Tuning of capacitance behavior of NiO using anionic, cationic, nonionic surfactants by hydrothermal synthesis, J. Phys. Chem. C, 2010, vol. 114(11), p. 5205.
Liu W.W., Yan X.B., and Xue Q.J., Multilayer hybrid films consisting of alternating graphene and titanium dioxide for high-performance supercapacitors, J. Mater. Chem. C, 2013, vol. 1, p. 1413.
Lee, M., Balasingam, S.K., Jeong, H.Y., Hong, W.G., Lee, H.B.R., Kim, R.H., and Jun, Y., One-step hydrothermal synthesis of graphene decorated V2O5 nanobelts for enhanced electrochemical energy storage, Sci. Rep., 2015, vol. 5, p. 8151.
Wu, Y., Gao, G., and Wu, G., Self-assembled three-dimensional hierarchical porous V2O5/graphene hybrid aerogels for supercapacitors with high energy density and long cycle life, J. Mater. Chem. A, 2015, vol. 3, p. 1828.
Perera, S.D., Liyanage, A. D., Nijem, N., Ferraris, J.P., Chabal, Y.J., and Balkus K.J., Jr., Vanadium oxide nanowire–Graphene binder free nanocomposite paper electrodes for supercapacitors: A facile green approach, J. Power Source, 2013, vol. 230, p. 130.
Kalambate, P.K., Riyaz, A.Dar., Karna, S.P., and Srivastava, A.K., High performance supercapacitor based on graphene-silver nanoparticles-polypyrrole nanocomposite coated on glassy carbon electrode, J. Power Sources, 2015, vol. 276, p. 262.
Дополнительные материалы отсутствуют.