Электрохимия, 2022, T. 58, № 7, стр. 325-360
Углеродные материалы, модифицированные гетероатомами, и их использование в качестве носителей и электрокатализаторов в топливных элементах с твердым полимерным электролитом (обзор)
А. С. Пушкарев a, b, c, *, И. В. Пушкарева a, b, М. В. Козлова a, b, **, М. А. Соловьев a, b, С. И. Бутрим a, b, Цз. Гэ d, В. Син d, В. Н. Фатеев a
a НИЦ “Курчатовский институт”
Москва, Россия
b Национальный исследовательский университет “МЭИ”
Москва, Россия
c Московский физико-технический институт (национальный исследовательский университет)
Долгопрудный, Россия
d Чанчуньский институт прикладной химии, Академия наук Китая
Чанчунь, Китай
* E-mail: pushkarev_as@outlook.com
** E-mail: kozlova_mv@nrcki.ru
Поступила в редакцию 30.04.2021
После доработки 23.11.2021
Принята к публикации 01.02.2022
- EDN: OMJWGQ
- DOI: 10.31857/S0424857022070118
Аннотация
Носители электрокаталитически активных наночастиц в значительной степени определяют активность и стабильность электрокатализаторов реакций окисления водорода и восстановления кислорода в мембранно-электродных блоках топливных элементов (ТЭ) с твердым полимерным электролитом (ТПЭ). В настоящее время главным образом в этом качестве применяются углеродные сажи, которые характеризуются целым рядом недостатков, включая недостаточно высокую стабильность в условиях работы топливных элементов. В этой связи на роль носителей предлагаются альтернативные углеродные наноматериалы, среди которых можно выделить графен и производные наноматериалы на его основе. Такие материалы характеризуются высокой удельной поверхностью, стабильностью, электропроводностью, а также предоставляют широкие возможности по управлению свойствами своей поверхности за счет ее функционализации. В настоящем обзоре обобщены последние достижения в области использования ближайших аналогов графена и производных углеродных наноматериалов на его основе, функционализированных различными элементами, как в качестве электрокатализаторов, так и в качестве носителей электрокаталитически активных наночастиц для ТЭ с ТПЭ (включая ТЭ с прямым окислением спиртов). Рассмотрены последние достижения в отношении активности и стабильности таких наноматериалов и электрокатализаторов на их основе в условиях протекания характерных электрохимических реакций (восстановления кислорода, окисления спиртов и др.), а также особенности их применения в составе мембранно-электродных блоков ТЭ с ТПЭ.
СПИСОК ИСПОЛЬЗОВАННЫХ СОКРАЩЕНИЙ
АС – активный слой
ВОГ – восстановленный оксид графена
МУ – мезопористый углерод
МУНТ – многослойные углеродные нанотрубки
МЭБ – мембранно-электродный блок
ОГ – оксид графена
РВК – реакция восстановления кислорода
РОМ – реакция окисления метанола
РФЭС – рентгеновская фотоэлектронная спектроскопия
СВЭ – стандартный водородный электрод
ТПЭ – твердый полимерный электролит
ТФП – теория функционала плотности
ТФФ – трифенилфосфин
ТЭ – топливный элемент
УНВ – углеродные нановолокна
УНМ – углеродные наноматериалы
УНТ – углеродные нанотрубки
УСТ – ускоренное стресс-тестирование
ЭАП – электрохимически активная поверхность
1. ВВЕДЕНИЕ
Постоянно возрастающая потребность в энергии является важнейшим вызовом, стоящим перед человечеством. Запасы ископаемых видов топлива ограничены, а доля возобновляемых источников энергии в энергобалансе все еще невелика. На этом фоне энергоустановки на основе топливных элементов (ТЭ) с твердым полимерным электролитом (ТПЭ) являются одними из наиболее многообещающих благодаря низкой рабочей температуре, способности к быстрому запуску и остановке, высокой удельной мощности и экологичности. Высокая удельная мощность ТЭ с ТПЭ определяется высокой скоростью протекания реакций восстановления кислорода (РВК) и окисления водорода на поверхности электрокатализаторов на основе Pt и углеродного носителя [1].
Кислая среда и поляризация катода приводят к коррозии электрокатализатора РВК, включая окисление углеродного носителя (традиционно – углеродной сажи с турбостратной структурой, отличающейся высокой степенью аморфизации своей поверхности). Коррозия углеродного носителя может иметь химическую или электрохимическую природу. Предполагается, что окисление углерода протекает через перенос электрона с последующим гидролизом и образованием СО2 (уравнения (1)–(3))11 [2]:
(2)
${\text{C}}_{{\text{s}}}^{{2 + }} + {{{\text{H}}}_{{\text{2}}}}{\text{O}} \to {{{\text{C}}}_{{\text{s}}}}{\text{O}} + 2{{{\text{H}}}^{ + }},$(3)
${{{\text{C}}}_{{\text{s}}}}{\text{O}} + {{{\text{H}}}_{{\text{2}}}}{\text{O}} \to {\text{C}}{{{\text{O}}}_{2}} + 2{{{\text{H}}}^{ + }} + 2{\text{e}}.$На смену углеродной саже стали приходить более упорядоченные углеродные наноматериалы (УНМ), такие как углеродные нанотрубки (УНТ) [3, 4], нановолокна [5] и др. [6], а к наиболее многообещающим альтернативам можно отнести графен и производные УНМ на его основе [7]. Такие материалы характеризуются высокой удельной поверхностью, стабильностью, электропроводностью [8, 9], а также предоставляют широкие возможности по управлению свойствами своей поверхности за счет ее модификации [10–12]. В частности, существующие в настоящее время методы позволяют получать УНМ с различной электропроводностью, гидрофильностью и донорно-акцепторными свойствами, в том числе, за счет допирования различными функциональными группами и гетероатомами [13]. С одной стороны, ряд производных графена может быть использован в качестве функциональных добавок в электрокаталитические слои на основе традиционных носителей, существенно улучшая транспортные свойства слоев [14–17]. С другой стороны, такие материалы представляются перспективными в качестве носителей электрокатализаторов ТЭ с ТПЭ (а также электролизеров воды [18–21], кислородных концентраторов [22, 23] и др. устройств), в частности, за счет облегчения переноса электрона на хемосорбированный кислород и ускорения РВК, а также за счет формирования поверхностных дефектов для осаждения активных металлических наночастиц и повышения их стабильности [24]. Взаимодействие металл–носитель, возникающее между наночастицами и УНМ [25, 26], в существенной степени определяет как морфологию наночастиц, так и их структуру, активность и стабильность. Упрощенно носитель можно представить в виде супрамолекулярного лиганда, взаимодействующего с металлическими наночастицами, а функциональные группы на его поверхности можно рассматривать как центры преимущественного взаимодействия, электронодонорные или электроноакцепторные заместители [25].
Разработка новых носителей металлических наночастиц (включая Pt) позволит повысить активность и стабильность наночастиц, снизить загрузку благородного металла, а также обеспечить оптимальные свойства активного (электрокаталитического) слоя (АС) (гидрофобность/гидрофильность, пористая структура и др.), позволяющие сбалансировать в нем массоперенос реагентов/продуктов электрохимических реакций [27–30].
Другим важным применением допированных УНМ является непосредственное их использование в качестве катализаторов [31–33]. В указанных случаях в качестве активных центров могут выступать как различные дефекты УНМ (“дырки”, “зиг-заг”, “кресло” [34], пятичленные кольца [35], дефекты Стоуна–Уэйлса, единичные или двойные вакансии, дислокации и др. [36]), так и атомы углерода, активированные внедренными в структуру гетероатомами [37]. При этом показано, что краевые дефекты более активны [38], в частности краевой дефект типа “пентагон” более активен в РВК, чем азот в пиридиновой форме [39], хотя точное определение активности определенных видов дефектов сильно затруднено. В одной из последних работ подчеркивается роль микропор [40, 41], высокая доля которых позволяет добиться сильной адсорбции кислорода, высокого числа активных центров и эффективности РВК (n ≈ 4). С другой стороны, высокая доля микропор (<2 нм), вероятно, негативно скажется на массопереносе реагентов и продуктов РВК в каталитическом слое.
За последние годы было опубликовано несколько обзорных работ, в которых рассматриваются различные УНМ, включая графен и его производные, допированные гетероатомами: их получение [13], характеристики, структура и свойства [42], а также возможность их применения в различных областях, включая электрохимическое хранение и преобразование энергии [43‒45], в частности в ТЭ (неплатиновые катализаторы РВК [31, 37, 46, 47]), хранении водорода [48, 49] и др.). Указанные обзорные работы представляют большой интерес для научного сообщества, однако в них либо недостаточно подробно, либо вовсе не рассматриваются аспекты, касающиеся непосредственно применения модифицированного графена и его производных в ТЭ с ТПЭ как в качестве неплатиновых катализаторов [50], так и в качестве носителей активных металлических наночастиц (обычно Pt) в ТЭ с ТПЭ.
В представленном обзоре обобщены последние достижения в области использования ближайших аналогов графена и производных УНМ на его основе, модифицированных различными элементами в качестве электрокатализаторов и носителей электрокаталитически активных наночастиц для ТЭ с ТПЭ. Хотя к настоящему времени более десяти неметаллов удалось успешно инкорпорировать в sp2-углерод [50], в представленном обзоре рассмотрены УНМ, допированные атомами B, N, P, S и F – широко распространенными в качестве гетероатомов для УНМ, используемых в ТЭ с ТПЭ. В табл. 1 приведены основные характеристики указанных атомов: электронная структура, размеры, величина электроотрицательности и др., которые позволяют сравнить их между собой и с углеродом. В обзоре рассмотрены методы получения УНМ (главным образом, графена и его производных), допированных атомами вышеуказанных элементов, их электрохимические свойства и возможность применения таких наноматериалов в качестве носителей активных наночастиц или электрокатализаторов реакций, протекающих в ТЭ с ТПЭ (включая ТЭ с прямым окислением спиртов). Существенная часть работ, представленных в литературе, ограничены исследованием электрохимических свойств электрокатализаторов и их активности в модельных условиях в жидком электролите (зачастую – щелочном, игнорируя кислые электролиты [31]), что не является достаточным для того, чтобы сделать вывод о возможности и перспективности их использования в составе мембранно-электродных блоков (МЭБ) ТЭ. Фокус данного обзора направлен именно на материалы, предлагаемые для ТЭ с ТПЭ (кислые электролиты), а также на особенности, последние достижения и проблемы, связанные с их применением в составе МЭБ ТЭ с ТПЭ. В табл. 2, приведенной в конце статьи, представлены сравнительные характеристики МЭБ ТЭ с ТПЭ на основе различных модифицированных производных графена.
Таблица 1.
Характеристики различных атомов
| Элемент | Радиус Ван-дер-Ваальса, пм | Электронное строение | Кол-во валентных электронов | Электро-отрицательность |
|---|---|---|---|---|
| B | 180 | 1s22s22p1 | 3 | 2.04 |
| F | 147 | 1s22s22p5 | 7 | 3.98 |
| N | 155 | 1s22s22p3 | 5 | 3.04 |
| P | 195 | 1s22s22p63s23p3 | 5 | 2.19 |
| S | 180 | 1s22s22p63s23p4 | 6 | 2.58 |
| C | 170 | 1s22s22p2 | 4 | 2.55 |
Таблица 2.
Сравнительные характеристики различных МЭБ ТЭ с ТПЭ на основе различных модифицированных производных графена
| Топливо/ окислитель (влажность, %) | Анодный каталитический слой | Мембрана | Катодный каталитический слой | Максимальная удельная мощность, Вт/см2 | Стабильность | Источ-ник | ||||
|---|---|---|---|---|---|---|---|---|---|---|
| катали-затор | доля Pt в катализа-торе, % | загрузка платины, мг Pt/см2 | катализатор | доля Pt в катали-заторе | загрузка платины, мг Pt/см2 | |||||
| H2/О2 (100/100) | Pt/C | 20 | 2.5 | Nafion 212 | NF–CC (пористый углерод, допированный атомами N и F) | – | 2 | 0.043 при 0.278 А/см2 и 80°C | NF–CC: незначительный сдвиг E1/2 после
10 000 циклов (0–1 В, насыщ. O2 р-р 0.1 М HClO4 при 50 мВ/с). Pt/C: уменьшение E1/2 на ~50 мВ после 10 000 циклов (те же условия) |
[215] |
| Pt/C | 20 | 2.5 | ~0.7 | |||||||
| H2/O2 (100/100) | Pt/C | 40 | 0.5 | Nafion | P12-900 (графен, допированный атомами Fe и S) | – | 2 | 0.345 при 1.1 А/см2 и 60°C | P12-900: уменьшение E1/2 на 30 мВ после
10 000 циклов (0.6–1 В, насыщ. O2 р-р H2SO4 при 10 мВ/с) Pt/C: уменьшение E1/2 на 73 мВ после 5000 циклов (те же условия) |
[210] |
| FeN/C900 | 2 | 0.306 при 1 А/см2 и 60°C | ||||||||
| H2/воздух (сухой/100) | Tanaka TEC10E40E | 40 | 0.4 | Nafion XL | YS–F-14% (фторированная графитизированная углеродная сажа) | 24 | ~0.4 | ~0.42 при 0.8 А/см2 и 80°C | YS–F-14%: потеря 48% ЭАП после 15000 циклов (прямоугольная волна 0.6–1 В,
3/3 с)*1; 62% ЭАП после 5000 циклов (прямоугольная волна 1–1.5 В,
3/3 с) Pt/C: потеря 7 и 69% ЭАП, соответственно* |
[196] |
| Tanaka TEC10E40E | 40 | 1 | ~0.55 при 1.1 А/см2 и 80°C | |||||||
| H2/O2 (?/?) | Pt/C (E-TEK) | – | 0.5 | Nafion 112 | Pt/CNx | 30 | 0.2 | 0.7 при 1.7 А/см2 и 80°C | – | [153] |
| Pt/CNTs | 0.35 при 1.2 А/см2 и 80°C | |||||||||
| H2/O2 (100/100) | Pt/C | 28.2 | 0.2 | Nafion 211 | Fe–N–C–Phen | – | 4 | 0.56 при ~1.5 А/см2 и 80°C | Fe–N–C–Phen-PANI: Снижение плотности тока (‒70 мА/см2) при 0.6 В после 5000 циклов (0.6–1 В, МЭБ на основе Nafion 115, 80°C, 50 мВ/с)*. Снижение E1/2 на 18 мВ после 10000 циклов (0.6–1 В, насыщ. О2 р-р 0.5 М H2SO4, 50 мВ/с) | [180] |
| Fe–N–C–PANI | 0.87 при ~2 А/см2 и 80°C | |||||||||
| Fe–N–C–Phen–PANI | 1.06 при ~2.1 А/см2 и 80°C | |||||||||
| Pt/C | 28.2 | 0.2 | 1.4 и 80°C | |||||||
| H2/воздух (100/100) | Fe–N–C–Phen | – | 0.26 при ~0.42 А/см2 и 80°C | |||||||
| Fe–N–C–PANI | 0.34 при ~0.6 А/см2 и 80°C | |||||||||
| Fe–N–C–Phen–PANI | 0.38 при ~0.7 А/см2 и 80°C | |||||||||
| H2/O2 (100/100) | Pt/C | 19.87 | 0.1 | Nafion 117 | Pt/N–graphene | 19.22 | 0.3 | 0.29 при 0.655 А/см2 и 40°C | Pt/N–graphene: снижение E1/2 на 33 мВ после 10000 циклов (0,6–?2 В, насыщ. О2 р-р 0.5 М H2SO4, 10 мВ/с). Pt/N–graphene foam: снижение E1/2 на 24 мВ после 10 000 циклов (те же условия) | [162] |
| Pt/N–graphene foam | 19.48 | 0.394 при 0.84 А/см2 и 40°C | ||||||||
| H2/O2 (увлажненные) | Pt/C | 40 | 0.4 | Nafion 112 | Pt/FeN–GnPs | 18.7 | 1.5 | 0.7 при 1.7 А/см2 и 80°C | Pt/FeN–GnPs: 85.8% ЭАП после 3000 циклов
(0–1 В, насыщ. O2 р-р 0.1 М HClO4) Pt/C: 24.2% ЭАП после 3000 циклов (те же условия) |
[183] |
| H2/O2 (100/100) | Pt/C | 20 | 0.5 | Nafion 211 | Fe/N/S–MC | – | 3 | 0.386 при 1.15 А/см2 и 80°C | Fe/N/S–MC: снижение E1/2 на 27 мВ после
10 000 циклов (0.7–1.2 В, насыщ. О2 р-р 0.5 М H2SO4,
50 мВ/с при 25°C) Fe/N–MC: снижение E1/2 на 48 мВ после 10000 циклов (те же условия) |
[204] |
| Fe/N–MC | – | 3 | 0.313 при 0.8 А/см2 и 80°C | |||||||
| H2/O2 (80/80) | Pt/C | 20 | 0.10 | Nafion 212 | Pt/GNF | ~20 | 0.10 | 0.548 при 1.25 А/см2 при 70°C | Pt/C: ЭАП 33% после 10000 циклов (0–1.05 В, насыщ. О2 р-р
0.5 М HClO4, 50 мВ/с). Стабильность носителя: 27% ЭАП после 500 циклов (прямоугольная волна 1.4-0.6 В, 150/30 с, насыщ. О2 р-р 0.5 М HClO4) Pt/GNF: 33% ЭАП после 10000 циклов (те же условия) Pt/N–GNF: 71% ЭАП (те же условия). Стабильность носителя: 53% ЭАП после 500 циклов (те же условия). Pt/NF–GNF: 88% ЭАП (те же условия). Стабильность носителя: 65% ЭАП после 500 циклов (те же условия) |
[216] |
| Pt/N–GNF | ~20 | 0.10 | 0.775 при 1.75 А/см2 при 70°C | |||||||
| Pt/NF–GNF | ~20 | 0.10 | 0.867 при 1.9 А/см2 при 70°C | |||||||
| H2/O2 (увлажненные) | Pt/C | 21 | 0.2 | Nafion 212 | Pt/NC | 21 | 0.4 | 0.365 при 0.98 А/см2 при 60°C | Плотность тока МЭБ су-щественно не изменилась после 20 ч при 0.5 В и 60°C | [146] |
| H2/O2 (100/100) | Pt/C | 20 | ? | Nafion N211 | N–G–CNT/KB | – | 0.5 | 0.3 при 1 А/см2 | Плотность тока МЭБ снизилась на 20% после 100 ч непрерывной работы при 0.5 В | [175] |
| H2/O2 (100/100) | Pt/C | 40 | 0.1 | Nafion 212 | N–CNT/Pt/NC | 40 | 0.1 | 0.604 при 1.4 А/см2 | N–CNT/Pt/NC: 35% ЭАП после 42000 циклов (прямоугольная волна 0.6–1 В, 3/3 с) | [164] |
| H2/O2 (90/90) | Pt/C | 20 | 0.1 | 212 CS Nafion | Pt/DPC | 20 | 0.2 | 0.520 при 1.85 А/см2 | Плотность тока МЭБ существенно не изменилась после 35 ч непрерывной работы при 0.6 В | [60] |
| DPC | – | 2 | 0.021 при 2.4 А/см2 | – | ||||||
| H2/O2 (увлажненные) | Pt/C | 20 | 0.2 | Nafion 212 | Pt/BG-1 | 35 | 0.4 | 0.540 при 1.25 А/см2 | – | [62] |
| Pt/BG-2 | 0.580 при 1.39 А/см2 | – | ||||||||
| Pt/BG-3 | 0.650 при 1.6 А/см2 | Плотность тока МЭБ существенно не изменилась после 25 ч непрерывной работы при 0.6 В | ||||||||
| H2/O2 (90/90) | Pt/C | 40 | 0.25 | Nafion 212 CS | Fe–NSG | – | 4 | 0.225 при 0.870 А/см2 при 80°C; 0.115 при 0.580 А/см2 при 50°C | Плотность тока МЭБ существенно не изменилась после 50 ч непрерывной работы при 0.4 В | [108] |
| H2/O2 (?/?) | Pt-C | ? | 0.2 | Nafion NR211 | F,N,S–rGO | – | 1.5 | 0.045 при 1.45 А/см2 | – | [115] |
| H2/O2 (100/100) | Pt/NCS | 20 | 0.025 | Gore M820.15 | Pt/C | 47 | 0.033 | 0.63 при 1.5 А/см2 | – | [170] |
2.1. Графен и его производные, модифицированные атомами бора
Бор соседствует с углеродом в периодической таблице элементов и имеет лишь на один валентный электрон меньше, что позволяет ему эффективно замещать атомы углерода в гексагональной кристаллической решетке графена. При этом, замещение атома углерода в базальной плоскости (B–C3) графена является наиболее стабильной формой модификации [51]. Атом бора является менее электроотрицательным, чем атом углерода или азота, и его внедрение приводит к возникновению в графене проводимости p-типа. Длина связи B–C лишь незначительно больше длины связи C–C, поэтому замещение углерода атомом бора вызывает не такие сильные деформации, как в случае с азотом, и такое замещение протекает легче. Кроме того, благодаря высокой энергии связи B–C, механические свойства графена после допирования сохраняются, а теплопроводность значительно снижается [52].
Как правило, модифицированные бором производные графена получают двумя способами: путем прямого синтеза в одну стадию или в два этапа, используя для этого исходный графеновый материал (обычно графит, оксид графена (ОГ) или восстановленный оксид графена (ВОГ)) и прекурсор бора [13]. К наиболее распространенным методам модификации УНМ атомами бора можно отнести высокотемпературные твердофазные реакции [53], гидротермальный/сольвотермальный синтез [53–55], синтез в плазме дугового разряда [53] и химическое парофазное осаждение [56–58].
Если модифицировать графит путем твердофазной реакции при высокой температуре (>2000°C), то преимущественно происходит замещение атомов углерода. При использовании оксида графита в качестве исходного материала и более низких температур (900–1200°C) помимо замещения атомов углерода также образуются функциональные группы, включая эфиры борной и бориновой кислот (рис. 1) [53].
Твердофазный синтез является одним из наиболее широко используемых подходов благодаря своей высокой производительности скорости и дешевизне [53]. Например, в [59] в качестве исходного углеродного материала использовался оксид графита, полученный методом Штауденмайера, а BF3Et2O использовали в качестве прекурсора бора. Регулируя температуру и состав атмосферы, удавалось варьировать концентрацию атомов бора в решетке графена, хотя максимальное содержание бора не превысило 1 ат. %. С другой стороны, в [60] предложен легко масштабируемый метод получения допированного атомами бора графена с концентрацией бора до 5.93 ат. %, с использованием борной кислоты и оксида графита в качестве прекурсоров бора и углерода соответственно. В [61] результаты исследований методом рентгеновской фотоэлектронной спектроскопии (РФЭС) показали присутствие в допированном бором УНМ атомов бора в следующих конфигурациях: B4C, BC3, BC2O и BCO2. ОГ и B2O3 использовались в качестве прекурсоров допированного бором графена, который получили методом отжига первого при 1200°С.
Метод гидротермального синтеза является относительно простым и дешевым, а также позволяет получать производные графена, допированные бором, в больших масштабах [13, 54, 55]. Зачастую борная кислота используется в качестве прекурсора бора [55]. В частности, в [59] для получения графена, допированного бором c содержанием последнего 3.3 ат. %, использовали гомогенный водный раствор оксида графита (3 мг/мл) и H3BO3. В [62] фотоэлектронный спектр линии B1s показал наличие атомов бора в следующих конфигурациях (в порядке убывания): BC2O, ВСО2, ВС3 (замещение атома углерода) и B2O3 (непрореагировавший остаток прекурсора – около 1.5%).
Метод химического парофазного осаждения также широко используется для получения графена и его производных на поверхности различных переходных металлов (Ni, Pd, Fe, Cu и др.). Пленки многослойного графена с концентрацией атомов бора до 1.5 ат. % (преимущественно в форме BC3) были получены в работе [63], используя метан и диборан в качестве прекурсоров. Недостатками этого метода является необходимость в переносе графеновой пленки с поверхности подложки на целевую поверхность, а также в контроле роста единичного слоя пленки [53].
К многообещающим подходам можно отнести импульсное лазерное напыление [64]. В частности, в работе [52] на подложку SiO2, предварительно покрытую пленкой Ni толщиной 60 нм, в результате лазерной абляции соответствующих мишеней конденсировалась пленка допированного бором графена толщиной 10 нм с концентрацией бора около 2 ат. %, преимущественно связанного с углеродом в конфигурациях BC3 и BC2O. Число слоев составило от 1 до 4.
Другим перспективным подходом является синтез нанодисперсных порошков в плазме дугового разряда, который был детально исследован в работе [65]. Образцы многослойного графена, допированные бором, готовились в атмосфере водорода и B2H6. Показано, что атомы бора могут замещать атомы углерода с sp2-гибридизированной структурой в концентрации 1–3 ат. %. Число слоев допированного материала составило от 2 до 5, а его структура характеризуется более высокой степенью дефектности. Аналогичный метод был использован в работе [66], в которой допированные бором (преимущественно в форме B4C и BCO2) графеновые нанолисты получены дуговым разрядом графитизированных электродов в присутствии диборана, He и H2.
2.2. Графен и его производные, модифицированные атомами азота
До настоящего времени наибольшее внимание научного сообщества уделялось допированию азотом УНМ. В целом, методы получения УНМ, допированных азотом, можно разделить на два основных направления: синтез УНМ (например, активированного углерода [67], УНТ [68], графена [69], ОГ или ВОГ [70, 71]) с его последующим допированием азотом и непосредственный синтез модифицированного азотом УНМ [71]. Первая группа методов включает в себя непосредственную обработку УНМ азотсодержащими прекурсорами, которая может включать: гидротермальную карбонизацию [72, 73], высокотемпературный отжиг [74, 75], плазменную обработку [76, 77] или дуговой разряд [65]. В качестве прекурсоров азота используются аммиак [71], мочевина [68, 78], меламин [79] и др. [71]. Ко второй группе относятся такие методы, как химическое парофазное осаждение [80], пиролиз различных видов биомассы (например, раковины креветок [81] или ферментированный рис [82]) или азотсодержащих полимеров (полипиррол, полианилин [83, 84]). Необходимо отметить, что последняя группа методов отличается относительной простотой исполнения, широким многообразием доступных исходных веществ, а также потенциалом формирования гомогенно допированных азотом УНМ.
Будучи внедренным в структуру графена, атом азота может находиться в одном из трех основных состояний, которые определяются конфигурацией его связей с соседними атомами: графитоподобный (N–C3), пиридиновый (C=N–C) или пиррольный (C–N–C) [71, 85] (рис. 2). В частности, пиридиновый атом азота связывается с двумя атомами углерода и вносит один p-электрон в общую π-систему. Пиррольный атом азота вносит два p-электрона в общую π-систему и связывается с атомами углерода с образованием пятичленного кольца. Графитоподобный атом азота замещает атом углерода в гексагональном кольце. При этом пиридиновый и графитоподобный азот являются sp2-гибридизированными, а пиррольный – sp3-гибридизированным. Помимо указанных состояний пиридиновый атом азота может связываться с кислородом, образуя N-оксид [35, 86].
Отжиг ОГ в присутствии аммиака преимущественно приводит к внедрению атомов азота в пиридиновой и графитоподобной форме, а отжиг с полианилином и полипирролом – в пиридиновой и пиррольной форме [35]. Использование плазменной обработки приводит к формированию центров пиррольного, пиридинового и графитоподобного азота [69, 87], а также некоторого количества N-оксида [88]. Конкретная конфигурация атомов азота в модифицированных УНМ определяется методом синтеза и используемым прекурсором.
2.3. Графен и его производные, модифицированные атомами P
Атомы фосфора обладают высокой донорной способностью, в связи с чем могут замещать собой атомы углерода в кристаллической решетке графена. Поскольку длина связи C–P (1.84 Å) больше длины связи C–C (1.54 Å), при внедрении атома фосфора образуется пирамидальная структура с атомом фосфора в вершине [13]. В силу несколько меньшей электроотрицательности фосфора (2.19) также происходит перераспределение заряда на поверхности УНМ и нарушение его электронейтральности [89].
Основным методом модифицирования графена и его производных фосфором является термическая обработка при высоких температурах (400–1000°С) в атмосфере Ar, N2 и H2 с использованием различных прекурсоров. Как правило, в качестве прекурсоров фосфора выступает фосфорная кислота [90–93] и трифенилфосфин (ТФФ) [94–97], реже – фитиновая кислота [98], и гексафторфосфат 1-бутил-3-метилимидазолия (BMIM–PF6) [99]. Концентрация фосфора в полученных модифицированных наноматериалах составляет 0.6–4.96 ат. %. Исследований, посвященных другим методам синтеза, пока немного. Стоит отметить сольвотермальный синтез с использованием микроволн (прекурсоры – ОГ и фосфорная кислота) [100] и электрохимический метод (электролит – фитат натрия C6H6Na12O24P6), описанный в работе [101], которые позволяют достичь значений концентрации фосфора 20.4 и 7.0 ат. %, соответственно.
Согласно работам [90, 93], для получения модифицированного фосфором графена ОГ смешали с фосфорной кислотой и деионизованной водой с образованием гомогенной смеси, которую после обработки ультразвуком заморозили, высушили, а затем отжигали при 800°С в течение 2 ч в атмосфере H2/Ar (5/95%). Значительное количество связей C–P свидетельствует о внедрении атомов P в решетку графена. Авторами работы [91] показано, что более высокая температура обработки способствует увеличению удельной поверхности до 1014 м2/г (1000°С), а в фотоэлектронном спектре P2p полученных образцов преобладают –C–PO2 и –C–PO3.
Применение ТФФ в качестве прекурсора фтора подробно описано в работе [94]. Смесь ОГ и ТФФ отжигали в печи при 950°С в течение 45 мин в атмосфере Ar. Авторы [95] выдерживали смесь ОГ, ТФФ и изопропанола при 1000°С в течение 30 мин в атмосфере Ar и еще 30 мин в атмосфере H2/Ar (10/90%), что позволило частично восстановить остаточные кислородные функциональные группы ОГ и снизить содержание кислорода. Содержание фосфора в полученных образцах составило 0.92–1.26 ат. %. При исследовании выявлено, что в образцах преобладают внедренные атомы фосфора, связанные с тремя sp2-гибридизированными атомами углерода, однако присутствует и элементный фосфор.
Использование фитиновой кислоты для допирования фосфором графена подробно описано в [98]. В частности, смесь водной дисперсии ОГ и раствора фитиновой кислоты помещалась в автоклав и выдерживалась при 180°С в течение 12 ч, а затем отжигалась при 850°C в течение 2 ч в атмосфере N2. Приготовленный наноматериал содержит 2.4 ат. % фосфора. Элементное картирование полученных образцов указывает на достаточно равномерное распределение атомов P по полученному образцу. Внедрение атомов фосфора в углеродную структуру подтверждается наличием связей C–P, хотя часть атомов фосфора связана с кислородом P–O.
2.4. Графен и его производные, модифицированные атомами серы
Согласно теории функционала плотности (ТФП), атомы серы могут адсорбироваться на поверхности графена (рис. 3а), замещать краевые атомы углерода (рис. 3б, 3в), замещать краевые атомы углерода с образованием оксида (рис. 3г, 3д) и образовывать кольцевой кластер, соединяющий два листа (рис. 3е) [34].
Рис. 3.
Формы атомов серы в составе графена согласно ТФП: адсорбированный атом S (а), замещение атомом S краевого атома C типа “зигзаг” (б) и “кресло” (в), замещение атомом S краевого атома C типа “зигзаг” (г) и “кресло” (д) с образованием оксида и образование кольцевого кластера (е). Шарики белого, серого, желтого и красного цветов обозначают атомы водорода, углерода, серы и кислорода, соответственно [34].

Согласно [102], в результате пиролиза ОГ и бензилдисульфида атомы серы могут быть инкорпорированы в структуру УНМ с помощью ковалентных связей. В частности, результаты исследований методом РФЭС выявили присутствие связей C–S–C (тиофен), C–SOx–C (x = 2, 3 и 4) и C–SH (тиол). При этом длина связи C–S (1.78 Å) примерно на 25% длиннее связи C–С (1.54 Å) [103]. В отличие от бора, азота и фосфора внедрение серы в структуру графена не вызывает существенного перераспределения заряда, так как значения электроотрицательности углерода (2.55) и серы (2.58) близки между собой. Графен обладает нулевой спиновой плотностью (плотностью неспаренных электронов); несовпадение внешних орбиталей серы и углерода вызывает неравномерное распределение спиновой плотности на допированном серой материале, что может отвечать за его электрокаталитическую активность, например в РВК [102, 104].
Наиболее распространенными методами допирования графена и его производных атомами серы является высокотемпературная термическая обработка (чаще всего – пиролиз органических прекурсоров или термическое отшелушивание) при температурах 900–1100°C [13, 93, 105–109], а также этанол–термический синтез [110, 111] сольвотермальный/гидротермальный синтез [112, 113] и тионирование [114, 115].
Отжиг прекурсора графена (например, ОГ [93, 116]) в атмосфере газообразного серосодержащего вещества является простым, доступным и потому широко используемым методом допирования производных графена. Зачастую H2S [117] используется в качестве источника серы, ОГ размещается на подложке из кремния или диоксида кремния, а допирование осуществляется посредством отжига при температуре ~1000°C. Концентрацию серы в полученном материале и его пористую структуру можно варьировать путем изменения дозировки прекурсора серы и температуры нагрева [13, 93, 116]. Также для синтеза производных графена применяют термическую обработку ОГ и органических прекурсоров, таких как фенил дисульфид [102, 107, 118], бензил дисульфид [106, 119], сульфированный полианилин [105], дибензотиофен [120, 121] и др., а содержание серы варьируется в широких пределах 0.2–13.8 ат. % в зависимости от конкретной методики и прекурсора. Другим схожим подходом является метод термического отшелушивания [108]. В работе [109] авторы исследовали процесс термического отшелушивания ОГ в атмосфере SO2, H2S или CS2 при 600 или 1000°C. Результаты исследований методом РФЭС показали максимум C–S при ~286.5 эВ, что указывает на успешное внедрение атомов серы при отслаивании и ее ковалентное связывание с углеродной структурой. Для ОГ, обработанного в атмосфере SO2, характерна более высокая концентрация кислорода. Относительная концентрация серы в полученных образцах составила 0.10–11.99 мас. %.
Достаточно новым и экологически безопасным подходом является этанол-термический синтез. В работе [110] показано, что этот метод позволяет эффективно предотвратить образование окисленных форм серы, которые образуются при синтезе путем отжига. Сера в составе полученного материала находится преимущественно в форме C–S–C, а ее концентрация составила ~1.2 ат. %, что сравнимо с образцами, приготовленными методом отжига.
Недавно в работе [113] был продемонстрирован простой сольвотермальный метод получения ВОГ, допированного серой. В частности, раствор ОГ в диметилсульфоксиде после ультразвуковой гомогенизации обрабатывали в тефлоновом автоклаве при 180°С в течение 18 ч. Сера в полученном материале присутствует в виде C–S–C (инкорпорирована в углеродную структуру) и незначительная доля – в окисленной форме [113]. Содержание серы (по данным энергодисперсионной рентгеновской спектроскопии) составило 4.7–5.3 ат. %.
Тионирование является другим перспективным методом производства допированного серой графена, в котором ОГ используется в качестве прекурсора углерода [114, 115]. В частности, при обработке ОГ и P4S10 в кипящем диметилформамиде, атомы кислорода в ОГ были частично замещены серой и одновременно восстановлены. Полученный наноматериал также содержит тиоловые группы [122], что способствует его растворению в различных растворителях и облегчает последующие этапы синтеза (в частности, если необходимо получить наноматериал, допированный несколькими элементами) [115], а подавляющая доля серы находится в форме тиофена [114]. Достигнутые значения концентрации серы составляют 1.06–2.2 ат. %.
2.5. Графен и его производные, модифицированные атомами фтора
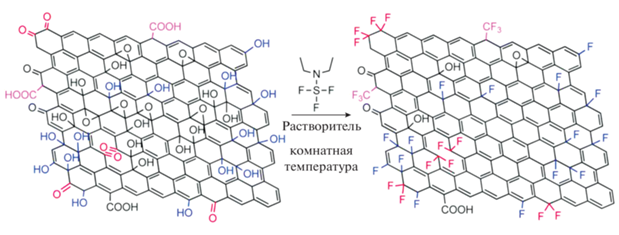
Фторированные УНМ обладают важными отличительными свойствами, такими как химическая стабильность, возможность регулировать запрещенную зону, хорошая теплопроводность и стабильность, а также, в некоторых случаях, супергидрофобность за счет своей уникальной структуры и полярной связи C–F [123–125]. Они содержат в своем составе различные фторуглеродные связи, включая ионные, донорно-акцепторные и ковалентные (C–F, C–F2, C–F3) с различным соотношением F/C [124]. Рисунок 4 иллюстрирует структурные изменения, которые происходят с ОГ в результате фторирования с использованием диэтиламиносульфотрифторида.
Рис. 4.
Принципиальная схема синтеза фторированного графена при реакции между ОГ и диэтиламиносульфотрифторидом, при комнатной температуре [126].
Основные методы приготовления УНМ, допированных фтором, включают в себя прямую обработку прекурсора фторсодержащим газом [127, 128], в том числе химическое парофазное осаждение [129], плазменные методы [130, 131], термический отжиг [132, 133] и различные “мокрые” химические методы синтеза [134–137]. Содержание фтора в модифицированном наноматериале в зависимости от методики синтеза и прекурсора может достигать 48 ат. % и более.
В частности, в работе [138] продемонстрирован простой и масштабируемый способ фторирования ВОГ с помощью прямой обработки УНМ газовой смесью N2/F2 (20 об. % F2) при температурах 20–180°С и давлении 3 бар. Соотношение F/С, полученного фторированного ВОГ, достигало 1.05 при температуре 180°С и продолжительности процесса 72 ч. Результаты РФЭС линии C1s показали следующее соотношение фторсодержащих компонентов: C–F : C–F2 : C–F3 = 5.5 : 6 : 11.9, причем содержание C–F3 значительно возрастает с ростом содержания фтора в образце.
Химические методы модификации основаны на химической реакции между фторсодержащим прекурсором и раствором прекурсора углерода, а концентрация фтора и структура полученного наноматериала регулируются, главным образом, путем изменения концентрации раствора фторсодержащего прекурсора и температуры реакции [124]. К ним, в частности, можно отнести гидротермальный/сольвотермальный синтез [134–136], где в качестве прекурсоров фтора часто используют плавиковую кислоту (HF) [136].
При плазменной модификации зачастую используется плазма SF6 [130, 131] или SF4 [139]. В частности, в работе [131] показано, что при плазменной обработке однослойного графена содержание фтора зависит от продолжительности процесса, а максимальная концентрация атомов фтора составила 24.6 ат. % (при обработке в течение 20 с), что близко к результатам теоретических расчетов.
Интересно отметить, что при обработке многослойных углеродных нанотрубок (МУНТ) газообразным фтором или фторсодержащим газом фтор реагирует только с поверхностью внешнего углеродного слоя, в то время как внутренние слои остаются нетронутыми [123].
2.6. Выводы по разделу
К настоящему времени разработано большое число различных методов получения производных графена и других УНМ, допированных гетероатомами, концентрация которых варьируется в широких пределах от 0.1 до 20–25 ат. %. Полученные материалы характеризуются высокой удельной площадью поверхности – от 300 (ВОГ) до 1500 м2/г (мезопористый углерод), и характеризуются, как правило, мезопористой структурой и низким средним диаметром пор (2–8 нм). Известные методы получения позволяют в некоторых пределах управлять не только концентрацией допантов в структуре УНМ, но и регулировать соотношение различных функциональных групп, что дает возможность управлять характеристиками допированных материалов в зависимости от поставленной задачи.
3. ПРИМЕНЕНИЕ МОДИФИЦИРОВАННЫХ ГРАФЕНОВЫХ МАТЕРИАЛОВ В ТЭ С ТПЭ
3.1. Графеновые материалы, модифицированные одним элементом
3.1.1. Графеновые материалы, модифицированные атомами бора. Авторы [62, 140] сравнили характеристики ВОГ, допированного бором, в качестве носителя электрокаталитически активных частиц, синтезированных тремя различными методами, а именно путем восстановления боргидридом натрия (BG-1), полиольным (BG-2) и модифицированным полиольным методом (с использованием микроволнового излучения) синтеза (BG‑3). Атомы бора находятся в форме BC2O, ВСО2, ВС3 и B2O3 (непрореагировавший остаток ~1.5%). Полученные катализаторы были исследованы в составе водородно-кислородного ТЭ с ТПЭ. ТЭ на основе Pt/BG-3 продемонстрировал наибольшую удельную мощность – 565 мВт/см2 (при 70°С), что в 3.3 раза выше по сравнению с ТЭ на основе Pt/G [62]. Такое значительное улучшение характеристики авторы связывают с высокой активностью ВОГ, допированного атомами B, по сравнению с недопированным носителем, которая в свою очередь связана с более низкой электроотрицательностью бора по сравнению с углеродом (облегчение адсорбции кислорода), а также их способностью быть донорами электронов. Pt/BG-3, полученный модифицированным полиольным методом, продемонстрировал более высокую удельную электрохимически активную поверхность (ЭАП) (49.57 м2/г Pt) за счет равномерного распределения более мелких наночастиц Pt (~4 нм) по сравнению с другими образцами [140].
Методом пиролиза смеси ОГ/H3BO4 при 700°С синтезировали ВОГ, допированный бором, а катализатор на его основе – Pt/BG – удалось получить полиольным методом [141]. Для преодоления известного недостатка производных графена – рестекинга нанолистов (агломерации) и сопутствующего снижения ЭАП и активности в РВК – авторы применили “интеркалирование” катализатора Pt/BG различным количеством сажи (Pt/BG/С). МЭБ ТЭ с ТПЭ на основе Pt/BG/C с добавкой 30 мас. % сажи в качестве катодного катализатора показал наилучшие рабочие характеристики, в частности при напряжении 0.6 В плотность тока составила 0.166 А/см2. Результат объясняется высокой активностью Pt/BG в РВК и формированием более крупных пор за счет внедрения частиц (агломератов) сажи в активный слой, способствующих ускорению диффузии кислорода к активным центрам. Дальнейшее повышение содержания сажи приводит к частичному экранированию наночастиц Pt и снижению ЭАП. Кроме того, показано, что Pt/BG также отличается более высокой долговечностью благодаря более прочной связи между наночастицами Pt и допированным носителем. Согласно результатам работы [142], допирование ВОГ атомами B в различной концентрации позволило значительно улучшить дисперсию наночастиц Pt по поверхности носителя и повысить содержание Pt в составе катализатора Pt/BG, которое сопровождалось снижением размера наночастиц Pt с 2.73 до 1.95 нм при содержании В около 3 ат. %. При этом увеличение содержания Pt (до 13%) оказалось пропорционально росту концентрации атомов В в носителе, конфигурации которых включают BC2O и BCO2. Допирование атомами B приводит к переносу π-электронов через сопряжение электронно-дефицитного атома B с неактивной π‑электроной системой ВОГ. Работа выхода электрона из атомов B меньше, чем у атомов Pt (4.45 и 4.48 против 5.45 эВ). Следовательно, электрон переносится от атома B в допированном носителе к атому Pt, что приводит к увеличению содержания металлической Pt и соответствует улучшению кинетики РВК на катоде [142].
В работе [143] допированный бором ВОГ (полученный отжигом ОГ и H3BO4 в атмосфере H2/Ar при 1000°С) использован в качестве носителя катализатора Pt/BG (40 мас. % Pt) в реакции окисления метанола (РОМ). Допирование носителя атомами В в форме BC2O и BCO2 позволило повысить число дефектов и обеспечить равномерное восстановление мелких наночастиц Pt. Высокая активность катализатора в РОМ связана со снижением энергии d-орбитали Pt и соответствующим ослаблением связи с отравляющими интермедиатами, например СО.
3.1.2. Графеновые материалы, модифицированные атомами азота. Допирование азотом позволяет изменять электронные свойства УНМ и придавать им полупроводниковые металлические свойства, в связи с чем допированные наноматериалы демонстрируют повышенную подвижность электронов по сравнению с их недопированными формами [144, 145].
Применение углеродных носителей, допированных азотом, не только способствует лучшей дисперсии наночастиц Pt при их восстановлении [146, 147], но также повышает их стабильность [148, 149]. Согласно расчетам [150], внедренные атомы азота не связываются непосредственно с Pt, но способствуют двукратному увеличению энергии связи соседних атомов С и Pt, что, в свою очередь, предотвращает миграцию и рост наночастиц в условиях РВК, хотя в работе [151] показано, что существенная доля атомов N в электрокатализаторе на основе азотированного ВОГ (5 мас. % Pt) оказалась связана с Pt (Pt–N). Применение углеродных носителей, допированных азотом, способствует росту электрокаталитической активности наночастиц Pt в РВК. В частности, согласно [152], более высокая активность и стабильность электрокатализатора на основе азотированного ВОГ связана с (1) оптимальным размером и распределением наночастиц по поверхности носителя, (2) более высокой проводимостью носителя и (3) участием атомов азота непосредственно в качестве активных центров РВК. С другой стороны, повышение активности связывается и с взаимодействием между носителем и наночастицами на его поверхности, которое выражается в изменении их электронной структуры [153]. Предполагается, что перенос электронов от носителя на незаполненные орбитали Pt осуществляется посредством азотсодержащих групп, что приводит к увеличению электронной плотности наночастиц Pt, способствует поддержанию поверхности в металлическом состоянии и, таким образом, приводит к росту электрокаталитической активности наночастицы в РВК. Более высокая активность Pt на модифицированных азотом носителях в РВК связана с изменением энергии адсорбции кислорода на поверхности такого катализатора. Показано, что адсорбция атомарного кислорода слабее в случае углерода, допированного атомами азота, длина связи O–O увеличивается и диссоциация O2 протекает легче, что объясняет сравнительно более высокую электрокаталитическую активность наночастиц Pt на модифицированных носителях в РВК [148, 151]. Сильное взаимодействие между Pt и пиридиновым N экспериментально и теоретически показано в [154], которое интерпретировано как способность кластера Pt4 деформировать поверхность, формируя стабилизированный “карман” с одним атомом N и двумя атомами C. Указанное взаимодействие вызывает сдвиг энергии связи пиридинового азота величиной 0.5 эВ и поддерживает положительный заряд Pt, выражаясь в росте доли Pt2+ на соответствующем спектре. Также авторы отмечают корреляцию между возросшей активностью катализаторов (в форме потенциала полуволны E1/2) и содержанием азота в пиридиновой форме. Аналогично, корреляция между концентрацией азота в пиридиновой форме и электрокаталитической активностью наночастиц Pt на модифицированном носителе отмечается в работе [147]. Результаты работы [155] показывают, что графитоподобный N в допированном носителе NC может способствовать нуклеации и дисперсии наночастиц в силу электрон-донорного характера орбитали pz, а пиридиновый N способствует их закреплению за счет образования связей Npx–Me. Делокализация переноса электронов приводит к снижению поляризации между носителем и наночастицами, подавляя окисление последних и поддерживая поверхность наночастиц в металлическом состоянии.
Результаты, представленные авторами [156], свидетельствуют о том, что использование углеродного материала, допированного атомами азота, позволяет повысить активность катализатора на основе Pt и углеродного ксерогеля, и этот эффект усиливается при увеличении концентрации азота в пиридиновой и пиррольной форме в составе ксерогеля. С другой стороны, согласно результатам модельных исследований [157], пять возможных конфигураций атомов N (пиридиновая, графитоподобная, пиррольная, аминная и N-оксид) в разной степени могут усилить взаимодействие Pt с УНТ, однако только графитоподобный N может достаточно сильно изменить спиновую плотность и плотность заряда Pt, а также уменьшить запрещенную зону между высшими заполненными и низшими незанятыми молекулярными орбиталями. Другими словами, графитоподобный N оказывает наиболее сильное влияние на повышение активности нанесенных на модифицированные УНТ наночастиц Pt. Между тем, на примере модельной реакции выделения водорода (из Н+) экспериментально показана прямая корреляция собственной активности наночастиц Pt с содержнием графитоподобного N [157].
Сольвотермический метод синтеза, предложенный авторами [158], позволяет получить электрокатализатор Pt/N–rGO, в котором наночастицы Pt со средним размером около 2.8 нм равномерно распределены по поверхности азотированного ВОГ. Полученный электрокатализатор продемонстрировал высокую активность и стабильность в РВК. Это обеспечивается как эффективной морфологией электрокатализатора, так и высокой активностью наночастиц благодаря преобладанию в структуре кристаллической решетки граней Pt (111) и влиянию внедренных атомов азота. Авторы заключают, что атомы азота служат “мостами” между углеродной матрицей носителя и наночастицами Pt (посредством связей Pt–N и C–N): увеличивается энергия связи наночастиц с носителем и происходит перераспределение заряда в пользу последних. В результате увеличивается стабильность и активность наночастиц Pt. При этом обнаруженные конфигурации атомов азота включают пиридиновый, пиррольный, графитоподобный азот, N-оксид и Pt‒N. Авторы полагают, что пиридиновый (24.7%) и пиррольный (34.7%) азот отвечают за низкое сопротивление носителя, поскольку их sp2-гибридизация не нарушает сопряжение связей ВОГ.
Одноступенчатый метод, представленный в работе [159], позволяет синтезировать наночастицы Pt на поверхности ВОГ, допированного атомами N. Метод основан на отжиге ацетилацетоната Pt и ОГ в атмосфере NH3 при температуре 500–700°С. Представленный метод синтеза обеспечивает такие преимущества, как: (1) исключает возможность загрязнения катализатора хлором, (2) обеспечивает оптимальный для РВК размер наночастиц Pt (2–3 нм) и (3) содержание 5 мас. % N в пиридиновой и пиррольной форме. Кроме того, предложенный одностадийный метод синтеза авторы характеризуют как достаточно быстрый, воспроизводимый и масштабируемый. Другим важным преимуществом является отсутствие хлорсодержащих прекурсоров (таких как, например, гексахлорплатиновая кислота, которая используется в общепринятых методиках восстановления наночастиц Pt), что позволяет исключить наличие остаточного хлора и возможное отравление активных центров катализатора. Активность полученных электрокатализаторов оказалась сравнима с активностью коммерческого электрокатализатора Pt/C как в кислой, так и в щелочной среде, а их стабильность осталась за рамками исследования.
Гибридная методика для приготовления допированного атомами азота графенового аэрогеля, предложенная авторами [160], включает в себя гидротермальную самосборку, лиофилизацию и термическую обработку. В результате удалось получить наночастицы Pt, распределенные по поверхности графенового аэрогеля, допированного азотом. Полученный катализатор характеризуется взаимосвязанной трехмерной пористой структурой, высоким содержанием азота (4.66 ат. %) и равномерным распределением наночастиц по размерам (со средним размером ~2 нм), высоким значением ЭАП – до 90.7 м2/г, активностью и циклической стабильностью в реакции электроокисления метанола (сохраняет 55.9% ЭАП после 1000 циклов в диапазоне потенциалов 0.6–1.2 В относительно стандартного водородного электрода (СВЭ)22) по сравнению с Pt/G (21.3% от ЭАП). Необходимо отметить, что в составе катализатора обнаружен пиридиновый, пиррольный и графитоподобный азот, а также N-оксид. В более поздней работе [161] предложен иной метод получения графенового аэрогеля с использованием металлоорганической каркасной структуры ZIF-8. Ее использование способствует снижению рестекинга графеновых нанолистов и более равномерному распределению наночастиц Pt. С помощью простого гидротермального метода авторами [162] синтезирован катализатор на основе наночастиц Pt, нанесенных на поверхность вспененного азотированного графена. По мнению авторов, трехмерная взаимосвязанная пористая структура вспененного носителя способствует равномерному распределению наночастиц Pt и иономера, а также транспорту реагентов к активным центрам РВК. Максимальная удельная мощность МЭБ ТЭ с ТПЭ (Nafion 117) на основе полученного катализатора оказалась вдвое выше (394 мВт/см2) по сравнению с МЭБ на основе коммерческого катализатора Pt/C.
В работе [163] в качестве носителя предложен эксфолиированный азотированный графен c углеродными наносферами, размещенными между его плоскостями. Полученный на основе такого носителя и Pt-катализатор продемонстрировал увеличение активности и стабильности в РВК, хотя исследований МЭБ ТЭ с ТПЭ на его основе не проводилось.
Авторы [164, 165] синтезировали многослойный электрокатализатор, в котором УНТ (или УНТ, допированные азотом) использовались в качестве носителя наночастиц Pt, которые в свою очередь стабилизировались путем нанесения поверх слоя поливинилпирролидона, который далее был преобразован (путем карбонизации в атмосфере азота) в углеродную пленку, допированную азотом (CN). Показано, что внешний допированный слой углерода обеспечивает высокую стабильность наночастиц Pt и поддержание высокой степени использования Pt на протяжении ускоренного стресс-тестирования, оказывая при этом незначительное влияние на активность электрокатализатора в РВК по сравнению с катализатором без CN–покрытия. МЭБ водород-кислородного ТЭ с ТПЭ на основе полученного многослойного композита в качестве катодного катализатора продемонстрировал более высокую максимальную удельную мощность по сравнению с МЭБ на основе коммерческого Pt/C (0.6–0.65 и 0.35 Вт/см2, соответственно), а нанесение второго CN-слоя несколько снизило это значение (на 0.05 Вт/см2), что вполне компенсируется возросшей стабильностью. С другой стороны, полученные значения невелики для МЭБ водород-кислородного ТЭ с ТПЭ, изготовленного в лабораторных условиях. Позднее с помощью CN-пленки, полученной методом карбонизации in situ полимеризованного полианилина, удалось стабилизировать наночастицы PtRu для реакции электроокисления метанола [166].
Близкий метод стабилизации наночастиц Pt предложен в работах [167, 168], где авторы приготовили наночастицы Pt размером около 4–5 нм, инкапсулированные в углерод, допированный азотом. Необходимо отметить, что впервые предложенная авторами методика приготовления такого электрокатализатора является одностадийной, что достигнуто за счет термической обработки Pt-анилинового комплекса, полученного, в свою очередь, путем ультразвуковой обработки смеси прекурсора Pt (H2PtCl6·6H2O), углеродной сажи и мономера анилина. Авторы полагают, что более высокая активность полученного электрокатализатора в РВК (измеренная в жидком электролите) связана с дополнительными активными центрами (пиридиновые атомы азота, внедренные в sp2-струкутру углеродной оболочки), хотя характеристики водород-кислородного ТЭ на его основе заметно уступают коммерческому катализатору из-за возросшей толщины катодного АС. Максимальной удельной мощности МЭБ ТЭ с ТПЭ (~0.95 Вт/см2) удалось достичь снизив загрузку катализатора и, соответственно, содержание Pt с 0.2 до 0.04 мг/см2 [167]. Главным преимуществом полученных катализаторов является их более высокий ресурс, определенный с помощью ускоренного стрес-тестирования активного в составе МЭБ ТЭ с ТПЭ (5000 циклов в диапазоне потенциалов 0.6–1.2 В отн. СВЭ в атмосфере азота).
Применение УНМ, допированных азотом, перспективно и в качестве носителя анодного катализатора реакции окисления водорода. Согласно результатам, приведенным в работе [169], допирование графена азотом снижает его стабильность, однако, повышает толерантность катализатора на его основе к СО. Увеличение толерантности к СО авторы связывают с образованием дополнительных дефектов и снижением энергии адсорбции СО. При этом атомы азота распределены следующим образом: пиридиновый – 31%, пиррольный – 35.5% и графитоподобный – 33.5, и влияние конкретных форм азота не рассматривалось [169]. В работе [170] удалось получить углеродные нанолисты с высоким содержанием азота (до 12 ат. %) и иммобилизованными на их поверхности атомами Pt. Полученный электрокатализатор (Pt/CNS) продемонстрировал высокую активность в реакциях окисления и выделения водорода. Активность Pt/CNS в 7 раз превосходила активность Pt/C (20 мас. %) в реакции окисления водорода (в жидком электролите на вращающемся дисковом электроде). Однако, для достижения характеристики МЭБ ТЭ, эквивалентной МЭБ с Pt/C, пришлось повысить загрузку Pt на аноде (в случае Pt/CNS) до 0.025 мг Pt/см2), что составило половину от таковой на аноде в МЭБ ТЭ с ТПЭ на основе Pt/C (20 мас. %) (табл. 2).
За последнее время были достигнуты некоторые успехи в области разработки не содержащих металлических наночастиц катодных электрокатализаторов в ТЭ с ТПЭ. На примере катализаторов на основе высокоориентированного пиролитического графита авторы [171] предлагают следующий механизм протекания РВК (рис. 5): в начале молекула кислорода адсорбируется на атом углерода, соседний с атомом азота в пиридиновой форме (основный центр Льюиса), с последующим протонированием. Далее реакция может идти по 4- или 2-электронному пути. В первом случае два протона присоединяются к двум атомам кислорода, что приводит к разрыву связи О−ОН и образованию адсорбированной частицы ОН и молекулы Н2O (рис. 5г). Дополнительный протон реагирует с адсорбированной частицей ОН с образованием второй молекулы Н2O (рис. 5е). Во втором случае в результате реакции протона и ООН образуется H2O2, которая может вновь адсорбироваться и восстановиться с образованием двух молекул Н2O. В любом случае атомы углерода рядом с азотом в пиридиновой форме выступают в качестве активных центров, на которых адсорбируются молекулы кислорода на первой стадии РВК [171].
Влияние конфигурации атомов азота, внедренного в УНМ, на их активность в РВК было изучено в работе [172]. Указанные УНМ получали методом высокотемпературного синтеза. Образцы УНМ показали высокую активность в РВК, при этом их активность не коррелирует с концентрацией атомов N в графитоподобной форме, но хорошо коррелирует с концентрацией атомов N в пиридиновой форме. Аналогичный тренд также обнаружен и в отношении активности полученных УНМ в реакции выделения кислорода. В более поздней работе [173] авторам удалось получить УНМ методом высокотемпературного отжига с использованием MgO, допированного Fe. Показано, что их активность в РВК можно существенно повысить с помощью промывки HCl, что связывается с удалением неактивных металлических частиц и непроводящего оксидного слоя, блокирующего активные центры РВК. При этом необходимы дальнейшие исследования, которые позволили бы прояснить роль собственно атомов азота: являются ли они непосредственно активными центрами РВК или же придают соседним атомам углерода свойства оснований Льюиса и способность выступать в роли активных центров? Например, в работе [174] продемонстрирован подход, включающий расчеты по ТФП и постреакционное исследование РФЭС-спектра катализаторов после потенциостатической поляризации, которая позволяет пронаблюдать изменение азотных функциональных групп в катализаторе вида CNx в результате протекания РВК и проанализировать роль различных конфигураций азота в механизме РВК [174]. Авторы [175] синтезировали композит, состоящий из графеновых нанолент и УНТ, допированных азотом (Г-УНТ-N), которые получили в несколько стадий: сначала методом Хаммерса был получен ОГ, который затем в смеси с окисленными УНТ лиофильно высушивался, и смесь отжигалась в атмосфере NH3 при 800°С в течение 3 ч. Полученный композит Г-УНТ-N продемонстрировал высокую активность в РВК по сравнению с УНТ-N и ВОГ, допированным азотом, в кислой среде благодаря своей уникальной пенообразной трехмерной структуре, которая не нарушается при модельных исследованиях на дисковом электроде. Удельный ток в МЭБ водородно-кислородного ТЭ с ТПЭ составил 30 А/г при 0.8 В, а максимальная удельная мощность – 300 Вт/г. Необходимо отметить, что при приготовлении АС добавление углеродной сажи (Ketjenblack, 2 мг/см2) вызвало увеличение плотности тока ТЭ на ~85% в области низких значений напряжения (<0.4 В), хотя углеродная сажа практически не обладает электрокаталитической активностью в РВК. Это можно объяснить тем, что введение сажи приводит к образованию сети пор и соответствующему ускорение диффузии O2, так как пористость АС на основе Г-УНТ-N (без введения сажи) значительно снижается при формировании соответствующего МЭБ путем прессования [175].
Отдельно необходимо отметить разработки, посвященные катализаторам РВК на основе неблагородных металлов и допированных УНМ, таких как M/N/C (где М = Fe, Co, Mn и др.). Подробному рассмотрению катализаторов такого типа посвящен ряд обзорных работ [176–178]. Сравнительно высокая активность и стабильность указанных катализаторов обусловлена особенностями координации атома металла (Fe, Co и др.) и четырех окружающих атомов N, которые образуют активный центр РВК. В целом к настоящему времени достигнут существенный прогресс в разработке активных и достаточно стабильных катализаторов этого типа: максимальная удельная мощность МЭБ водород-кислородного ТЭ с ТПЭ достигает 1.18 Вт/см2 при 0.47 В (мембрана Nafion 211, 80°C, относительная влажность газов 100%, избыточное давление газов 2.5 бар) [179], однако для успешного замещения катализаторов на основе Pt в МЭБ ТЭ с ТПЭ необходимы дальнейшие исследования, направленные на оптимизацию структуры и морфологии катодов на основе M/N/C. Катоды на основе M/N/C и других неплатиновых катализаторов оказываются более толстыми, что приводит к дополнительным транспортным ограничениям (особенно при использовании воздуха в качестве окислителя), неэффективной трехфазной границе и др. [177].
В работе [180] предложена методика получения катализатора Fe/N/C, используя одновременно два прекурсора азота – полианилин и фенантролин. Максимальная удельная мощность водород-кислородного и водород-воздушного ТЭ с ТПЭ на основе мембраны Nafion 211 достигла 1.06 и 0.38 Вт/см2, соответственно, что существенно превосходит характеристики МЭБ ТЭ на основе Fe/N/C, полученного из полианилина или фенантролина в отдельности. Это объясняется уникальной структурой полученного катализатора, которая сочетает высокую удельную поверхность и долю мезо- и макропор. Фенантролин выступает в роли порообразователя, который “расширяет” оболочку полианилина при разложении, структура которого, в свою очередь, трансформируется в графеноподобную. В работе [181] предлагается использовать цепочки из наночастиц SiO2, которые позволяют регулировать мезопористую структуру АС и повысить гидрофобность его поверхности – улучшить транспортные свойства АС с высокой загрузкой неплатинового катализатора Fe/N/C. Кроме того, SiO2–Fe/N/C характеризуется большей долей атомов N в пиридиновой форме и большим числом дефектов (исследование методом рамановской спектроскопии показали существенно более высокие значения ID/IG катализатора SiO2–Fe/N/C (1.07) по сравнению с Fe/N/C (0.87)), которые компенсируют снижение удельной активности катализатора, а также существенным снижением транспортных потерь. В частности, плотность тока МЭБ водород-воздушного ТЭ с ТПЭ (на катоде: 3.0 мг/см2 Fe/N/C + 0.6 мг/см2 SiO2) при напряжении 0.4 В выросла с 620 до ~780 мА/см2 (данные приведены за вычетом омических потерь). В качестве носителя катализатора предложен ВОГ, полученный из биомассы, и рассмотрено влияние различных прекурсоров азота на этапе пиролиза на активность катализатора Fe–N–RGO в РВК в кислом электролите [182]. Показано, что двухстадийный пиролиз позволяет удалить летучие компоненты и сформировать стабильные активные центры: графитоподобный N и Fe–Nx.
С другой стороны, графеновые нанопластинки, допированные Fe и N, также могут выступать носителем для наночастиц Pt. Согласно результатам работы [183], такой подход позволяет добиться увеличения активности и стабильности электрокатализатора, а также снижения загрузки Pt на катоде МЭБ ТЭ с ТПЭ. В частности, при снижении загрузки Pt вдвое, значение удельной мощности МЭБ ТЭ с ТПЭ составило ~70% от значения для МЭБ на основе коммерческого катализатора Pt/C (~0.7 Вт/см2, в расчете на Pt – 3.6 Вт/мг Pt).
В [184] впервые рассмотрены продолжительные (500 ч) ресурсные исследования ТЭ с прямым окислением метанола, в котором используется коммерческий катализатор Fe/N/C (фирмы Pajarito Powder LLC). Использование неплатинового катализатора позволило повысить концентрацию метанола до 5 М, несмотря на его высокий кроссовер. В ходе хроноамперометрического теста после 500 ч непрерывной работы при напряжении 0.3 В плотность тока ТЭ упала на 80% до 25 мА/см2. Помимо уже описанных в литературе механизмов деградации катализатора РВК, таких как “вымывание” металла из Fe/N/C, затопление микропор и окисление углерода, авторы отмечают растворение Ru (из анодного катализатора) и его последующую миграцию и осаждение на катоде, которая ведет к снижению проводимости ТПЭ и снижению активности катодного катализатора.
3.1.3. Графеновые материалы, модифицированные атомами фосфора. Фосфор, обладая более низкой электроотрицательностью по сравнению с углеродом (табл. 1), способен успешно внедряться в структуру графена с образованием связей C‒P, что приводит к возникновению структурных дефектов, благоприятных для равномерного осаждения наночастиц Pt [93, 185, 186]. Действительно, согласно результатам работы [90], внедренные атомы P обеспечивают больше центров для закрепления наночастиц Pt и способствуют более равномерному распределению наночастиц и снижению их среднего размера с 3.12 до 2.68 нм, что подтверждается результатами рентгеноструктурного анализа. Полученный полиольным методом катализатор Pt/PG проявляет более высокую активность в РОМ в кислой среде. В частности, пиковая плотность тока окисления метанола на циклической вольтамперограмме (измеренной в 0.5 М Н2SO4 + 0.5 M СН3OH) составила 687 А/г Pt, что в 1.54 и 2.42 раза выше по сравнению с Pt/G и коммерческим катализатором Pt/C соответственно. Кроме того, Pt/PG проявил более высокую стабильность в ускоренном стресс-тестировании и высокую устойчивость к отравлению СО. Такой эффект от допирования атомами Р связан с образованием большего числа кислородсодержащих частиц, способствующих более полному и быстрому окислению метанола, а также снижению величины энергии связи Pt с отравляющими ее частицами (например, СО) [90].
3.1.4. Графеновые материалы, модифицированные атомами серы. Как упоминалось выше, инкорпорирование атомов S в УНМ, благодаря небольшой разнице в электроотрицательности элементов, не вызывает существенного перераспределения заряда, а рост каталитической активности, по-видимому, связан с перераспределением спиновой плотности в результате внедрения атомов серы. Кроме того, Pt способна прочно связываться с S, что обычно выражается в отравлении металлических активных центров [187]. С другой стороны, в случае инкорпорирования атомов S в структуру носителя это свойство можно использовать для усиления взаимодействия между активными наночастицами Pt и носителем [46].
Авторам работы [188] удалось получить допированный серой графен методом пиролиза и исследовать его в качестве носителя для наночастиц Pt (Pt/SG) в РВК. Максимум на спектре Pt4f образца Pt/SG характеризуется положительным сдвигом величиной 0.23 эВ по сравнению с Pt/G. Это указывает на более сильное взаимодействие между Pt и носителем и облегчение переноса электронов от носителя к активным центрам, что в конечном счете приводит к увеличению активности в РВК. Pt/SG обладает более высокой удельной активностью в РВК (139 А/г Pt при 0.9 В по сравнению с коммерческими Pt/C (121 А/г Pt) и Pt/G (101 А/г Pt) при близких значениях среднего размера наночастиц 2.1–2.25 нм (по результатам анализа изображений, полученных методом просвечивающей электронной микроскопии). Ускоренное стресс-тестирование Pt/SG продемонстрировало также и его высокую электрохимическую стабильность: остаточное значение ЭАП Pt/SG составило 87%, что существенно выше значений Pt/C (48%) и Pt/G (54%). После стресс-тестирования наночастицы Pt предпочтительно переосаждались в областях носителя, богатых серой, а средний размер частиц вырос незначительно (до 2.3, 3.8 и 5.25 нм у Pt/SG, Pt/G и Pt/C, соответственно). Такие результаты авторы связывают с сильным взаимодействием между допированным носителем и Pt, что подтверждается также и результатами моделирования. Подобный характер влияния допирования носителя атомами серы на активность и стабильность катализатора в РВК показан и в работе [189] для наностержней Pt на допированном серой ВОГ. Позднее авторы [190] показали, что катализатор PtNW/SG-2 с содержанием серы 1.40 ат. % продемонстрировал лучшие кинетические характеристики – высокую плотность тока обмена и низкую энергию активации РВК. По мнению авторов, носитель с указанным оптимальным содержанием серы способствует формированию Pt с оптимальной структурой и морфологией, что выражается в наибольшей величине ЭАП, активности и стабильности катализатора PtNW/SG-2. При увеличении содержания серы количество графеновых слоев увеличивается, соотношение sp2/sp3-гибридизированного углерода (степень графитизации носителя) уменьшается, а также снижается электропроводность графеновой матрицы и увеличивается ширина запрещенной зоны, что хорошо согласуется с результатами моделирования по ТФП.
Перспективность графена, допированного графитоподобной S, показана в рамках моделирования кинетики РВК на его поверхности [191]. Модельный катализатор представлял собой суперячейку графена 4 × 4 с одним атомом C, замещенным атомом S (SGV), и оказался устойчивым благодаря сильному взаимодействию между серой и дефектным графеном. Молекула O2 предпочтительно образует адсорбированные частицы OOH* совместно с адсорбированным H*, а активным центром является сам допант. Далее имеют место два возможных пути для РВК в целом: прямая диссоциация OOH* и гидрирование OOH* (рис. 6). Реакционные барьеры для лимитирующих стадий обоих предложенных механизмов составляют 0.75 и 0.62 эВ соответственно. Согласно моделированию свободной энергии Гиббса, механизм РВК через гидрирование ООН является предпочтительным, а диссоциация OOH исключается.
Рис. 6.
Предполагаемые механизмы РВК для допированного серой графена. Предпочтительный путь обозначен красными линиями [191].

В работе [113] ВОГ, допированный серой (S–RGO), был приготовлен с помощью сольвотермического метода, в котором диметилсульфоксид выступал не только в роли растворителя, но и в качестве источника S. Показано, что синтезированный S–RGO может быть использован в качестве эффективного электрокатализатора РВК, не содержащего металлических наночастиц. В ТЭ с прямым окислением метанола S–RGO продемонстрировал высокую устойчивость к отравлению метанолом и продуктами его анодного окисления, которые проникают в катодную камеру через мембрану благодаря кроссовер-эффекту, а также более высокую стабильность, по сравнению с коммерческим электрокатализатором Pt/C. Похожий материал S–RGO был приготовлен методом тионирования в работе [114]. Данный катализатор представляет собой однослойные графеновые листы с атомами S, инкорпорированными в углеродную структуру графена. Согласно результатам РФЭС, подавляющая доля серы находится в форме тиофена. При испытаниях МЭБ ТЭ с ТПЭ с использованием S–RGO в качестве катодного АС наблюдается низкий начальный потенциал РВК (0.3 В), и предельного значения плотности тока (ilim) достигнуть не удалось, что указывает на невысокую эффективность работы катализатора. Максимальная удельная мощность составила лишь немногим более 1 мВт/см2. В работе [107] ВОГ, допированный атомами S (SG), получали путем высокотемпературной обработки ОГ и фенилдисульфида в трубчатой печи в потоке Ar при 1000°С. Осаждение наночастиц Pt на носитель осуществлялось полиольным методом, а биметаллический катализатор Pt–Ni/SG готовили при помощи термической обработки Pt/SG с нитратом никеля и далее подвергали обработке в 0.5 М H2SO4 и повторной термической обработке (Pt–Ni/SG–PHT). Полученный катализатор Pt–Ni/SG–PHT продемонстрировал высокие значения остаточных ЭАП и удельной массовой активности после ускоренного стресс-тестирования (1500 циклов в диапазоне потенциалов 0.05–1.3 В). Необходимо отметить стойкость биметаллических наночастиц к агломерации и растворению благодаря сильному взаимодействию с носителем.
3.1.5. Графеновые материалы, модифицированные атомами фтора. Фторирование углеродных носителей рассматривается в качестве одного из способов повышения их стабильности при использовании в ТЭ с ТПЭ благодаря высокой устойчивости связей C–F к электроокислению [192]. Показано, что фторирование носителя имеет смысл проводить до осаждения наночастиц Pt, так как в противном случае фторирование электрокатализатора с уже нанесенными наночастицами ведет к их деактивации [193]. Фторирование углеродного носителя позволяет связать атомы фтора с атомами углерода с “оборванными” связями, которые наиболее склонны к окислению при работе ТЭ [194].
В работе [195] получение фторированного ВОГ проводилось путем обработки графита в среде IF7 при 25°C в атмосфере аргона с последующим термическим восстановлением и эксфолиацией. Электрокатализатор Pt/ВОГ–F c содержанием Pt 40 мас. % был синтезирован полиольным методом. Необходимо отметить, что согласно изображениям, полученным методом просвечивающей электронной микроскопии, несмотря на невысокий размер наночастиц Pt, наблюдается высокая степень их агломерации. ЭАП Pt/ВОГ–F оказалась в 2–2.5 раза ниже по сравнению с Pt/ВОГ. Это может объясняться сильными акцепторными свойствами фтора и низкой доступностью поверхности носителя для сорбции прекурсора.
Показано, что фторирование оказало положительное влияние на стабильность структурно-неупорядоченных углеродных носителей (например, углеродных саж), которое можно объяснить взаимодействием атомов углерода с прекурсором фтора и связыванием его вакантных “оборванных” связей с фтором, что привело к существенному повышению стойкости носителей к электроокислению на катоде ТЭ. В случае упорядоченных носителей (таких, как графит и т.п.) фторирование привело к обратному эффекту – созданию структурных дефектов (разрыву C–C-связей) и снижению коррозионной стойкости [193]. Дальнейшие исследования стабильности катализаторов на основе фторированных носителей в составе МЭБ ТЭ с ТПЭ не показали заметного увеличения стабильности катализаторов как по сравнению с нефторированным носителем, так и по сравнению с коммерческим Pt/C при использовании различных протоколов УСТ (“старт/стоп”, при котором основным механизмом деградации является разрушение углеродного носителя или циклическое изменение напряжения, когда основным механизмом является оствальдовское созревание наночастиц Pt). Важно отметить, что предполагаемое увеличение стойкости носителя (отмеченное в работе [193]) не подтвердилось в рамках соответствующего протокола УСТ МЭБ ТЭ с ТПЭ с катализатором на основе фторированного носителя, что говорит об ограниченной предсказательной силе исследований стабильности катализаторов в жидком электролите [196].
С другой стороны, F является наиболее электроотрицательным элементом (табл. 1), поэтому допирование графена фтором обеспечивает наиболее сильную электронную поляризацию поверхности и, как следствие, высокую электрохимическую активность и стабильность [132], что является полезным при разработке электрокатализаторов РВК, не содержащих металлических наночастиц.
3.1.6. Выводы по разделу. Свойства и характеристики электрокатализаторов РВК и других электрохимичеких реакций в существенной степени связаны с электроотрицательностью допантов и изменением электронной структуры производных графена (и других УНМ) в результате допирования. Общим для большинства основных допантов (азота, бора, серы и фосфора) является то, что в результате допирования увеличивается дефектность материала, которая при дальнейшем осаждении металлических наночастиц Pt обеспечивает большее число центров нуклеации наночастиц, снижение их размера и степени агломерации. Перераспределение электронной плотности между допантами и соседними атомами углерода обеспечивает формирование активных центров, на которых, в зависимости от направления переноса электронов, могут протекать электрохимические реакции либо адсорбироваться кислородосодержащие частицы. Последнее ведет к повышению толерантности соседних наночастиц Pt к отравлению СО и продуктами окисления спиртов, что безусловно, является полезным для соответствующего типа топливных элементов и катализаторов окисления водорода. В случае элементов с более высокой электроотрицательностью (азот, сера) снижение размера наночастиц Pt сопровождается переносом электронной плотности от носителя к наночастицам, повышая их активность и, что более важно, стабильность в РВК. В отношении различных форм атомов азота можно отметить, что пиррольный и пиридиновый азот могут выступать в качестве центров нуклеации наночастиц.
В ряде работ отмечается возможное повышение активности катализаторов в РВК за счет дополнительных активных центров, в роли которых могут выступать сами допанты (пиридиновый или графитоподобный азот, тиофеновая сера и др.) либо соседние атомы углерода (соседние с внедренными атомами азота или серы). Однако, количественный вклад возможных дополнительных активных центров, образующихся в результате допирования, особенно при работе катализатора в составе МЭБ, требует дальнейшего прояснения.
Исследования, посвященные допированию УНМ атомами F, достаточно редки, а их выводы, особенно в отношении повышения стабильности углеродного носителя – противоречивы. Тем не менее, допирование УНМ фтором также приводит к формированию активных центров, что подробнее рассмотрено в следующем разделе.
3.2. Графеновые материалы, модифицированные двумя элементами
Авторами [197] предложена методика синтеза нанолистов графена с двойным допированием атомами B и N, которая включает одностадийный пиролиз комплекса боран–трет-бутиламина, пропитанного ионами Co. Концентрация атомов B и N составила 7.18 и 7.72 ат. % соответственно. Согласно РФЭС, атомы бора находились в конфигурации BN, BC3 и частично окисленном состоянии (BN3, BCO2 и BC2O). Массовая активность катализатора на основе наночастиц Pt и допированного носителя в РВК более чем в 2 раза превысила таковую у Pt/C. Высокая стабильность допированного носителя и катализатора на его основе по сравнению с Pt/C подтверждена методом УСТ. Авторы отмечают, что атомы бора (акцепторы электронов) притягивают электроны от соседних атомов углерода, что создает общий положительный заряд и способствует адсорбции ${\text{PtCl}}_{6}^{{2 - }},$ а атомы азота (доноры электронов) ускоряют его восстановление. Частичный перенос электронов от допированного носителя (атомы азота – доноры электронов) на незаполненные орбитали Pt приводит к более высокой электронной плотности на поверхности Pt и снижению энергии адсорбции O2. Кроме того, сильное взаимодействие между носителем и Pt сдерживает агрегацию и коалесценцию наночастиц.
Другим перспективным направлением для использования производных графена в качестве носителей электрокатализаторов является анодная реакция в ТЭ с прямым окислением метанола. В работе [57] допированный атомами B и N графен был получен путем двухстадийного высокотемпературного твердофазного отжига (в качестве прекурсоров использовались ОГ, борная кислота и меланин). Атомы В внедряются в допированный азотом графен в конфигурации B–N–C и B–C–O. Средний размер наночастиц Pt у катализатора, полученного на основе модифицированного носителя, составил около 2.3 нм, а сами наночастицы характеризуются более равномерным распределением по поверхности носителя по сравнению с распределением на поверхности сажи. ЭАП катализатора составила 70.6 м2/г, что выше, чем у образца на основе монодопированного азотом графена Pt/NG (61.2 м2/г) и стандартного катализатора PtRu/C (58.5 м2/г). Использование допированного атомами B и N носителя приводит к синергетическому эффекту: атомы B обеспечивают снижение энергии d-орбитали Pt и ускорение РОМ, а атомы N – обеспечивают адсорбцию кислородсодержащих частиц, необходимых для доокисления промежуточных продуктов по бифункциональному механизму. В работе [198] гидротермальным методом удалось получить катализатор реакции электроокисления метанола на основе мелких наночастиц Pt на поверхности графенового аэрогеля, который характеризуется эффективной трехмерной структурой (включающей взаимосвязанные макро- и мезопоры), высокой удельной поверхностью (~360 м2/г), равномерным распределением допантов B и N и наночастиц Pt, а также высокой электропроводностью. Содержание атомов B (B–C3, B–N и B–C–O) и N (С–N=С, C–N–B, С–N–C и N–C3) составило 2.0 и 3.3 ат. % соответственно. Влияние атомов-допантов и вышеуказанные свойства носителя позволили достичь высокой активности катализатора в РОМ (пиковое значение плотности тока прямой волны циклической вольтамперограммы в 1 М растворе CH3OH оказалось на порядок выше по сравнению с Pt/C), а также стойкости к отравлению. Авторы [199] также отмечают, что взаимодействие Pt и B ответственно за рост активности катализатора в РОМ, а атомы азота – рост стойкости наночастиц Pt к отравлению СО.
УНМ, допированный одновременно атомами B и N, также и сам по себе может выступать в роли электрокатализатора РВК. В частности, в работе [200] рассмотрены неметаллические катализаторы на основе допированных углеродных нанооболочек (полых внутри наноструктур в форме цилиндра или шара). Показано, что допирование позволило повысить активность углеродных нанооболочек в 8–10 раз, хотя селективность РВК осталась невысокой (среднее число переносимых электронов составило 2.9). Допирование приводит к ускорению стадии переноса первого электрона, а также ускоряет восстановление H2O2.
Авторам [201] удалось допировать ВОГ атомами N и S с использованием методов клик-химии. Носитель для наночастиц Pt представляет собой смесь из допированного ВОГ и двустенных нанотрубок (выполняющих функции спейсера и проводящей матрицы). Необходимо отметить, что предложенный метод синтеза в отличие от других не включает в себя стадий высокотемпературной обработки. Полученный катализатор продемонстрировал высокую активность в реакции окисления этанола при низких потенциалах (соответствующих напряжению ТЭ с прямым окислением спиртов) и стойкость к отравлению СО, хотя авторы не уделили внимания ролям каждого из допантов.
В работе [202] показано, что в результате допирования атомами S неактивные атомы углерода, расположенные по соседству с графитоподобным азотом, становятся активными центрами РВК (увеличивается их спиновая плотность), что подтверждается модельными расчетами по ТФП и экспериментальными результатами. В работе [203] в качестве катализатора, не содержащего металлических наночастиц, предложен пористый углеродный лист, допированный серой и азотом, который получен пиролизом полимерных материалов и тиомочевины при 1000°С в атмосфере N2 с последующей обработкой в мельнице. Полученный катализатор (N,S1,S2-CM1000-b) продемонстрировал высокую активность в РВК в 0.1 M растворе HClO4, что выражается в высоком значении потенциала полуволны (E1/2) – 0.75 В. Азот главным образом присутствовал в пиридиновой, графитоподобной форме и в форме N-оксида, а около 2/3 атомов S – в форме C–S–C (тиофен), которая также может служить активным центром РВК [204]. Нужно отметить, что обработка в мельнице способствует трансформации изначально сферической структуры материала после синтеза в листовую с увеличением числа активных центров тиофена. С другой стороны, авторы [205] отмечают, что высокая активность в РВК спирально раскрытых МУНТ, допированных одновременно атомами N и S, отчасти связана с высокой концентрацией азота в пиридиновой форме (~6 ат. % в лучшем образце). Атомы S, напротив, присутствуют в концентрации не более 1 ат. % в окисленной или элементной форме и способствуют формированию именно пиридиновых функциональных групп преимущественно на краях поликристаллической углеродной структуры, которая также вносит существенный вклад в активность материала. В работе [206] показано, что за высокую активность допированного углеродного 3D аэрогеля отвечают активные центры N–S–C, формирующиеся за счет краевых тиофеновых S-групп, графитоподобного N и пентагональных дефектов. Полученный материал отличается высокой активностью и стабильностью в РВК как в кислом, так и в щелочном электролите. Среднее число перенесенных электронов составило около 4, а выход Н2О2 не превысил 3%.
Как отмечалось выше, одной из активно разрабатываемых альтернатив традиционным катализаторам РВК на основе Pt являются композиты на основе Fe и допированных углеродных носителей [207]. Активность таких катализаторов на основе Fe определяется содержанием азота в пиридиновой и графитоподобной форме, а также наличием активных центров Fe–N4 [208]. В [108] получен катализатор РВК на основе графена, допированного азотом и серой, и инкапсулированных наночастиц железа (Fe–NSG). Максимальная удельная мощность ТЭ с ТПЭ с Fe–NSG в качестве катодного катализатора при 80°С составила 225 мВт/см2. Показано, что оптимальное содержание атомов S способствует подавлению процесса образования карбида железа и формированию центров Fe–N4, активных в РВК. По мнению авторов [209], внедрение атомов S в форме тиофена приводит к снижению локализации электронов вокруг центров Fe и, соответственно, усиливают их взаимодействие с кислородсодержащими частицами, и способствуют более быстрому протеканию РВК по 4-электронному механизму. Авторы [210] путем пиролиза поли(3,4-этилендиокситиофен)а в атмосфере Ar при 800–1000°С (2 стадии пиролиза, разделенных отмывкой в растворе 0.5 M H2SO4) получили свернутый графеновый материал с активными центрами C–S и Fe–S, который характеризуется высокой активностью в РВК как в кислой, так и в щелочной среде. Удельная мощность водородно-кислородного ТЭ с ТПЭ на основе полученного катодного катализатора достигает 345 мВт/см2 при 60°С. Позднее авторам удалось путем пиролиза in situ-сформированного поли(3,4-этилендиокситиофен)а в присутствии УНТ и меламина в аналогичных условиях получить “листовой” активный материал, характеризующийся наличием большого числа различных активных центров: Fe–S, Fe–N, Fe–Nx, графитоподобного азота, тиофена и др., которые ответственны за высокую активность катализатора в РВК. Роль УНТ заключается в предотвращении агрегации нанолистов, поскольку нанотрубки выступают в роли спейсеров между нанолистами и обеспечивают высокую удельную поверхность материала (до 1645 м2/г). При этом максимальная мощность МЭБ ТЭ с ТПЭ с катодным АС на основе полученного катализатора PMCNT-900 составила 500 мВт/см2 при плотности тока ок. 1.6 А/см2. Также необходимо отметить, что механизм протекания РВК на PMCNT-900 и Pt/C практически одинаков, о чем свидетельствуют близкие значения тафелевского наклона – 74 и 76 мВ/дек., соответственно, и невысокая доля выделяющегося Н2О2 [211].
В работе [120] мезопористый углерод (МУ), допированный атомами N и S, был получен методом пиролиза различных прекурсоров, в частности таких, как 1,10-фенантролин (N–MC-1), карбазол (N–MC-2), фенотиазин (N,S–MC-1), дибензотиофен (S–MC-1), индигокармин (N,S–MC-2) и фенантрен (MC). Полученные катализаторы представляют собой наночастицы круглой формы с диаметром пор 3.6–4.1 нм, удельной площадью поверхности (определенной по методу Брунауэра, Эммета и Теллера) от 409 до 1103 м2/г. Содержание N и S в них варьировалось в диапазоне 3–8 и 0.6–14 мас. % соответственно. Исследование влияния температуры пиролиза на физико-химические свойства полученных катализаторов показали, что с ростом температуры пиролиза в их составе обнаруживаются в основном наиболее термодинамически стабильные пиридиновая и графитоподобная формы N и тиофеновая форма S. В кислой среде N–MC проявили наиболее высокую активность в РВК (следует отметить, что N–MC-1 и N–MC-2 содержат в своем составе 0.6–1.6 мас. % S, а увеличение концентрации S (до 4–13.8 мас. % в случае N,S–MC и S–MC) приводило к заметному снижению активности катализатора в РВК (вплоть до наименьшей в случае S–MC). Авторы предполагают, что высокая концентрация атомов серы приводит к плохой смачиваемости электрода, снижению площади поверхности тройного контакта (поверхность соприкосновения между активными центрами, ионным и электронным проводниками в активном слое, “triple phase boundary” [212]) и сильному замедлению транспорта протонов. Также необходимо отметить, что РВК на полученных катализаторах предпочтительно протекает по 2-электронному механизму, когда основным продуктом является Н2О2.
Более поздняя работа авторов [121] посвящена катализатору на основе наночастиц Pt, осажденных на допированный МУ (N,S–MC), который был получен с использованием фенотиазина в качестве прекурсора серы. Благодаря наличию микро- и мезопор поверхность допированных носителей составила 855–1183 м2/г. Наночастицы Pt наносили путем твердофазного восстановления ацетилацетоната Pt в потоке N2/H2. Величина ЭАП катализаторов Pt/N,S–MC, Pt/N–MC и Pt/S–MC составила 28.7, 69.1 и 64.1 м2/г Pt, соответственно, что уступает коммерческому катализатору фирмы TKK (79.83 м2/г Pt). Такое различие авторы объясняют несколькими факторами, в числе которых низкая проводимость допированных носителей (около 300 мСм/м, что почти на порядок уступает проводимости углеродной сажи, которая составляет 3970 мСм/м), более высокий размер наночастиц и их сильная агломерация, а также предполагаемая потеря части частиц в микропорах. При этом массовая активность образца Pt/N,S–MC в РВК составила 24.3 А/г Pt, что существенно ниже по сравнению с Pt/S–MC (77.4 А/г Pt), Pt/C (76.4 А/г Pt) и Pt/N–MC (59.4 А/г Pt). Необходимо отметить, что с ростом содержания серы уменьшается размер наночастиц Pt и растет активность катализатора в РВК. С другой стороны, тестирование наиболее активного образца, допированного атомами S, в составе МЭБ ТЭ продемонстрировало, что выигрыш в активности оказался нивелирован возросшими омическими и транспортными потерями. Применение ТФП позволило проанализировать как атомы N и S влияют на зарождение и рост наночастиц Pt на углеродной матрице (суперячейка графена 4 × 4). Во всех случаях, когда в рамках моделирования в суперячейке графена размещается единичный дефект (единичное внедрение в структуру графена атомов азота или серы – графитоподобный, пиридиновый, пиррольный азот или тиофен) энергия взаимодействия Pt и носителя росла в следующем порядке: пиррольный N > > графитоподобный N > S-тиофен > пиридиновый N > графен. Предсказано более слабое взаимодействие и меньшая стабилизация зародыша Pt на поверхности, допированной одновременно пиррольным N- и S-тиофеном, которое хорошо согласуется с почти двукратным ростом среднего размера наночастиц Pt в Pt/N,S–MC – с 1.8 до 3.5 нм по сравнению с Pt/S–MC. Энергия взаимодействия Pt с носителем и ее стабилизация снижаются при сближении двух дефектов (N и S). Кроме того, атомы S являются более предпочтительными центрами закрепления Pt, что связано с их электрон-донорной природой и переносом электронов на атомы Pt.
В работе [60] в одностадийном и достаточно экологичном процессе удалось получить пористый углерод, допированный атомами N и S (около 7 и 1.7 ат. %, соответственно), который отличается высокой удельной поверхностью – 1424 м2/г и продемонстрировал высокие удельные характеристики при исследовании в жидком электролите. Попытки использовать полученный допированный материал в качестве катализатора непосредственно в МЭБ ТЭ оказались неудачными (максимальная удельная мощность такого МЭБ не превысила 20 мВт/см2 при 60°С) в силу высоких транспортных ограничений и невысокой степени использования активных центров (в структуре полученного материала преобладают микро- и мезопоры размером 0.6–2 нм). Однако он положительно проявил себя в качестве носителя наночастиц Pt. Максимальная удельная мощность МЭБ водород-кислородного ТЭ с ТПЭ на основе полученного катализатора составила в тех же условиях 518 мВт/см2, что на 20% выше по сравнению с МЭБ на основе коммерческого Pt/C при невысоком содержании Pt – всего 0.2 мг Pt/см2 на катоде (0.3 мг Pt/см2 в МЭБ в целом). Структурные характеристики коммерческого эталонного катализатора (как и его марку) для анализа их вклада в различие характеристик авторы не привели.
В [93] авторы показали, что дополнительное допирование графена атомами S способствует увеличению концентрации атомов Р, внедренных в структуру графена, с 1.9 до 4.6 ат. %, а результаты исследований методом РФЭС указывают на наличие связей C–P, т.е. успешное внедрение атомов P в структуру носителя. Такой подход способствует более равномерному распределению наночастиц Pt, усилению их взаимодействия с носителем и увеличению доли Pt в металлическом состоянии. В частности, расчеты по ТФП показали, что изменения в плотности заряда, вызванные одновременным присутствием атомов S и P, способствуют формированию большего числа связей Pt–C и более сильному взаимодействию Pt и носителя. Удельная поверхность допированных носителей достигает 336.1 м2/г, а размер пор лежит в диапазоне 0–30 нм (размер большей части которых близок к 5 нм). Полученный катализатор на основе носителя, допированного атомами P и S одновременно (Pt/SPG), продемонстрировал более высокую величину ЭАП (70.2 м2/г) и более высокую активность (пиковое значение плотности тока прямой волны циклической вольтамперограммы в 0.5 М растворе метанола – 1127 А/г Pt) в РОМ, по сравнению с образцом на основе Р-допированного (61 м2/г и 685 А/г Pt, соответственно), S-допированного (57 м2/г и 609 А/г Pt, соответственно) и недопированного (53 м2/г и 409 А/г Pt, соответственно) гетероатомами носителя. Кроме того, Pt/SPG характеризуется более высокой стабильностью и толерантностью к отравлению СО. Позднее авторы [213] предложили простой сольвотермальный метод получения электрокатализатора РОМ на основе S,P-допированного графена Pt/3D-SPG, который характеризуется развитой 3D пористой структурой, способствующей формированию мелких и равномерно распределенных наночастиц Pt и улучшению массопереноса реагентов и продуктов РОМ в каталитическом слое на его основе.
В работе [214] показано, что одновременное допирование атомами N и F углеродных нановолокон (УНВ) (пиролиз смеси C6H3N6, NH4F и УНВ) ведет к их трансформации в графеновые листы с большим числом краевых активных центров, доступных для адсорбции и восстановления О2. За сравнительно высокую активность полученного материала в РВК (по сравнению с монодопированными УНВ) отвечают азот в пиридиновой и графитовой конфигурации, а также семиполярные связи С–F (концентрация атомов F и N составила 1.1 и 13 ат. %, соответственно). Максимальная удельная мощность МЭБ водород-кислородного ТЭ с ТПЭ на основе полученного N,F-допированного УНМ в качестве катодного АС и мембраны Nafion 212 составила 165 мВт/см2 при плотности тока 850 мА/см2, температуре 80°C и давлении 2 бара.
Авторами [215] разработан катализатор РВК на основе пористого углерода, допированного атомами N и F, полученного пиролизом и механической обработкой кофейной гущи. Допирование атомами F индуцирует возникновение открытых краевых дефектов, увеличивающих разупорядоченность УНМ, а присутствие в углеродной структуре различных функциональных групп (азот в различных конфигурациях, а также ионные и семиполярные связи C–F) приводят к сильной поляризации C–C-связей, перераспределению заряда и высокой спиновой плотности на поверхности материала. Допированные образцы характеризуются развитой мезопористой структурой со средним размером пор в диапазоне 3.2–6.2 нм и удельной поверхностью до 950 м2/г (УНМ, допированный атомами N и F). Согласно исследованиям, проведенным в жидком электролите, указанный допированный пористый углерод характеризуется сравнимой с коммерческим Pt/C (20% Pt) катализатором удельной активностью, более высокой стабильностью и толерантностью к СО и СН3ОН. Необходимо отметить, что выход Н2О2 при потенциалах <0.6 В значительно выше такового у Pt/C и составляет 0.5–4%. Максимальная удельная мощность МЭБ ТЭ с ТПЭ на основе допированного пористого углерода составила ок. 45 мВт/см2 (мембрана Nafion 212, 80°C, Н2/О2), что существенно уступает таковой у МЭБ ТЭ с ТПЭ на основе коммерческого платинового катализатора, что, по-видимому, связано с несбалансированными составом и структурой АС.
Позднее в работе [216] авторы использовали рассмотренные выше N,F–УНВ в качестве высокостабильного носителя в катализаторах Pt/N,F–УНВ также для применения на катоде ТЭ с ТПЭ. Хорошее распределение и взаимодействие частиц Pt с носителем способствуют увеличению ЭАП и активности электрокатализатора в РВК. Максимальная удельная мощность МЭБ водород-кислородного ТЭ с ТПЭ с Pt/NF–GNF в качестве катодного электрокатализатора достигает 867 мВт/см2 при 70°С с минимальной загрузкой Pt – около 0.1 мг/см2. Фторирование графитовых нановолокон обеспечивает возникновение C–F-связей, которые изменяют электронную плотность окружающих атомов углерода, а также увеличивают термическую и электрохимическую стабильность наночастиц Pt в условиях работы ТЭ. В частности, снижение ЭАП катализаторов Pt/C, Pt/N–УНВ и Pt/N,F–УНВ в результате УСТ (10 000 вольтамперометрических циклов в диапазоне потенциалов 0–1.05 В) составило 67, 29 и 12%, соответственно.
Подводя итоги, можно отметить, что допирование производных графена и других УНМ одновременно несколькими элементами позволяет: 1) сформировать большое число структурных дефектов и, соответственно, активных центров; 2) обеспечить эффективное окисления спиртов (в частности, метанола) по бифункциональному механизму и 3) повысить стабильность наночастиц Pt за счет пераспределения электронной плотности на поверхности катализатора. Полученные активные центры (например, пиридиновый и графитоподобный азот, сера в тиофеновой форме и др.) в зависимости от типа допантов и их сочетания обеспечивают лучшую дисперсию и снижение размера наночастиц Pt, сами могут выступать в роли активных центров РВК (B/N, N/P, P/S, N/F, противоречивые разультаты в отношении N/S), окисления (дегидрирования) метанола или способствуют окислению промежуточных продуктов РОМ по бифункциональному механизму. Необходимо отметить, что одновременное использование допантов-доноров и допантов-акцепторов электронов позволяет достичь синергетического эффекта, особенно в РОМ, в случае как катализаторов на основе Pt, так и катализаторов, не содержащих металлических наночастиц. В частности, в случае катализаторов на основе наночастиц Pt одновременное сочетание электрон-донорного и электрон-акцепторного допанта (например, N и B) позволяет нарушить электронейтральность носителя с sp2-структурой и облегчить хемосорбцию О2, а также обеспечить высокое число структурных дефектов для равномерного закрепления наночастиц Pt. В случае реакций окисления спиртов: электронакцепторный допант обеспечивает повышение активности активного центра Pt, а электрон-донорный – доокисление промежуточных продуктов по бифункциональному механизму.
3.3. Графеновые материалы, модифицированные тремя элементами
В работе [105] показан синергетический эффект от использования пористого углерода, допированного азотом, серой и фтором. Пиролиз сульфонированного полианилина, нанесенного на углеродную сажу Ketjenblack (KB) в атмосфере NH4F, позволяет обеспечить одновременное допирование углеродного носителя атомами N, S и F (N–S–F/KB). Показано, что допирование атомами N, S и F приводит к увеличению поляризации/спиновой плотности поверхности и числа активных центров, что выражается в высокой удельной активности катализатора, сравнимой с активностью коммерческого образца Pt/C. Высокое число активных центров подтверждается увеличением значения соотношения ID/IG, характеризующего степень дефектности (разупорядоченности) sp2-структуры, полученного методом рамановской спектроскопии. Причем допирование атомами F также приводит к росту значения ID/IG с 1.07 (N–S/KB) до 1.13 (N–S–F/KB), а атомы F образуют ионные и полуионные связи с углеродом, которые способствуют росту активности углеродного материала в РВК в отличие от ковалентных связей [217]. Важно отметить высокую стабильность полученных неметаллических катализаторов в РВК как в кислой, так и в щелочной среде, которая превосходит таковую у Pt/C по результатам ускоренного стресс-тестирования в жидком электролите.
Авторами [218] предложен простой и дешевый метод получения МУ, допированного атомами N, S, и P (NPSpC), путем пиролиза (900°С, атмосфера N2) металл-органической каркасной структуры ZIF-8 после его предварительной обработки раствором фитата натрия и додецилмеркаптаном. Полученный материал характеризуется высокой удельной поверхностью (1641 м2/г), мезопористой структурой (преобладают поры с размером около 3–4 нм) и высокой активностью в РВК в щелочных, нейтральных и кислых растворах. В частности, его активность в насыщенном О2 0.5 М растворе H2SO4 (E1/2 = 0.757 В, ilim ≈ 5.0 мА/см2) сравнима с активностью Pt/C (E1/2 = 0.788 В, ilim ≈ ≈ 5.5 мА/см2). Кроме того, РВК протекает на NPSpC по четырехэлектронному механизму, что подтверждается результатами измерений на вращающемся дисковом электроде с кольцом (n = = 3.68–3.87), а выход ${\text{HO}}_{2}^{ - }$ составил менее 6.2%, что сравнимо со значениями для Pt/C (n = 3.91, выход ${\text{HO}}_{2}^{ - }$ – менее 4.1%). В работе [219] рассмотрено влияние атомов S на свойства N,P-допированного пористого углерода. Активность катализатора, допированного атомами N, P и S, оказалась существенно выше по сравнению с N,P-допированным образцом и коррелирует с соотношением Sred/Sox, где Sred соответствует конфигурациям –C–S–C– и –C=S–. Указанные конфигурации атомов серы играют ключевую роль в перераспределении спиновой плотности соседних атомов углерода и снижении энергии адсорбции О2.
В заключение можно сделать вывод, что использование большего числа допантов, по-видимому, может быть востребовано в случае катализаторов, не содержащих металлических наночастиц. Это позволяет сформировать дополнительные активные центры за счет более сильной поляризации поверхности. Необходимо отметить, что во многих работах не уделяется достаточно внимания роли допантов и физико-химическим характеристикам полученных материалов, которые в существенной степени определяют как характеристики собственно катализаторов, так и электродов на их основе в составе ТЭ с ТПЭ. Исследования характеристик ТЭ с ТПЭ на основе таких материалов не рассматривались.
ЗАКЛЮЧЕНИЕ
Традиционные углеродные носители электрокатализаторов для ТЭ с ТПЭ, такие как углеродные сажи, обладают целым рядом недостатков, важнейшим из которых является недостаточно высокая стабильность. Благодаря преобладанию sp2-гибридизированной углеродной структуры, стабильность ближайших аналогов графена и его производных достаточно высока, и эти материалы рассматриваются в качестве альтернативных носителей. Однако базальная поверхность графена инертна и не имеет достаточно дефектов, которые могли бы выступать в качестве активных центров электрохимических реакций или зарождения наночастиц. Допирование УНМ любыми гетероатомами (главным образом, B, N, S или P) позволяет нарушить электронейтральность поверхности и перераспределить электронную плотность.
В отношении катализаторов на основе активных металлических наночастиц и модифицированных гетероатомами УНМ анализ рассмотренных публикаций показывает, что последние выступают не только как электропроводный носитель, но и оказывают существенное влияние на морфологию, структуру и электронную конфигурацию активных наночастиц и, следовательно, их активность и стабильность в электрохимических реакциях. При этом основное внимание исследователей сосредоточено на влиянии допантов на механизм реакций (РВК, РОМ, окисление водорода) и активность катализаторов в этих реакциях. Действительно, за счет вышеуказанных причин применение графеновых носителей, модифицированных любыми допантами, способствует росту активности и стабильности катализаторов, хотя механизм действия электродонорных и электроакцепторных допантов несколько различен. Общим является то, что допирование любыми из рассмотренных гетероатомов способствует формированию большого числа структурных дефектов для равномерного закрепления и стабилизации мелких наночастиц Pt. При этом в отношении допантов-доноров электронов (N и S) убедительно показано их положительное влияние на активность и стабильность наночастиц Pt за счет переноса электронной плотности от носителя к наночастицам, а роль допантов-акцепторов ограничена влиянием на морфологию наночастиц. Наиболее предпочтительным является одновременное допирование допантом-акцептором и допантом-донором электронов, поскольку это позволяет одновременно обеспечить равномерное распределение наночастиц при их минимальном размере, а также высокой активности и стабильности. Еще более полезным двойное допирование оказывается в случае катализаторов реакций окисления спиртов, поскольку наличие допанта-донора и допанта-акцептора электронов вблизи активного центра Pt обеспечивает высокую скорость и эффективность реакции окисления спиртов по бифункциональному механизму.
Вместе с тем, лишь немногие катализаторы были исследованы в составе МЭБ ТЭ. Более того, зачастую не уделяется достаточно внимания физико-химическим характеристикам полученных материалов, которые в существенной степени определяют как некоторые показатели собственно катализаторов (активность), так и электродов на их основе в составе ТЭ с ТПЭ. Это затрудняет анализ приводимых результатов и ставит под сомнение перспективность использования разработанных материалов в составе реальных устройств. Непосредственное влияние носителей допированных гетероатомами (особенно если их несколько) на производительность, ресурсные характеристики и механизмы деградации в различных режимах работы ТЭ с ТПЭ остается малоизученным.
Также сохраняется потребность в дополнительных усилиях научного сообщества, направленных на разработку таких методов получения допированных графеновых материалов (и УНМ в целом), которые были бы экологичными, легко масштабируемыми, дешевыми и одновременно позволили бы контролировать концентрацию, вид (функциональные группы) и распределение гетероатомов в носителе.
Отдельно необходимо остановиться на неплатиновых катализаторах (M/N/C) и катализаторах, не содержащих металлических наночастиц. Модифицированные графеновые наноматериалы также сами могут выступать в роли катализаторов электрохимических реакций, таких как реакции окисления спиртов, водорода или РВК. Допирование УНМ гетероатомами, главным образом двойное (B–N, S–N и др.) и тройное (N‒S–F, N–S–P и др.), способно существенно повысить удельную активность и селективность УНМ. Неплатиновые катализаторы (например, M/N/C-катализаторы) и катализаторы РВК, не содержащие металлических наночастиц, при переходе от модельных исследований в жидком электролите к формированию МЭБ характеризуются специфическими для них трудностями: удельная концентрация активных центров все равно оказывается невысокой и сохраняется необходимость в высоких загрузках катализатора. Это ведет к росту толщины АС и существенным транспортным ограничениям. Поэтому важно уделять внимание не только разработке катализаторов как таковых, но и оптимизации состава и структуры МЭБ с точки зрения организации в нем оптимального баланса всех потоков, включая диффузию кислорода, водный баланс, перенос заряда и теплоты. В частности, простым и перспективным вспомогательным подходом может быть введение каталитически неактивных функциональных добавок (ВОГ, МУНТ, УНВ) в АС. Традиционные методы формирования МЭБ ТЭ с ТПЭ приводят к нарушению пористой структуры АС, снижению его удельной поверхности и числа активных центров в результате воздействия высокого давления и температуры. Это делает их неподходящими для формирования АС на основе неплатиновых катализаторов и катализаторов, не содержащих металлических наночастиц. По-видимому, для достижения высокой эффективности МЭБ на их основе стоит рассмотреть альтернативные методы формирования МЭБ, такие как, например, самосвязывание МЭБ [220], прямое нанесение мембраны [221] и др.
Необходимо отметить, что совокупность рассмотренных в статье работ позволяет сделать вывод, что допирование УНМ любым из рассмотренных гетероатомов приводит к перераспределению электронной плотности на поверхности УНМ и, с высокой вероятностью, приведет к увеличению активности самого материала, снижению размера осаждаемых на его поверхности наночастиц и т.д. В этой связи можно отметить тендецию последних лет, состоящую в росте числа исследований, в которых “фиксируется” ожидаемое увеличение электрокаталитической активности полученных материалов, но отсутствует должный анализ причин и закономерностей этого эффекта. На это в ироничной манере указали авторы самой читаемой в 2020 г. статьи журнала ACS Nano [222]. Ученым следует избегать избыточного исследования всех возможных вариантов допирования графена в погоне за числом публикаций и их цитируемостью, получая вполне ожидаемые результаты. Такие усилия вряд ли позволят существенно продвинуться в данном направлении.
Список литературы
Wang, Y., Ruiz Diaz, D.F., Chen, K.S., Wang, Z., and Adroher, X.C., Materials, technological status, and fundamentals of PEM fuel cells – A review, Mater. Today, 2020, vol. 32, p. 178.
Zhang, S., Yuan, X.-Z., Hin, J.N.C., Wang, H., Friedrich, K.A., and Schulze, M., A review of platinum-based catalyst layer degradation in proton exchange membrane fuel cells, J. Power Sources, 2009, vol. 194, p. 588.
Danilov, M.O., Dovbeshko, G.I., Rusetskyi, I.A., Pekhnyo, V.I., Nikolenko, A.S., and Kolbasov, G.Y., Partially unzipped multi-walled carbon nanotubes–promising material for oxygen electrodes of fuel cells, Appl. Phys. A, 2020, vol. 126, p. 764.
Mohideen, M.M., Liu, Y., and Ramakrishna, S., Recent progress of carbon dots and carbon nanotubes applied in oxygen reduction reaction of fuel cell for transportation, Appl. Energy, 2020, vol. 257, p. 114027.
Wang, Y., Li, G., Jin, J., and Yang, S., Hollow porous carbon nanofibers as novel support for platinum-based oxygen reduction reaction electrocatalysts, Int. J. Hydrogen Energy, 2017, vol. 42, p. 5938.
Antolini, E., Carbon supports for low-temperature fuel cell catalysts, Appl. Catal. B Environ., 2009, vol. 88, p. 1.
Antolini, E., Graphene as a new carbon support for low-temperature fuel cell catalysts, Appl. Catal. B Environ., 2012, vol. 123–124, p. 52.
Hossain, S., Abdalla, A.M., Suhaili, S.B.H., Kamal, I., Shaikh, S.P.S., Dawood, M.K., and Azad, A.K., Nanostructured graphene materials utilization in fuel cells and batteries: A review, J. Energy Storage, 2020, vol. 29, p. 101386.
Baskakov, S.A., Baskakova, Y.V., Kalmykova, D.S., Komarov, B.A., Krasnikova, S.S., and Shul’ga, Y.M., Comparison of the Electrode Properties of Graphene Oxides Reduced Chemically, Thermally, or via Microwave Irradiation, Inorg. Mater., 2021, vol. 57, p. 262.
Rabchinskii, M.K., Ryzhkov, S.A., Kirilenko, D.A., Ulin, N.V., Baidakova, M.V., Shnitov, V.V., Pavlov, S.I., Chumakov, R.G., Stolyarova, D.Y., Besedina, N.A., Shvidchenko, A.V., Potorochin, D.V., Roth, F., Smirnov, D.A., Gudkov, M.V., Brzhezinskaya, M., Lebedev, O.I., Melnikov, V.P., and Brunkov, P.N., From graphene oxide towards aminated graphene: facile synthesis, its structure and electronic properties, Sci. Rep., 2020, vol. 10, p. 6902.
Кулакова, И.И., Лисичкин, Г.В. Химическое модифицирование графена. Журн. общей химии. 2020. Т. 90. С. 1601. [Kulakova, I.I. and Lisichkin, G.V., Chemical Modification of Graphene, Russ. J. Gen. Chem., 2020, vol. 90, p. 1921.]
Chandran, P., Ghosh, A., and Ramaprabhu, S., High-performance Platinum-free oxygen reduction reaction and hydrogen oxidation reaction catalyst in polymer electrolyte membrane fuel cell, Sci. Rep., 2018, vol. 8, p. 3591.
Feng, L., Qin, Z., Huang, Y., Peng, K., Wang, F., Yan, Y., and Chen, Y., Boron-, sulfur-, and phosphorus-doped graphene for environmental applications, Sci. Total Environ., 2020, vol. 698, p. 134239.
Pushkarev, A.S., Pushkareva, I.V., Grigoriev, S.A., Kalinichenko, V.N., Presniakov, M.Y., and Fateev, V.N., Electrocatalytic layers modified by reduced graphene oxide for PEM fuel cells, Int. J. Hydrogen Energy, 2015, vol. 40, p. 14492.
Григорьев, С.А., Пушкарев, А.С., Калиниченко, В.Н., Пушкарева, И.В., Пресняков, М.Ю., Фатеев, В.Н. Электрокаталитические слои на основе восстановленного оксида графена для приготовления низкотемпературных топливных. Кинетика и катализ. 2015. Т. 56. С. 698. [Grigor’ev, S.A., Pushkarev, A.S., Kalinichenko, V.N., Pushkareva, I.V., Presnyakov, M.Y., and Fateev, V.N., Electrocatalytic layers based on reduced graphene oxide for fabrication of low-temperature fuel cells, Kinet. Catal., 2015, vol. 56, p. 689.]
Baranov, I.E., Nikolaev, I.I., Pushkarev, A.S., Pushkareva, I.V., Kalinnikov, A.A., and Fateev, V.N., Numerical Modeling of Polymer Electrolyte Fuel Cell Catalyst Layer with Different Carbon Supports, Int. J. Electrochem. Sci., 2018, vol. 13, p. 8673.
Sung, C.-C., Liu, C.-Y., and Cheng, C.C.J., Durability improvement at high current density by graphene networks on PEM fuel cell, Int. J. Hydrogen Energy, 2014, vol. 39, p. 11706.
Pushkarev, A.S., Solovyev, M.A., Grigoriev, S.A., Pushkareva, I.V., Voloshin, Y.Z., Chornenka, N.V., Belov, A.S., Millet, P., Kalinichenko, V.N., and Dedov, A.G., Electrocatalytic hydrogen production using the designed hexaphenanthrene iron, cobalt and ruthenium(II) cage complexes as cathode (pre)catalysts immobilized on carbonaceous substrates, Int. J. Hydrogen Energy, 2020, vol. 45. https://doi.org/10.1016/j.ijhydene.2020.02.098
Pushkarev, A.S., Pushkareva, I.V., Solovyev, M.A., Grigoriev, S.A., Voloshin, Y.Z., Chornenka, N.V., Belov, A.S., Millet, P., Antuch, M., Kalinichenko, V.N., and Dedov, A.G., Polyaromatic-terminated iron(ii) clathrochelates as electrocatalysts for efficient hydrogen production in water electrolysis cells with polymer electrolyte membrane, Mendeleev Commun., 2021, vol. 31, p. 20.
Kuriganova, A.B., Leontyev, I.N., Maslova, O.A., and Smirnova, N.V., Electrochemically synthesized Pt-based catalysts with different carbon supports for proton exchange membrane fuel cell applications, Mendeleev Commun., 2018, vol. 28, p. 444.
Su, H. and Hu, Y.H., Recent advances in graphene-based materials for fuel cell applications, Energy Sci. Eng., 2021, vol. 9, p. 958.
Калинников, А.А., Островский, С.В., Порембский, В.И., Пушкарев, А.С., Фатеев, В.Н. Исследование электрохимического кислородного насоса на основе твердого полимерного электролита. Журн. прикл. химии. 2018. Т. 91. С. 798. [Kalinnikov, A.A., Ostrovskii, S.V., Porembskii, V.I., Pushkarev, A.S., and Fateev, V.N., Study of the Electrochemical Oxygen Pump Based on Solid Polymer Electrolyte, Russ. J. Appl. Chem., 2018, vol. 91, p. 927.]
Пушкарев, А.С., Пушкарева, И.В., Соловьев, М.А., Бутрим, С.И., Григорьев, С.А. Исследование кислородного концентратора с твердым полимерным электролитом с наноструктурными катализаторами на основе гидрофобизированного носителя. Рос. нанотехнологии. 2020. Т. 15. С. 106. [Pushkarev, A.S., Pushkareva, I.V., Solovyev, M.A., Butrim, S.I., and Grigoriev, S.A., The Study of the Solid Polymer Electrolyte Oxygen Concentrator with Nanostructural Catalysts Based on Hydrophobized Support, Nanotechnol. Russ., 2020, vol. 15, p. 785.]
Pushkareva, I.V., Pushkarev, A.S., Kalinichenko, V.N., Chumakov, R.G., Soloviev, M.A., Liang, Y., Millet, P., and Grigoriev, S.A., Reduced Graphene Oxide-Supported Pt-Based Catalysts for PEM Fuel Cells with Enhanced Activity and Stability, Catalysts, 2021, vol. 11, p. 256.
Campisi, S., Chan-Thaw, C., and Villa, A., Understanding Heteroatom-Mediated Metal–Support Interactions in Functionalized Carbons: A Perspective Review, Appl. Sci., 2018, vol. 8, p. 1159.
van Deelen, T.W., Hernández Mejía, C., and de Jong, K.P., Control of metal-support interactions in heterogeneous catalysts to enhance activity and selectivity, Nat. Catal., 2019, vol. 2, p. 955.
Baranov, I.E., Porembskii, V.I., Lyutikova, E.K., Nikolaev, I.I., Markelov, V.V., Alekseeva, O.K., Ostrovskii, S.V., Kalinnikov, A.A., Akelkina, S.V., Pushkarev, A.S., Solovyev, M.A., Pushkareva, I.V., and Fateev, V.N., Comparative study of Pt-based catalysts supported on various carbon supports for solid polymer electrolyte electrochemical systems, Chem. Probl., 2019, vol. 17, p. 489.
Pak Hoe, L., Boaventura, M., Lagarteira, T., Kee Shyuan, L., and Mendes, A., Polyol synthesis of reduced graphene oxide supported platinum electrocatalysts for fuel cells: Effect of Pt precursor, support oxidation level and pH, Int. J. Hydrogen Energy, 2018, vol. 43, p. 16998.
Şanlı, L.I., Bayram, V., Yarar, B., Ghobadi, S., and Gürsel, S.A., Development of graphene supported platinum nanoparticles for polymer electrolyte membrane fuel cells: Effect of support type and impregnation–reduction methods, Int. J. Hydrogen Energy, 2016, vol. 41, p. 3414.
Yazici, M.S., Azder, M.A., Salihoglu, O., and Boyaci San, F.G., Ultralow Pt loading on CVD graphene for acid electrolytes and PEM fuel cells, Int. J. Hydrogen Energy, 2018, vol. 43, p. 18572.
Gouse Peera, S., Kwon, H.-J., Lee, T.G., and Hussain, A.M., Heteroatom- and metalloid-doped carbon catalysts for oxygen reduction reaction: a mini-review, Ionics (Kiel)., 2020, vol. 26, p. 1563.
Akula, S. and Sahu, A.K., Structurally Modulated Graphitic Carbon Nanofiber and Heteroatom (N,F) Engineering toward Metal-Free ORR Electrocatalysts for Polymer Electrolyte Membrane Fuel Cells, ACS Appl. Mater. Interfaces, 2020, vol. 12, p. 11438.
Sibul, R., Kibena-Põldsepp, E., Ratso, S., Kook, M., Sougrati, M.T., Käärik, M., Merisalu, M., Aruväli, J., Paiste, P., Treshchalov, A., Leis, J., Kisand, V., Sammelselg, V., Holdcroft, S., Jaouen, F., and Tammeveski, K., Iron- and Nitrogen-Doped Graphene-Based Catalysts for Fuel Cell Applications, ChemElectroChem, 2020, vol. 7, p. 1739.
Zhang, L., Niu, J., Li, M., and Xia, Z., Catalytic Mechanisms of Sulfur-Doped Graphene as Efficient Oxygen Reduction Reaction Catalysts for Fuel Cells, J. Phys. Chem. C, 2014, vol. 118, p. 3545.
Wang, H., Maiyalagan, T., and Wang, X., Review on Recent Progress in Nitrogen-Doped Graphene: Synthesis, Characterization, and Its Potential Applications, ACS Catal., 2012, vol. 2, p. 781.
Yang, G., Li, L., Lee, W.B., and Ng, M.C., Structure of graphene and its disorders: a review, Sci. Technol. Adv. Mater., 2018, vol. 19, p. 613.
Jorge, A.B., Jervis, R., Periasamy, A.P., Qiao, M., Feng, J., Tran, L.N., and Titirici, M., 3D Carbon Materials for Efficient Oxygen and Hydrogen Electrocatalysis, Adv. Energy Mater., 2020, vol. 10, p. 1902494.
Mamtani, K. and Ozkan, U.S., Heteroatom-Doped Carbon Nanostructures as Oxygen Reduction Reaction Catalysts in Acidic Media: An Overview, Catal. Letters, 2015, vol. 145, p. 436.
Jia, Y., Zhang, L., Zhuang, L., Liu, H., Yan, X., Wang, X., Liu, J., Wang, J., Zheng, Y., Xiao, Z., Taran, E., Chen, J., Yang, D., Zhu, Z., Wang, S., Dai, L., and Yao, X., Identification of active sites for acidic oxygen reduction on carbon catalysts with and without nitrogen doping, Nat. Catal., 2019, vol. 2, p. 688.
Florent, M., Wallace, R., and Bandosz, T.J., Oxygen Electroreduction on Nanoporous Carbons: Textural Features vs Nitrogen and Boron Catalytic Centers, ChemCatChem, 2019, vol. 11, p. 851.
Barrera, D., Florent, M., Kulko, M., and Bandosz, T.J., Ultramicropore-influenced mechanism of oxygen electroreduction on metal-free carbon catalysts, J. Mater. Chem. A, 2019, vol. 7, p. 27110.
Duan, J., Chen, S., Jaroniec, M., and Qiao, S.Z., Heteroatom-Doped Graphene-Based Materials for Energy-Relevant Electrocatalytic Processes, ACS Catal., 2015, vol. 5, p. 5207.
Kumar, R., Sahoo, S., Joanni, E., Singh, R.K., Maegawa, K., Tan, W.K., Kawamura, G., Kar, K.K., and Matsuda, A., Heteroatom doped graphene engineering for energy storage and conversion, Mater. Today, 2020. https://doi.org/10.1016/j.mattod.2020.04.010
Cui, H., Zhou, Z., and Jia, D., Heteroatom-doped graphene as electrocatalysts for air cathodes, Mater. Horizons, 2017, vol. 4, p. 7.
Feng, X., Bai, Y., Liu, M., Li, Y., Yang, H., Wang, X., and Wu, C., Untangling the respective effects of heteroatom-doped carbon materials in batteries, supercapacitors and the ORR to design high performance materials, Energy Environ. Sci., 2021, vol. 14, p. 2036.
Higgins, D., Zamani, P., Yu, A., and Chen, Z., The application of graphene and its composites in oxygen reduction electrocatalysis: a perspective and review of recent progress, Energy Environ. Sci., 2016, vol. 9, p. 357.
Shao, Y., Jiang, Z., Zhang, Q., and Guan, J., Progress in Nonmetal-Doped Graphene Electrocatalysts for the Oxygen Reduction Reaction, ChemSusChem, 2019, vol. 12, p. 2133.
Алексеева, О.К., Пушкарева, И.В., Пушкарев, А.С., Фатеев, В.Н. Графен и графеноподобные материалы для водородной энергетики. Рос. нанотехнологии. 2020. Т. 15. С. 262. [Alekseeva, O.K., Pushkareva, I.V., Pushkarev, A.S., and Fateev, V.N., Graphene and Graphene-Like Materials for Hydrogen Energy, Nanotechnol. Russ., 2020, vol. 15, p. 273.]
Nagar, R., Vinayan, B.P., Samantaray, S.S., and Ramaprabhu, S., Recent advances in hydrogen storage using catalytically and chemically modified graphene nanocomposites, J. Mater. Chem. A, 2017, vol. 5, p. 22897.
Yang, L., Shui, J., Du, L., Shao, Y., Liu, J., Dai, L., and Hu, Z., Carbon-Based Metal-Free ORR Electrocatalysts for Fuel Cells: Past, Present, and Future, Adv. Mater., 2019, vol. 31, p. 1804799.
Rani, P. and Jindal, V.K., Designing band gap of graphene by B and N dopant atoms, RSC Adv., 2013, vol. 3, p. 802.
Bleu, Y., Bourquard, F., Barnier, V., Lefkir, Y., Reynaud, S., Loir, A.-S., Garrelie, F., and Donnet, C., Boron-doped graphene synthesis by pulsed laser co-deposition of carbon and boron, Appl. Surf. Sci., 2020, vol. 513, p. 145843.
Agnoli, S. and Favaro, M., Doping graphene with boron: a review of synthesis methods, physicochemical characterization, and emerging applications, J. Mater. Chem. A, 2016, vol. 4, p. 5002.
Kang, G.-S., Lee, S., Lee, D.C., Yoon, C.W., and Joh, H.-I., Edge-enriched graphene with boron and nitrogen co-doping for enhanced oxygen reduction reaction, Curr. Appl. Phys., 2020, vol. 20, p. 456.
Hu, M., Yao, Z., Li, L., Tsou, Y.-H., Kuang, L., Xu, X., Zhang, W., and Wang, X., Boron-doped graphene nanosheet-supported Pt: a highly active and selective catalyst for low temperature H 2-SCR, Nanoscale, 2018, vol. 10, p. 10203.
Cattelan, M., Agnoli, S., Favaro, M., Garoli, D., Romanato, F., Meneghetti, M., Barinov, A., Dudin, P., and Granozzi, G., Microscopic View on a Chemical Vapor Deposition Route to Boron-Doped Graphene Nanostructures, Chem. Mater., 2013, vol. 25, p. 1490.
Sun, Y., Du, C., Han, G., Qu, Y., Du, L., Wang, Y., Chen, G., Gao, Y., and Yin, G., Boron, nitrogen co-doped graphene: a superior electrocatalyst support and enhancing mechanism for methanol electrooxidation, Electrochim. Acta, 2016, vol. 212, p. 313.
Suo, N., Huang, H., Wu, A.M., Cao, G.Z., and Zhang, G.F., A Novel Method of Synthesizing Boron-doped Carbon Catalysts, Fuel Cells, 2018, vol. 18, p. 681.
Wang, L., Sofer, Z., Šimek, P., Tomandl, I., and Pumera, M., Boron-Doped Graphene: Scalable and Tunable p-Type Carrier Concentration Doping, J. Phys. Chem. C, 2013, vol. 117, p. 23251.
Sahoo, M. and Ramaprabhu, S., Nitrogen and sulfur co-doped porous carbon—is an efficient electrocatalyst as platinum or a hoax for oxygen reduction reaction in acidic environment PEM fuel cell?, Energy, 2017, vol. 119, p. 1075.
Sheng, Z.-H., Gao, H.-L., Bao, W.-J., Wang, F.-B., and Xia, X.-H., Synthesis of boron doped graphene for oxygen reduction reaction in fuel cells, J. Mater. Chem., 2012, vol. 22, p. 390.
Pullamsetty, A., Subbiah, M., and Sundara, R., Platinum on boron doped graphene as cathode electrocatalyst for proton exchange membrane fuel cells, Int. J. Hydrogen Energy, 2015, vol. 40, p. 10251.
Wang, H., Zhou, Y., Wu, D., Liao, L., Zhao, S., Peng, H., and Liu, Z., Synthesis of Boron-Doped Graphene Monolayers Using the Sole Solid Feedstock by Chemical Vapor Deposition, Small, 2013, vol. 9, p. 1316.
Bleu, Y., Bourquard, F., Tite, T., Loir, A.-S., Maddi, C., Donnet, C., and Garrelie, F., Review of Graphene Growth From a Solid Carbon Source by Pulsed Laser Deposition (PLD), Front. Chem., 2018, vol. 6. https://doi.org/10.3389/fchem.2018.00572
Panchakarla, L.S., Subrahmanyam, K.S., Saha, S.K., Govindaraj, A., Krishnamurthy, H.R., Waghmare, U.V., and Rao, C.N.R., Synthesis, Structure, and Properties of Boron- and Nitrogen-Doped Graphene, Adv. Mater., 2009, vol. 21, p. 4726.
Dey, S., Govindaraj, A., Biswas, K., and Rao, C.N.R., Luminescence properties of boron and nitrogen doped graphene quantum dots prepared from arc-discharge-generated doped graphene samples, Chem. Phys. Lett., 2014, vol. 595–596, p. 203.
Inagaki, M., Toyoda, M., Soneda, Y., and Morishita, T., Nitrogen-doped carbon materials, Carbon, 2018, vol. 132, p. 104.
Vikkisk, M., Kruusenberg, I., Joost, U., Shulga, E., and Tammeveski, K., Electrocatalysis of oxygen reduction on nitrogen-containing multi-walled carbon nanotube modified glassy carbon electrodes, Electrochim. Acta, 2013, vol. 87, p. 709.
Rybin, M., Pereyaslavtsev, A., Vasilieva, T., Myasnikov, V., Sokolov, I., Pavlova, A., Obraztsova, E., Khomich, A., Ralchenko, V., and Obraztsova, E., Efficient nitrogen doping of graphene by plasma treatment, Carbon, 2016, vol. 96, p. 196.
Li, X., Wang, H., Robinson, J.T., Sanchez, H., Diankov, G., and Dai, H., Simultaneous Nitrogen Doping and Reduction of Graphene Oxide, J. Am. Chem. Soc., 2009, vol. 131, p. 15939.
Deng, Y., Xie, Y., Zou, K., and Ji, X., Review on recent advances in nitrogen-doped carbons: preparations and applications in supercapacitors, J. Mater. Chem. A, 2016, vol. 4, p. 1144.
Braghiroli, F.L., Fierro, V., Izquierdo, M.T., Parmentier, J., Pizzi, A., and Celzard, A., Nitrogen-doped carbon materials produced from hydrothermally treated tannin, Carbon, 2012, vol. 50, p. 5411.
Long, D., Li, W., Ling, L., Miyawaki, J., Mochida, I., and Yoon, S.-H., Preparation of Nitrogen-Doped Graphene Sheets by a Combined Chemical and Hydrothermal Reduction of Graphene Oxide, Langmuir, 2010, vol. 26, p. 16096.
Tao, G., Zhang, L., Chen, L., Cui, X., Hua, Z., Wang, M., Wang, J., Chen, Y., and Shi, J., N-doped hierarchically macro/mesoporous carbon with excellent electrocatalytic activity and durability for oxygen reduction reaction, Carbon, 2015, vol. 86, p. 108.
Guo, B., Liu, Q., Chen, E., Zhu, H., Fang, L., and Gong, J.R., Controllable N-Doping of Graphene, Nano Lett., 2010, vol. 10, p. 4975.
Imran Jafri, R., Rajalakshmi, N., and Ramaprabhu, S., Nitrogen doped graphene nanoplatelets as catalyst support for oxygen reduction reaction in proton exchange membrane fuel cell, J. Mater. Chem., 2010, vol. 20, p. 7114.
Lin, Y.-P., Ksari, Y., Prakash, J., Giovanelli, L., Valmalette, J.-C., and Themlin, J.-M., Nitrogen-doping processes of graphene by a versatile plasma-based method, Carbon, 2014, vol. 73, p. 216.
Lin, Z., Waller, G., Liu, Y., Liu, M., and Wong, C.-P., Facile Synthesis of Nitrogen-Doped Graphene via Pyrolysis of Graphene Oxide and Urea, and its Electrocatalytic Activity toward the Oxygen-Reduction Reaction, Adv. Energy Mater., 2012, vol. 2, p. 884.
Vikkisk, M., Kruusenberg, I., Joost, U., Shulga, E., Kink, I., and Tammeveski, K., Electrocatalytic oxygen reduction on nitrogen-doped graphene in alkaline media, Appl. Catal. B Environ., 2014, vol. 147, p. 369.
Wei, D., Liu, Y., Wang, Y., Zhang, H., Huang, L., and Yu, G., Synthesis of N-Doped Graphene by Chemical Vapor Deposition and Its Electrical Properties, Nano Lett., 2009, vol. 9, p. 1752.
Liu, Q., Duan, Y., Zhao, Q., Pan, F., Zhang, B., and Zhang, J., Direct Synthesis of Nitrogen-Doped Carbon Nanosheets with High Surface Area and Excellent Oxygen Reduction Performance, Langmuir, 2014, vol. 30, p. 8238.
Gao, S., Chen, Y., Fan, H., Wei, X., Hu, C., Luo, H., and Qu, L., Large scale production of biomass-derived N-doped porous carbon spheres for oxygen reduction and supercapacitors, J. Mater. Chem. A, 2014, vol. 2, p. 3317.
Jiang, Z., Yu, J., Huang, T., and Sun, M., Recent Advance on Polyaniline or Polypyrrole-Derived Electrocatalysts for Oxygen Reduction Reaction, Polymers (Basel)., 2018, vol. 10, p. 1397.
Zhou, F., Wang, G., Huang, F., Zhang, Y., and Pan, M., Polyaniline derived N- and O-enriched high surface area hierarchical porous carbons as an efficient metal-free electrocatalyst for oxygen reduction, Electrochim. Acta, 2017, vol. 257, p. 73.
Rabchinskii, M.K., Ryzhkov, S.A., Gudkov, M.V., Baidakova, M.V., Saveliev, S.D., Pavlov, S.I., Shnitov, V.V., Kirilenko, D.A., Stolyarova, D.Y., Lebedev, A.M., Chumakov, R.G., Brzhezinskaya, M., Shiyanova, K.A., Pavlov, S.V., Kislenko, V.A., Kislenko, S.A., Makarova, A., Melnikov, V.P., and Brunkov, P.N., Unveiling a facile approach for large-scale synthesis of N-doped graphene with tuned electrical properties, 2D Mater., 2020, vol. 7, p. 045001.
Rabchinskii, M.K., Saveliev, S.D., Stolyarova, D.Y., Brzhezinskaya, M., Kirilenko, D.A., Baidakova, M.V., Ryzhkov, S.A., Shnitov, V.V., Sysoev, V.V., and Brunkov, P.N., Modulating nitrogen species via N-doping and post annealing of graphene derivatives: XPS and XAS examination, Carbon, 2021, vol. 182, p. 593.
Пушкарев, А.С., Алексеева, О.К., Пушкарева, И.В., Шапир, Б.Л., Чумаков, Р.Г., Тишкин, В.В., Козлова, М.В., Фатеев, В.Н. Плазменное азотирование наноструктурного восстановленного оксида графена. Рос. нанотехнологии. 2020. Т. 15. С. 71. [Pushkarev, A.S., Alekseeva, O.K., Pushkareva, I.V., Shapir, B.L., Chumakov, R.G., Tishkin, V.V., Kozlova, M.V., Kalinichenko, V.N., and Fateev, V.N., Plasma doping of nanostructed reduced graphene oxide, Nanotechnol. Russ., 2020, vol. 15, p. 735.]
Wang, Y., Yu, F., Zhu, M., Ma, C., Zhao, D., Wang, C., Zhou, A., Dai, B., Ji, J., and Guo, X., N-Doping of plasma exfoliated graphene oxide via dielectric barrier discharge plasma treatment for the oxygen reduction reaction, J. Mater. Chem. A, 2018, vol. 6, p. 2011.
Zhang, C., Mahmood, N., Yin, H., Liu, F., and Hou, Y., Synthesis of phosphorus-doped graphene and its multifunctional applications for oxygen reduction reaction and lithium ion batteries, Adv. Mater., 2013, vol. 25, p. 4932.
An, M., Du, C., Du, L., Sun, Y., Wang, Y., Chen, C., Han, G., Yin, G., and Gao, Y., Phosphorus-doped graphene support to enhance electrocatalysis of methanol oxidation reaction on platinum nanoparticles, Chem. Phys. Lett., 2017, vol. 687, p. 1.
Kobayashi, R., Ishii, T., Imashiro, Y., and Ozaki, J., Synthesis of P- and N-doped carbon catalysts for the oxygen reduction reaction via controlled phosphoric acid treatment of folic acid, Beilstein J. Nanotechnol., 2019, vol. 10, p. 1497.
Wen, Y., Wang, B., Huang, C., Wang, L., and Hulicova-Jurcakova, D., Synthesis of phosphorus-doped graphene and its wide potential window in aqueous supercapacitors, Chem. – A Eur. J., 2015, vol. 21, p. 80.
An, M., Du, L., Du, C., Sun, Y., Wang, Y., Yin, G., and Gao, Y., Pt nanoparticles supported by sulfur and phosphorus co-doped graphene as highly active catalyst for acidic methanol electrooxidation, Electrochim. Acta, 2018, vol. 285, p. 202.
Shiva Kumar, S., Ramakrishna, S.U.B., Rama Devi, B., and Himabindu, V., Phosphorus-doped graphene supported palladium (Pd/PG) electrocatalyst for the hydrogen evolution reaction in PEM water electrolysis, Int. J. Green Energy, 2018, vol. 15, p. 558.
MacIntosh, A.R., Jiang, G., Zamani, P., Song, Z., Riese, A., Harris, K.J., Fu, X., Chen, Z., Sun, X., and Goward, G.R., Phosphorus and Nitrogen Centers in Doped Graphene and Carbon Nanotubes Analyzed through Solid-State NMR, J. Phys. Chem. C, 2018, vol. 122, p. 6593.
Dong, F., Cai, Y., Liu, C., Liu, J., and Qiao, J., Heteroatom (B, N and P) doped porous graphene foams for efficient oxygen reduction reaction electrocatalysis, Int. J. Hydrogen Energy, 2018, vol. 43, p. 12661.
Some, S., Kim, J., Lee, K., Kulkarni, A., Yoon, Y., Lee, S., Kim, T., and Lee, H., Highly Air-Stable Phosphorus-Doped n-Type Graphene Field-Effect Transistors, Adv. Mater., 2012, vol. 24, p. 5481.
Chu, K., Wang, F., Tian, Y., and Wei, Z., Phosphorus doped and defects engineered graphene for improved electrochemical sensing: synergistic effect of dopants and defects, Electrochim. Acta, 2017, vol. 231, p. 557.
Li, R., Wei, Z., Gou, X., and Xu, W., Phosphorus-doped graphene nanosheets as efficient metal-free oxygen reduction electrocatalysts, RSC Adv., 2013, vol. 3, p. 9978.
Some, S., Shackery, I., Kim, S.J., and Jun, S.C., Phosphorus-Doped Graphene Oxide Layer as a Highly Efficient Flame Retardant, Chem. – A Eur. J., 2015, vol. 21, p. 15480.
Li, Y., Li, S., Wang, Y., Wang, J., Liu, H., Liu, X., Wang, L., Liu, X., Xue, W., and Ma, N., Electrochemical synthesis of phosphorus-doped graphene quantum dots for free radical scavenging, Phys. Chem. Chem. Phys., 2017, vol. 19, p. 11631.
Yang, Z., Yao, Z., Li, G., Fang, G., Nie, H., Liu, Z., Zhou, X., Chen, X., and Huang, S., Sulfur-Doped Graphene as an Efficient Metal-free Cathode Catalyst for Oxygen Reduction, ACS Nano, 2012, vol. 6, p. 205.
Denis, P.A., Band gap opening of monolayer and bilayer graphene doped with aluminium, silicon, phosphorus, and sulfur, Chem. Phys. Lett., 2010, vol. 492, p. 251.
Wang, X., Sun, G., Routh, P., Kim, D.-H., Huang, W., and Chen, P., Heteroatom-doped graphene materials: syntheses, properties and applications, Chem. Soc. Rev., 2014, vol. 43, p. 7067.
Akula, S., Peera, S.G., and Sahu, A.K., Uncovering N, S, F Tri-Doped Heteroatoms on Porous Carbon as a Metal-Free Oxygen Reduction Reaction Catalyst for Polymer Electrolyte Fuel Cells, J. Electrochem. Soc., 2019, vol. 166, p. F897.
Li, Y., Yang, J., Huang, J., Zhou, Y., Xu, K., Zhao, N., and Cheng, X., Soft template-assisted method for synthesis of nitrogen and sulfur co-doped three-dimensional reduced graphene oxide as an efficient metal free catalyst for oxygen reduction reaction, Carbon, 2017, vol. 122, p. 237.
Xu, C., Hoque, M.A., Chiu, G., Sung, T., and Chen, Z., Stabilization of platinum–nickel alloy nanoparticles with a sulfur-doped graphene support in polymer electrolyte membrane fuel cells, RSC Adv., 2016, vol. 6, p. 112226.
Vinayan, B.P., Diemant, T., Behm, R.J., and Ramaprabhu, S., Iron encapsulated nitrogen and sulfur co-doped few layer graphene as a non-precious ORR catalyst for PEMFC application, RSC Adv., 2015, vol. 5, p. 66494.
Poh, H.L., Šimek, P., Sofer, Z., and Pumera, M., Sulfur-Doped Graphene via Thermal Exfoliation of Graphite Oxide in H 2 S, SO 2, or CS 2 Gas, ACS Nano, 2013, vol. 7, p. 5262.
Wang, Z., Li, P., Chen, Y., He, J., Zhang, W., Schmidt, O. G., and Li, Y., Pure thiophene–sulfur doped reduced graphene oxide: synthesis, structure, and electrical properties, Nanoscale, 2014, vol. 6, p. 7281.
Yan, Y., Li, H., Liu, Q., Hao, N., Mao, H., and Wang, K., A facile strategy to construct pure thiophene-sulfur-doped graphene/ZnO nanoplates sensitized structure for fabricating a novel “on-off-on” switch photoelectrochemical aptasensor, Sensors Actuators B Chem., 2017, vol. 251, p. 99.
Liu, Y., Ma, Y., Jin, Y., Chen, G., and Zhang, X., Microwave-assisted solvothermal synthesis of sulfur-doped graphene for electrochemical sensing, J. Electroanal. Chem., 2015, vol. 739, p. 172.
Zhai, C., Sun, M., Zhu, M., Song, S., and Jiang, S., A new method to synthesize sulfur-doped graphene as effective metal-free electrocatalyst for oxygen reduction reaction, Appl. Surf. Sci., 2017, vol. 407, p. 503.
Klingele, M., Pham, C., Vuyyuru, K.R., Britton, B., Holdcroft, S., Fischer, A., and Thiele, S., Sulfur doped reduced graphene oxide as metal-free catalyst for the oxygen reduction reaction in anion and proton exchange fuel cells, Electrochem. commun., 2017, vol. 77, p. 71.
Van Pham, C., Klingele, M., Britton, B., Vuyyuru, K.R., Unmuessig, T., Holdcroft, S., Fischer, A., and Thiele, S., Tridoped Reduced Graphene Oxide as a Metal-Free Catalyst for Oxygen Reduction Reaction Demonstrated in Acidic and Alkaline Polymer Electrolyte Fuel Cells, Adv. Sustain. Syst., 2017, vol. 1, p. 1600038.
Li, M., Liu, C., Zhao, H., An, H., Cao, H., Zhang, Y., and Fan, Z., Tuning sulfur doping in graphene for highly sensitive dopamine biosensors, Carbon, 2015, vol. 86, p. 197.
Liang, C., Wang, Y., and Li, T., Synthesis of sulfur-doped p-type graphene by annealing with hydrogen sulfide, Carbon, 2015, vol. 82, p. 506.
Wang, R., Higgins, D.C., Hoque, M.A., Lee, D., Hassan, F., and Chen, Z., Controlled Growth of Platinum Nanowire Arrays on Sulfur Doped Graphene as High Performance Electrocatalyst, Sci. Rep., 2013, vol. 3, p. 2431.
Zehtab Yazdi, A., Roberts, E.P.L., and Sundararaj, U., Nitrogen/sulfur co-doped helical graphene nanoribbons for efficient oxygen reduction in alkaline and acidic electrolytes, Carbon, 2016, vol. 100, p. 99.
Perazzolo, V., Durante, C., Pilot, R., Paduano, A., Zheng, J., Rizzi, G.A., Martucci, A., Granozzi, G., and Gennaro, A., Nitrogen and sulfur doped mesoporous carbon as metal-free electrocatalysts for the in situ production of hydrogen peroxide, Carbon, 2015, vol. 95, p. 949.
Perazzolo, V., Brandiele, R., Durante, C., Zerbetto, M., Causin, V., Rizzi, G.A., Cerri, I., Granozzi, G., and Gennaro, A., Density Functional Theory (DFT) and Experimental Evidences of Metal–Support Interaction in Platinum Nanoparticles Supported on Nitrogen- and Sulfur-Doped Mesoporous Carbons: Synthesis, Activity, and Stability, ACS Catal., 2018, vol. 8, p. 1122.
Pham, C.V., Eck, M., and Krueger, M., Thiol functionalized reduced graphene oxide as a base material for novel graphene-nanoparticle hybrid composites, Chem. Eng. J., 2013, vol. 231, p. 146.
Adamska, M. and Narkiewicz, U., Fluorination of Carbon Nanotubes – A Review, J. Fluor. Chem., 2017, vol. 200, p. 179.
Liu, Y., Jiang, L., Wang, H., Wang, H., Jiao, W., Chen, G., Zhang, P., Hui, D., and Jian, X., A brief review for fluorinated carbon: synthesis, properties and applications, Nanotechnol. Rev., 2019, vol. 8, p. 573.
Chausov, D.N., Kurilov, A.D., Kazak, A.V., Smirnova, A.I., Belyaev, V.V., Gevorkyan, E.V., and Usol’tseva, N.V., Conductivity and dielectric properties of cholesteryl tridecylate with nanosized fragments of fluorinated graphene, J. Mol. Liq., 2019, vol. 291, p. 111259.
Zhao, F.-G., Zhao, G., Liu, X.-H., Ge, C.-W., Wang, J.-T., Li, B.-L., Wang, Q.-G., Li, W.-S., and Chen, Q.-Y., Fluorinated graphene: facile solution preparation and tailorable properties by fluorine-content tuning, J. Mater. Chem. A, 2014, vol. 2, p. 8782.
Jung, M.-J., Jeong, E., and Lee, Y.-S., The surface chemical properties of multi-walled carbon nanotubes modified by thermal fluorination for electric double-layer capacitor, Appl. Surf. Sci., 2015, vol. 347, p. 250.
Bi, X., Li, Y., Qiu, Z., Liu, C., Zhou, T., Zhuo, S., and Zhou, J., Fluorinated Graphene Prepared by Direct Fluorination of N, O-Doped Graphene Aerogel at Different Temperatures for Lithium Primary Batteries, Materials (Basel)., 2018, vol. 11, p. 1072.
Wang, B., Wang, J., and Zhu, J., Fluorination of Graphene: A Spectroscopic and Microscopic Study, ACS Nano, 2014, vol. 8, p. 1862.
Struzzi, C., Sezen, H., Amati, M., Gregoratti, L., Reckinger, N., Colomer, J.-F., Snyders, R., Bittencourt, C., and Scardamaglia, M., Fluorine and sulfur simultaneously co-doped suspended graphene, Appl. Surf. Sci., 2017, vol. 422, p. 104.
Zhang, H., Fan, L., Dong, H., Zhang, P., Nie, K., Zhong, J., Li, Y., Guo, J., and Sun, X., Spectroscopic Investigation of Plasma-Fluorinated Monolayer Graphene and Application for Gas Sensing, ACS Appl. Mater. Interfaces, 2016, vol. 8, p. 8652.
Qiao, X., Liao, S., Wang, G., Zheng, R., Song, H., and Li, X., Simultaneous doping of nitrogen and fluorine into reduced graphene oxide: A highly active metal-free electrocatalyst for oxygen reduction, Carbon, 2016, vol. 99, p. 272.
Jiang, S., Sun, Y., Dai, H., Hu, J., Ni, P., Wang, Y., Li, Z., and Li, Z., Nitrogen and fluorine dual-doped mesoporous graphene: a high-performance metal-free ORR electrocatalyst with a super-low HO 2 – yield, Nanoscale, 2015, vol. 7, p. 10584.
Peng, W., Li, H., and Song, S., Synthesis of Fluorinated Graphene/CoAl-Layered Double Hydroxide Composites as Electrode Materials for Supercapacitors, ACS Appl. Mater. Interfaces, 2017, vol. 9, p. 5204.
Sun, C., Feng, Y., Li, Y., Qin, C., Zhang, Q., and Feng, W., Solvothermally exfoliated fluorographene for high-performance lithium primary batteries, Nanoscale, 2014, vol. 6, p. 2634.
An, H., Li, Y., Long, P., Gao, Y., Qin, C., Cao, C., Feng, Y., and Feng, W., Hydrothermal preparation of fluorinated graphene hydrogel for high-performance supercapacitors, J. Power Sources, 2016, vol. 312, p. 146.
Kakaei, K. and Balavandi, A., Hierarchically porous fluorine-doped graphene nanosheets as efficient metal-free electrocatalyst for oxygen reduction in gas diffusion electrode, J. Colloid Interface Sci., 2017, vol. 490, p. 819.
Mazánek, V., Jankovský, O., Luxa, J., Sedmidubský, D., Janoušek, Z., Šembera, F., Mikulics, M., and Sofer, Z., Tuning of fluorine content in graphene: towards large-scale production of stoichiometric fluorographene, Nanoscale, 2015, vol. 7, p. 13646.
Bulusheva, L.G., Fedoseeva, Y.V., Flahaut, E., Rio, J., Ewels, C.P., Koroteev, V.O., Van Lier, G., Vyalikh, D.V., and Okotrub, A.V., Effect of the fluorination technique on the surface-fluorination patterning of double-walled carbon nanotubes, Beilstein J. Nanotechnol., 2017, vol. 8, p. 1688.
Pullamsetty, A. and Sundara, R., Investigation of catalytic activity towards oxygen reduction reaction of Pt dispersed on boron doped graphene in acid medium, J. Colloid Interface Sci., 2016, vol. 479, p. 260.
Yang, H.N., Lee, D.C., Park, K.W., and Kim, W.J., Platinum–boron doped graphene intercalated by carbon black for cathode catalyst in proton exchange membrane fuel cell, Energy, 2015, vol. 89, p. 500.
Yang, H.N. and Kim, W.J., Effect of boron-doping levels in Pt–B–graphene on the electrochemical properties and cell performance of high temperature proton exchange membrane fuel cells, Electrochim. Acta, 2016, vol. 209, p. 430.
Sun, Y., Du, C., An, M., Du, L., Tan, Q., Liu, C., Gao, Y., and Yin, G., Boron-doped graphene as promising support for platinum catalyst with superior activity towards the methanol electrooxidation reaction, J. Power Sources, 2015, vol. 300, p. 245.
Zhou, X., Qiao, J., Yang, L., and Zhang, J., A Review of Graphene-Based Nanostructural Materials for Both Catalyst Supports and Metal-Free Catalysts in PEM Fuel Cell Oxygen Reduction Reactions, Adv. Energy Mater., 2014, vol. 4, p. 1301523.
Karim, N.A., Shamsul, N.S., Alias, M.S., and Kamarudin, S.K., Structural and electronic properties of the adsorption molecules on Co and Fe/N-doped graphene towards the application in direct liquid fuel cell, Struct. Chem., 2021, vol. 32, p. 405.
Puthusseri, D. and Ramaprabhu, S., Oxygen reduction reaction activity of platinum nanoparticles decorated nitrogen doped carbon in proton exchange membrane fuel cell under real operating conditions, Int. J. Hydrogen Energy, 2016, vol. 41, p. 13163.
Melke, J., Peter, B., Habereder, A., Ziegler, J., Fasel, C., Nefedov, A., Sezen, H., Wöll, C., Ehrenberg, H., and Roth, C., Metal–Support Interactions of Platinum Nanoparticles Decorated N-Doped Carbon Nanofibers for the Oxygen Reduction Reaction, ACS Appl. Mater. Interfaces, 2016, vol. 8, p. 82.
Jukk, K., Kongi, N., Rauwel, P., Matisen, L., and Tammeveski, K., Platinum Nanoparticles Supported on Nitrogen-Doped Graphene Nanosheets as Electrocatalysts for Oxygen Reduction Reaction, Electrocatalysis, 2016, vol. 7, p. 428.
Chen, Y., Wang, J., Liu, H., Li, R., Sun, X., Ye, S., and Knights, S., Enhanced stability of Pt electrocatalysts by nitrogen doping in CNTs for PEM fuel cells, Electrochem. commun., 2009, vol. 11, p. 2071.
Groves, M. N., Chan, A. S. W., Malardier-Jugroot, C., and Jugroot, M., Improving platinum catalyst binding energy to graphene through nitrogen doping, Chem. Phys. Lett., 2009, vol. 481, p. 214.
Ma, J., Habrioux, A., Luo, Y., Ramos-Sanchez, G., Calvillo, L., Granozzi, G., Balbuena, P. B., and Alonso-Vante, N., Electronic interaction between platinum nanoparticles and nitrogen-doped reduced graphene oxide: effect on the oxygen reduction reaction, J. Mater. Chem. A, 2015, vol. 3, p. 11891.
He, D., Jiang, Y., Lv, H., Pan, M., and Mu, S., Nitrogen-doped reduced graphene oxide supports for noble metal catalysts with greatly enhanced activity and stability, Appl. Catal. B Environ., 2013, vols. 132–133, p. 379.
Chen, Y., Wang, J., Liu, H., Banis, M. N., Li, R., Sun, X., Sham, T.-K., Ye, S., and Knights, S., Nitrogen Doping Effects on Carbon Nanotubes and the Origin of the Enhanced Electrocatalytic Activity of Supported Pt for Proton-Exchange Membrane Fuel Cells, J. Phys. Chem. C, 2011, vol. 115, p. 3769.
Brandiele, R., Durante, C., Zerbetto, M., Vicentini, N., Kosmala, T., Badocco, D., Pastore, P., Rizzi, G.A., Isse, A.A., and Gennaro, A., Probing the correlation between Pt-support interaction and oxygen reduction reaction activity in mesoporous carbon materials modified with Pt–N active sites, Electrochim. Acta, 2018, vol. 277, p. 287.
Mao, S., Wang, C., and Wang, Y., The chemical nature of N-doping on N-doped carbon supported noble metal catalysts, J. Catal., 2019, vol. 375, p. 456.
Alegre, C., Sebastián, D., Gálvez, M., Baquedano, E., Moliner, R., Aricò, A., Baglio, V., and Lázaro, M., N-Doped Carbon Xerogels as Pt Support for the Electro-Reduction of Oxygen, Materials (Basel)., 2017, vol. 10, p. 1092.
Han, F., Liu, Z., Jia, J., Ai, J., Liu, L., Liu, J., and Wang, Q.-D., Influences of N species in N-doped carbon carriers on the catalytic performance of supported Pt, Mater. Chem. Phys., 2019, vol. 237, p. 121881.
Li, Z., Gao, Q., Zhang, H., Tian, W., Tan, Y., Qian, W., and Liu, Z., Low content Pt nanoparticles anchored on N-doped reduced graphene oxide with high and stable electrocatalytic activity for oxygen reduction reaction, Sci. Rep., 2017, vol. 7, p. 43352.
Varga, T., Varga, Á.T., Ballai, G., Haspel, H., Kukovecz, Á., and Kónya, Z., One step synthesis of chlorine-free Pt/Nitrogen-doped graphene composite for oxygen reduction reaction, Carbon, 2018, vol. 133, p. 90.
Zhao, L., Sui, X.-L., Li, J.-L., Zhang, J.-J., Zhang, L.-M., and Wang, Z.-B., Ultra-fine Pt nanoparticles supported on 3D porous N-doped graphene aerogel as a promising electro-catalyst for methanol electrooxidation, Catal. Commun., 2016, vol. 86, p. 46.
Sui, X.-L., Zhang, L.-M., Zhao, L., Gu, D.-M., Huang, G.-S., and Wang, Z.-B., Nitrogen-doped graphene aerogel with an open structure assisted by in-situ hydrothermal restructuring of ZIF-8 as excellent Pt catalyst support for methanol electro-oxidation, Int. J. Hydrogen Energy, 2018, vol. 43, p. 21899.
Karuppanan, K.K., Raghu, A.V., Panthalingal, M.K., Thiruvenkatam, V.P.K., and Pullithadathil, B., 3D-porous electrocatalytic foam based on Pt@N-doped graphene for high performance and durable polymer electrolyte membrane fuel cells, Sustain. Energy Fuels, 2019, vol. 3, p. 996.
Xiong, Y., You, M., Liu, F., Wu, M., Cai, C., Ding, L., Zhou, C., Hu, M., Deng, W., and Wang, S., Pt-Decorated, Nanocarbon-Intercalated, and N-Doped Graphene with Enhanced Activity and Stability for Oxygen Reduction Reaction, ACS Appl. Energy Mater., 2020, vol. 3, p. 2490.
Zhang, Q., Zhang, Y., Cai, W., Yu, X., Ling, Y., and Yang, Z., Nitrogen doped carbon layer coated platinum electrocatalyst supported on carbon nanotubes with enhanced stability, Int. J. Hydrogen Energy, 2017, vol. 42, p. 16773.
Zhang, Q., Yu, X., Ling, Y., Cai, W., and Yang, Z., Ultrathin nitrogen doped carbon layer stabilized Pt electrocatalyst supported on N-doped carbon nanotubes, Int. J. Hydrogen Energy, 2017, vol. 42, p. 10354.
Zhang, Q., Yang, Z., Ling, Y., Yu, X., Zhang, Y., and Cheng, H., Improvement in stability of PtRu electrocatalyst by carbonization of in-situ polymerized polyaniline, Int. J. Hydrogen Energy, 2018, vol. 43, p. 12730.
Lee, H., Sung, Y.-E., Choi, I., Lim, T., and Kwon, O.J., Novel synthesis of highly durable and active Pt catalyst encapsulated in nitrogen containing carbon for polymer electrolyte membrane fuel cell, J. Power Sources, 2017, vol. 362, p. 228.
Mohanraju, K., Lee, H., and Kwon, O.J., High Loading Pt Core/Carbon Shell Derived from Platinum-Aniline Complex for Direct Methanol Fuel Cell Application, Electroanalysis, 2018, vol. 30, p. 1604.
González-Hernández, M., Antolini, E., and Perez, J., CO Tolerance and Stability of Graphene and N-Doped Graphene Supported Pt Anode Electrocatalysts for Polymer Electrolyte Membrane Fuel Cells, Catalysts, 2020, vol. 10, p. 597.
Zhang, Z., Jiang, C., Li, P., Feng, Q., Zhao, Z., Liang, Yao, K., Fan, J., Li, H., and Wang, H., Pt atoms on doped carbon nanosheets with ultrahigh N content as a superior bifunctional catalyst for hydrogen evolution/oxidation, Sustain. Energy Fuels, 2021, vol. 5, p. 532.
Guo, D., Shibuya, R., Akiba, C., Saji, S., Kondo, T., and Nakamura, J., Active sites of nitrogen-doped carbon materials for oxygen reduction reaction clarified using model catalysts, Science, 2016, vol. 351, p. 361.
Mamtani, K., Jain, D., Dogu, D., Gustin, V., Gunduz, S., Co, A.C., and Ozkan, U.S., Insights into oxygen reduction reaction (ORR) and oxygen evolution reaction (OER) active sites for nitrogen-doped carbon nanostructures (CNx) in acidic media, Appl. Catal. B Environ., 2018, vol. 220, p. 88.
Mamtani, K., Singh, D., Dogu, D., Jain, D., Millet, J.-M. M., and Ozkan, U.S., Effect of Acid-Washing on the Nature of Bulk Characteristics of Nitrogen-Doped Carbon Nanostructures as Oxygen Reduction Reaction Electrocatalysts in Acidic Media, Energy & Fuels, 2018, vol. 32, p. 11038.
Jain, D., Zhang, Q., Hightower, J., Gustin, V., Asthagiri, A., and Ozkan, U.S., Changes in Active Sites on Nitrogen-Doped Carbon Catalysts Under Oxygen Reduction Reaction: A Combined Post-Reaction Characterization and DFT Study, ChemCatChem, 2019, vol. 11, p. 5945.
Shui, J., Wang, M., Du, F., and Dai, L., N-doped carbon nanomaterials are durable catalysts for oxygen reduction reaction in acidic fuel cells, Sci. Adv., 2015, vol. 1, p. e1400129.
Sun, T., Tian, B., Lu, J., and Su, C., Recent advances in Fe (or Co)/N/C electrocatalysts for the oxygen reduction reaction in polymer electrolyte membrane fuel cells, J. Mater. Chem. A, 2017, vol. 5, p. 18933.
He, Y., Liu, S., Priest, C., Shi, Q., and Wu, G., Atomically dispersed metal–nitrogen–carbon catalysts for fuel cells: advances in catalyst design, electrode performance, and durability improvement, Chem. Soc. Rev., 2020, vol. 49, p. 3484.
Osmieri, L., Park, J., Cullen, D. A., Zelenay, P., Myers, D.J., and Neyerlin, K.C., Status and challenges for the application of platinum group metal-free catalysts in proton-exchange membrane fuel cells, Curr. Opin. Electrochem., 2021, vol. 25, p. 100627.
Wan, X., Liu, X., Li, Y., Yu, R., Zheng, L., Yan, W., Wang, H., Xu, M., and Shui, J., Fe–N–C electrocatalyst with dense active sites and efficient mass transport for high-performance proton exchange membrane fuel cells, Nat. Catal., 2019, vol. 2, p. 259.
Fu, X., Zamani, P., Choi, J.-Y., Hassan, F. M., Jiang, G., Higgins, D.C., Zhang, Y., Hoque, M. A., and Chen, Z., In Situ Polymer Graphenization Ingrained with Nanoporosity in a Nitrogenous Electrocatalyst Boosting the Performance of Polymer–Electrolyte–Membrane Fuel Cells, Adv. Mater., 2017, vol. 29, p. 1604456.
Yang, X., Wang, Y., Zhang, G., Du, L., Yang, L., Markiewicz, M., Choi, J., Chenitz, R., and Sun, S., SiO2–Fe/N/C catalyst with enhanced mass transport in PEM fuel cells, Appl. Catal. B Environ., 2020, vol. 264, p. 118523.
Sudarsono, W., Wong, W.Y., Loh, K.S., Majlan, E.H., Syarif, N., Kok, K.-Y., Yunus, R.M., Lim, K.L., and Hamada, I., Sengon wood-derived RGO supported Fe-based electrocatalyst with stabilized graphitic N-bond for oxygen reduction reaction in acidic medium, Int. J. Hydrogen Energy, 2020, vol. 45, p. 23237.
Kim, J., Kim, C., Jeon, I.-Y., Baek, J.-B., Ju, Y.-W., and Kim, G., A New Strategy for Outstanding Performance and Durability in Acidic Fuel Cells: A Small Amount Pt Anchored on Fe, N co-Doped Graphene Nanoplatelets, ChemElectroChem, 2018, vol. 5, p. 2857.
Vecchio, C.Lo, Serov, A., Dicome, M., Zulevi, B., Aricò, A.S., and Baglio, V., Investigating the durability of a direct methanol fuel cell equipped with commercial Platinum Group Metal-free cathodic electro-catalysts, Electrochim. Acta, 2021, p. 139108.
Yang, N., Zheng, X., Li, L., Li, J., and Wei, Z., Influence of Phosphorus Configuration on Electronic Structure and Oxygen Reduction Reactions of Phosphorus-Doped Graphene, J. Phys. Chem. C, 2017, vol. 121, p. 19321.
Kumar, N.A. and Baek, J.-B., Carbon-Based Metal-Free Catalysts. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, Germany, 2018, p. 529.
Liu, Y.-X., Zhang, W.-Y., Han, G.-K., Zhou, Y.-W., Li, L.-F., Kong, F.-P., Gao, Y.-Z., Du, C.-Y., Wang, J.-J., Du, L., Cai, W.-B., and Yin, G.-P., Deactivated Pt Electrocatalysts for the Oxygen Reduction Reaction: The Regeneration Mechanism and a Regenerative Protocol, ACS Catal., 2021, vol. 11, p. 9293.
Higgins, D., Hoque, M.A., Seo, M.H., Wang, R., Hassan, F., Choi, J.-Y., Pritzker, M., Yu, A., Zhang, J., and Chen, Z., Development and Simulation of Sulfur-doped Graphene Supported Platinum with Exemplary Stability and Activity Towards Oxygen Reduction, Adv. Funct. Mater., 2014, vol. 24, p. 4325.
Hoque, M.A., Hassan, F.M., Higgins, D., Choi, J.-Y., Pritzker, M., Knights, S., Ye, S., and Chen, Z., Multigrain Platinum Nanowires Consisting of Oriented Nanoparticles Anchored on Sulfur-Doped Graphene as a Highly Active and Durable Oxygen Reduction Electrocatalyst, Adv. Mater., 2015, vol. 27, p. 1229.
Hoque, M.A., Hassan, F. M., Seo, M.-H., Choi, J.-Y., Pritzker, M., Knights, S., Ye, S., and Chen, Z., Optimization of sulfur-doped graphene as an emerging platinum nanowires support for oxygen reduction reaction, Nano Energy, 2016, vol. 19, p. 27.
Lu, Z., Li, S., Liu, C., He, C., Yang, X., Ma, D., Xu, G., and Yang, Z., Sulfur doped graphene as a promising metal-free electrocatalyst for oxygen reduction reaction: a DFT-D study, RSC Adv., 2017, vol. 7, p. 20398.
Nansé, G., Papirer, E., Fioux, P., Moguet, F., and Tressaud, A., Fluorination of carbon blacks: An X-ray photoelectron spectroscopy study: I. A literature review of XPS studies of fluorinated carbons. XPS investigation of some reference compounds, Carbon, 1997, vol. 35, p. 175.
Asset, T., Chattot, R., Maillard, F., Dubau, L., Ahmad, Y., Batisse, N., Dubois, M., Guérin, K., Labbé, F., Metkemeijer, R., Berthon-Fabry, S., and Chatenet, M., Activity and Durability of Platinum-Based Electrocatalysts Supported on Bare or Fluorinated Nanostructured Carbon Substrates, J. Electrochem. Soc., 2018, vol. 165, p. F3346.
Berthon-Fabry, S., Dubau, L., Ahmad, Y., Guerin, K., and Chatenet, M., First Insight into Fluorinated Pt/Carbon Aerogels as More Corrosion-Resistant Electrocatalysts for Proton Exchange Membrane Fuel Cell Cathodes, Electrocatalysis, 2015, vol. 6, p. 521.
Grigoriev, S., Fateev, V., Pushkarev, A., Pushkareva, I., Ivanova, N., Kalinichenko, V.Yu., Presnyakov, M., and Wei, X., Reduced Graphene Oxide and Its Modifications as Catalyst Supports and Catalyst Layer Modifiers for PEMFC, Materials (Basel)., 2018, vol. 11, p. 1405.
Bott-Neto, J.L., Asset, T., Maillard, F., Dubau, L., Ahmad, Y., Guérin, K., Berthon-Fabry, S., Mosdale, A., Mosdale, R., Ticianelli, E.A., and Chatenet, M., Utilization of graphitized and fluorinated carbon as platinum nanoparticles supports for application in proton exchange membrane fuel cell cathodes, J. Power Sources, 2018, vol. 404, p. 28.
Zhu, J., He, G., Tian, Z., Liang, L., and Shen, P.K., Facile synthesis of boron and nitrogen-dual-doped graphene sheets anchored platinum nanoparticles for oxygen reduction reaction, Electrochim. Acta, 2016, vol. 194, p. 276.
Li, M., Jiang, Q., Yan, M., Wei, Y., Zong, J., Zhang, J., Wu, Y., and Huang, H., Three-Dimensional Boron- and Nitrogen-Codoped Graphene Aerogel-Supported Pt Nanoparticles as Highly Active Electrocatalysts for Methanol Oxidation Reaction, ACS Sustain. Chem. Eng., 2018, vol. 6, p. 6644.
Zhou, Q., Wu, J., Pan, Z., Kong, X., Cui, Z., Wu, D., and Hu, G., Pt supported on boron, nitrogen co-doped carbon nanotubes (BNC NTs) for effective methanol electrooxidation, Int. J. Hydrogen Energy, 2020, vol. 45, p. 33634.
Ishii, T., Maie, T., Kimura, N., Kobori, Y., Imashiro, Y., and Ozaki, J., Enhanced catalytic activity of nanoshell carbon co-doped with boron and nitrogen in the oxygen reduction reaction, Int. J. Hydrogen Energy, 2017, vol. 42, p. 15489.
Kanninen, P., Luong, N.D., Sinh, L.H., Flórez-Montaño, J., Jiang, H., Pastor, E., Seppälä, J., and Kallio, T., Highly active platinum nanoparticles supported by nitrogen/sulfur functionalized graphene composite for ethanol electro-oxidation, Electrochim. Acta, 2017, vol. 242, p. 315.
Chao, G., Zhang, L., Wang, D., Chen, S., Guo, H., Xu, K., Fan, W., and Liu, T., Activation of graphitic nitrogen sites for boosting oxygen reduction, Carbon, 2020, vol. 159, p. 611.
Yang, C., Jin, H., Cui, C., Li, J., Wang, J., Amine, K., Lu, J., and Wang, S., Nitrogen and sulfur co-doped porous carbon sheets for energy storage and pH-universal oxygen reduction reaction, Nano Energy, 2018, vol. 54, p. 192.
Kwak, D.-H., Han, S.-B., Lee, Y.-W., Park, H.-S., Choi, I.-A., Ma, K.-B., Kim, M.-C., Kim, S.-J., Kim, D.-H., Sohn, J.-I., and Park, K.-W., Fe/N/S-doped mesoporous carbon nanostructures as electrocatalysts for oxygen reduction reaction in acid medium, Appl. Catal. B Environ., 2017, vol. 203, p. 889.
Zehtab Yazdi, A., Fei, H., Ye, R., Wang, G., Tour, J., and Sundararaj, U., Boron/Nitrogen Co-Doped Helically Unzipped Multiwalled Carbon Nanotubes as Efficient Electrocatalyst for Oxygen Reduction, ACS Appl. Mater. Interfaces, 2015, vol. 7, p. 7786.
Li, D., Jia, Y., Chang, G., Chen, J., Liu, H., Wang, J., Hu, Y., Xia, Y., Yang, D., and Yao, X., A Defect-Driven Metal-free Electrocatalyst for Oxygen Reduction in Acidic Electrolyte, Chem, 2018, vol. 4, p. 2345.
Chen, Z., Higgins, D., Yu, A., Zhang, L., and Zhang, J., A review on non-precious metal electrocatalysts for PEM fuel cells, Energy Environ. Sci., 2011, vol. 4, p. 3167.
Kramm, U. I., Herranz, J., Larouche, N., Arruda, T.M., Lefèvre, M., Jaouen, F., Bogdanoff, P., Fiechter, S., Abs-Wurmbach, I., Mukerjee, S., and Dodelet, J.-P., Structure of the catalytic sites in Fe/N/C-catalysts for O2-reduction in PEM fuel cells, Phys. Chem. Chem. Phys., 2012, vol. 14, p. 11673.
Shen, H., Gracia-Espino, E., Ma, J., Zang, K., Luo, J., Wang, L., Gao, S., Mamat, X., Hu, G., Wagberg, T., and Guo, S., Synergistic Effects between Atomically Dispersed Fe–N–C and C–S–C for the Oxygen Reduction Reaction in Acidic Media, Angew. Chemie Int. Ed., 2017, vol. 56, p. 13800.
Bhange, S.N., Unni, S.M., and Kurungot, S., Graphene with Fe and S Coordinated Active Centers: An Active Competitor for the Fe–N–C Active Center for Oxygen Reduction Reaction in Acidic and Basic pH Conditions, ACS Appl. Energy Mater., 2018, vol. 1, p. 368.
Bhange, S.N., Soni, R., Singla, G., Ajithkumar, T.G., and Kurungot, S., FeNx/FeSx – Anchored Carbon Sheet–Carbon Nanotube Composite Electrocatalysts for Oxygen Reduction, ACS Appl. Nano Mater., 2020, vol. 3, p. 2234.
Qiao, M. and Titirici, M., Engineering the Interface of Carbon Electrocatalysts at the Triple Point for Enhanced Oxygen Reduction Reaction, Chem. – A Eur. J., 2018, vol. 24, p. 18374.
An, M., Du, C., Du, L., Wang, Y., Wang, Y., Sun, Y., Yin, G., and Gao, Y., Enhanced Methanol Oxidation in Acid Media on Pt/S, P Co-doped Graphene with 3D Porous Network Structure Engineering, ChemElectroChem, 2019, vol. 6, p. 1157.
Peera, S.G., Sahu, A.K., Arunchander, A., Bhat, S.D., Karthikeyan, J., and Murugan, P., Nitrogen and fluorine co-doped graphite nanofibers as high durable oxygen reduction catalyst in acidic media for polymer electrolyte fuel cells, Carbon, 2015, vol. 93, p. 130.
Akula, S. and Sahu, A.K., Heteroatoms co-Doping (N, F) to the Porous Carbon Derived from Spent Coffee Grounds as an Effective Catalyst for Oxygen Reduction Reaction in Polymer Electrolyte Fuel Cells, J. Electrochem. Soc., 2019, vol. 166, p. F93.
Peera, S.G., Arunchander, A., and Sahu, A.K., Platinum nanoparticles supported on nitrogen and fluorine co-doped graphite nanofibers as an excellent and durable oxygen reduction catalyst for polymer electrolyte fuel cells, Carbon, 2016, vol. 107, p. 667.
Wang, H., Ding, J., Zhang, J., Wang, C., Yang, W., Ren, H., and Kong, A., Fluorine and nitrogen co-doped ordered mesoporous carbon as a metal-free electrocatalyst for oxygen reduction reaction, RSC Adv., 2016, vol. 6, p. 79928.
Rong, H., Zhan, T., Sun, Y., Wen, Y., Liu, X., and Teng, H., ZIF-8 derived nitrogen, phosphorus and sulfur tri-doped mesoporous carbon for boosting electrocatalysis to oxygen reduction in universal pH range, Electrochim. Acta, 2019, vol. 318, p. 783.
Zan, Y., Zhang, Z., Dou, M., and Wang, F., Enhancement mechanism of sulfur dopants on the catalytic activity of N and P co-doped three-dimensional hierarchically porous carbon as a metal-free oxygen reduction electrocatalyst, Catal. Sci. Technol., 2019, vol. 9, p. 5906.
Hack, J., Heenan, T.M.M., Iacoviello, F., Mansor, N., Meyer, Q., Shearing, P., Brandon, N., and Brett, D.J.L., A Structure and Durability Comparison of Membrane Electrode Assembly Fabrication Methods: Self-Assembled Versus Hot-Pressed, J. Electrochem. Soc., 2018, vol. 165, p. F3045.
Vierrath, S., Breitwieser, M., Klingele, M., Britton, B., Holdcroft, S., Zengerle, R., and Thiele, S., The reasons for the high power density of fuel cells fabricated with directly deposited membranes, J. Power Sources, 2016, vol. 326, p. 170.
Wang, L., Sofer, Z., and Pumera, M., Will Any Crap We Put into Graphene Increase Its Electrocatalytic Effect?, ACS Nano, 2020, vol. 14, p. 21.
Дополнительные материалы отсутствуют.
Инструменты
Электрохимия