Журнал эволюционной биохимии и физиологии, 2019, T. 55, № 3, стр. 208-210
О НЕКОТОРЫХ ГЕНЕТИЧЕСКИХ ДЕТЕРМИНАНТАХ СОСУДИСТЫХ РЕАКЦИЙ ПРИ ИМИТАЦИИ НЫРЯНИЯ У ЧЕЛОВЕКА
Т. И. Баранова 1, *, Д. Н. Берлов 3, А. С. Глотов 2, О. С. Глотов 2, Л. Б. Заварина 1, Т. А. Качанова 4, Е. Ю. Подъячева 1, С. Ш. Намозова 1, А. В. Шлейкина 4
1 Санкт-Петербургский государственный университет
Санкт-Петербург, Россия
2 Ресурсный центр “Центр Биобанк” Санкт-Петербургского государственного университета
Санкт-Петербург, Россия
3 Российский государственный педагогический университет им. А.И. Герцена
Санкт-Петербург, Россия
4 Национальный государственный университет физической культуры, спорта и здоровья им. П.Ф. Лесгафта
Санкт-Петербург, Россия
* E-mail: baranovati@gmail.com
Поступила в редакцию 09.04.2018
После доработки 07.12.2018
Принята к публикации 20.02.2019
Исследованы адаптивные реакции сосудистой системы на пробу с имитацией ныряния у представителей с различными полиморфизмами генов ADBR2 (A/G, rs1042713), ACE (I/D, rs4340), AGTR1 (A/C, rs5186), BDKRB2 (T/C, rs1799722) и REN (G/A, rs2368564). Обследовано 80 человек в возрасте 19 ± 0.9 лет. Полиморфизм генов исследовали с помощью двухэтапной мультиплексной ПЦР. Кровенаполнение периферических сосудов косвенно определяли по показателю амплитуды пульсовой волны фотоплетизмограммы, а тонус сосудов – по времени ее распространения. Во время пробы с имитацией ныряния выявлена различная эффективность адаптивных сосудистых реакций у обследованных с различным сочетанием аллелей исследуемых генов. Наиболее выраженное повышение тонуса периферических сосудов выявлено у представителей с BDKRB2 (C/C), ACE (D/D) and ADBR2 (G/G, G/A) генотипами.
Нырятельная реакция – это комплекс сердечно-сосудистых рефлексов (замедление сердечного ритма, констрикция периферических сосудов, селективное перераспределение крови к мозгу и сердцу и пр.). Эти реакции обеспечивают рациональное потребление кислорода при нырянии в условиях прекращения поступления его в организм. Защитный механизм нырятельного рефлекса сложился у ныряющих млекопитающих в результате освоения водной среды и закрепился генетически в процессе эволюции. Многочисленными исследованиями показано, что подобный защитный механизм присущ и человеку. Особенности реализации нырятельного рефлекса у животных определяются принадлежностью к виду. У человека эффективность защитного механизма нырятельной реакции, как нами было показано [1], зависит от характера вегетативной регуляции.
Известно, что любая физиологическая функция находится под контролем определенных генов, формирующих генную сеть. Логично предположить, что индивидуальная “динамическая норма” функции (верхняя и нижняя граница допустимых отклонений) будет определяться полиморфизмами генов данной сети [2]. Исследования в области физиологической генетики человека немногочисленны и связаны либо с генетикой спортивных качеств [3], либо с предиктивной медициной [4], из них только небольшая часть посвящена генетическим детерминантам вегетативной регуляции, и обусловленных ею стратегий приспособления.
Цель настоящей работы состояла в изучении сосудистых реакций нырятельного рефлекса у людей с различными полиморфными вариантами генов, продукты которых участвуют в регуляции сосудистого тонуса. Обследовано 80 человек (20–23 года), из них 54 девушки и 26 юношей, не имевших заболеваний сердечно-сосудистой системы. Ныряние имитировали погружением лица в воду 12 ± 2.3°С, при температуре воздуха 22 ± 2.5°С. Перед погружением, во время и в процессе восстановления регистрировали ЭКГ, АД и фотоплетизмограмму. Кровенаполнение периферических сосудов оценивали по амплитуде систолической волны (АСВ, pm), их тонус – по времени распространения пульсовой волны (ВПРП, mc). Запись и анализ фотоплетизмограммы проводили с использованием программно-диагностического комплекса реограф-полианализатор РГПА-6/12 “РЕАН-ПОЛИ”, фирмы “Медиком-МТД” (Таганрог, Россия). Гипоксическую и гиперкапническую нагрузку определяли по парциальному содержанию кислорода и углекислого газа (pO2 и pСO2) в выдыхаемом после апноэ воздухе. Газоанализ проводили при помощи микропроцессорного анализатора MF01 (предприятие изготовитель – ООО “Научно-производственный центр экологии и здоровья – ЦЭЗ”, СПб).
Полиморфизм гена ACE (I/D, rs4340) исследовали методом полимеразной цепной реакции (ПЦР). Полиморфизм генов REN (G/A, rs2368564), AGTR1 (A/C, rs5186), BDKRB2 (T/C, rs1799722), ADBR2 (A/G, rs1042713) исследовали с помощью двухэтапной мультиплексной ПЦР с добавлением флуоресцентно меченных праймеров и последующим проведением аллельспецифической гибридизации на биочипе. Типирование проводили на основе интенсивности флуоресцентного сигнала от ячеек микрочипа по ранее разработанной методике [5]. Достоверность отличий оценивали по критериям Уилкоксона и Манна–Уитни.
Длительность апноэ при имитации ныряния в среднем по группе составила: Т = 31 ± 11.1 с, при этом рО2 в выдыхаемом воздухе после апноэ – 98.8 ± 8.7 мм рт.ст., рСО2 = 49.1 ± 3.5 мм рт.ст. АСВ и ВРПВ при имитации ныряния уменьшались у всех обследованных. АСВ в среднем по группе обследуемых (n = 80) в покое была – 1.67 ± 0.91 pm, при апноэ – 0.35 ± 0.22 pm (p < 0.001), при восстановлении – 0.97 ± 0.31 pm (относительно исходного состояния p < 0.01); ВРПВ в исходном состоянии – 217 ± 11.1 с, при апноэ – 200 ± 25.9 с (p < 0.05), при восстановлении – 191.4 ± 17.8 с (относительно исходного состояния p < 0.01). При этом уменьшение периферического кровотока у обследованных сильно варьировало.
В исходном состоянии кровенаполнение периферических сосудов (АСВ) значительно ниже (p < 0.01) у носителей генотипа G/G по гену REN, чем у представителей с генотипами G/A и A/A (табл. 1), что соответствует данным литературы о роли полиморфизма гена ренина в регуляции вазоконстрикции и вазодилатации [5]. Аналогичные результаты получены и для полиморфизма гена AGTR1: тонус сосудов был ниже – больше ВРПВ, у представителей с генотипом A/A по сравнению с носителями аллели С (рис. 1). При имитации ныряния менее всего кровенаполнение сосудов (самая высокая АСВ ) снижалось у G/G гомозигот по гену ADRB2 по сравнению с носителями аллели A (p < 0.05), а самый высокий тонус сосудов (по показателю ВРПВ) был выявлен у С/С-гомозигот по гену BDKRB2 относительно представителей других генотипов этого гена (p < 0.05), и D/D-гомозигот по гену АСЕ относительно представителей других генотипов (p < 0.05). У D/D-гомозигот по гену АСЕ наблюдали и более длительное восстановление тонуса сосудов (по показателю ВРПВ) после апноэ (рис. 1).
Таблица 1.
Амплитуда систолической волны, pm
| Исследуемые гены | Варианты аллелей | Исходный фон Х ± m | Погружение Х ± m | Восстановление Х ± m |
|---|---|---|---|---|
| REN | GA, n = 23 | 2.20 ± 0.35 | 0.38 ± 0.06 | 1.20 ± 0.22 |
| GG, n = 43 | 1.27 ± 0.21**[GG–GA] | 0.35 ± 0.05 | 0.87 ± 0.15 | |
| ADBR2 | AA, n = 3 | 2.44 ± 0.37 | 0.51 ± 0.11 | 1.57 ± 0.52 |
| GA, n = 13 | 1.49 ± 0.30 | 0.29 ± 0.05*[ GA–GG] | 0.93 ± 0.24 | |
| GG, n = 22 | 1.72 ± 0.25 | 0.44 ± 0.06 | 1.03 ± 0.18 | |
| AA, n = 36 | 1.66 ± 0.29 | 0.35 ± 0.05 | 1.03 ± 0.19 |
Рис 1.
Время распространения пульсовой волны. По оси абсцисс – исследованные гены, по оси ординат – время в мс.
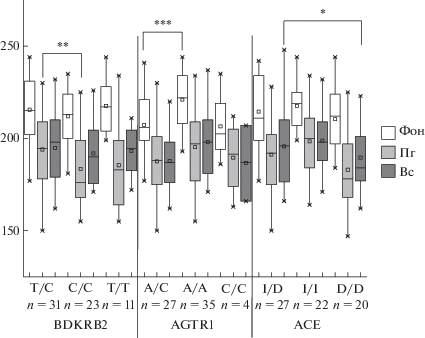
Сужение периферических сосудов при реализации нырятельной реакции происходит рефлекторно. Ведущая роль при этом принадлежит симпатическим норадренергическим влияниям на α- и β‑адренорецепторы периферических сосудов. Сила этих воздействий зависит от соотношения α- и β‑адренорецепторов, которое в большой мере детерминировано генетически. Вместе с тем существенное влияние на реализацию рефлекторных реакций оказывает текущий биохимический фон, который зависит, в частности, от активности ренин-ангиотензиновой и кинин-брадикининовой систем. Активность этих систем определяется полиморфными вариантами кодирующих их генов. Биохимический фон может либо потенцировать адренергические влияния, либо, напротив, уменьшать их выраженность, влияя, таким образом, на эффективность адаптивных реакций.
Список литературы
Баранова Т.И. Об особенностях сердечно-сосудистой системы при нырятельной реакции у человека. Рос. физиол. журн. им. И.М. Сеченова. 90 (1): 20–31. 2004. [Baranova T.I. Characteristics of the human cardiovascular system in the human diving response. Ros. fiziol. jurn. im. I.M. Sechenova. 90 (1): 20–31. 2004 (in Russ).].
Баранов В.С., Иващенко Т.Э., Глотов А.С. Баранова Е.В., Асеев М.В., Глотов О.С., Беспалова О.Н., Демин Г.С., Москаленко М.В., Швед Н.Ю. Генетический паспорт – основа индивидуальной и предиктивной медицины. СПб.: 2009. [Baranov V.S., Ivaschenko T.E., Glotov A.S., Baranova E.V., Aseev M.V., Glotov O.S., Bespalova O.N., Demin G.S., Moskalenko M.V. Shved N.Yu. Geneticheskii pasport osnova individualnoi i prediktivnoi medicini [The genetic passport is the basis for individual and predictive medicine]. SPb.: 2009].
Ахметов И.И. Молекулярная генетика спорта. М., 2009. [Akhmetov I.I. Molekulyarnaya genetika sporta [Molecular genetics of sport]. M. 2009].
Глотов А.С., Иващенко Т.Э., Образцова Г.И., Наседкина Т.В., Баранов В.С. Зависимость между возникновением стабильной артериальной гипертензии у детей и полиморфизмом генов ренин-ангиотензиновой и кинин-брадикининовой систем. Молекулярная биология. 41 (1): 18–25. 2007. [Glotov A.S., Ivaschenko T.E., Obrazcova G.I., Nasedkina T.V., Baranov V.S. Association of permanent arterial hypertension with the Renin-Angiotensin and Kinin-Bradykinin system genes in children. Molecular Biology. 41 (1):18–25. 2007. (In Russ).].
Образцова Г.И., Юрьев В.В., Глотов А.С., Иващенко Т.Э. Генетические аспекты формирования артериальной гипертензии у детей. Молекулярная медицина. 3: 32–35. 2013. [Obrazcova G.I., Yurev V.V., Glotov A.S., Ivaschenko T.E. Genetic aspects of arterial hypertension in children. Molecular medicine. 3: 32–35. 2013. (In Russ).].
Дополнительные материалы отсутствуют.
Инструменты
Журнал эволюционной биохимии и физиологии


