Физика металлов и металловедение, 2020, T. 121, № 4, стр. 365-373
Изучение термоциклического окисления двухфазных электроспеченных титаналюминиевых сплавов с добавками хрома, молибдена и кремния
a Кафедра металлургии и материаловедения, Технологический факультет,
Сакарьинский университет прикладных наук, кампус в Есентепе
54187 пров. Сакарья, Турция
* E-mail: oozdemir@sakarya.edu.tr
Поступила в редакцию 26.02.2019
После доработки 16.04.2019
Принята к публикации 22.10.2019
Аннотация
Интерметаллические сплавы Ti–48Al–2Cr–2Mo–(0 и 0.5 ат. %)Si были синтезированы спеканием при пропускании электрического тока (ЭТС). Аттестация микроструктуры сплавов выполнена с использованием растровой электронной микроскопии (РЭМ), энергодисперсионной спектроскопии (ЭДС) и рентгеноструктурного анализа (РСА). Было установлено, что микроструктура полученных сплавов представляла собой смесь фаз α2-Ti3Al и γ-TiAl. Цикл окислительного поведения сплавов проведен в температурном интервале от 700 до 900°C в воздушной среде при выдержке 180 ч. Шкала оксидов состояла из внутреннего слоя смеси TiO2 и Al2O3, промежуточного слоя Al2O3 и поверхностного слоя TiO2. Выполнен расчет энергии активации и констант скорости окисления сплавов.
ВВЕДЕНИЕ
Сплавы на основе TiAl являются перспективными материалами в сфере высокотемпературных приложений благодаря таким свойствам, как малый удельный вес, жаропрочность, высокие значения модуля упругости, температуры плавления, сопротивления в испытаниях на ползучесть, а также их относительно хорошая устойчивость к окислению. Комбинация этих свойств делает TiAl-сплавы привлекательными для высокотемпературных приложений, таких как авиационное турбиностроение и автомобильное моторостроение [1–3]. Доля сплавов на основе титана в современных авиационных двигателях достигает одной трети их общей массы, а в узлах и деталях газотурбинных установок указанная доля занимает второе место после суперсплавов на основе никеля [4]. Более того, эти материалы рассматриваются как потенциальные заменители суперсплавов на основе никеля [4]. Вместе с тем применение данных материалов ограничено из-за их неудовлетворительной пластичности при комнатных температурах, низкому сопротивлению ползучести и окислению при температурах выше 800°C [3, 5]. Легирующие добавки Nb, Ta, Mo, W и Si обеспечивают существенный вклад в повышение сопротивления к окислению сплавов на основе TiAl [4, 6, 7]. Такое повышение объясняют главным образом эффектом легирования, а также увеличением диффузионной подвижности атомов Al и их активности. Эффект легирования обусловлен снижением концентрации вакансий кислорода и подавлением его диффузии [6].
Процесс спекания при пропускании электрического тока (ЭТС метод) является консолидацией или процессом синтезом, при котором наряду с давлением прикладывается напряжение с протеканием электрического тока через порошок, помещенный в пресс-форму, или формуемый вхолодную компакт. Тепловыделение в этом процессе есть результат Джоулева эффекта при протекании электрического тока через материал, обладающий омическим сопротивлением. ЭТС-метод имеет ряд преимуществ в сравнении с традиционными методами спекания, такими как горячее прессование или спекание без приложения давления. Эти преимущества заключаются в более низкой температуре синтеза, меньшей продолжительности спекания, большей скорости нагрева, в исключении необходимости в “катализаторах” спекания, в меньшей чувствительности к выбору элементного состава порошковой смеси. При всем при этом, “плотность” ЭТС-синтезируемых материалов достаточно близка к значениям, предсказываемым теоретически [8–10].
Целью данной статьи является установление влияния ЭТС-метода синтеза сплавов на основе TiAl с малой добавкой Si на их поведение при термоциклическом окислении (ТЦО). Поведение интерметаллических сплавов Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si (ат. %) при ТЦО было исследовано на воздухе, в интервале температур от 700 до 900°C, при общей продолжительности ТЦО в 180 ч.
ПОДРОБНОСТИ ЭКСПЕРИМЕНТА
Приготовление образцов
Интерметаллические сплавы на основе TiAl номинального состава Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si (ат. %) были синтезированы ЭТС-методом (спекание при пропускании электрического тока). В состав смеси входили порошки титана (чистоты 99.5%, размер частиц 40 мкм), алюминия (99.5%, 10 мкм), хрома (99.8%, 5 мкм), молибдена (99.9%, 3 мкм) и кремния (99.9%, 5 мкм). Вес каждого порошка определялся путем взвешивания на электронных весах.
С целью получения гомогенной порошковой смеси порошки проходили предварительный размол в планетарной шаровой мельнице (ПШМ) с контейнером (К) и шарами из нержавеющей стали. Скорость вращения (К) 200 об./мин, продолжительность размола 4 ч, массовое отношение шаров к каждому из порошков составило 5 : 1. Затем 6 граммов порошковой смеси помещалось в стальную пресс-форму внутреннего диаметра 20 мм. Смесь порошков компактировали в пресс-форме при одноосном давлении 60 MПa в течение 1 мин. Компакт был синтезирован ЭТС-методом, прикладывая давление спекания 80 MПa, при электрическом токе 4200 А, в течение 35 мин на воздухе. Давление спекания поддерживали на указанном уровне вплоть до завершения технологического процесса. По окончании синтеза образец извлекали из стальной пресс-формы под действием одноосного давления и охлаждали до комнатной температуры.
Тест на термоциклическое окисление
Перед проведение ТЦО-теста исходная поверхность каждого из образцов проходила аттестацию с привлечением программных и аппаратных средств Корпорации “SolidWorks”. Затем образцы взвешивали на электронных весах, с погрешностью 0.01 мг. ТЦО-тесты проводили в резистивной электропечи при температурах 700, 800 и 900°C в течение 180 ч. Тест на окисление проводили на воздухе (во всех 15 циклах) и каждый цикл состоял из нагрева образцов до предписанной температуры, выдержке при ней в течение 12 ч, и охлаждения образца на воздухе до температуры окружающей среды. Изменение веса после каждого цикла окисление измеряли с помощью электронных весов с чувствительностью 0.01 мг. Более того, в каждом цикле проведено по два измерения, с последующим усреднением результата замеров. После этого образцы вновь помещали в печь для продолжения теста. Данную процедуру повторяли вплоть до окончания ТЦО-теста.
Аттестация
Фазовый состав образцов после ТЦО идентифицирован методами РСА на рентгеновском дифрактометре фирмы RIGAKU, в CuKα-излучении, при рабочем напряжении 40 кВ и токе 40 мA. Данные получены в диапазоне углов 2θ от 10 до 90°. Морфология продуктов окисления, локализованных в приповерхностном слое образцов и их поперечном сечении, исследована средствами растровой электронной микроскопии (РЭМ, микроскоп марки JEOL), а микроанализ производен методами энергодисперсионной спектроскопии (ЭДС). После проведения теста на окисление, изменение веса образца на единицу его поверхности (ΔW) оценивали по формуле:
где ΔW – изменение веса образца на единицу поверхности (мг см–2), Δm – изменение веса, A – площадь поверхности образца (cм2).РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Поведение при ТЦО
Кинетика термоциклического окисления на воздухе в течение 180 ч, сплавов Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si ат. % была изучена при температурах 700, 800 и 900°C. Кинетика окисления сплавов определена как зависимость веса образцов на единицу площади поверхности от времени окисления, представлена на рис. 1. Как можно видеть на рисунке, изменение веса образцов сплавов на основе TiAl при ТЦО возрастали с увеличением температуры. Температура ТЦО имела существенный эффект на изменении веса образцов, поскольку ее подъем приводил к возрастанию скорости окисления. После выдержки в течение 180 ч при 700, 800 и 900°C, суммарное изменение веса каждого из образцов составило ~1.4, 2.1 и 7.8 мг см–2 для сплава Ti–48Al–2Cr–2Mo и 0.85, 1.3 и 3.6 мг см–2 для сплава Ti–48Al–2Cr–2Mo–0.5Si соответственно. Для обоих сплавов весовые изменения в их образцах при 700°C оказались меньше 1.4 мг см–2, это означает, что окислении образцов при этой температуре незначительное. Для всех температур испытаний видно, что весовые изменения для сплава с добавкой кремния были в два раза меньше, чем для сплавов без Si. Было установлено, что сопротивление сплавов воздействию ТЦО возрастало с увеличением содержания Si. Указанное благотворное влияние добавки Si наблюдали также для других сплавов на основе интерметаллида TiAl [11, 12]. Наблюдали, что такие сплавы интенсивно окислялись на ранних стадиях ТЦО испытаний при всех тестированных температурах. Это можно объяснить адсорбцией атмосферного кислорода, сопровождающейся зарождением и ростом оксидов на ранних стадиях из-за того, что Ti и Al обладают высокой степенью сродства к кислороду. По мере развития окисления наблюдающееся последующее снижение его скорости предполагает, что слой, богатый оксидом алюминия, начинает контролировать этот процесс. Поскольку скорости диффузии и реакционоспособности возрастали с увеличением ТЦО-температуры, наиболее заметное изменение веса сплавов наблюдали при 900°C (рис. 1в). Более того, при ТЦО-испытаниях в области температур 700–900°C отслаивание слоя окалины в их процессе не наблюдали. Кинетика окисления сплавов была такова, что весовые изменения сплавов подчинялись следующему уравнению [13]:
где ΔW – изменение массы на единицу площади поверхности, kp – константа скорости окисления (мг2 см–4 ч–1), t – время экспозиции (ч), n – показатель степени в законе кинетики роста оксидов. Зависимости весовых изменений от корня квадратного от времени экспозиции для сплавов представлены на рис. 1а–1в. Кинетические кривые окисления были практически линейными при 700, 800 и 900°C, показывая, что процесс окисления подчиняется параболическому закону, n = 0.5. В теории Вагнера константа в квадратичном законе может быть представлена как функция коэффициента диффузии (КД) ионов металла из объема или КД атомов кислорода в объем через оксидный слой, и наименьшая диффузионная подвижность через оксидный слой является лимитирующей составляющей, контролирующей скорость окислительного процесса [13]. Линейный регрессивный анализ весовых изменений как функции времени был проведен на базе уравнения (4), используя пакет GraphPad Prism 7. Наклон “оптимального” графика может дать константу в законе для скорости протекания окислительного процесса в сплаве. Как показано в табл. 1, значения kp исследованных сплавов возрастают с ростом температуры. Это означает, что более высокая константа в законе скорости роста отражает более высокую скорость окисления. Было установлено, что константа в законе для скорости окисления уменьшается с добавлением Si, что говорит о благотворном влиянии Si на развитие устойчивости сплава к окислению.Рис. 1.
Графики “изменение веса–время окисления” и “изменение веса–корень квадратный из времени окисления” (образцов), снятые на сплавах Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si при ТЦО тестировании в течение 180 часов при температуре (a) 700, (б) 800 и (в) 900°C.
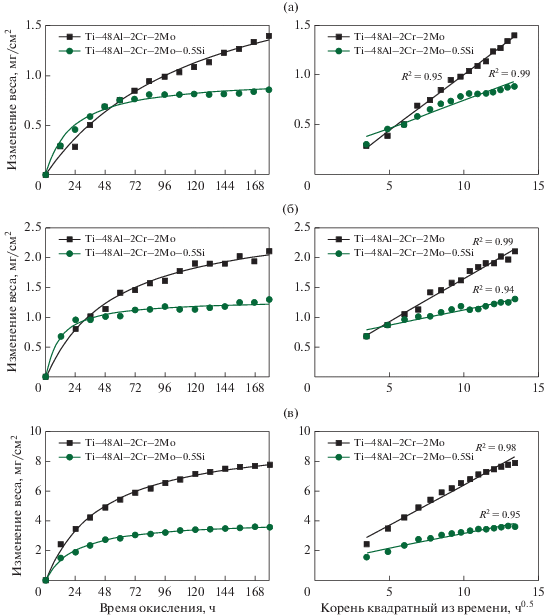
Таблица 1.
Значения константы в законе для скорости окисления (kp, мг2 см–4 ч–1) сплавов в течение 180 ч
| T, °C | Ti–48Al–2Cr–2Mo | Ti–48Al–2Cr–2Mo–0.5Si |
|---|---|---|
| 700 | 0.01087 | 0.00356 |
| 800 | 0.01857 | 0.00669 |
| 900 | 0.33315 | 0.06677 |
Предстепенная постоянная в законе изменения скорости окисления (kp) зависит от температуры протекания реакции и может быть представлена в уравнением Аррениуса:
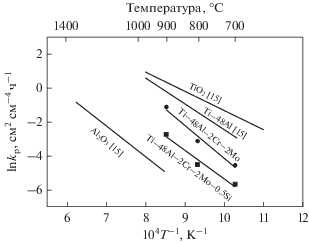
где k0 – константа, Q – энергия активации, R – газовая постоянная (8.314 Дж/(моль K)), T – абсолютная температура (K). Взяв логарифм от обеих сторон выражения, имеемЗначения постоянной в законе изменения скорости окисления (kp) наших сплавов мы сравнили с литературными экспериментальными данными, результаты представлены на рис. 2. Можно видеть, что значения kp для сплавов Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si располагаются между значениями для Al2O3 и TiO2. Энергию активации можно вычислить по наклону графика линейной регрессии ln(kp) от 1/T. Значения энергии активации (диффузии) в наших сплавах и сплавах на основе TiAl, взятые из литературных источников, представлены в табл. 2. Значения энергии активации для сплавов Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si оказались меньше, чем для сплава Ti–45.9Al–8Nb, но больше, чем для сплавов Ti–48Al–2Cr–2Nb и Ti–48Al–2Cr–2Nb–(0.5–1)W. Это может быть связано с температурой ТЦО, составом атмосферы выдержки, исходной микроструктурой сплава, эффектом от легирующих компонентов и степенью совершенства поверхности образцов.
Рис. 2.
Кинетика формирования оксидов в сплавах Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si в сравнении с ранее опубликованными данными авторов [15].
Состав и морфология продуктов окисления
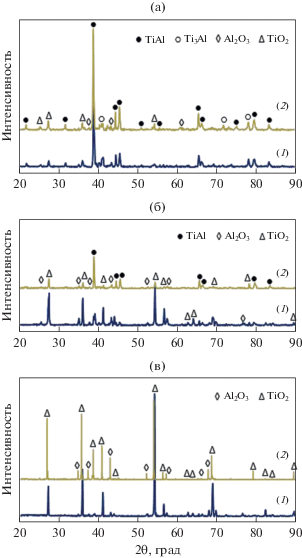
Присутствие продуктов ТЦО-окисления (ПО) было отмечено на всех поверхностях образцов сплавов, выдержанных при 800 и 900°C. Вместе с тем, при 700°C ПО не было зафиксировано. Результаты РСА образцов сплавов Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si (ат. %) после их ТЦО при 700, 800 и 900°C в течение 180 ч (в каждом случае) представлены на рис. 3. РСА показал, что поверхности образцов сплавов после ТЦО при всех температурах и экспозиции 180 ч были покрыты оксидными пленками TiO2 и Al2O3. Вследствие неоднородности и небольшой толщины сформировавшегося оксидного слоя можно было наблюдать присутствие фаз TiAl и Ti3Al. После ТЦО-выдержки при 700°C была идентифицирована Ti3Al-фаза, но после выдержки при 800 и 900°C ее следы на рентгенограммах отсутствовали. По-видимому, это явилось результатом окисления Ti3Al до TiO2 с увеличением температуры. При 800°C, интенсивность рефлексов от фаз TiO2 и Al2O3 возросла, что является результатом увеличения толщины оксидного слоя с увеличением температуры ТЦО-тестов. На рис. 3в можно видеть, что сформировавшийся при 900°C оксидный слой состоял из фаз TiO2 и Al2O3 в обоих сплавах. Из-за его достаточной толщины фаза TiAl не была детектирована при РСА.
Рис. 3.
Рентгенограммы сплавов на основе TiAl после ТЦО в течение 180 ч при (a) 700, (б) 800 и (в) 900°C: Ti–48Al–2Cr–2Mo (1), Ti–48Al–2Cr–2Mo–0.5Si (2) (ат. %).
Более того, оксиды легирующих элементов (Cr, Mo и Si) не были зафиксированы из-за их растворения в оксидной пленке. Следы от оксидов Si на рентгенограммах отсутствовали из-за того, что концентрация Si была недостаточной для того, чтобы сформировать отдельный слой SiO2 или слой из островков SiO2 в сформированном оксидном слое. Морфология оксидированных поверхностей сплавов после ТЦО при 700°C в течение 180 ч представлена на рис. 4. На рис. 4а, 4б можно видеть, что изображение поверхности образцов сплавов Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si (ат. %) состоит из темных (отмечены как 1 и 3) и серых (2 и 4) участков разных фаз. Химический состав участков установлен ЭДС-анализом (табл. 3) и отмечены присутствием титана, алюминия и кислорода. Из табл. 3 видно, что содержание O в богатых Al участках поверхности (TiAl) было пониженным. Из-за высокой растворимости кислорода в α2-Ti3Al-фазе можно полагать, что данные участки подверглись более быстрому окислению, чем участки γ-TiAl-фазы [16]. Более того, указанное различие в скоростях окисления было обусловлено большим различием в содержании Ti и Al в фазах α2-Ti3Al и γ-TiAl. Поскольку содержание Ti в фазе α2-Ti3Al значительно больше, чем в фазе γ-TiAl, то фаза α2-Ti3Al быстро продуцировала TiO2 в условиях высоких температур [17]. Согласно результатам РСА (см. рис. 3), оксиды Ti и Al, сформировавшие эти участки поверхности, были идентифицированы как TiO2 и Al2O3 фазы. Кроме того, из рис.4a видно, что продуктов окисления, образовавшихся на поверхностях образцов сплава Ti–48Al–2Cr–2Mo, было больше чем в другом сплаве. Как показано на рис. 1a, это сказалось на кинетических кривых оксидированных сплавов. Оксиды (отмечены как (1)), которые дополнительно сформировались на поверхности образцов сплавов, были неоднородно распределены в кластерах (см. рис. 3a). Тем самым, поверхности сплава имела нерегулярную морфологию. Результаты РЭМ-микроскопии области кластеризации (ОК) представлены на рис. 4a. Можно видеть, что ОК включала дисперсные оксиды с кристаллами округлой формы.
Рис. 4.
РЭМ-изображения поверхности сплавов после ТЦО при 700°C в течение 180 ч; (a) Ti–48Al–2Cr–2Mo и (б) Ti–48Al–2Cr–2Mo–0.5Si (ат. %). Точками очерчены области, прошедшие ЭДС-анализ. На вставках – их детали.

Таблица 3.
Химический состав (в ат. %) окисных участков, отмеченных на рис. 4
| ×Точки | Элемент | |||||
|---|---|---|---|---|---|---|
| O | Ti | Al | Cr | Mo | Si | |
| 1 | 57.9 | 25.2 | 16.6 | 0.2 | 0.1 | – |
| 2 | 38.2 | 28.4 | 32.8 | 0.3 | 0.2 | – |
| 3 | 51.4 | 27.7 | 19.3 | 0.9 | 0.5 | 0.2 |
| 4 | 43.2 | 26.5 | 29.6 | 0.4 | 0.2 | 0.1 |
Поверхность оксидированных образцов сплава Ti–48Al–2Cr–2Mo–0.5Si была более гладкой, чем сплава без Si (рис. 4б). Большее увеличение помеченных областей показало, что поверхность сплава состоит из оксидов с решетчатой структурой.
Принимая в расчет то, что оксидная (островковая) пленка образуется на поверхности сплавов на основе TiAl при высокой температуре после ранней стадии, двуокись титана TiO2 формирует внешний оксидный слой, поскольку растущие с более высокой скоростью зерна TiO2 перекрывают зерна Al2O3 [17]. Как можно видеть из рис. 5, после выдержки при температурах 800 и 900°C, морфология поверхности сплавов была совершенно другая в сравнении с 700°C, а поверхности содержали больше продуктов окисления. Также было отмечено, что частицы оксидов на некоторых участках росли быстрее, чем в других местах, что в итоге привело к неоднородной морфологии поверхностей. Согласно данным ЭДС анализа (табл. 4) областей, в которых быстро растущие зерна обозначены как (×2) и (×3) на рис. 5а, 5б, эти зерна формировались из оксида Ti. Вместе с тем, результаты ЭДС-анализа областей с более медленным ростом оксидов (помечены как ×1) показали, что эти области были обогащены алюминием. Как можно видеть на рентгенограммах (см. рис. 3б), оксиды алюминия и титана, формирующие эти области, были идентифицированы как Al2O3 and TiO2.
Рис. 5.
РЭМ-изображения поверхностей сплавов (a) Ti–48Al–2Cr–2Mo и (б) Ti–48Al–2Cr–2Mo–0.5Si (ат. %) после ТЦО при 800°C в течение 180 ч. В точках (×) был проведен ЭДС-анализ. На вставках приведены детали морфологии оксидов.

Таблица 4.
Химический состав (в ат. %) оксидных “фрагментов” поверхности в точках, отмеченных на рис. 5
| ×Точки | Элемент | |||||
|---|---|---|---|---|---|---|
| O | Ti | Al | Cr | Mo | Si | |
| 1 | 52.3 | 14.1 | 32.8 | 0.6 | 0.2 | – |
| 2 | 65.1 | 33.3 | 1.4 | 0.1 | 0.1 | – |
| 3 | 63.7 | 33.6 | 2.1 | 0.3 | 0.2 | 0.1 |
Кроме того, отмеченные участки поверхности при большем увеличении (рис. 5a, 5б) показывают, что крупнозернистые оксиды титана имели полиэдрическую огранку. Как можно судить по рис. 6а, 6б, увеличение температуры до 900°C привел к увеличению скорости окисления, что, в свою очередь, повлекло за собой укрупнение зерен оксида титана. После окисления при 800 и 900°C различия в морфологии поверхностных оксидов отсутствовали, чего нельзя сказать о размере их зерен.
Рис. 6.
РЭМ-изображения поверхностей сплавов (a) Ti–48Al–2Cr–2Mo и (б) Ti–48Al–2Cr–2Mo–0.5Si (ат. %) после ТЦО при 900°C в течение 180 ч. В точках (×) был проведен ЭДС-анализ. На вставках приведены детали морфологии оксидов.

Таблица 5.
Химический состав (в ат. %) оксидной шкалы поверхности в точках, отмеченных на рис. 6
| Элемент | ||||||
|---|---|---|---|---|---|---|
| ×Точки | O | Ti | Al | Cr | Mo | Si |
| 1 | 60.3 | 39.1 | 0.4 | 0.1 | 0.1 | – |
| 2 | 59.4 | 38.8 | 0.5 | 0.1 | 0.1 | 0.1 |
Аналогично, зерна оксида титана, сформировавшиеся при 900°C, обладали столбчатоподобной структурой. Подобные результаты были получены целым рядом авторов [15, 16, 18]. Можно видеть по РЭМ-изображениям при большем увеличении, что имеет место увеличение послойного роста оксидных частиц при 900°C в сравнении с 800°C. Покрытие поверхности относительно крупными зернами оксида Ti при повышении температуры окисления приводит к увеличению интенсивности дифракционного пика TiO2 на рентгенограммах (см. рис. 3в).
Вследствие того факта, что слой Al2O3 лежал под слоем TiO2 на оксидной шкале, отсутствие значительного роста интенсивности пика от Al2O3 при 900°C может быть объяснено более быстрым ростом зерен оксида титана, – в их сравнении с температурой 800°C. Как можно судить по рис. 1в, изменение веса увеличивается при увеличении температуры ТЦО. Этот вывод подтверждается результатами РЭМ-микроскопии.
Микроструктура в поперечных сечениях образцов
После ТЦО при 900°C в течение 180 ч, микроструктура в поперечных срезах образцов сплавов показана на рис. 7.
Рис. 7.
РЭМ-изображения микроструктуры в поперечных сечениях оксидного слоя сплавов (a) Ti–48Al–2Cr–2Mo и (б) Ti–48Al–2Cr–2Mo–0.5Si после ТЦО при 900°C в течение 180 ч.

Микроструктура в поперечном сечении образцов сплавов после ТЦО при 700°C не представлена из-за крайне малой толщины окисного слоя. ЭДС анализ показал, что островковый оксидный слой на поверхности ТЦО образцов состоял из внутреннего смешанного слоя TiO2 + Al2O3, промежуточной прослойки из Al2O3 и внешнего слоя TiO2.
Поскольку содержание титана было недостаточно для образования самого внешнего слоя TiO2, промежуточный слой из Al2O3 формировался благодаря возрастанию активности алюминия в пространстве под этим слоем. Поскольку Al2O3 включает меньшее количество дефектов структуры и проходов в сравнении с TiO2, что затрудняет диффузию анионов кислорода через этот слой [3, 17]. Под слоем Al2O3 находился смешанный слой, включавший в себя “неизолирующий” слой двуокиси титана и слой островкового оксида Al2O3. Состав окисного слоя образцов ТЦО исследованных сплавов был определен как TiO2 + Al2O3/Al2O3/TiO2 – в последовательности из объема к поверхности образца, составляющие его оксиды являются наиболее часто встречающимися в сплавах TiAl.
Поскольку Al2O3 не является препятствием для проникновения ионов как O, так и Ti, внутренний смешанный слой и самый внешний слой TiO2 будут продолжать развиваться. Из рис. 7а, 7б можно заключить, что внешний слой из TiO2 растет медленнее, чем внутренний смешанный оксидный слой. После ТЦО наших сплавов при 800 и 900°C в течение 180 ч, средняя толщина оксидных слоев проиллюстрирована на рис. 8. Для того чтобы определить толщину суммарного окисного слоя, было проведено РЭМ-исследование трех различных участков поверхности ТЦО-образцов каждого сплава. Было установлено, что на толщину суммарного оксидного слоя существенно влиял смешанный оксидный слой поскольку он был достаточно толстый. Более того, толщина оксидных слоев возрастала с подъемом температуры ТЦО от 800 до 900°C. Например, в обоих сплавах наблюдали трехкратное увеличение толщины суммарного оксидного слоя при увеличении температуры от 800 до 900°C.
Рис. 8.
Средняя толщина оксидных слоев, образовавшихся на поверхности ТЦО образцов сплавов (a, в) Ti–48Al–2Cr–2Mo и (б, г) Ti–48Al–2Cr–2Mo–0.5Si.
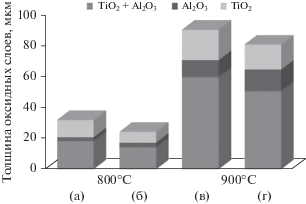
Было установлено, что толщина оксидного слоя в образцах с добавкой Si была несколько меньше в сравнении с другими сплавами. Такое поведение можно объяснить большей толщиной “защитного” слоя Al2O3. Таким образом, Si можно расценивать как “полезный” легирующий элемент. Тем не менее, этот Al2O3 слой не препятствует ни направленной внутрь диффузии атомов кислорода, ни направленной вовне диффузии ионов титана.
Кроме того, измеренная толщина оксидного слоя хорошо согласуется с результатами изменения веса (см. рис. 1). Ближайшие к поверхности слои TiO2, показанные на рис. 7а, 7б, формировались в процессе направленной вовне диффузии ионов титана [18]. Подъем температуры ТЦО ускоряет направленную вовне диффузии ионов титана, что, в свою очередь, приводит к образованию слоя TiO2 значительно быстрее в сравнении со случаем 800°C.
ЗАКЛЮЧЕНИЕ
Поведение сплавов на основе TiAl в ходе термоциклического окисления (ТЦО) было изучено при температурах 700–900°C и продолжительности ТЦО в 180 ч на воздухе. Изменение веса образцов Ti–48Al–2Cr–2Mo–0.5Si было всегда меньше в сравнении с Ti–48Al–2Cr–2Mo при всех исследованных температурах ТЦО. Сплавы с добавкой Si продемонстрировали лучшую устойчивость к окислению, чем сплавы без Si. Значения энергий активации для сплавов Ti–48Al–2Cr–2Mo и Ti–48Al–2Cr–2Mo–0.5Si равны 160 и 137 кДж моль–1 соответственно.
Состав и структура сформировавшейся оксидной пленки на поверхности сплавов были подобными в обоих случаях. После ТЦО при 800 и 900°C, на поверхности образцов возникла трехслойная оксидная пленка, состоявшая из прослоек TiO2 + Al2O3/Al2O3/TiO2 по направлению из объема к поверхности.
Список литературы
Ye S., Hao H., Mo W., Yu K., Litao L., Deng C., Yu P. Effects of cold compacting pressure on the expansion behavior of Ti–48Al during sintering // J. Alloy Compd. 2016. V. 673. P. 399–404.
Zhang Z., Xu M., Zhang C.Z., Han J.C., Chen Y.F., Kong F.T., Chen Y.Y. Microstructure Homogeneity and Mechanical Properties of Large-Size As-Cast High Nb Containing TiAl Alloy Ingot // Phys. Met. Metallogr. 2018. V. 119. № 9. P. 953–960.
Garip Y., Ozdemir O. Comparative study of the oxidation and hot corrosion behaviors of TiAl-Cr intermetallic alloy produced by electric current activated Sintering // J. Alloy Compd. 2019. V. 780. P. 364–377.
Banu A., Marcu M., Petrescu S., Ionescu N., Paraschiv A. Effect of niobium alloying level on the oxidation behavior of titanium aluminides at 850°C // Int. J. Min. Met. Mater. 2016. V. 23. № 12. P. 1452–1457.
Liu C., Lu X., Yang F., Xu W., Wang Z., Qu X. Metal Injection Moulding of High Nb-Containing TiAl Alloy and Its Oxidation Behavior at 900°C // Metals. 2018. V. 8. P. 1–14.
Brotzu A., Felli F., Pilone D. Effect of alloying elements on the behavior of TiAl-based alloys // Intermetallics. 2014. V. 54. P. 176–180.
Kim D.J., Seo D.Y., Saari H., Sawatzky T., Kim Y.-W. Isothermal oxidation behavior of powder metallurgy beta gamma TiAl–2Nb–2Mo alloy // Intermetallics. 2011. V. 19. P. 1509–1516.
Grasso S., Sakka Y., Maizza G. Electric current activated/assisted sintering (ECAS): a review of patents 1906–2008, Sci. Technol. Adv. Mater. // 2009. V. 10. P. 1–24.
Garip Y., Ozdemir O. Hot Corrosion Behavior of Ti–48Al and Ti–48Al–2Cr Intermetallic Alloys Produced by Electric Current Activated Sintering // Metall. Mater. Trans. A. 2018. V. 49A. P. 2455–2462.
Orru R., Licheri R., Locci A.M., Cincotti A., Cao G. Consolidation/synthesis of materials by electric current activated/assisted sintering // Materials Science and Engineering R. 2009. V. 63. P. 127–287.
Lee D.-B. Effect of Cr, Nb, Mn, V, W and Si on High Temperature Oxidation of TiAl Alloys // Met. Mater. Int. 2005. V. 11. № 2. P. 141–147.
Shida Y., Anada H. The Effect of Various Ternary Additives on the Oxidation Behavior of TiA1 in High-Temperature Air // Oxid. Met. 1996. V. 45. № 1–2. P. 197–219.
Li H., Cao Q. Zhu Z. Oxidation behavior of Super 304H stainless steel in supercritical water. // Corros. Eng. Sci. Techn. 2008. V. 53. № 4. P. 293–301.
Godlewska E., Mitoraj M., Devred F., Nieuwenhuys B.E. Reactivity of a Ti–45.9Al–8Nb alloy in air at 700–900°C // J. Therm. Anal. Calorim. 2007. V. 88. № 1. P. 225–230.
Seo D.Y., Nguyen T.D., Lee D.B. Oxidation of Powder Metallurgy (PM) Ti–48% Al–2% Cr–2% Nb–(0–1%) W Alloys between 800 and 1000°C in Air // Oxid. Met. 2010. V. 74. P. 145–156.
Kothari K., Radhakrishnan R., Wereley N.M. Advances in gamma titanium aluminides and their manufacturing techniques // Prog. Aerosp. Sci. 2012. V. 55. P. 1–16.
Liu X., You K., Wang Z., Zhang M., He Z. Effect of Mo-alloyed layer on oxidation behavior of TiAl-based alloy // Vacuum. 2013. V. 89. P. 209–214.
Kim D.J., Seo D.Y., Yang Q., Saari H., Sawatzky T. Kim Y.-W. Isothermal oxidation behaviour of beta gamma powder metallurgy TiAl–4Nb–3Mn alloys // Can. Metall. Quart. 2011. V. 50. № 4. P. 416–424.
Дополнительные материалы отсутствуют.
Инструменты
Физика металлов и металловедение


