Физика металлов и металловедение, 2020, T. 121, № 8, стр. 842-848
Синтез, структура и свойства материала на основе MAX-фазы V2AlC
В. А. Горшков a, *, А. В. Карпов a, Д. Ю. Ковалев a, А. Е. Сычев a
a Институт структурной макрокинетики и проблем материаловедения им. А.Г. Мержанова РАН
142432 Черноголовка,
ул. Академика Осипьяна, 8, Россия
* E-mail: gorsh@ism.ac.ru
Поступила в редакцию 20.02.2020
После доработки 28.04.2020
Принята к публикации 30.04.2020
Аннотация
Впервые методом самораспространяющегося высокотемпературного синтеза (СВС) получен материал на основе МАХ-фазы V2AlC с использованием реакционной смеси порошков оксидов ванадия(V) и (IV), с алюминием и углеродом (графитом). Полученный материал охарактеризован методами рентгенофазового и микроструктурного анализов. Количественный анализ выполнен методом Ритвельда. Синтезированный материал на основе МАХ-фазы V2AlC является электрическим проводником, демонстрирующим металлический характер проводимости во всем измеренном диапазоне температур 300–1300 К в вакууме 2 × 10–3 Па. Высказано предположение, что определяющий вклад в электросопротивление синтезированного материала, вносит фаза V2AlC, что может быть связано с образованием контактирующих между собой в объеме материала наноламинатных зерен V2AlС.
ВВЕДЕНИЕ
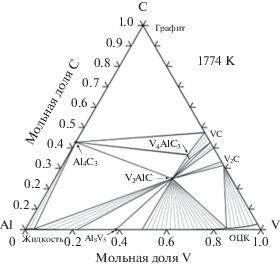
Фазовая диаграмма V–Al–C впервые исследована в работе [1], где было показано существование тройной фазы V2AlC. Позже была синтезирована высокотемпературная фаза V4AlC3 [2, 3]. Оба соединения V2AlC и V4AlC3 принадлежат к группе фаз Mn + 1AXn (или MAX-фаз), где M – переходный металл, А – элемент группы А (в основном группа IIIA и IVA), X – либо C, либо N. Фаза V4AlC3 устойчива при температуре выше 1392 К и на изотермическом сечении при 1773 K [4]. На рис. 1 показаны области существования двух фаз V2AlC и V4AlC3 и небольшого диапазона твердых растворов при 1773 К. При этой температуре видна некоторая растворимость С в ОЦК. Растворимость углерода постепенно уменьшается с увеличением содержания Al. В результате формирования слоистой структуры эти соединения проявляют интересные свойства: они эластично жестки, легко обрабатываются, термостойки. Эти материалы также являются электропроводящими. Компактный материал на основе V2AlC был синтезирован методами горячего изостатического прессования (HIP) [5], магнетронного распыления [6] и горячего прессования [7]. В работе [8] материал на основе V2AlC был получен методом СВС из смеси элементарных порошков V, Al и C. Адиабатическая температура системы 2V–Al–C составляет 2767 К. Синтезированный продукт в режиме теплового взрыва состоит из V2AlC и небольшого количества VCx и AlV3, при этом зерна V2AlC имеют форму ламелей длиной 10 мкм. В работе предложен механизм реакции синтеза V2AlC, который предполагает, что V2AlC может быть образован из жидкого раствора V–Al и твердого VC.
Эти соединения имеют высокие температуры плавления более 1973 K, но низкую стойкость к окислению из-за образования расплавов оксидов уже при 973 K в воздухе. Известно [9], что титан, хорошо растворяющийся в ванадии, может находиться как в твердом растворе V–Al в заметных количествах, так и в форме тройного интерметаллида V2TiAl [10], дифракционные максимумы которого совпадают с линиями твердого раствора V(Al).
Среди хорошо изученных МАХ-фаз Ti2AlC, V2AlC, Cr2AlC и Nb2AlC, V2AlC имеет самый большой коэффициент остаточного сопротивления – RRR [RRR = ρ(300 R)/ρ(5 K) равный 6.5 [11]. Электросопротивление тройного соединения V2AlC, полученное в [12], составляет ρ = 0.8 мкОм при комнатной температуре, что более чем в два раза выше, чем в работе [11]. Такое отличие объясняется способом получения материала, а также наличием примесей, размером зерен и структурной однородностью [12].
В данной работе впервые методом самораспространяющегося высокотемпературного синтеза (СВС) с использованием смеси порошков оксидов ванадия(V) и (IV), алюминия и углерода получен материал на основе МАХ-фазы V2AlC, исследован его фазовый состав, микроструктура и электропроводность в интервале температур от 300 до 1300 К. Ранее этим способом были успешно синтезированы материалы на основе MAX фазы Cr2AlC [13, 14] и Nb2AlC [15].
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Для получения образцов использовали смеси порошков оксида ванадия(V) и оксида ванадия(IV) марки “Ч”, алюминия марки АСД–1 и углерод (графит). Расчет соотношений компонентов исходных смесей производили, используя следующие химические реакции:
(I)
${\text{3}}{{{\text{V}}}_{{\text{2}}}}{{{\text{O}}}_{5}} + 13{\text{Al}} + 3{\text{C}} = 3{{{\text{V}}}_{{\text{2}}}}{\text{AlC}} + 5{\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{3}};$(II)
$6{\text{V}}{{{\text{O}}}_{2}} + 11{\text{Al}} + 3{\text{C}} = 3{{{\text{V}}}_{{\text{2}}}}{\text{AlC}} + 4{\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{3}};$(III)
$4{{{\text{V}}}_{{\text{2}}}}{{{\text{O}}}_{5}} + 2{\text{V}}{{{\text{O}}}_{2}} + 21{\text{Al}} + 5{\text{C}} = {{{\text{V}}}_{{\text{2}}}}{\text{AlC}} + 8{\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{3}}.$Содержание каждого компонента (ai) рассчитывали по формуле: ai = mi/M, где mi – молекулярный вес компонента, М – молекулярный вес всех компонентов смеси.
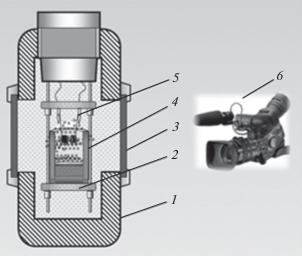
Перед проведением экспериментов все реагенты просушивали в сушильном шкафу (СНОЛ) в течение 3 ч при температуре 330 К. Исходные смеси массой 30 г готовили вручную в фарфоровой ступке. При изучении закономерностей синтеза и процессов формирования состава и микроструктуры продуктов синтеза реакционные смеси сжигали в кварцевых или графитовых тиглях диаметром 25–30 мм, высотой 55–60 мм. В экспериментах тигель с реакционной шихтой насыпной плотности помещали в СВС-реактор, объемом V = 3 л (рис. 2).
Рис. 2.
Схема СВС-реактора: 1 – корпус, 2 – основание, 3 – окна для наблюдений, 4 – кварцевый тигель с образцом, 5 – инициирующая спираль, 6 – видеокамера.
Для проведения экспериментов реактор герметизировали, создавали избыточное давление (Рн = 5 МПа) инертного газа (Ar) и воспламеняли исходную смесь с помощью металлической спирали (Mo, NiCr) путем подачи на нее напряжения U = 30 В. Процесс горения изучали визуально, а также с помощью видеокамеры. Среднюю линейную скорость рассчитывали по формуле Нсм/tг, где Нсм – высота смеси, tг – время сгорания всего образца. Выход целевого продукта в слиток (η1) относительно массы смеси рассчитывали по формуле η1 = Мсл/Мсм × 100%, выход целевого продукта в слиток (η2) относительно расчетного значения η2 = ${{{{М}_{{{\text{сл}}}}}} \mathord{\left/ {\vphantom {{{{М}_{{{\text{сл}}}}}} {М_{{{\text{сл}}}}^{{{\text{расч}}}}}}} \right. \kern-0em} {М_{{{\text{сл}}}}^{{{\text{расч}}}}}}$ × 100%, потерю массы (диспергирование) при горении η3 = (Мн – Мк)/Мн × 100%, где Мсл – масса целевого продукта, Мсм – масса исходной смеси, $М_{{{\text{сл}}}}^{{{\text{расч}}}}$ – масса слитка, рассчитанная из состава смеси, Мн – начальная масса, Мк – конечная масса. Адиабатическую температуру горения рассчитывали с использованием программы термодинамического расчета “THERMO” [16]. Фазовый состав продуктов синтеза исследован методом рентгенофазового анализа (РФА) на дифрактометре ДРОН-3М на излучении Cu с монохроматором на вторичном пучке. Съемка велась в режиме пошагового сканирования в интервале углов 2θ = 10°–100° с шагом съемки 0.02° и экспозицией 2 с. Количественный анализ выполнен методом Ритвельда в программном комплексе [17], используя известные структурные данные фаз. В качестве исходной модели для уточнения брали структурные данные соединений, приведенные в Crystallography Open Database и Materials Project [18, 19]. Исследование микроструктуры поверхности излома образцов проводили на сканирующем электронном микроскопе LEO 1450
VP, CarlZeiss и системы энергодисперсионного микроанализа INCA Energy SEM 300, Oxford Instrument.
Для проведения электрофизических измерений из образцов, синтезированных в графитовых тиглях (п. 4, табл. 1), вырезали образцы прямоугольного сечения размером 1.5 × 1.5 × 15.0 мм3. Для снятия остаточных напряжений перед проведением измерений исследуемые образцы подвергали термообработке в вакууме в течение 30 мин при температуре 1300 К. Измерения удельного электросопротивления проводили в диапазоне температур 300–1300 K в вакууме 2 × 10–3 Па по стандартной 4-точечной методике [20] при постоянном токе. Скорость изменения температуры при цикле нагрев/охлаждение составляла 10 К/мин.
РЕЗУЛЬТАТЫ ЭКСПЕРИМЕНТОВ И ОБСУЖДЕНИЕ
В процессе горения исходных смесей со стехиометрическим соотношением реагентов, рассчитанным из формулы (I), было обнаружено, что смеси горят в нестационарном режиме с искривленным фронтом и сильным диспергированием (выбросом) конечных продуктов из реакционного тигля. При горении исходных смесей со стехиометрическим соотношением реагентов, рассчитанным из формулы (II), было обнаружено, что после воспламенения смеси происходила остановка фронта горения. При горении исходных смесей со стехиометрическим соотношением реагентов, рассчитанным из формулы (III), было обнаружено, что смеси горят в стационарном режиме с практически плоским фронтом распространения волны горения.
В процессе горения продукты синтеза находятся в жидкофазном состоянии и из-за различного удельного веса, под действием гравитации разделяются на два слоя: нижний – металлоподобный (V2AlC), верхний – оксидный (Al2O3). Эти слои не имеют прочного сцепления и легко отделяются друг от друга при механическом воздействии (ударе). Внешний вид конечных продуктов синтеза представлен на рис. 3. Плотность материала, образующего нижний металлоподобный слой, составляет 4.85 г/см3. Составы исходных реакционных смесей, и параметры синтеза и составы конечных продуктов приведены в табл. 1.
Рис. 3.
Вид конечных продуктов синтеза из смесей, соотношение реагентов которых рассчитывали по формуле (III): 1 – оксидный (Al2O3) и 2 – металлоподобный (V–Al–C)-слои.

Таблица 1.
Составы реакционных смесей, параметры синтеза и составы конечных продуктов
| № | Шихта | Материал тигля | Uг, см/с | η1, вес. % | η2, вес. % | η3, вес. % | Фазовый состав |
|---|---|---|---|---|---|---|---|
| 1 | 3V2O5/13Al/3C | Кварц | 4.5 | 30.2 | 83.2 | 7.8 | V2AlC, VCx, VAl, VAl3, V2C, V5Si3 |
| 2 | 6VO2/11Al/3C | Кварц | – | 0 | 0 | 0 | – |
| 3 | 4V2O5/2VO2/21Al/5C | Кварц/графит | 1.2 | 39.1 | 88.3 | 5.3 | V2AlC, VCx, V2C, VAl, VAl3, V5Si3 |
| 4 | 4V2O5/2VO2/21Al/5C | Графит | – | 38.5 | 87.5 | 5. 1 | V2AlC, VCx, V2C, VAl, VAl3 |
Проведенные эксперименты показали, что:
– смесь, состав которой рассчитывали по формуле (I), является самой экзотермической. Для этой системы расчетная адиабатическая Тг составляет 2890 К. Горение протекает с высокой скоростью и большим выбросом (диспергированием) конечных продуктов из тигля. Из-за больших потерь массы конечных продуктов (η3 = 7.8%) выход целевого продукта сравнительно невысокий (табл. 1, п. 1);
– смесь, состав которой рассчитывали по формуле (II), является менее экзотермической по сравнению с предыдущей (I). Расчетная адиабатическая Тг в этом случае составляет 2720 К. Инициировать СВС-реакцию в образце данного состава при помощи электрической спирали не удалось. После воспламенения с помощью поджигающего состава (3CaO2/Al) через 15–20 мм прохождения фронта происходит затухание (табл. 1, п. 2);
– смесь, состав которой рассчитывали по формуле (III), горит в стационарном режиме и с небольшим диспергированием. Расчетная адиабатическая горения Тг данного состава составляет 2800 К (табл. 1, п. 3 и 4).
Рентгенофазовый анализ показал (рис. 4), что в синтезированном материале, наряду с основной фазой V2AlC, содержатся карбидные и интерметаллидные фазы ванадия (табл. 2).
Рис. 4.
Дифрактограмма образца, синтезированного в кварцевом тигле с графитовым дном из смеси, состав которой рассчитан по формуле (III).
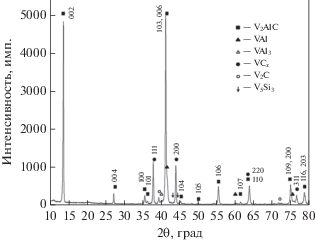
Таблица 2.
Составы реакционных смесей, параметры синтеза и составы конечных продуктов
| Фаза | V2AlC | VCх | V2C | VAl | VAl3 | V5Si3 |
|---|---|---|---|---|---|---|
| Пр. группа | P63/mmc | Fm–3m | Pbcn | Im3m | I4/mmm | P63/mcm |
| мас. % | 65 | 22 | 6 | 4 | 2 | 1 |
Содержание МАХ-фазы V2AlC составило 65%. Основной примесной фазой является VCх, причем образовавшийся карбид не является стехиометрическим. Дифракционные линии VCх существенно сдвинуты относительно VC в область больших углов, т.е. он характеризуется меньшим параметром элементарной ячейки, что свидетельствует о заселенности позиций атомов углерода в ячейке менее 1.
Также обнаружено незначительное количество интерметаллидных фаз VAl3 и VAl. На дифрактограмме присутствуют линии V5Si3 (рис. 4). Ввиду отсутствия кремний-содержащих фаз в составе исходной смеси, очевидно, что образование V5Si3 связано с взаимодействием расплава конечного продукта с кварцем, из которого был изготовлен контейнер. Видно, что основной фазой синтезированного продукта является MAX-фаза V2AlC. Дифракционные линии фазы V2AlC узкие, что указывает на высокую степень совершенства ее структуры, сформировавшейся в условиях кристаллизации из жидкой фазы.
В широком интервале температур существуют две фазы карбидов ванадия, имеющие широкие области гомогенности: кубическая модификация VC1 – x, устойчивая от комнатной температуры до точки ее плавления 3070 К с граничным максимальным содержанием углерода ~VC0.88, и фаза V2C1 – x, устойчивая также до температуры ее плавления 2460 К. Все вышеуказанные температуры имеют значения ниже адиабатической температуры горения 2800 К, рассчитанной для исследуемого состава.
Типичные микрофотографии поперечного сечения и поверхности разрушения образца, полученного в кварцевом тигле с графитовым дном из смеси, состав которой рассчитан по формуле (III), представлены на рис. 5 и 6. Структура материала беспористая, “пачки” наноламинатных зерен V2AlC находятся в плотном контакте между собой. Видно, что материал имеет слоистую наноламинантную структуру, характерную для MAX-фаз [7] с размером зерен фазы V2AlC 8–10 мкм и толщиной 40–70 нм, (рис. 6).
Рис. 5.
Микроструктура излома образца, синтезированного в кварцевом тигле с графитовым дном из смеси, состав которой рассчитан по формуле (III).
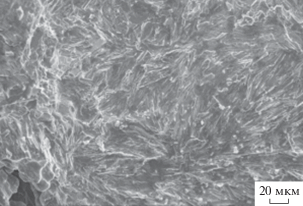
Рис. 6.
Характерная морфология излома (а) и увеличенное изображение фрагментов (б, в) материала на основе МАХ фазы V2AlC.
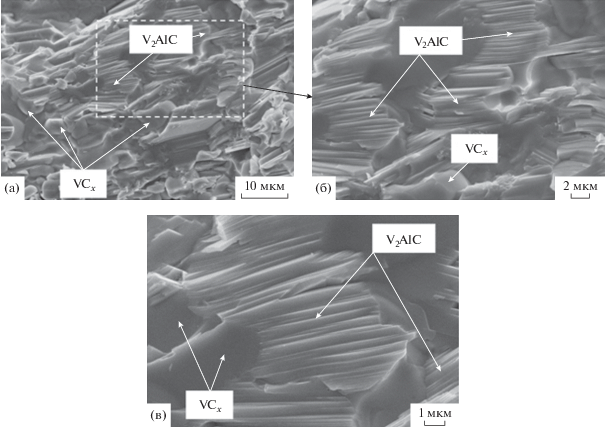
В межзеренном пространстве между ламинатными “пачками” МАХ-фазы V2AlC расположены включения зерен карбида ванадия VCх округлой формы, размер которых достигает 10 мкм. Структурные составляющие (включения) на основе интерметаллидной фазы VAl3 и фазыV5Si3 находятся в виде мелких включений между зерен МАХ фазы V2AlC и VCх. По данным энергодисперсионного анализа, проведенного с поверхности излома образца, многослойные наноламинатные зерна (рис. 6в) имеют следующий состав: V – 72.75 мас. %, Al – 17.65 мас. % и C – 9.6 мас. %.
На рис. 7 представлена температурная зависимость удельного электросопротивления ρ полученного продукта. Материал на основе V2AlC, синтезированный из исходной реакционной смеси 4V2O5/2VO2/21Al/5C (табл. 1, п. 3) обладает металлической проводимостью во всем измеренном диапазоне температур 300–1300 K в вакууме 2 × × 10–3 Па.
Рис. 7.
Температурная зависимость удельного электросопротивления ρ синтезированного материала на основе V2AlC.
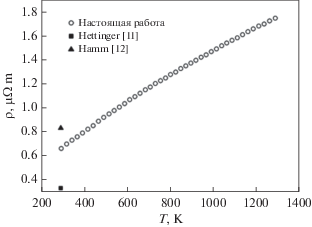
Увеличение температуры приводит к возрастанию тепловых колебаний кристаллической решетки, и сопротивление движению электронов проводимости возрастает. Температурный коэффициент электросопротивления исследованного материала составляет β = 0.0019 K–1 при комнатной температуре и β = 0.0013 K–1 при 1300 К. Для сравнения на графике зависимости удельного электросопротивления (ρ)) образца на основе V2AlC от температуры (рис. 7) нанесены данные, полученные в работах [11, 12]. Отличие этих результатов объясняется различным способом получения материала, а также наличием примесей, размерами зерен и наличием структурной неоднородности. Так в работе [12] образцы V2AlC получали с помощью микроволнового синтеза с последующей консолидацией методом плазменно-искрового спекания. Начиная с комнатной температуры, удельное сопротивление синтезированного сплава увеличивается с ростом температуры.
Многофазовый состав синтезированного материала существенно затрудняет анализ факторов, влияющих на проводимость сплава, поскольку она определяется свойствами и концентрацией фазовых составляющих, наличием межфазных границ и природой их контактов. Поскольку в состав синтезированного материала наряду с V2AlC (65 мас. %) входят вторичные фазы VCx, VAl, VAl3, V5Si3, то естественно предположить присутствие их вклада в удельное сопротивление.
В работе [21] зависимость электросопротивления от состава неупорядоченного карбида ванадия VCx имеет аналогичный нашему материалу характер поведения и объясняется атомно-вакансионным взаимодействием и изменением концентрации носителей тока в области гомогенности VCх. При этом значения удельного электросопротивления при комнатной температуре для карбидов ванадия VC0.66, VC0.79, VC0.83 и VC0.873 в закаленном и отожженном состояниях находится в диапазоне 0.39–1.43 мкОм, а при 1300 К лежит в диапазоне 0.65–1.60 мкОм. В свою очередь, фаза VAl3 имеет удельное электросопротивление при комнатной температуре 1.15–1.20 мкОм [22]. Этот результат указывает на определяющий вклад фазы V2AlC в электросопротивление синтезированного материала, что может быть связано с образованием в процессе синтеза цепочек из контактирующих наноламинатных зерен V2AlС, создающих непрерывный каркас в объеме материала.
ЗАКЛЮЧЕНИЕ
В данной работе впервые показано, что методом СВС с использованием смеси порошков оксидов ванадия(V) и (IV), алюминия и углерода получен материал на основе МАХ-фазы V2AlC (65 мас. %), в котором присутствуют также карбидные, интерметаллидные и силицидные фазы ванадия. Наличие этих фаз в конечном продукте синтеза связано, по-видимому, с неравновесностью процесса из-за малого времени “жизни” расплава и быстрым его остыванием, и кристаллизацией. В результате промежуточные продукты (VCx, V2C, VAl, VAl3) не успевают полностью прореагировать с образованием МАХ-фазы V2AlC.
Показано, что материал реакционного тигля, в которой производили синтез, также оказывает влияние на состав конечного продукта. Это обусловлено тем, что расплав частично успевает прореагировать с углеродом (графитом) или кварцем, из которых изготовлены тигли.
Материал на основе МАХ-фазы V2AlC является электрическим проводником, демонстрирующим металлический характер проводимости во всем измеренном диапазоне температур 300–1300 К в вакууме 2 × 10–3 Па. Высказано предположение, что определяющий вклад в электросопротивление синтезированного материала вносит фаза V2AlC что может быть связано с образованием в процессе синтеза цепочек из контактирующих наноламинатных зерен V2AlС, создающих непрерывный каркас в объеме материала.
Список литературы
Schuster J.C., Nowotny H., Vaccaro C. The ternary systems: Cr–Al–C, V–Al–C, and Ti–Al–C and the behavior of H-phases (M2AlC) // J. Solid State Chem. 1980. V. 32. P. 213–219.
Etzkorn J., Ade M., Hillebrecht H. V2AlC, V4AlC3 −x (x ≈ 0 : 31), and V12Al3C8: synthesis, crystal growth, structure, and superstructure // Inorg. Chem. 2007. V. 46. P. 7646–7653.
Hu C., Wang J., Li F., Wang J., Zhou Y. Crystal structure of V4AlC3: a new layered ternary carbide // J. Am. Ceram. Soc. 2008. V. 91. P. 636–639.
Bengt Hallstedt. Thermodynamic evaluation of the Al–V–C system // CALPHAD: Computer Coupling of Phase Diagrams and Thermochemistry. 2013. V. 41. P. 156–159. https://doi.org/10.1016/j.calphad.2013.03.002
Gupta S., Barsoum M.W. Synthesis and oxidation of V2AlC and (Ti0.5,V0.5)2AlC in air // J. Electrochem. Soc. 2004. V. 151. P. D24–D29.
Schneider J.M., Mertens R., Music D. Structure of V2AlC studied by theory and experiment // J. Appl. Phys. 2006. V. 99. P. 013501.
Chunfeng Hu, Lingfeng He, Mingyue Liu, Xiaohui Wang, Jingyang Wang, Meishuan Li, Yanchun Zhou. In situ Reaction Synthesis and Mechanical Properties of V2AlC // J. Am. Ceram. Soc. 2008. V. 91. P. 4029–4035. https://doi.org/10.1111/j.1551-2916.2008.02774.x
Liang B.-Y., Zhang J., Mu Y.-C. Combustion synthesis of V2AlC materials. June 2013, Fenmo Yejin Cailiao Kexueyu Gongcheng // Materials Sci. Eng. Powder Metal. 2013. V. 18. № 3. P. 447–451.
Киффер Р., Браун Х. Ванадий, ниобий, тантал (Металлургия чистых металлов и их сплавов). Перевод с немецкого Минц Р.С. М.: Металлургия. 1968. 311 с.
База данных ICDD. PDF № 01-074-5286.
Hettinger J.D., Lofland S.E., Finkel P., Meehan T., Palma J., Harrell K., Gupta S., Ganguly A., El-Raghy T., Barsoum M.W. Electrical transport, thermal transport, and elastic properties of M2AlC (M = Ti, Cr, Nb, and V) // Phys. Rev. B. 2005. V. 72. P. 115120.
Christin M. Hamm, Michael DuËrrschnabel, Leopoldo Molina-Luna, Ruslan Salikhov, Detlef Spoddig, Michael Farle, Ulf Wiedwald, Christina S. Birkel. Structural, magnetic and electrical transport properties of non-conventionally prepared MAX phases V2AlC and (V/Mn)2AlC // Mater. Chem. Front. 2018. V. 2. P. 483. https://doi.org/10.1039/C7QM00488E
Gorshkov V.A., Miloserdov P.A., Luginina M.A., Sachkova N.V., Belikova A.F. High-Temperature Synthesis of a Cast Material with a Maximum Content of the MAZ Phase Cr2AlC // Inorganic Materials. 2017. V. 53. № 3. P. 271–277. https://doi.org/10.1134/S0020168517030062
Gorshkov V.A., Miloserdov P.A., Karpov A.V., Shchu-kin A.S., Sytschev A.S. Investigation of the Composition and Properties of a Cr2AlC MAX Phase-Based Material Prepared by Metallothermic SHS. // Phys. Met. Metal. 2019. V. 120. № 5. P. 471–475. https://doi.org/10.1134/S0031918X19050041
Miloserdov Pavel A., Gorshkov Vladimir A., Kovalev Ivan D., Kovalev Dmitrii Yu. High-temperature synthesis of cast materials based on Nb2AlC MAX phase // Ceramics International. 2019. V. 45. Issue 2. Part A. P. 2689–2691. https://doi.org/10.1016/j.ceramint.2018.10.198
Shiryaev A. Thermodynamics of SHS processes: An advanced approach // Int. J. SHS. 1995. V. 4. № 4. P. 351–362.
Фирсова В.А., Пятыгина Н.Г., Иванова Т.И. Метод Ритфельда – Rietveld. Свидетельство о регистрации программы для ЭВМ № 2010613016 от 06.05.10.
Crystallography Open Database. http://www.crystallography.net/cod/.
Materials Project. https://materialsproject.org/.
Карпов А.В., Морозов Ю.Г., Бунин В.А., Боровинская И.П. Влияние оксида иттрия на электропроводность нитридной СВС-керамики // Неорганич. матер. 2002. Т. 38. № 6. С. 762–766.
Гусев А.И. Влияние углеродных вакансий на электросопротивление нестехиометрического карбида ванадия VCy // Письма в ЖЭТФ. 2009. Т. 90. № 3. C. 210–215.
Ratnadwip Singha, Shubhankar Roy, Arnab Pariari, Biswarup Satpati, Prabhat Mandal. Planar Hall effect in the type-II Dirac semimetal VAl3 // Phys. Rev. B. V. 98. P. 081103(R). https://doi.org/10.1103/PhysRevB.98.081103
Дополнительные материалы отсутствуют.
Инструменты
Физика металлов и металловедение