Физиология растений, 2021, T. 68, № 2, стр. 151-160
Пластидные РНК-полимеразы ядерного кодирования являются компонентами антероградного контроля гормональной регуляции экспрессии хлоропластных генов
И. А. Бычков a, А. А. Андреева a, Н. В. Кудрякова a, *, Е. С. Пожидаева a, А. С. Дорошенко a, В. В. Кузнецов a
a Федеральное государственное бюджетное учреждение науки Институт физиологии растений
им. К.А. Тимирязева Российской академии наук
Москва, Россия
* E-mail: nvkudryakova@mail.ru
Поступила в редакцию 28.07.2020
После доработки 11.08.2020
Принята к публикации 11.08.2020
Аннотация
Известно, что фитогормоны играют важную роль в регуляции биогенеза хлоропластов, однако информация о путях восприятия гормонального сигнала хлоропластами ограничена. С целью анализа возможных механизмов действия гормонов изучали ответ мутантов Arabidopsis thaliana (L.) Heynh. scabra3-2 (sca3-2) и rpotmp с дефектными генами пластидных РНК-полимераз ядерного кодирования на обработку абсцизовой кислотой (АБК) и цитокининами (ЦК). Реакция мутанта rpotmp, как правило, не отличалась от ответа растений дикого типа: транс-зеатин активировал накопление транскриптов генов аппарата транскрипции и генов, кодируемых пластидным геномом, тогда как АБК в слабой степени подавляла их экспрессию или не оказывала достоверного эффекта. Однако базовые уровни матриц генов, входящих в транскрипционный ферментный комплекс PEP-А (plastid-encoded RNA polymerase), у rpotmp оказались выше, чем у растений дикого типа, что, вероятно, связано с компенсаторным механизмом, позволяющим мутанту усилить РЕР-зависимую транскрипцию при отсутствии фермента RPOTmp. Дисфункция фермента пластидной РНК-полимеразы RPOTp у sca3-2 индуцировала измененный гормональный ответ генов транскрипционного комплекса пластид и генов пластидного кодирования в сравнении с реакцией растений дикого типа. Отсутствие значимого активирующего эффекта ЦК на экспрессию генов аппарата транскрипции коррелировало с сохранением базового уровня транскриптов хлоропластных генов и пластидных белков. Кроме того, sca3-2 имел увеличенную базовую экспрессию генов метаболизма ЦК – IPT3, IPT5 и CKX5. При этом реакция на ингибирующее действие АБК у этого мутанта, напротив, была выражена сильнее, возможно, в связи с изменением базовых уровней матриц ряда генов, кодирующих белки сигналинга и метаболизма АБК. Таким образом, изменение экспрессии генов NEP (nuclear-encoded RNA polymerases) под действием гормонов может трансформироваться в активацию или подавление экспрессии хлоропластных генов ядерного или пластомного кодирования, обеспечивая регуляцию функций хлоропластов за счет механизмов антероградного сигналинга.
ВВЕДЕНИЕ
Фитогормоны играют важнейшую роль в регуляции биогенеза хлоропластов и их адаптации к меняющимся условиям среды на разных этапах онтогенеза. Однако пути восприятия гормонального сигнала в этих органеллах остаются до сих пор малоизученными и, по-видимому, могут дублироваться несколькими механизмами. Наряду с непосредственным связыванием цис-элементов в промоторных зонах пластидных генов гормон-регулируемыми транс-факторами действие гормона может быть опосредовано через ядерные гены, определяющие экспрессию генов пластома. Примерно из 3000–4000 белков хлоропластов около 98% кодируются ядерным геномом, и именно они определяют тип пластид и их метаболическую активность, все этапы экспрессии пластидного генома и систему импорта белков в хлоропласты. Это позволяет предположить, что фитогормоны, модулируя ядерный сигнал, влияют на биогенез хлоропластов. Возможная справедливость этого утверждения косвенно подтверждается тем, что антероградный сигналинг является ведущим в регуляции биогенеза хлоропластов и, кроме того, до настоящего времени, несмотря на огромные успехи в изучении механизма действия фитогормонов, ни один рецептор ни для одного фитогормона не был обнаружен в хлоропластах.
Хорошо известно, что фитогормоны цитокинины и АБК оказывают противоположный эффект на биогенез хлоропластов, причем нами установлено, что они влияют на экспрессию пластидных генов как на транскрипционном [1, 2], так и на посттранскрипционном уровне [3, 4]. Для изучения возможного вовлечения этих фитогормонов в антероградный сигналинг мы выбрали два ядерных гена аппарата транскрипции пластид RPOTp и RPOTmр, кодирующих моносубъединичные РНК-полимеразы фагового типа (NEP – nuclear-encoded RNA polymerase). Помимо RPOTp и RPOTmр геном Arabidopsis содержит ген РНК-полимеразы фагового типа RPOTm, которая осуществляет транскрипцию митохондриальных генов. Полагают, что гены RPOTp и RPOTmр произошли за счет дупликации гена RPOTm и последующего приобретения полимеразами транзитного пептида, направляющего их в пластиды (RPOTp) или в пластиды и митохондрии (RPOTmp, у двудольных растений) [5]. В отличие от митохондрий гены пластид транскрибируются также мультисубъединичной РНК-полимеразой прокариотического типа, кодируемой пластомом (PEP – plastid-encoded RNA polymerase).
Специфичность действия пластидных полимераз была предметом детального анализа ряда исследователей. Показано, что РЕР-полимераза отвечает, прежде всего, за транскрипцию генов фотосинтеза, а ферменты NEP активны на ранних стадиях онтогенеза и транскрибируют гены домашнего хозяйства, включая четыре коровые субъединицы PEP. Однако при подавлении PEP-зависимой транскрипции за счет генетических дефектов или неблагоприятных физиологических условий NEP способны транскрибировать даже фотосинтетические гены с NEP-зависимых промоторов [6, 7].
Ферменты NEP транскрибируют пластидные гены, связываясь с тремя различными типами промоторов, похожих на промоторы генов бактериофагов и митохондрий. Наличие различных типов промоторов предполагает существование специфичных транс-факторов, которые помогали бы РНК-полимеразам определять сайты инициации транскрипции. Тем не менее, до настоящего времени для NEP не был идентифицирован ни один транс-фактор, возможно, из-за низкой концентрации, не позволяющей выделить их современными методами.
Вопрос о гормональной регуляции активности NEP также остается открытым. Поэтому задачи нашего исследования включали анализ особенностей гормональной регуляции хлоропластных генов, а также генов метаболизма и сигналинга цитокининов (ЦК) и АБК у растений дикого типа и мутантов с дефектными генами RPOTp и RPOTmp.
МАТЕРИАЛЫ И МЕТОДЫ
Исследования выполнены на трехнедельных растениях дикого типа Arabidopsis thaliana (L.) Heynh. (Columbia-0), гомозиготных инсерционных Т-ДНК нокаут-мутантах scabra3-2 (sca3-2) и rpotmp-2, отобранных из стоковых линий NASC N593884 (Salk 0938840) и N6328420 (Salk 132842), соответственно. Растения выращивали на агаризованной половинной МС-среде в климатической камере при интенсивности освещения 70 мкЭ/(м2 с), температуре 23°C и фотопериоде 16 ч – свет / 8 ч – темнота.
Содержание пигментов и показатели переменной флуоресценции хлорофилла с использованием флуориметра PAM-100 (Heinz Walz GmbH, Германия) оценивали в соответствии с протоколом, описанным ранее [8].
Для исследования действия гормонов растения обрабатывали растворами АБК (50 мкМ) и транс-зеатина (5 мкМ) в течение 3 или 24 ч, после чего фиксировали в жидком азоте. Оптимальные концентрации фитогормонов определяли в предварительных экспериментах. Относительный уровень транскриптов целевых генов определяли методом количественного ПЦР в режиме реального времени после обратной транскрипции (ПЦР-РВ) на амплификаторе LigthCyclerR96 (Roche, Швейцария) согласно методике, описанной в предыдущей работе [9]. Последовательности использованных праймеров приведены в Supplementary (Table S1 ).
Оценку изменений в содержании хлоропластных белков при действии фитогормонов проводили методом вестерн-блоттинга с использованием специфичных антител против белков RbcL (AS03 037), PsbD (AS06 146), AtpB (AS05 085) и Lhcb2 (AS01 003) фирмы Agrisera (Швеция). Тотальный растительный белок получали путем гомогенизации розеточных листьев в буфере, содержащем 50 мМ HEPES-KOH, pH 7.5, 330 мМ сорбит, 2 мМ ЭДТА, 1 мМ MgCl2, с последующей фильтрацией гомогената через 2 слоя фильтра Miracloth (Calbiochem, США). Количественное определение тотального белка в полученных экстрактах проводили бицинхониновым методом с использованием набора BCA™ Protein Assay Kit (Thermo Fisher Scientific, США). Образцы, содержащие 20 мкг тотального белка, разделяли в 10% SDS-PAGE, и затем белки переносили на PVDF мембрану методом полусухого переноса на приборе semi-dry (Bio-Rad, США). Взаимодействие специфических антител с исследуемыми образцами белков, иммобилизированных на мембране, проводили в условиях, рекомендованных фирмой-производителем антител (Agrisera, Швеция). Иммунореакцию визуализировали при помощи набора ECL (Bio-Rad, США) и хемилюминесцентный сигнал регистрировали на цифровом сканнере C-Digit (Li-Сor, США).
Эксперименты проводили не менее чем в 3-кратной биологической повторности. Достоверность различий проверяли с помощью метода ANOVA с последующим тестом Тьюки.
РЕЗУЛЬТАТЫ
Инактивация генов RPOTp и RPOTmp способствовала изменению физиологических характеристик и экспрессии генов сигналинга и метаболизма ЦК и АБК
Убедительным доказательством того, что NEP принимают непосредственное участие в гормональных ответах, является анализ соответствующих нокаут-мутантов. В экспериментах мы использовали трансгенные растения scabra3-2 (sca3-2), мутантные по гену RPOTp. Мутантный ген содержит Т-ДНК вставку в положении 1894 (от кодона инициации трансляции) и кодирует полипептид, в котором отсутствуют 604 аминокислоты и 9 из 11 доменов, включая С-мотив. Этот мотив является частью каталитического сайта T7 РНК полимераз, и его отсутствие вызывает дисфункцию фермента RPOTp [10]. Растения scabra3-2 обнаружили существенные изменения физиологических показателей, включая пигментацию и показатели флуоресценции (табл. 1). В частности, растения характеризовались примерно в десять раз сниженным содержанием хлорофиллов и в пять с лишним раз меньшим количеством каротиноидов по сравнению с диким типом. Уменьшение количества хлорофилла полностью коррелировало с показателями базовой флуоресценции (Fs), что, вероятно, говорит о меньшем количестве реакционных центров. Однако расчетные показатели потенциального максимального квантового выхода (Fv/Fm), квантового выхода на свету (Y(II)) и нефотохимического тушения (NPQ), характеризующие эффективность фотосистемы II, были лишь незначительно ниже, чем у дикого типа. Это, по-видимому, свидетельствует о сохранении и относительно нормальном функционировании всех элементов фотосистемы.
Таблица 1.
Содержание пигментов и показатели фотосинтетической активности фотосистемы II в трехнедельных растениях дикого типа (Columbia-0) и инсерционных нокаут-мутантах по гену RPOTp (sca3-2) и по гену RPOTm (rpotmp-2)
| Показатель | Генотип | ||
|---|---|---|---|
| дикий тип (Col-0) | scabra3-2 | rpotmp-2 | |
| Содержание хлорофилла (a + b), мг/г сырой массы | 0.705 ± 0.036a | 0.071 ± 0.004b | 0.777 ± 0.033a |
| Содержание каротиноидов, мг/г сырой массы | 0.124 ± 0.003a | 0.021 ± 0.001b | 0.158 ± 0.004c |
| Стационарный уровень флуоресценции Fs | 0.202 ± 0.034a | 0.054 ± 0.006b | 0.194 ± 0.014a |
| Показатель Fv/Fm | 0.827 ± 0.002a | 0.815 ± 0.005b | 0.828 ± 0.003a |
| Квантовый выход фотосистемы II на свету Y(II) | 0.675 ± 0.009a | 0.595 ± 0.017b | 0.689 ± 0.016a |
| Параметр нефотохимического тушения NPQ | 0.261 ± 0.014a | 0.228 ± 0.015b | 0.260 ± 0.017a |
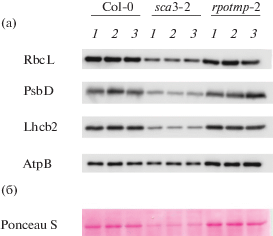
В отличие от sca3-2, у rpotmp-2 мутанта, дефектного по гену RPOTm, транскрипты RPOTmp полностью отсутствовали. Этот мутант также характеризовался замедленным развитием, особенно заметным у ювенильных проростков, однако по содержанию хлорофилла и показателям активности фотосинтетического аппарата взрослых листьев не отличался от растений дикого типа или даже несколько превосходил их (табл. 1). Мы также не обнаружили каких-либо различий в содержании белков основных комплексов фотосинтетических мембран у rpotmp-2 мутанта (рис. 1).
Рис. 1.
Уровни хлоропластных белков у трехнедельных растений дикого типа (Columbia-0) и мутантов по генам RPOTp (sca3-2) и RPOTmp (rpotmp-2) (а). Растения обрабатывали АБК (50 мкМ) или транс-зеатином (5 мкМ) в течение 24 ч. Белки тотального экстракта анализировали методом вестерн-блоттинга, используя специфические антитела к RbcL, AtpB, PsbD и Lhcb2. Одинаковая загрузка треков (20 мкг) проверялась окрашиванием Ponceau S (б). 1 – без обработки, 2 – обработка транс-зеатином, 3 – обработка АБК.
Для подтверждения эффективности гормональной обработки анализировали накопление транскриптов генов ARR5 (Response Regulator 5) и RD29А (Responsive-to-Dehydration 29A), используемых в качестве маркеров действия цитокинина и АБК, соответственно. Оба гена активировались гормонами у всех исследованных образцов, причем мутант scabra3-2 оказался особо восприимчивым к действию АБК (табл. 2, Supplementary Table S2 ). Недавно о гиперчувствительности этого мутанта к АБК при прорастании семян и формировании проростков сообщали Lidón-Soto с соавт. [11]. Чтобы оценить причины повышенной чувствительности этой мутантной линии к АБК, мы исследовали влияние экзогенного гормона на экспрессию некоторых генов метаболизма и передачи сигнала АБК. У sca3-2 оказалась снижена базовая экспрессия генов пути биосинтеза АБК ABA1 и ABA2, однако по реакции этих генов на экзогенную АБК мутант не отличался от растений дикого типа (табл. 2). Среди генов цепи передачи сигнала АБК – ABI1, ABI2 и HAB1, активируемых АБК [12, 13], у sca3-2 отмечен повышенный базовый уровень экспрессии HAB1, однако уровни индукции этих генов гормоном практически не различались, как и уровни кратного подавления транскриптов генов рецепторов АБК – PYR1 и PYL5 (табл. 2). Таким образом, инактивация гена RPOTp способствовала изменению базовых уровней некоторых генов метаболизма и сигналинга АБК и, как следствие, могла усиливать реакцию генов ответа на АБК, но не приводила к существенному изменению экспрессии генов сигналинга в ответ на обработку экзогенной АБК.
Таблица 2.
Изменение экспрессии генов сигналинга и метаболизма цитокининов и АБК у трехнедельных растений дикого типа (Columbia-0) и инсерционного нокаут-мутанта по гену RPOTp (sca3-2). Опытные растения обрабатывали АБК (50 мкМ) и транс-зеатином (5 мкМ) в течение 3 ч
| Гены | Генотип и вид обработки | |||||
|---|---|---|---|---|---|---|
| дикий тип без обработки | дикий тип транс-зеатин | дикий тип АБК | sca3-2 без обработки | sca3-2 транс-зеатин | sca3-2 АБК | |
| RD29 | 1.000 ± 0.055a | 0.363 ± 0.014b | 3.605 ± 0.174c | 2.540 ± 0.363d | 0.632 ± 0.025b | 14.610 ± 0.125e |
| ABA1 | 1.000 ± 0.036a | 0.793 ± 0.017b | 2.332 ± 0.078c | 0.601 ± 0.043b | 0.476 ± 0.056b | 1.866 ± 0.105d |
| ABA2 | 1.000 ± 0.079a | 1.197 ± 0.087a | 0.599 ± 0.033b | 0.541 ± 0.032b | 0.755 ± 0.054c | 0.414 ± 0.024b |
| СYP707a1 | 1.000 ± 0.064a | 0.750 ± 0.047b | 0.862 ± 0.031b | 0.873 ± 0.030b | 0.730 ± 0.059b | 0.745 ± 0.059b |
| ABI1 | 1.000 ± 0.069a | 0.572 ± 0.036b | 4.433 ± 0.338c | 1.294 ± 0.090a | 0.589 ± 0.048b | 3.149 ± 0.437d |
| ABI2 | 1.000 ± 0.074a | 0.777 ± 0.102b | 6.357 ± 0.363c | 1.283 ± 0.088a | 0.815 ± 0.111ab | 6.774 ± 0.687c |
| HAB1 | 1.000 ± 0.106a | 0.642 ± 0.077b | 8.074 ± 1.188c | 2.266 ± 0.208d | 1.227 ± 0.124a | 9.221 ± 0.760c |
| PYR1 | 1.000 ± 0.070a | 1.945 ± 0.206b | 0.769 ± 0.060c | 1.447 ± 0.103b | 1.400 ± 0.123b | 0.402 ± 0.033d |
| PYL5 | 1.000 ± 0.089a | 1.877 ± 0.213b | 0.141 ± 0.012c | 1.210 ± 0.148a | 1.486 ± 0.149b | 0.200 ± 0.015c |
| ARR5 | 1.000 ± 0.090a | 55.010 ± 5.226b | 0.620 ± 0.042c | 2.505 ± 0.205d | 14.070 ± 1.870e | 1.625 ± 0.126f |
| ARR1 | 1.000 ± 0.069abc | 0.853 ± 0.049b | 1.270 ± 0.078c | 0.745 ± 0.041b | 0.451 ± 0.049d | 0.476 ± 0.024d |
| ARR10 | 1.000 ± 0.066a | 1.419 ± 0.132b | 1.418 ± 0.085b | 1.161 ± 0.085ab | 1.094 ± 0.086a | 0.777 ± 0.054a |
| ARR12 | 1.000 ± 0.069ac | 1.569 ± 0.077b | 1.275 ± 0.048a | 0.832 ± 0.047c | 0.853 ± 0.067c | 0.486 ± 0.028d |
| AHK2 | 1.000 ± 0.118a | 2.063 ± 0.174b | 1.569 ± 0.170c | 1.385 ± 0.122ac | 0.986 ± 0.083a | 0.534 ± 0.045d |
| AHK3 | 1.000 ± 0.133a | 0.956 ± 0.092a | 1.855 ± 0.218b | 1.636 ± 0.159b | 1.371 ± 0.136ab | 1.347 ± 0.128ab |
| AHK4 | 1.000 ± 0.113ae | 10.540 ± 1.081b | 0.678 ± 0.075c | 1.439 ± 0.213a | 5.850 ± 0.513d | 0.898 ± 0.104e |
| GNL | 1.000 ± 0.079a | 11.790 ± 1.232b | 0.900 ± 0.091a | 1.553 ± 0.112c | 6.336 ± 0.448d | 0.449 ± 0.035e |
| IPT3 | 1.000 ± 0.065a | 1.753 ± 0.133b | 1.668 ± 0.099b | 3.972 ± 0.266c | 2.532 ± 0.158d | 1.141 ± 0.054a |
| IPT5 | 1.000 ± 0.139a | 1.189 ± 0.117a | 1.763 ± 0.176b | 3.117 ± 0.253c | 1.753 ± 0.199b | 2.612 ± 0.220c |
| CKX3 | 1.000 ± 0.055a | 5.075 ± 0.439b | 0.430 ± 0.038c | 1.097 ± 0.082a | 10.690 ± 0.588d | 0.510 ± 0.031c |
| CKX5 | 1.000 ± 0.062a | 4.449 ± 0.381b | 1.052 ± 0.067a | 4.526 ± 0.342b | 5.401 ± 0.404b | 2.040 ± 0.098c |
Транс-зеатин не оказывал значимого влияния на экспрессию генов рецепторов ЦК АНК2 и АНК3 и регуляторов ответа типа B – ARR1, ARR10 и ARR12, но резко индуцировал экспрессию гена рецептора АНК4 и ЦК-регулируемого транс-фактора GNL у всех исследованных образцов (табл. 2, Supplementary Table S2 ). При этом мутант sca3-2 отличался пониженной по сравнению с диким типом ЦК-активируемой экспрессией генов АНК4 и GNL, как и маркерного гена ARR5 (табл. 2). Сниженная индукция трех последних генов, возможно, также была следствием измененного гормонального статуса этого мутанта. Действительно, sca3-2 обнаружил увеличенный втрое уровень базовой экспрессии генов синтеза ЦК IPT3 и IPT5 и гена катаболизма гормона CKX5. При этом уровень базовой экспрессии второго из исследованных генов цитокининоксидазы CKX3 не отличался от показателей растений дикого типа. Таким образом, измененная чувствительность мутанта sca3-2 могла быть следствием повышенного содержания эндогенных ЦК. Заметим, что у мутанта rpotmp-2 также наблюдалось увеличенное накопление матриц IPT3, IPT5 и CKX5, хотя и не столь существенное как у sca3-2 (Supplementary Table S2 ).
Дифференцированное воздействие ЦК и АБК на экспрессию пластидных генов и генов аппарата транскрипции мутантов rpotmp и rpotp
При обработке транс-зеатином и АБК ответы растений дикого типа и мутанта rpotmp-2 практически не различались. Цитокинин активировал накопление транскриптов генов аппарата транскрипции хлоропластов RPOTp, RPOTm, SIG2, SIG6 и CKA4 в 2–4 раза по сравнению с исходными значениями, а также генов РЕР-ассоциированных белков (PAP1–12), тогда как АБК лишь в слабой степени подавляла их экспрессию или не оказывала достоверного воздействия (Supplementary Table S3 ). При этом АБК стимулировала накопление мРНК гена SIG5 у обоих образцов. Подобная реакция не случайна. В условиях стресса и повышенного уровня АБК этот транс-фактор в комплексе с PEP обеспечивает транскрипцию ряда хлоропластных генов с промоторов типа BLRP на фоне подавления экспрессии основной части генов пластома [14].
Таблица 3.
Изменение экспрессии генов аппарата транскрипции у трехнедельных растений дикого типа (Columbia-0) и инсерционного нокаут-мутанта по гену RPOTp (sca3-2). Опытные растения обрабатывали АБК (50 мкМ) и транс-зеатином (5 мкМ) в течение 3 ч
| Гены | Генотип и вид обработки | |||||
|---|---|---|---|---|---|---|
| дикий тип без обработки | дикий тип транс-зеатин | дикий тип АБК | sca3-2 без обработки | sca3-2 транс-зеатин | sca3-2 АБК | |
| RPOTp | 1.000 ± 0.050a | 3.972 ± 0.197b | 0.686 ± 0.078c | 1.464 ± 0.111d | 1.580 ± 0.073d | 0.714 ± 0.098c |
| RPOTm | 1.000 ± 0.066a | 2.639 ± 0.186b | 0.695 ± 0.052c | 1.102 ± 0.062a | 1.834 ± 0.279b | 0.480 ± 0.035d |
| RPOTmp | 1.000 ± 0.071a | 3.630 ± 0.204b | 0.486 ± 0.035c | 0.611 ± 0.110c | 1.410 ± 0.086d | 0.254 ± 0.019e |
| CKA4 | 1.000 ± 0.114a | 2.723 ± 0.260b | 1.193 ± 0.125a | 1.357 ± 0.124ac | 1.474 ± 0.144c | 0.661 ± 0.080d |
| SIG2 | 1.000 ± 0.077a | 2.704 ± 0.205b | 0.976 ± 0.087a | 1.113 ± 0.085a | 1.490 ± 0.127c | 0.523 ± 0.031d |
| SIG5 | 1.000 ± 0.079a | 2.523 ± 0.164b | 2.761 ± 0.245b | 2.151 ± 0.124c | 1.516 ± 0.117d | 2.387 ± 0.149bc |
| SIG6 | 1.000 ± 0.088a | 2.938 ± 0.193b | 0.818 ± 0.075a | 0.898 ± 0.059a | 1.451 ± 0.121c | 0.342 ± 0.030d |
| PAP1 | 1.000 ± 0.075a | 2.354 ± 0.152b | 1.017 ± 0.086a | 1.214 ± 0.039a | 1.586 ± 0.097c | 0.478 ± 0.036d |
| PAP2 | 1.000 ± 0.047a | 2.308 ± 0.231b | 1.113 ± 0.085a | 1.333 ± 0.111a | 1.454 ± 0.091c | 0.509 ± 0.043d |
| PAP3 | 1.000 ± 0.066a | 2.063 ± 0.180b | 0.708 ± 0.059c | 1.025 ± 0.089a | 1.790 ± 0.092b | 0.258 ± 0.032d |
| PAP4 | 1.000 ± 0.053a | 2.136 ± 0.159b | 0.758 ± 0.044c | 1.202 ± 0.086a | 1.647 ± 0.064d | 0.371 ± 0.041e |
| PAP5 | 1.000 ± 0.070a | 3.010 ± 0.241b | 0.681 ± 0.063c | 0.968 ± 0.073a | 2.346 ± 0.223b | 0.293 ± 0.030d |
| PAP6 | 1.000 ± 0.099a | 3.387 ± 0.286b | 0.742 ± 0.063c | 0.883 ± 0.055ac | 2.158 ± 0.187d | 0.419 ± 0.028e |
| PAP7 | 1.000 ± 0.074a | 1.905 ± 0.164b | 0.853 ± 0.083a | 0.963 ± 0.101a | 1.602 ± 0.090b | 0.313 ± 0.033c |
| PAP8 | 1.000 ± 0.059a | 2.848 ± 0.286b | 0.768 ± 0.057c | 0.821 ± 0.065ac | 1.548 ± 0.077d | 0.371 ± 0.019e |
| PAP9 | 1.000 ± 0.085a | 2.063 ± 0.149b | 1.202 ± 0.081a | 1.338 ± 0.098a | 2.465 ± 0.383b | 1.253 ± 0.088a |
| PAP10 | 1.000 ± 0.106a | 2.099 ± 0.150b | 0.678 ± 0.062c | 0.683 ± 0.035c | 1.371 ± 0.092a | 0.236 ± 0.019d |
| PAP11 | 1.000 ± 0.064a | 2.815 ± 0.146b | 0.646 ± 0.054c | 0.954 ± 0.049a | 1.442 ± 0.116d | 0.316 ± 0.019e |
| PAP12 | 1.000 ± 0.073ac | 2.526 ± 0.177b | 0.809 ± 0.059c | 1.008 ± 0.050a | 1.226 ± 0.094a | 0.469 ± 0.028d |
Несколько иная картина была получена при анализе ЦК-зависимой экспрессии генов аппарата транскрипции у мутанта scabra3-2. ЦК практически не регулировал накопление транскриптов фрагмента гена RPOTp и генов РАР2 и СКА4, и в незначительной степени активировал накопление транскриптов других генов аппарата транскрипции (табл. 3). Эти результаты свидетельствуют о снижении активирующего эффекта ЦК. Вместе с тем реакция на действие АБК у мутанта sca3-2, напротив, была выражена сильнее: после трех часов воздействия гормона экспрессия большинства исследованных генов оказалась подавлена в 2–3 раза по сравнению с исходными уровнями. Таким образом, генетическая среда оказывала непосредственное влияние на характер и величину позитивного или негативного эффекта гормонов на экспрессию генов аппарата транскрипции пластид.
Это, в свою очередь, предполагает возможное изменение экспрессии, по крайней мере, двух классов генов, кодируемых пластидным геномом: класса II (NEP и PEP-зависимые гены) и класса III (NEP-транскрибируемые гены). Действительно, гены rpoB (класс III), atpB и clpP (класс II) не активировались транс-зеатином у sca3-2, в отличие от линии rpotmp или растений дикого типа, где транс-зеатин стимулировал повышенное содержание транскриптов этих генов (табл. 4, Supplementary Table S4 ). Таким образом, отсутствие активирующего эффекта ЦК на экспрессию генов аппарата транскрипции коррелировало у этого мутанта с сохранением базового уровня транскриптов NEP-зависимых генов пластома. Количество матриц РEP-зависимого гена psbD (класс I) также достоверно не регулировалось ЦК, в отличие от мутанта rpotmp-2 или растений дикого типа, где экспрессия этого гена активировалась под действием гормона. АБК не оказывала значимого воздействия на экспрессию генов пластома у растений дикого типа и мутанта rpotmp-2 при использованной экспериментальной системе, но подавляла накопление транскриптов пластидных генов у sca3-2. Из полученных данных следует, что повышенная чувствительность к АБК, продемонстрированная у sca3-2 маркерным АБК-индуцируемым геном (RD29а), распространяется, в том числе, и на экспрессию генов пластома.
Таблица 4.
Изменение экспрессии хлоропластных генов и гена ядерного кодирования LHCB2 у трехнедельных растений дикого типа (Columbia-0) и инсерционного нокаут-мутанта по гену RPOTp (sca3-2). Опытные растения обрабатывали АБК (50 мкМ) и транс-зеатином (5 мкМ) в течение 3 ч
| Гены | Генотип и вид обработки | |||||
|---|---|---|---|---|---|---|
| дикий тип без обработки | дикий тип транс-зеатин | дикий тип АБК | sca3-2 без обработки | sca3-2 транс-зеатин | sca3-2 АБК | |
| rpoB | 1.000 ± 0.101a | 1.859 ± 0.182b | 1.141 ± 0.100a | 0.862 ± 0.067a | 0.853 ± 0.061a | 0.440 ± 0.038c |
| rbcL | 1.000 ± 0.048a | 1.501 ± 0.072b | 0.877 ± 0.057ac | 0.886 ± 0.028ac | 1.575 ± 0.069b | 0.690 ± 0.125c |
| psbD | 1.000 ± 0.083a | 1.511 ± 0.131b | 1.110 ± 0.119a | 0.523 ± 0.076c | 0.595 ± 0.045c | 0.468 ± 0.047c |
| atpB | 1.000 ± 0.043a | 1.414 ± 0.108b | 1.137 ± 0.078a | 0.663 ± 0.023c | 0.631 ± 0.031c | 0.390 ± 0.014d |
| clpP | 1.000 ± 0.060a | 1.892 ± 0.119b | 1.338 ± 0.092c | 0.812 ± 0.053d | 0.772 ± 0.032d | 0.440 ± 0.031e |
| LHCB2 | 1.000 ± 0.057a | 1.303 ± 0.088ab | 1.604 ± 0.115b | 0.324 ± 0.023c | 0.208 ± 0.013cd | 0.139 ± 0.010d |
Влияние ЦК и АБК на посттранскрипционный уровень регуляции экспрессии хлоропластных генов у мутантов NEP
Посттранскрипционный уровень регуляции имеет принципиальное значение для экспрессии пластидных генов. Как мы ранее показали, накопление матриц генов пластома не всегда коррелирует с уровнем кодируемых ими хлоропластных белков [3]. В этой связи для выявления механизмов реализации генетической информации в хлоропластах большой интерес представляет оценка особенностей влияния гормонов на содержание пластидных белков.
Согласно результатам вестерн-анализа, у линий Arabidopsis с мутантными генами RPOTp и RPOTmp уровни хлоропластных белков при гормональной обработке лишь частично коррелировали с накоплением матриц кодирующих их генов. У мутанта rpotmp-2 накопление белков практически не индуцировалось транс-зеатином, а у линии sca3-2 содержание белков не снижалось в ответ на воздействие АБК или ЦК (рис. 1, рис. 2). Вместе с тем у растений дикого типа модуляции в содержании белков соответствовали гормон-зависимому ответу, наблюдаемому на уровне РНК, то есть в присутствии ЦК фиксировалось некоторое повышение в накоплении хлоропластных белков PsbD, AtpB и Lhcb 2, а при обработке АБК сохранялись контрольные уровни. Очевидно, содержание транскриптов вряд ли можно рассматривать как единственный фактор, определяющий скорость синтеза и распада хлоропластных белков у мутантов NEP в ответ на действие экзогенных гормонов. Следует, однако, отметить, что в количественном отношении содержание хлоропластных белков у линии sca3-2 существенно уступало их содержанию у растений дикого типа или мутанта rpotmp, что коррелировало с накоплением матриц и показателями флуоресценции.
Рис. 2.
Изменение экспрессии генов пластидного кодирования и гена ядерного кодирования (LHCB2) у трехнедельных растений дикого типа (Columbia-0) и мутантов по генам RPOTp (sca3-2) и RPOTmp (rpotmp-2). Опытные растения обрабатывали АБК (50 мкМ) и транс-зеатином (5 мкМ) в течение 24 ч. Обозначение вариантов опыта. 1 – дикий тип без обработки; 2 – дикий тип, обработанный транс-зеатином; 3 – дикий тип, обработанный АБК; 4 – sca3-2 без обработки; 5 – sca3-2, обработанный транс-зеатин; 6 – sca3-2, обработанный АБК; 7 – rpotmp-2 без обработки; 8 – rpotmp-2, обработанный транс-зеатин; 9 – rpotmp-2, обработанный АБК. Значения нормированы относительно контроля (дикий тип без обработки гормонами). Данные представляют собой средние значения ± стандартные ошибки (n ≥ 3). Буквы обозначают статистически значимые различия при P < 0.05 (ANOVA с последующим тестом Тьюки).

ОБСУЖДЕНИЕ
Как показали результаты исследования, изменение экспрессии генов NEP под действием гормонов трансформируется в активацию или подавление экспрессии фотосинтетических генов ядерного или пластомного кодирования, обеспечивая, таким образом, регуляцию функций хлоропластов за счет механизмов антероградного сигналинга. Вместе с тем дисфункция пластид, связанная с повреждением NEP, может инициировать обратный поток информации от хлоропластов к ядру и вызвать компенсаторное изменение экспрессии генов аппарата транскрипции и переформатирование работы компонентов гормональной системы.
Согласно полученным нами данным инактивация генов пластидных РНК-полимераз ядерного кодирования изменяла профили гормон-зависимой экспрессии генов транскрипционного комплекса пластид и генов пластидного кодирования. Наибольшие отклонения по степени и специфичности регуляции были выявлены для линии sca3-2. Реакция мутанта rpotmp-2 на гормоны, как правило, не отличалась от ответа растений дикого типа. При этом состав и встречаемость предполагаемых цис-элементов, связывающих АБК и ЦК-регулируемые транс-факторы в промоторах обоих генов и отвечающих за индуцибельность гормонами, варьировали незначительно. Эти результаты соответствуют представлению о главенствующей роли RPOTp при разделении функций между RPOTp и RPOTmp в пластидах.
Известно, что на стадии замачивания семян RPOTmp способна транскрибировать оперон rRNA с РС-промотора, а также с ряда других пластидных промоторов [15–17], однако по мере прорастания основная функция этого фермента смещается в митохондрии. По мнению Тарасенко с соавт. [18], RPOTmp у Arabidopsis играет более важную роль не в хлоропластах, а в митохондриях, где этот фермент необходим для экспрессии ряда генов, кодирующих субъединицы комплексов I и IV дыхательной цепи (nad6, cox1, cob и nad3). Интересно, что согласно данным транскрипционного анализа, приведенным на сайте http://bar.utoronto.ca/efp/ cgi-bin/efpWeb.cgi, уровень матриц митохондриальных генов, транскрибируемых RPOTmp, достоверно не изменялся в ответ на действие ЦК или АБК. Аналогичный результат был нами получен для транскрибируемого RPOTmp гена cox1. Согласно литературным данным, митохондриальным полимеразам для эффективной транскрипции in vivo необходимы дополнительные транс-факторы, способные стабилизировать промоторные комплексы или способствовать высвобождению фермента по окончании синтеза РНК [19]. Можно предположить, что эти транс-факторы не регулируются гормонами, в отличие от транс-факторов хлоропластов. Подобный механизм активации цитокининами транс-факторов хлоропластов был недавно продемонстрирован для сигма-факторов РНК-полимеразы бактериального типа SIG2 и SIG6 [20], с промоторными элементами которых, содержащих GATA-сайты, связывался цитокинин-зависимый транс-фактор GNL.
Хотя в целом фенотипические последствия инактивации гена RPOTmp были выражены значительно слабее, чем у sca3-2, базовые уровни матриц генов сигма-факторов и генов РАР, входящих в ферментный комплекс PEP-А, у rpotmp оказались вдвое выше, равно как и экспрессия генов РЕР субъединиц. Эта реакция, вероятно, связана с компенсаторным механизмом, позволяющим мутанту усилить РЕР-зависимую транскрипцию при отсутствии фермента RPOTmp. Добавим также, что, несмотря на замедленное развитие, мутант rpotmp, отличался повышенными базовыми уровнями транскриптов хлоропластных генов и параметров флуоресценции. В то же время мутант sca3-2 имел увеличенный вдвое по сравнению с диким типом базовый уровень экспрессии митохондриального гена cox1, транскрибируемого RPOTmp. Это доказывает, что функции NEP и PEP не только специфичны, но и взаимозависимы.
Для части исследованных генов у мутанта scabra3-2 мы обнаружили снижение активации при обработке ЦК по сравнению с растениями дикого типа или даже ее отсутствие. К их числу, наряду с пластидными генами, относились некоторые ядерные гены, кодирующие белки, ассоциированные с РЕР. Для фотосинтетических генов эта тенденция была выражена как на уровне содержания транскриптов, так и на уровне соответствующих белков (рис. 1, рис. 2). Таким образом, при инактивации гена RPOTp цитокинины и АБК могут действовать однонаправлено, оказывая репрессивное воздействие на экспрессию хлоропластных генов. Причины этого явления нуждаются в дополнительных исследованиях. Не исключено, что для ядерных генов подобный биологический ответ был обусловлен механизмами ретроградного сигналинга, который способствовал изменению экспрессии ядерных генов, кодирующих белки РЕР комплекса в ответ на дисфункцию хлоропластов у scabra3-2. При этом репрессивный сигнал, посылаемый дефектными хлоропластами в ответ на действие ЦК или, наоборот, отсутствие позитивного сигнала воспринимались избирательно лишь частью генов аппарата транскрипции. Интересно, что в недавнем исследовании Lidón-Soto с соавт. [11] было показано, что ретроградная передача сигналов из поврежденных органелл в условиях солевого стресса активирует экспрессию NEP. Однако механизм такой индукции не был связан с действием АБК, поскольку в условиях длительного воздействия этого гормона гены NEP у растений Col-0 достоверно подавлялись.
Дисфункция хлоропластов, по-видимому, могла повлечь изменение гормонального статуса мутанта и, как следствие, меньшую чувствительность к действию ЦК, которая, возможно, была связана с повышенным содержанием гормона. Косвенным свидетельством в пользу этого являются данные по экспрессии гена ARR5 и генов метаболизма ЦК IPT3, IPT5 и CKX5, накопление транскриптов которых существенно превышало уровни дикого типа.
Пониженная реакция на действие ЦК могла быть также обусловлена изменением баланса между ЦК и АБК. Согласно данным Hricova с с-оавт. [10], полученным методом микрочипирования, у мутанта scabra3-2 была уменьшена экспрессии генов, кодирующих белки изопреноидного пути биосинтеза, включая ген ключевого фермента биосинтеза АБК зеаксантиндегидрогеназы ABA1. Для гена ABA1, продукт которого локализуется преимущественно в строме и тилакоидных мембранах хлоропластов [21], этот результат был нами подтвержден методом ПЦР-РВ (табл. 2). Кроме того, у scabra3-2 оказалась снижена базовая экспрессия гена метаболизма АБК ABA2 и повышен уровень транскриптов гена сигналинга HAB1. Таким образом, плейотропный эффект мутации затрагивал не только экспрессию хлоропластного генома, но и оказывал влияние на регуляцию гормональной системы растения. Среди возможных последствий – нарушение синтеза каротиноидов, которые необходимы как для фотосинтезирующих тканей, где они играют фотозащитную роль, так и для нормального прохождения скотоморфогенеза и последующего развития хлоропластов при переходе к фотоморфогенезу [22].
Неоспоримым свидетельством в пользу прямого участия генов NEP в гормональной регуляции хлоропластных генов могло бы стать изменение их экспрессии при непосредственном связывании гормон-регулируемых транс-факторов с промоторной областью генов NEP. Как показал анализ in silico промоторных областей генов NEP-полимераз, в пределах последовательности в 500 п.н. в направлении 5’ от стартового кодона ATG содержатся предполагаемые цис-элементы для целого ряда АБК и ЦК-регулируемых транс-факторов, включая RAV1, DREB/CBF, RAP2.6, MYB52, АTHB12, ARR11, ARR14 и GLK1. Однако ни один из этих транс-факторов не обнаружил изменений в уровне экспрессии у sca3-2, как следует из данных микрочипирования этого мутанта [10]. Тем не менее, инактивация гена RPOTp способствовала изменению сигнала для целого ряда транс-факторов, при этом некоторые из них (MYB47, NF-YB2) в сильной степени индуцировались АБК. Таким образом, гормон-зависимые ответы, регулируемые этими транс-факторами, могут быть непрямыми, хотя выявление конкретных участников этого процесса и всех ее компонентов остается задачей для будущих исследований.
Изучение биологической роли ЦК и АБК в функционировании аппарата транскрипции хлоропластов было бы неполным без учета их воздействия на уровень хлоропластных белков. Обработка экзогенной АБК не изменяла содержание этих белков у всех исследованных образцов, что для растений дикого типа и мутанта rpotmp соответствовало данным транскрипционного анализа. Однако у мутантной линии scabra3-2 сохранение уровней хлоропластных белков при подавлении накопления транскриптов кодирующих генов в результате обработки ЦК или АБК могло быть связано с особенностями их посттранскрипционной регуляции на фоне измененного генетического фона. Не исключено, что подобный эффект был обусловлен нарушениями деградации хлоропластных белков у мутанта sca3-2. На это указывает уменьшение в 1.5–2 раза экспрессии генов протеаз FtsH8, FtsH9 и DEG1, локализованных в хлоропластах и участвующих в расщеплении пластидных белков [10]. Кроме того, по данным транскриптомного анализа, у мутанта sca3-2 была в 2–3 раза снижена экспрессия четырех генов E3-убиквитинлигаз (At5g01880, At5g01520, At1g57820, At1g66050) [10], связанных с протеасомной деградацией белков. Интересно, что убиквитинлигаза, кодируемая одним из этих генов AtAIRP2 (Arabidopsis ABA-insensitive RING protein 2), причастна к регуляции сигнала АБК, в частности к убиквитинированию ключевых компонентов сигнальной цепи протеинкиназ SNF1 (SnRK) [23], что, наряду с изменением экспрессии генов метаболизма, могло способствовать изменению чувствительности мутанта к действию этого гормона.
Подводя итоги, можно сказать, что гены аппарата транскрипции пластид дифференцированно отвечают на воздействие экзогенных ЦК и АБК. Активация экспрессии или ее ингибирование определяются не только специфичностью действия конкретного гормона, но и нормальным функционированием хлоропластов, контролируемым генетической средой. Инактивация генов пластидных РНК-полимераз ядерного кодирования изменяет профили гормон-зависимой экспрессии активных генов компонентов аппарата транскрипции и хлоропластных генов. При этом наблюдается регуляция как на уровне содержания транскриптов, так и на уровне соответствующих белков.
Исследование выполнено за счет гранта Российского научного фонда (проект № 20-14-00065).
Авторы заявляют об отсутствии конфликтов интересов. Настоящая статья не содержит каких-либо исследований с участием людей и животных в качестве объектов исследований.
Список литературы
Zubo Y.O., Yamburenko M.V., Selivankina S.Y., Shakirova F.M., Avalbaev A.M., Kudryakova N.V., Zubkova N.K., K. Liere K., Kulaeva O.N., Kusnetsov V.V., Börner T. Cytokinin stimulates chloroplast transcription in detached barley leaves // Plant Physiol., 2008. V. 148. P. 1082.
Yamburenko M.V., Zubo Y.O., Vanková R., Kusnetsov V.V., Kulaeva O.N., Börner T. Abscisic acid represses the transcription of chloroplast genes // J. Exp. Bot. 2013. V. 64. P. 4491.
Kusnetsov V.V., Oelmüller R., Sarwat M.I., Porfirova S.A., Cherepneva G.N., Herrmann R.G., Kulaeva O.N. Cytokinins, abscisic acid and light affect accumulation of chloroplast proteins in Lupinus luteus cotyledons without notable effect on steady-state mRNA levels // Planta. 1994. V. 194. P. 318.
Sherameti I., Shahollari B.M.,Westermann M., Cherepneva G., Kusnetsov V., Oelmüller R. Cytokinin stimulates polyribosome loading of nuclear-encoded mRNAs for the plastid ATP synthase in etioplasts of Lupinus luteus: the complex accumulates in the inner-envelope membrane with the CF(1) moiety located towards the stromal space // The Plant Journal. 2004. V. 38. P. 578.
Liere K., Weihe A., Börner T. The transcription machineries of plant mitochondria and chloroplasts: composition, function, and regulation // J. Plant Physiol. 2011. V. 168. P. 1345.
Legen J., Kemp S., Krause K., Profanter B., Herrmann R.G., Maier R. Comparative analysis of plastid transcription profiles of entire plastid chromosomes from tobacco attributed to wild-type end PEP-deficient transcription machineries // Plant J. 2002. V. 31. P. 171.
Lerbs-Mache S. Function of plastid sigma factors in higher plants: regulation of gene expression or just preservation of constitutive transcription? // Plant Mol. Biol. 2011. V. 76. P. 235.
Bychkov I., Kudryakova N., Andreeva A., Pojidaeva E., Kusnetsov V. Melatonin modifies the expression of the genes for nuclear- and plastid encoded chloroplast proteins in detached Arabidopsis leaves exposed to photooxidative stress // Plant Physiology and Biochemistry. 2019. V. 144. P. 404.
Danilova M.N., Kudryakova N.V., Doroshenko A.S., Zabrodin D.A., Rakhmankulova Z.F., Oelmüller R., Kusnetsov V.V. Opposite roles of the Arabidopsis cytokinin receptors AHK2 and AHK3 in the expression of plastid genes and genes for the plastid transcriptional machinery during senescence // Plant Molecular Biology. 2017. V. 93. P. 533.
Hricová A., Quesada V., Micol J.L. The SCABRA3 nuclear gene encodes the plastid RpoTp RNA polymerase, which is required for chloroplast biogenesis and mesophyll cell proliferation in Arabidopsis // Plant Physiol. 2006. V. 141. P. 942.
Lidón-Soto A., Núñez-Delegido E., Pastor-Martínez I., Robles P., Quesada V. Arabidopsis plastid-RNA polymerase RPOTp is involved in abiotic stress tolerance // Plants. 2020. V. 9. P. 834.
Santiago J., Rodrigues A., Saez A., Rubio S., Antoni R., Dupeux F., Park S.-Y., Márquez J.A., Cutler S.R., Rodriguez P.L. Modulation of drought resistance by the abscisic acid receptor PYL5 through inhibition of clade A PP2Cs. // Plant J. 2009. V. 60. P. 575.
Wang M., Lee J., Choi B., Park Y., 2, Sim H.J., Kim H., Hwang I. Physiological and molecular processes associated with long duration of ABA treatment // Front. Plant Sci. 2018. V. 9. P. 176.
Yamburenko M., Zubo Y.O., Börner T. Abscisic acid affects transcription of chloroplast genes via protein phosphatase 2C-dependent activation of nuclear genes: repression by guanosine-3′-5′-bisdiphosphate and activation by sigma factor 5 // Plant J. 2015. V. 82. P. 1030.
Bligny M., Courtois F., Thaminy S., Chang Ch.-Ch., Lagrange Th., Baruah-Wolff J., Stern D., Lerbs-Mache S. Regulation of plastid rDNA transcription by interaction of CDF2 with two different RNA polymerases // The EMBO J. 2000. V. 19. P. 1851.
Courtois F., Merendino L., Demarsy E., Mache R., Lerbs-Mache S. Phage-type RNA polymerase RPOTmp transcribes the rrn operon from the PC promoter at early developmental stages in Arabidopsis // Plant Physiol. 2007. V.145. P. 712.
Swiatecka-Hagenbruch M., Liere K., Börner T. High diversity of plastidial promoters in Arabidopsis thaliana // Mol. Genet. Genomics .2007. V. 277. P. 725.
Tarasenko V.I., Katyshev A.I., Yakovleva T.V., Garnik E.Y., Chernikova V.V., Konstantinov Y.M., Koulintchenko M.V. RPOTmp, an Arabidopsis RNA polymerase with dual targeting, plays an important role in mitochondria, but not in chloroplasts // J. Exp. Bot. 2016. V. 67. P. 5657.
Kühn K., Richter U., Meyer E.H., Delannoy E., de Longevialle A.F., Börner T., Millar A.H., Small I., Whelan J. Phage-type RNA polymerase RPOTmp performs gene-specific transcription in mitochondria of Arabidopsis thaliana // Plant Cell. 2009. V. 21. P. 2762.
Bastakis E., Hedtke B., Klermund C., Grimm B., Schwechheimera C. LLM-domain B-GATA transcription factors play multifaceted roles in controlling greening in Arabidopsis // The Plant Cell. 2018. V. 30. P. 582.
Schwarz N.U., Iven T., Brückle L., Melzer M., Feussner I., Jahns P. Tissue-specific accumulation and regulation of zeaxanthin epoxidase in Arabidopsis reflect the multiple functions of the enzyme in plastids // Plant Cell Physiol. 2015. V. 56. P. 346.
Barrero J.M., Piqueras P., Gonza’lez-Guzma’n M., Serrano R., Rodrı’guez P.L.,Ponce M.R., Micol J.L. A mutational analysis of the ABA1 gene of Arabidopsis highlights the involvement of ABA in vegetative development // J. Exp. Bot. 2005. V. 56. P. 2071.
Cho S.K., Ryu M.Y., Seo D.H., Kang B.G., Kim W.T. The Arabidopsis RING E3 ubiquitin ligase AtAIRP2 plays combinatory roles with AtAIRP1 in abscisic acid-mediated drought stress responses // Plant Physiol. 2011. V. 157. P. 2240.
Дополнительные материалы отсутствуют.
Инструменты
Физиология растений


