Генетика, 2019, T. 55, № 7, стр. 854-858
Причины эксцесса частоты митотипа SCH34 в популяции амурского осетра, Acipenser schrenckii (Acipenseridae), согласно анализу полных митохондриальных геномов
1 Федеральный научный центр Биоразнообразия наземной биоты Восточной Азии Дальневосточного отделения Российской академии наук
690022 Владивосток, Россия
* E-mail: shedko@biosoil.ru
Поступила в редакцию 06.11.2018
После доработки 28.11.2018
Принята к публикации 03.12.2018
Аннотация
Большинство видов осетров находятся под угрозой исчезновения и включены в разнообразные Красные списки. Исследование спектров аллельных частот может помочь в оценке и мониторинге состояния их популяций. Нами секвенированы девять полных митогеномов амурского осетра, представляющих собой семь различных вариантов контролирующего региона мтДНК, один из которых (SCH34), согласно полученным ранее данным, имеет необычно высокую частоту в популяции. Селективно значимых замен в нуклеотидных последовательностях, кодирующих белки, а также замен в других функциональных участках митохондриального генома, выделяющих митотип SCH34 среди других, не найдено. Один из трех митогеномов, имевших один и тот же митотип SCH34 контролирующего региона, нес нуклеотидную замену за его пределами. Рассчитанный минимальный эволюционный возраст митотипа SCH34 составил порядка 4500–5400 лет. Высокая частота SCH34 и близких к нему митотипов (производных от него и отличающихся по одной-двум нуклеотидным позициям) в современной популяции амурского осетра не могла быть вызвана ни отбором, ни хозяйственной деятельностью человека и, скорее всего, обусловлена прохождением одной из его изолированных популяций через фазу низкой численности (“бутылочное горлышко”) в прошлом.
Хозяйственная деятельность человека часто негативным образом сказывается на благополучии тех или иных видов организмов напрямую через промысел или путем изменения среды их обитания. Чаще всего это выражается в падении их численности. Падение численности может сопровождаться изменением частот аллелей (особенно в тех случаях, когда изъятию подверглась какая-то определенная часть видовой популяции). Аналогичный эффект могут вызывать и естественные процессы – отбор, дрейф генов. Решить каковы причины сдвига частот аллелей (вмешательство человека или результат естественного хода событий) – часто непростая задача, но в некоторых случаях она представляется актуальной.
Популяции осетровых р. Амур – калуги Acipenser dauricus и амурского осетра A. schrenckii в настоящий момент находятся в депрессивном состоянии [1, 2]. Ранее оба вида были широко распространены по всему бассейну Амура, но в настоящее время они сохранились лишь в нижнем течении Амура. Падение численности амурских осетровых совпало с более чем десятикратным (в сравнении с началом прошлого века) ростом численности населения в бассейне р. Амур, превысившей оценку в 75 млн человек [3], и, вероятно, вызвано сопровождающими этот процесс негативными явлениями – ростом промышленной и любительской добычи осетровых, загрязнением природной среды бытовыми и промышленными отходами и т.п. В последние десятилетия положение усугубилось тем, что в связи с падением численности каспийских осетровых на популяции калуги и амурского осетра усилился пресс браконьерского вылова.
Ранее при анализе изменчивости контролирующего региона мтДНК (D-петли) в выборке амурских осетров, собранных в бассейне нижнего Амура [4], было выявлено 73 различных митотипа. За исключением одного из них (митотипа SCH34), встречаемость каждого из митотипов в выборке варьировала от одного до трех и составила в среднем 1.3. Митотип SCH34 был обнаружен у 16 особей. На фоне остальных частота данного митотипа выглядит аномально высокой. Именно высокая представленность митотипа SCH34 и обусловила, согласно результатам теста Ювенса–Воттерсена, статистически значимое отклонение частотного спектра митотипов D-петли от ожидаемого для равновесной популяции.
Повышенная частота митотипа SCH34 может быть результатом как действия в прошлом естественного отбора или генетического дрейфа, так и каких-то недавних факторов, связанных с хозяйственной деятельностью человека, которая могла сказаться на генетическом составе популяции амурского осетра.
В первом случае (естественный отбор) можно ожидать, что митотип SCH34 должен нести селективно значимые замены в каких-то (прежде всего в последовательностях белковых генов) областях митохондриального генома.
Во втором случае (дрейф генов) можно предполагать, что частота данного митотипа выросла в прошлом по каким-то случайным причинам (прохождение популяции через “бутылочное горлышко”, к примеру) и, несмотря на то что она постоянно размывалась мутациями, до сих пор сохранилась на сравнительно высоком уровне. Тогда можно ожидать, что в митотипах, имеющих один и тот же вариант последовательности D-петли (SCH34), в других областях митогенома могли успеть накопиться какие-то мутации.
В третьем случае из-за краткости промежутка времени (в бассейне Амура хозяйственная деятельность получила свое интенсивное развитие лишь с начала прошлого столетия) мутаций за пределами D-петли ожидать не приходится.
Задача настоящей работы – оценить вероятность каждого из этих сценариев с помощью секвенирования и анализа полных митохондриальных геномов амурского осетра.
Материалом для работы послужили образцы тотальной ДНК, выделенной от амурских осетров, собранных и проанализированных ранее на предмет изменчивости у них контролирующего региона мтДНК [4], а также один образец из новых сборов.
Для секвенирования полных митохондриальных геномов амурского осетра были отобраны три образца (выделены от особей с длиной тела 54, 151 и 202 см), имевшие один и тот же тип контролирующего региона мтДНК – SCH34. Кроме них были отобраны образцы, имевшие близкие к SCH34 митотипы – SCH20 и SCH25. Кроме того, из той же BG мтДНК-гаплогруппы (о гаплогруппах амурского осетра см. [4]) были взяты образцы с более отдаленными от SCH34 митотипами – SCH75 и SCH1 (митогеном с этим митотипом секвенирован нами ранее [5], номер доступа в GenBank – KX276659). Из SM мтДНК-гаплогруппы амурского осетра, в дополнение к секвенированному нами ранее [5] митогеному с митотипом SCH52 (KX276660), в анализ был включен образец с митотипом SCH65.
Полные митохондриальные геномы амурского осетра в каждом случае были амплифицированы в двух реакциях с помощью набора 6kB+ (СибЭнзим, Новосибирск) с использованием двух пар праймеров [6]: S-LA-16S-L и H12293-Leu; L12321-Leu и S-LA-16S-H. Секвенирование полученных ампликонов, помеченных индивидуальными RL MID-адаптерами и смешанных в эквимолярной пропорции, проведено на приборной базе ЦКП “Биотехнология и генетическая инженерия” (ФНЦ Биоразнообразия ДВО РАН, г. Владивосток) методом пиросеквенирования с помощью секвенатора Roche GS Junior. Приготовление быстрой библиотеки с лигированными адаптерами, проведение эмульсионной ПЦР, секвенирование с реагентами GS Junior Titanium Series выполнялись согласно инструкциям фирмы-изготовителя прибора и реактивов – 454 Life Science Corp., A Roche Company, Branford, CT 06405, USA. Анализ полученных прочтений и сборка митогеномов осуществлены с помощью пакета программ GS De Novo Assembler v. 2.7 (Roche). Анализ изменчивости митогеномов выполнен с помощью программ PAUP v. 4a163 [7] и MEGA6 [8].
Митогеномы амурского осетра были секвенированы со средним покрытием в сто и более крат. Собранные последовательности были депонированы в GenBank (NCBI) под номерами доступа MH973728–MH973734.
Размер митохондриального генома у амурского осетра составил 16 608 пар нуклеотидов (пн) у митогеномов SCH34а–с, SCH20 и SCH25, 16 676 пн у митотипа SCH65 и 16 690 пн у митотипа SCH75. Вариация вызвана изменчивостью контролирующего региона мтДНК: сравнительно протяженной делецией, дифференцирующей гаплогруппы SM и BG, а также неодинаковым числом копий повторяющихся элементов. Для последующего анализа из всех копий повторяющихся элементов в контролирующем регионе мтДНК осетров, как и ранее [4], оставляли лишь предпоследнюю полную и последнюю неполную копию. Таким образом, длина матрицы выравненных последовательностей составила 16 524 нуклеотидных позиций.
У трех образцов амурского осетра, имевших один и тот же тип контролирующего региона мтДНК (SCH34), было найдено два варианта митогеномов, различающихся одной молчащей нуклеотидной заменой в стартовом кодоне гена ND3 (замена A > G у митотипа SCH34с в позиции 9695 – см. рис. 1).
Рис. 1.
Вариабельные позиции в секвенированных митогеномах амурского осетра из SM (SCH52 и SCH65) и BG (остальные последовательности) гаплогрупп. Позиции с мутациями, приводящими к аминокислотным замещениям, выделены полужирным с подчеркиванием. Тире – делеции. Функциональные области: R – гены рРНК, I – межгенные спейсеры, P – гены белков, T – гены тРНК, D – контролирующий регион (D-петля).

Всего, с учетом секвенированных ранее, нами было получено восемь различающихся вариантов полных митохондриальных геномов амурского осетра. Их филогенетические взаимоотношения, установленные MJ-методом [9] с помощью пакета программ PopART [10], представлены на рис. 2. Аналогичный порядок их филогенетических связей был установлен с помощью пакета программ PAUP при использовании методов максимальной экономии (MP) или максимального правдоподобия (ML) на основе оптимальной модели TrN+I .
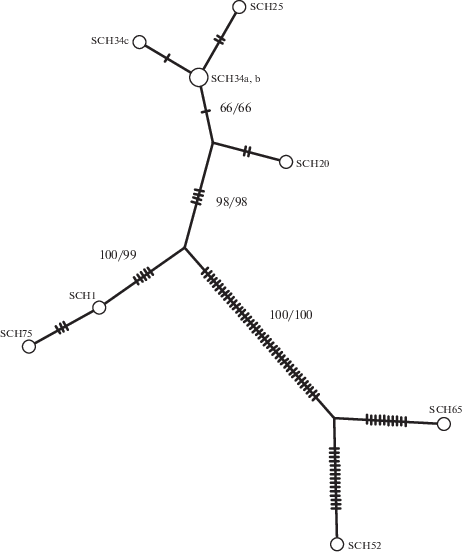
Рис. 2.
Филогенетические взаимоотношения (MJ-нетворк) секвенированных митогеномов амурского осетра. Поперечные черточки – мутационные замены. Цифры у ветвей – бутстреп-поддержка (% от 1000 псевдослучайных реплик) в случае построения MP- и (отделены косой чертой) ML-деревьев.
В целом в девяти митогеномах амурского осетра изменчивость наблюдалась по 95 позициям. В области D-петли найдена 41 варьирующая позиция с нуклеотидными заменами и одна делеция длиной 14 пн; в последовательностях белковых генов – 32 варьирующие позиции; в межгенных спейсерах – пять позиций; в генах рРНК и тРНК – две и одна соответственно.
В белковых генах лишь две точечные нуклеотидные замены приводили к аминокислотным замещениям в последовательностях белков11 – Thr > Ile в гене ND2 у митотипов SCH52 и SCH65 и Val > Met в гене COI у митотипа SCH52. Оба этих митотипа принадлежат к SM-гаплогруппе. Поэтому можно заключить, что наблюдаемый в настоящее время в популяции амурского осетра избыток митотипа SCH34 не обусловлен какими-то значимыми его селективными отличиями от остальных митотипов из BG-гаплогруппы по генам, кодирующим последовательности белков. В этом отношении митотип SCH34 и близкие к нему, но редко встречающиеся митотипы SCH20 и SCH25 селективно эквивалентны. Аналогичный вывод можно сделать и при рассмотрении отличий этих митотипов по другим функциональным областям митогенома – не обнаруживается ни одной позиции с мутациями, свойственными только митотипу SCH34.
Фактор хозяйственной деятельности человека в свете полученных данных также представляется несущественным. Различие между девятью митогеномами амурского осетра в среднем составило 0.00167 ± 0.00020 замен на позицию (p-расстояние) для всей последовательности (16 524 позиций в матрице данных). Для области D-петли (811 позиций) и остальной части митогенома без D-петли (15 713 позиций) – 0.01682 ± 0.00257 и 0.00089 ± ± 0.00011 соответственно. Если расчет провести лишь для митогеномов, входящих в состав BG-гаплогруппы, то соответствующие оценки составят 0.00043 ± 0.00010, 0.00470 ± 0.00160 и 0.00021 ± ± 0.00006. Отсюда следует, что у амурского осетра скорость нуклеотидных замещений в контролирующем регионе примерно в 20 раз выше скорости нуклеотидных замещений, характерной для остальной части митохондриального генома. Тогда, взяв известную оценку скорости нуклеотидных замещений в контролирующем регионе мтДНК осетров – 0.782–0.939 × 10–7 замещений на позицию/год/линию [11], можно получить скорость замещений за пределами D-петли – 3.91–4.70 × 10–9. Средние нуклеотидные отличия трех митогеномов, принадлежащих к одному и тому же митотипу SCH34, вне пределов контролирующего региона оказались равными 1/15 713/3 = 0.0000212 замен. Отсюда минимальный эволюционный возраст митотипа SCH34 составляет 0.0000212/3.91 × 10–9–0.0000212/4.70 × 10–9 = 4500–5400 лет. То есть в популяции амурского осетра этот митотип появился задолго до того, как человек мог приступить к кардинальным преобразованиям природной среды в бассейне р. Амур.
Таким образом, из трех возможных альтернатив, объясняющих эксцесс частоты митотипа SCH34, дрейф генов представляется наиболее вероятной. Митотип SCH34 и близкие к нему митотипы (SCH21–33, 36–39), отличающиеся от него по одной-двум нуклеотидным позициям, составляют большинство (56%) в BG-гаплогруппе ([4]: рис. 1). Наличие у амурского осетра двух гаплогрупп мтДНК может быть вызвано существованием в прошлом двух изолированных популяций этого осетра, что обсуждалось нами ранее [4]. Возможно, одна из них прошла через фазу резкого падения численности (“бутылочное горлышко”) и последующий интенсивный восстановительный рост, что привело к доминированию в ней одного из митотипов. Во второй популяции эти процессы, если и происходили, то не имели такого драматического влияния на частотный спектр митотипов.
Работа выполнена при финансовой поддержке Дальневосточного отделения РАН (Программа “Дальний Восток”, грант № 18-4-032).
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Ruban G., Qiwei W. Acipenser schrenckii // The IUCN Red List of Threatened Species. 2010. e.T228A13039546. https://doi.org/10.2305/IUCN.UK.2010-1.RLTS.T228A13039546.en (Downloaded on 16 October 2018).
Ruban G., Qiwei W. Huso dauricus // The IUCN Red List of Threatened Species. 2010. e.T10268A3186676. https://doi.org/10.2305/IUCN.UK.2010-1.RLTS.T10268A3186676.en (Downloaded on 16 October 2018).
Amur-Heilong River Basin Reader / Eds Simonov E.A., Dahmer T.D. Hong Kong, China: Ecosystems Ltd., 2008. 442 p.
Шедько С.В., Мирошниченко И.Л., Немкова Г.А. и др. Изменчивость митохондриальной ДНК, историческая демография и популяционная структура амурского осетра, Acipenser sсhrenckii Brandt, 1869 // Генетика. 2015. Т. 51. № 2. С. 200–216. https://doi.org/10.7868/ S0016675815020125
Шедько С.В. Низкий уровень различий митогеномов сахалинского осетра Acipenser mikadoi Hilgendorf, 1892 и зеленого осетра A. medirostris Ayeres, 1854 (Acipenseridae) свидетельствует об их недавней дивергенции // Биол. моря. 2017. Т. 43. № 2. С. 144–147.
Inoue J.G., Miya M., Tsukamoto K., Nishida M. A mitogenomic perspective on the basal teleostean phylogeny: resolving higher-level relationships with longer DNA sequences // Mol. Phylogenet. Evol. 2001. V. 20. № 2. P. 275–285. https://doi.org/10.1006/mpev.2001.0970
Swofford D.L. PAUP*: Phylogenetic Analysis Using Parsimony (*and other methods). Version 4.0. Sunderland, Mass.: Sinauer Assoc., 2002.
Tamura K., Stecher G., Peterson D. et al. MEGA6: Molecular Evolutionary Genetics Analysis version 6.0 // Mol. Biol. Evol. 2013. V. 30. № 12. P. 2725–2729. https://doi.org/10.1093/molbev/mst197
Bandelt H., Forster P., Röhl A. Median-joining networks for inferring intraspecific phylogenies // Mol. Biol. Evol. 1999. V. 16. № 1. P. 37–48. https://doi.org/10.1093/oxfordjournals.molbev.a026036
Leigh J.W., Bryant D. PopART: full-feature software for haplotype network construction // Methods Ecol. Evol. 2015. V. 6. № 9. P. 1110–1116. https://doi.org/10.1111/2041-210X.12410
Shedko S.V. Revision of nucleotide substitution rate in mtDNA control region of white sturgeon Acipenser transmontanus (Acipenseridae) // e-print arXiv:1705.02336 [q-bio. PE]. 2017. 8 p.
Дополнительные материалы отсутствуют.


