Геоэкология. Инженерная геология, гидрогеология, геокриология, 2021, № 1, стр. 3-13
АММОНИЙНЫЙ АЗОТ В ФИЛЬТРАТЕ ПОЛИГОНОВ ТКО: ОБРАЗОВАНИЕ, ТРАНСФОРМАЦИЯ, ДОЛГОСРОЧНОСТЬ ЗАГРЯЗНЕНИЯ
И. В. Галицкая 1, *, В. С. Путилина 1, **, Т. И. Юганова 1, ***
1 Институт геоэкологии им. Е. М. Сергеева РАН
101000 Москва, Уланский пер., 13, стр. 2, Россия
* E-mail: galgeoenv@mail.ru
** E-mail: vputilina@yandex.ru
*** E-mail: tigryu@gmail.com
Поступила в редакцию 22.10.2020
После доработки 22.10.2020
Принята к публикации 05.11.2020
Аннотация
В настоящей статье на основании анализа отечественной и зарубежной литературы проведено исследование вопросов, связанных с продолжительностью выделения аммонийного азота из твердых коммунальных отходов в свалочный фильтрат, форм нахождения азота в фильтрате, процессов связывания и преобразования ${\text{NH}}_{4}^{ + }$ в свалочном теле. Рассмотрены механизмы обратимой и необратимой сорбции иона аммония, приведены значения коэффициентов его распределения для различных горных пород. Проанализированы процессы трансформации ${\text{NH}}_{4}^{ + }$ в аэробных и анаэробных условиях, в том числе недавно установленный процесс анаэробной микробиальной реакции окисления ${\text{NH}}_{4}^{ + }$ нитритом, названной “анаммокс” и выполняющей важную роль в биологическом цикле азота. Процессы образования и трансформации ${\text{NH}}_{4}^{ + }$ на свалках и полигонах ТКО наглядно прослежены на примере утилизации отходов в аэробных и анаэробных свалках-биореакторах.
ВВЕДЕНИЕ
Несмотря на новые прогрессивные методы утилизации твердых коммунальных отходов (ТКО), во многих странах по-прежнему преобладает захоронение отходов на свалках и полигонах; таким образом, проблемы загрязнения природных сред на участках расположения данных объектов остаются чрезвычайно актуальными. В настоящее время все больший интерес вызывают вопросы, связанные с продолжительностью влияния закрытых полигонов и свалок. Один из наиболее острых аспектов – длительность загрязнения свалочного фильтрата как источника воздействия на качество водных систем на участках размещения свалок и полигонов ТКО.
Как известно, свалочный фильтрат содержит значительное количество загрязняющих веществ, в том числе и высокотоксичных. В предыдущей статье [14] на основании анализа отечественных и зарубежных литературных источников проведено исследование длительности выщелачивания металлов из свалочного тела, изменения их подвижности в аэробных и анаэробных условиях и форм связывания в твердой фазе. Сделан вывод, что риск поступления металлов в подземные воды после прекращения эксплуатации полигона ТКО минимален. В отличие от этого, как следует из многих публикаций, концентрации другого важнейшего компонента фильтрата – аммонийного азота – в свалочном фильтрате остаются очень высокими в течение длительного периода.
Аммоний, как правило, присутствует в свалочных фильтратах в весьма значительных концентрациях, что является одной из основных причин токсичности фильтрата [19, 23, 32]. Неорганический азот в форме аммиака (NH3) и иона аммония (${\text{NH}}_{4}^{ + }$) признан одним из наиболее распространенных загрязнителей подземных вод, образующихся в результате деятельности по удалению отходов [7]. Учитывая его подвижность при определенных условиях, аммоний обычно рассматривается как основной компонент загрязнения при оценке риска загрязнения водных систем на участках расположения свалок и полигонов [16]. В последние годы внимание обращается также на органический азот, который признан опасным компонентом водной среды. Результаты исследований показали, что биологически очищенный свалочный фильтрат содержит до 60 мг/л органического азота, и что в свалочном фильтрате органический азот является более биостойким, чем другие органические вещества [35, 36].
В данной статье рассматриваются вопросы продолжительности выделения аммония из твердых коммунальных отходов в фильтрат, форм нахождения азота в свалочном фильтрате, процессов связывания и преобразования аммония в свалочном теле. Исследование проводилось на основании анализа отечественной и зарубежной литературы.
ПРОДОЛЖИТЕЛЬНОСТЬ ВЫДЕЛЕНИЯ АММОНИЯ ИЗ СВАЛОЧНОГО ТЕЛА
Исследованиям продолжительности выделения аммония из ТКО, приводящего к загрязнению свалочного фильтрата, посвящены многочисленные публикации, однако тенденции уменьшения концентрации аммонийного азота в фильтратах выявлены далеко не во всех работах.
По данным, приведенным в [19], во многих случаях концентрации аммонийного азота в фильтратах очень высоки, могут достигать 2000 мг/л, и тенденции к снижению концентрации со временем не наблюдается. Данные, приведенные в табл. 1, свидетельствуют, что концентрации аммония остаются высокими даже в фильтрате с более старых свалок. В исследовании 50 полигонов Германии содержание аммонийного азота не показало значительного снижения через 30 лет после закрытия полигона [20]. По данным [12], в период от кислой до метаногенной фазы значительные изменения концентрации аммония отсутствовали, среднее значение составляло 740 мгN/л.
Таблица 1.
Концентрации аммония в свалочных фильтратах (все значения получены для старых свалок в метаногенной фазе) [19]
| Аммоний-N, мг/л | Описание и ссылка |
|---|---|
| 110 | Средняя концентрация аммония для 104 старых свалок, Дания [18] |
| 233 | Сводные результаты для свалки Sandsfarm, Великобритания [28] |
| 282 | Сводные результаты для свалки Bishop Middleham, Великобритания [28] |
| 399 | Сводные результаты для свалки Odsal Wood, Великобритания [28] |
| 43 | Сводные результаты для свалки East Park Drive, Великобритания [28] |
| 30 | Сводные результаты для свалки Marton Mere, Великобритания [28] |
| 12–1571 | Диапазон концентраций для 21–30-летних свалок, Германия [20] |
| 445 | Средняя концентрация для 21–30-летних свалок, Германия [20] |
| 740 | Средняя концентрация [12] |
При исследовании 43 полигонов Финляндии отмечалось, что концентрации аммонийного азота немного увеличились через 30 лет после закрытия [1].
В отличие от вышеприведенных примеров, результаты исследований [29, 34] позволяют судить о возможном снижении концентрации аммонийного азота с увеличением продолжительности депонирования отходов и об ориентировочном времени достижения концентраций, не представляющих опасности для окружающей природной среды.
Результаты определения содержания аммонийного, нитритного и нитратного азота в отходах разного срока захоронения на четырех объектах Пермского края [34] показали, что с увеличением продолжительности депонирования отходов в водной вытяжке отмечается снижение концентраций аммонийного и нитритного азота, хлорида, значений ХПК, БПК5, сухого остатка наряду с увеличением содержания в отходах нитратного азота (рис. 1).
Рис. 1.
Изменение содержания аммонийного, нитритного и нитратного азота в отходах разных сроков захоронения [34].
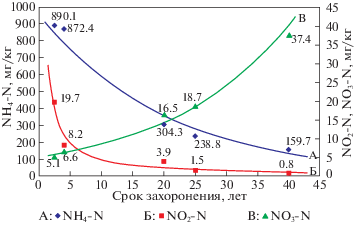
По мнению авторов, высокие концентрации аммонийного азота в отходах со сроком захоронения 2–6 лет объясняются процессами биодеструкции легкоразлагаемых фракций ТКО с образованием жирных кислот, аминокислот, глицерина, полисахаридов, аммиака. Уменьшение содержания нитритного азота связано с замедлением процессов денитрификации отходов и их переходом в нитраты, а низкое содержание нитритного азота в отходах с продолжительностью депонирования более 30 лет свидетельствует о стабилизации биохимических процессов разложения отходов и завершении процессов денитрификации.
В статье [29], посвященной оценке долгосрочных эмиссий объектов захоронения ТКО, отмечается, что срок достижения приемлемых концентраций ионов аммония в фильтрате полигонов составляет 110–140 лет.
Ряд интересных результатов об особенностях изменения содержания аммонийного азота получен при исследовании форм азота в свалочном фильтрате на полигоне в шт. Кентукки (США) [36]. Полигон состоял из восьми отдельных секций. Секция 3 ‒ неактивная (возраст 30 лет), она была закрыта и перестала принимать ТКО. Секции 5, 7 и 8 – действующие, со средним возрастом депонирования 16, 9 лет и 2.5 года соответственно. Секция 5 была выбрана для исследования в качестве “свалки-биореактора”, т.е. осуществлялась рециркуляция фильтрата с возможным добавлением жидкости: нитрифицированный фильтрат, промышленные жидкости, дренажные воды и т.д. Секция 7 использовалась как “контроль” без добавления жидкости. Секция 8 была построена после исследования “свалки-биореактора”.
Концентрации общего азота и различных форм азота в необработанных и обработанных образцах фильтрата представлены в табл. 2 (в обозначение образца включен номер секции).
Таблица 2.
Формы азота в свалочных фильтратах полигона в шт. Кентукки (США) в различных условиях [36]
| Обозна-чение образца | Возраст секции, лет | Характеристика фильтрата | Концентрация вида азота, мг N/л | ||||
|---|---|---|---|---|---|---|---|
| Общий азот | ${\text{NH}}_{4}^{ + }$ | ${\text{NO}}_{3}^{ - }$ | ${\text{NO}}_{2}^{ - }$ | Органический азот белков (по Лоури) | |||
| KY-8 | 2.5 | Свежий | 1462.7 ± 43.3 | 1297.5 ± 3.5 | н.о.а | 0.8 | 106.4 |
| Аэрированный 21 сут | 189.0 ± 4.2 | 22.40 ± 1.6 | 0.9 | 1.1 | 62.9 | ||
| Аэрированный 38 сут | 148.0 ± 2.8 | 4.54 ± 0.1 | 1.0 | 0.6 | н.д.б | ||
| Аэрированный 53 сут | 227.0 ± 4.2 | 23.00 ± 1.0 | 4.8 | 0.5 | н.д. | ||
| Гидрофильная фракция | 244.0 ± 13.4 | 94.1 ± 1.8 | н.о. | 0.4 | 71.7 | ||
| KY-7 | 9 | Свежий | 1409.8 ± 24.4 | 1309.5 ± 2.1 | н.о. | 0.4 | 81.2 |
| Аэрированный 21 сут | 93.0 ± 1.4 | 7.2 ± 0.2 | 3.0 | 0.3 | 33.9 | ||
| Аэрированный 38 сут | 86.0 ± 0.0 | 2.3 ± 0.1 | 3.2 | 0.4 | н.д. | ||
| Аэрированный 53 сут | 102.0 ± 2.8 | 6.1 ± 0.1 | 3.0 | 0.3 | н.д. | ||
| Гидрофильная фракция | 53.8 ± 1.5 | 23.3 ± 0.4 | н.о. | 0.1 | 36.6 | ||
| KY-5 | 16 | Свежий | 574.2 ± 24.5 | 509.0 ± 18.3 | 0.1 | 10.6 | 35.8 |
| Аэрированный 21 сут | 33.5 ± 5.0 | 0.9 ± 0.0 | 1.1 | 4.1 | 22.5 | ||
| Гидрофильная фракция | 41.0 ± 1.8 | 27.7 ± 0.4 | 0.0 | 3.9 | 23.6 | ||
| KY-3 | 30 | Свежий | 516.6 ± 18.2 | 491.5 ± 2.1 | н.о. | н.о. | 16.7 |
| Аэрированный 21 сут | 18.5 ± 2.1 | 1.4 ± 0.0 | 0.5 | 0.7 | 13.8 | ||
| Гидрофильная фракция | н.д. | н.д. | н.д. | н.д. | 14.3 | ||
Во всех необработанных фильтратах были обнаружены значительные количества аммонийного азота в качестве преобладающей формы и незначительное содержание нитрата и нитрита. Неорганические формы аммонийного азота образовались в результате восстановления нитратов, поступивших в свалку, а также ферментации органических веществ, в основном, протеинов. Концентрации аммонийного азота составляли 1298 и 1310 мг/л в фильтратах из секций с возрастом депонирования 2.5 (KY-8) и 9 лет (KY-7) соответственно. В фильтратах из секций с возрастом депонирования отходов 16 (KY-5) и 30 (KY-3) лет эти концентрации значительно ниже – 509 и 492 мг/л. Снижение содержания аммонийного азота, в отличие от предыдущих исследований, было связано с разбавлением в результате обслуживания “свалки-биореактора”, поступлением атмосферных осадков и т.д.
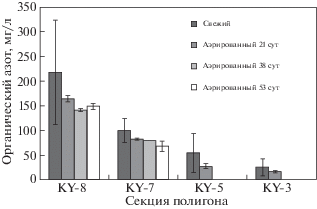
Следует отметить, что при различных состояниях стабилизации в фильтратах было обнаружено значительное количество органического азота (рис. 2). Его концентрация в неочищенных фильтратах варьировала от 25 до 218 мг/л. Из-за высокого уровня аммония в необработанных образцах наблюдались большие вариации при определении общего азота и, следовательно, при определении органического азота. Азотсодержащее органическое вещество имело явную тенденцию к снижению с возрастом полигона, что аналогично поведению общего органического вещества, измеренного как общий органический углерод.
Рис. 2.
Концентрация органического азота в свалочных фильтратах секций полигона в шт. Кентукки при различных состояниях стабилизации [36].
В большинстве свалочных фильтратов идентифицированы две основные категории органического азота: белковый органический азот и органический азот, полученный из гумусовых веществ. Белковый органический азот присутствовал, главным образом, в свежих фильтратах. Считается, что его источником являются пищевые отходы. Возможный путь разложения белкового органического азота включает два этапа: гидролиз от белков до пептидов и аминокислот, затем аммонификация от аминокислот до ионного аммония. Поэтому выделение аммония из ТКО в фильтрат происходит медленнее, чем у легкорастворимых соединений. Это частично объясняет относительно высокую концентрацию аммония в фильтрате из более старой секции полигона (KY-7).
Для лучшего понимания процессов, приводящих к изменению концентрации аммонийного азота в течение жизненного цикла свалочного тела, необходимы дальнейшие исследования, в том числе поведения различных видов органического азота в свалочных фильтратах.
ПРОЦЕССЫ СВЯЗЫВАНИЯ И ПРЕОБРАЗОВАНИЯ АММОНИЯ
Процессы сорбции
Сорбция иона ${\text{NH}}_{4}^{ + }$ в основном осуществляется за счет катионообменных реакций на отрицательно заряженных минеральных поверхностях. В водных растворах с низким или нейтральным pH катионный обмен происходит главным образом на поверхностях глинистых частиц, но при значениях pH выше нейтрального, значительный вклад также вносит сорбция на оксигидроксидах железа.
Относительная сила, с которой катионы связываются с заряженной минеральной поверхностью, определяется их коэффициентами селективности, которые являются функцией как минеральной поверхности, так и состава раствора. Относительную селективность в порядке уменьшения сродства к участкам катионного обмена можно представить как Al3+ > Ca2+ > Mg2+ > ${\text{NH}}_{4}^{ + }$ > > K+ > H+ > Na+ [9].
В фильтрате полигонов ТКО ион ${\text{NH}}_{4}^{ + }$ – не самый распространенный катион. Доминирующий катион – это обычно натрий, который наряду с калием, кальцием и магнием, конкурирует с ионами ${\text{NH}}_{4}^{ + }$ за обменные участки. Значения коэффициентов распределения (Kd) иона аммония, определенные для одних и тех же пород, но различными методами (и особенно в разных по составу растворах) могут варьировать более чем на два порядка: например, для мела (Lower Chalk) Kd = 0–0.03 мл/г, юрской глины (Lias Clay) – 1.2–2.6 мл/г, валунной глины (Cohesive Boulder Clay) – 2–4 мл/г (табл. 3) [7]. В большинстве случаев миграцию иона ${\text{NH}}_{4}^{ + }$ определяет конкурентный катионный обмен [10]. Однако имеются подтверждения, что сорбция ${\text{NH}}_{4}^{ + }$ не всегда происходит по механизму обмена. Например, сорбция ${\text{NH}}_{4}^{ + }$ иллитом и другими глинистыми минералами типа 2:1 может быть фактически необратимым процессом, поскольку ион ${\text{NH}}_{4}^{ + }$ поступает в состав внутрислойной глинистой матрицы. В отложениях со значительным содержанием иллита доля ${\text{NH}}_{4}^{ + }$, зафиксированного в межслоевом пространстве, обычно может составлять 20–40% от общего азота [6]. Глинистые отложения представляют собой важный “резервуар” ионов ${\text{NH}}_{4}^{ + }$, который может поддерживать устойчивое выделение этого поллютанта [10].
Таблица 3.
Коэффициенты распределения аммония для различных горных пород в Великобритании [7]
| Литологияа | Диапазон Kd, мл/гб | Комментарии |
|---|---|---|
| Мел Chalk | 0–0.03 | Низкая достоверность, поскольку изотермы не идентифицированы. |
| Триасовый песчаник Triassic Sherwood Sandstone |
0–0.2–0.6 | Приемлемая достоверность, поскольку было проведено несколько независимых тестов, хотя большинство значений получены только на одном участке (Burntstump). |
| Известняк Lincolnshire Limestone |
0.065–0.65 | Низкая достоверность, поскольку изотермы не идентифицированы. |
| Глауконитовый песок Lower Greensand “Hassock” |
0.18–1.8 | Низкая достоверность, поскольку не было получено никаких изотерм. Измерения проводились только по литологии “Hassock”. В общем, для Lower Greensand в качестве нижней границы следует использовать нуль. |
| Глауконитовый песок Lower Greensand (недифференцированный) |
0–1.8 | |
| Красный песчанистый мергель Red Crag | 0.05–0.5 | Низкая достоверность, поскольку изотермы не идентифицированы. |
| Каолинит Oxford Clay | 0.135–1.35 | На основе моделирования экспериментов в колонке. |
| Аргиллит Mercia Mudstone | 0.5–5 | Низкая достоверность, поскольку изотермы не идентифицированы. |
| Смектит Gault Clay | 0.65–6.5 | Низкая достоверность, поскольку изотермы не идентифицированы. |
| Юрская глина Lias Clay | 1.2–2.6 | Низкая достоверность, поскольку изотермы не идентифицированы. |
| Угольная глина Coal Measures Clay |
0.18–1.8 | На основе моделирования экспериментов в колонке с глинисто-песчаными смесями. Значение 1.8 мл/г получено для системы со 100% глины. |
| Песок и гравий, без прослоев | 0–0.4–0.9 | Приемлемая достоверность, поскольку было проведено несколько независимых тестов. Однако это, естественно, весьма неоднородная литология, поэтому следует использовать полную характеристику участка, если используется “глинистый” диапазон значений. |
| Песок и гравий, глинистые | 0.4–0.9 | |
| Валунная глина Cohesive Boulder Clay |
2–4 | Низкая достоверность, поскольку изотермы не идентифицированы. Валунная глина, естественно, представляет собой весьма неоднородную литологию, поэтому следует провести полную характеризацию участка, и специалист по оценке риска должен быть вполне уверен, что в породе нет песчаных последовательностей. |
| Изолирующие глинистые слои полигонов отходов | 0.1–0.5–5 | Приемлемая достоверность, поскольку было проведено несколько независимых тестов, которые дают, по-видимому, последовательные результаты. Было показано, что Kd коррелирует с содержанием глины и/или ЕКО, поэтому допустим меньший консерватизм при подходящем тестировании и обосновании. Следует учитывать доминирующий глинистый минерал. |
В табл. 3 представлены значения Kd из литературных источников в предположении, что осуществляется линейная модель сорбции. Эти значения считаются актуальными для ориентировочной оценки рисков, связанных с миграцией ${\text{NH}}_{4}^{ + }$ в различных горных породах для разбавленных растворов.
Процессы трансформации
Аммоний может окисляться некоторыми бактериями для выработки энергии – процесс, известный как нитрификация. Нитрификация обычно проходит в две стадии, каждая из которых реализуется различными микроорганизмами-нитрификаторами:
У нитрифицирующих бактерий углерод для биосинтеза обеспечивается растворенным CO2 (в виде бикарбоната). Представляя химический состав микробной биомассы как C5H7NO2, две стадии нитрификации можно объединить для получения общей реакции [15]:
Процесс является аэробным, и потребление кислорода составляет около 3.3 кг O2 на каждый килограмм деградировавшего аммонийного азота (NH4–N). Это означает, что нитрификация требует постоянного поступления кислорода. Выход биомассы при нитрификации также низкий, около 0.13 кг/кг NH4–N, т.е. рост нитрифицирующих бактерий будет медленным. Нитрификация также может происходить в анаэробных условиях с нитратом или оксидами марганца, действующими в качестве окислителя, например:
В 2002 г. [30] было доказано существование анаэробной микробиальной реакции окисления ${\text{NH}}_{4}^{ + }$ нитритом, названной “анаммокс” и выполняющей важную роль в биологическом цикле азота. Данная реакция проходит по уравнению:
Нитрит и нитрат, образующиеся при аэробной нитрификации ${\text{NH}}_{4}^{ + }$, подвержены биологическому разложению (денитрификации) до азота (N2) в анаэробных условиях.
Нитрификация играет существенную роль в истощении ${\text{NH}}_{4}^{ + }$ в зоне аэрации и в подземных водах. Этот процесс был отмечен при оценке загрязнения ${\text{NH}}_{4}^{ + }$ на полигонах отходов [5] и при сбросе сточных вод [11]. В условиях, когда истощение за счет катионного обмена ограничено, например, при низком содержании глинистых минералов в водовмещающих породах, нитрификация может быть основным процессом, ограничивающим образование шлейфа ${\text{NH}}_{4}^{ + }$ [8, 9].
В большинстве исследований нитрификация оценивалась в аэробных условиях. Однако, в [5] подчеркнута важность анаэробного окисления ${\text{NH}}_{4}^{ + }$. Авторы сообщили, что нитрификация была существенным процессом, управляющим истощением ${\text{NH}}_{4}^{ + }$ в шлейфе свалочного фильтрата в песчано-гравийном водоносном горизонте в Дании, и показали значительный вклад анаэробного окисления ${\text{NH}}_{4}^{ + }$. Следует отметить, что другие натурные исследования свидетельствовали, что анаэробное окисление ${\text{NH}}_{4}^{ + }$ происходит в незначительной степени [11, 17]. В связи с этим неясно, является ли оно существенным процессом истощения аммония для многих шлейфов фильтратов или этот процесс становится важным только в определенных условиях [7].
В водоносных горизонтах нитрификация может быть ограничена относительно низкой растворимостью кислорода в воде (максимум 10 мг/л при стандартных температуре и давлении) и физическим смешиванием путем дисперсии анаэробного шлейфа ${\text{NH}}_{4}^{ + }$ с аэробными подземными водами. Согласно предположению, принятому в [11] и многих других исследованиях, разложение ${\text{NH}}_{4}^{ + }$ является процессом первого порядка, который требует оценки параметра, соответствующего периоду полураспада. В исследовании [11] расчетная скорость нитрификации составила около 0.017 кг NH4–N /сут, что соответствует периоду полураспада около 13 сут при концентрации 27 мг NH4–N /л. Однако такие показатели, скорее всего, будут иметь место только в том случае, если высокие скорости биологического роста могут поддерживаться другими питательными веществами в смеси поллютантов. Значительно более низкие скорости нитрификации, которые можно ожидать в обычных условиях водоносного горизонта, были представлены в [13], где обсуждались скорости нитрификации, полученные из натурных данных для двух шлейфов свалочного фильтрата. Для полигона отходов Llwn Isaf в Северном Уэльсе была рассчитана аэробная нитрификация в неглубоком песчано-гравийном водоносном горизонте с периодом полураспада ${\text{NH}}_{4}^{ + }$ около 6 лет. Данные, полученные по водоносному горизонту Sherwood Sandstone (песчаник) под полигоном Burntstump в Ноттингемшире, предполагают период полураспада близкий к 3.5 годам, хотя более поздние работы на этом же участке предлагали период полураспада 2.2 года [7].
Изучение пути миграции иона аммония в шлейфе коммунальных сточных вод с относительно низкой дисперсией и нереактивной структурой водоносного горизонта показало, что окисление аммония ограничивалось узкими зонами бокового смешивания с насыщенными кислородом грунтовыми водами на границах шлейфа. Несколько более широкие зоны окисления ${\text{NH}}_{4}^{ + }$ могут присутствовать вблизи фронта шлейфов в тех случаях, когда водоносные горизонты являются аэробными, а ионный обмен ограничен [9]. В целом, можно ожидать, что загрязнение ${\text{NH}}_{4}^{ + }$ будет сохраняться в загрязненных субоксических водоносных горизонтах еще долгое время после того, как будут удалены более подвижные поллютанты [10].
ПРОЦЕССЫ ТРАНСФОРМАЦИИ АММОНИЯ В СВАЛКАХ-БИОРЕАКТОРАХ
Процессы образования и трансформации аммония на свалках и полигонах наглядно могут быть прослежены на свалках-биореакторах.
Свалка-биореактор – это управляемая система, в которой используется добавление влаги (часто рециркуляция фильтрата) и/или нагнетание воздуха для создания в твердых отходах среды, способной активно разлагать легко биоразлагаемую органическую фракцию отходов. Одним из преимуществ является то, что повышенные темпы деградации отходов, характерные для свалки-биореактора, позволяют увеличить ее срок службы по сравнению с обычными полигонами. По мере рециркуляции фильтрата он обрабатывается in situ, в результате чего снижается органическая нагрузка и, следовательно, потенциальное воздействие на окружающую среду. Обработка in situ сокращает продолжительность периода обслуживания после закрытия полигона и связанные с этим расходы [3, 25]. Кроме того, нитрификация аммония in situ более экономична и может происходить на более старых полигонах [4, 27].
Несмотря на то, что в свалках-биореакторах органическая нагрузка фильтрата значительно снижается, проблема загрязнения фильтрата аммонийным азотом остается. Его концентрация выше, чем в фильтрате с обычных полигонов, поскольку в свалках-биореакторах добавление влаги и/или рециркуляция фильтрата увеличивает скорость аммонификации [2, 3]. Традиционно удаление аммония из фильтрата часто проводилось ex situ. Однако обработка ex situ является трудной и дорогостоящей.
Процесс нитрификации–денитрификации in situ оказался более перспективным из-за его более низких эксплуатационных затрат и меньших требований к пространству. В процессе органической ферментации широко применяется двухфазная обработка (фазы образования кислот и метановой ферментации). Микроорганизмы в этих фазах имеют разные скорости роста, оптимальные для окружающей среды и питания. Таким образом, оптимизация этих условий позволяет повысить производительность и степень стабилизации твердых отходов на полигонах в первые несколько лет.
На основе концепции разделения фаз в исследовании [21] в рамках экспериментальной свалки-биореактора были построены три реактора: 1) заполненный свежими отходами для бескислородной денитрификации и гидролиза, 2) для метаногенеза и 3) для аэробной нитрификации. В первом реакторе органическое вещество свежих отходов гидролизуется и растворяется. Полученный фильтрат характеризуется как кислый с высоким содержанием органического вещества. Сначала этот фильтрат подается в метаногенный реактор для метаногенеза, а затем стоки поступают в нитрифицирующий реактор для окисления аммония до нитрата. В конечном итоге выходной поток возвращается в реактор анаэробной денитрификации и гидролиза.
Поскольку метаногенез не только производит достаточную щелочность для буферизации кислот, но и устраняет угрозу, которую гетерогенные бактерии представляют для нитрифицирующих бактерий в нитрифицирующем реакторе, очень важно поддерживать этот процесс, особенно на начальной стадии.
В метаногенном и нитрифицирующем реакторах используются выдержанные отходы. Они содержат широкий спектр и большое количество микроорганизмов, которые обладают значительной способностью к деградации трудноразлагающихся органических соединений, присутствующих в некоторых сточных водах [37]. При этом эффект рециркуляции фильтрата становится максимальным, когда свалка достигает стабильной фазы [33].
Добавление воздуха в тело полигона улучшает процессы деградации отходов, поскольку аэробные процессы имеют тенденцию разлагать органические соединения за более короткие периоды времени, чем процессы анаэробной деградации. Описанные преимущества аэробной эксплуатации полигона включают увеличение оседания, снижение подвижности металлов, снижение затрат на управление составом фильтрата и контроль метана [3, 24].
Многие из процессов трансформации/удаления азота поддерживаются аэробными процессами, включая нитрификацию и вывод из системы (отвод) аммиака воздухом или улетучивание. Отвод воздухом и улетучивание могут быть предпочтительными в аэробных свалках-биореакторах из-за более высоких значений pH и температур, которые присущи аэробной среде.
Во время аэробной деградации ТКО биоразлагаемые материалы превращаются в основном в диоксид углерода и воду, при этом метана выделяется мало. Кроме того, в процессе анаэробной деградации устанавливаются нейтральные или слабощелочные значения рН, что снижает подвижность металлов [3, 24]. Образование летучих органических кислот в аэробных биореакторах достаточно низкое.
В анаэробных свалках-биореакторах практикуется добавление влаги. Источники добавления жидкости могут включать грунтовые воды, ливневые воды, инфильтрирующиеся атмосферные осадки или фильтрат. Повышение содержания влаги приводит к увеличению производства метана, что неоднократно демонстрировалось в различных лабораторных и натурных исследованиях [31]. Поскольку в анаэробных биореакторах деградация отходов увеличивается и органические материалы возвращаются в тело отходов посредством рециркуляции фильтрата [25], метан образуется гораздо быстрее. Общий объем производимого газа также увеличивается, поскольку органические вещества фильтрата рециркулируются и затем биодеградируют в теле полигона. Бóльшая часть производства газа может быть завершена несколькими годами ранее, чем это происходит на обычных полигонах, что обеспечивает более эффективный сбор и последующее использование газа [25].
Анаэробные свалки-биореакторы более эффективны для деградации твердых отходов, чем обычные полигоны. Однако по сравнению с другими типами свалок-биореакторов анаэробные системы имеют тенденцию к более низким температурам и более медленным темпам разложения. Недостатком эксплуатации анаэробной свалки-биореактора является накопление аммонийного азота. В таких биореакторах аммонийный азот, присутствующий в фильтрате, постоянно возвращается в тело полигона. Преимущество анаэробной работы биореактора по сравнению с другими типами свалок-биореакторов состоит в том, что не требуется добавление воздуха; следовательно, эксплуатационные расходы меньше, чем были бы в аэробных условиях, и метан можно собирать и использовать [3].
Менее изученный, но перспективный тип свалки-биореактора – это гибридный биореактор [3], включающий сочетание аэробных и анаэробных условий. Были исследованы два типа таких систем: циклическое кратковременное нагнетание воздуха в тело полигона и последовательность аэробных и анаэробных условий.
Циклическое нагнетание воздуха в тело полигона определяется как чередование in situ аэробных и анаэробных условий, которое повторяется на протяжении всего жизненного цикла свалки-биореактора, тогда как последовательность нагнетания воздуха в отходы представляет собой начальную аэробную фазу, за которой следует конечная анаэробная фаза. Поскольку имеется много преимуществ, связанных как с аэробной, так и с анаэробной деградацией, исследователи видят в объединении этих процессов способ максимизировать потенциал свалки-биореактора. Существуют некоторые компоненты, как в отходах, так и в фильтрате, которые являются устойчивыми в анаэробных условиях, но разлагаются в аэробных средах, такие как лигнины и ароматические соединения. Использование одного из указанных гибридных методов может позволить более полно обрабатывать фильтрат и/или отходы [22, 26].
Использование гибридной свалки-биореактора может служить для объединения нескольких процессов трансформации и удаления азота, таких как нитрификация и денитрификация, потенциально приводящих к полному удалению азота с полигона. Проведено несколько лабораторных исследований по оценке влияния циклического нагнетания воздуха на производительность свалок-биореакторов [22]. Каждая из рассмотренных систем достигала биологически стабильного фильтрата по отношению к ХПК за более короткий период времени, чем для чисто аэробных систем. В нескольких исследованиях также оценивался эффект последовательной системы нагнетания воздуха [3]. В такой системе отходы размещаются по слоям. Первый слой аэрируется в течение определенного периода времени; когда второй этаж заполнен, аэрация первого слоя прекращается, и начинается аэрация второго слоя. Фильтрат непрерывно рециркулируется. Этот процесс продолжается до тех пор, пока полигон не будет заполнен. Предполагается, что такая система ускоряет типичные процессы анаэробной деградации, в частности, начало метаногенеза.
Факультативные свалки-биореакторы эксплуатируются с целью активного разложения массы отходов и в то же время для управления высокими концентрациями аммония, обычно присутствующими в фильтрате со свалок-биореакторов. В факультативных системах фильтрат удаляется из свалки-биореактора и нитрифицируется во внешней системе обработки перед рециркуляцией [3]. Таким образом, концентрации аммонийного азота в обработанном фильтрате низки или отсутствуют, тогда как уровни нитрата высоки. По мере того, как богатый нитратом фильтрат рециркулируется и проходит через тело полигона, происходит денитрификация, где несколько видов микроорганизмов, включая факультативные микроорганизмы, используют нитрат для дыхания. Хотя этот тип биореактора во многих исследованиях не оценивался, имеются лабораторные данные, свидетельствующие о том, что внедрение такой системы является оправданным [3, 23].
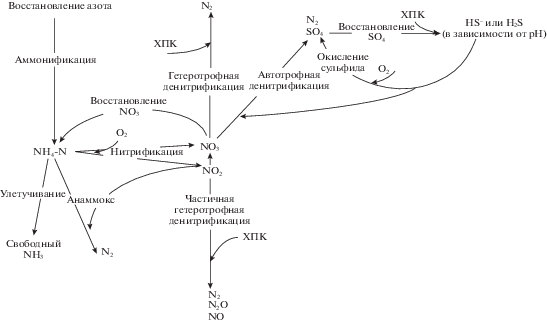
Таким образом, эксплуатация полигона как биореактора предоставляет дополнительные возможности для процессов трансформации и удаления азота in situ. При добавлении воздуха в тело полигона такие биологические процессы, как нитрификация, которые традиционно обнаруживаются и ожидаются только в грунтовых покрытиях полигонов в результате диффузии воздуха, теперь могут происходить внутри массы отходов. Кроме того, рециркуляция нитрифицированного фильтрата позволяет проводить процессы денитрификации в бескислородных зонах, обнаруженных как в анаэробных, так и в аэробных свалках-биореакторах. На рис. 3 показаны возможные пути трансформации и/или удаления азота, которые могут происходить в свалках-биореакторах.
ЗАКЛЮЧЕНИЕ
Длительность загрязнения фильтрата аммонийным азотом является одной из наиболее острых проблем на свалках и полигонах ТКО, и вполне вероятно, что именно его присутствие определит, когда свалка станет биологически стабильной и можно будет закончить мониторинг после закрытия полигона [23]. Продолжительность выделения ${\text{NH}}_{4}^{ + }$ из отходов в значительной степени определяется их составом, содержанием органического вещества, технологией захоронения. В связи с этим существуют различные мнения о времени снижения концентраций ${\text{NH}}_{4}^{ + }$ до значений, безопасных для природной среды. Однако все исследователи подчеркивают весьма значительную продолжительность загрязнения фильтрата аммонийным азотом.
Традиционно полигоны считались системами хранения и локализации, функционирующими в основном для депонирования отходов. Однако в последнее время подход к управлению ТКО изменился в связи с внедрением новой технологии захоронения отходов – метода биореактора. Конструкция системы свалки-биореактора обеспечивает гибкость в расположении и продолжительности нагнетания жидкости и воздуха, позволяя регулировать pH, окислительно-восстановительный потенциал и содержание влаги для создания среды, способствующей микробиальной деградации и биологическому удалению аммония. По сравнению с обычными полигонами свалки-биореакторы показали более быстрый и полный процесс конверсии и стабилизации отходов [3], в связи с чем существует вероятность значительного сокращения длительности загрязнения фильтрата аммонийным азотом и минимизации загрязнения компонентов природной среды на участках размещения полигонов ТКО.
Статья подготовлена в рамках выполнения государственного задания и плана НИР по теме № г.р. АААА-А19-119101890052-5 и при финансовой поддержке гранта РФФИ № 20-05-00574.
Список литературы
Assmuth, T.W., Strandberg T. Ground-water contamination at Finnish landfills, Water, Air & Soil Pollution. 1993. V. 69. № 1–2. P. 179–199.
Barlaz, M.A., Rooker, A.P., Kjeldsen, P., Gabr, M.A., Borden, R.C. Critical evaluation of factors required to terminate the postclosure monitoring period at solid waste landfills, Environmental Science & Technology. 2002. V. 36. № 16. P. 3457–3464.
Berge, N.D., Reinhart, D.R., Townsend, T.G. The fate of nitrogen in bioreactor landfills, Critical Reviews in Environmental Science & Technology. 2005. V. 35. № 4. P. 365–399.
Berge, N.D., Reinhart, D.R., Dietz, J., Townsend, T. In situ ammonia removal in bioreactor landfill leachate, Waste Management. 2006. V. 26. № 4. P. 334–343.
Bjerg, P.L., Rügge, K., Pedersen, J.K., Christensen, T.H. Distribution of redox-sensitive groundwater quality parameters downgradient of a landfill (Grindsted, Denmark), Environmental Science & Technology. 1995. V. 29. P. 1387–1394.
Brady, N.C., Weil, R.R. The Nature and Properties of Soils: 13th edition, NJ, USA: Prentice-Hall, Englewood Cliffs. 2002, 960 p., ISBN: 978-0130167637.
Buss, S.R., Herbert, A.W., Morgan, P., Thornton, S.F., Smith, J.W.N. A review of ammonium attenuation in soil and groundwater, Quarterly Journal of Engineering Geology & Hydrogeology. 2004. V. 37. № 4. P. 347–359.
Christensen, T.H., Bjerg, P.L., Kjeldsen. P. Natural attenuation: a feasible approach to remediation of groundwater pollution at landfills? Ground Water Monitoring & Remediation. 2000. V. 20. № 1. P. 69–77.
Christensen, T.H., Kjeldsen, P., Bjerg, P.L., Jensen, D.L., et al. Biogeochemistry of landfill leachate plumes, Applied Geochemistry. 2001. V. 16. № 7–8. P. 659–718.
Cozzarelli, I.M., Böhlke, J.K., Masone,r J., Breit, G.N., et all. Biogeochemical evolution of a landfill leachate plume, Norman, Oklahoma, Ground Water. 2011. V. 49. № 5. P. 663–687.
DeSimone, L.A., Barlow, P.M., Howes, B.L. A Nitrogen-rich Septage-effluent Plume in a Glacial Aquifer, Cape Cod, Massachusetts, February 1990 through December 1992, 1996, 96 p., (US Geological Survey Water Supply Paper; 2456). https://pubs.usgs.gov/wsp/2456/report.pdf.
Ehrig, H.-J. Water and element balances of Landfills // The Landfill / Baccini P., ed., Berlin, Germany: Springer Verlag. 1989. P. 83–115, (Lecture Notes in Earth Sciences. V. 20).
Erskine, A.D. Transport of ammonium in aquifers: retardation and degradation, Quarterly Journal of Engineering Geology & Hydrogeology. 2000. V. 33. № 2. P. 161–170.
Galitskaya, I.V., Putilina, V.S., Yuganova, T.I. Prodolzhitel`nost` vy`shhelachivaniya metallov iz svalochnogo tela pri zaxoronenii tverdy`x kommunal`ny`x otxodov [Duration of leaching of heavy metals from the landfill body at the municipal solid waste disposal] Geoekologiya. 2020. № 6. P. 3–13. (in Russian)
Horan, N.J. Biological Wastewater Treatment Systems, Theory and Operation. Chichester, England, NY, USA: John Wiley & Sons. 1990, 310 p., ISBN: 0471922587, 0471924253.
Hydrogeological Risk Assessments for Landfills and the Derivation of Groundwater Control and Trigger Levels: Landfill Directive Project LFTGN01, Bristol, UK: Environment Agency. 2003. http://adlib.everysite.co.uk/resources/000/064/494/Hydrogeological_Risk.pdf.
Jiang, J.G., Yang, G.D., Deng, Z., Huang, Y.F., Huang, Z.L. et all. Pilot-scale experiment on anaerobic bioreactor landfills in China, Waste Management. 2007. V. 27. № 7. P. 893–901.
Kjeldsen, P., Christophersen, M. Composition of leachate from old landfills in Denmark, Waste Management & Research. 2001. V. 19. № 3. P. 249–256.
Kjeldsen, P., Barlaz, M.A., Rooker, A.P., Baun, A., et al. Present and long-term composition of MSW landfill leachate: A Review, Critical Reviews in Environmental Science & Technology. 2002. V. 32. № 4. P. 297–336.
Kruempelbeck, I., Ehrig, H.-J. Long-term behavior of municipal solid waste landfills in Germany, Sardinia 99, Seventh International Waste Management and Landfill Symposium, 48 October, S. Margherita di Pula, Cagliari, Proceedings V. I / Christensen T. H., Cossu R., Stegmann R., eds., CISA - Environmental Sanitary Engineering Centre, Cagliari, Italy 1999. P. 27–36. (from [19])
Long, Y., Guo, Q.-W., Fang, C.-R., Zhu, Y.-M., Shen, D.-S. In situ nitrogen removal in phase-separate bioreactor landfill, Bioresource Technology. 2008. V. 99. № 13. P. 5352–5361.
Pichler, M., Kogner-Knabner, I. Chemolytic analysis of organic matter during aerobic and anaerobic treatment of municipal solid waste, Journal of Environmental Quality. 2000. V. 29. № 4. P. 1337–1344.
Price, G.A., Barlaz, M.A., Hater, G.R. Nitrogen management in bioreactor landfills, Waste Management. 2003. V. 23. № 7. P. 675–688.
Read, A.D., Hudgins, M., Philips. P. Perpetual landfilling through aeration of the waste mass; lessons from test cells in Georgia (USA), Waste Management. 2001. V. 21. № 7. P. 617–629.
Reinhart, D.R., Al-Yousfi, A.B. The impact of leachate recirculation on municipal solid waste landfill operating characteristics, Waste Management & Research. 1996. V. 14. № 4. P. 337–346.
Reinhart, D.R., McCreanor, P.T., Townsend, T.G. The bioreactor: its status and future, Waste Management & Research. 2002. V. 20. № 2. P. 172–186.
Ritzkowski, M., Heyer, K.-U., Stegmann, R. Fundamental processes and implications during in situ aeration of old landfills, Waste Management. 2006. V. 26. № 4. P. 356–372.
Robinson, H.D. The Technical Aspects of Controlled Waste Management. A Review of the Composition of Leachates from Domestic Wastes in Landfill Sites: Report for the UK Department of the Environment. Waste Science and Research / Aspinwall & Company, Ltd, London, UK. 1995.
Sliusar, N., Vaisman, Y., Korotaev, V. Ocenka dolgosrochnyx emissij ob`ektov zahoroneniya tverdyx kommunalnyx otxodov: rezultaty polevyx issledovanij i laboratornogo modelirovaniya [The estimation of long-term emissions from municipal solid waste landfill-sites: the results of field studies and Laboratory Modeling]. Ekologiya i promyshlennost' Rossii. 2016. V. 20. № 4. P. 32–39. (in Russian)
Thamdrup, B., Dalsgaard, T. Production of N2 through anaerobic ammonium oxidation coupled to nitrate reduction in marine sediments, Applied & Environmental Microbiology. 2002. V. 68. № 3. P. 1312–1318.
Townsend, T.G., Miller, W., Lee, H., Earle, J. Acceleration of landfill stabilization using leachate recycle, Journal of Environmental Engineering. 1996. V. 122. № 4. P. 263–268.
Vodyanitskii, Yu.N. Biochemical processes in soil and groundwater contaminated by leachates from municipal landfills (Mini review), Annals of Agrarian Science. 2016. V. 14. № 3. P. 249–256.
Wang, Q., Matsufuji, Y., Dong, L., Huang, Q.F. et all. Research on leachate recirculation from different types of landfills, Waste Management. 2006. V. 26. № 8. P. 815–824.
Zavizion, Yu.V., Slyusar, N.N., Glushankova, I.S., Zagorskaya, Yu.M. Ocenka fiziko-ximicheskix parametrov otxodov raznogo sroka zaxoroneniya [Evaluation of physicochemical parameters of wastes with different disposal periods] Vestnik PNIPU. Prikladnaya e`kologiya. Urbanistika. 2015. № 3 (19). P. 82–96. (in Russian)
Zhao, R.Z., Novak, J.T., Goldsmith, C.D. Evaluation of on-site biological treatment for landfill leachates and its impact: a size distribution study, Water Research. 2012. V. 46. № 12. P. 3837–3848.
Zhao, R., Gupta, A., Novak, J.T., Goldsmith, C.D. Evolution of nitrogen species in landfill leachates under various stabilization states, Waste Management. 2017. V. 69. P. 225–231.
Zhao, Y., Song, L., Huang, R., Song, L., Li, X. Recycling of aged refuse from a closed landfill, Waste Management & Research. 2007. V. 25. № 2. P. 130–138.
Дополнительные материалы отсутствуют.
Инструменты
Геоэкология. Инженерная геология, гидрогеология, геокриология