Геохимия, 2020, T. 65, № 4, стр. 343-361
Распределение REE, Y, Sc и Li между алюмосиликатным и алюмофторидным расплавами в модельной гранитной системе в зависимости от давления и содержания воды
Т. И. Щекина a, *, А. А. Русак a, Я. О. Алферьева a, **, Е. Н. Граменицкий a, А. Р. Котельников b, Н. Г. Зиновьева a, А. Ю. Бычков a, Я. В. Бычкова a, В. А. Хвостиков c
a Московский государственный университет им. М.В. Ломоносова, Геологический факультет
119991 Москва, Ленинские горы, Россия
b Институт экспериментальной минералогии РАН
142432 Черноголовка, ул. Академ. Осипьяна, д. 4, Россия
c Институт проблем технологии микроэлектроники и особочистых материалов РАН
142432 Черноголовка, ул. Академ. Осипьяна, д. 6, Россия
* E-mail: t-shchekina@mail.ru
** E-mail: yanaalf@yandex.ru
Поступила в редакцию 04.02.2019
После доработки 25.07.2019
Принята к публикации 04.10.2019
Аннотация
Экспериментально изучено распределение редкоземельных элементов, Y, Sc и Li между алюмосиликатным (L) и алюмофторидным (LF) расплавами в гранитной системе с предельными концентрациями фтора при 800°С и 1, 2 кбар и содержании воды от 2 до 13 мас. %. Показано, что все редкоземельные элементы, Y, Sc и Li распределяются в пользу солевого алюмофторидного расплава, независимо от заданных условий эксперимента. Коэффициенты разделения элементов ${\text{К}}{{{\text{d}}}_{{{\text{REE}}}}} = {{{\text{С}}_{{{\text{REE}}}}^{{{\text{LF}}}}} \mathord{\left/ {\vphantom {{{\text{С}}_{{{\text{REE}}}}^{{{\text{LF}}}}} {{\text{С}}_{{{\text{REE}}}}^{{\text{L}}}}}} \right. \kern-0em} {{\text{С}}_{{{\text{REE}}}}^{{\text{L}}}}}$ между этими фазами зависят от давления. Впервые показано, что увеличение давления от 1 до 2 кбар при температуре 800°С вызывает существенное уменьшение КdREE. Коэффициенты разделения между расплавами монотонно снижаются от легких к тяжелым REE как при 1, так и при 2 кбар. Не обнаружено четкой зависимости между значениями КdREE и концентрацией воды в системе. Показана ключевая роль лития в распределении редкоземельных элементов, Y и Sc, поскольку литий, наряду с фтором, является фактором ликвации в изучаемой системе и способствует концентрации REE, Y и Sc в солевых расплавах. Во всех экспериментах наблюдается прямая корреляция коэффициентов разделения КdLi и КdREE,Y,Sc между солевым и силикатным расплавами. Причины зависимости поведения REE от давления в системе связаны, вероятно, с изменением структуры расплавов при растворении в них воды и фтора и процессами комплексообразования при различных условиях эксперимента.
ВВЕДЕНИЕ
В основе работы лежат экспериментальные исследования равновесных соотношений фаз в ликвидусной части насыщенной фтором гранитной системы. В предшествующих работах авторов в системе Si–Al–Na–K–Li–H–O–F была обнаружена область несмесимости при 800°C, 1 кбар и 4–7 мас. % воды (Граменицкий и др., 2005; Девятова и др., 2007; Алферьева и др., 2011). Отделяющийся от силикатного солевой расплав имеет щелочной алюмофторидный состав. Наиболее широкое поле несмесимости относится к литиевой части системы и соответствует составам литий-фтористых топаз- и криолитсодержащих гранитов, онгонитов, эльванов и пегматитов (Алферьева и др., 2011; Щекина и др., 2013). Установлено, что солевая фаза эффективно экстрагирует многие рудные компоненты, в частности, все редкоземельные элементы (REE), Y, Sc и Li (Shchekina, Gramenitskiy, 1997; Gramenitskiy, Shchekina, 2002; Граменицкий и др., 2005; Граменицкий, Щекина, 2005). В группу редкоземельных элементов, следуя классификации В.И. Вернадского (1954), включены 15 элементов от La до Lu, а Y и Sc рассматриваются отдельно. Эти результаты были подтверждены экспериментальными работами И.В. Векслера с соавторами (2005; 2012) в сухих условиях при 1100 и 1200°С при атмосферном давлении и в присутствии водного флюида при 700 и 800°С и 1 кбар. В конце 1990-х–начале 2000-х годов к работам в этой области возрос интерес в связи с тем, что солевым и, в частности, фторидным расплавам и флюидам стали придавать особое значение в процессах дифференциации гранитных магм, метасоматоза и рудообразования (Маракушев и др., 1983; Царева и др., 1991; Candela, Piccoli, 1995; Badanina et al, 2006; Андреева и др., 2007; Соловова и др., 2010; Перетяжко и др., 2010). Они были получены в искусственных включениях в минералах (Котельникова, Котельников, 2008). Солевым расплавам стала отводиться определяющая роль в аномальном поведении REE в богатых фтором гранитоидах и гранитных пегматитах (Ясныгина, Рассказов, 2008; Скублов, 2005; Перетяжко, Савина, 2010; Гусев А.И., Гусев A.А, 2011; Zheng-Hang Lv et al., 2018). Имеются в виду необычные отношения Y/Ho < 15 в породах и проявление тетрад-эффекта M-типа в спектрах REE, нормированных на содержание REE в хондрите. Особый характер распределения редкоземельных элементов объясняется (Bau, 1996; Irber, 1999) влиянием высокофтористого водного флюида, способного образовывать фторидные комплексы с REE. Согласно (Takahashi et al., 2002) распределение W-типа REE присуще водным фторидным средам, в которых комплексообразование имеет большое значение.
Для обозначения богатых фтором жидких фаз, промежуточных по свойствам между расплавами и концентрированными водными флюидами или растворами, использовали разнообразные термины: рудные магмы, расплавы-рассолы, тяжелые флюиды, флюидные расплавы и др. В англоязычной литературе наиболее употребителен термин “brine”.
Используемых в настоящее время в экспериментах закалочных методов не достаточно для изучения сложных фазовых отношений в системе: силикатный расплав – солевой фторидный расплав – флюид, особенно, для определения составов сосуществующих фаз. Мало также данных о растворимости солевых фторидных фаз (FP) типа (Li,Na,K)AlF6 и соединений редкоземельных элементов в водных флюидах при высоких температурах и давлениях. Опубликованные в литературе экспериментальные и расчетные величины (Балашов, 1976; Кравчук и др., 1989; 1995; Haas et al., 1995; Абрамов, 2004; Луканин, Дернов-Пегарев, 2010), показывают, что коэффициенты разделения KdREE (Fl/L) между водно-хлоридной, водно-фторидной или чисто водной флюидными фазами (Fl) с одной стороны, и гранитным расплавом (L) – с другой, всегда намного меньше единицы. Повышение их при увеличении солевой составляющей мы склонны связывать (Граменицкий и др., 2005) с анализом гетерогенного флюида, одна из фаз которого обогащена солевыми компонентами, растворяющими редкие элементы, гораздо в большей степени, чем разбавленный флюид.
Нерешенные вопросы заставляют продолжать экспериментальные работы во фторсодержащей гранитной системе. Нами была расширена область условий экспериментов в сторону более высокого давления до 2 кбар и более широкого интервала содержаний вводимой в систему воды. Предполагалось изучить влияние воды (от недосыщенного до пересыщенного водой состояния) на фазовые отношения в модельной гранитной системе с предельными содержаниями фтора (насыщенной избыточными фторидными фазами) и характер распределения редкоземельных элементов между алюмосиликатным и солевым расплавами, а также по возможности провести оценку содержаний редкоземельных элементов во флюидной фазе.
МЕТОДИКА
Исходные материалы
Для экспериментов был выбран один исходный состав алюмосиликатного расплава, близкий по составу к гранитной эвтектике Qtz-Ab-Or при 690°, 1 кбар H2O, 1 мас. % F, но содержащий ~1.5 мас. % Li. Соотношение атомных количеств главных элементов в этом составе составляло Si : Al : (Na + K + + Li) = 70 : 15 : 15. Соотношение щелочных элементов Nа : K : Li соответствовало 7.5 : 2.5 : 5. К этому силикатному составу добавляли алюмофторидную составляющую (отвечавшую по стехиометрии соединению (Na,K,Li)3AlF6 в количестве, достаточном для насыщения ею алюмосиликатного расплава и выделения обособленной алюмофторидной фазы (табл. 1). Расчет основан на результатах изучения системы в предыдущих работах авторов. Обращаем внимание читателя на то, что исходный состав системы рассчитан на 100%, учитывая все компоненты, включая добавляемые REE и H2O.
Таблица 1.
Средние составы закаленных алюмосиликатных (L) и алюмофторидных (LF) расплавов (мас. %) и коэффициенты разделения элементов Kd между ними при температуре 800°С, давлении 1 и 2 кбар и различных содержаниях воды в системе
| Компо-ненты | № опыта; давление; содержание воды, мас. % | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 776; 1 кбар; 2.06 | 778; 1 кбар; 5.12 | 777; 1 кбар; 9.34 | 775**; 1 кбар; 13.27 | |||||||||||||
| исх. состав | L(8)* | LF (4) | Kd | исх. состав | L (7) | LF (4) | Kd | исх. состав | L(4) | LF(4) | Kd | исх. состав | L(8)* | LF (4) | Kd | |
| Si | 21.49 | 27.66 | 0.35 | 0.01 | 20.87 | 27.50 | 0.35 | 0.01 | 20.01 | 26.75 | 0.57 | 0.02 | 19.20 | 27.06 | 3.46 | 0.13 |
| Al | 8.31 | 7.30 | 8.87 | 1.21 | 8.07 | 7.62 | 9.05 | 1.19 | 7.74 | 7.35 | 7.73 | 1.05 | 7.44 | 7.49 | 3.94 | 0.53 |
| Na | 5.19 | 2.66 | 14.12 | 5.04 | 3.16 | 14.42 | 4.56 | 4.83 | 3.10 | 14.75 | 4.77 | 4.64 | 3.07 | 15.23 | 4.96 | |
| K | 6.67 | 7.44 | 5.77 | 6.47 | 7.37 | 5.91 | 0.80 | 6.21 | 7.31 | 5.51 | 0.75 | 5.96 | 7.33 | 4.01 | 0.55 | |
| Li | 1.39 | 0.83 | 8.55 | 10.35 | 1.36 | 0.85 | 11.23 | 13.24 | 1.30 | 0.98 | 9.04 | 9.23 | 1.24 | 0.50 | 5.03 | 9.97 |
| F | 18.45 | 15.32 | 45.49 | 2.97 | 17.92 | 19.62 | 48.89 | 2.49 | 17.17 | 17.47 | 48.27 | 2.76 | 16.49 | 17.57 | 60.05 | 3.42 |
| H | 0.21 | н.о. | н.о. | н.о. | 0.53 | н.о. | н.о. | н.о. | 0.95 | н.о. | н.о. | н.о. | 1.37 | н.о. | н.о. | н.о. |
| REE | 6.30 | 0.17 | 5.92 | » | 6.11 | 0.19 | 7.61 | » | 5.86 | 0.20 | 6.74 | » | 5.63 | 0.24 | 5.28 | » |
| O | 31.98 | 40.10 | 3.25 | » | 33.63 | 39.11 | 1.94 | » | 35.91 | 38.60 | 2.71 | » | 38.04 | 39.10 | 6.13 | » |
| Сумма | 100.00 | 101.47 | 92.30 | » | 100.00 | 105.42 | 99.39 | » | 101.74 | 95.32 | » | 100.00 | 102.36 | 103.12 | » | |
| Содержание REE, Y, Sc, ppm | ||||||||||||||||
| La | 4518 | 66 | 3703 | 56 | 4418 | 71 | 4818 | 68 | 4208 | 59 | 4319 | 73 | 4040 | 35 | 3035 | 87 |
| Ce | 2264 | 43 | 2090 | 48 | 2214 | 52 | 2750 | 52 | 2108 | 44 | 2463 | 56 | 2024 | 20 | 1402 | 69 |
| Pr | 4527 | 70 | 3305 | 47 | 4427 | 76 | 4324 | 57 | 4217 | 73 | 3845 | 53 | 4048 | 42 | 2508 | 60 |
| Nd | 4464 | 72 | 3346 | 46 | 4366 | 79 | 4327 | 55 | 4158 | 76 | 3816 | 50 | 3992 | 48 | 2952 | 62 |
| Sm | 4491 | 92 | 3879 | 42 | 4392 | 100 | 5046 | 50 | 4183 | 102 | 4451 | 44 | 4016 | 62 | 3460 | 56 |
| Eu | 4500 | 93 | 3867 | 41 | 4401 | 104 | 4979 | 48 | 4191 | 104 | 4459 | 43 | 4024 | 59 | 3048 | 52 |
| Gd | 4518 | 85 | 3610 | 42 | 4418 | 95 | 4674 | 49 | 4208 | 93 | 4119 | 44 | 4040 | 58 | 3523 | 61 |
| Tb | 4446 | 103 | 3946 | 38 | 4348 | 115 | 5056 | 44 | 4141 | 120 | 4529 | 38 | 3976 | 68 | 3586 | 52 |
| Dy | 4464 | 113 | 3968 | 35 | 4366 | 125 | 5035 | 40 | 4158 | 135 | 4524 | 34 | 3992 | 80 | 3779 | 47 |
| Ho | 4473 | 105 | 3617 | 34 | 4375 | 118 | 4567 | 39 | 4166 | 125 | 4097 | 33 | 4000 | 67 | 3228 | 48 |
| Er | 4473 | 139 | 4377 | 31 | 4375 | 154 | 5616 | 36 | 4166 | 164 | 4975 | 30 | 4000 | 96 | 4086 | 43 |
| Tm | 4482 | 137 | 4013 | 29 | 4383 | 153 | 5147 | 34 | 4175 | 165 | 4567 | 28 | 4008 | 94 | 3760 | 40 |
| Yb | 4491 | 127 | 3519 | 28 | 4392 | 144 | 4466 | 31 | 4183 | 155 | 3867 | 25 | 4016 | 97 | 3294 | 34 |
| Lu | 4500 | 137 | 3719 | 27 | 4401 | 157 | 4739 | 30 | 4191 | 169 | 4148 | 25 | 4024 | 93 | 3369 | 36 |
| Y | 4509 | 117 | 4575 | 39 | 4410 | 133 | 5931 | 45 | 4200 | 125 | 5248 | 42 | 4032 | 67 | 3991 | 60 |
| Sc | 4455 | 212 | 3709 | 18 | 4357 | 230 | 4644 | 20 | 4150 | 258 | 3960 | 15 | 3984 | 177 | 3752 | 21 |
| Компо-ненты | № опыта; давление; содержание воды, мас. % | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 785**; 2 кбар; 2.44 | 786; 2 кбар; 4.94 | 787; 2 кбар; 11.11 | 784**; 2 кбар; 12.89 | |||||||||||||
| исх. состав | L (7) | LF (4) | Kd | исх. состав | L(4) | LF(4) | Kd | исх. состав | L(8)* | LF (4) | Kd | исх. состав | L (7) | LF (4) | Kd | |
| Si | 21.12 | 27.68 | 0.59 | 0.02 | 20.91 | 28.22 | 0.62 | 0.02 | 19.65 | 26.53 | 1.04 | 0.04 | 19.28 | 26.96 | 0.92 | 0.03 |
| Al | 8.28 | 7.27 | 9.50 | 1.31 | 8.10 | 7.20 | 9.74 | 1.35 | 7.60 | 7.57 | 8.07 | 1.07 | 7.46 | 7.25 | 9.86 | 1.36 |
| Na | 5.17 | 2.65 | 14.41 | 5.44 | 5.05 | 2.51 | 14.46 | 5.77 | 4.75 | 3.25 | 13.48 | 4.15 | 4.66 | 2.94 | 14.70 | 5.01 |
| K | 6.64 | 7.17 | 6.25 | 0.87 | 6.49 | 7.04 | 6.74 | 0.96 | 6.09 | 7.00 | 5.26 | 0.75 | 5.98 | 7.00 | 5.55 | 0.79 |
| Li | 1.39 | 0.44 | 2.22 | 5.07 | 1.34 | 1.11 | 4.66 | 4.20 | 1.26 | 2.17 | 5.35 | 2.47 | 1.24 | 0.57 | 4.44 | 7.86 |
| F | 18.38 | 14.91 | 44.11 | 2.96 | 17.96 | 13.37 | 45.30 | 3.39 | 16.88 | 18.48 | 46.00 | 2.49 | 16.55 | 16.90 | 46.84 | 2.77 |
| H | 0.25 | н.о. | н.о. | н.о. | 0.51 | н.о. | н.о. | н.о. | 1.15 | н.о. | н.о. | н.о. | 1.33 | н.о. | н.о. | н.о |
| REE | 6.27 | 0.74 | 1.54 | » | 6.13 | 2.58 | 4.26 | » | 5.76 | 0.50 | 5.56 | » | 5.65 | 0.33 | 7.08 | » |
| O | 32.18 | 40.67 | 3.36 | » | 33.52 | 41.60 | 3.02 | » | 36.87 | 37.49 | 3.19 | » | 37.85 | 38.96 | 2.87 | » |
| Сумма | 100.00 | 101.50 | 81.96 | » | 100.00 | 100.87 | 81.96 | » | 100.00 | 102.99 | 82.95 | » | 100.00 | 102.21 | 92.25 | » |
| Содержание REE, Y, Sc, ppm | ||||||||||||||||
| La | 4502 | 21 | 1073 | 52 | 4427 | 128 | 2693 | 21.10 | 4159 | 189 | 3697 | 19.52 | 4081 | 105 | 3936 | 37 |
| Ce | 2255 | 14 | 457 | 34 | 2218 | 82 | 1557 | 18.88 | 2084 | 126 | 2178 | 17.29 | 2045 | 65 | 1801 | 28 |
| Pr | 4511 | 27 | 906 | 34 | 4436 | 121 | 2331 | 19.24 | 4167 | 211 | 3217 | 15.22 | 4090 | 124 | 3406 | 27 |
| Nd | 4448 | 29 | 981 | 34 | 4374 | 128 | 2434 | 18.96 | 4109 | 232 | 3303 | 14.22 | 4033 | 145 | 3775 | 26 |
| Sm | 4475 | 41 | 1083 | 27 | 4401 | 158 | 2884 | 18.20 | 4134 | 306 | 3869 | 12.64 | 4057 | 188 | 4493 | 24 |
| Eu | 4484 | 39 | 909 | 23 | 4409 | 154 | 2738 | 17.80 | 4143 | 304 | 3702 | 12.20 | 4065 | 172 | 4011 | 23 |
| Gd | 4502 | 39 | 951 | 24 | 4427 | 142 | 2599 | 18.32 | 4159 | 273 | 3575 | 13.07 | 4081 | 188 | 4830 | 26 |
| Tb | 4430 | 42 | 847 | 20 | 4357 | 164 | 2812 | 17.13 | 4093 | 337 | 3776 | 11.22 | 4017 | 220 | 5063 | 23 |
| Dy | 4448 | 48 | 972 | 20 | 4374 | 170 | 2714 | 16.01 | 4109 | 346 | 3605 | 10.41 | 4033 | 227 | 4994 | 22 |
| Ho | 4457 | 47 | 767 | 16 | 4383 | 162 | 2621 | 16.20 | 4118 | 346 | 3425 | 9.90 | 4041 | 216 | 4887 | 23 |
| Er | 4457 | 60 | 1184 | 20 | 4383 | 202 | 3124 | 15.50 | 4118 | 431 | 4080 | 9.46 | 4041 | 277 | 6041 | 22 |
| Tm | 4466 | 60 | 1003 | 17 | 4392 | 195 | 2898 | 14.88 | 4126 | 428 | 3773 | 8.81 | 4049 | 266 | 5445 | 20 |
| Yb | 4475 | 59 | 934 | 16 | 4401 | 178 | 2513 | 14.15 | 4134 | 390 | 3201 | 8.21 | 4057 | 263 | 4491 | 17 |
| Lu | 4484 | 61 | 887 | 14 | 4409 | 191 | 2696 | 14.11 | 4143 | 425 | 3402 | 8.00 | 4065 | 250 | 4904 | 20 |
| Y | 4493 | 43 | 1396 | 33 | 4418 | 186 | 3273 | 17.60 | 4151 | 312 | 4621 | 14.82 | 4073 | 199 | 5618 | 28 |
| Sc | 4439 | 112 | 1063 | 9 | 4365 | 217 | 2687 | 12.40 | 4101 | 312 | 2223 | 7.13 | 4025 | 407 | 3105 | 8 |
Содержание воды в системе составляло от 2 до 13 мас. %. В качестве исходных материалов для приготовления шихты использовались следующие реактивы и соединения: высушенный гель SiO2, NaF, LiF, AlF3, Al2O3, K2SiF6. Редкоземельные элементы La, Ce, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Lu, а также Y и Sc вводились в систему в виде оксидов количестве 0.5 мас. % элемента (табл. 1). Все исходные вещества тщательно смешивали в яшмовой ступке в атмосфере спирта и помещали в платиновые ампулы, куда вводили дистиллированную воду.
Аппаратура и методика экспериментов
Опыты проводились на установке высокого газового давления с внутренним нагревом при температуре 800°С и давлении 1 и 2 кбар. Погрешность измерения температуры составляла ±5°C, давления ±10 бар. Летучесть кислорода в опытах отвечала создаваемой буфером NNO + 3.5 (Berndt et al., 2005). Скорость закалки на установке составляла 150–200 градусов в минуту. Длительность опытов составляла 5–7 суток.
В качестве контейнеров для вещества опытов использовали платиновые ампулы диаметром 3 мм, с толщиной стенки 0.2 мм и высотой 25–30 мм. В них загружали смеси исходных твердых веществ и заливали дистиллированную воду в количестве от 2 до 15 мас. % от массы навески шихты. Ампулы заваривали с помощью электродуговой сварки. Опыт считался успешно проведенным, если разница массы ампулы до и после опыта не превышала 0.001 г.
После опыта ампулы вскрывали и вместе с содержимым помещали в специальные пробирки, куда заливали дистиллированную воду в количестве 40–50 мл. Пробирки выдерживали в ультразвуковой ванне для лучшего отделения кристаллических фаз и продуктов закалки флюида от стенок ампул. Затем из этих пробирок отбирали аликвоту в количестве 10 мл, пропускали этот раствор через специальный тонкий фильтр в пробирку меньшего размера. Отфильтрованный раствор заливали смесью кислот HNO3 и HCl и затем анализировали с помощью метода ICP MS. Платиновая ампула и образец промывали на фильтре дистиллированной водой и высушивали. Затем образцы изучали под бинокуляром. Часть образца, состоящего обычно из полупрозрачного силикатного стекла и включенных в него округлых выделений (глобулей) солевой фазы, отделяли для изучения фазовых отношений на электронном микроскопе и химического анализа состава фаз на микрозонде. Из оставшегося образца с максимально возможной чистотой отбирали стекло и глобули солевой фазы, сложенные сахаровидным веществом белого цвета. Часто эти глобули сами отделялись от стекла. После этого каждая их этих фаз – матрица стекла и глобули солевой фазы проходили ту же процедуру обработки кислотами, как и флюидная фаза для анализа методом ICP MC.
Методы анализа вещества
Методы электронной микроскопии и микрозондового анализа. Изучение структуры образцов, морфологии фаз, фазовых отношений и химического состава твердых продуктов опытов проводили в Лаборатории локальных методов исследования вещества кафедры петрологии геологического факультета МГУ. Электронные изображения получены в режиме отраженных электронов (BSE). Определение главных элементов и фтора в фазах проводили с помощью сканирующего электронного микроскопа Jeol JSM-6480LV (Япония) с энерго-дисперсионным Oxford X-MaxN и кристалл-дифракционным INCA Wave-500 (Oxford Instrument Ltd., Великобритания) спектрометрами. Условия съемки: напряжение 20 kV, ток 0.7 nA. Точность оценки главных элементов в составе синтезированных фаз составляла 2–5 отн. %. Приборная погрешность при измерении фтора составила ±1% от концентрации элемента.
В ряде образцов главные и редкоземельные элементы в силикатных стеклах изучались с помощью электронно-зондового микроанализатора Superprobe JXA-8230 (Япония). Для предотвращения разрушения стекол анализы проводили в режиме расфокусированного пучка (до 10 µm) при ускоряющем напряжении 10 кВ и силе тока 10 нА. При времени измерения интенсивности пика и фона (30/15 с) дисперсия измерения Si, Al и O составляла 0.8 отн. %, K – 1.5 отн. %, Na – 2 отн. %, а F – 2 отн. %. Определение редкоземельных элементов проводили при ускоряющем напряжении 20 кВ и токе 30 nA. Время накопления для различных редкоземельных элементов подбиралось таким образом, чтобы предел их обнаружения не превышал 0.01%.
Метод масс-спектрометрии с индуктивно-связанной плазмой (для анализа микроэлементов из силикатных образцов). Определение редкоземельных элементов, Y, Sc и Li проводили методом масс-спектрометрии с индуктивно-связанной плазмой в лаборатории экспериментальной геохимии кафедры геохимии геологического факультета МГУ.
Вскрытие образцов осуществляли по методике кислотного разложения, подробно описанной в (Бычкова и др., 2016). Навеску порошка пробы, истертой до консистенции пудры, массой 1–10 мг (в зависимости от количества отобранной фазы) разлагали в тефлоновых виалах Savillex в смеси концентрированных кислот: плавиковой и азотной (5 : 1) 1.5 ml и соляной 0.5 ml. Разложение производили в микроволновой печи Вольта в режиме быстрого нагрева (150 W) в течение 3 мин и последующего длительного воздействия микроволнового излучения (50 W) в течение 35 мин. Фториды металлов разрушали путем трехкратного выпаривания пробы в концентрированной соляной кислоте под лампами до сухих солей. Затем к пробе добавляли 1 мл соляной кислоты, после чего в препарат добавляли 0.5 н HNO3 до объема 50 мл. Разбавление производили весовым способом. Конечная концентрация азотной кислоты составляла 0.5 н. На этапе последнего разбавления в 50 раз пробу в качестве внутреннего стандарта добавляли раствор индия в таком количестве, чтобы в препарате его концентрация составляла 10 ppb. Для разложения и разбавления проб использовали кислоты, перегнанные из исходных реактивов квалификации о. с. ч. и разбавленные дважды дистиллированной водой.
Измерения проводили на масс-спектрометре с ионизацией в индуктивно-связанной плазме с двойной фокусировкой Element-2. Детектирование ионов производится электронным умножителем сохраняющим линейность в диапазоне 1…1 × 1010 ионов в секунду. Для расчета концентраций элементов использовалась серия градуировочных растворов с концентрациями 0.03, 0.3, 3, 10 нг/г, приготовленных из стандартного 68-элементного раствора ICP-MS-68A, HPS (A и B). Пределы обнаружения элементов составляли от 0.01 нг/г для тяжелых и средних по массе элементов с возрастанием до 1 нг/г для легких элементов. Погрешность измерения составляла 1–3 отн. %.
В связи с малым количеством анализируемого вещества концентрации пересчитывали на содержание в фазах алюминия, заблаговременно определенные микрозондовым анализом.
Метод масс-спектрометрии с индуктивно связанной плазмой и лазерной абляцией. Определение редкоземельных элементов, Li, Sc и Y в алюмосиликатном стекле и в солевой фазе в полированных образцах проводили также методом масс-спектрометрии с индуктивно связанной плазмой и лазерной абляцией в Аналитическом сертификационном испытательном центре Института проблем технологии микроэлектроники и особочистых материалов РАН (АСИЦ ИПТМ РАН). Измерения проводили на квадрупольном масс-спектрометре с индуктивно связанной плазмой Х Series II (Thermo Scientific, США) с приставкой для лазерной абляции UP266 MACRO (New Wave Research, США) при следующих рабочих параметрах: масс-спектрометр – выходная мощность ВЧ-генератора 1200 Вт, расход плазмообразующего потока аргона 13 л/мин, вспомогательного – 0.90 л/мин, расход несущего газа He 0.6 л/мин с последующим смешиванием с Ar 0.6 л/мин, разрешение 0.4 и 0.8 M; приставка для лазерной абляции – длина волны лазера 266 нм, частота повторения импульсов 10 Гц, энергия импульса 3 мДж, длительность импульса 4 нс, диаметр кратера 60 мкм. Время одного измерения составляло 10 с. Если размеры образца позволяли, лазерный луч сканировали по поверхности со скоростью 20 мкм/с, в противном случае использовали режим абляции “в точке”. На каждом образце проводили до 5 измерений (в зависимости от размеров образца) и результаты усредняли. При этом значения, резко отличающиеся от других из той же выборки, отбрасывались в соответствии с критерием Смирнова–Граббса (с доверительной вероятностью 90%). Внешнюю калибровку проводили с помощью стандартных образцов силикатного стекла NIST SRM-610–616. В качестве внутреннего стандарта использовали кремний. Кроме того проводили дополнительную коррекцию матрицы, учитывая что элементы основы фазы стекла находятся в ней в форме оксидов, а солевой фазы – в виде фторидов.
Пределы определения элементов, найденные с использованием 3σ-критерия (с доверительной вероятностью P = 0.95), для РЗЭ составляют от 1 × 10–7 до 1 × 10–6 мас. %; относительно высокий предел для Sc 2 × 10–4 мас. % обусловлен полиатомными интерференциями: 45Sc (28Si17OH, 29Si16O).
РЕЗУЛЬТАТЫ ЭКСПЕРИМЕНТА
Фазовые отношения и распределение породообразующих и редкоземельных элементов рассматриваются по результатам двух серий экспериментов в системе Si–Al–Na–K–Li–F–O–H, проведенных с одним и тем же опорным отношением главных компонентов и содержаниями редких элементов, при одинаковой температуре 800°С, но при различных давлениях и содержаниях воды: 1) P = 1 кбар, (2.06); (5.12); (9.34) и (13.27) мас. % H2O; 2) Т = 800°С, P = 2 кбар, (2.44); (4.94); (11.11) и (12.89)% H2O от всей массы системы.
Изучение продуктов проведенных опытов методом электронной микроскопии подтвердило результаты изучения фазовых отношений в системе (Алферьева и др., 2011). При температуре 800°С, давлении 1 и 2 кбар и различном содержании воды стабильно воспроизводится равновесие двух расплавов - алюмосиликатного (L) и алюмофторидного (солевого LF). Условия эксперимента, исходный состав системы, средние составы главных равновесных фаз и содержания редкоземельных элементов в этих фазах приведены в табл. 1.
Фазовый состав продуктов опытов
800°C, 1 кбар. Основу образцов составляет алюмосиликатное стекло (закаленный расплав L), в которое погружены крупные солевые глобули, представляющие собой закаленный солевой щелочноалюмофторидный расплав (LF). Количество солевого расплава по объему составляет около 20–25%. Стекло (рис. 1а, 1б) представлено однородным веществом серого цвета (в BSE) с мелкими выделениями Li–Na–K алюмофторидных фаз (FP) разных оттенков и различно й формы, иногда обладающих элементами огранки. Эти фазы мы считаем закалочными вследствие малого размера (2–10 мкм в диаметре) и неоднородности их состава, выраженной в соотношении Al, F, К, Na и, вероятно, Li. Анализ стекла (матрицы) на микрозонде проводили по большим площадям (0.008 до 0.02 мм2), включающим эти закалочные фазы (табл. 1). Такие фрагменты стекла с мелкими закалочными фторидными фазами, представляющие валовой состав силикатного расплава, с одной стороны, и крупные солевые глобули, отражающие безводный валовой состав солевого расплава, с другой, отбирали под бинокуляром для анализа на редкоземельные элементы методом ICP MS.
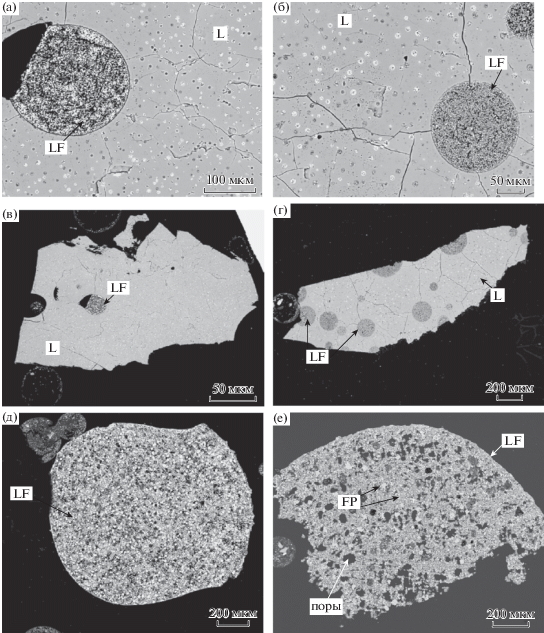
Рис. 1.
Фазовые отношения алюмосиликатного расплава (стекла L) и закаленного алюмофторидного расплава (полифазного глобуля LF) в опытах при 800°С, 1 кбар при содержаниях воды 2.06%, опыт 776 (а, в, д) и 13.27%, опыт 775 (б, г, е).

Глобули (LF) округлой и овальной формы диаметром от 20 до 1000 мкм имеют четкие границы с силикатной матрицей. Солевой расплав при закалке кристаллизуется и образует полифазный агрегат мелких кристаллов фторидов и алюмофторидов Li, Na, K размером от 2–3 до 5–7 мкм. Анализ солевой фазы также проводили по большим площадям, включающим все закалочные фазы глобулей (табл. 1). Солевые глобули, помимо Li-, K-, Na-алюмофторидов и LiF, богаты фторидами REE, Y и Sc, образующимися при закалке солевого расплава. В их составе нередко присутствуют первые проценты Na и K. Они образуют микроскопические светлые (в BSE) кристаллы, ярко выделяющиеся на фоне фторидов щелочей. Часто они равномерно распределены в объеме солевых глобулей, но иногда группируются в более крупные агрегаты кристаллов в их краевых частях. Нередко фториды REE образуют прерывистые тонкие (1–3 мкм) каймы на границы матрицы стекла и солевых глобулей. Эти каймы не было возможности проанализировать, не захватив при этом материал матрицы и глобулей. В силикатном стекле фториды редкоземельных элементов не встречаются. В пределах крупных глобулей нередко наблюдаются выделения силикатного стекла в виде капель (рис. 1е).
В силикатных стеклах образцов в зависимости от условий присутствует различное количество мелких пор, характеризующих потерю воды расплавом в процессе закалки. В стеклах опытов с небольшим исходным содержанием воды (2.06%) количество пор составляет менее 1% (рис. 1а). В солевых глобулях (рис. 1в, 1д) небольшое количество мельчайших пор. В стеклах опытов в более богатой водой части системы (13.27%) отмечаются мелкие поры $ \ll $1 мкм (рис. 1б), часто образующие гирлянды вокруг выделений фторидов. В крупных глобулях опытов с большим содержанием воды (рис. 1г, 1е) пористость значительно увеличивается: размер пор возрастает до 50 мкм, их количество примерно до 5%.
800°C, 2 кбар. Фазовый состав образцов, полученных при 2 кбар, подобен тому, что наблюдается в опытах при 1 кбар (рис. 2). Во всех опытах присутствуют те же две главные фазы – алюмосиликатное стекло в виде матрицы и солевые фазы в виде глобулей. Редкоземельные фториды иногда образуют небольшие скопления или тонкие каймы на границе этих двух фаз. По электронномикроскопическим снимкам видно, что в образцах, особенно, в глобулях солевых фаз, наблюдается большее количество пор, чем было замечено в опытах при меньшем давлении 1 кбар. Размер пор более крупный в опыте с более высоким содержанием воды (опыт 784, 12.89% H2O, рис. 2е), чем в опыте 785 с 2.44% H2O (рис. 2в, 2д).
Химический состав и распределение главных компонентов между фазами в системе при 800°С, 1 и 2 кбар
Принципиальных отличий состава фаз в отношении породообразующих компонентов в опытах, проведенных при различных давлениях и содержаниях воды, в системе не наблюдается. Нарушение баланса для этих элементов между исходным и измеренным количеством элемента обычно не превышает точности анализа. Величины стандартного отклонения для Si, Al, Na, K не превышают первых десятых процента. Они возрастают для F до 0.5–5% и кислорода до 0.5–3%. Во всех опытах по коэффициентам разделения элементов отмечается преимущественное распределение Na, Al и F в пользу алюмофторидной (солевой) фазы и K, Si и O – в пользу алюмосиликатной (табл. 1). При этом KdAl и KdK солевая/силикатная фаза близки к 1. Лишь для одного из опытов (775) коэффициенты разделения заметно отличаются от других, что можно связать с большей неоднородностью фторидной фазы. Оценка изменения относительных количеств фаз в опытах показала, что при увеличении содержания воды в системе количество фторидной солевой фазы относительно силикатной уменьшается (от ~15 до ~8% при 1 кбар и от ~17 до ~9% при 2 кбар). Количество кислорода в закалочном силикатном стекле превышает необходимое для насыщения зарядов катионов. Оно в большей степени может относиться к растворенной в расплаве воде. Отчасти в связи с этим при анализе стекла на микрозонде получаются суммы, превышающие допустимые (100 ± 2 мас. %) при анализе. Суммы, превышающие 102% появляются в стеклах с содержанием фтора, превышающим 15%. Очевидно, для выявления причин этого явления и улучшения анализа требуется дополнительная методическая работа, которую предстоит провести. Заниженные суммы в анализах солевых фаз связаны, по-видимому, с высокой пористостью фаз, высокими неоднородностью их состава и необычно высокими содержаниями фтора (40–60%), не столь точно определяемым в солевой фазе на микрозонде, как главные компоненты.
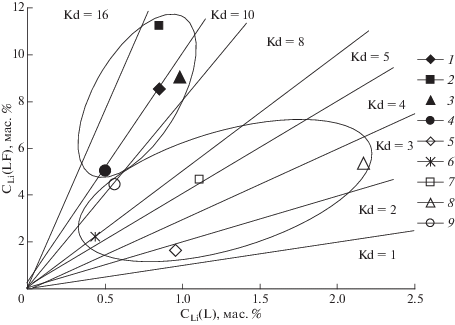
Распределение Li между алюмосиликатным и солевым расплавами в системе. Содержание Li в исходном составе опытов 1.26–1.38 мас. % с учетом его низкой атомной массы позволяет считать его одним из главных компонентов. Ранее (Граменицкий и др., 2005; Алферьева и др., 2011) было показано, что даже небольшое количество лития существенно влияет на фазовые отношения в системе. Если в безлитиевой области составов в богатых фтором условиях реализуется равновесие расплав L-криолит, то добавление ~1 мас. % Li приводит к формированию солевого алюмофторидного расплава LF с большим полем его существования (L + LF) и, соответственно, уменьшению поля (L + Crl). В проведенных при давлении 1 кбар экспериментах Li концентрируется преимущественно в солевом расплаве от 8.55 до 11.23 мас. %, но также входит в состав алюмосиликатного расплава в количестве 0.83–0.98 мас. % (табл. 1, рис. 3). Коэффициенты разделения между солевым и силикатным расплавами KdLi = = ${{С_{{{\text{Li}}}}^{{{\text{LF}}}}} \mathord{\left/ {\vphantom {{С_{{{\text{Li}}}}^{{{\text{LF}}}}} {{\text{С}}_{{{\text{Li}}}}^{{\text{L}}}}}} \right. \kern-0em} {{\text{С}}_{{{\text{Li}}}}^{{\text{L}}}}}$ при 1 кбар составляют от 9.23 до 13.24 (табл. 1, рис. 3). В опытах, проведенных при 2 кбар, поведение Li изменяется. Концентрация Li в алюмофторидном расплаве в большинстве опытов и коэффициенты разделения KdLi уменьшаются до значений 1.7–7.86 (табл. 1, рис. 3). На рис. 3 на примере опыта 785 (точки 5 и 6) видно, что содержания Li, полученные двумя методами отличаются незначительно, но они приводят к существенному изменению KdLi. Однако это не изменяет тенденции уменьшения KdLi(LF/L) при увеличении давления в системе. Наибольшие коэффициенты разделения характерны для обеих величин давления при содержании воды в системе более 5 мас. %.
Рис. 3.
Распределение Li между алюмосиликатным (L) и солевым (LF) расплавами при 800°С и давлении 1 и 2 кбар. Условные обозначения: 1, 2, 3, 4 – опыты 775–778 при 1 кбар; 5, 6, 7, 8, 9 – опыты 785–787 при 2 кбар. Содержание воды в системе, соответственно, 2.06; 5.12; 9.34; 13.27; 2.44; 4.94; 11.11; 12.89 мас. %. Составы определены методом масс-спектрометрии с индуктивно связанной плазмой: 1, 6, 9 – с помощью приставки для лазерной абляции; 2, 3, 4, 5, 7, 8 путем растворения проб. Линии соответствуют коэффициентам разделения (LF/L), равным от 1 до 16.
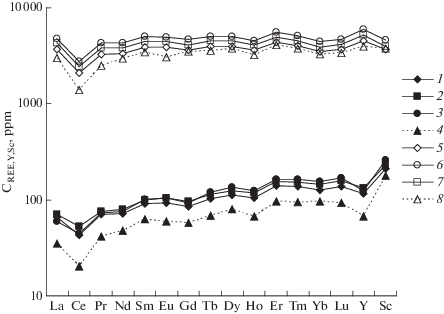
Распределение REE, Y и Sc при 800°C, 1 кбар. Во всех опытах содержания редкоземельных элементов, иттрия и скандия в солевом расплаве более, чем на порядок, выше, чем в силикатном (табл. 1, рис. 4). В табл. 1 большая часть приведенных данных по редким элементам относится к полученным методом ICP MS путем анализа из растворов. Однако для опытов 775 и 784, в материале которых не удалось отобрать глобули солевой фазы, сделаны анализы REE, Y, Sc и Li методом лазерной абляции в аншлифах. Для опыта 785 также приведены данные, полученные с помощью лазерной абляции, имеющие лучший баланс вещества, чем сделанные путем анализа из раствора. Содержания элементов в силикатном стекле повышаются в рядах в зависимости от атомного номера от La до Lu, но не монотонно. Для всех опытов содержание Ce, Gd, Ho меньше, а Eu, Dy, Er – больше, чем у соседних элементов. Содержания Y такие же, как у средних членов группы (от Tb до Er), а Sc – выше, чем у любого из них. Минимум по Ce, очевидно, связан с меньшим введенным в шихту количеством реактива (табл. 1, рис. 4). Возрастание содержаний в ряду редкоземельных элементов в алюмофторидной солевой фазе не выражено, но максимумы и минимумы сохраняются по тем же элементам, что и в силикатной фазе. Концентрации Y и Sc довольно резко отличаются в силикатных стеклах: концентрация Y ниже, а Sc выше по сравнению с содержаниями REE. Во фторидных же фазах концентрации Y заметно выше, чем у всех элементов REE, а Sc на уровне или немного ниже Lu. Эти соотношения элементов четко отражают относительно большее сродство Y к солевому, а Sc к силикатному расплаву. Зависимость концентраций элементов от содержания воды, введенной в систему, практически отсутствует, различия не превосходят аналитические ошибки. Концентрации REE, Y и Sc, определенные как в стекле, так и во фторидной фазе большинства образцов, ниже, чем, чем исходные. Наибольший вклад в сумму REE вносят содержания в солевой фазе. Только в одном опыте 778 сумма определенных REE в солевой фазе превышает сумму введенных элементов на ~3%. В остальных опытах полученная сумма REE меньше суммы введенных REE на 6–18%. В опыте 785 были получены (методом ICP MS анализа из раствора) слишком низкие концентрации REE, поэтому содержания в табл. 1 приводятся по данным лазерной абляции, по которым баланс немного лучше. Потери при анализе REE могут быть связаны, видимо, с наличием не анализированных фаз с высокими содержаниями этих элементов, которыми являются кристаллы их фторидов. В продуктах закалки опытов они постоянно образуют вкрапленность в виде кайм на границе солевой и алюмосиликатной фаз, иногда на границе с порами. Части обеих фаз, прилегающие к их границе, невозможно было отобрать в соответствующие фракции, подлежащие анализу методом ICP MS. Оценка баланса масс редкоземельных элементов показала, что для его соблюдения в системе должно быть около 0.005 весовых долей редкоземельных фторидов. Поскольку в них очень высокая концентрация REE, то даже небольшое количество кристаллов REE, не попавшее в пробу при анализе из раствора, должно привести к понижению измеряемых концентраций. Пограничные между силикатной и солевой фазами кристаллы REE не были проанализированы и при применении метода лазерной абляции, поскольку пограничную область не включали в анализ, чтобы не захватить окружающее стекло (при диаметре кратера 60 мкм). Пока невозможно однозначно сказать, являются ли не попавшие в пробу кристаллы редкоземельных фторидов 3-й равновесной фазой в условиях проведения опыта, закристаллизовавшейся в системе наряду с двумя расплавами вследствие их насыщения REE, или их следует считать принадлежностью солевой фазы LF. Авторы отдают предпочтение первой точке зрения. Поэтому было правомочно изучать KdREE между двумя равновесными закаленными расплавами, не включая третью фазу редкоземельных фторидов, как и было сделано в данной работе.
Рис. 4.
Различие содержаний CREE,Y,Sc (ppm) в силикатном L (1–4) и солевом расплава LF (5–8) при 800°С, 1 кбар и различных концентрациях воды (мас. %). Условные обозначения: 1, 5 – 2.06%, опыт 776; 2, 6 – 4.12%, опыт 778; 3, 7 – 9.34%, опыт 777; 4, 8 – 13.27%, опыт 775. Пунктирные линии построены по данным метода лазерной абляции.
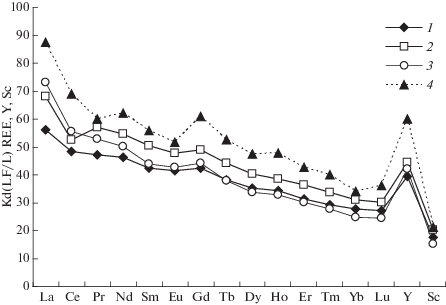
Коэффициенты разделения КdREE между алюмосиликатным и алюмофторидным расплавами опытов при 1 кбар имеют очень высокие значения от 15 для Lu до 73 для La, главным образом, за счет изменения содержаний REE в силикатной фазе. В каждом спектре KdREE монотонно понижаются c увеличением атомного номера от La к Lu (рис. 5). Во всех спектрах коэффициентов разделения KdREE имеются небольшие максимумы для Gd по сравнению с KdREE рядом расположеных Eu и Tb. В двух спектрах KdREE (2.06 и 5.12% H2O) проявлены минимумы для Ce. Наиболее высокие значения KdREE характерны для опыта 778 с содержанием воды 5.12%. Для этого же опыта определены наиболее высокие KdLi. Значения Kd для La и Ce близки друг к другу в опытах с 5.12 и 9.34% воды, но, начиная с Pr, спектры Kd расходятся. При этом Kd для опытов с 9.34 и 2.06% воды практически не отличаются, начиная с Sm. Коэффициент разделения скандия в каждом опыте ниже, чем для всех редкоземельных элементов. Величина Kd иттрия близка к значениям для легких REE во всех опытах. Наиболее высокие KdREE получились для опыта 775 (13.27% H2O), определение которого проведен методом лазерной абляции. Видно (рис. 5), что форма профиля REE вполне сопоставима с данными, полученными методом ICP MS путем растворения проб, но максимальные значения Kd в 1.2 раза больше тех, что получены из данных лазерной абляции.
Рис. 5.
Коэффициенты разделения REE, Y и Sc между солевым и силикатным расплавами при 800°С и 1 кбар и различных содержаниях воды в системе: 1 – 2.06%, опыт 776; 2 – 5.12%, опыт 778; 3 – 9.34%, опыт 777; 4 – 13.27%, опыт 775. Пунктирные линии построены по данным метода лазерной абляции.
800°C, 2 кбар. При большем давлении сохраняется преимущественное накопление REE в солевом расплаве и тенденции повышения содержаний REE от легких к тяжелым (табл. 1, рис. 6). Содержания Y и Sc в силикатном стекле не расходятся столь заметно, как при 1 кбар. Уровень концентраций REE в солевом расплаве понижается по сравнению с опытами при 1 кбар, а в силикатном – повышается. На графиках KdREE проявлен максимум по Gd (рис. 7) для всех опытов. На одном из графиков (4.94% H2O) есть минимум для Ce. В серии при давлении 2 кбар мы использовали результаты анализа методом лазерной абляции для опытов 784 и 785. Данные лазерной абляции характеризуются похожими тенденциями изменения концентраций REE в фазах (рис. 6), но более высокими (около 2 раз) значениями KdREE. Особенно эти различия проявлены для легких REE. Поскольку данные для опытов при 2 кбар получены разными методами, их трудно сравнивать в отношении влияния воды на KdREE.
Рис. 6.
Сближение содержаний CREE,Y,Sc (ppm) в алюмосиликатном L (1–4) и солевом LF расплавах (5–8) при 800°С, 2 кбар и различных концентрациях воды (мас. %): 1, 5 – 2.4%, опыт 785; 2, 6 – 4.94%, опыт 786; 3, 7 – 11.11%, опыт 787; 4, 8 – 12.89%, опыт 784. Пунктирные линии построены по данным метода лазерной абляции.
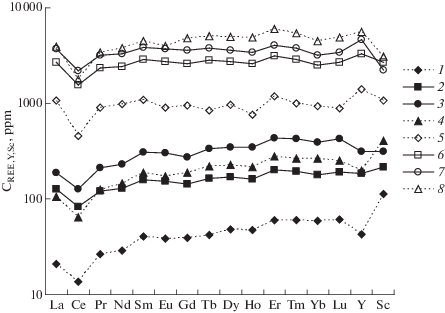
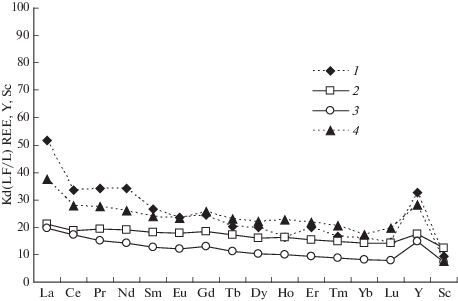
Рис. 7.
Коэффициенты разделения REE, Y и Sc между алюмофторидным и алюмосиликатным расплавами при 800°С и 2 кбар с различными исходными содержаниями воды в системе (мас. %): 1 – 2.44%, опыт 785; 2 – 4.94%, опыт 786; 3 – 11.11%, опыт 787; 4 – 12.89%, опыт 784. Пунктирные линии построены по данным метода лазерной абляции.
Существенное понижение концентраций REE в солевом расплаве и небольшое их повышение в силикатном расплаве приводит к ранее неизвестному эффекту: существенному уменьшению коэффициента разделения КdREE, Y и Sc между солевым и алюмосиликатным расплавами при увеличении давления от 1 до 2-х кбар (рис. 5, 7).
Распределение REE,Y, Sc и Li между расплавами и флюидом при 800°C и 2 кбар. В серии опытов при 800°С и 2 кбар по методике, изложенной выше, отбирали продукты закалки флюидной фазы, в которых определяли концентрацию REE, Y, Sc и Li (табл. 2, рис. 8). Содержание Li в них на 1–2 порядка ниже, чем в силикатной (табл. 2) и в солевой фазах. Коэффициенты разделения Li KdLi (Fl/L) между флюидом и силикатным расплавом составляют 0.0009–0.04. Для REE и Y концентрации в силикатной фазе превышают содержания во флюидной фазе в тясячи раз, для Sc в сотни раз (табл. 1, 3). Характер спектров РЗЭ близок для четырех опытов. Имеются различия лишь для Pr и Nd, коэффициенты разделения Kd (Fl/L) которых дают максимумы (по отношению к соседним Ce и Sm) для опытов с 2.44 и 11.11% воды в системе. Есть отличие в распределении иттрия, KdY(Fl/L) которого понижается по сравнению с KdREE для опытов с 2.44 и 4.94% воды, и KdSc скандия, который повышается для всех опытов, кроме, содержавшего с 4.94% воды. Заметно небольшое увеличение Kd (Fl/L) от легких к тяжелым REE. Различия в Kd (Fl/L), получившиеся при анализе REE c силикатном стекле методом лазерной абляции, превышают в 2–4 раза значения, получившиеся при анализе проб методом из раствора, что связано с более высокими содержаниями REE в стеклах в последнем случае.
Таблица 2.
Содержание РЗЭ, Y, Sc и Li (ppm) в силикатном расплаве (стекле L) и во флюидной фазе (Fl) и коэффициенты разделения Kd (Fl/L) между флюидом (Fl) и силикатным расплавом (L) в опытах при 800°С, 2 кбар при различных содержаниях H2O (мас. %)
| Эле- мент |
785; 2.44 | 786; 4.94 | 787; 11.11 | 784; 12.89 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Fl* | L* | Kd * | L** | Kd** | Fl* | L * | Kd * | Fl* | L* | Kd* | Fl* | L* | Kd* | L** | Kd** | |
| La | 0.0112 | 78 | 0.0001 | 21 | 0.0005 | 0.1053 | 128 | 0.0008 | 0.0072 | 189 | 0.00004 | 0.0058 | 314 | 0.00002 | 105 | 0.00006 |
| Ce | 0.0120 | 49 | 0.0002 | 14 | 0.0009 | 0.0652 | 82 | 0.0008 | 0.0047 | 126 | 0.00004 | 0.0033 | 202 | 0.00002 | 65 | 0.00005 |
| Pr | 0.0398 | 81 | 0.0005 | 27 | 0.0015 | 0.1144 | 121 | 0.0009 | 0.0197 | 211 | 0.00007 | 0.0058 | 322 | 0.00002 | 124 | 0.00005 |
| Nd | 0.1279 | 86 | 0.0015 | 29 | 0.0044 | 0.1219 | 128 | 0.0009 | 0.0438 | 232 | 0.00019 | 0.0061 | 340 | 0.00002 | 145 | 0.00004 |
| Sm | 0.0290 | 110 | 0.0003 | 41 | 0.0007 | 0.1634 | 158 | 0.0010 | 0.0167 | 306 | 0.00005 | 0.0079 | 417 | 0.00002 | 188 | 0.00004 |
| Eu | 0.0351 | 110 | 0.0003 | 39 | 0.0009 | 0.1776 | 154 | 0.0012 | 0.0208 | 304 | 0.00007 | 0.0088 | 407 | 0.00002 | 172 | 0.00005 |
| Gd | 0.0345 | 101 | 0.0003 | 39 | 0.0009 | 0.1624 | 142 | 0.0011 | 0.0203 | 273 | 0.00007 | 0.0080 | 385 | 0.00002 | 188 | 0.00004 |
| Tb | 0.0483 | 125 | 0.0004 | 42 | 0.0012 | 0.2174 | 164 | 0.0013 | 0.0315 | 337 | 0.00009 | 0.0107 | 439 | 0.00002 | 220 | 0.00005 |
| Dy | 0.0505 | 128 | 0.0004 | 48 | 0.0010 | 0.2228 | 170 | 0.0013 | 0.0322 | 346 | 0.00009 | 0.0115 | 429 | 0.00003 | 227 | 0.00005 |
| Ho | 0.0475 | 126 | 0.0004 | 47 | 0.0010 | 0.2101 | 162 | 0.0013 | 0.0283 | 346 | 0.00008 | 0.0102 | 421 | 0.00002 | 216 | 0.00005 |
| Er | 0.0663 | 159 | 0.0004 | 60 | 0.0011 | 0.2680 | 202 | 0.0013 | 0.0366 | 431 | 0.00008 | 0.0125 | 516 | 0.00002 | 277 | 0.00005 |
| Tm | 0.0771 | 159 | 0.0005 | 60 | 0.0013 | 0.2825 | 195 | 0.0015 | 0.0418 | 428 | 0.00010 | 0.0121 | 494 | 0.00002 | 266 | 0.00005 |
| Yb | 0.0888 | 146 | 0.0006 | 59 | 0.0015 | 0.2866 | 178 | 0.0016 | 0.0474 | 390 | 0.00010 | 0.0114 | 431 | 0.00003 | 263 | 0.00004 |
| Lu | 0.1098 | 158 | 0.0007 | 61 | 0.0018 | 0.3168 | 191 | 0.0017 | 0.0523 | 425 | 0.00010 | 0.0117 | 462 | 0.00003 | 250 | 0.00005 |
| Y | 0.0397 | 138 | 0.0003 | 43 | 0.0009 | 0.2401 | 186 | 0.0013 | 0.0372 | 312 | 0.00010 | 0.0130 | 455 | 0.00003 | 199 | 0.00007 |
| Sc | 0.1366 | 133 | 0.0010 | 112 | 0.0012 | 0.1797 | 217 | 0.0008 | 0.1811 | 312 | 0.00058 | 0.4823 | 391 | 0.00123 | 407 | 0.00118 |
| Li | 176.48 | 9520 | 0.0185 | 4369 | 0.0401 | 319.36 | 11 096 | 0.0288 | 137.20 | 21 700 | 0.00063 | 14.55 | 15 503 | 0.00094 | 5653 | 0.00255 |
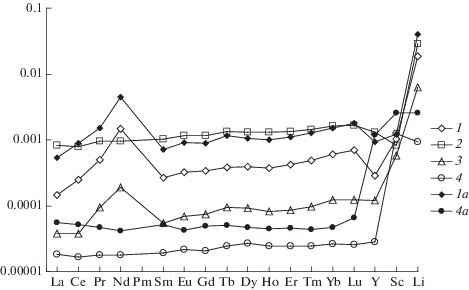
Рис. 8.
Распределение редкоземельных элементов и лития (KdREE,Y,Sc,Li) между флюидом и силикатным расплавом (Fl/L) при 800° и 2 кбар в опытах с различными исходными содержаниями воды в системе: 1 – 2.44%, опыт 785; 2 – 4.94%, опыт 786; 3 – 11.11%, опыт 787; 4 – 12.89%, опыт 784; 1а и 4а – ,данные по о содержанию REE, Y, Sc, Li в L для опытов 785 и 784, полученные методом лазерной абляции.
В заключение раздела по результатам эксперимента следует сказать, что авторы статьи провели опыты и изучили распределение редкоземельных элементов и лития двумя методами. Опорными результатами мы считаем полученные методом ICP MS путем анализа фаз из раствора, поскольку они наиболее полно характеризуют валовые составы силикатной, солевой и флюидной фаз в отношении всех компонентов в соответствии с пониманием авторами фазовых отношений в системе. Мы также провели определение содержаний REE и Li в твердых фазах методом лазерной абляции и получили коэффициенты разделения элементов, несколько выше, чем полученные при анализе растворов. Отличия эти связаны, главным образом, с меньшей концентрацией REE в силикатном расплаве, поскольку применение локального метода лазерной абляции обеспечивало анализ относительно чистого стекла, возможно, лишь с небольшим содержанием закалочных фаз фторидов. Тенденции изменения концентраций REE не противоречат полученным при использовании метода ICP MS путем анализа растворов. Абсолютные значения коэффициентов разделения элементов при применении метода лазерной абляции приближаются к данным работы (Veksler, 2005), но все же меньше по величине. Появление каймы из фторидов REE вокруг глобулей в наших экспериментах связано, по-видимому, с насыщением солевого расплава REE при введении каждого элемента в количестве 0.5%. В работе (Граменицкий, Щекина, 2005) вводилось от 1 до 2% каждого REE. Вероятно, в этом случае в кайме и внутри самих солевых глобулей возникали равновесные кристаллы фторидов REE, которые мы относили к фазе солевого расплава. В работе (Veksler et al., 2005) исходные содержания были на порядок меньше, и концентрация насыщения REE, по-видимому, не достигалась. В системе не было кристаллических фаз REE, и распределение изучалось четко между силикатной и солевой фазами. Этим объясняется лучший баланс в системе по REE.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Одной из целей экспериментов в данной работе было уточнение фазовых отношений в модельной литийсодержащей гранитной системе с предельными содержаниями фтора при 800°С с разной степенью насыщения водой и различных величинах давления. Проведенные опыты подтвердили главное ожидаемое принципиальное изменение фазовых отношений, заключающееся в том, что при обоих давлениях (1 и 2 кбар) и повышении содержания воды (от 2 до 13 мас. % H2O) в системе проявлялось трехфазное равновесие: силикатный и солевой расплавы + свободный водный флюид. При дальнейшем увеличении содержания воды неизбежно должен происходить переход снова к двухфазным равновесиям: флюид + силикатный расплав и флюид + фторидный расплав и появлению области флюидной фазы, равновесной с обоими расплавами. Для изучения этой фазы требуются дальнейшие исследования. Поскольку флюид не закаливается или дает в некоторых случаях похожие на фторидный расплав продукты закалки, которые трудно отделить от других фаз, изменение фазовых отношений искали в косвенных признаках. К примеру, было обнаружено, что при увеличении содержания воды в системе от 2 до 13% при обоих давлениях количество солевой фазы уменьшалось, что предполагает ее частичное растворение в силикатной фазе. Об этом можно судить по тенденции возрастания содержания фтора в силикатном расплаве при повышении содержания в системе воды, как это и ожидалось, исходя из предшествующих работ (Holtz et al., 1993; Алферьева и др., 2018). Согласно нашим оценкам содержаний воды, растворимость воды в силикатном расплаве в присутствии алюмофторидного расплава достигала 7–8 мас. %. По расчетным данным в солевом расплаве растворимость воды может быть почти в 2 раза больше, чем алюмосиликатном (Алферьева и др., 2018). Именно об этом свидетельствует высокая насыщенность порами солевых фаз (рис. 1, 2) в опытах с высокой концентрацией воды в системе. Определить содержание воды в солевом расплаве не представляется возможным, т.к. в нем после закалки нет водосодержащих фаз. Вероятно, что увеличение взаимной растворимости фаз и сближение их составов может произойти, при более существенном изменении давления, чем было в наших экспериментах. (Смирнов, 2015; Котельников и др., 2018).
Напрашивается предположение, что при повышении давления от 1 до 2 кбар происходит изменение структуры расплава, связанное с заменой кислорода фтором, кремния алюминием и другими факторами, на которые отзываются редкоземельные элементы. Они выступают в этом случае как геохимические индикаторы изменений, происходящих в алюмосиликатном расплаве (магме).
Свойства расплава алюмосиликатного расплава кислого состава меняются при добавлении в систему фтора, способствуя возникновению комплексов Al с F. Часть Al переходит из четырех- в шестерную координацию, образуя группировки [${\text{AlF}}_{6}^{{3 - }}$] (Manning, 1980; Sсhaller et al., 1992). При закалке силикатного расплава часть фтора в составе алюмофторидов выделяется в виде мелких закалочных фаз. Судя по продуктам его закалки в наших экспериментах и кристаллизации ликвидусных фаз, группировки [${\text{AlF}}_{6}^{{3 - }}$] составляют основу солевого расплава. Щелочные элементы Li, Na и K, соединяясь с [${\text{AlF}}_{6}^{{3 - }}$], формируют в солевом расплаве комплексы, подобные (Li,Na,K)3AlF6, которые при закалке расплава образуют кристаллы K,Na- и Na,K-криолита, Li-содержащего K,Na-криолита, криолитионита Na3Li3Al2F12 и симмонсита Na2LiAlF6. Литий присутствует также в виде грайсита LiF, образуя агрегаты мелких кристаллов с фторидами редкоземельных элементов, иттрия и скандия (LnF3, YF3, ScF3). Среди закалочных фаз имеются также комплексные фториды состава (Na,K,Li)3LnF6 или (Na,K,Li)LnF4. Эти данные свидетельствуют о реальной структуре солевого расплава, основу которого образуют комплексные соединения фтора с Al, РЗЭ, Y, Sc и щелочными элементами Na, K и Li.
Высокая прочность связи Ln–F, Sc–F, Y–L определяет устойчивость фторидных комплексов и их малую растворимость в воде. Имеющихся в настоящее время данных по растворимости соединений REE, Y и Sc и их комплексообразованию (Комиссарова, 2001; Степанчикова, 2014; Haas et al., 1995), не достаточно для оценки состава флюидной фазы при высоких параметрах, отвечающих условиям наших экспериментов.
Редкоземельные элементы, Y, Sc и Li оказались значительно более чувствительными к процессам, происходящим в системе, чем петрогенные элементы. Был обнаружен четкий эффект фракционирования REE, Y, Sc и Li между несмешивающимися силикатным и солевым расплавами, зависящий от давления и содержания воды в системе, который может указывать на изменения в свойствах самих расплавов. При увеличении давления от 1 до 2-х кбар уменьшается контрастность распределения редкоземельных элементов в сосуществующих расплавах за счет существенного понижения концентраций РЗЭ в солевом и небольшого их повышения в силикатном расплаве (рис. 4, 6). Это приводит к резкому уменьшению коэффициентов разделения Kd (рис. 5, 7). Литий играет ключевую роль как в возникновении несмесимых расплавов в изучаемой системе, так и распределении редкоземельных элементов. Во всех опытах наблюдается прямая корреляция между коэффициентами разделения Li и REE, Y, Sc.
Исследования показали, что все РЗЭ, Y и Sc имеют сходный характер распределения, но в ряде случаев обладают особенностями. Поведение Y и Sc резко отличаются в силикатных стеклах: содержание Y отвечает средним REE, а концентрация Sc выше, чем у любого члена группы. Во фторидных же фазах содержание Y заметно выше, чем у всех REE, а концентрация Sc – на уровне или немного ниже Lu. Эти соотношения элементов четко отражают относительно большее сродство Y к солевому, а Sc – к силикатному расплаву, что должно вести к расхождению их геохимической истории. Наблюдается последовательное уменьшение коэффициентов разделения от легких к тяжелым REE, но на всех спектрах проявляется максимум Kd гадолиния. При переходе от Gd к Tb происходит скачок потенциала ионизации, вызванный 50% заполнением f-уровня седьмого, находящегося в середине ряда REE атома Gd. Такой эффект носит название “Gd разрыва” (Lottermoser, 1992; Скублов, 2011). В то же время Eu образует небольшой минимум на некоторых спектрах KdREE. Несмотря на равенство ионных радиусов Y и Ho, во всех опытах коэффициенты разделения KdY $ \gg $ KdHo. При близости ионных радиусов Sc и Lu между их коэффициентами разделения наблюдаются большие различия: KdSc$ \ll $ KdLu. Эти различия должны сказываться на их геохимическом поведении.
При изучении распределения РЗЭ между силикатным и солевым расплавами ожидалось проявление тетрад эффекта, который был обнаружен в спектрах РЗЭ (нормированных по содержаниям РЗЭ в хондрите) высоко дифференцированных, богатых фтором гранитоидов (Скублов, 2005; Ясныгина и др., 2008; Перетяжко, Савина, 2010; 2010; Гусев А.И., Гусев A.А., 2011; 2014; Irber, 1999; Веа, 1996; Zheng-Hang Lv et al., 2018). Реальность тетрад-эффекта была продемонстрирована в работе (Veksler et al., 2005, 2012) при изучении распределения REE между силикатным и солевым расплавами в гранитной системе при 800°C, 1 кбар. По данным нашей работы в распределении REE тетрад-эффекта не обнаружено. На спектрах Kd РЗЭ (LF/L), как при давлении 1, так и 2 кбар (рис. 7 и 9), можно наблюдать лишь слабые минимумы в районе тетрады Sm–Gd и на некоторых спектрах небольшие прогибы между Lа–Nd и Gd–Ho. Щелочноалюмофторидные солевые расплавы являются очевидными концентраторами всех REE, Y и Sc. Для солевых расплавов такого типа предполагалось наличие распределения REE W-типа (Ясныгина и др., 2008; Перетяжко, Савина, 2010 и др.). Однако в наших экспериментах оно не было выявлено.
На характер спектров REE могут влиять различные солевые и летучие компоненты (Бычков и др., 2012; Луканин, Дернов-Пегарев, 2010; Попова и др., 2017), содержащиеся во флюидной фазе, связанной с гранитным магматизмом, метасоматозом и рудообразованием. В магматическую и постмагматическую стадию может происходить гетерогенизация флюидных фаз с образованием концентрированных и разбавленных флюидов (Бычков и др. 2012). Появление спектров REE с выраженными тетрадными эффектами в гранитоидах нередко связывается с влиянием флюидов, содержащих комплексы REE с фтором (Lottermoser, 1992; Irber, 1999). Действительно, образование комплексов REE (${\text{LnF}}_{2}^{ - },$ LnF2–, ${\text{LnF}}_{3}^{0}$, ${\text{LnF}}_{4}^{ - }$) в растворах добавляет ковалентный вклад в ионную химическую связь в такие соединения редкоземельных элементов (Мартыненко, 1991; Haas et al., 1995) и влияет на W-образную зависимость “свойство–атомный номер”. Однако на основании наших данных, мы можем судить только о влиянии солевых расплавов на характер распределения REE. Ограниченные данные по составу флюидов в изучаемой системе не позволяют пока рассматривать его влияние на характер спектров разделения REE, Y и Sc.
ВЫВОДЫ
Показано, что в модельной гранитной системе с предельными содержаниями фтора REE, Y и Sc распределяются преимущественно в алюмофторидную фазу при 800°С, 1 и 2 кбар и содержаниях воды в системе от 2 до 13 мас. %.
Впервые показано, что распределение REE, Y, Sc и Li между сосуществующими алюмофторидным (солевым) и алюмосиликатным расплавами зависит от давления. Коэффициенты разделения REE, Y и Sc между этими расплавами уменьшаются в 3–7 раз при увеличение давления от 1 до 2 кбар.
Коэффициенты разделения REE монотонно снижаются от легких к тяжелым как при 1, так и при 2 кбар за исключением KdGd, образующего максимум по отношению к соседними элементами.
Величина KdY близка к значениям для легких и средних REE, а KdSc ниже, чем для всех REE. Эти соотношения элементов четко отражают относительно большее сродство Y к солевому, а Sc к силикатному расплаву.
Литий играет ключевую роль в изучаемой системе, определяя фазовые отношения и оказывая влияние на характер распределение редких элементов между несмесимымим алюмосиликатным и солевым расплавами.
Флюид является фазой, наиболее обедненной всеми изучаемыми редкими элементами: Li, REE, Y и Sc.
Аналитические данные были получены в Лаборатории локальных методов исследования вещества (кафедра петрологии, Геологический факультет МГУ) с использованием сканирующего электронного микроскопа Jeol JSM-6480LV (Япония) с энерго-дисперсионным спектрометром Oxford X-MaxN и электронно-зондового микроанализатора JEOL JXA-8230, приобретенного за счет средств Программы развития Московского университета. Авторы выражают благодарность сотрудникам лаборатории Н.Н. Коротаевой, Е.В. Гусевой и В.О. Япаскурту за разработку методики и помощь в проведении анализов. Анализ редкоземельных элементов и лития проводился на установке ICP-MS2000 в лаборатории экспериментальной геохимии (кафедра геохимии геологический факультет МГУ), за что приносим благодарность сотрудникам лаборатории. Благодарим В.А. Хвостикова за проведение анализа методом лазерной абляции в Аналитическом сертификационном испытательном центре Института проблем технологии микроэлектроники и особочистых материалов РАН (АСИЦ ИПТМ РАН).
Работа выполнена в рамках проекта: грант РФФИ, номер 16-05-00859, номер ЦИТИС АААА-А16-116021010369-0.
Список литературы
Абрамов С.С. (2004) Образование высокофтористых магм путем фильтрации флюида через кислые магмы: петрологические и геохимические свидетельства магматизма. Петрология 12(1), 22-45.
Алферьева Я.О., Граменицкий Е.Н., Щекина Т.И. (2011) Экспериментальное изучение фазовых отношений в литийсодержащей богатой фтором гаплогранитной и нефелин-сиенитовой системе. Геохимия (7), 713-728.
Alferyeva Ya.O., Gramenitskii E.N., Shchekina T.I. (2011) Experimental Study of Phase Relations in a Lithium Bearing Fluorine Rich Haplogranite and Nepheline Syenite System Geochem. Int. 49(7), 676-690.
Алферьева Я.О., Щекина Т.И., Граменицкий Е.Н. (2018) Предельные содержания фтора и воды в гранитных высокоэволюционированных расплавах. Вестник Московского университета. Серия 4: Геология (3), 70-76.
Андреева И.А., Коваленко В.И., Ярмолюк В.В., Листратова Е.Н., Кононкова Н.Н. (2007) Несмесимость силикатных и солевых (Li, Na, F) расплавов в комендитах проявления Дзарта-Худук (центральная Монголия): данные изучения расплавных включений. ДАН 414(4), 528-534.
Балашов Ю.А. (1976) Геохимия редкоземельных элементов. М.: Наука, 267 с.
Бычков А.Ю., Матвеева С.С., Сущевская Т.М., Некрасов С.Ю., Игнатьев А.В. (2012) Изотопно-геохимические критерии режима фильтрации гетерогенных флюидов при формировании месторождений грейзеновой формации. Геохимия (11), 1058-1063.
Bychkov A.Yu, Matveeva S.S., Suchchevskaya T.M., Nekrasov S.Yu., Ignat’ev A.V. (2012) Isotopic-geochemical criteria of the filtration dynamics of heterogeneous fluid at greisen mineral deposits. Geochem. Int. 50 (11), 952-957.
Бычкова Я.В., Синицын М.Ю., Петренко Д.Б., Николаева И.Ю., Бугаев И.А., Бычков А.Ю. (2016) Методические особенности многоэлементного анализа горных пород методом масс-спектрометрии с индуктивно связанной плазмой. Вестник Московского университета. Серия 4: Геология (6), 56-63.
Вернадский В.И. (1954) Очерки геохимии. В книге “Избранные сочинения”. М.: АН СССР 1, 7-392.
Граменицкий Е.Н., Щекина Т.И. (2005) Поведение редкоземельных элементов и иттрия на заключительных этапах дифференциации фторсодержащих магм по экспериментальным данным. Геохимия (1), 45-59.
Gramenitkii E.N., Shchekina T.I. (2005) Behavior of rare earth elements and yttrium during the final differentiation stages of fluorine-bearing magmas. Geochem. Int. 43(1), 39-52.
Граменицкий Е.Н., Щекина Т.И., Девятова В.Н. (2005) Фазовые отношения во фторсодержащих гранитной и нефелин-сиенитовой системах и распределение элементов между фазами. М.: ГЕОС. 186 с.
Гусев А.И., Гусев A.А (2011) Тетрадный эффект фракционирования редкоземельных элементов и его использование в решении проблем петрологии гранитоидов. Успехи современного естествознания (5), 45-49.
Котельникова З.А., Котельников А.Р. (2008) NaF-содержащие флюиды: экспериментальное изучение при 500–800°C и Р = 2000 бар методом синтетических флюидных включений в кварце. Геохимия (1), 54-68.
Kotelnikova Z.A., Rotelnikov A.R. (2008) NaF-bearing fluids: experimental investigation at 500–800°C and P = = 2000 bar using synthetic fluid inclusion in quartz. Gochem. Int. 46(1), 48-61.
Котельников А.Р., Сук Н.И., Коржинская В.С., Котельникова З.А., Шаповалов Ю.Б. (2017) Исследование распределения редких и редкоземельных рудных компонентов в системе алюмосиликатный расплав – фторидный солевой расплав при T = 800–1200°С и P = 1–2 кбар (в присутствии воды). Труды Всероссийского ежегодного семинара по экспериментальной минералогии, петрологии и геохимии (ВЕСЭМПГ-2017) Москва, 18–19 апреля 2017 г., 60-63.
Комиссарова Л.Н. Неорганическая и аналитическая химия скандия. (2001) М.: Эдиториал УРСС, 512 с.
Кравчук И.Ф., Иванова Г.Ф., Варежкина Н.С., Малинин С.Д. (1995) Фракционирование редкоземельных элементов в кислых флюидно-магматических системах. Геохимия (3), 377-385.
Кравчук И.Ф., Малинин С.Д., Варежкина Н.С. (1989) Экспериментальное исследование распределения европия между силикатным расплавом и флюидом при 800°С и 1.5 кбар. Геохимия (12), 1771-1781.
Луканин О.А., Дернов-Пегарев В.Ф. (2010) Распределение редкоземельных элементов между водно-хлоридной флюидной фазой и расплавом в процессе дегазации гранитных магм, вызванной снижением. Геохимия (10), 1-21.
Lukanin O.A., Dernov-Pegarev V.F. (2010) Partitioning of rare earth elements between an aqueous chloride fluid phase and melt during the decompression-driven degassing of granite magmas. Geochem. Int. 48(10), 961-978.
Маракушев А.А., Граменицкий Е.Н., Коротаев М.Ю. (1983) Петрологическая модель эндогенного рудообразования. Геология рудных месторождений (1), 2-20.
Мартыненко Л.И. (1991) Особенности комплексообразования редкоземельных элементов. Успехи химии 60(9), 1969-1998.
Перетяжко И.С., Савина Е.А. (2010) Тетрад-эффекты в спектрах распределения редкоземельных элементов гранитоидных пород как индикатор процессов фторидно-силикатной жидкостной несмесимости в магматических системах. Петрология 18(5), 536-566.
Попова Ю.А., Матвеева С.С., Бычков А.Ю., Тарнопольская М.Е., Бычкова Я.В. (2017) Поведение лантаноидов при формировании минерализованных куполов на примере Спокойнинского месторождения (Забайкалье). Геохимия (2), 178-185.
Popova Yu.A., Matveeva S.S., Bychkov A.Yu., Ternopol’skaya M.E., Bychkova Ya.V. (2017) Behavior of Lanthanides during the Origin of Mineralized Domes: an Example of the Spokoininskoe Deposit, Transbaikalia. Geochem. Int. 55(2), 211-217.
Скублов С.Г. (2005) Геохимия редкоземельных элементов в породообразующих метаморфических минералах. СПб: Наука, 147 с.
Смирнов С.З. (2015) Флюидный режим кристаллизации водонасыщенных гранитных и пегматитовых магм: физико-химический анализ. Геология и геофизика 56(9), 1643-1663.
Соловова И.П., Гирнис Ф.А., Коваленко В.И. (2010) Жидкостная несмесимость в системе пантеллеритовый расплав-F–Cl. ДАН 433(3), 390-393.
Степанчикова С.А., Битейкина Р.П., Широносова Г.П., Колонин Г.Р. (2014) Экспериментально поведение гидроксильных комплексов в близнейтральных и щелочных растворах редкоземельных элементов и иттрия при 25°С. Геология и геофизика 55(8), 1188-1193.
Царева Г.М., Наумов В.Б., Коваленко В.И., Цепин А.И., Бабанский А.Д. (1991) Состав и параметры кристаллизации топазовых риолитов формации Спор-Маунтин (США) по данным изучения расплавных включений. Геохимия (10), 1453-1462.
Щекина Т.И., Граменицкий Е.Н., Алферьева Я.О. (2013). Лейкократовые магматические расплавы с предельными концентрациями фтора: эксперимент и природные отношения. Петрология 21(5), 499-516.
Щекина Т.И., Котельников А.Р., Русак А.А., Граменицкий Е.Н., Алферьева Я.О., Бычков А.Ю., Зиновьева Н.Г. (2016) Первые результаты по распределению редкоземельных элементов между алюмосиликатным и солевым расплавами и флюидом Тезисы докладов Всероссийского ежегодного семинара по экспериментальной петрологии и геохимии (ВЕСЭМПГ-2016, место издания ГЕОХИ РАН, Россия, Москва, тезисы, с. 139.
Ясныгина Т.А., Рассказов С.В. (2008) Редкоземельные спектры с тетрад-эффектом: проявление в палеозойских гранитоидах окинской зоны Восточного Саяна. Геохимия (8), 877-889.
Yasnygina T.A., Rasskazov S.V. (2008) Tetrad effect in rare earth element distribution patterns: Evidence from the Paleozoic granitoids of the Oka zone, Eastern Sayan. Geochem. Int. 46(8), 814-825.
Badanina E.V., Trumbull R.B., Dulski P., Wiedenbeck M., Veksler I.V., Syritso L.F. (2006) The behavior of rare earth and lithopile trace elements in rare-metal granites: a sudy of fluorite, melt in clusions and host rocks from the Khangilay complex, Transbaikalia, Russia. Can. Mineral. 44, 667-692.
Bau M. (1995) Controls on the fractionation of isivalent trace elements on magmatic and aqueous systems: evidence fromY/Ho, Zr/Hf and lanthanide tetrad effect. Contrib. Mineral. Petrol. 123, 323-333.
Berndt J., Koepke J., Holtz F. (2005) An experimental investigation of the influence of water and oxygen fugacity on differentiation of MORB at 200 MPa. J. Petrol. 46, 135-167.
Candella P.A., Piccoli P.M. (1995) Model ore-metal partitioning from melts into vapor and vapot/brine mixtures. In: Magmas, fluids, and ore deposits. Ser.: Short course series. Victoria, British Columbia. Min. Assoc. of Canada 23 (5), 101-127.
Gramenitskiy E.N., Shchekina T.I. (2002) Experimental data on geochemistry of REE and Y in the fluorine-bearing granite and nepheline-syenite magmas. Nine International Symposium on Experimental Mineralogy, Petrology and Geochemistry. J. of Conf. Abstr. Zurich: Cambridge Publ. 7(1), 40.
Irber W. (1999) The lanthanide tetrad effect and its correlation with K/Rb, Eu/Eu*, Sr/Eu, Y/Ho, and Zr/Hf of evolving peraluminous granite suites. Geochim. Cosmochim. Acta 63(3–4), 489-508.
Haas J.R., Shock E.L., Sassani D.C. (1995) Rare earth elements in hydrotermal systems: Estimates of standard partial molal thermodynamic properties of aqueous complexes of the rare earth elements at high pressures and temperatures. Geochim. Cosmochim. Acta 59(21), 4329-4350.
Holtz F., Dingwell D.B., Behrens. H. (1993) Effects of F, B2O3 and P2O5 on the solubility of water in haplogranite melts compared to natural silicate melts. Contrib. Mineral. Petrol. 113(4), 492-501.
Lottermoser B.G. Rare earth elements and hydrothermal ore formation processes (1992) Ore Geol. Rev. 7(1), 25-41.
Manning D.A.C., Hamilton D.L., Henderson C.M.B., Dempsey M.J. (1980) The probable occurrence of intersticial A1 in hydrous, F-bearing and F-free aluminosilicate melts. Contrib. Mineral Petrol. 75, 257-262.
Shchekina T.I., Gramenitskiy E.N. (1997) The genetic connection of rare-metal deposites with granites according to experimental data. European Union of Geosciencts. Strasburg-France, 23–27 March, 1997. Abstr. Supplement. № 1. Terra Nova 9, 530.
Takahashi Y., Yoshida H., Sato N., Hama K., Yusa Y., Shimizu H. (2002) W and M_type tetrad effect in REE patterns for water_rock systems in the Tono uranium deposit, central Japan. Chem. Geol. 184, 311-335.
Veksler I.V., Dorfman A.M., Kamenetcky M., Dulskii P., Dingwell D.B. (2005) Partitioning of lanthanides and Y between immiscible silicate and fluoride melts, fluorite and cryolite and the origin of the lanthanide tetrad effect in igneous rocks. Geochim. Cosmochim. Acta 69(11), 2847-2860.
Veksler I.V., Dorfman A.M.C, Dulski P., Kamenetsky V.S., Danyushevsky L.V., Jeffries T., Dingwell D.B. (2012) Partitioning of elements between silicate melt and immiscible fluoride, chloride, carbonate, phosphate and sulfate melts, with implications to the origin of natrocarbonatite. Geochim. Cosmochim. Acta. 79. 20-40.
Zheng-Hang Lv, Hui Zhang, YongTang (2018) Lanthanide tetrads with implications for liquid immiscibility in an evolving magmatic-hydrothermal system: Evidence from rare earth elements in zircon from the No. 112 pegmatite, Kelumute, Chinese Altai. J. Asian Earth Sciences. 164. 9-22.
Дополнительные материалы отсутствуют.