Геохимия, 2020, T. 65, № 7, стр. 693-710
Биогеохимическая миграция элементов в системе “атмосферные осадки–кроновые воды–почвенные воды–озеро” в фоновом регионе (Валдайский национальный парк)
Н. А. Гашкина a, *, Т. И. Моисеенко a, М. И. Дину a, Ю. Г. Таций a, Д. Ю. Баранов a
a Институт геохимии и аналитической химии им. В.И. Вернадского РАН
119991 Москва, ул. Косыгина, 19, Россия
* E-mail: ngashkina@gmail.com
Поступила в редакцию 15.11.2018
После доработки 29.07.2019
Принята к публикации 11.09.2019
Аннотация
Рассмотрено распределение элементов в системе “атмосферные осадки–кроновые воды–почвенные воды–озеро” водосбора оз. Гусиного на территории Валдайского национального парка. Определены особенности химического состава атмосферных осадков, кроновых, почвенных и озерных вод, а также почвы. В генетических горизонтах почвы по месяцам рассчитаны потоки элементов, обусловленные биогеохимическим выносом или поглощением, и подведен их бюджет в исследуемом профиле почв за летне-осенний период. Дана оценка обогащения почв элементами и интенсивности их водной миграции в почвенных и озерных водах.
Рассеивание и миграция элементов в окружающей среде происходит в результате как естественных, так и антропогенно-обусловленных процессов. К последним относятся: промышленное производство, добыча полезных ископаемых, сжигание различного вида топлив. А.Е. Ферсман (1934) отмечал, что природные геохимические законы распределения и концентрирования элементов сравнимы с законами технохимии, т.е. химическими преобразованиями, вносимыми промышленностью и хозяйственной деятельностью. Такой показатель как технофильность элементов, отношение объемов использования к содержанию в литосфере, неукоснительно растет для многих элементов (Геохимия ландшафтов…, 2012). Проблема оценок техногенного рассеяния элементов в силу своей актуальности привлекала и привлекает большое количество исследователей, такие оценки выполнены на как глобальном, так и региональном уровнях (Глазовский, 1982; Мур, Рамамурти, 1987; Перельман, 1982; Bryan, 1976). Ю.Е. Сает и соавторы (1990) приводят интересные данные по степени концентрирования рассеянных элементов в компонентах окружающей среды на промышленных, сельскохозяйственных и урбанизированных территориях, т.е. на локальном уровне. Не менее важными являются оценки рассеивания и миграционных потоков элементов на больших территориях, не подверженных локальному загрязнению. Однако, летучесть соединений Hg, Se, Sn, Sb, Bi, As, Pb и других, в том числе алкилированных форм, может составлять проблему повсеместного распространения загрязнения этими элементами (Handbook on the Toxicology of Metals, 2007).
В процессе техногенного перераспределения элементов обогащается не только верхняя часть литосферы, но и гидросфера. Водные объекты являются в конечном итоге коллекторами антропогенного рассеивания элементов в окружающей среде. За счет человеческой деятельности в окружающую среду и, в частности, в пресноводные системы в глобальном масштабе поступают большие объемы элементов, включая как эссенциальных, так и неэссенциальных – Fe, Zn, Cd, Cr, Mn, Mo, Sb, Sn, Ni, Cu и Pb (Moiseenko et al., 2019). Поверхность Земли (почвы и растительность) являются биогеохимическим барьером на пути миграции элементов от источника выбросов в атмосферу и осаждения на поверхности суши – до водного объекта. В лесных биогеоценозах древесные растения являются мощным средообразующим фактором, перераспределяя атмосферное поступление элементов, изменяя свойства почв, их кислотность и режим элементов (Лукина и др., 2008). В условиях природной по геологическим условиям чувствительности территории к закислению почв и вод может усиливаться миграция и обогащение вод элементами (Моисеенко, Гашкина, 2011).
Исследования целостной системы от выпадений элементов из атмосферы и миграции на водосборе до поступления в озеро крайне редки. Для оценки эволюции биосферных процессов и рассеивания элементов необходимо понимание их круговорота на фоновых участках, отражающих глобальные процессы поведения элементов в природных условиях.
Целью работы было представить оригинальные результаты исследований миграционных потоков элементов в системе “атмосферные осадки–кроновые воды–почвенные воды–озеро”, дать характеристику процессам обогащения элементами почв и вод в фоновом регионе.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЙ
Исследования велись на территории Валдайского национального парка, не подверженного каким-либо прямым загрязнениям. В основу исследований был заложен методологический подход, используемый в международной практике (ICP Forest, 2011). Для наблюдения за химическим составом почвенных вод, внутрипрофильной миграции элементов, а также трансформации атмосферных осадков, прошедших сквозь полог древостоя, были заложены лизиметры в подкроновом пространстве елей на водосборе оз. Гусиного, которое можно отнести к чувствительным к кислотным выпадениям по геологическим условиям водосбора (отсутствие известняков в тульском горизонте каменноугольных отложений, четвертичные отложения – флювиогляциальные отложения, представленные песками с гравием и галькой). Озеро Гусиное (средняя глубина – 2.5 м), площадью водного зеркала 0.14 км2, водосбора – 0.99 км2, расположенное в зоне южной тайги умеренного климата с избыточным увлажнением. Рельеф водосбора озера холмисто-моренный, значительная часть водосбора заболочена, в древесном ярусе преобладает ель.
Согласно иерархии мировой реферативной базы почвенных ресурсов WRB (2015) в районе исследования находятся подзолистые почвы (PZ). Ниже приводиться морфологическое описание разреза:
0–10 см – Folic horizon. Органический горизонт, представлен лесной подстилкой в виде грубого гумуса и малой мощности мягкого гумуса.
10–20 см – Albic horizon. Элювиальный горизонт, сложенный светло-коричневым песком с сероватым оттенком.
20–30 см – Spodic horizon. Иллювиальный горизонт, сложенный коричневым песком.
30–40 см – почвообразующие породы, сложенные светло-бурым и коричневым флювиогляциальным песком средней крупности.
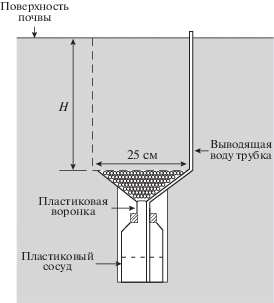
В начале июня были установлены гравитационные с ненарушенным монолитом лизиметры конструкции Джона Дерома (Лукина, Никонов, 1996). С помощью специально изготовленного бура (диаметром 25 см) извлекали почвенный монолит необходимой глубины, а буром меньшего диаметра извлекали монолит для приемной пластиковой бутыли объемом 2 литра. Схема лизиметра представлена на рис. 1. Воронка заполнялась дренажом – стеклянные шарики диаметром 4–6 см. После установки лизиметра верхний почвенный монолит аккуратно возвращали на место. Была заложено 2 лизиметра под элювиальным и иллювиальным горизонтами. Откачку лизиметрических вод производили из выходящей на поверхность нейлоновой трубки с помощью вакуумного насоса.
Одновременно на открытом участке местности (осадкомерный полигон Валдайского филиала ГГИ) и на водосборе оз. Гусиного под кроной деревьев (кроновые воды) были установлены осадкоприемники. Наблюдения за химическим составом атмосферных осадков, кроновых, почвенных и озерных вод велось ежемесячно с 09.06.2015 по 19.10.2015. Также измеряли объем просочившихся почвенных вод с площади 0.049 м2. Данные по количеству осадков были предоставлены Валдайским филиалом ГГИ.
Анализы гидрохимических параметров проводились в течение 48 часов после отбора проб и включали:
рН, электропроводность – потенциометрическое определение;
перманганатная окисляемость – титриметрическое определение;
щелочность – потенциометрическое титрование по методу Грана;
цветность – спектрофотометрическое определение;
нитраты и нитриты – спектрофотометрическое определение с реактивом Грисса;
аммоний – спектрофотометрическое определение с реактивом Несслера;
фосфаты – спектрофотометрическое определение фосфорно-молибденового комплекса в кислой среде;
анионно-катионный макро-состав (ионы кальция, магния, калия, натрия, аммония; сульфаты, хлориды, фториды, нитраты, нитриты, орто-/полифосфаты) – ионная хроматография;
ионы меди, свинца, кадмия, никеля, кобальта, железа – инверсионная вольтамперометрия;
ионы щелочноземельных металлов, алюминия, меди, никеля, кадмия, кобальта – атомно-абсорбционным метод.
Широкий спектр элементов в микро- и нано- концентрациях в атмосферных осадках, кроновых, почвенных, озерной вод, а также в образцах почв после соответствующей пробоподготовки определяли методами атомно-эмиссионной спектрометрии с индуктивно связанной плазмой (iCAP-6500, Thermo Scientific, США) и масс-спектрометрии с индуктивно-связанной плазмой (Х-7, Thermo Scientific, США) в Аналитическом центре ФГБУН Института проблем технологии микроэлектроники и особо чистых материалов РАН.
Результаты параллельных определений концентраций элементов разными методами были сопоставлены и служили критерием достоверности измерений конкретных параметров. Контроль качества полученного массива данных был основан на электронейтральности водных проб. Общее количество отрицательно и положительно заряженных частиц, выраженных в мили- или микроэквивалентах на литр было равным.
В рассмотрение не вошли элементы, концентрации которых были ниже предела обнаружения во всех исследуемых водах (Se, Sc, Ga, Ge, Nb, Ru, Rh, Pd, In, Te) и с единичными значениями (Cr, Ag, Br), из лантаноидов рассмотрены только лантан и церий.
Минералогический анализ минеральных почвенных горизонтов выполнен на геологическом факультете Московского университета им. М.В. Ломоносова. Рентгенодифракционный анализ порошковых препаратов проводили на рентгеновском дифрактометре ULTIMA-IV фирмы Rigaku (Япония). Для ускорения съемки и повышения качества экспериментальных данных использовали полупроводниковый детектор – DTex/Ultra. Количественный анализ осуществляли методом полнопрофильной обработки рентгеновских картин от неориентированных препаратов по методу Ритвельда (Bish, Post, 1993) в программном продукте BGMN. В основе метода лежит сопоставление расчетных и экспериментальных значений интенсивностей дифракционных отражений, которые измеряются в определенных точках дифрактограммы, полученной при пошаговом сканировании. В ходе анализа уточняются параметры элементарной ячеек всех ваз, содержащихся в смеси и определенных на предварительном этапе анализе, и координаты атомов каждой фазы. В результате сопоставления экспериментального и уточненного спектров рассчитывается весовое содержание фаз.
Концентраций элементов в почве также нормировали как относительно таковых в Земной коре (Виноградов, 1962), так и в песчаных осадочных породах (Turekian, Wedepohl, 1961). Коэффициенты водной миграции элементов в почвенных и озерных водах рассчитывались по А.И. Перельману (Перельман, 1982) относительно содержания элементов в исследуемых почвенных горизонтах почвы.
Потоки элементов (поступление с атмосферными осадками и кроновыми водами, результирующие поглощения и возврата, сорбции и десорбции и других разнонаправленных процессов в исследуемом почвенном профиле и их вынос за его пределы) оценивали на основе баланса массы элементов. Для слоя 0–20 см приходная составляющая – масса элемента в кроновых водах, расходная – масса элемента в лизиметрических водах, прошедших слой почвы 0–20 см, для слоя 20–30 см – это соответственно разница масс элементов в лизиметрических водах слоя почвы 0–20 и 0–30 см. Поступление элементов в озеро с почвенными водами ориентировочно оценивалось на основе водного баланса: разница объемов кроновых вод и лизиметрических вод слоя почвы 0–20 и разница объемов лизиметрических вод слоя почвы 0–20 и 0–30 см. Оценка поступления элементов в озеро с почвенными водами может быть завышена, т. к. если испарение в данном случае учитывается, то транспирация – нет. В расчетах запасов элементов в озере использовали объем воды в озере, оцениваемый по средней его глубине.
Органический анион (Аn–) рассчитан на основе эмпирических зависимостей между Аn– и содержанием общего органического углерода (Cорг), оцениваемого по перманганатной окисляемости (ПО) (Henriksen et al., 1992, 1998):
(1)
${{A}^{{n - }}} = {{{\text{C}}}_{{{\text{орг}}}}}\left( {{\text{4}}{\text{.7}} - {\text{6}}{\text{.87exp}}\left( { - 0.332{\text{TOC}}} \right)} \right),$Для расчета доли сильных и слабых органических кислот в системе были использованыы работы Evans, Montheith (2008). Согласно данным этих авторов, исходя из электронейтральности системы, доля сильных органических кислот может быть вычислена как разность между макрокатионами (включая ион аммония, ионы алюминия и железа) и анионами сильных кислот включая общую щелочность. В расчете учитываются лабильные (несвязанные в комплексы с органическими лигандами) ионы алюминия и железа (полученные с помощью программы ACIDFORMMET) (Дину, Моисеенко, 2015):
(3)
$\begin{gathered} {\text{C}}{{{\text{a}}}^{{{\text{2}} + }}} + {\text{M}}{{{\text{g}}}^{{{\text{2}} + }}} + {\text{N}}{{{\text{a}}}^{ + }} + {{{\text{K}}}^{ + }} + {\text{NH}}_{{\text{4}}}^{ + } + \\ + \,\,{\text{Al}}_{{{\text{inorg}}}}^{{{\text{3}} + }} + {\text{Fe}}_{{{\text{inorg}}}}^{{{\text{3}} + }} = {\text{C}}{{{\text{l}}}^{ - }} + {\text{SO}}_{{\text{4}}}^{{{\text{2}} - }} + \\ + \,\,{\text{NO}}_{{\text{3}}}^{ - } + {\text{Org}}{{{\text{A}}}_{{{\text{strong}}}}} + {\text{Alk}}, \\ \end{gathered} $(4)
$\begin{gathered} {\text{Org}}{{{\text{A}}}_{{{\text{strong}}}}} = \left( {{\text{C}}{{{\text{a}}}^{{{\text{2}} + }}} + {\text{M}}{{{\text{g}}}^{{{\text{2}} + }}} + {\text{N}}{{{\text{a}}}^{ + }} + {{{\text{K}}}^{ + }} + } \right. \\ \left. {{\text{ + }}\,\,{\text{NH}}_{{\text{4}}}^{ + } + {\text{ Al}}_{{{\text{inorg}}}}^{{{\text{3}} + }} + {\text{Fe}}_{{{\text{inorg}}}}^{{{\text{3}} + }}} \right) - \\ --\,\,\left( {{\text{C}}{{{\text{l}}}^{ - }} + {\text{SO}}_{{\text{4}}}^{{{\text{2}} - }} + {\text{NO}}_{{\text{3}}}^{ - } + {\text{Alk}}} \right). \\ \end{gathered} $В приведенных формулах несвязанные с органическим веществом ионы алюминия и железа были рассчитаны с помощью условных констант устойчивости комплексов, полученных экспериментально. Согласно Evans, Montheith (2008) доля слабых органических кислот определяется методом Гран-титрования и входит в величину общей щелочности, поэтому ее численное значение вычисляют по разности между общим органическим анионом и долей сильных кислот.
Кислотонейтрализующая способность вод рассчитана как разница между суммой доминирующих катионов и суммой анионов минеральных кислот (Van Breemen et al., 1984):
(5)
$\begin{gathered} {\text{ANC}} = \left( {{\text{C}}{{{\text{a}}}^{{{\text{2}} + }}} + {\text{M}}{{{\text{g}}}^{{{\text{2}} + }}} + {\text{N}}{{{\text{a}}}^{ + }} + {{{\text{K}}}^{ + }} + {\text{NH}}_{{\text{4}}}^{ + }} \right)-- \\ - \,\,\left( {{\text{SO}}_{{\text{4}}}^{{{\text{2}}--}} + {\text{C}}{{{\text{l}}}^{ - }} + {\text{NO}}_{{\text{3}}}^{--}} \right). \\ \end{gathered} $РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ И ОБСУЖДЕНИЕ
Химический состав атмосферных осадков, кроновых, почвенных и озерных вод
Результаты химического анализа атмосферных осадков (АО), кроновых вод (КВ), почвенных и озерных вод в летне-осенний период 2015 г. приведены в табл. 1.
Таблица 1.
Средние значения и пределы варьирования химического состава озерных вод, атмосферных осадков, кроновых вод, почвенных вод в слое 0–20 и 0–30 см на водосборе озера Гусиного в летне-осенний период 2015 г.
| Параметры | Атмосферные осадки | Кроновые воды | Почвенные воды | Озерные воды | |
|---|---|---|---|---|---|
| 0–20 см | 0–30 см | ||||
| pH | 6.41 (5.44–6.86) | 5.71 (5.21–6.34) | 5.11 (4.22–6.97) | 6.00 (5.72–6.29) | 6.03 (5.75–6.30) |
| χ, мкСм/см | 63.4 (7.50–232) | 50.7 (18.6–159) | 60.2 (43.1–102) | 90.3 (65.0–108) | 12.9 (11.2–15.6) |
| Ca2+, мг/л | 1.60 (0.73–3.16) | 2.14 (1.03–6.06) | 2.41 (1.28–3.66) | 3.44 (3.16–3.86) | 1.67 (1.50–2.10) |
| Mg2+, мг/л | 0.13 (0.06–0.33) | 0.45 (0.22–1.12) | 0.40 (0.30–0.51) | 0.62 (0.56–0.74) | 0.26 (0.25–0.27) |
| Na+, мг/л | 1.47 (0.08–4.80) | 1.99 (0.28–8.47) | 1.94 (0.43–3.73) | 6.15 (4.84–8.16) | 0.35 (0.30–0.41) |
| K+, мг/л | 0.31 (0.08–1.05) | 5.75 (1.35–21.1) | 5.37 (1.85–18.7) | 1.46 (1.34–1.70) | 0.49 (0.20–1.69) |
| НС${\text{O}}_{3}^{ - },$ мг/л | 2.56 (0.63–4.50) | 3.13 (0.60–4.50) | 5.02 (1.11–8.40) | 2.51 (1.20–3.92) | 4.15 (1.81–6.00) |
| S${\text{O}}_{4}^{{2 - }},$ мг/л | 4.29 (0.54–15.5) | 5.57 (1.85–18.5) | 5.78 (2.86–11.4) | 12.0 (8.20–15.0) | 3.23 (0.25–6.50) |
| Cl–,мг/л | 1.34 (0.10–4.50) | 2.12 (0.25–7.65) | 3.07 (1.20–7.89) | 1.72 (1.10–2.25) | 1.33 (0.25–2.69) |
| Цв., °Cr-Co | 20.3 (3.50–65.0) | 96.6 (83.0–140) | 244 (115–395) | 123 (95.4–153) | 68.3 (55.8–92.0) |
| Сорг, мгС/л | 7.96 (3.38–20.1) | 49.3 (13.8–75.2) | 79.1 (28.9–151) | 70.5 (35.6–93.7) | 36.9 (23.4–54.6) |
| P${\text{O}}_{4}^{{3 - }},$ мкгP/л | 6.35 (0.05–23.3) | 68.6 (0.50–130) | 293 (3.80–1260) | 117 (103–141) | 2.76 (0.02–10.0) |
| N${\text{O}}_{2}^{ - },$ мкгN/л | 19.8 (0–96.5) | 39.5 (0.61–122) | 292 (1.83–1080) | 60.1 (6.70–152) | 8.62 (3.04–15.2) |
| N${\text{O}}_{3}^{ - },$ мкгN/л | 76.9 (0.23–203) | 124 (0–271) | 495 (90.3–1547) | 670 (497–1016) | 242 (4.52–1095) |
| N${\text{H}}_{4}^{ + }$, мкгN/л | 196 (15.6–684) | 228 (11.7–661) | 311 (7.78–786) | 28.5 (7.78–70.0) | 77.8 (9.33–202) |
| Si, мг/л | 0.06 (0.02–0.13) | 0.21 (0.08–0.48) | 1.87 (1.09–2.47) | 3.00 (2.36–3.95) | 0.15 (0.110–0.20) |
| Al, мкг/л | 20.1 (5.92–68.6) | 151 (29.9–544) | 1515 (1033–1880) | 924 (857–996) | 40.5 (28.8–61.5) |
| Fe, мкг/л | 11.1 (<8–25.5) | 42.2 (16.7–99.2) | 397 (227–451) | 159 (141–179) | 107 (96.8–124) |
| Mn, мкг/л | 4.67 (2.96–7.65) | 195 (94.5–329) | 386 (298–529) | 221 (138–281) | 22.3 (13.6–30.1) |
| Sr, мкг/л | 10.5 (2.51–19.5) | 5.45 (2.05–17.1) | 11.6 (6.45–14.9) | 16.5 (15.3–18.5) | 3.01 (2.17–3.55) |
| Ba, мкг/л | 4.77 (2.12–6.62) | 14.0 (5.23–42.7) | 48.9 (4.54–68.3) | 43.5 (37.2–48.6) | 6.30 (4.35–11.2) |
| B, мкг/л | 2.47 (<0.5–4.65) | 13.8 (6.40–27.5) | 14.0 (7.02–21.4) | 16.9 (15.0–17.9) | 2.44 (2.01–2.58) |
| Zn, мкг/л | 258 (13.0–497) | 1875 (1082–3224) | 1383 (540–2063) | 2472 (1059–2063) | 6.33 (2.43–20.4) |
| Cu, мкг/л | 45.1 (2.80–24.4) | 376 (227–548) | 353 (210–435) | 244 (126–362) | 0.65 (<0.6–3.59) |
| Ni, мкг/л | 10.7 (0.76–28.6) | 1.63 (0.48–5.33) | 4.55 (2.62–10.3) | 3.45 (3.06–3.71) | 1.76 (<0.3–10.6) |
| Co, мкг/л | 1.56 (0.42–4.29) | 0.21 (<0.07–0.61) | 1.21 (0.74–1.46) | 0.33 (0.30–0.37) | <0.07 (<0.07–0.17) |
| Pb, мкг/л | 1.21 (0.35–4.00) | 1.06 (0.46–2.88) | 3.16 (1.44–7.44) | 2.30 (1.38–3.17) | 0.52 (0.20–1.42) |
| Cd, мкг/л | 0.070 (<0.007–0.110) | 0.090 (0.030–0.230) | 0.200 (0.160–0.230) | 0.197 (0.150–0.217) | 0.032 (<0.007–0.139) |
| As, мкг/л | 0.22 (<0.07–0.75) | 0.19 (<0.07–0.70) | 0.56 (0.35–0.84) | 0.53 (0.45–0.58) | 0.27 (0.21–0.29) |
| V, мкг/л | 0.08 (<0.07–0.16) | 0.26 (<0.07–0.71) | 0.55 (0.14–0.89) | 0.45 (0.41–0.47) | 0.10 (<0.07–0.26) |
| Mo, мкг/л | 0.137 (0.043–0.259) | 0.147 (0.066–0.327) | 0.087 (0.042–0.167) | 0.094 (0.066–0.116) | 0.096 (<0.011–0.352) |
| Hg, мкг/л | <0.01 | 0.01 (<0.01–0.03) | 0.03 (<0.01–0.06) | 0.02 (<0.01–0.04) | 0.01 (<0.01–0.03) |
| Be, мкг/л | <0.004 (<0.004–0.007) | 0.011 (<0.004–0.037) | 0.095 (0.049–0.115) | 0.069 (0.056–0.077) | 0.004 (<0.004–0.009) |
| Sn, мкг/л | 0.094 (0.018–0.234) | 0.178 (0.051–0.310) | 0.152 (0.054–0.486) | 0.047 (0.035–0.060) | 0.120 (0.030–0.508) |
| Sb, мкг/л | 0.174 (0.068–0.413) | 0.227 (0.090–0.688) | 0.179 (0.099–0.351) | 0.189 (0.144–0.267) | 0.060 (0.050–0.090) |
| Ti, мкг/л | <0.70 (<0.70–0.77) | 1.02 (<0.70–3.21) | 4.49 (3.19–5.42) | 4.00 (3.50–4.30) | <0.70 (<0.70–0.70) |
| Li, мкг/л | 0.194 (0.041–0.387) | 0.373 (0.118–0.688) | 1.10 (0.102–2.50) | 1.63 (1.33–1.97) | 0.210 (0.146–0.280) |
| Rb, мкг/л | 0.611 (0.170–1.43) | 19.1 (8.11–41.3) | 17.1 (3.67–56.1) | 8.51 (6.46–9.24) | 1.31 (1.14–1.51) |
| Y, мкг/л | 0.024 (0.008–0.051) | 0.066 (0.020–0.193) | 0.813 (0.510–1.04) | 0.562 (0.556–0.567) | 0.013 (0.010–0.020) |
| Zr, мкг/л | 0.013 (<0.005–0.055) | 0.066 (0.024–0.195) | 0.321 (0.218–0.387) | 0.324 (0.264–0.400) | 0.019 (0.015–0.026) |
| Cs, мкг/л | 0.026 (0.006–0.049) | 0.064 (0.018–0.130) | 0.094 (0.015–0.284) | 0.054 (0.049–0.059) | 0.014 (0.012–0.016) |
| Bi, мкг/л | 0.002 (<0.001–0.005) | 0.013 (0.004–0.033) | 0.012 (0.007–0.024) | 0.005 (0.004–0.006) | 0.005 (<0.001–0.011) |
| W, мкг/л | 0.014 (<0.005–0.028) | 0.016 (<0.005–0.043) | 0.033 (0.015–0.072) | 0.024 (0.019–0.030) | <0.005 (<0.005–0.014) |
| Tl, мкг/л | 0.031 (0.006–0.077) | 0.070 (0.026–0.202) | 0.092 (0.029–0.264) | 0.052 (0.050–0.056) | 0.008 (0.005–0.009) |
| La, мкг/л | 0.040 (0.012–0.071) | 0.094 (0.027–0.303) | 1.35 (0.851–1.72) | 0.621 (0.580–0.691) | 0.020 (0.008–0.040) |
| Ce, мкг/л | 0.102 (0.027–0.216) | 0.203 (0.049–0.654) | 2.97 (1.73–3.20) | 1.33 (1.25–1.41) | 0.041 (0.022–0.078) |
| Th, мкг/л | 0.006 (<0.002–0.027) | 0.023 (0.004–0.078) | 0.173 (0.154–0.206) | 0.122 (0.112–0.130) | 0.004 (0.003–0.005) |
| U, мкг/л | 0.005 (0.001–0.011) | 0.011 (0.006–0.029) | 0.022 (0.015–0.032) | 0.028 (0.026–0.033) | 0.002 (0.001–0.003) |
Количество АО было следующее: 9 июня–7 июля – 25.5, 7 июля–4 августа – 117, 4 августа–30 августа – 20.8, 30 августа–28 сентября – 77.2, 28 сентября–19 октября – 36.0 мм. Максимальные концентрации основных ионов минерализации и большинства микроэлементов наблюдались в более сухие месяцы года (июнь, август, октябрь), тогда как биогенных элементов – смещались на август и сентябрь. Минимальные концентрации наблюдались в дождливые месяцы (июль, август).
Сравнение химического состава КВ с АО показывает значительное их обогащение основными ионами, биогенными элементами и микроэлементами (для таких биофильных элементов, как Zn, Cu, Mn, Rb – на порядок) при более низких значениях рН кроновых вод. Исключения составляют более высокие концентрации таких элементов, как Ni, Co и Pb, в АО на открытой местности. Причем, концентрации основных ионов минерализации, углерода, форм азота, Al, Fe в атмосферных выпадениях, а также концентрации ионов водорода могут увеличиваться на порядок: в кроновых водах по сравнению с осадками в межкроновом пространстве и в стволовых водах по сравнению с кроновыми (Лукина и др., 2002).
Ретроспективный анализ современного состояния атмосферных выпадений (табл. 1) показал, что средние значения главных ионов и форм азота в АО не сильно изменились с 60-х гг. прошлого века. В работе (Никоноров, 2001) приводятся следующие средние значения их концентраций по пункту “Валдай” за 1958–1961 гг.: кальция – 0.4 мг/л, магния – 0.2 мг/л, натрия – 1.1 мг/л, калия – 0.4 мг/л, гидрокарбонатов – 5.0 мг/л, сульфатов – 3.6 мг/л, хлоридов – 0.8 мг/л, нитратов – 135 мкгN/л, аммонийного азота – 311 мкгN/л.
Микроэлементный состав ОА и КВ также исследовался на лесном водосборе Таежного лога (Валдай) в 1983–1984 гг. (Алексеенко, 1989). Для теплого периода приводятся следующие концентрации элементов в АО и КВ соответственно: Cr – 0.8 и 1.2 мкг/л, Zn – 8.1 и 330 мкг/л, Cu – 6.2 и 17 мкг/л, Fe – 82 и 140 мкг/л, Mn – 91 и 800 мкг/л, Ni – 2.0 и 3.0 мкг/л, Pb – 7.6 и 19.2 мкг/л. Таким образом, к 2015 г. произошло снижение концентраций Cr (до значений меньше порога обнаружения), Pb, Fe и Mn, но значительное увеличение Zn и Cu как в атмосферных осадках, так и в кроновых водах.
Почвенные воды гумусового и подзолистого горизонтов обогащались практически всеми элементами и превышали их концентрации в кроновых водах, за исключением Na, Mg, К, Zn, Cu, Мо, а также Rb, Sn, Sb. Почвенные воды иллювиального горизонта отличались меньшими концентрациями элементов от таковых гумусового и подзолистого горизонтов, за исключением в основном сульфатов, Na и Са (табл. 1). В 1980–1983 гг. исследование химического состава почвенных вод дерново-подзолистых суглинистых почв под ельником велось также в Таежном логе (Шитикова, 1986). Приводятся следующие средние концентрации Са – 11.9 и 7.0 мг/л, Mg – 3.9 и 1.7 мг/л, Na – 3.9 и 3.1 мг/л, К – 16.7 и 38.0 мг/л, HCO3 – 3.9 и 3.1 мг/л, SO4 – 37.6 и 3.1 мг/л Cl – 5.4 и 5.8 мг/л, РО4 – 292 и 636 мкгР/л, NО2 – 36.2 и 54.7 мкгN/л, NО3 – 3661 и 2395 мкгN/л, NH4 – 1132 и 419 мкгN/л, Si – 3.49 и 3.60 мг/л, Fe – 243 и 190 мг/л при рН 5.5 и 6.2 соответственно в почвенных водах выше иллювиального и в самом иллювиальном горизонтах. Таким образом, по сравнению с суглинистыми почвами в почвенных водах песчаной почвы за исключением в некоторой степени Na, Si и Fe содержание остальных сравниваемых показателей ниже, особенно для К и N.
В водах оз. Гусиного приведенные в табл. 1 максимальные концентрации большинства элементов соответствуют началу периода наблюдений после половодья. Средние концентрации Са, Mg, K, HCO3, Cорг, NO3, Si, Al, Fe, Mn, Ba, V, Sn, Li, Rb в воде озера, а также цветность вод выше, чем в АО, но ниже, чем в почвенных водах. Следует отметить, что, несмотря на высокое поступление с АО и КВ Zn и Cu, их утилизация в биологическом круговороте значительна и концентрации их в воде озера были невелики, а для меди – меньше предела обнаружения.
Минералогический и химический состав почвы
Результаты минералогического анализа минеральных горизонтов исследуемой почвы следующие: содержание кварца – 70.9, 66.5, 75.6%, альбита – 13.9, 12.5, 11.1%, микроклина – 7.8, 6.6, 9.2%, кальцита – 0.6, 4.2, 0.2%, иллита – 4.8, 6.6, 3.9%, каолинита – 1.1, 1.8, 0%, смектита – 0, 0, 0%, хлорита – 1.0, 1.8, 0% соответственно в слоях почвенных горизонтов 10–20, 20–30, 30–40 см. Процессы оподзоливания отразились на распределении минералов в генетических горизонтах почв, которое имеет элювиально-иллювиальный характер: с большим содержанием кварца и альбита и меньшим содержанием кальцита и каолинита в элювиальном горизонте. В бедных элементами питания песчаных почвах примечательно, что в иллювиальном горизонте более низкое содержание алюмосиликата калия – микроклина при увеличении содержания иллита, а также хлорита. Иллитизацию и хлоритизацию почв можно рассматривать как результат современного почвообразования (Рябова, Кузнецов, 1998).
В профильном распределении содержания большинства элементов закономерно проявляется элювиально-иллювиальный характер (особенно для Са и Mg). Исключение составляют Fe, Mn, Rb, Pb, Mo, As, V, Sn, Sb, Cs, Bi, W и Tl (табл. 2), которые, по-видимому, закрепляются в органогенном горизонте почв, их биогеохимическая миграция определяется как особенностями биогеоценоза, так и, возможно, усилена процессами современного техногенеза. Нормированные величины концентраций элементов в почвах водосбора оз. Гусиного по сравнению с Земной корой показывают обогащение почв только Bi и Cd. В то же время по сравнению с песчаными осадочными породами – обогащение происходит Mn, K, Co, Ba, V, Sb и Cs более чем в 10 раз, а Pb, Ni, Sr и Th – более чем в 2 раза. В органогенном и подзолистом горизонтах происходит концентрирование Mo и As, в иллювиальном горизонте – Zn и U (табл. 2). При росте технофильности Fe, Ti, Sr, Li, Al, Cr, Ni, Co, Nb, Tr, Ga, B, I на протяжении полувека, в последние 20 лет увеличилась технофильность Y, V, In, Pd, Pt, Re, Mo, Bi, Sb, Cu, Zn (Геохимия ландшафтов…, 2012).
Таблица 2.
Содержание элементов в горизонтах почвы и их нормированные величины, а также коэффициенты водной миграции элементов в почвенных водах и в озере Гусином
| Элемент | Содержание в почве | Нормированные величины концентраций элементов в почве | Коэффициенты водной миграции | ||||
|---|---|---|---|---|---|---|---|
| 0–20 см | 20–30 см | Почвенные воды | Озеро | ||||
| мкг/г | 0–20 см | 20–30 см | 0–20 см | 0–30 см | |||
| Ca | 2442 | 3101 | 0.06 (0.06) | 0.08 (0.08) | 25.6 | 22.4 | 75.9 |
| Mg | 1329 | 2076 | 0.07 (0.19) | 0.11 (0.30) | 7.89 | 6.84 | 20.1 |
| Na | 4453 | 6053 | 0.22 (1.67) | 0.24 (1.86) | 9.13 | 18.6 | 7.33 |
| K | 13 278 | 13 627 | 0.53 (12.5) | 0.55 (12.8) | 10.5 | 1.88 | 4.45 |
| Al | 27 698 | 31 025 | 0.35 (1.13) | 0.39 (1.26) | 1.39 | 0.54 | 0.17 |
| Fe | 12 260 | 12 132 | 0.27 (1.28) | 0.27 (1.27) | 0.82 | 0.23 | 1.06 |
| Mn | 659 | 538 | 0.67 (x00) | 0.55 (x00) | 14.9 | 6.04 | 4.26 |
| Sr | 80.3 | 90.5 | 0.24 (4.01) | 0.27 (4.53) | 3.76 | 3.42 | 4.36 |
| Ba | 376 | 446 | 0.58 (x0) | 0.69 (x0) | 3.38 | 1.89 | 1.91 |
| Zn | 28.4 | 37.0 | 0.34 (1.78) | 0.45 (2.32) | 1264 | 1367 | 24.5 |
| Cu | 4.36 | 6.31 | 0.09 (0.x) | 0.13 (0.x) | 2104 | 841 | 15.7 |
| Ni | 5.58 | 9.74 | 0.10 (2.79) | 0.17 (4.87) | 21.2 | 8.56 | 30.6 |
| Co | 3.31 | 4.23 | 0.18 (11.0) | 0.24 (14.1) | 9.51 | 1.60 | 0.95 |
| Pb | 16.4 | 14.9 | 1.02 (2.34) | 0.93 (2.13) | 5.00 | 2.51 | 3.99 |
| Cd | 0.068 | 0.070 | 5.21 (x) | 5.38 (x) | 76.0 | 49.7 | 55.9 |
| As | 2.58 | 1.16 | 1.52 (2.58) | 0.68 (1.16) | 5.61 | 4.36 | 15.4 |
| V | 30.8 | 26.5 | 0.34 (15.4) | 0.29 (13.2) | 0.46 | 0.26 | 0.43 |
| Mo | 0.92 | 0.18 | 0.84 (4.61) | 0.17 (0.91) | 2.46 | 2.42 | 17.1 |
| Hg | 0.019 | 0.019 | 0.23 (-) | 0.23 (–) | 35.6 | 15.6 | 52.4 |
| Be | 0.66 | 1.16 | 0.17 (x) | 0.31 (x) | 3.71 | 1.44 | 0.59 |
| Sn | 0.661 | 0.513 | 0.26 (x) | 0.21 (x) | 5.97 | 1.34 | 23.8 |
| Sb | 0.210 | 0.127 | 0.42 (x0) | 0.25 (x0) | 22.2 | 17.9 | 43.1 |
| Ti | 1400 | 1536 | 0.41 (1.22) | 0.45 (1.34) | 0.06 | 0.04 | 0.01 |
| Li | 7.83 | 9.75 | 0.24 (0.52) | 0.30 (0.65) | 3.66 | 3.32 | 2.93 |
| Rb | 52.3 | 51.1 | 0.35 (0.87) | 0.34 (0.85) | 8.50 | 2.83 | 3.06 |
| Y | 6.87 | 7.70 | 0.34 (0.17) | 0.39 (0.19) | 3.07 | 1.36 | 0.22 |
| Zr | 98.5 | 110 | 0.57 (0.44) | 0.64 (0.50) | 0.09 | 0.06 | 0.02 |
| Cs | 1.18 | 1.16 | 0.32 (x0) | 0.31 (x0) | 2.06 | 0.80 | 1.42 |
| Bi | 0.097 | 0.080 | 10.8 (–) | 8.86 (–) | 3.30 | 0.97 | 6.11 |
| W | 0.383 | 0.348 | 0.29 (0.24) | 0.27 (0.22) | 2.26 | 1.10 | 1.33 |
| Tl | 0.344 | 0.324 | 0.34 (–) | 0.32 (–) | 6.95 | 2.68 | 2.81 |
| La | 13.6 | 15.3 | 0.47 (0.45) | 0.53 (0.51) | 2.57 | 0.76 | 0.17 |
| Ce | 27.2 | 28.4 | 0.39 (0.30) | 0.41 (0.31) | 2.83 | 0.83 | 0.18 |
| Th | 3.53 | 4.15 | 0.27 (2.07) | 0.32 (2.44) | 1.27 | 0.56 | 0.13 |
| U | 0.850 | 0.933 | 0.34 (1.89) | 0.37 (2.07) | 0.67 | 0.54 | 0.27 |
Примечания. Нормированные величины концентраций приведены относительно Земной коры (Виноградов, 1962), а в скобках относительно песчаных осадочных пород (Turekian, Wedepohl, 1961). Жирным шрифтом выделены значения более 2 для нормированных величин концентраций и более 5 для коэффициентов водной миграции.
Содержания элементов в почве не превышали токсикологический порог для определенных в (ГН 2.1.7.2041-06; ГН 2.1.7.2511-09) ПДК и ОДК следующих элементов Hg, Cd, Pb, As, Cu, Ni, Zn, V, Sb. Нидерландскими учеными предложена максимальная недействующая концентрация металлов и металлоидов в почве, определенная на основе максимальных концентраций, не оказывающих значимого влияния на рост или репродукцию тестовых организмов (как представителей почвенной фауны, так и развитие микробиологических процессов и реакцию растений), а также гармонизирована с учетом подвижности элементов в почве (Crommentuijn et al., 2000). Так для исследуемых почв значения данного критерия были превышены по Ва в ~300 раз, Be – 100 раз, V, Zn, Ni и As – 2 раза, Tl – 1.5 раза, а также по Cu, но без превышений по Hg, Сd, Pb, Sb, Sn, Мо и Со.
Кислотность и кислотонейтрализующая способность исследуемых вод
Предваряя рассмотрение кислотности и кислотонейтрализующей способности вод (ANC), следует отметить, что, во-первых, в уязвимых к закислению водах снижение кислотонейтрализующей способности менее 50 мкг-экв/л принято считать критическим (Brаkke et al., 1988; Nenonen, 1991), во-вторых, органические кислоты могут быть не только слабыми и обеспечивать буферные свойства вод, но и выступать как сильные кислоты, усиливающие закисление вод (Clark et al., 2010, Моисеенко и др., 2017).
На рис. 2 представлена динамика рН, цветности вод, концентраций органического аниона сильных и слабых кислот, а также величин ANC атмосферных осадков, кроновых, почвенных и озерных вод в летне-осенний период 2015 г. Атмосферные осадки на протяжении всего периода имели значения рН > 6 (за исключением июля) характеризовались низкими значениями цветности, незначительным содержанием органических кислот, лишь только в августе наблюдались значимые концентрации сильных органических кислот. Кроновые воды за исключением октября имели значения рН < 6, в отличие от АО характеризовались высокими значениями цветности вод, а до сентября и высокими концентрациями слабых органических кислот. В июне КВ в отличие от АО имели крайне высокие значения ANC вследствие смыва пыли с кроны деревьев в этот засушливый период.
Рис. 2.
Динамика рН, цветности вод, концентраций органического аниона (An–) сильных и слабых кислот, а также величин кислотонейтрализующей способности вод (ANC) на конец исследуемых периодов 2015 г. (1 – вода оз. Гусиного, 2 – атмосферные осадки, 3 – кроновые воды, 4 – почвенные воды в слое 0–20 см, 5 – почвенные воды в слое 0–30 см).
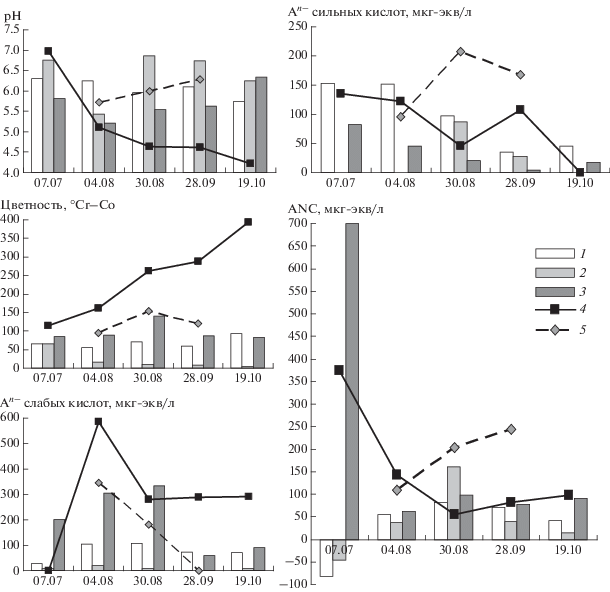
Отличительной особенностью почвенных вод органогенного и элювиального горизонтов являлась высокая кислотность образцов, которая связана не только регулярным обогащением водных проб низкомолекулярными органическими кислотами, смываемыми кроновыми водами, но и органическими веществами гумусовой природы с большей молекулярной массой и более высокими кислотными свойствами. Большая кислотность органогенного и подзолистого горизонтов по сравнению с иллювиальным вполне закономерна (Лукина и др., 2002; Пристова, Забоева, 2007) вследствие различного вклада гумусовых кислот, а также, что характерно для органогенного горизонта, изменения молекулярной массы органических веществ гумусовой природы, и, следовательно, их кислотно-основных свойств в течение исследуемого периода. Если значения рН почвенных вод гумусового и подзолистого горизонтов снижались с ~7 до 4.2 при значительном возрастании цветности почвенных вод в примерно 4 раза к концу осени, то значения рН почвенных вод иллювиального горизонта увеличились с 5.1 до 6.3 при сравнительно стабильной цветности вод. Максимумы концентраций слабых органических кислот в почвенных водах всех горизонтов приходились на июль, что связано с большей долей низкомолекулярных метаболитов негумусовой природы, а также с усилением буферных свойств автохтонных органических веществ.
Согласно рис. 2, достаточно динамичное изменение ANC, слабых кислот (которые буферируют систему) и доли сильных кислот (которые способствуют образованию протона) связано с образованием и расходованием низкомолекулярных органических веществ аллохтонного типа и изменением структуры и молекулярных масс гумусовой органики, что зависит от внешних факторов – температуры, количества осадков и горизонта почвенных вод. Наиболее показательны отрицательные значения ANC для озера, которые сопровождаются максимумом содержания сильных кислот, что означает значимый прирост содержания протонов в ходе диссоциации кислот.
Значения рН вод оз. Гусиного в течение периода наблюдений колебались в районе 6, цветность вод была относительно стабильна, увеличиваясь к концу августа и в октябре. Если содержание слабых органических кислот было значительно ниже, чем в почвенных водах гумусового и подзолистого горизонтов, то напротив содержание сильных органических кислот летом даже несколько их превосходило.
Сезонные особенности выщелачивания
Потоки элементов на водосборе и в водоеме отражают превалирующее направление всего комплекса биогеохимических процессов – поглощение элементов биотой и разложение органических веществ, сорбция и десорбция на минеральной и органической основе почв, растворение и ионный обмен, выветривание первичных и вторичных минералов и синтез вторичных минералов и другие. В табл. 3 представлены потоки элементов, рассчитанные балансовым методом. Для удобства изложения положительно направленное доминирование процессов обозначим “поглощение”, а отрицательно – “возврат”.
Таблица 3.
Потоки элементов (мкг/м2 сут), характеризующих их превалирующее поглощение (положительные значения) или возврат (отрицательные значения) в слое 0–20 см (числитель) и 20–30 см (знаменатель) на водосборе озера Гусиного в исследуемые периоды 2015 г.
| Элемент | Период наблюдений | ||||
|---|---|---|---|---|---|
| 09.06–07.07.2015 | 07.07–04.08.2015 | 04.08–30.08.2015 | 30.08–28.09.2015 | 28.09–19.10.2015 | |
| Ca | 465/0 | –2018/1182 | –416/1587 | –865/2538 | –513/0 |
| Mg | 182/0 | 88.4/–62.8 | –12.0/354 | –120/564 | –109/0 |
| Na | 1420/0 | –4422/–1666 | –643/335 | –953/72 | –231/0 |
| K | –1921/0 | 2400/1798 | 978/2090 | 118/3547 | –853/0 |
| Снеорг | –928/0 | –93/308 | 151/1014 | 1325/228 | –1104/0 |
| S (S${\text{O}}_{4}^{{2 - }}$) | 1185/0 | –3800/–805 | –425/1320 | –197/854 | –525/0 |
| Cl | –1351/0 | –678/427 | –1723/1736 | –2167/4789 | –1242/0 |
| Сорг | 8913/0 | 29408/117285 | 7801/74188 | –118023/137499 | –52272/0 |
| P(P${\text{O}}_{4}^{{3 - }}$) | –19335/0 | 2212/–4131 | 626/2868 | 1216/1852 | –1182/0 |
| N(N${\text{O}}_{2}^{ - }$) | –24.4/0 | –1785/1783 | 132/19.7 | –363/462 | –36.9/0 |
| N(N${\text{O}}_{3}^{ - }$) | –912/0 | 605/–294 | –46.1/146 | –698/504 | 93.3/0 |
| N(N${\text{H}}_{4}^{ + }$) | –/– | 136/–60.8 | 4.96/8.60 | –363/733 | –272/0 |
| Si | –435/0 | –2604/–571 | –2920/2755 | –3854/3349 | –1668/0 |
| Al | –376/0 | –2333/1200 | –1901/1835 | –3143/3052 | –1859/0 |
| Fe | –91.2/0 | –622/525 | –507/527 | –714/740 | –521/0 |
| Mn | –171/0 | –189/144 | –245/445 | –269/648 | –209/0 |
| Sr | –1.42/0 | –21.5/–0.67 | –7.52/–18.0 | –11.5/–29.8 | –5.79/0 |
| Ba | –21.9/0 | 12.1/–45.4 | –56.3/57.1 | –102/107 | –56.9/0 |
| B | –0.68 / | 11.7/5.99 | –1.17/15.4 | 2.07/15.3 | –1.91/0 |
| Zn | 1081/0 | 3556/819 | 24/2109 | –501/2578 | –148/0 |
| Cu | 113/0 | 771/434 | –42/511 | –104/678 | –152/0 |
| Ni | –3.78/0 | –1.82/0.65 | –2.96/3.37 | –5.08/5.68 | –2.72/0 |
| Co | –0.172/0 | –1.68/1.56 | –1.60/1.78 | –2.27/2.45 | –1.43/0 |
| Pb | –3.16/0 | –1.81/2.62 | –1.91/2.34 | –2.37/2.84 | –1.29/0 |
| Cd | –0.039/0 | –0.093/0.078 | –0,181/0.227 | –0.242/0.325 | –0.165/0 |
| As | –0.171/0 | –0.981/0.577 | –0.393/0.490 | –0.593/0.487 | –0.428/0 |
| V | –0.218/0 | –0.546/0.644 | –0.291/0.549 | –0.516/0.711 | –0.174/0 |
| Mo | –0.017/0 | 0.166/–0.036 | 0.031/0.042 | 0.478/0.126 | –0.001/0 |
| Hg | –0.015/0 | 0.021/0.049 | –0.020/0.033 | –0.025/0.025 | 0/0 |
| Be | –0.013/0 | –0.131/0.060 | –0.137/0.125 | –0.179/0.186 | –0.125/0 |
| Sn | –0.153/0 | 0.111/0.054 | 0.109/0.096 | 0.407/0.119 | 0.014/0 |
| Sb | 0.091/0 | 0.178/0.084 | –0.006/0.144 | –0.042/0.190 | –0.027/0 |
| Ti | –0.497/0 | –5.47/3.21 | –4.74/5.36 | –8.22/7.40 | –5.43/0 |
| Li | –0.113/0 | 0.379/–1.72 | –0.019/–0.086 | –3.92/4.00 | –1.88/0 |
| Rb | –15.3/0 | 30.3/6.50 | 15.0/9.29 | 14.7/8.12 | 4.01/0 |
| Y | –0.219/0 | –1.26/0.638 | –1.04/1.00 | –1.75/1.68 | –0.942/0 |
| Zr | –0.045/0 | –0.479 /0.177 | –0.326/0.344 | –0.613/0.587 | –0.377/0 |
| Cs | –0.112/0 | –0.002/0.087 | 0.060/0.049 | 0.019/0.035 | 0.001/0 |
| Bi | –0.003/0 | 0.011/0.019 | 0.009/0.010 | –0.005/0.021 | –0.004/0 |
| W | –0.024/0 | –0.017/0.033 | –0.014/0.026 | –0.007/0.030 | –0.019/0 |
| Tl | –0.069/0 | 0.041/0.035 | –0.015/0.069 | –0.007/0.064 | –0.008/0 |
| La | –0.373/0 | –2.10/1.46 | –1.74/1.69 | –2.89/2.85 | –1.66/0 |
| Ce | –0.740/0 | –4.84 /3.43 | –3.90/3.80 | –6.35/6.25 | –3.60/0 |
| Th | –0.077/0 | –0.290/0.168 | –0.178/0.177 | –0.268/0.251 | –0.186/0 |
| U | –0.002/0 | –0.028/0.016 | –0.017/0.021 | –0.017/0.023 | –0.012/0 |
В органогенном и подзолистом горизонтах на протяжении всего периода наблюдения, по-видимому, превалировали процессы выщелачивания большинства элементов, как вследствие гидратации, гидролиза, ацидолиза, так и гумусовыми кислотами. Если интенсивность последнего постепенно нарастала (увеличение цветности почвенных вод – см. рис.), то первых увеличивалась в сентябре и особенно июле, когда выпало максимальное количество осадков и в почвенных водах содержалось наибольшее количество органических кислот (рис. 2).
Поток кремнезема превосходил таковой глинозема вплоть до октября. Кремний практически всегда накапливается в опадающих органах (Базилевич, Титлянова, 2008). Если для северной тайги обнаруживается обогащение хвои ели Са, Al, Fe, Mn с увеличением возрастного класса, то в южной тайге этого не происходит (Рассеянные элементы…, 2004). Песчаные породы являются гипоглиноземистыми, но и указанные выше обстоятельства также способствуют большему выносу кремния.
На протяжении всего исследуемого периода из гумусового и подзолистого горизонтов выщелачивались Si, Al, Fe, Mn, Sr, Ti, Co, Ni, Pb, Ce, La, Y, As, V, Cd, Zr, Be, W, Th, U (табл. 3). Например, на основе рассчитанных констант устойчивости металлов с гумусовыми веществами, выделенными из почв тайги, при достаточной щелочности приводиться следующий конкурентный ряд элементов: Fe > Al > Pb > Co > Ni > Zn > Cd > Cu > > Mg > Ca > Cr > Mn > Sr (Моисеенко и др., 2012). Если в водах озер тайги содержание органического вещества может достигать 25 мгС/л, Fe – 1129 мкг/л, Al – 238 мкг/л (Моисеенко и др., 2006), то в почвенных водах 151 мгС/л, 451 мкг/л, 1880 мкг/л, соответственно (табл. 1). Если в поверхностных водах тайги связывание элементов гумусовыми веществами лимитируется как количеством органических веществ, так и количеством железа, то в исследуемых почвенных водах центры связывания гумусовых веществ могут также занимать алюминий и другие элементы, склонные к комплексообразованию.
Гидролиз и ацидолиз значительно усиливал вынос Al, Fe, Ti, Co, V, Y, Zr, La, Ce. В июле и сентябре также был усилен вынос Na, Ca, Sr, при этом только в июле потоки достигали больших значений при максимальном выносе сульфатов. Именно в этот период, возможно, могут создаваться условия для растворения кальцитов. Потоки же Pb и Ni были наиболее интенсивны в июне и сентябре, когда превалировал возврат нитратов.
Условия для возврата неорганического углерода формировались только в июне, когда заканчивался интенсивный прирост древостоя, и в октябре, когда интенсивность почвенного дыхания связана с микробиологическим разложением органических веществ, в сентябре и октябре возврат органического углерода превалировал. Максимумы численности микроорганизмов почв приходятся на весну, конец осени и начало зимы (Рассеянные элементы…, 2004). В июле были максимальны как ассимиляция форм неорганического азота, так и накопление промежуточных продуктов – нитритов, что связано с высокой интенсивностью биотического оборота питательных веществ и метаболитов в этот период (максимальные концентрации и слабых органических кислот – рис. 2).
Калий и Р наиболее подвержены ретранслокации (переток элементов из стареющих тканей в запасающие или вновь образующиеся), но и наиболее быстро освобождающиеся из подстилки элементы, легко выщелачиваются из разложившихся растительных остатков (Базилевич, Титлянова, 2008). После половодья запасы К и Р в почвенных водах были велики и в июне их возврат превосходил поглощение, однако с июля по сентябрь включительно в органогенном горизонте почвы они активно поглощались. Сходство Rb с К, по-видимому, определяет и высокое поглощение Rb в те же периоды. В июле-сентябре идет превалирующее поглощение Мо, что связано с сочетанием интенсивностей множества метаболических процессов биоценоза: ассимиляция неорганического азота (нитратредуктаза), окисление альдегидов в соответствующие карбоновые кислоты (альдегидоксидаза), метаболизма серосодержащих аминокислот (сульфитоксидаза), деградация пуринов (ксантиноксидаза) и др. До августа также поглощались крайне необходимые для биологических систем Mg, Cu, а Zn до сентября. В июле, когда велика интенсивность метаболических процессов, превалировало поглощение не только В и Li, но и токсичных Tl (в биохимических процессах может выступать аналогом К), Bi, Sb и Ba, что может быть негативным явлениям при отсутствие в экосистеме Sе, необходимого в биохимической адаптации и детоксикации биологических систем. Иная ситуация складывается с оловом, которое начиная с июля закреплялось в почве, по-видимому, вследствие следующих обстоятельств. Широкое использование оловоорганических соединений привело к их проникновению в различные экосистемы и в пищевую цепь; в атмосфере олово существует как газы и пары или связанные с частицами пыли, а в почвах оно относительно неподвижно, причем деградация оловоорганических соединений в анаэробных условиях может варьироваться от года до десятилетий (Handbook on the Toxicology of Metals, 2007).
В иллювиальном горизонте на протяжении всего исследуемого периода (июль-сентябрь) наблюдалась аккумуляция всех элементов за исключением Sr, что закономерно для педолитогенного барьера. Только в условиях промывного режима в июле из иллювиального горизонта выносились сульфаты, нитраты, фосфаты, Si, Mg, Na, Ва, Мо и Li (табл. 3).
В целом для всего исследуемого периода в почвенных водах интенсивность водной миграции элементов (табл. 2), оцениваемая по отношению к их содержанию в бедных песчаных почвах водосбора оз. Гусиного, крайне высока для Zn и Cu, значительна для Hg, Cd, Sb, Pb, As, а также Са, Mg, Na. В почвенных водах гумусового и подзолистого горизонтов интенсивность водной миграции значительно усиливается для K, Mn, Со, также отмечается ее некоторое усиление для Rb, Ni, Bi, Sn, Tl по сравнению с иллювиальным горизонтом почв.
Бюджет элементов в почвенном профиле
В табл. 4 представлены средние потоки элементов с атмосферными осадками и кроновыми водами, а также рассчитанный бюджет элементов в 30 см слое исследуемых почв в летне-осенний период 2015 г.
Таблица 4.
Поступление элементов с атмосферными осадками (АО) и кроновыми водами (КВ), поглощение, возврат в слое почвы 0–30 см, вынос за пределы почвенного профиля (мкг/м2 сут) в летне-осенний период 2015 г.
| Элемент | Поступление с АО | Поступление с КВ | Поглощение | Возврат | Вынос за пределы почвенного профиля | Отношение КВ/АО | Отношение поглощение/возврат |
|---|---|---|---|---|---|---|---|
| Ca | 1760 | 2337 | 1220 | 782 | 1899 | 1.32 | 1.56 |
| Mg | 133 | 518 | 251 | 59.5 | 327 | 3.87 | 4.23 |
| Na | 816 | 1368 | 398 | 1664 | 2634 | 1.72 | 0.24 |
| K | 256 | 4793 | 2300 | 543 | 3036 | 18.7 | 4.24 |
| Снеорг | 669 | 955 | 636 | 392 | 711 | 1.43 | 1.62 |
| S | 671 | 1729 | 699 | 1187 | 2217 | 1.76 | 0.59 |
| Cl | 1039 | 1758 | 1485 | 1443 | 1716 | 1.69 | 1.03 |
| Сорг | 12 247 | 90 529 | 79 365 | 34 245 | 45409 | 7.34 | 2.32 |
| P(P${\text{O}}_{4}^{{3 - }}$) | 19.4 | 85.2 | 66.5 | 187 | 206 | 4.39 | 0.36 |
| N(ΣNмин) | 681 | 655 | 1037 | 1060 | 678 | 0.96 | 0.98 |
| Si | 71.7 | 285 | 1278 | 2453 | 1460 | 3.97 | 0.52 |
| Al | 29.6 | 143 | 1286 | 1935 | 792 | 4.78 | 0.67 |
| Fe | 22.4 | 54.1 | 378 | 491 | 167 | 2.34 | 0.77 |
| Mn | 7.44 | 261 | 260 | 217 | 218 | 34.6 | 1.20 |
| Sr | 9.97 | 5.45 | 0 | 20.2 | 25.5 | 0.54 | 0 |
| Ba | 8.99 | 13.8 | 37.3 | 56.9 | 33.4 | 1.50 | 0.66 |
| B | 3.23 | 19.1 | 10.6 | 0.68 | 9.18 | 5.84 | 9.33 |
| Zn | 411 | 2757 | 2144 | 134 | 747 | 6.72 | 16.1 |
| Cu | 70.6 | 603 | 529 | 55.2 | 129 | 8.66 | 9.59 |
| Ni | 14.1 | 1.67 | 2.05 | 3.32 | 2.94 | 0.12 | 0.62 |
| Co | 2.32 | 0.232 | 1.22 | 1.43 | 0.442 | 0.10 | 0.85 |
| Pb | 3.81 | 1.28 | 1.64 | 2.15 | 1.79 | 0.33 | 0.76 |
| Cd | 0.120 | 0.108 | 0.129 | 0.144 | 0.123 | 0.89 | 0.89 |
| As | 0.100 | 0.180 | 0.326 | 0.520 | 0.374 | 1.80 | 0.63 |
| V | 0.107 | 0.323 | 0.402 | 0.364 | 0.285 | 3.00 | 1.10 |
| Mo | 0.173 | 0.233 | 0.182 | 0.011 | 0.062 | 1.39 | 16.0 |
| Hg | 0 | 0.027 | 0.027 | 0.013 | 0.013 | – | 2.08 |
| Be | 0.001 | 0.014 | 0.078 | 0.117 | 0.053 | 14.0 | 0.67 |
| Sn | 0.128 | 0.236 | 0.193 | 0.032 | 0.075 | 1.84 | 6.03 |
| Sb | 0.212 | 0.245 | 0.145 | 0.015 | 0.115 | 1.16 | 9.67 |
| Ti | 0.053 | 1.23 | 3.36 | 4.87 | 2.74 | 23.2 | 0.69 |
| Li | 0.192 | 0.363 | 0.958 | 1.57 | 0.973 | 1.89 | 0.61 |
| Rb | 0.601 | 25.3 | 18.2 | 3.24 | 10.3 | 42.1 | 5.62 |
| Y | 0.037 | 0.077 | 0.703 | 1.05 | 0.427 | 2.08 | 0.67 |
| Zr | 0.006 | 0.072 | 0.234 | 0.370 | 0.208 | 12.0 | 0.63 |
| Cs | 0.029 | 0.084 | 0.052 | 0.024 | 0.056 | 2.90 | 2.17 |
| Bi | 0.003 | 0.016 | 0.012 | 0.002 | 0.006 | 5.33 | 6.00 |
| W | 0.018 | 0.021 | 0.019 | 0.016 | 0.018 | 1.17 | 1.19 |
| Tl | 0.034 | 0.078 | 0.044 | 0.020 | 0.054 | 2.29 | 2.20 |
| La | 0.055 | 0.098 | 1.27 | 1.77 | 0.598 | 1.78 | 0.72 |
| Ce | 0.124 | 0.217 | 2.85 | 3.92 | 1.29 | 1.75 | 0.73 |
| Th | 0.002 | 0.024 | 0.126 | 0.201 | 0.099 | 12.0 | 0.63 |
| U | 0.007 | 0.013 | 0.013 | 0.015 | 0.015 | 1.86 | 0.87 |
Увеличение поступления многих элементов с кроновыми водами по сравнению с атмосферными осадками отмечается многими исследованиями (Алексеенко, 1989; Лукина и др., 2002; Пристова, Забоева, 2007; Fišák et al., 2006 и другими). Данное явление объясняется смывом и выщелачиванием как накопленных продуктов метаболизма, так и сухих выпадений (пыли) с поверхности кроны. Можно сопоставить поступление элементов с атмосферными осадками и кроновыми водами с таковыми в еловых лесах Богемии вдали от индустриальных центров и городов на водосборе, сложенном гранитами (Fišák et al., 2006). Так, с атмосферными осадками на исследуемую территорию при несколько меньших потоках Al, Fe и Mn, в 2 раза и более поступает сульфатов, хлоридов, Ca, Mg, Na, K, Rb, Pb, Cd и более чем в 10 раз Zn. Например, по оценкам атмосферное поступление Zn и Cu с пылью может достигать 0.5–30 и 0.07–5 мкг/м2 сут в фоновых районах и 7–1400 и 20–600 мкг/м2 сут соответственно в урбанизированных районах (Norra, Stüben, 2004). Поступление Zn и Cu на водосборе оз. Гусиного с атмосферными осадками соответствует уровню их поступления с пылью в урбанизированных районах, а с кроновыми водами даже превосходит. В еловых лесах Богемии кроновые воды значительно обогащаются Rb (в 30 раз), К (в 18 раз) и Mn (в 8 раз). Обогащение кроновых вод этими элементам, по-видимому, связано с большим оборотом в метаболических процессах (крайне необходимого элемента питания К, его гомолога Rb и необходимого для углеводного обмена и фотолиза воды при фотосинтезе Mn). Кроновые воды на водосборе оз. Гусиного в большей степени обогащаются этими элементами, а также в значительной степени не только Р, органическим С, Zn, Cu, В, но и Ti, Zr, Al, Be, Th и Bi.
Самыми высокими коэффициентами биологического поглощения у различных растений характеризуются марганец и бор, а у рубидия он больше, чем у цинка и кальция (Рассеянные элементы…, 2004). Хотя, представленное в табл. 4, отношение величин поглощения элемента к его возврату отчасти характеризует и его аккумуляцию в почве, это отношение велико не только для В, K, Mg, Zn, Cu, Мо, но и для Rb, Bi, Sb, Sn.
Не менее интересно соотношение приходных и расходных составляющих бюджета элементов в 30 см слое исследуемых почв. Если вынос фосфора за пределы почвенного профиля превосходил более чем в 2 раза его поступления с кроновыми водами, то для азота они приблизительно равны. Например, показано, что продуктивность озер в тундре и тайге больше лимитируется поступлением азота, чем фосфора, в отличие от смешанных лесов и степей (Гашкина, 2011). Даже окультуривание песчаных подзолистых и дерново-подзолистых почв незначительно сказывается на содержании в них минеральных соединений азота, в отличие от фосфора, а также калия (Иванов и др., 2004). Превалирующий вынос характерен для сульфатов и Na, также превалирующе выщелачиваются не только Si, Al, Fe, Sr, Ва, Ti, Y, Zr, La, Ce, Be, Th, но и Cd, Pb, As, Ni. Несмотря на крайне высокие коэффициенты водной миграции в почвенных водах у Zn и Cu и отмеченное увеличение их поступления с АО и КВ по сравнению с предыдущими десятилетиями, превалирующего выноса их за пределы почвенного профиля не происходит, что может свидетельствовать об удержании и рециркуляции меди и цинка в экосистеме водосбора оз. Гусиного. Также следует отметить, что вынос за пределы почвенного профиля не превосходил поступления с КВ не только для К, Mg, Са, Mn, Мо, Со, В, Li, но и Rb, Cs, Sb, Sn, W, Bi, V, Tl, Hg аккумулировались в почве.
Влияние поступлений элементов на их запас в озере
В табл. 5 представлены максимальный запас элементов в оз. Гусиное и их массовое и процентное, оцениваемое от максимального запаса, поступление с атмосферными осадками и почвенными водами в озеро в летне-осенний период 2015 г.
Таблица 5.
Максимальный запас элементов в оз. Гусиное и их поступление с атмосферными осадками (АО) и почвенными водами в озеро в летне-осенний период 2015 г.
| Элемент | Максимальный запас | Поступление с АО | Поступление с почвенными водами | ||
|---|---|---|---|---|---|
| г | г | % | г | % | |
| Ca | 760 000 | 34 900 | 4.59 | 37 300 | 4.91 |
| Mg | 98 400 | 2650 | 2.69 | 7020 | 7.13 |
| Na | 149 000 | 16 000 | 10.7 | 29 500 | 19.8 |
| K | 612 000 | 5110 | 8.35 | 46 700 | 7.63 |
| Снеорг | 428 000 | 13 200 | 3.08 | 9520 | 2.22 |
| S | 785 000 | 19 500 | 2.48 | 29 700 | 3.79 |
| Cl | 975 000 | 20 900 | 2.14 | 34 400 | 3.53 |
| Сорг | 19 796 000 | 244 000 | 1.23 | 1 512 000 | 7.64 |
| P(P${\text{O}}_{4}^{{3 - }}$) | 3625 | 393 | 10.8 | 1312 | 36.2 |
| N(ΣNмин) | 397 000 | 12 000 | 3.01 | 13 900 | 3.51 |
| Si | 73 600 | 1403 | 1.94 | 45 300 | 61.5 |
| Al | 22 300 | 598 | 2.68 | 20 400 | 91.5 |
| Fe | 45 000 | 460 | 1.02 | 5230 | 11.6 |
| Mn | 10 900 | 148 | 1.36 | 5300 | 48.6 |
| Sr | 1288 | 197 | 15.3 | 165 | 12.8 |
| Ba | 4047 | 180 | 4.44 | 638 | 15.8 |
| B | 962 | 65.0 | 6.76 | 239 | 24.8 |
| Zn | 7391 | 8084 | 109 | 32 878 | 445 |
| Cu | 1300 | 1381 | 106 | 7318 | 563 |
| Ni | 3830 | 2.74 | 0.07 | 49.8 | 1.30 |
| Co | 62.0 | 46.2 | 74.5 | 16.5 | 22.6 |
| Pb | 514 | 77.2 | 15.0 | 33.8 | 6.58 |
| Cd | 50.4 | 2.40 | 4.76 | 2.87 | 5.69 |
| As | 107 | 1.96 | 1.83 | 6.75 | 6.31 |
| V | 95.8 | 2.13 | 2.22 | 7.64 | 7.97 |
| Mo | 128 | 3.39 | 2.65 | 1.86 | 1.45 |
| Hg | 12.2 | 0 | 0 | 0.478 | 3.92 |
| Be | 3.38 | 0.020 | 0.59 | 1.34 | 39.6 |
| Sn | 185 | 2.56 | 1.38 | 1.78 | 0.962 |
| Sb | 31.5 | 4.24 | 13.5 | 2.84 | 9.02 |
| Ti | 253 | 1.08 | 0.43 | 63.3 | 25.0 |
| Li | 101 | 3.82 | 3.78 | 18.2 | 18.0 |
| Rb | 545 | 11.9 | 2.18 | 109 | 20.0 |
| Y | 7.10 | 0.739 | 10.4 | 11.3 | 159 |
| Zr | 9.55 | 0.111 | 1.16 | 4.59 | 48.1 |
| Cs | 5.83 | 0.570 | 9.78 | 0.952 | 16.3 |
| Bi | 4.03 | 0.054 | 1.34 | 0.177 | 4.39 |
| W | 4.93 | 0.368 | 7.46 | 0.403 | 8.17 |
| Tl | 3.28 | 0.680 | 20.7 | 0.993 | 30.3 |
| La | 14.6 | 1.10 | 7.53 | 18.1 | 124 |
| Ce | 28.1 | 2.49 | 8.86 | 40.2 | 143 |
| Th | 1.78 | 1.80 | 101 | 2.11 | 119 |
| U | 0.913 | 0.135 | 14.8 | 0.319 | 34.9 |
Поступление элементов с атмосферными осадками в озеро за весь исследуемый период для большинства элементов составляло 0–20% от максимального их запаса, только у Zn, Cu, Th оно было больше их максимального запаса в озере, а у Со было значительно. Для главных ионов максимальный их запас в озере не полностью обеспечивался поступлением с почвенными водами за исследуемый период и формировался в значительной степени в период половодья. В летне-осенний период выщелачивались в основном литофильные элементы и поступление их с почвенными водами было больше чем с атмосферными осадками, а для Y, La, Ce, Th составляло более 100% максимального запаса в озере. Притом, что не менее значительно поступление с почвенными водами Zn, Cu (табл. 5). Судя по коэффициентам водной миграции (табл. 2), обогащения озерных вод литофильными элементами не происходит. По отношению к содержанию элементов в бедных песчаных почвах водосбора оз. Гусиного, помимо Са, Mg, Na, озерные воды обогащаются Hg, Cd, Ni, Zn, Cu, Sb, Sn, Mo, As, Bi. Так, в работе (Моисеенко, Гашкина, 2007) получены коэффициенты водной миграции для озер, не подверженных каким-либо прямым источникам загрязнения на Восточно-Европейской равнине, которые были высокими у Mo, As, U, Bi, Sb, Cd, Ag, Se, Re и, главным образом, обусловлены аэротехногенной нагрузкой на водосборы, как следствие их глобального и регионального рассеивания.
ЗАКЛЮЧЕНИЕ
На основе изучения распределения элементов в системе “атмосферные осадки–кроновые воды–почвенные воды–озеро” водосбора оз. Гусиного на территории Валдайского национального парка выявлены основные закономерности биогеохимических миграционных потоков элементов.
Установлено значительное обогащение кроновых вод основными ионами, биогенными элементами и микроэлементами (для таких биофильных элементов, как Zn, Cu, Mn, Rb – на порядок) по сравнению с атмосферными осадками на фоне более низких значениях рН кроновых вод. Исключения составляют более высокие концентрации Ni, Co и Pb в атмосферных осадках.
На основе анализа сезонной динамики потоков элементов с почвенными водами показано, что в гумусовом и подзолистом горизонтах на протяжении всего периода наблюдения превалировали процессы выщелачивания большинства литофильных элементов, а также Fe, Co, Ni, Pb, As, Cd, W. В то время как практически до осени превалировало поглощение не только К, Р, Mg, Zn, Cu, Мо, но и Rb, Sn. В иллювиальном горизонте на протяжении всего исследуемого периода наблюдалась в основном аккумуляция всех элементов (за исключением Sr). В условиях промывного режима из иллювиального горизонта выносились сульфаты, нитраты, фосфаты, Si, Mg, Na, Ва, Мо и Li.
В исследованиях выявлено увеличение поступления Zn и Cu с атмосферными осадками и кроновыми водами по сравнению с предыдущими десятилетиями. Однако, превалирующего выноса их за пределы почвенного профиля не происходит, что может свидетельствовать об удержании и рециркуляции меди и цинка в биогеохимических процессах на водосборе оз. Гусиного. Доказано, что вынос не только К, Mg, Са, Mn, Мо, Со, В, Li, но и Rb, Cs, Sb, Sn, W, Bi, V, Tl, Hg за пределы почвенного профиля не превосходил поступления этих элементов с кроновыми водами, что свидетельствует о биогеохимическом барьере почв на пути миграционных потоков.
На основе определения нормированных величин концентраций элементов в почве и коэффициентов их водной миграции диагностированы не только направленность биогеохимического их круговорота, но и антропогенное влияние в фоновом регионе. По сравнению с песчаными осадочными горными породами почвы водосбора оз. Гусиного обогащаются не только литофильными Mn, Sr, Ba, V, Cs, Th, но и Cd, Pb, Ni, Co, Bi, Sb, Sn, а в гумусовом и подзолистом горизонтах происходит концентрирование Mo и As. Интенсивность водной миграции элементов в почвенных и озерных водах, оцениваемая по отношению к их содержанию в бедных песчаных почвах водосбора оз. Гусиного, значительна, помимо Са, Mg, Na, и для Hg, Cd, Zn, Cu, Sb, As, а озерные воды также обогащаются Ni, Sn, Mo, Bi. В почвенных водах гумусового и подзолистого горизонтов по сравнению с иллювиальным горизонтом почв интенсивность водной миграции значительно усиливается не только для K, Mn и Со, но и для Rb, Ni, Bi, Sn, Tl.
Несмотря на то, что исследованная площадка находилась в отдалении от каких либо прямых техногенных воздействий на территории национального парка, возможными причинами антропогенного влияния могут быть: 1) глобальный интенсивный техногенез прошедшего столетия; 2) влияние воздушного трансрегионального переноса загрязненных масс из более отдаленных индустриальных регионов; 3) увеличением антропогенного влияния в данном регионе (г. Валдай); 4) ускорением в целом биологического круговорота в связи с наблюдаемым в прошедшие десятилетия потеплением климата в северо-западных регионах России.
Авторы выражают глубокую признательность сотрудникам и администрации Валдайского филиала Государственного гидрологического института и Национального парка “Валдайский” за помощь в проведении работ.
Определение минералогического состава почв выполнено с использованием рентгеновского дифрактометра ULTIMA-IV, приобретенного за счет средств Программы развития Московского университета им. М.В. Ломоносова.
Работа выполнена при финансовой поддержке РНФ (грант № 18-17-00184).
Список литературы
Алексеенко В.А. (1989) Изучение геохимических потоков микроэлементов на фоновом лесном водосборе Северо-запада ЕТС. Водные ресурсы (6), 91-96.
Базилевич Н.И., Титлянова А.А. (2008) Биотический круговорот на пяти континентах: азот и зольные элементы в природных наземных экосистемах. Новосибирск: Изд-во СО РАН, 381 с.
Виноградов А.П. (1962) Среднее содержание химических элементов в главных типах изверженных горных пород земной коры. Геохимия (7), 565-571.
Гашкина Н.А. (2011) Зональные особенности распределения биогенных элементов и органического вещества в малых озерах. Водные ресурсы 38(3), 325-345.
Геохимия ландшафтов и география почв. 100 лет со дня рождения М.А. Глазовской. (2012) М.: АПР, 600 с.
Глазовский Н.Ф. (1982) Техногенные потоки вещества в биосфере. Добыча полезных ископаемых и геохимия природных экосистем (ред. Глазовская М.А.) М.: Наука, 7-28.
ГН 2.1.7.2041-06 (2006) Гигиенические нормативы “Предельно допустимые концентрации (ПДК) химических веществ в почве”.
ГН 2.1.7.2511-09 (2009) Гигиенические нормативы “Ориентировочно-допустимые концентрации (ОДК) химических веществ в почве”.
Дину М.И., Моисеенко Т.И. (2015) Компьютерная программа ACIDFORMMET, свидетельство № 2 015 617 036.
Иванов И.А., Иванов А.И., Цыганова Н.А. (2004) Изменение свойств подзолистых и дерново-подзолистых почв на песчаных породах при окультуривании. Почвоведение (4), 489-499.
Лукина Н.В., Горбачева Т.Т. Горбачева, Никонов В.В., Лукина М.А. (2002) Пространственная изменчивость кислотности Al-Fe-гумусовых подзолов. Почвоведение (2), 163-176.
Лукина Н.В., Никонов В.В. (1996) Биогеохимические циклы в лесах Севера в условиях аэротехногенного загрязнения. Апатиты: КНЦ РАН. Ч. 1. 213 с.
Лукина Н.В., Полянская Л.М., Орлова М.А. (2008) Питательный режим почв северотаежных лесов. М.: Наука, 342 с.
Моисеенко Т.И, Гашкина Н.А. (2011) Зональные особенности закисления озер. Водные ресурсы 38(1), 39-56.
Моисеенко Т.И., Гашкина Н.А. (2007) Распределение микроэлементов в поверхностных водах суши и особенности их водной миграции. Водные ресурсы 34(4), 454-468.
Моисеенко Т.И., Гашкина Н.А., Дину М.И. (2017) Закисление вод: уязвимость и критические нагрузки. М.: ЛЕНАНД, 400 с.
Моисеенко Т.И., Гашкина Н.А., Кудрявцева Л.П., Былиняк Ю.А., Сандимиров С.С. (2006) Зональные особенности формирования химического состава вод малых озер на территории Европейской части России. Водные ресурсы 33(2), 163-180.
Моисеенко Т.И., Дину М.И., Гашкина Н.А., Кремлева Т.А. (2012) Формы нахождения металлов в природных водах и их комплексообразование с гумусовыми веществами. ДАН 442(5), 691-695.
Мур Дж. В., Рамамурти С. (1987) Тяжелые металлы в природных водах. Контроль и оценка влияния. М. Мир, 288 с.
Никоноров А.М. (2001) Гидрохимия. СПб: Гидрометеоиздат, 444 с.
Перельман А.И. (1982) Геохимия природных вод. М.: Наука, 154 с.
Пристова Т.А., Забоева И.В. (2007) Химический состав атмосферных осадков и лизиметрических вод подзола иллювиально-железистого под хвойно-лиственными насаждениями (Республика Коми). Почвоведение (12), 1472-1481.
Рассеянные элементы в бореальных лесах. (2004) М.: Наука, 616 с.
Рябова Л.Н., Кузнецов В.А. (1998) Педогеохимические процессы преобразования осадочного материала в голоценовых почвах. Лiтасфера (9), 134-140.
Сает Ю.Е., Ревич Б.А., Янин Е.П. (1990) Геохимия окружающей среды. М.: Недра, 335 с.
Ферсман А.П. (1934) Геохимия. Т.2. Ленинград: ОНТ-И-ХИМТЕОРЕТ, 354 с.
Шитикова Т.Е. (1986) Состав лизиметрических вод дерново-подзолистых почв. Почвоведение (4), 27-38.
Bish D.L., Post J.E. (1993) Quantitative mineralogical analysis using the Rietveld full-pattern fitting method. Am. Mineral. 78, 932-940.
Brakke D.F., Landers D.H., Eilers J.M. (1988) Chemical and physical characteristics of lakes in the northeastern United States. Environ. Sci. Technol. 22(2), 155-163.
Bryan G.W. (1987) Heavy metal contamination in the sea. Marine Pollution (ed. R. Johnston). Amsterdam: Elsevier P. 185-302.
Clark J.M., Bottrell S.H., Evans C.D., Monteith D.T., Bartlett R., Rose R., Newton R.J., Chapman P.J. (2010) The importance of the relationship between scale and process in understanding long-term DOC dynamics. Sci. Total Environ. 408(13), 2768-2775.
Crommentuijn T., Sijm D., de Bruijn J., van den Hoop M., van Leeuwen K., van de Plassche E. (2000) Maximum permissible and negligible concentrations for metals and metalloids in the Netherlands, taking into account background concentrations. J. Environ. Manage. 60, 121-143.
Evans C.D., Monteith D.T., Reynolds B., Clark J.M. (2008) Buffering of recovery from acidification by organic acids. Sci. Total Environ. 404, 316-25.
Fišák J., Skřivan P.,Tesař M., Fottová D., Dobešová I., Navrátil T. (2006) Forest vegetation affecting the deposition of atmospheric elements to soils. Biologia, Bratislava 61(19), S255-S260.
Handbook on the Toxicology of Metals. (2007) 3th edition. Hardcover, Amsterdam, Boston: Academic Press. 1024 p.
Henriksen A., Kamari I., Posch M., Wilander A. (1992) Critical loads of acidity: Nordic surface waters. Ambio 21(5), 356‑363.
Henriksen A., Skjelkvåle B.L., Mannio J., Wilander A., Harriman R., Curtis C., Jensen J.P., Fjeld E., Moiseenko T. (1998) Northern European lake survey. Finland, Norway, Sweden, Denmark, Russian Kola, Russian Karelia, Scotland and Wales. Ambio 27(2), 80-91.
ICP Forest (2011) Manual on methods and criteria for harmonized sampling, assessment, monitoring and analysis of the effects of air pollution on forest. Hamburg: UNECE ICP Forest Programme Co-ordinating Centre. Http:/www.icp-forest.org/Manual.htm
Moiseenko T.I., Dinu M.I., Gashkina N.A., Kremleva T.A. (2019) Aquatic environment and anthropogenic factor effects on distribution of trace elements in surface waters of European Russia and Western Siberia. Environmental Research Letters 14(6), 065010
Nenonen M. (1991) Report on acidification in the arctic countries: man-made acidification in a world of natural extremes. The state of the Arctic environment: Reports, Arctic Centre, University of Lapland, Rovaniemi, Finland, 7-81.
Norra S., Stüben D. (2004) Trace element patterns and seasonal variability of dust precipitation in a low polluted city – the example of Karlsruhe/Germany. Environ. Monit. Assess. 93, 203-228.
Turekian K.K., Wedepohl K.H. (1961) Distribution of elements in some major units of the earth’s crust. Geological Society of America Bulletin 72, 175-192.
Van Breemen N., DriscollC.T., Mulder J. (1984) Acid deposition and internal proton sources in acidification of soils and waters. Nature 307, 599-604.
WRB (2015) World reference base for soil resources. Rome: FOOD AND AGRICULTURE ORGANIZATION OF THE UNITED NATION, 192 p.
Дополнительные материалы отсутствуют.