Геохимия, 2020, T. 65, № 9, стр. 930-936
Формы миграции тяжелых металлов и химический состав поверхностных вод в районе шахты “Мышьяковая” (Питкярантский рудный район, Южная Карелия)
А. А. Конышев a, *, Е. С. Сидкина a, **, Е. В. Черкасова a, М. В. Мироненко a, А. Г. Гридасов b, А. В. Жилкина a, И. А. Бугаев a
a Институт геохимии и аналитической химии им. В.И. Вернадского РАН
119991 Москва, ул. Косыгина, 19, Россия
b Томский политехнический университет
634050 Томск, просп. Ленина, 30, Россия
* E-mail: icelopa@gmail.com
** E-mail: sidkinaes@yandex.ru
Поступила в редакцию 31.01.2019
После доработки 28.08.2019
Принята к публикации 03.12.2019
Аннотация
Опробованы и проанализированы рудоносные породы и природные воды Питкярантского рудного района (окрестности шахты “Мышьяковая”, Хопунваарское рудное поле). В воде отмечены повышенные значения перманганатной окисляемости, а также превышение относительно ПДК содержаний железа, марганца, в пробах воды из “Мышьяковой” шахты – цинка, меди и мышьяка. Термодинамическими расчетами определены формы нахождения Fe, Mn, Cu, Zn, Cr, As, Ni в водах, при этом учтена возможность образования комплексов металлов с гуминовыми и фульвокислотами. Практически все содержание фульвокислоты расходуется на образование комплекса Fe(OH)2Fu–. Ni, Cd, Co находятся преимущественно в ионной форме, доля Mn и Zn в ионной форме также значительна.
ВВЕДЕНИЕ
Питкярантский рудный район расположен в Южной Карелии, на северо-восточном берегу Ладожского озера. Значимость изучения химического состава поверхностных вод на данной территории обусловлена тем, что речной сток региона направлен в крупнейший пресный водоем Европы – Ладожское озеро.
Воды озера используются для хозяйственно-питьевого водоснабжения, в сельском хозяйстве, в озере осуществляется промышленное рыболовство. Расчет форм нахождения элементов необходим для оценки миграционной способности и их токсикологического воздействия на живые организмы. Например, соединения As(V) более токсичны, чем As(III). Ионные формы большинства металлов являются наиболее опасными. При связывании металлов в фульватные и гуматные комплексы их токсический эффект снижается (Моисеенко и др., 2006; Дину, 2015; Крайнов и др., 2004; Варшал, 1994; Линник, 1986).
В Питкярантском рудном районе находятся многочисленные скарновые месторождения и рудопроявления с комплексным Fe-Sn-редкометально-полиметаллическим и флюоритовым оруденением, известные с ХVIII в. и интенсивно эксплуатировавшиеся во второй половине XIX–начале ХХ в. За весь период эксплуатации скарноворудных образований Питкярантского района было добыто около: 500 т Sn, 7000 т Cu, 60 000 т Fe, 11 т Ag и 16 кг Au (Иващенко, Голубев, 2015).
Все месторождения расположены в узкой полосе, протягивающейся вдоль северо-западного контакта Салминского батолита более чем на 50 км, и приурочены к метакарбонатным горизонтам сортавальской серии, обрамляющей гнейсогранитные купола.
На сегодняшний момент эти объекты не отрабатываются, шахты затоплены водой, отвалы находятся под воздействием атмосферного воздуха и осадков. Через ручьи и небольшие реки вода из шахт и отвалов поступает в Ладожское озеро. В связи с этим детальное изучение химического состава вод является актуальной экологической задачей.
ОБЪЕКТ ИССЛЕДОВАНИЯ
Питкярантский рудный район расположен в юго-восточной части Фенноскандинавского щита, в Карельской зоне Свекокарельской складчатой области. В месте сочленения Свекокарельской складчатой области и Карельского кратона располагается Салминский анортозит-рапакивигранитный батолит, полого погружающийся вдоль своего северо-западного контакта (рис. 1).
Рис. 1.
Карта-схема части Питкярантского рудного района по (Иващенко, Голубев, 2015; Ларин, 2011), с упрощениями и дополнениями. 1 – гнейсограниты куполов (AR2-PR1); 2 – сортавальская серия: амфиболиты, амфиболовые, графитистые и графитсодержащие сланцы, доломитовые и аподоломитовые кальцитовые мраморы и скарны по ним; 3 – ладожская серия: биотит-кварцевые, кварц-полевошпато-биотитовые, местами амфибол- и графитсодержащие сланцы с прослоями роговиков и скарноидов; 4 – биотит-амфиболитовые граниты (граниты рапакиви); 5 – биотитовые крупнозернистые граниты; 6 – скарны, грейзенизированные скарны и низкотемпературные метасоматиты по ним с Fe–Cu–Zn–Sn оруденением; 7 – жилые постройки: г. Питкяранта; 8 – железная дорога; 9 – система р. Ристиоя; 10 – точки пробоотбора: 1 – ручей напротив известковой штольни (выше по течению от “мышьяковых” шахт); мышьяковые шахты: 2, 4 – с поверхности и 3, 5 – с глубины 2 м; 6 – р. Ристиоя (точка сравнения).
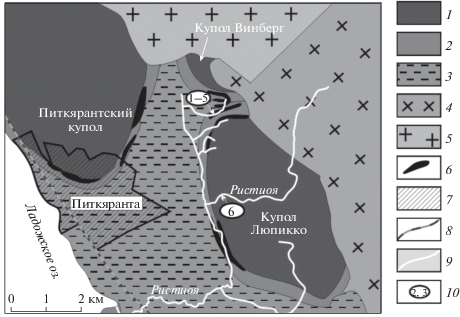
Изученная нами территория локализована в пределах Хопунваарского рудного поля, которое расположено между северной оконечностью гнейсо-гранитного купола Люпикко и южной оконечностью небольшого гнейсо-гранитного купола Винберг, в 4 км к востоку от восточной границы г. Питкяранта. С востока метакарбонатные породы сортавальской серии срезаны гранитами Салминского батолита. Выделяется два метакарбонатных горизонта к которым приурочены месторождения: верхний (Пеллинен-Клара) и нижний (Бек-Коскело). Нижняя метакарбонатная толща непосредственно примыкает к гранитоидам и мигматитам куполовидных выступов архейского фундамента. В верхней метакарбонатной толще расположен известковый карьер и “мышьяковые” шахты, являющиеся предметом нашего внимания (рис. 2). В нашей работе используется наравне с историческим названием шахты “Мышьяковая” название “Мышьяковые” шахты, а также “мышьяковая I и II”, во избежание недоразумений постараемся внести ясность. В работе (Trüstedt, 1907) на плане показана только одна шахта называемая "Мышьяковая", которая совершенно однозначно привязывается на местности, в нашей работе - это шахта I. Шахте “Мышьяковая” В работе (Valkama et al., 2016) соответствует шахта II в данной работе. Вероятно, шахта “Мышьяковая” II появилась позже публикации монографии (Trüstedt, 1907). В связи с их пространственной близостью и схожестью пород мы их объединяем под одним названием.
Рис. 2.
Геологическая карта и схематический разрез по линии A–B по (Trüstedt, 1907), с упрощениями и дополнениями. 1 – биотит-амфиболитовые граниты (граниты рапакиви); 2 – амфиболиты сортавальской серии; 3 – верхний метакарбонатный горизонт сортавальской серии; 4 – зоны скарнирования; 5 – контур известкового карьера на разрезе; 6 – зоны проявления рудной минерализации; 7 – закрытые горные выработки: а – известковая штольня; б – мышьяковая шахта (шахта 1); в – мыщьяковая шахта (шахта 2); 8 – контуры известкового карьера; 9 – ручей; 10 – точки пробоотбора (1–5).
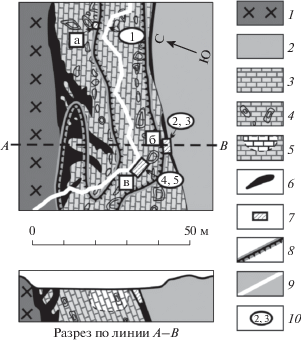
ИСХОДНЫЕ ДАННЫЕ И МЕТОДЫ ИССЛЕДОВАНИЯ
В 2017 и 2018 гг. были осуществлены полевые выезды для взятия образцов воды, а также породы с рудной минерализацией из стенки Мышьяковой шахты I.
Пробы воды
Точки отбора проб указаны на рис. 1 и 2. Для анализа на макрокомпоненты пробы были отобраны в пластиковые бутылки объемом 1 литр с предварительным многократным ополаскиванием тары природной водой. Для анализов методами ICP пробы отбирались в пробирки 15 мл с консервацией 0.45 мл HNO3 ос. ч. Пробы воды были отфильтрованы при помощи фильтр-шприца с мембраной 0.45 мкм. В лабораторию также была сдана холостая проба с 0.45 мл HNO3 ос. ч. При пробоотборе анализировались pH, ${\text{CO}}_{3}^{{2 - }},$ Fe3+. Пробы были доставлены в лабораторию в течение трех дней после пробоотбора и в это время были в темном месте. Общую S определяли методом ICP AES. Концентрации ионов Ca2+, Mg2+, ${\text{SO}}_{4}^{{2 - }},$ Cl–, ${\text{HCO}}_{3}^{ - }$ и величины общей минерализации и перманганатной окисляемости определяли методом титрования. Na+ и K+ определялись потенциометрическим методом ионселективными электродами при помощи прибора ЭКОТЕСТ 2000. Содержания As, Cd, Co, Cr, Cs, Cu, Mn, Ni, Zn определены методом ICP-MS в лаборатории методов исследования и анализа веществ и материалов ГЕОХИ РАН. Сводные данные по химическим анализам проб воды приведены в табл. 1.
Таблица 1.
Химический состав поверхностных вод, отобранных в районе мышьяковой шахты
| Показатели и компоненты | Номера проб | |||||
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | |
| pH | 7.53 | 7.25 | 7.22 | 7.24 | 7.39 | 5.82 |
| Тип воды | HCO3 Mg-Ca | HCO3 Ca-Mg | HCO3 Ca-Mg | HCO3 Mg-Ca | HCO3 Mg-Ca | Cl-HCO3 Ca-Na |
| мг/дм3 | ||||||
| ПО, мгО2/дм3 | 16.56 | 11.20 | 6.32 | 20.13 | 12.68 | 53.09 |
| Минерализация | 226.23 | 287.28 | 420.77 | 140.5 | 175.6 | 44.18 |
| ${\text{HCO}}_{3}^{ - }$ | 147.42 | 211.97 | 314.46 | 86.36 | 111.65 | 15.7 |
| ${\text{SO}}_{4}^{{2 - }}$ | 11.91 | 5.64 | 6.9 | 6.9 | 13.17 | 4.39 |
| Cl– | 9.69 | 6.71 | 6.71 | 8.2 | 6.71 | 8.95 |
| Ca2+ | 32.06 | 29.82 | 42.08 | 19.24 | 22.44 | 3.61 |
| Mg2+ | 10.21 | 24.32 | 34.78 | 7.3 | 9.24 | 0.73 |
| Na+ | 12.77 | 4.1 | 10.56 | 6.91 | 7.08 | 10.59 |
| K+ | 2.17 | 4.72 | 5.28 | 5.59 | 5.31 | 0.21 |
| Fe3+ | 0.6 | 1 | 0.6 | 3.5 | 3.5 | 6.5 |
| мкг/дм3 | ||||||
| As | 0.2 | 37.1 | 89.3 | 2 | 4.5 | 0.4 |
| Cd | 0.06 | 0.04 | 0.04 | 0.09 | 0.13 | 0.03 |
| Co | 0.24 | 0.14 | 0.17 | 0.65 | 0.98 | 0.25 |
| Cr | 0.03 | 0.06 | 0.41 | 0.13 | 0.25 | 0.29 |
| Cs | 0.08 | 0.04 | 0.03 | 0.08 | 0.07 | 0.04 |
| Cu | 3.86 | 0.92 | 0.46 | 7.35 | 5.53 | 1.86 |
| Mn | 35 | 289 | 952 | 176 | 377 | 38 |
| Ni | 0.61 | 0.25 | 0.52 | 1.11 | 0.66 | 0.5 |
| Zn | 6.3 | 9.04 | 10.1 | 12.4 | 16.1 | 6.29 |
Примечания. Номера проб соответствуют обозначениям на рис. 2. Жирным выделены концентрации, превышающие ПДК (Об утверждении…, 2018).
Поверхностные воды изучаемой территории являются преимущественно гидрокарбонатными магниево-кальциевыми или кальциево-магниевыми с минерализацией от 44.18 до 420.77 мг/дм3 (ультра или умеренно пресная по классификации С.Л. Шварцева), по величине pH в основном околонейтральные.
Образцы породы
Во всех месторождениях Хопунваарского рудного поля наблюдаются схожие минеральные ассоциации, различие между ними состоит только в их пропорциях, которые могут широко варьировать даже в пределах одного рудного тела (Valkama et al., 2016). Руды представлены, главным образом развивающимися по метакарбонатам минералами группы серпентина и гумита, магнетитом, сфалеритом, халькопиритом. Выявлены закономерности распределения рудных элементов (Valkama et al., 2016): в верхнем горизонте сосредоточены богатые Cu руды, с высокими содержаниями Ag и As; в нижнем – преимущественно богатые Fe руды.
В отвалах шахты II по данным (Valkama et al., 2016) наблюдаются руды, богатые, главным образом, Fe, Zn, но также найдены и богатые Cu, максимальные содержания компонентов в отобранных пробах достигают: Fe 36.7 мас. %, Cu 15.2 мас. %, Zn 37.9 мас. %, Sn 2.7 мас. %, As 4.23 мас. %, In 605 ppm, Ag 1770 ppm, Bi 1440 ppm.
В коренной стенке шахты I нами был отобран штуф скарнированных мраморов с рудной минерализацией. При изучении макро и микроэлементного состава твердой пробы применены методы XRF (ИГЕМ РАН), ICP-MS (МГУ), а также методы оптической микроскопии и рентгеноспректрального микроанализа для определения минеральных фаз и их состава.
Минеральный состав образца включает в себя силикаты (мусковит, минералы группы гумита, минералы группы серпентина), оксиды (магнетит, гематит, касситерит, цинкит, шеелит), сульфиды и сульфоарсениды (сфалерит, халькопирит, пирит, молибденит, лёллингит), карбонаты (кальцит, доломит, смитсонит), фосфаты (апатит), фториды (флюорит, флюоборит), самородные (висмут, сера). Также обнаружены минералы висмута, но в связи с их незначительными размерами, выделить различные их виды не удалось.
Кроме описанных нами минеральных разновидностей, другие исследователи (Valkaama et al., 2016), также отмечают в отвалах шахты II минералы висмута: эмплектит, виттихенит, висмит, а-рсенопирит. Присутствуют: станноидит, борнит, ковеллин, дигенит, кубанит, алтаит, галенит, гессит, рокезит, а также неизвестная Cu‒Ag–Fe–S фаза.
Термодинамические расчеты
Для расчета форм нахождения металлов в водных растворах база данных Geocheq (Мироненко и др., 2008) была дополнена свободными энергиями образования комплексов металлов с гуминовыми (ГК) и фульвовыми (ФК) кислотами для стандартных условий. Энергии рассчитаны с использованием эффективных констант устойчивости (табл. 2), при этом свободные энергии ГК и ФК приняты равными нулю, а сами ГК и ФК введены в базу данных как новые независимые компоненты. Пересчет данных по перманганатной окисляемости в содержания гуминовых и фульвокислот произведен согласно (Крайнов и др., 1988).
Таблица 2.
Эффективные константы комплексообразования катионов с гуминовыми и фульвокислотами (298.15 К, 1 бар), использованные при расчетах
| Комплексная частица | pK | Литературный источник |
|---|---|---|
| HFu– | 4.8 | Красинцева и др., 1982 |
| CaFu0 | 3.64 | Варшал и др., 1979 |
| CaHum+ | 3.83 | Липатникова, Гричук, 2011 |
| MgFu0 | 3.81 | Mantoura et al., 1978 |
| MgHum+ | 3.67 | Липатникова, Гричук, 2011 |
| MnFu0 | 4.17 | Mantoura et al., 1978 |
| FeFu0 | 4.67 | Варшал и др., 1979 |
| FeFu+ | 7 | Варшал и др., 1975 |
| FeOHFu0 | 19.5 | Липатникова, Гричук, 2011 |
| Fe(OH)2Fu– | 29.41 | Липатникова, Гричук, 2011 |
| CoFu0 | 4.51 | Mantoura et al., 1978 |
| NiFu0 | 4.98 | Mantoura et al., 1978 |
| NiHum+ | 3.67 | Липатникова, Гричук, 2011 |
| CuFu0 | 7.85 | Mantoura et al., 1978 |
| Cu(OH)2Fu2– | 7.74 | Варшал и др., 1983 |
| CuHum+ | 7.8 | Ernst et al., 1975 |
| ZnFu0 | 4.83 | Mantoura et al., 1978 |
| ZnHum+ | 5.19 | Липатникова, Гричук, 2011 |
| CdFu0 | 4.57 | Mantoura et al., 1978 |
| Cr(OH)Fu0 | 6.76 | Кощеева и др., 2007 |
| MnHum+ | 4.58 | Красинцева и др., 1982 |
Для оценки форм нахождения металлов рассчитывался равновесный состав многокомпонентных систем, соответствующих химическому составу изучаемых вод, при стандартных температуре и давлении (298.15 К, 1 бар). Система состояла из 21 независимых компонентов: H, O, C, Ca, Mg, Na, K, S, Cl, Fe, As, Cd, Co, Cr, Cs, Cu, Mn, Ni, Zn, Fu(ФК) и Hum(ГК). В качестве потенциально возможных твердых фаз были приняты: кальцит, доломит, магнетит, пирит, гетит, гематит, магнезит, арсенопирит, лёллингит, халькозин, халькопирит, малахит, Mn2O3, MnO2, аурипигмент, реальгар, родохрозит, сидерит, смитсонит, сфалерит, тенорит. В водном растворе для металлов, помимо свободных катионов и кислород-содержащих анионов, рассматривалась возможность нахождения в виде, гидроксо-, карбонатных, гидрокарбонатных, сульфатных, хлоридных, фульфатных и гуматных комплексов.
РЕЗУЛЬТАТЫ ТЕРМОДИНАМИЧЕСКОГО МОДЕЛИРОВАНИЯ
Для воды пробы 6 рассчитано пересыщение по гетиту и MnO2. В пробах 1–3 выпадают гетит, MnO2 и доломит, а для воды проб 4 и 5 рассчитано насыщение для гетита, MnO2, доломита и тенорита.
Согласно результатам термодинамических расчетов (табл. 3), макрокомпоненты природных вод кальций и магний присутствуют в ионной форме. Их содержания находятся в пределах 96.03–98.70 и 96.37–98.66 мол. % соответственно. Содержание железа в исследованных пробах составляет 0.6–6.5 мг/дм3, что значительно превышает ПДК (0.1 для водоемов рыбохозяйственного значения и 0.3 мг/л для хозяйственно-питьевого) (Об утверждении…, 2018). Самое высокое содержание железа и перманганатная окисляемость наблюдается в воде р. Ристиоя (точка сравнения, вода р. Ристиоя не подвержена влиянию выноса вещества из мышьяковых шахт). Высокая концентрация железа в растворе обусловлена образованием устойчивого комплекса Fe(OH)2Fu– (100 мол. %), который препятствует образованию Fe(OH)3, тем самым увеличивая миграционную способность железа. Практически все содержание фульвокислоты расходуется на образование гидроксофульватного комплекса с железом. Никель, кадмий, кобальт и цезий находятся в воде преимущественно в ионной форме (99.71–99.82 мол. %). Их содержания не превышают ПДК для водоемов рыбохозяйственного значения. Марганец также в основном находится в форме свободного иона (98.87–99.45 мол. %), его концентрации значительно превышают ПДК во всех пробах. Цинк присутствует в виде Zn2+ (27.8–53.46 мол. %) и ZnOH+ (44.86–71.07 мол. %), остальные формы имеют явно подчиненное значение. Превышение ПДК по цинку отмечено в 3–5 пробах, в пробе 2 содержание близко к ПДК. Эти пробы отобраны из шахты (с поверхности и с глубины). В пробах 1 (выше по течению ручья) и 6 (проба сравнения, р. Ристиоя) содержание Zn значительно ниже. Вероятно повышенные концентрации цинка в воде шахт обусловлены взаимодействием со смитсонитом и цинкитом, которые были определены при анализе образца, взятого из стенки шахты. Медь в изученных природных водах района в основном находится в виде CuO (до 91.68 мол. %). В пробах с наибольшим содержанием (3.86–7.35 мкг/дм3) эта тенденция наиболее ярко выражена. Наибольшие концентрации меди, обнаруженные в пробах 4–5 (шахта II), связаны вероятно с взаимодействием воды с халькопиритом. Остальная часть меди находится в гуминовом и гидроксокомплексе, а также в ионной форме. Мышьяк в основном находится в форме ${\text{HAsO}}_{4}^{{2 - }}.$ Наибольшая концентрация мышьяка обнаружена в пробе 3, отобранной в шахте I на глубине 2 м. По-видимому, с глубины около 2 метров в шахте устанавливается застойный режим и растворенный мышьяк не выносится в ручей.
Таблица 3.
Результаты расчетов основных форм миграции химических элементов в природных водах исследуемой территории (мол. %)
| Формы нахождения элементов в растворе | Номера проб | |||||
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | |
| CaCl+ | 0.01 | 0.01 | 0.01 | 0.01 | 0.01 | 0.01 |
| CaCO3,aq | 0.97 | 0.21 | 1.45 | 1.08 | 1.84 | 1.05 |
| ${\text{CaHCO}}_{3}^{ + }$ | 0.84 | 0.39 | 1.03 | 0.89 | 1.16 | 0.88 |
| CaSO4,aq | 1.62 | 0.57 | 1.45 | 0.67 | 0.83 | 0.86 |
| Ca2+ | 96.54 | 98.7 | 96.03 | 97.35 | 96.15 | 97.16 |
| CaHum+ | 0.02 | 0.12 | 0.03 | 0 | 0.01 | 0.04 |
| MgCl+ | 0.01 | 0.02 | 0.02 | 0.01 | 0.01 | 0.02 |
| MgCO3,aq | 0.43 | 0.09 | 0.65 | 0.49 | 0.83 | 0.48 |
| ${\text{MgHCO}}_{3}^{ + }$ | 0.82 | 0.39 | 1.00 | 0.87 | 1.14 | 0.86 |
| MgOH+ | 0.03 | 0.01 | 0.03 | 0.03 | 0.04 | 0.03 |
| MgSO4,aq | 2.12 | 0.75 | 1.91 | 0.88 | 1.10 | 1.13 |
| Mg2+ | 96.57 | 98.66 | 96.37 | 97.72 | 96.87 | 97.46 |
| MgHum+ | 0.02 | 0.08 | 0.02 | 0 | 0.01 | 0.03 |
| Fe(OH)2Fu– | 100 | 100 | 100 | 100 | 100 | 100 |
| MnCl+ | 0.01 | 0.02 | 0.01 | 0.01 | 0.01 | 0.01 |
| Mn2+ | 98.91 | 98.87 | 99.1 | 99.45 | 99.42 | 99.21 |
| ${\text{MnO}}_{4}^{{2 - }}$ | 0.02 | 0 | 0.04 | 0.03 | 0.05 | 0.03 |
| MnOH+ | 0.22 | 0.13 | 0.21 | 0.22 | 0.21 | 0.22 |
| MnSO4,aq | 0.75 | 0.35 | 0.54 | 0.29 | 0.27 | 0.38 |
| MnHum+ | 0.10 | 0.63 | 0.09 | 0 | 0.04 | 0.15 |
| Cu2+ | 3.34 | 5.55 | 2.30 | 3.29 | 1.90 | 2.99 |
| CuO,aq | 84.05 | 29.10 | 87.17 | 91.41 | 91.68 | 81.47 |
| CuOH+ | 5.08 | 3.86 | 4.29 | 5.25 | 4.00 | 4.73 |
| CuHum+ | 7.53 | 61.50 | 6.24 | 0.05 | 2.42 | 10.81 |
| ZnO,aq | 0.67 | 0.21 | 0.87 | 0.71 | 1.01 | 0.70 |
| ${\text{HZnO}}_{2}^{ - }$ | 0.01 | 0 | 0.02 | 0.01 | 0.03 | 0.01 |
| ZnOH+ | 64.21 | 44.86 | 68.60 | 65.46 | 71.07 | 64.98 |
| Zn2+ | 34.91 | 53.46 | 30.30 | 33.80 | 27.80 | 33.99 |
| ZnCl+ | 0.01 | 0.02 | 0.01 | 0.01 | 0.01 | 0.01 |
| ZnHum+ | 0.19 | 1.45 | 0.20 | 0 | 0.09 | 0.30 |
| ${\text{CrO}}_{4}^{{2 - }}$ | 97.46 | 94.62 | 97.93 | 97.59 | 98.15 | 97.56 |
| ${\text{HCrO}}_{4}^{ - }$ | 2.54 | 5.38 | 2.07 | 2.41 | 1.85 | 2.44 |
| ${{{\text{H}}}_{{\text{2}}}}{\text{AsO}}_{4}^{ - }$ | 4.26 | 8.90 | 3.51 | 4.07 | 3.13 | 4.12 |
| ${\text{HAsO}}_{4}^{{2 - }}$ | 95.71 | 91.09 | 96.55 | 95.90 | 96.83 | 95.85 |
| ${\text{AsO}}_{4}^{{3 - }}$ | 0.03 | 0.01 | 0.04 | 0.03 | 0.04 | 0.03 |
| Ni2+ | 99.78 | 99.82 | 99.73 | 99.79 | 99.71 | 99.76 |
| NiOH+ | 0.20 | 0.09 | 0.25 | 0.21 | 0.28 | 0.21 |
| NiHum+ | 0.02 | 0.08 | 0.02 | 0 | 0.01 | 0.03 |
ВЫВОДЫ
Проведенный анализ химического состава отобранных проб воды показал превышения ПДК по железу, марганцу и перманганатной окисляемости, а в пробах воды из мышьяковых шахт – цинка, меди, мышьяка. Изученный минералогический состав пробы породы из стенки Мышьяковой шахты I дает объяснение повышенным концентрациям металлов в шахтной воде: повышенные концентрации цинка обусловлены взаимодействием воды со смитсонитом и цинкитом, меди – с халькопиритом, мышьяка – с арсенопиритом и лёллингитом. Проведенное термодинамическое моделирование показывает, что практически все содержащееся органическое вещество в воде комплексуется с железом, а марганец, никель, кадмий, кобальт, медь, цинк, цезий, хром находятся преимущественно в ионной форме или в неорганических комплексах. Таким образом, можно сделать вывод, что изученный водоток вносит вклад в вынос металлов в воды Ладожского озера из скарнированных пород сортавальской серии. Однако для того, чтобы сделать обоснованное заключение о его значимости, необходимо провести исследование по оценке выщелачивания металлов из пород отвалов и шахт на других рудных объектах данной территории.
Авторы выражают благодарность профессору А.Ю. Бычкову за ценные советы и помощь в проведении исследования.
Список литературы
Варшал Г.М., Инцкирвели И.С., Сироткина И.С., Колосов И.В., Кощеева И.Я. (1975) Об ассоциации фульвокислот в водных растворах. Геохимия. (10), 1581-1585.
Варшал Г.М., Кощеева И.Я., Сироткина И.С., Велюханова Т.К., Инцкирвели Л.Н., Замокина Н.С. (1979) Изучение органических веществ поверхностных вод и их взаимодействие с ионами металлов. Геохимия. (4), 598-607.
Варшал Г.М., Велюханова Т.К., Кощеева И.Я., Дорофеева В.А., Баучидзе Н.С., Касимова О.Г., Махарадзе Г.А. (1983) Изучение химических форм элементов в поверхностных водах. ЖАХ. 38(9), 1590-1600.
Дину М.И. (2015) Взаимодействие ионов металлов в водах с гумусовыми веществами глееподзолистых почв. Геохимия. (3), 276-288.
Dinu M.I. (2015) Interaction between metal ions in waters with humic acids in gley-podzolic soils. Geochem. Int. 53(3), 265-276.
Иващенко В.И., Голубев А.И. (2015) Новые аспекты минералогии и металлогении Питкярантского рудного района. Труды КарНЦ РАН. (7), 127-148.
Кощеева И.Я., Хушвахтова С.Д., Левинский В.В., Данилова В.Н., Холин Ю.В. (2007) О Взаимодействии хрома(III) с гумусовыми веществами почв, вод, донных осадков Геохимия. (2), 208-215.
Koshcheeva I.Y., Khushvakhtova S.D., Levinskii V.V., Danilova V.N., Kholin Y.V. (2007) Interaction of Cr(III) with the humus acids of soil, water, and bottom sediments. Geochem. Int. 45(2), 178-184.
Крайнов С.Р., Шваров Ю.В., Гричук Д.В., Добровольский Е.В., Соломин Г.А., Борисов М.В., Рыженко Б.Н., Матвеева Л.И., Лялько В.И., Швец В.М. (1988) Методы геохимического моделирования и прогнозирования в гидрогеологии. М.: Недра, 254 с.
Красинцева В.В., Гричук Д.В., Романова Г.И., Кадукин А.И. (1982) Процессы миграции и формы нахождения химических элементов в поровых водах донных отложений в Иваньковском водохранилище. Геохимия. (9), 1342-1354.
Ларин А.М. (2011) Граниты рапакиви и ассоциирующие породы. СПб.: Наука, 402 с.
Линник И.А., Набиванец Б.И. (1986) Формы миграции металлов в пресных поверхностных водах. Л.: Гидрометиздат, 272 с.
Липатникова О.А., Гричук Д.В. (2011) Термодинамическое моделирование форм нахождения тяжелых металлов в донных отложения на примере Иваньковского водохранилища. Вестник Московского Университета Серия 4. Геология. (2), 51-59.
Мироненко М.В., Мелихова Т.Ю., Золотов М.Ю., Акинфиев Н.Н. (2008) GEOCHEQ_M – комплекс для термодинамического и кинетического моделирования геохимических процессов. Версия 2008 года. URL: http://www.scgis.ru/russian/cp1251/h_dgggms/1-2008/ informbul-1_2008/mineral-22.pdf. Mironenko M.V., Melikhova T.Yu., Zolotov M.Yu., Akinfiev N.N., 2008. GEOCHEQ_M: Program complex for thermodynamic and kinetic modeling of geochemical processes in rock–water–gas systems. Version 2008. Vestnik Otdelenia Nauk o Zemle RAN. 1(26).
Моисеенко Т.И., Кудрявцева Л.П., Гашкина Н.А. (2006) Рассеянные элементы в поверхностных водах суши: Технофильность, биоаккумуляция и экотоксикология. М.: Наука, 261 с.
Приказ от 13 декабря 2016 г. N 552 “Об утверждении нормативов качества воды водных объектов рыбохозяйственного значения, в том числе нормативов предельно допустимых концентраций вредных веществ в водах водных объектов рыбохозяйственного значения” (с изменениями на 12 октября 2018 г.).
Ernst R., Allen H.E., Mancy K.H. (1975) Characteristic of trace metal species and measurements of trace metal stability constants by electrochemical techniques. Water Res. (6), 969-979.
Mantoura R.F.C., Dickson A., Riley S.P. (1978) The complexation of metals with humic materials in natural waters. Estuar. Coast. Mar. Sci. (6), 387-408.
Trüstedt O. (1907) Die Erzlagerstätten von Pitkäranta am Ladoga-See. Bull Comm Géol Finlande no 19. Helsingfors.
Valkama M., Sundblad K., Cook N.J., Ivashchenko V.I. (2016) Geochemistry and petrology of the indium-bearing polymetallic skarn ores at Pitkäranta, Ladoga Karelia, Russia. Miner Deposita. 51(6), 823-839.
Дополнительные материалы отсутствуют.


