Геохимия, 2021, T. 66, № 5, стр. 450-456
Применение 137Сs при оценке содержания вермикулита в пахотных почвах европейской части РФ
И. В. Коноплева a, *, А. А. Забежайлова b
a Институт геохимии и аналитической химии им. В.И. Вернадского РАН
119991 Москва, ул. Косыгина, 19, Россия
b Всероссийский научно-исследовательский институт радиологии и агроэкологии
249032 Обнинск, Киевское шоссе, 109-й км, Россия
* E-mail: konopleva@geokhi.ru
Поступила в редакцию 06.11.2019
После доработки 04.12.2019
Принята к публикации 24.12.2019
Аннотация
В настоящее время важнейшей особенностью почвообразования является воздействие человека на естественный почвообразовательный процесс. При интенсивном ведении агропроизводства активно протекают процессы выветривания и трансформации глинистых минералов, унаследованных от породы, в которых содержатся основные запасы доступного растениям калия. Надежным диагностическим критерием обеднения почв калием является положительный баланс вермикулита и, поэтому, для регулирования почвенного плодородия необходим мониторинг содержания этого минерала. В настоящей работе предложен простой быстрый количественный метод определения вермикулита в почвах. В основу метода положено свойство селективной адсорбции и фиксации ионов Cs+ глинистыми минералами с кристаллической решеткой типа 2:1. Процедура включает в себя процесс насыщения почвенного обменного комплекса ионами Cs+, меченного радиоизотопом. Для этого образец почвы подвергается промыванию раствором СsCl, содержащим в качестве метки 137Сs в следовой концентрации. После высушивания образца в печи при 110°С, приводящего к фиксации в кристаллической решетке части Сs+, обменный Cs+ замещается на ионы ${\text{NH}}_{{\text{4}}}^{ + }.$ Активность фиксированного 137Сs определяется методом гамма-спектрометрии. С учетом известного соотношения изотопов Cs+/137Сs, содержание вермикулита рассчитывается из отношения количества фиксированного Cs+ к внутрислоевой обменной емкости вермикулита, принятой равной 154 мг-экв/100 г. Методом фиксации Cs, меченного 137Cs, проведено определение содержания вермикулита в образцах пахотных почв, отобранных в различных климатических зонах европейской части РФ. В ряду исследованных почв наименьшее содержание вермикулита наблюдалось в дерново-подзолистой почве (2.3 г/кг), наибольшее – в черноземах (26.9–28.6 г/кг). Показано, что вермикулит присутствует и в крупнодисперсных фракциях почв (с размером частиц >1 мкм). Среди всех образцов почв наибольшее содержание вермикулита в крупных фракциях обнаружено в песчаной дерново-подзолистой почве (20.8% от общего содержания), в суглинистых и глинистых почвах эта величина варьирует в пределах 2.1–5.4.0%.
ВВЕДЕНИЕ
Современное сельскохозяйственное использование почв приводит к существенным изменениям их состава и свойств. При интенсивном ведении традиционного агропроизводства, а также при биоорганическом земледелии активно протекают процессы выветривания и трансформации минералов илистой фракции, что приводит к деградации почв. Наиболее широко распространенным в почвах процессом трансформационных изменений является превращение слюд в лабильные минералы. Примером деградации может служить ряд превращений глинистых минералов с кристаллической решеткой 2 : 1: иллит → смешаннослойный иллит-вермикулит → вермикулит → → монтмориллонит.
Иллит и продукты его выветривания представляют собой слоистые силикаты, образованные слоями кремнекислородных тетраэдров и алюмогидроксильных октаэдров, и имеющих в кристаллической решетке изоморфные замещения катионов Si4+ и Al3+ на катионы меньшего заряда. В результате такого замещения внутри решетки формируется отрицательный заряд, компенсирующийся ионами K+ (частично ${\text{NH}}_{{\text{4}}}^{ + }$), расположенными в гексагональных пустотах тетраэдрических слоев двух смежных пакетов. В результате между пакетами возникает весьма прочная связь. Однако, благодаря процессам выветривания (вымывания), решетка глинистого минерала теряет межслоевой K+ на концах слоев. Выход K+ из межпакетного пространства приводит к появлению отрицательного поверхностного заряда, взаимному отталкиванию и расширению 2-х соседних слоев на их концах (Jackson, 1963). Сорбционные места, расположенные на расширенных краевых участках межпакетных пространств слоистых глинистых минералов, характеризуются высокой селективностью по отношению к K+, ${\text{NH}}_{{\text{4}}}^{ + },$ Rb+ и, в особенности, Сs+ (Brouwer et al., 1983). Эти ионы, имеющие низкие энергии гидратации и маленький гидратированный радиус легко проникают в расширенные концы слоев минералов, легко теряют гидратационную воду и адсорбируются на расположенных там селективных сорбционных местах. Если достаточное количество ионов адсорбируется на селективных местах клиновидной зоны, заряд внутренних поверхностей нейтрализуется, снижая силы отталкивания между расширенными слоями минерала. Селективная адсорбция дегидратированного катиона индуцирует схлопывание (коллапс) соседних слоев и фиксирует этот катион внутри близкой по размеру гексагональной полости базальной кислородной плоскости кристаллической решетки (Page, Baver, 1940; Sawhney, 1972). Радиус этих полостей составляет около 1.4 Å. Почти такой же радиус имеет ионы ${\text{NH}}_{{\text{4}}}^{ + }$ (1.43 Å) и K+ (1.33 Å). Катионы несколько большего размера, Cs+ (1.69 Å) и Rb+ (1.48 Å), как полагают, “впрессовываются” в гексагональные пустоты в результате поляризации электронной оболочки (Van der Marel, 1954). Ионы Cs+ и Rb+, имеющие более низкую энергию гидратации, чем K+ (Некрасов, 1973), адсорбируются и фиксируются сильнее. Однозарядные катионы, характеризующиеся низкой энергией гидратации, K+, ${\text{NH}}_{{\text{4}}}^{ + },$ Rb+, Cs+ вызывают межслойный коллапс и фиксацию. Заряд слоя минерала также влияет на степень катионной фиксации. Энергия взаимодействия катиона, помещенного в гексагональную полость с отрицательными зарядами решетки, зависит от местонахождения зарядов. Заряды тетраэдрического слоя, находящиеся ближе к катиону в гексагональной плоскости, чем заряды октаэдрического слоя, взаимодействуют с катионом сильнее (Bouabid et al., 1991). В соответствии с этим наибольшая фиксация наблюдается у иллита, имеющего наибольшую степень замещения в тетраэдрическом слое (De Koning et al., 2007). Меньшая степень фиксации н-аблюдается у монтмориллонита, у которого изоморфное замещение в большей степени происходит в октаэдрическом слое (Šucha, Širáńová, 1991; Feng et al., 2003; Ohnuki, Kozai, 2013). Вермикулит занимает промежуточное положение.
Вермикулит и монтмориллонит относятся к лабильным силикатам. Особенностью их кристаллической структуры является то, что при увлажнении в их межпакетные пространства может входить вода, вызывая их расширение (с 10 до 15–21 Å) и в них проникают ионы K+. В межпакетном пространстве катионы K+ лишаются гидратной оболочки и занимают гексагональные ячейки кремнекислородных тетраэдров и благодаря электростатическому взаимодействию с атомами кислорода, стягивают пакеты, что приводит к построению иллит-подобной структуры. Особенностью структуры вермикулита является то, что фиксация однозарядных слабогидратированных катионов встречается как в межслоевом пространстве, так и на краевых расширенных концах (Fan et al., 2014).
Таким образом, области в кристаллической структуре слоистых глинистых минералов, в которых возможна фиксация однозарядных катионов, можно назвать “вермикулитовыми местами”.
Присутствие иллита и продуктов его выветривания в составе минеральной фракции почв приводит к тому, что часть вносимого в почву с удобрениями калия оказывается прочно связанным в его кристаллической решетке (Ross et al., 1985; Simonsson et al., 2007).
Естественные природные процессы увлажнения-высушивания способствуют усилению фиксации (Badraouri, Bloom, 1989). Фиксация носит обратимый характер. Интенсивное орошение и корневое поглощение сельскохозяйственных растений приводит к удалению калия из почвенного раствора и в результате ремобилизации (процесса обратного фиксации) калий из необменных мест переходит в обменную и водорастворимую формы (Rahmatullah et al., 1994). Длительное потребление межпакетного калия при его дефицитном балансе в агроценозе приводит к значительному изменению состава, а, следовательно, и свойств почвенных минералов (Møberg, Nilson, 1983; Hartemink, 1997; Simonsson et al., 2009).
При интенсивном ведении агропроизводства для стабилизации калийного режима и обеспечения сбалансированного минерального питания сельскохозяйственных растений возникает задача контроля степени выветривания глинистых минералов. Надежным диагностическим критерием обеднения почв калием является положительный баланс “вермикулитовых мест”.
Способы определения вермикулита в глинах и почвах
Под вермикулитом подразумеваются “вермикулитовые места”, расположенные в расширенных краевых участках межпакетных пространств и внутри кристаллической решетки слоистых глинистых минералов.
Известен рентгенодифракционный способ определения глинистых минералов в почвах (Moore, Reynolds, 1997; Соколова и др., 2005). Анализ проводят в илистой фракции, которую выделяют из почвы методом седиментации. Далее из образца удаляют карбонаты, ионы Са2+ и Mg2+. Для разрушения органического вещества (ОВ) образец илистой фракции обрабатывают Н2О2, а затем помещают в диализные ячейки, где одну часть насыщают ионами K+, вторую – ионами Mg2+. Проводят рентген-дифрактометрическую съемку образцов в исходном состоянии и после 2-часового прокаливания при 350°C. Для проведения анализа пробу, насыщенную глицерином, помещают на пути монохроматического рентгеновского луча, а затем измеряют интенсивность излучения, отраженного под разными углами. Для расшифровки рентген-дифрактограмм используют специальные таблицы.
Недостатком способа рентгеновской дифракции является: 1) длительность процесса; 2) неполное измерение вермикулитовых мест, поскольку исключается минеральная фракция больших по размеру частиц (>1 мкм), которые также содержат сорбционные места; 3) затруднено измерение вермикулитовых мест в смешаннослойных структурах.
В работе (Alexiades, Jackson, 1965) был впервые предложен количественный метод определения глинистого минерала, основанный на свойстве вермикулита фиксировать K+ в кристаллической решетке. В этом методе количество вермикулита в илистой фракции почв рассчитывают как разность между емкостью катионного обмена (ЕКО) образца, насыщенного Са2+(Са2+ЕКО) и емкостью катионного обмена образца, насыщенного K+(K+ ЕКО), после его нагревания при 110°С. Для насыщения образцов используют раствор 0.5 н CaОАс и 0.5 н KОАс, для вымывания обменного Са2+-раствор 1 н MgОАс, обменного К+- 1 н раствор NH4ОАс (рН 7). Содержание избыточных катионов Са2+ и K+ в растворах определяют методом атомно-абсорбционной спектрофотометрии.
Расчет процентного содержания вермикулита (Vr) основан на разнице Са2+ и K+ емкости катионного обмена (выраженной в мг-экв/100 г) и внутрислоевой обменной емкости вермикулита, принятой равной 154 мг-экв/100 г:
(1)
${\text{\% \;}}Vr = \frac{{{\text{С}}{{{\text{а}}}^{{2 + }}}{\text{ЕКО}} - {{{\text{К}}}^{ + }}{\text{ЕКО}}}}{{154}} \times 100.$Недостатком метода является длительность процесса, занимающего недели времени за счет предварительной подготовки образца: удаления ОВ химическим окислением с последующим фракционированием частиц и выделением илистой фракции.
В работе (Coffman, Fanning, 1974) метод K+-фиксации был применен для определения вермикулита во всей почве. Предложенная модификация позволила сократить время анализа. Было показано, что органическое вещество и гидроксиды железа, присутствующие в почве, не влияют на результат. В работе была выявлена необходимость проводить анализ не только ила почв, но и крупных фракций, так как в минералах этих фракций также были обнаружены вермикулитовые места. Недостатком этого метода, как и предыдущего, является то, что результат рассчитывают как разницу измерений двух больших величин, что снижает точность определения.
Известен метод определения содержания вермикулита в почве, включающий процесс насыщения почвенного обменного комплекса ионами Rb+ (Ross еt al., 1989). Сущность метода состоит в процедуре фиксации Rb+, когда обменный Rb+ из образца глинистой фракции почвы, насыщенного Rb+ и подвергнутого нагреванию, вымывается ионами ${\text{NH}}_{{\text{4}}}^{ + }.$ Образец растворяют смесью HNO3–HF–HClO4 и фиксированный Rb+ определяется методом атомно-абсорбционной спектрофотометрии. Так как Rb+ определяется непосредственно в пробе, метод является более точным по сравнению со способами, основанными на фиксации K+. Метод включает в себя предварительную подготовку почвы: удаление органического вещества посредством NaOCl и разделение минеральной составляющей по фракциям методом седиментации. Анализ проводят в илистой фракции (<2 мкм). Недостатком метода является неполное измерение вермикулитовых мест, поскольку исключается минеральная фракция больших по размеру частиц (>2 мкм), которые также содержат сорбционные места, способные фиксировать однозарядные катионы внутри кристаллической решетки. Способ является многостадийным и включает длительные по времени операции выделения илистой фракции.
Целью настоящей работы была разработка более точного, несложного в исполнении и ускоренного количественного метода определения вермикулита в почве. Под вермикулитом в настоящей работе подразумеваются “вермикулитовые места” в концевых клиновидных областях межпакетных пространств иллит-подобных структур и внутри кристаллической решетки вермикулита, высокозарядного монтмориллонита и смешаннослойных структур, попадая в которые калий переходит в необменное (фиксированное) состояние в результате коллапса.
МАТЕРИАЛЫ И МЕТОДЫ
Для проведения исследования были выбраны образцы из коллекции зональных пахотных почв европейской части РФ, куда входили почвы различного генезиса и гранулометрического состава. Образцы почв были отобраны из верхнего пахотного горизонта глубиной до 20 см. Из почв предварительно механическим путем удаляли неразложившиеся органические остатки. Почвы высушивали при комнатной температуре до воздушно-сухого состояния, размалывали и просеивали через сито с диаметром отверстий 2 мм.
Физико-химический анализ проводили согласно общепринятым методикам химического анализа (Аринушкина, 1970): рН – потенциометрически, органическое вещество (гумус) – методом мокрого озоления смесью K2Cr2O7 и H2SO4. Обменные катионы почв определялись в экстрактах 1 М NH4ОAc методом атомно-абсорбционной спектрофотометрии при соотношении твердой и жидкой фаз 1 : 10.
Из почв была выделена илистая фракция (<1 мкм) седиментационным методом (Практикум по почвоведению, 1980). Минералогический состав ила исследовали методом рентген-дифрактометрии. Экспериментальные условия анализа описаны в работе Соколовой с соавторами, 2010.
Определение содержания вермикулита в почвах методом фиксации Cs, меченного 137Cs. Метод основан на свойстве селективной адсорбции и фиксации глинистыми минералами типа 2 : 1 ионов Cs+ и применен для цельных почв, без разделения на гранулометрические фракции. В методе также может быть использован радиоизотоп 134Cs.
Образец почвы (~1 г) подвергали 3-х кратному промыванию 10 мл 0.5 М раствора СsCl, содержащим в качестве метки 137Сs. Удельная активность раствора промывки СsCl составляла ≈800 МБк/л. Образец почвы помещали в центрифужную пробирку, заливали 10 мл 0.5 М раствора СsCl, меченного 137Сs, оставляли на 15–30 мин, периодически перемешивая. Разделение фаз проводили центрифугированием. Образец выдерживали в течение ночи в печи при 110°С. После высушивания образца обменный Cs+ замещали на ионы ${\text{NH}}_{{\text{4}}}^{ + }$ 4-х кратным промыванием 10 мл 1 М раствором NH4ОАс. Активность фиксированного в кристаллической решетке 137Сs определяли гамма-спектрометрическим методом, используя HPGe детектор GEM-1200 с многоканальным анализатором спектра IN-1200. С учетом известного соотношения стабильного и радиоактивного изотопов Cs+, содержание вермикулита рассчитывается из отношения количества фиксированного Cs+ (мг-экв/100 г) к внутрислоевой обменной емкости вермикулита. Формула расчета выглядит как: [Vr] г/кг почвы = [Cs]/0. 154.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Почвы, отобранные для исследования, характеризуются высокой вариабельностью почвенных свойств: рН, содержания обменных катионов K+ и Са2+, емкости катионного обмена, содержания органического вещества (табл. 1 ). На юге лесной зоны европейской части РФ наиболее распространены дерново-подзолистые почвы. Они характеризуются низким рН, малым содержанием гумуса и ила, низким значением ЕКО. Светло-серые лесные почвы сформированы в лесостепной зоне, почвообразующими породами служат преимущественно покровные лёссовидные суглинки. Почвы морфологически близки к дерново-подзолистым, также имеют кислую реакцию (рН 5.4), обеднены органическим веществом и илистой фракцией. Черноземы распространены в степной и лесостепной зоне суббореального пояса, сформированы на лёссах и лёссовидных суглинках. Характеризуются большими запасами ОВ, минералогический состав обогащен тонкой дисперсной фракцией. Каштановые почвы формируются в аридном климате степей на лёссовидных карбонатных суглинках, имеют относительно низкое содержание ОВ (в сравнении с черноземами), щелочную реакцию (рН 7.4), обогащены илистой фракцией.
Таблица 1.
Классификация, место отбора и физико-химические характеристики почв
| Образец почвы | Тип, подтип почвы, место отбора | Гранулометри-ческий состав | рНKCl | Илистая фракция, % | ОВ, % |
Обменные катионы | ЕКО | |||
|---|---|---|---|---|---|---|---|---|---|---|
| K | Ca | Mg | Нг | |||||||
| мг-экв /100 г | ||||||||||
| Sp | Дерново-подзолистая (Брянская обл.) |
Песчаная | 5.8 | 3.6 | 1.8 | 0.37 | 4.8 | 1.3 | 2.96 | 9.4 |
| Lgf | Светло-серая лесная (Орловская обл.) |
Легкосуглинистая | 5.4 | 14.0 | 0.6 | 0.45 | 5.2 | 1.2 | 2.30 | 9.2 |
| LchK | Выщелоченный чернозем (Курская обл.) |
Среднесуглинистая | 5.5 | 18.5 | 2.1 | 0.51 | 23.3 | 3.7 | 4.85 | 32.4 |
| LchT | Выщелоченный чернозем (Тульская обл.) |
Среднесуглинистая | 5.6 | 18.9 | 1.6 | 0.37 | 22.5 | 4.2 | 2.88 | 30.0 |
| Pch | Оподзоленный чернозем (Курская обл.) |
Среднесуглинистая | 6.9 | 21.2 | 1.6 | 0.46 | 28.7 | 2.0 | 0.64 | 31.8 |
| Och | Обычный чернозем (Воронежская обл.) |
Глинистая | 6.0 | 29.6 | 2.8 | 0.66 | 26.6 | 5.4 | 3.53 | 36.2 |
| Tch | Типичный чернозем (Воронежская обл.) |
Глинистая | 6.2 | 35.9 | 2.8 | 0.76 | 28.4 | 4.7 | 2.96 | 36.8 |
| Chn | Каштановая (Ростовская обл.) |
Глинистая | 7.4 | 30.7 | 1.8 | 1.04 | 24.9 | 6.2 | 0.29 | 32.4 |
Содержание ила обычно колеблется от нескольких процентов в почвах легкого гранулометрического состава до 20–40% в суглинистых и глинистых почвах. В ряду исследованных почв содержание илистой фракции изменялось от 3.6% в дерново-подзолистой почве до 35.9% в типичном черноземе.
Результаты рентгенодифракционного анализа показали, что иллит является преобладающим минералом тонкодисперсной фракции во всех изученных образцах почв (табл. 2 ). Доля иллита в составе илистой фракции варьировала от 48 до 59%, доля лабильных минералов менялась в пределах 22–31%. Лабильные минералы не регистрировались в виде индивидуальных фаз и представлены пакетами смешаннослойных структур: иллит-монтмориллонитовых или иллит-вермикулитовых образований.
Таблица 2.
Минералогический состав илистой фракции почв
| Образец почвы | Каолинит + хлорит | Иллит | Лабильные силикаты |
|---|---|---|---|
| % от суммы трех компонентов в иле | |||
| Sp | Не опр | Не опр | Не опр |
| Lgf | 23 | 55 | 22 |
| LchK | 18 | 59 | 23 |
| LchT | 20 | 49 | 31 |
| Pch | 19 | 55 | 26 |
| Och | 15 | 57 | 28 |
| Tch | 18 | 51 | 31 |
| Chn | 22 | 48 | 30 |
Результаты определения вермикулита в почвах методом фиксации Cs, меченного 137Cs, представлены в табл. 3 . В ряду исследованных почв наименьшее содержание вермикулита наблюдалось в дерново-подзолистой почве (2.3 г/кг), а в черноземах различных подтипов количество этого минерала изменялось от 16.8 до 28.6 г/кг.
Таблица 3.
Содержание вермикулита в почве и крупных фракциях почв (с размером частиц от 1 до 2000 мкм)
| Образец почвы | Содержание вермикулита*, г/кг | Содержание вермикулита в крупных фракциях почв, f %** |
|---|---|---|
| Sp | 2.3 | 20.8 |
| Lgf | 7.0 | 5.4 |
| LchK | 21.2 | 4.0 |
| LchT | 16.8 | 4.0 |
| Pch | 17.8 | 3.5 |
| Och | 28.6 | 2.5 |
| Tch | 26.9 | 2.1 |
| Chn | 20.3 | 2.4 |
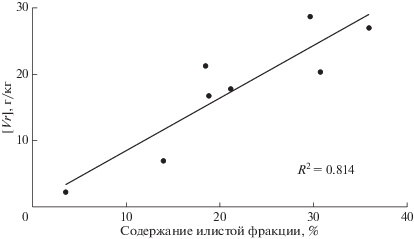
Уместно предположить, что количество вермикулита в почвах тесно связано с содержанием в ней минеральной тонкодисперсной фракции. Для проверки этой связи был проведен анализ данных, который выявил достоверную положительную корреляцию между количеством вермикулита в почве и содержанием в ней илистой фракции (r = 0.902, р < 0.05, рис. 1). Уравнение корреляции имеет следующий вид:
где: [Vr] – содержание вермикулита, [Clay] – % содержание илистой фракции в почве. Корреляционное уравнение (2) позволяет рассчитать содержание вермикулита в составе крупнодисперсной фракции почв (с размером частиц от 1 до 2000 мкм). Эта величина выражена отношением свободного члена к произведению коэффициента уравнения корреляции и % содержания илистой фракции в почве.Расчеты показали, что относительное содержание вермикулита в крупнодисперсных фракциях среднесуглинистых и глинистых почв (черноземов и каштановой) было незначительным и варьировало в пределах 2.1–4.0% (табл. 3 ). В легкосуглинистой почве (светло-серой лесной) эта величина составляла 5.4%. Доля вермикулита в крупных фракциях песчаной почвы (дерново-подзолистой) была более существенной и составляла 20.8% от его общего содержания в почве. Очевидно, что присутствие вермикулита в крупнодисперсных фракциях дерново-подзолистых, и близких к ним по гранулометрическому составу, почв необходимо учитывать при его количественном определении.
Предложенный метод позволяет вести контроль степени выветривания слоистых глинистых минералов почв в процессе агропроизводства. По содержанию вермикулита может быть проведена оценка калийных запасов пахотных почв, что дает возможность рассчитать оптимальные дозы и сроки внесения калийных удобрений. Такие расчеты наиболее актуальны для легких по гранулометрическому составу почв с низким содержанием органического вещества, на которых наблюдается значительный вынос калия урожаем сельскохозяйственных растений и вымывание с инфильтрационными водами.
ЗАКЛЮЧЕНИЕ
Предложен новый способ оценки содержания вермикулита в почвах методом фиксации Cs+, меченного 137Cs. Преимущество предлагаемого метода по сравнению с описанными в литературе: 1) значительное снижение времени и трудоемкости процесса, 2) повышение точности определения за счет того, что анализ проводится в цельной почве, тем самым учитывается вклад крупнодисперсных фракций, где также присутствуют “вермикулитовые места”.
Проведено определение содержания вермикулита в образцах пахотных почв, отобранных в различных климатических зонах европейской части РФ. Показано, что доля вермикулита в крупных фракциях песчаной дерново-подзолистой почвы составляет 20.8% от его общего содержания, а в суглинистых и глинистых почвах варьирует в пределах 2.1–5.4%.
Метод позволяет вести мониторинг изменения состава глинистых минералов почв в результате естественного и антропогенного воздействия.
Авторы выражают благодарность д. б. н. Н.И. Санжаровой за предоставленные образцы почв и полезные обсуждения, д. б. н. Т.А. Соколовой и сотрудникам кафедры химии почв факультета почвоведения МГУ им. Ломоносова за проведение минералогического анализа образцов.
Список литературы
Аринушкина Е.В. (1970) Руководство по химическому анализу почв. М.: MГУ, 488 с.
Некрасов Б.В. (1973) Основы общей химии. Т.I. М.: Химия, 210 с.
Практикум по почвоведению (под ред. И.С. Кауричева) (1980) М.: Колос, 273 с.
Соколова Т.А., Дронова Т.Я., Толпешта И.И. (2005) Глинистые минералы в почвах. Тула: Гриф и К, 336 с.
Соколова Т.А., Зайдельман Ф.Р., Гинзбург Т.М. (2010) Состав глинистых минералов черноземовидных почв мезопонижений севера лесостепи Европейской России. Почвоведение. (1), 87-96.
Alexiades C.A., Jackson M.L. (1965) Quantitative determination of vermiculite in soils. Soil Sci. Soc. Am. Proc. 29, 522-527.
Badraouri M., Bloom P.R. (1989) The effects of wetting and drying cycles, temperature and extracting solutions on measured potassium fixation in soils of two regions of Morocco. Comm. in Soil Sci. and Plant Anal. 20(13–14), 1353-1375.
Bouabid R., Badraoui M., Bloom P.R. (1991) Potassium fixation and charge characteristics of soil clays. Soil. Sci. Soc. Am. J. 55, 1493-1498.
Brouwer E., Baeyens B., Maes A., Cremers A. (1983) Cesium and rubidium ion equilibria in illite clay. J. Phys. Chem. 87, 1213-1219.
Coffman C.B., Fanning D.S. (1974) ‘Vermiculite’ determination on whole soils by cation exchange capacity methods. Clay and Clay Miner. 22, 271-283.
De Koning A., Konoplev A.V., Comans R.N.J. (2007) Measuring the specific caesium sorption capacity of soils, sediments and clay minerals. Appl. Geochem. 22(1), 219-229.
Fan Q., Yamaguchi N., Tanaka M., Tsukada H., Takahashi Y. (2014) Relationship between the adsorption species of cesium and radiocesium interception potential in soil sand minerals: an EXAFS study. J. Environ. Radioact. 138, 92-100. https://doi.org/10.1016/j.jenvrad.2014.08.009
Feng K., Wang X.L., Wnag X.Z., Tang Y. (2003) Relationship between 2 : 1 mineral structure and the fixation and release of cations. Pedosphere. 13, 81-86.
Hartemink A.E. (1997) Soil fertility decline in some major soil groupings under permanent cropping in Tanga Region, Tanzania. Geoderma. 15, 215-229.
Jackson M.L. (1963) Interlayering of expansible layer silicates in soils by chemical weathering. Clays and Clay Miner. 11, 29-46.
Moore D.M., Reynolds R.C. (1997) X-ray diffraction and identification and analysis of clay minerals. Oxford, N.Y.: Oxford University Press. 378 p.
Møberg J.P., Nilson J.D. (1983) Mineralogical changes in soils used for potassium-depletion experiments for some years in pots and in field. Acta Agric. Scand. 33, 21-27.
Ohnuki T., Kozai N. (2013) Adsorption behavior of radioactive cesium by non-mica minerals. J. Nucl. Sci. Technol. 50, 369-375.
Page Y.B., Baver L.D. (1940) Ionic size in relation to fixations by colloidal clay. Soil Sci. Soc. Am. Proc. 4(2), 150-160.
Rahmatullah B., Shaikh Z., Gill M.A., Salim M. (1994) Bioavailable potassium in riverbed sediments and release of interlayer potassium in irrigated arid soils. Soil Use and Manag. 10, 43-46.
Ross G.J., Phillips P.A., Culley J.L.R. (1985) Transformation of vermiculite to pedogenic mica by fixation of potassium and ammonium in a six-year field manure application experiment. Can. J. Soil Sci. 65, 599-603.
Ross G.J., Schuppli P.A., Wang C. (1989) Quantitative determination of vermiculite by a Rubidium fixation method. Soil Sci. Soc. Am. J. 53, 1588-1589.
Sawhney B.L. (1972) Selective sorption and fixation of cations by clay minerals: a review. Clays and Clay Miner. 20, 93-100.
Simonsson M., Andersson S., Andrist-Rangel Y., Hillier S., Mattsson L., Öborn I. (2007) Potassium release and fixation as a function of fertilizer application rate and soil parent material. Geoderma. 140, 188-198.
Simonsson M., Hillier S., Öborn I. (2009) Changes in clay minerals and potassium fixation capacity as a result of release and fixation of potassium in long-term field experiments. Geoderma. 151, 109-120. https://doi.org/10.1016/j.geoderma.2009.03.018
Šucha V., Širáńová V. (1991) Ammonium and potassium fixation in smectite by wetting and drying. Clays and Clay Miner. 39, 556-559.
Van der Marel. H.W. (1954) Potassium fixation in Dutch soils: mineralogical analyses. Soil Sci. 78(3), 163-166.
Дополнительные материалы отсутствуют.