Геохимия, 2022, T. 67, № 5, стр. 494-500
Применение in situ методов эксперимента для изучения полей стабильности водород-содержащих фаз при высоких давлениях
Н. В. Черткова a, *, Ю. А. Литвин a, **, В. С. Ефимченко b, А. В. Спивак a, Е. С. Захарченко a, b, О. Г. Сафонов a, К. П. Мелетов a, b, А. И. Бурова a, c
a Институт экспериментальной минералогии им. Д.С. Коржинского РАН
142432 Московская обл, Черноголовка, ул. Академ. Осипьяна, 4, Россия
b Институт физики твердого тела РАН
142432 Черноголовка, ул. Академ. Осипьяна, 2, Россия
c Московский государственный университет им. М.В. Ломоносова, Геологический факультет
119991 Москва, Ленинские горы, Россия
* E-mail: nadezda@iem.ac.ru
** E-mail: litvin@iem.ac.ru
Поступила в редакцию 14.02.2021
После доработки 05.06.2021
Принята к публикации 05.06.2021
- EDN: XGOLNJ
- DOI: 10.31857/S0016752522050041
Аннотация
Разработана и испытана методика генерирования молекулярного водорода при термическом разложении борана аммиака BH3NH3 в рабочем объеме ячейки высокого давления с алмазными наковальнями и внешним резистивным нагревом. Диссоциация борана аммиака с выделением молекулярного Н2 исследована в диапазоне давлений 2–5 ГПа при нагреве до температур выше 198°С в присутствии SiO2. В интервале температур 25–250°С сохраняется постоянный оптический доступ к исследуемым водородсодержащим веществам, обеспечивая идентификацию и определение свойств фаз in situ. Разработанный метод перспективен для проведения исследований водородсодержащих систем коры и мантии Земли в восстановительных условиях.
ВВЕДЕНИЕ
Водород является одним из ключевых компонентов флюидных систем глубинных оболочек Земли и принимает активное участие в процессах глобальной мантийной конвекции и геохимической эволюции. Наряду с кислородом, он определяет окислительно-восстановительные условия образования минералов и пород, причем роль водорода возрастает с глубиной при переходе от относительно окислительных условий (буфер фаялит-магнетит-кварц) в самых верхних слоях мантии до восстановительных (буфер железо-вюстит) на глубинах свыше 200 км (Frost, McCammon, 2008). При взаимодействии водорода с минералами группы оливина при давлениях ~10 ГПа и температурах до ~1000°С происходит распад последних на ряд различных летучих (SiH4, H2O) и твердых соединений (MgO, Fe, FeH, FeSiO3) (Shinozaki et al., 2013; Efimchenko et al., 2019, 2021), что говорит о важности учета влияния водорода на высокобарные фазовые ассоциации. Кроме того, водород может входить в состав полиморфов оливина – вадслеита и рингвудита, устойчивых при высоких давлениях (Kohlstedt et al., 1996; Litasov et al., 2011; Mrosko et al., 2013). Таким образом, изучение полей стабильности водородсодержащих фаз при Р-Т параметрах нижних горизонтов коры и мантии Земли является актуальной экспериментальной задачей, направленной на раскрытие физико-геохимических условий вхождения водорода как в состав глубинных флюидных фаз, так и в структуры мантийных минералов.
Экспериментальные исследования в данном направлении требуют создания специализированной аппаратуры высоких давлений и температуры с внутренним источником элементарного водорода. В этом отношении особый интерес представляет твердый боран аммиака (амминоборан) BH3NH3, который был впервые испытан Антоновым с соавторами (Antonov et al., 2017) как эффективный источник водорода. Эксперименты проводили методом закалки в твердофазовой аппаратуре высоких давлений и температур типа “тороид” с внутренним резистивным нагревом (Khvostantsev et al., 2004). Использование амминоборана как источника водорода позволило впервые синтезировать сверхпроводящий гидрид лантана с рекордно высокой критической температурой Тс = 250 К (Drozdov et al., 2019).
Условия стабильности BH3NH3 в системах с силикатными компонентами детально не исследовались, тогда как его фазовое состояние изучалось при давлениях до 16 ГПа (например, Andersson et al., 2011; Lin, Mao, 2014), а кривые диссоциации при высоких давлениях описаны в ряде работ (Стороженко и др., 2005; Nylén et al., 2009). Реакции термического диспропорционирования борана аммиака многоступенчатые с образованием промежуточных продуктов (Стороженко и др., 2005). При температурах ниже 300°С разложение с выделением молекулярного водорода не является полным и сопровождается образованием соединений (BH2NH2)x и (BNHy)x (y < 0.5) (Nylén et al., 2009). Важное значение имеют экспериментальные данные о полном разложении борана аммиака на молекулярный водород H2 и аморфизованный нитрид бора BN в интервале 300–800°С до 8 ГПа, полученные в твердофазовом аппарате типа “тороид” методом закалки (Шолин, 2020). Отличаясь высокой химической инертностью и термоустойчивостью, BN состоит из легких элементов и в рентгеноструктурных исследованиях не вносит искажения в рентгенограммы изучаемых кристаллических материалов.
Целями данной работы являются разработка и применение in situ методов исследования сильно сжатого вещества в ячейке с алмазными наковальнями и внешним резистивным нагревом (с внутренним источником элементарного водорода) для определения полей стабильности и составов водородсодержащих кристаллических и флюидных фаз при высоких давлениях. При внешнем нагреве оптический доступ к образцу сохраняется вплоть до максимальных температур, что дает возможность проводить спектроскопический анализ сосуществующих фаз непосредственно во время эксперимента. Разработанная методика впервые применена для исследования условий диссоциации борана аммиака в системе с силикатным компонентом (BH3NH3–SiO2) в диапазоне давлений 2–5 ГПа и температур 25–250°С.
ЭКСПЕРИМЕНТАЛЬНЫЕ МЕТОДЫ
Экспериментальные исследования выполнялись в аппарате высоких давлений и температур с алмазными наковальнями и системой внешнего резистивного нагрева (Черткова и др., 2021), с использованием вспомогательного технологического оборудования и измерительных приборов, в лаборатории мантии Института экспериментальной минералогии им. Д.С. Коржинского РАН.
Регулировка усилия на алмазные наковальни ячейки типа “поршень-цилиндр” осуществляется посредством винтового механизма (Новиков и др., 2019). Широкий оптический доступ к образцу, помещенному в отверстие в рениевой или стальной прокладке между двумя алмазными наковальнями с диаметром кулеты от 0.4 до 0.6 мм обеспечивается конусными отверстиями с апертурой 60° с двух сторон. Нагревательный элемент расположен вокруг прокладки с образцом внутри ячейки и соединяется с внешними платиновыми электродами по схеме, описанной в работе Чертковой Н.В. с соавторами (Chertkova et al., 2018). В тестовых экспериментах было опробовано несколько типов нагревательных элементов, изготовленных из металлов платиновой группы, включая иридий и платину, однако низкие значения тока при плавлении этих элементов (порядка 10 А для проволочного нагревательного элемента с диаметром 0.25–0.3 мм) не позволяют использовать их при температурах выше 400°С. Целесообразным оказалось применение рениевого нагревательного элемента, характеризующегося более высокими удельными сопротивлениями и температурами плавления.
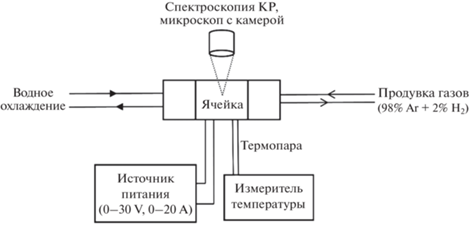
Общая схема подключения установки к внешним системам и приборам вспомогательного оборудования приведена на рис. 1. Постоянный ток подается на нагреватель с помощью регулируемого линейного источника питания Ningbo JiuYuan Electronic (QJ3020E). Нагрев ячейки контролируется с помощью PtRh–Pt термопары, R-типа (13% Rh) или S-типа (10% Rh), спай которой расположен в непосредственной близости от прокладки с образцом, с подключением к микропроцессорному измерителю-регулятору OVEN (ТРМ101). Точность соответствия измеренной температуры реальной температуре образца внутри прокладки, определенная в тестах по плавлению NaNO3, составила ±6°C. Ячейка с блоком охлаждения устанавливается под микроскоп Olympus BX51 на усиленную опорную площадку с прорезью для проходящего света, размещенную на трехкоординатном столике с микрометрическим приводом. К микроскопу подключена цифровая камера GigE uEye (SUXGA, 2048х1536) и спектрограф Acton SpectraPro-2500i с охлаждаемым до –70°C детектором CCD Pixis2K. Измерение спектров комбинационного рассеяния (КР) проводится в геометрии обратного рассеяния с использованием непрерывного твердотельного лазера с длиной волны λ = 532 нм с диодной накачкой и краевого фильтра с полосой ~100 см–1. Лазерный пучок диаметром ~2 мкм фокусируется на образец при помощи объектива Olympus 20x с рабочим расстоянием 25 мм.
Рис. 1.
Общая схема подключения экспериментальной установки к внешним системам и приборам для проведения оптических наблюдений и высокотемпературных спектроскопических измерений in situ.
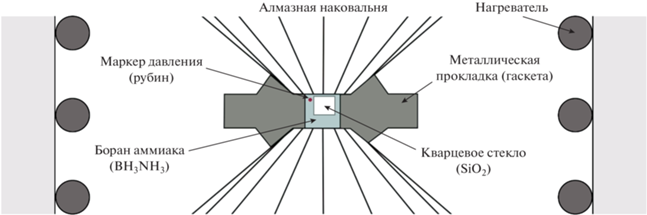
В качестве стартовых материалов для экспериментов использованы порошок кристаллического борана аммиака (99% BH3NH3), приготовленный по методике, описанной в работе Антонова с соавторами (Antonov et al., 2017), и тонкий срез кварцевого стекла (SiO2). Эти вещества помещались в рабочую камеру вместе с микрокристаллом рубина, выполняющего роль маркера давления (рис. 2). Усилие на алмазные наковальни создавалось внешними винтами, после чего осуществлялся нагрев ячейки со скоростью ~150°C/ч, с выдержкой 10–15 минут при каждой заданной температуре. Спектры КР образца и спектры люминесценции рубина регистрировались непосредственно во время эксперимента. Давление в рабочей камере рассчитывалось по положению линии флуоресценции R1 в спектре рубина в соответствии с калибровочными данными (Zha et al., 2000; точность определения давления 1%) и поправкой на температуру (Ragan et al., 1992; точность в пределах 0.5 ГПа). Полученные спектры обрабатывались с помощью программного комплекса PeakFit.
РЕЗУЛЬТАТЫ
Примеры микрофотографий рабочей камеры с образцом и маркером давления, а также спектров КР, записанных во время нагрева образца в ячейке высокого давления, приведены на рис. 3.
Рис. 3.
Микрофотографии рабочей камеры с образцом и спектры КР за вычетом базисной линии, снятые при соответствующих параметрах температуры и давления во время эксперимента (область анализа обозначена звездочкой). Интенсивная линия алмазной наковальни первого порядка (на частотах КР ~1335 см–1) удалена из спектров.
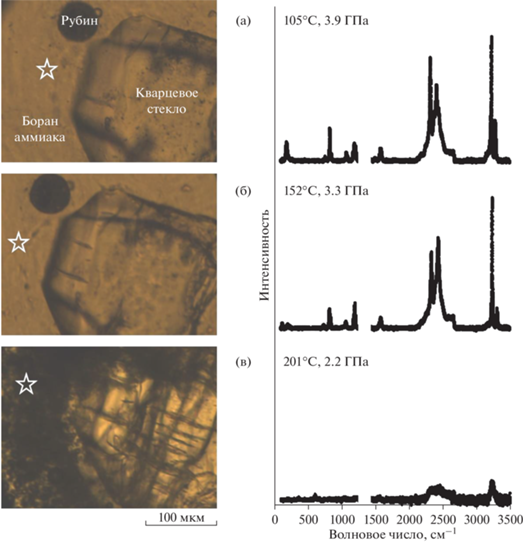
При комнатной температуре и атмосферном давлении боран аммиака представляет собой кристаллическое вещество со структурой тетрагональной симметрии, пространственной группы I4mm (Andersson, 2011), которая с повышением давления и температуры претерпевает ряд твердофазовых переходов. В диапазоне давлений от 2 до 9 ГПа и температурах выше 110°C происходит переход в фазу с пространственной группой симметрии Pnma (1') (Nylén et al., 2013). Спектр КР этой фазы (рис. 3б) характеризуется линиями валентных колебаний B–N около ~825 см–1, деформационных B–H3 около ~1200 см–1, деформационных N–H3 около ~1580 см–1. В области частот 2250–2550 см–1 отчетливо видны линии симметричных и асимметричных валентных колебаний B–H (около ~2340 см–1 и ~2440 см–1 соотвественно), а в области 3200–3350 см–1 наибольшей интенсивностью обладают линии симметричных валентных колебаний N–H (около ~3240 см–1) (Hess et al., 2008).
В системе BH3NH3–SiO2 в интервале давлений 2–5 ГПа первая стадия термического разложения борана аммиака с выделением водорода наблюдается при температурах 198–215°C. Водород выделяется в виде темных пузырей (рис. 3в), а в высокотемпературных спектрах КР появляются ротационные линии H2 на частотах ~600 см–1. Наряду с этим происходит изменение спектра борана аммиака с потерей интенсивности линий валентных колебаний B–N, деформационных B–H3 и N–H3. Согласно литературным данным (Nylén et al., 2009), продуктом диссоциации BH3NH3 при высоких давлениях является полимерная фаза (BH2NH2)x, что соответствует наблюдаемым в высокотемпературных спектрах КР линиям валентных колебаний B–H и N–H (рис. 3в).
В ходе закалки образца до комнатной температуры водород сконцентрировался у стенок рабочей камеры, что позволило получить спектры КР с высокой интенсивностью линий молекулярного H2. При давлении 2.1 ГПа в низкочастотной области спектра хорошо различимы ротационные линии, отвечающие пара- и орто-водороду (рис. 4а), а в высокочастотной – вибрационные линии с преобладанием орто-водорода (рис. 4б).
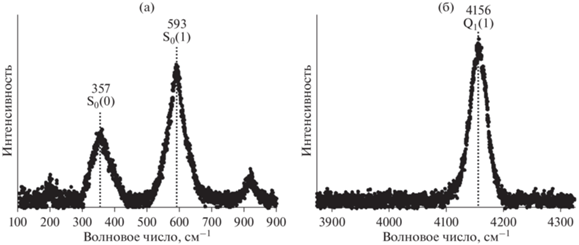
Рис. 4.
Спектры КР водорода, зарегистрированные при давлении 2.1 ГПа в ячейке с алмазными наковальнями после закалки: а – ротационные пики S0(0) и S0(1), отвечающие пара- и ортоводороду соответственно; б – вибрационный пик с доминирующей составляющей ортоводорода Q1(1) (Goncharov et al., 2001; Fang et al., 2018). Положение пиков указано цифрами.
Фазовая диаграмма системы BH3NH3–SiO2, построенная на основе полученных во время экспериментов спектроскопических данных, приведена на рис. 5.
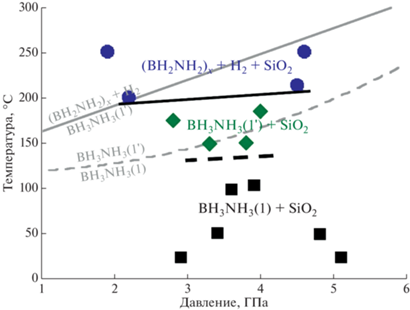
Рис. 5.
P-T-параметры фазовых переходов в системе BH3NH3–SiO2, по данным in situ измерений в ячейке с алмазными наковальнями и внешним нагревом. Прерывистой черной линией обозначен переход в фазу с пространственной группой Pnma, сплошной черной линией – первая стадия диссоциации борана аммиака с выделением молекулярного водорода. Серыми линиями показаны границы фазовых переходов в системе BH3NH3 (Nylén et al., 2009) с учетом влияния температуры на положение линий флуоресценции рубина и значения давлений. Квадраты, ромбы и круги обозначают положение экспериментальных точек.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Для корректного сравнения построенных линий фазовых переходов в системе BH3NH3–SiO2 с литературными данными для BH3NH3, был проведен пересчет давлений, указанных в работе (Nylén et al., 2009), учитывающий влияние температуры на положение линий флуоресценции рубина (Ragan et al., 1992). Как видно из диаграммы (рис. 5), в системе BH3NH3–SiO2 наклон линии фазового перехода борана аммиака в фазу с пространственной группой Pnma, а также линии термического разложения с выделением водорода, более пологий, чем в простой системе BH3NH3. Разница между температурами диссоциации увеличивается с давлением и составляет свыше 50°C при давлениях >4.5 ГПа. Этот тренд согласуется с данными о понижении температуры выделения H2 в процессе термического разложения борана аммиака BH3NH3 в присутствии наночастиц SiO2 (Shin et al., 2020).
Изменение наклона линии термического разложения борана аммиака в системе с кварцевым стеклом может быть связано с реакцией BH3NH3 с SiO2. Так как спектры КР, зарегистрированные при температурах выше 200°C, не выявили продуктов диссоциации, отличных от образующихся в простой системе BH3NH3, то можно предположить, что эта реакция происходит путем отщепления молекулярного водорода и его взаимодействия с SiO2. По данным Ефимченко и др. (Efimchenko et al., 2012), растворимость водорода в стекле SiO2 (H2/SiO2 в мольных долях) увеличивается с 0.24 при 2 ГПа до 0.42 при 5 ГПа, что, по-видимому, приводит к более активному взаимодействию между этими двумя компонентами при высоких давлениях.
ЗАКЛЮЧЕНИЕ
На базе Института экспериментальной минералогии им. Д.С. Коржинского РАН разработан и апробирован комплекс in situ методов исследования образцов при высоких давлениях в ячейке с алмазными наковальнями и внешним резистивным нагревом.
Разработанный комплекс применен для исследования устойчивости борана аммиака BH3NH3 в присутствии стекла SiO2 в интервале давлений 2–5 ГПа и температур 25–250°С. В системе BH3NH3–SiO2 термическое разложение BH3NH3 с выделением молекулярного водорода H2 и продукта разложения (BH2NH2)x зафиксировано при 198°С, 2.2 ГПа и 215°С, 4.5 ГПа.
Р-Т-параметры экспериментов в аппарате с алмазными наковальнями могут быть существенно расширены при использовании in situ лазерного нагрева, а технология создания восстановительных условий в рабочем объеме при диссоциации BH3NH3 и выделении H2 имеет широкие перспективы применения в физико-геохимических исследованиях глубинных водород-содержащих систем коры и мантии Земли, а также других планет земной группы.
Авторы выражают благодарность сотрудникам ИЭМ РАН О.А. Мищенчуку, Л.Г. Полетаевой, Е.П. Мартынову, Г.В. Кирдееву за изготовление технологического оборудования, А.В. Кузюре, В.М. Полукееву, Н.Н. Жданову, Е.В. Лиманову и В.Г. Бутвиной за помощь в проведении работы. Особая благодарность Л.С. Дубровинскому за техническую поддержку.
Исследование выполнено за счет гранта Российского научного фонда (проект № 20-77-00079) и частично в рамках государственного задания АААА-А18-118020590140-7 Института экспериментальной минералогии имени академика Д.С. Коржинского РАН.
Список литературы
Новиков А.П., Ляпин С.Г., Стишов С.М. (2019) Ячейка высокого давления с алмазными наковальнями для оптических исследований при низких температурах. Приб. техн. эксперим. (1), 131-136.
Стороженко П.А., Свицын Р.А., Кецко В.А., Буряк А.К., Ульянов А.В. (2005) Синтез и физико-химические свойства амминоборана. Журн. неорг. хим. 50(7), 1066-1071.
Черткова Н.В., Спивак А.В., Захарченко Е.С., Литвин Ю.А., Сафонов О.Г., Новиков А.П., Ефимченко В.С., Мелетов К.П. (2021) Установка высокого давления с внешним нагревом для in situ исследований фазовых переходов. Приб. техн. эксперим. (3), 158-160.
Шолин И.А. (2020) Термодинамические свойства гидридов высокого давления. Дисс. канд. Физ.-мат. Наук. Черноголовка: Институт физики твердого тела, 126 с.
Andersson O., Filinchuk Y., Dmitriev V., Quwar I., Talyzin A.V., Sundqvist B. (2011) Phase coexistence and hysteresis effects in the pressure-temperature phase diagram of NH3BH3. Phys. Rev. B 84(2), 024115.
Antonov V.E., Bulychev B.M., Fedotov V.K., Kapustin D.I., Kulakov V.I., Sholin I.A. (2017) NH3BH3 as an internal hydrogen source for high pressure experiments. Int. J. Hydrogen Energy 42, 22454-22459.
Chertkova N., Ohfuji H., Nomura R., Kadobayashi H., Irifune T. (2018) A step toward better understanding of behavior of organic materials at simultaneous high pressures and high temperatures. High Press. Res. 38(3), 337-347.
Drozdov A.P., Kong P.P., Minkov V.S. et al. (2019) Superconductivity at 250 K in lanthanum hydride under high pressure. Nature 569, 528-531.
Efimchenko V.S., Fedotov V.K., Kuzovnikov M.A. et al. (2013) Hydrogen solubility in amorphous silica at pressures up to 75 kbar. J. Phys. Chem. B 117 (1), 422-425.
Efimchenko V.S., Barkovskii N.V., Fedotov V.K., Meletov K.P., Chernyak V.M., Khryapin K.I. (2019) Destruction of fayalite and formation of iron and iron hydride at high hydrogen pressures. Phys. Chem. Min. 46, 743-749.
Efimchenko V.S., Barkovskii N.V., Fedotov V.K., Meletov K.P., Prokoshin A.V. (2021) Chemical reactions in the Fe2SiO4-D2 system with a variable deuterium content at 7.5 GPa. Am. Min., in press. https://doi.org/10.2138/am-2021-7697
Fang J., Chou I.M., Chen Y. (2018) Quantitative Raman spectroscopic study of the H2—CH4 gaseous system. J. Raman Spectrosc. 49(4), 710-720.
Frost D.J., McCammon C.A. (2008) The redox state of Earth’s mantle. Annu. Rev. Earth Planet. Sci. 36, 389-420.
Goncharov A.F., Strzhemechny M.A., Mao H.K., Hemley R.J. (2001) Low-frequency Raman excitations in phase I of solid H2: Role of crystal fields. Phys. Rev. B 63(6), 064304.
Hess N.J., Bowden M.E., Parvanov V.M., Mundy C., Kathmann S.M., Schenter G.K., Autrey T. (2008) Spectroscopic studies of the phase transition in ammonia borane: Raman spectroscopy of single crystal NH3BH3 as a function of temperature from 88 to 330 K. J. Chem. Phys. 128(3), 034508.
Khvostantsev L.G., Slesarev V.N., Brazhkin V.V. (2004) Toroidal type high-pressure device: history and prospects. High Press. Res. 24(3), 371-383.
Kohlstedt D.L., Keppler H., Rubie D.C. (1996) Solubility of water in the α, β and γ phases of (Mg, Fe)2SiO4. Contr. Mineral. Petrol. 123(4), 345-357.
Lin Y., Mao W.L. (2014) High-pressure storage of hydrogen fuel: ammonia borane and its related compounds. Chinese Sci. Bull. 59(36), 5235-5240.
Litasov K.D., Shatskiy A., Ohtani E., Katsura T. (2011) Systematic study of hydrogen incorporation into Fe-free wadsleyite. Phys. Chem. Min. 38(1), 75-84.
Mrosko M., Lenz S., McCammon C.A., Taran M., Wirth R., Koch-Müller M. (2013) Hydrogen incorporation and the oxidation state of iron in ringwoodite: A spectroscopic study. Am. Min. 98(4), 629-636.
Nylén J., Eriksson L., Benson D., Häussermann U. (2013) Characterization of a high pressure, high temperature modification of ammonia borane (BH3NH3). Journ. Chem. Phys. 139(5), 054507.
Nylén J., Sato T., Soignard E., Yarger J.L., Stoyanov E., Häussermann U. (2009). Thermal decomposition of ammonia borane at high pressures. J. Chem. Phys. 131(10), 104 506.
Ragan D.D., Gustavsen R., Schiferl D. (1992) Calibration of the ruby R, and R2 fluorescence shifts as a function of temperature from 0 to 600 K J. Appl. Phys. 72(12), 5539-5544.
Rumyantsev V.N. (2016) Hydrogen in the Earth’s outer core, and its role in the deep Earth geodynamics. Geodynam. Tectonophys. 7(1), 119-135.
Shin S., Jin J.H., Jung J. (2020) Thermolytic dehydrogenation of cotton-structured SiO2-Ammonia borane nanocomposite. J. Ind. Eng. Chem. 88, 278-284.
Shinozaki A., Hirai H., Ohfuji H., Okada T., Machida S., Yagi, T. (2013) Influence of H2 fluid on the stability and dissolution of Mg2SiO4 forsterite under high pressure and high temperature. Am. Min. 98, 1604-1609.
Zha C.S., Mao H.K., Hemley R.J. (2000) Elasticity of MgO and a primary pressure scale to 55 GPa. Proceed. Nat. Acad. Sci. 97(25), 13494-13499.
Дополнительные материалы отсутствуют.