Вопросы ихтиологии, 2023, T. 63, № 2, стр. 179-191
Биологическая характеристика многоиглого керчака Myoxocephalus polyacanthocephalus (Cottidae) из тихоокеанских вод северных Курильских островов и Юго-Восточной Камчатки в осенний период
Ю. Н. Полтев *
Сахалинский филиал Всероссийского научно-исследовательского института
рыбного хозяйства и океанографии – СахНИРО
Южно-Сахалинск, Россия
* E-mail: y.poltev@sakhniro.ru
Поступила в редакцию 15.05.2022
После доработки 17.06.2022
Принята к публикации 17.06.2022
- EDN: EZXKPO
- DOI: 10.31857/S0042875223020182
Аннотация
Рассмотрены пространственное распределение, размерно-половой состав, питание многоиглого керчака Myoxocephalus polyacanthocephalus и сопутствующие виды в тихоокеанских водах северных Курильских островов и Юго-Восточной Камчатки в осенний период. В августе–ноябре 1997 г. этот вид в уловах был представлен особями длиной 30–89 (в среднем 47.8 ± 0.5) см и массой тела 300–11 000 (2321 ± 90) г. Самки доминировали над самцами в соотношении 1.2 : 1.0. Зависимость массы тела от длины керчака описывается степенным уравнением: W = 0.0031FL3.446 (R2 = 0.935). Основу питания керчака составили рыбы (56.2% массы пищи), преимущественно минтай Gadus chalcogrammus и северный однопёрый терпуг Pleurogrammus monopterygius (соответственно 19.9 и 11.9%); отходы рыбопереработки (19.6%), главным образом головы северного однопёрого терпуга (12.2%); а также десятиногие ракообразные (Decapoda) (18.6%), в основном краб-стригун Chionoecetes opilio (14.1%). С ростом в питании керчака десятиногие ракообразные замещаются рыбами, а минтай вытесняется северным однопёрым терпугом и Liparidae. Отдельные участки исследованного района различались как размерно-половым составом и составом пищи керчака, так и видовым составом сопутствующих ему видов. Совместная встречаемость керчака с минтаем и северной двухлинейной камбалой Lepidopsetta polyxystra составила 100%.
Многоиглый керчак Myoxocephalus polyacanthocephalus (Pallas) (далее керчак) – один из широко распространённых в северной части Тихого океана видов рогатковых рыб (Cottidae), представляющих демерсальную ихтиофауну (Борец, 1997; Шейко, Федоров, 2000). Обитает в Японском море в зал. Петра Великого, у берегов Приморья и в Татарском проливе, в Охотском море, тихоокеанских водах о. Хоккайдо, Курильских о-вов, Восточной Камчатки, в Беринговом море и далее на юг вдоль американского побережья до о. Ванкувер (Линдберг, 1927; Шмидт, 1950; Masuda et al., 1984; Линдберг, Красюкова, 1987; Борец, 1997, 2000; Mecklenburg et al., 2002; Федоров и др., 2003; Парин и др., 2014). Пространственно-батиметрическое распределение, размерно-весовой состав и экология этого вида в водах у восточного побережья северных Курильских о-вов и юго-восточной оконечности Камчатки в той или иной степени описаны в различных публикациях (Токранов, 1985, 1986, 2009, 2019; Орлов, 1998, 2010; Токранов, Орлов, 2011, 2013; Tokranov, Orlov, 2013). Цель настоящей работы – изучить биологию и пространственное распределение керчака вышеуказанного района в осенний период 1997 г., а также выявить участки с наибольшей плотностью вида, рассмотреть размерно-половой состав, оценить зависимость массы тела от длины, определить видовой состав и значение кормовых объектов, выявить сопутствующие виды.
МАТЕРИАЛ И МЕТОДИКА
Материалом послужили данные по уловам 69 промысловых донных тралений, в прилове которых присутствовал керчак (рис. 1), 23.08–02.11.1997 г. у восточного побережья северных Курильских о-вов и Юго-Восточной Камчатки на глубинах 100–300 м. Вертикальное и горизонтальное раскрытия трала составляли соответственно 6–8 и 26 м, верхняя подбора – 49.2 м, расстояние между траловыми досками – 110 м; размеры траловых досок – 4100 × 2700 мм, ячея тралового мешка – 110 мм (между узлами 130 мм). Жёсткий грунтроп длиной 60 м был оснащён бобинцами и грунтропными катушками (Тупоногов и др., 2006), кутец трала защищён пропиленом от порывов при тралении о грунт.
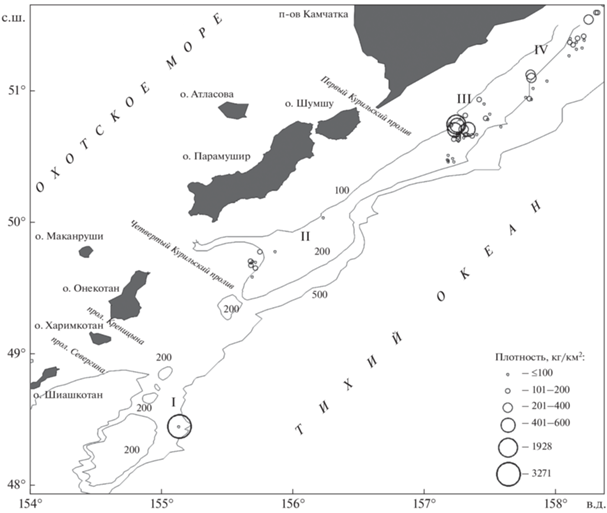
Рис. 1.
Участки обитания (I–IV) и плотность распределения многоиглого керчака Myoxocephalus polyacanthocephalus в августе–ноябре 1997 г. у восточного побережья северных Курильских островов и Юго-Восточной Камчатки; (—) – изобаты.
Размерно-весовую зависимость у керчака рассмотрели по данным биологического анализа 460 экз. (102 экз. – ноябрь–декабрь 1994 г., 100 экз. – ноябрь–декабрь 1996 г., 258 экз. – август–ноябрь 1997 г.), соотношение полов и питание – соответственно 258 и 230 экз. (август–ноябрь 1997 г.). У рыб измеряли длину по Смиту (FL) от вершины рыла до конца средних лучей хвостового плавника. Содержимое желудков исследовали общепринятыми методами (Руководство …, 1961). В отдельных случаях массу пищевых объектов устанавливали исходя из их примерной доли (в %) в пищевом комке с установленной массой, принимая, что полученные значения соответствуют долям по массе. Значение отдельных компонентов в питании керчака оценивали по доле их массы (в % общей массы пищи). Изменение питания в связи с ростом рассмотрели для особей FL 31–80 см.
Размерно-весовые характеристики, соотношение полов, значение в питании керчака кормовых объектов и видовой состав гидробионтов, встречающихся с ним в уловах, анализировали для всего района исследований и для четырёх пространственно разобщённых его участков: I – самого южного, находящегося напротив пролива Севергина (48°26′30′′–48°26′42′′ с.ш., 155°08′00′′–155°08′18′′ в.д.), с глубинами 252–292 м, в среднем 266 м (использована информация по двум тралениям, биоанализу 13 и питанию 12 экз.); II – напротив Четвёртого Курильского пролива (49°39′00′′–49°46′30′′ с.ш., 155°41′00′′–155°52′00′′ в.д.; 102–267 (186) м, семь тралений, 25 и 21 экз.); III – напротив Первого Курильского пролива до 50°56′00′′ с.ш. (50°27′30′′–50°56′00′′ с.ш., 157°10′30′′–157°30′00′′ в.д.; 100–280 (155) м, 23 траления, 80 и 70 экз.); IV – у Юго-Восточной Камчатки (50°56′00′′–51°39′00′′ с.ш., 157°46′24′′–158°21′′30′′ в.д.; 160–290 (248) м, 21 траление, 140 и 127 экз.).
Корреляцию показателей оценивали как очень сильную (>0.90), сильную (0.71–0.90), значительную (0.51–0.70), умеренную (0.31–0.50) и слабую (<0.3) (Лакин, 1973).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В августе–ноябре 1997 г. керчак в уловах донного трала у восточного побережья северных Курильских о-вов и юго-восточной оконечности Камчатки отмечен на участках с координатами 48°26′30′′–51°39′00′′ с.ш., 155°08′00′′–158°21′30′′ в.д. и глубинами обитания 100–300 м (рис. 1). Эти участки располагаются в пределах границ распространения вида в данном районе (Орлов, 1998; Токранов, Орлов, 2013). В целом являясь представителем элиторального ихтиоцена северо-западной части Тихого океана, керчак обитает на глубинах 0–775, преимущественно – 40–250 м (Федоров, 2000; Шейко, Федоров, 2000).
Уловы на часовое траление варьировали от 1 до 280 экз., составив в среднем 17.1 экз., что несколько выше значений по данному району в осенний период (максимальные – 235, средние – 13.4 экз.), представленных ранее (Орлов, Токранов, 2008; Токранов, Орлов, 2011, 2013). Плотность распределения керчака варьировала в пределах 3.5–3271.0 кг/км2 (184.8 кг/км2). Наиболее высокие средний улов на часовое траление и плотность распределения вида отмечены на глубинах 101–125 м (31.3 экз., 507.0 кг/км2). На глубинах 251–275 м эти показатели также были высокими (27.9 экз., 297.6 кг/км2) (табл. 1); низкие приходились на глубины 201–250 м (3.7–5.6 экз., 41.8–59.6 кг/км2) и 276–300 м (2 экз., 16.6 кг/км2). Высокие уловы на часовое траление и плотности распределения отмечены на I (109 экз., 1927.9 кг/км2; 101–115 м; 50°44′42′′ с.ш., 157°14′42′ в.д.) и III (280 экз., 3270.8 кг/км2; 252–255 м; 48°16′00′′ с.ш., 155°05′00′′ в.д.) участках при промысле соответственно минтая Gadus chalcogrammus и северного однопёрого терпуга Pleurogrammus monopterygius (далее терпуг). По данным других исследований (Токранов, Орлов, 2011, 2013), максимальные средние уловы на часовое траление (до 27 экз.) в осенний период приурочены к глубинам <100 м при нахождении >20% особей на глубинах 301–350 м. Возможно, полученные различия батиметрического распределения керчака обусловлены отсутствием в рассматриваемый нами период тралений на глубинах <100 м и >300 м.
Таблица 1.
Уловы многоиглого керчака Myoxocephalus polyacanthocephalus и плотность его распределения в зависимости от глубины обитания у восточного побережья северных Курильских островов и Юго-Восточной Камчатки в августе–ноябре 1997 г.
| Глубины, м | Улов, экз/ч траления | Плотность, кг/км2 | Число тралений |
|---|---|---|---|
| 101–125 | 5–109 (31.3) | 61.3–1927.9 (507.0) | 7 |
| 126–150 | 3–33 (14.3) | 9.4–319.7 (109.3) | 12 |
| 151–175 | 4–64 (16.6) | 25.1–550.3 (141.1) | 14 |
| 176–200 | 2–35 (15.5) | 18.2–388.2 (158.0) | 4 |
| 201–225 | 1–9 (3.7) | 5.2–88.6 (41.8) | 6 |
| 226–250 | 1–12 (5.6) | 3.5–163.5 (59.6) | 9 |
| 251–275 | 1–280 (27.9) | 6.3–3270.8 (297.6) | 15 |
| 276–300 | 1–3 (2.0) | 5.5–27.7 (16.6) | 2 |
Примечание. Здесь и в табл. 2, 4: перед скобками – пределы варьирования показателя, в скобках – среднее значение.
Средняя FL керчака в пределах глубин 101–175 м уменьшалась от 53.1 до 43.8 см (табл. 2). Доля самцов на этих глубинах составляла 46.2–51.4%. На глубинах 176–200 м средняя FL возрастала до 58.0 см при снижении доли самцов до 13.3%. С увеличением глубины обитания до 250 м средняя FL сокращалась до 47 см, а доля самцов возрастала до 39.4%. На участках с глубинами 276–300 м среднее значение FL составило 45.3 см, а доля самцов 25%. Эти данные не согласуются с закономерностью, ранее установленной для района исследований, согласно которой с увеличением глубины обитания керчака возрастает доля более крупных рыб (Орлов, Токранов, 2008; Токранов, Орлов, 2013).
Таблица 2.
Длина по Смитту (FL), масса тела и соотношение полов (%) многоиглого керчака Myoxocephalus polyacanthocephalus из уловов на различных глубинах у восточного побережья северных Курильских островов и Юго-Восточной Камчатки в августе–ноябре 1997 г.
| Глубины, м | FL, см | Масса, г | Самки : самцы | Число рыб, экз. |
|---|---|---|---|---|
| 101–125 | 34.0–76.5 (53.1) | 450–7500 (3336) | 48.6 : 51.4 | 35 |
| 126–150 | 30.0–76.0 (47.6) | 380–8300 (2231) | 53.8 : 46.2 | 26 |
| 151–175 | 32.0–79.0 (43.8) | 450–9100 (1627) | 50.0 : 50.0 | 24 |
| 176–200 | 36.5–89.0 (58.0) | 750–11000 (4167) | 86.7 : 13.3 | 15 |
| 201–225 | 38.0–67.0 (47.0) | 800–6000 (1976) | 61.9 : 38.1 | 21 |
| 226–250 | 36.0–67.5 (47.0) | 700–5500 (1989) | 60.6 : 39.4 | 33 |
| 251–275 | 32.0–72.0 (45.0) | 500–7000 (1807) | 61.0 : 39.0 | 100 |
| 276–300 | 40.0–52.5 (45.3) | 900–2500 (1575) | 75.0 : 25.0 | 4 |
Керчак – один из наиболее крупных представителей рогатковых в северной части Тихого океана. В водах залива Аляска достигает длины 72 см, Алеутских островов – 76 см, восточной части Берингова моря – 82 см (Ormseth, TenBrink, 2010; Spies et al., 2012), у западного побережья Камчатки – 85 см (Матвеев, Терентьев, 2016). Максимальная длина составляет 91.5 см (Линдберг, 1927), масса тела – 10 кг (Токранов, 2009, 2014, 2017). В тихоокеанских водах северных Курильских островов и Юго-Восточной Камчатки, согласно опубликованным данным (Токранов, Орлов, 2011, 2013), представлен особями FL 27–82 (в среднем 52.8 ± 8.5) см и массой 400–10000 (3100 ± 200) г. В настоящем исследовании FL керчака варьировала в пределах 30–89 см (47.8 ± 0.5) см, масса – 300–11000 (2321 ± 90) г. Самки имели FL и массу соответственно 31–89 (51.5 ± 0.7) см и 300–11000 (2961 ± 144) г, самцы – 30–74 (43.4 ± 0.4) см и 380–8300 (1526 ± 55) г. Максимальная масса отмечена у самки FL 80 см, в желудке которой зафиксирован осьминог Bathypolypus sp. массой 1700 г. Особь с максимальной FL также оказалась самкой с массой 9300 г. Содержимое её желудка было представлено на 88% минтаем, на 12% – северной двухлинейной камбалой Lepidopsetta polyxystra с общей массой 1600 г. Близкое значение средней длины керчака (45.5 см) получено для охотоморских вод северных Курильских островов и Юго-Западной Камчатки (Матвеев, Терентьев, 2016). Соотношение самок и самцов составило 1.2 : 1.0.
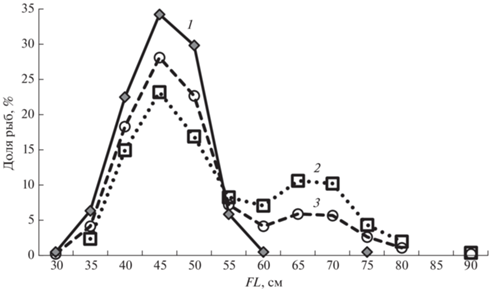
В уловах наиболее многочисленными были особи FL 36–50 см (68.9% общего количества рыб). У самок на долю таких особей пришлось 54.9%, у самцов – 86.3%. Доля особей размерных групп 36–40, 41–45 и 46–50 см составила соответственно 18.3, 28.0 и 22.6%, у самок – 14.9, 23.1 и 16.9%, у самцов – 22.4, 34.2 и 29.8% (рис. 2). Такие же размерные группы керчака были самыми многочисленными и в охотоморских водах северных Курильских островов и Юго-Западной Камчатки (Матвеев, Терентьев, 2016).
Рис. 2.
Размерный состав (длина тела по Смитту, FL) многоиглого керчака Myoxocephalus polyacanthocephalus в уловах в августе–ноябре 1997 г. у восточного побережья северных Курильских островов и Юго-Восточной Камчатки: 1 – самцы, 2 – самки, 3 – оба пола.
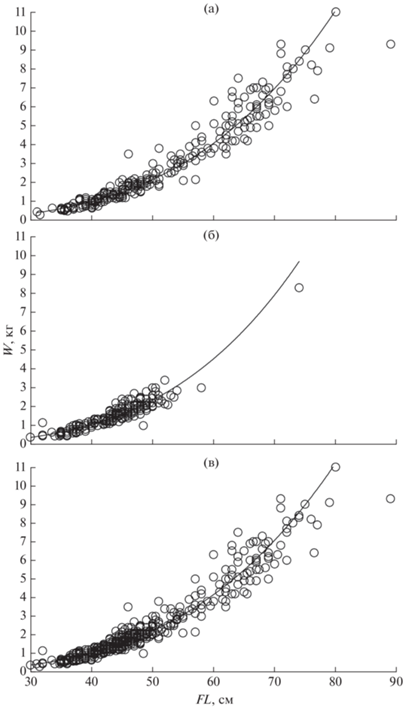
Зависимость массы тела (W, г) от длины (FL, см) керчака тихоокеанских вод северных Курильских островов и Юго-Восточной Камчатки описывается степенным уравнением: W = 0.0031FL3.446 (R2 = 0.935) (рис. 3). Для самок такая зависимость имеет вид: W = 0.0027FL3.4792 (R2 = 0.95), для самцов – W = 0.0017FL3.6188 (R2 = 0.858). Между FL и массой тела отмечена очень сильная корреляция для вида в целом и для самок (r = соответственно 0.95 и 0.96) и сильная (r = 0.90) – для самцов. Близкая к полученной нами зависимость для керчака в целом (W = 0.0057TL3.1828 (R2 = 0.941), где TL – общая длина тела), была описана ранее (Токранов, Орлов, 2013).
Рис. 3.
Зависимость массы тела (W) от длины тела по Смитту (FL) многоиглого керчака Myoxocephalus polyacanthocephalus из вод у восточного побережья северных Курильских островов и Юго-Восточной Камчатки в августе–ноябре 1997 г.: а – самки, б – самцы, в – оба пола.
Спектры питания керчака разнообразны, включая, например, в прибрежных водах Камчатки ~130 представителей различных систематических групп беспозвоночных и рыб (Токранов, 1986). Однако основа биомассы формируется за счёт рыб и десятиногих ракообразных (Decapoda) (Токранов, 1986, 2017, 2019; Tokranov, Orlov, 2013). Причём в одних районах доминируют рыбы, в других – десятиногие ракообразные. Так, в восточной части Берингова моря декаподы составляют 53% массы пищи (TenBrink, Buckley, 2012), в водах Северо-Западной Камчатки в зимний период – 54.2% (Токранов, 2009), в зал. Петра Великого – 62.2–85.3% (Панченко, Пущина, 2004; Пущина, Соломатов, 2010; Пущина и др., 2016). А вот у Юго-Западного Сахалина керчак в основном потребляет рыб (54%) (Ким Сен Ток, 2001). В зал. Шелихова в питании вида на рыб приходится 51.9% (Напазаков, 2008), в водах у Северо-Западной Камчатки и других районов п-ова – от 43.2% у юго-востока в зимний период до 87.2% у северо-запада в весенне-летний период (Борец, 1995; Токранов, 2009; Tokranov, Orlov, 2013). В настоящем исследовании среди объектов питания керчака выявлено 39 таксонов беспозвоночных и рыб, распознаваемых в полевых условиях. Из них доминировали рыбы (56.2% массы пищи) при значении десятиногих ракообразных 18.6% (табл. 3). В зимне-весенне-летний период в рассматриваемом районе на рыб приходилось 59.1%, на десятиногих ракообразных – 34.6% (Tokranov, Orlov, 2013). Основу рыбного питания составили минтай (19.9% от всей пищи) и терпуг (11.2%). Относительно высокое значение терпуга является особенностью питания керчака в исследованный период. Ранее ни в одном из районов камчатских вод этот вид в питании хищника не регистрировали, а в рассматриваемом районе его несущественная роль (<1%) отмечена в летний период (Tokranov, Orlov, 2013). В водах западной части Берингова моря доля терпуга в питании керчака составила 2.4% (TenBrink, Buckley, 2012). В зал. Петра Великого керчак потреблял другого представителя терпуговых – южного однопёрого терпуга P. azonus (6.1%) (Пущина и др., 2016). Как и в большинстве других районов, основу потреблённых десятиногих ракообразных составили крабы-стригуны – опилио Chionoecetes opilio (14.1%) и Бэрда Ch. bairdi (2.6%). Другой особенностью осеннего питания керчака является значительное потребление отходов рыбопереработки (19.6%), не отмеченное ранее для района исследований. В водах восточной части Берингова моря на отходы рыбопереработки приходилось 10.9% пищи вида (TenBrink, Buckley, 2012), а в водах западной части моря они составляли основу его питания (82.2%) (Глубоков, Орлов, 2004). Для самок в настоящем исследовании отмечено более высокое потребление моллюсков (6.8% всей пищи) и рыб (59.8%), для самцов – десятиногих ракообразных (21.2%) и отходов рыбопереработки (28.1%).
Таблица 3.
Состав пищи многоиглого керчака Myoxocephalus polyacanthocephalus из района тихоокеанских вод северных Курильских островов и Юго-Восточной Камчатки и разных его участков в августе–ноябре 1997 г., % от массы
| Компонент пищи и другие показатели | Весь район | Участок | |||||
|---|---|---|---|---|---|---|---|
| оба пола | самки | самцы | I | II | III | IV | |
| Alga | 0.02 | 0.07 | 0.05 | ||||
| Amphipoda | 0.02 | 0.02 | 0.04 | ||||
| Isopoda | 0.03 | 0.02 | 0.05 | 0.03 | |||
| Polychaeta | 0.01 | 0.01 | 0.04 | 0.01 | |||
| Sipuncula | 0.12 | 0.16 | 0.04 | 0.27 | |||
| Ophiuroidea | 0.05 | 0.16 | 0.13 | ||||
| Strongylocentrotus sp. | 0.25 | 0.33 | 0.07 | 0.62 | |||
| Decapoda | 18.58 | 17.30 | 21.23 | 29.25 | 15.13 | 7.24 | 28.87 |
| Crangonidae | 0.05 | 0.07 | 0.11 | ||||
| Pandalidae | 0.72 | 0.85 | 0.45 | 0.32 | 0.04 | 1.57 | |
| Paguridae | 0.83 | 0.54 | 1.44 | 0.91 | 1.08 | ||
| Majidae | 16.98 | 15.84 | 19.34 | 28.93 | 15.13 | 6.29 | 26.11 |
| Неопределённые остатки Chionoecetes | 0.28 | 0.24 | 0.35 | 0.71 | |||
| Ch. opilio | 14.07 | 12.95 | 16.40 | 28.93 | 7.52 | 1.99 | 25.62 |
| Ch. bairdi | 2.63 | 2.65 | 2.59 | 7.61 | 3.59 | 0.49 | |
| Mollusca | 5.08 | 6.75 | 1.62 | 22.67 | 0.80 | 4.04 | |
| Gastropoda | 0.38 | 0.30 | 0.53 | 1.55 | 0.40 | 0.04 | |
| Неопределённые остатки Gastropoda | 0.22 | 0.30 | 0.05 | 1.55 | 0.04 | ||
| Кладка Gastropoda | 0.16 | 0.48 | 0.40 | ||||
| Cephalopoda | 4.70 | 6.44 | 1.09 | 21.12 | 0.40 | 4.00 | |
| Неопределённые остатки Cephalopoda | 0.08 | 0.24 | 0.18 | ||||
| Bathypolypus sp. | 2.78 | 4.12 | 21.12 | ||||
| Octopus sp. | 1.15 | 1.42 | 0.60 | 0.19 | 2.44 | ||
| Berryteuthis magister | 0.61 | 0.90 | 1.38 | ||||
| Rossia pacifica | 0.08 | 0.25 | 0.21 | ||||
| Pisces | 56.20 | 59.82 | 48.68 | 70.75 | 57.85 | 51.53 | 58.75 |
| Неопределённые остатки Pisces | 11.27 | 12.64 | 8.42 | 17.63 | 16.52 | 6.52 | 13.44 |
| Arhynchobatidae | 0.05 | 0.07 | 0.13 | ||||
| Arctoraja parmifera | 0.05 | 0.07 | 0.13 | ||||
| Gadidae | 20.05 | 19.14 | 21.92 | 39.95 | 21.27 | 2.50 | 33.76 |
| Gadus chalcogrammus | 19.88 | 18.89 | 21.92 | 39.95 | 21.27 | 2.50 | 33.38 |
| G. macrocephalus | 0.17 | 0.25 | 0.38 | ||||
| Hexagrammidae | 11.18 | 11.51 | 10.50 | 28.47 | |||
| Pleurogrammus monopterygius | 11.18 | 11.51 | 10.50 | 28.47 | |||
| Cottidae | 3.99 | 4.03 | 3.95 | 0.32 | 2.48 | 8.65 | 0.60 |
| Неопределённые остатки Gymnocanthus | 0.92 | 1.02 | 0.73 | 1.75 | 0.53 | ||
| G. galeatus | 1.48 | 1.11 | 2.27 | 3.78 | |||
| G. detrisus | 1.13 | 1.43 | 0.50 | 2.48 | 2.05 | ||
| Triglops scepticus | 0.09 | 0.09 | 0.10 | 0.32 | 0.13 | 0.07 | |
| T. forficatus | 0.29 | 0.31 | 0.25 | 0.73 | |||
| Artediellus sp. | 0.03 | 0.10 | 0.08 | ||||
| Icelus uncinalis | 0.05 | 0.07 | 0.13 | ||||
| Hemitripteridae | 0.10 | 0.30 | 0.25 | ||||
| Hemitripterus villosus | 0.10 | 0.30 | 0.25 | ||||
| Agonidae | 0.27 | 0.83 | 0.72 | 0.62 | |||
| Sarritor sp. | 0.27 | 0.83 | 0.72 | 0.62 | |||
| Liparidae | 6.48 | 8.87 | 1.52 | 12.13 | 11.52 | 1.59 | 8.89 |
| Неопределённые остатки Elassodiscus | 0.62 | 0.93 | 1.59 | ||||
| Paraliparis grandis | 0.50 | 1.52 | 1.12 | ||||
| Неопределённые остатки Careproctus | 1.96 | 2.91 | 12.13 | 3.52 | |||
| C. furcellus | 1.87 | 2.77 | 5.31 | 2.65 | |||
| C. rastrinus | 0.71 | 1.05 | 1.60 | ||||
| C. roseofuscus | 0.82 | 1.21 | 6.21 | ||||
| Pleuronectidae | 2.65 | 3.44 | 1.01 | 6.06 | 2.80 | 1.70 | |
| Неопределённые остатки Pleuronectidae | 0.75 | 0.63 | 1.01 | 1.70 | |||
| Lepidopsetta polyxystra | 1.78 | 2.63 | 6.06 | 2.49 | |||
| Hippoglossoides elassodon | 0.12 | 0.18 | 0.31 | ||||
| Pisces ova | 0.16 | 0.13 | 0.23 | 0.36 | |||
| Ova Arhynchobatidae | 0.16 | 0.13 | 0.23 | 0.36 | |||
| Отходы рыбопереработки | 19.64 | 15.60 | 28.07 | 4.35 | 39.59 | 7.99 | |
| Головы P. monopterygius | 12.22 | 11.43 | 13.86 | 30.29 | 0.73 | ||
| Головы L. polyxystra | 2.45 | 7.55 | 6.25 | ||||
| Головы G. chalcogrammus | 2.27 | 2.89 | 1.00 | 2.92 | 2.55 | ||
| Неопределённые остатки Pisces | 2.08 | 1.28 | 3.75 | 4.71 | |||
| Внутренности Pisces | 0.62 | 1.91 | 4.35 | 0.13 | |||
| Число тралений | 53 | 53 | 53 | 2 | 7 | 23 | 21 |
| Число желудков с пищей | 230 | 133 | 97 | 12 | 21 | 70 | 127 |
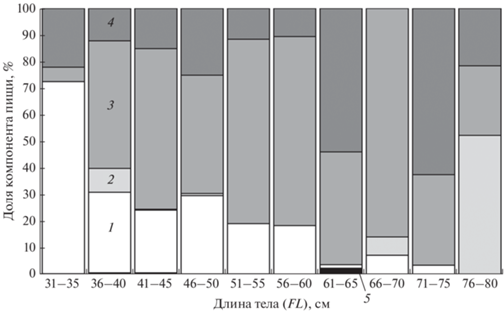
У керчаков, как и у других хищных рыб, с возрастом происходят изменения состава пищи. Причём в районах с преимущественным питанием беспозвоночными (восточная часть Берингова моря, зал. Петра Великого) рыбы по мере роста замещаются беспозвоночными (TenBrink, Buckley, 2012; Пущина и др., 2016), а в районах с преимущественным рыбным питанием (прикамчатские воды) беспозвоночные замещаются рыбами (Борец, 1997; Напазаков, Чучукало, 2003; Чучукало, 2006; Токранов, 2009). Вместе с тем в июльских исследованиях 2008 г. в западнокамчатских водах десятиногие ракообразные в питании керчака доминировали во всех размерных группах (Напазаков, 2015). Питание керчака рассматриваемого района в связи с ростом изменяется так же, как и в водах большинства районов Камчатки, – десятиногие ракообразные замещаются рыбами. Декаподы отмечены в питании всех размерных групп, за исключением наиболее крупноразмерной (рис. 4); с ростом керчаков их потребление снижалось. Преобладающее значение (72.2% массы пищи) декаподы имели для особей FL 31–35 см, существенное (18.4–30.3%) – для особей FL 36–60 см. Рыбы становились жертвами керчаков всех размерных групп. Были малозначимы в питании особей FL 31–35 см (5.5%) и составили его основу для размерных групп 41–45, 51–55, 56–60 и 66–70 см (соответственно 60.3, 69.3, 71.0, 85.9%). В других размерных группах являлись одними из основных пищевых объектов – от 26.2% (76–80 см) до 48.0% (36–40 см). Отходы рыбопереработки отмечены в желудках всех размерных групп, кроме особей FL 66–70 см. Составляли основу питания особей FL 61–65 см (54.0%) и 71–75 см (62.5%), у других размерных групп их доля варьировала от 10.6% (56–60 см) до 25.1% (46–50 см). Моллюсками питались рыбы FL 36–50, 61–70 и 76–80 см. Лишь у наиболее крупных особей имели преобладающее значение. У рыб FL 36–40 и 66–70 см их доля в питании не превышала 10%, у остальных была <1%.
Рис. 4.
Изменение состава пищи многоиглого керчака Myoxocephalus polyacanthocephalus в связи с его ростом у восточного побережья северных Курильских островов и Юго-восточной Камчатки в августе–ноябре 1997 г., % массы: 1 – десятиногие ракообразные, 2 – моллюски, 3 – рыбы, 4 – отходы рыбопереработки, 5 – другое.
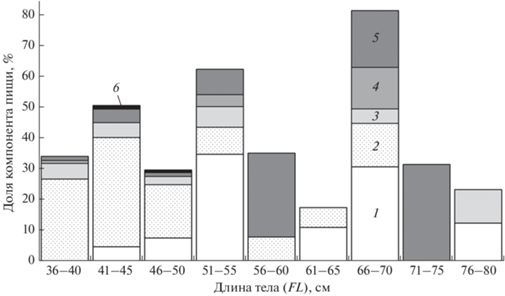
Среди рыб в питании керчака FL 36–50 см доминировал минтай (36–40 см – 26.5% пищи, 41–45 см – 35.5%, 46–50 см – 17.4%) (рис. 5). У особей большей длины основу рыбного питания составляли терпуг (51–55 см – 34.6%, 61–65 см – 10.9%, 76–80 см – 12%), и липаровые (Liparidae) (56–60 см – 27.3%, 71–75 см – 31.3%).
Рис. 5.
Изменение состава рыбной пищи многоиглого керчака Myoxocephalus polyacanthocephalus в связи с его ростом у восточного побережья северных Курильских островов и Юго-Восточной Камчатки в августе–ноябре 1997 г., % массы: 1 – терпуговые, 2 – тресковые, 3 – керчаковые, 4 – камбаловые, 5 – липаровые, 6 – другие.
Широкое пространственное распределение обусловливает различие как размерно-весовых характеристик и соотношения полов керчака, так и качественно-количественного состава сопутствующих ему видов на отдельных участках обитания. На участке IV отмечены наиболее мелкие особи (в среднем 44.9 см и 1736 г), на II – самые крупные (57.7 см и 3910 г) с наиболее сильным различием в соотношении полов (табл. 4). Керчаки с участков I и III были близки по соотношению полов, а также по средним значениям длины и массы тела.
Таблица 4.
Длина по Смитту (FL), масса тела и соотношение полов (%) многоиглого керчака Myoxocephalus polyacanthocephalus из уловов на разных участках тихоокеанских вод северных Курильских островов и Юго-Восточной Камчатки в августе–ноябре 1997 г.
| Участок | FL, см | Масса, г | Самки : самцы | Число рыб, экз. |
|---|---|---|---|---|
| I | 37.5–72.0 (49.5) | 800–6800 (2515) | 53.8 : 46.2 | 13 |
| II | 36.5–89.0 (57.7) | 750–11 000 (3910) | 76.0 : 24.0 | 25 |
| III | 30.0–76.5 (48.3) | 380–8300 (2436) | 54.2 : 45.8 | 83 |
| IV | 32.0–69.0 (44.9) | 500–7000 (1736) | 59.9 : 40.1 | 137 |
Известно, что керчак обитает совместно с наиболее типичными в нижней части шельфа и верхней зоне материкового склона представителями ихтиофауны (Токранов, Орлов, 2013). Из них в уловах с керчаком в целом по району исследований были отмечены с встречаемостью ≥50% 21 вид рыб и командорский кальмар Berryteuthis magister (табл. 5). Минимальное количество видов рыб со встречаемостью ≥50% пришлось на участок IV (17), максимальное – на II (25). Согласно ранее полученным данным, керчаку в рассматриваемом районе с частотой встречаемости >90% в уловах сопутствуют минтай, тихоокеанская треска Gadus macrocephalus, северная двухлинейная камбала и широколобый шлемоносец Gymnocanthus detrisus (Токранов, Орлов, 2011). В настоящем исследовании с такой частотой в уловах с керчаком по району в целом встречались минтай, тихоокеанская треска, северная двухлинейная камбала, большеглазый триглопс Triglops scepticus и узкозубая палтусовидная камбала Hippoglossoides elassodon. Максимальное количество видов рыб с частотой встречаемости >90% отмечено для участка I (15), минимальное – для III (6). Постоянное совместное с керчаком присутствие на каждом из четырёх участков отмечено для минтая и северной двухлинейной камбалы. Встречаемость широколобого шлемоносца вместе с керчаком в целом по району составила 73.9% при постоянной совместной встречаемости на участках I и II.
Таблица 5.
Встречаемость рыб и командорского кальмара Berryteuthis magister, сопутствующих многоиглому керчаку Myoxocephalus polyacanthocephalus в уловах на разных участках тихоокеанских вод северных Курильских островов и Юго-Восточной Камчатки в августе–ноябре 1997 г., %
| Вид | Участок | Весь район | |||
|---|---|---|---|---|---|
| I | II | III | IV | ||
| Bathyraja aleutica | 100 | 100 | 36.4 | 89.5 | 58.0 |
| B. maculata | 57.1 | 4.5 | 10.1 | ||
| Arctoraja parmifera | 50.0 | 85.7 | 45.5 | 5.3 | 39.1 |
| Malacocottus zonurus | 50.0 | 57.1 | 63.6 | 52.6 | 56.5 |
| Dasycottus setiger | 50.0 | 85.7 | 63.6 | 68.4 | 68.1 |
| Gymnocanthus detrisus | 100 | 100 | 77.3 | 47.4 | 73.9 |
| G. galeatus | 100 | 45.5 | 21.1 | 42.0 | |
| Hemilepidotus jordani | 100 | 100 | 65.2 | ||
| H. gilberti | 63.6 | 39.1 | |||
| Triglops forficatus | 100 | 72.7 | 21.1 | 60.9 | |
| T. scepticus | 100 | 71.4 | 100 | 89.5 | 94.2 |
| Percis japonica | 100 | 50.0 | 31.6 | 42.0 | |
| Sarritor frenatus | 100 | 85.7 | 63.6 | 89.5 | 84.1 |
| Hexagrammos lagocephalus | 14.3 | 86.4 | 5.3 | 46.4 | |
| Pleurogrammus monopterygius | 50.0 | 71.4 | 90.9 | 21.1 | 63.8 |
| Eleginus gracilis | 14.3 | 54.5 | 27.5 | ||
| Gadus chalcogrammus | 100 | 100 | 100 | 100 | 100 |
| G. macrocephalus | 100 | 100 | 100 | 89.5 | 94.2 |
| Atheresthes evermanni | 100 | 85.7 | 63.6 | 94.7 | 75.4 |
| Hippoglossus stenolepis | 100 | 100 | 72.7 | 94.7 | 87.0 |
| Reinchardtius hippoglossoides | 50.0 | 14.3 | 27.3 | 52.6 | 37.7 |
| Hippoglossoides elassodon | 100 | 71.4 | 86.4 | 100 | 91.3 |
| Lepidopsetta polyxystra | 100 | 100 | 100 | 100 | 100 |
| Careproctus rastrinus | 100 | 28.6 | 59.1 | 94.7 | 69.6 |
| C. roseofuscus | 50.0 | 85.7 | 9.1 | 36.8 | 31.9 |
| C. furcellus | 100 | 71.4 | 13.6 | 94.7 | 50.7 |
| Crystallichthys mirabilis | 100 | 85.7 | 50.0 | 63.2 | 59.4 |
| Liparis ochotensis | 50.0 | 71.4 | 81.8 | 42.1 | 66.7 |
| Lycodes albolineatus | 50.0 | 42.9 | 9.1 | 47.4 | 30.4 |
| L. brunneofasciatus | 100 | 100 | 45.5 | 94.7 | 72.5 |
| Berryteuthis magister | 50.0 | 71.4 | 50.0 | 52.6 | 56.5 |
В уловах на участках I, II и IV по численности доминировал минтай, на III – терпуг. Эти же виды на участках и составили основу рыбного питания керчака. На минтая пришлось соответственно 40.0, 21.3 и 33.4 пищи, на терпуга – 28.5% (табл. 3). Питание керчака на разных участках имело свои особенности. Так, на участке IV, кроме минтая, существенное значение имел краб-стригун опилио (25.6%). На участке I значимую роль играли краб-стригун опилио (28.9%) и рыбы рода Careproctus (12.1%). На участке II кроме минтая, крабов-стригунов (15.1%) и рыб рода Careproctus (11.5%) существенное место в питании занимал Bathypolypus sp. (21.1%). От этих участков разительно отличался участок III, на котором керчак преимущественно потреблял терпуга и отходы рыбопереработки (39.6%).
Для керчака различных районов обитания характерно декаподно-рыбное питание или, как в рассматриваемом районе, рыбно-декаподное с широким спектром жертв. Однако в отдельные периоды на отдельных участках керчаки могут частично или преимущественно переключаться на несвойственные им кормовые объекты. В частности, в мае–июле 1997 и в июле и сентябре 1998 гг. в западной части Берингова моря основу их пищи (82.3%) составили отходы переработки минтая – головы, позвоночники с хвостами и внутренности (Глубоков, Орлов, 2004). Очевидно, такое переключение обусловлено доступностью и таким обилием отходов, что при меньшей калорийности относительно обычных жертв их потребление становилось энергетически более выгодным, так как не требовало поиска добычи и охоты на неё. Согласно проведённым исследованиям охоты щук (Esocidae), форелей (Salmonidae), малоротого Micropterus dolomieu, большеротого M. salmoides и каменного (Serranidae) окуней, только у форели и большеротого окуня атаки на жертв были успешными в 60–70% случаях, в то время как у других – менее чем в 35% (Яржомбек, 2016). На участке III района в рассматриваемый период керчак откармливался терпугом и его головами. Причём потребление голов терпуга, вероятно, связано со вкусовыми предпочтениями хищника. Дело в том, что все траления в районе исследований сопровождались переработкой промысловых видов рыб, отходами которой были их головы. Исходя из численности этих видов в уловах, на участках I, II, IV это были в основном головы минтая, а также северной двухлинейной камбалы, на III – терпуга, северной двухлинейной камбалы и минтая. Однако только головы терпуга на участке III играли в питании керчака существенную роль (28.5%).
По способу питания керчака относят к типичным хищникам-засадчикам, ведущим сравнительно малоподвижный образ жизни (Чучукало и др., 1999; Токранов, 2009, 2017, 2019; Tokranov, Orlov, 2013). Такие хищники, как правило, оседлые или обитают на определенной территории, размеры которой, очевидно, зависят от её кормовой возможности. В табл. 6 приведены уловы керчака, минтая и терпуга в тралениях, выполненных на участках с близкими глубинами и координатами за период 1–10 сут. Показано, что даже в течение одних суток плотности этих видов могут значительно варьировать. Это означает, что в условиях динамичной кормовой обстановки площади занимаемых керчаком территорий постоянно меняются. Более того, в таких условиях у керчаков отсутствует жёсткая привязанность к определенной территории. Она может смещаться в сторону участков со скоплениями кормовых объектов. Предположительно на перераспределение этих хищников существенное влияние может оказывать промысел. С одной стороны, в районе ведения промысла керчаки постоянно облавливаются, и на освобождаемые таким образом территории могут перемещаться особи с сопредельных участков. С другой стороны, в период промысла происходит осаждение отходов рыбопереработки, вследствие обилия и доступности которых хищники могут временно скапливаться на таких участках. При этом их стратегия добычи пищи меняется. Керчаки из засадчиков становятся пасущимися хищниками-собирателями или же сочетают эти стратегии.
Таблица 6.
Данные некоторых донных тралений с приловом многоиглого керчака Myoxocephalus polyacanthocephalus, направленных на лов минтая Gadus chalcogrammus и северного однопёрого терпуга Pleurogrammus monopterygius у восточного побережья северных Курильских островов и Юго-Восточной Камчатки в 1997 г.
| Дата (число, месяц) |
Координаты | Глубина, м | Плотность распределения, кг/км2 | |||||
|---|---|---|---|---|---|---|---|---|
| с.ш. | в.д. | начальная | конечная | средняя | керчак | минтай | терпуг | |
| 27.08 | 51°35′48′′ | 158°19′12′′ | 260 | 265 | 262.5 | 109.5 | 4929 | |
| 30.08 | 51°35′48′′ | 158°18′18′′ | 260 | 260 | 260.0 | 138.4 | 3328 | |
| 23.08 | 50°47′00′′ | 157°29′00′′ | 158 | 160 | 159.0 | 25.1 | 1752 | |
| 18.09 | 50°47′30′′ | 157°28′00′′ | 157 | 161 | 159.0 | 181.0 | 9696 | |
| 30.09 | 50°44′42′′ | 157°14′42′′ | 101 | 115 | 105.7 | 1928.0 | 23 661 | |
| 30.09 | 50°44′18′′ | 157°15′00′′ | 108 | 115 | 110.3 | 516.0 | 10 442 | |
| 29.09 | 50°44′30′′ | 157°12′00″′′ | 102 | 105 | 103.5 | 181.5 | 41 076 | |
| 01.10 | 50°44′42′′ | 157°12′18′′ | 100 | 108 | 105.3 | 99.5 | 2355 | |
| 02.10 | 50°40′00′′ | 157°20′00′′ | 156 | 160 | 158.0 | 78.4 | 2293 | |
| 02–03.10 | 50°40′00′′ | 157°19′00′′ | 150 | 160 | 155.0 | 130.9 | 6698 | |
| 03.10 | 50°39′30′′ | 157°15′00′′ | 137 | 140 | 138.5 | 99.0 | 1615 | |
| 12.10 | 50°39′00′′ | 157°15′30′′ | 141 | 142 | 141.5 | 111.0 | 1804 | |
| 11.10 | 50°39′00′′ | 157°13′30′′ | 130 | 135 | 132.5 | 50.9 | 1828 | |
| 13.10 | 50°39′00′′ | 157°13′30′′ | 128 | 138 | 133.0 | 97.5 | 2376 | |
ВЫВОДЫ
1. Высокие плотности распределения многоиглого керчака, составившие 1927.9 и 3270.8 кг/км2, отмечены на участках с глубинами соответственно 101–115 м (50°44′42′′ с.ш. и 157°14′42′′ в.д.) и 252–255 м (48°16′00′′ с.ш. и 155°05′00′′ в.д.).
2. Длина тела керчака составляла 30–89 см (в среднем 47.8 ± 0.5) см, масса – 300–11 000 (2321 ± ± 90) г. Наиболее многочисленными были особи FL 36–50 см (68.9% общего количества рыб). Соотношение самок к самцам составило 1.2 : 1.0.
3. Объекты питания керчака представлены 39 таксонами. Основу питания составили рыбы (56.2% массы пищи). На отходы рыбопереработки пришлось 19.6%, на десятиногих ракообразных – 18.6%, на моллюсков – 5.1%, на прочих – 0.5%. С ростом керчака десятиногие ракообразные в питании замещались рыбами.
4. В уловах с керчаком в целом по району с частотой встречаемости ≥50% отмечены 21 вид рыб и командорский кальмар, с встречаемостью >90% – минтай, тихоокеанская треска, северная двухлинейная камбала, большеглазый триглопс и узкозубая палтусовидная камбала, со встречаемостью 100% – минтай и северная двухлинейная камбала.
Список литературы
Борец Л.А. 1995. Донные ихтиоцены российского шельфа дальневосточных морей: состав, структура, элементы функционирования и промысловое значение: Автореф. дис. … канд. биол. наук. Владивосток: ИБМ ДВО РАН, 48 с.
Борец Л.А. 1997. Донные ихтиоцены российского шельфа дальневосточных морей: состав, структура, элементы функционирования и промысловое значение. Владивосток: Изд-во ТИНРО-центр, 217 с.
Борец Л.А. 2000. Аннотированный список рыб дальневосточных морей. Владивосток: Изд-во ТИНРО-центр, 192 с.
Глубоков А.И., Орлов А.М. 2004. Некоторые морфофизиологические показатели и особенности питания многоиглого керчака Myoxocephalus polyacanthocephalus (Cottidae, Pisces) из западной части Берингова моря // Вопр. рыболовства. Т. 5. № 3 (19). С. 425–438.
Ким Сен Ток. 2001. Зимние миграции шельфовых рыб в зону материкового склона юго-западного Сахалина // Вопр. ихтиологии. Т. 41. № 5. С. 593–604.
Лакин Г.Ф. 1973. Биометрия. М.: Высш. шк., 343 с.
Линдберг Г.У. 1927. Промысловые рыбы Дальнего Востока и их использование // Производительные силы Дальнего Востока. Вып. 4. Животный мир. Хабаровск; Владивосток: Книж. дело. С. 19–59.
Линдберг Г.У., Красюкова З.М. 1987. Рыбы Японского моря и сопредельных частей Охотского и Желтого морей. Ч. 5. Л.: Наука, 526 с.
Матвеев А.А., Терентьев Д.А. 2016. Промысел, многолетняя динамика биомассы, распределение и размерный состав массовых видов рогатковых Cottidae у западного побережья Камчатки // Исслед. вод. биол. ресурсов Камчатки и сев.-зап. части Тихого океана. № 41. С. 17–42. https://doi.org/10.15853/2072-8212.2016.41.17-42
Напазаков В.В. 2008. Питание и пищевые отношения хищных рыб в зал. Шелихова (Охотское море) // Изв. ТИНРО. Т. 152. С. 215–224.
Напазаков В.В. 2015. Трофический статус и пищевые отношения массовых хищных рыб западнокамчатского шельфа // Вопр. ихтиологии. Т. 55. № 1. С. 63–73. https://doi.org/10.7868/S0042875215010154
Напазаков В.В., Чучукало В.И. 2003. Пищевые рационы и трофический статус массовых видов рогатковых рыб (Cottidae) в западной части Берингова моря в осенний период // Вопр. ихтиологии. Т. 43. № 2. С. 200–208.
Орлов А.М. 1998. Демерсальная ихтиофауна тихоокеанских вод северных Курильских островов и юго-восточной Камчатки // Биология моря. Т. 24. № 3. С. 146–160.
Орлов А.М. 2010. Количественное распределение демерсального нектона тихоокеанских вод северных Курильских островов и юго-восточной Камчатки. М.: Изд-во ВНИРО, 335 с.
Орлов А.М., Токранов А.М. 2008. Особенности распределения и динамика уловов некоторых потенциально промысловых видов рогатковых рыб (Cottidae) в тихоокеанских водах северных Курильских островов и юго-восточной Камчатки // Матер. Междунар. конф. “Современное состояние водных биоресурсов”. Новосибирск: Агрос. С. 173–178.
Панченко В.В., Пущина О.И. 2004. Биологическая характеристика керчаковых рыб рода Myoxocephalus (Cottidae) зал. Петра Великого Японского моря // Изв. ТИНРО. Т. 138. С. 120–153.
Парин Н.В., Евсеенко С.А., Васильева Е.Д. 2014. Рыбы морей России: аннотированный каталог. М.: Т-во науч. изд. КМК, 733 с.
Пущина О.И., Соломатов С.Ф. 2010. Трофические связи хищных рыб зал. Петра Великого в летний период // Матер. Междунар. науч.-техн. конф. “Актуальные проблемы освоения биологических ресурсов Мирового океана”. Владивосток: Изд-во Дальрыбвтуз. Ч. 1. С. 91–95.
Пущина О.И., Соломатов С.Ф., Калчугин П.В., Будникова Л.Л. 2016. Питание и пищевые отношения массовых видов рогатковых (Cottidae, Pisces) зал. Петра Великого (Японское море) в летний период // Изв. ТИНРО. Т. 184. С. 186–203. https://doi.org/10.26428/1606-9919-2016-184-186-203
Руководство по изучению питания рыб в естественных условиях. 1961. М.: Изд-во АН СССР, 263 с.
Токранов А.М. 1985. Биология массовых видов рогатковых (семейство Cottidae) прикамчатских вод: Автореф. дис. … канд. биол. наук. Владивосток: ДВНЦ АН СССР, 22 с.
Токранов А.М. 1986. Питание многоиглого керчака Myoxocephalus polyacanthocephalus Pallas и керчака-яока M. jaok (Cuvier) (Cottidae) в прибрежных водах Камчатки // Вопр. ихтиологии. Т. 26. № 6. С. 980–989.
Токранов А.М. 2009. Особенности биологии донных и придонных рыб различных семейств в прикамчатских водах: Автореф. дис. … докт. биол. наук. Владивосток: ИБМ ДВО РАН, 83 с.
Токранов А.М. 2014. Рогатковые рыбы (Cottidae) прикамчатских вод и проблемы использования их ресурсов // Сб. докл. Всерос. конф. “Водные и экологические проблемы, преобразование экосистем в условиях глобального изменения климата”. Хабаровск: Изд-во ИВЭП ДВО РАН. С. 162–165.
Токранов А.М. 2017. Рогатковые рыбы рода Myoxocephalus (Cottidae) прикамчатских вод и проблемы использования их ресурсов // Тр. V Балтийского морского форума Всерос. науч. конф. “Водные биоресурсы, аквакультура и экология водоемов”. Калининград: Изд-во КГТУ. С. 75–80.
Токранов А.М. 2019. Трофические группировки рогатковых рыб (Cottidae) в прикамчатских водах // Принципы экологии. Т. 8. № 3. С. 123–132. https://doi.org/10.15393/j1.art.2019.9662
Токранов А.М., Орлов А.М. 2011. Особенности распределения и экологии многоиглого керчака Myoxocephalus polyacanthocephalus (Pallas) (Cottidae) в тихоокеанских водах северных Курильских островов и юго-восточной Камчатки // Матер. Дальневост. регион. конф. “Геология, география, биологическое разнообразие и ресурсы Северо-Востока России”. Магадан: Изд-во СВНЦ ДВО РАН. С. 167–169.
Токранов А.М., Орлов А.М. 2013. Особенности распределения, экологии и динамика уловов многоиглого керчака Myoxocephalus polyacanthocephalus (Cottidae) в тихоокеанских водах северных Курильских островов и юго-восточной Камчатки // Биол. журн. Армении. Т. 4. № 65. С. 44–52.
Тупоногов В.Н., Орлов А.М., Мухаметов И.Н. Сравнительный анализ результатов донных траловых съемок разными судами на островном склоне северных Курил (методические аспекты интеркалибровочных работ) // Тр. ВНИРО. 2006. Т. 146. С. 181–190.
Федоров В.В. 2000. Видовой состав, распределение и глубины обитания видов рыбообразных и рыб северных Курильских островов // Промыслово-биологические исследования рыб в тихоокеанских водах Курильских о-вов и прилежащих районах Охотского и Берингова морей в 1992–1998 гг. М.: Изд-во ВНИРО. С. 7–41.
Федоров В.В., Черешнев И.А., Назаркин М.В. и др. 2003. Каталог морских и пресноводных рыб северной части Охотского моря. Владивосток: Дальнаука, 204 с.
Чучукало В.И. 2006. Питание и пищевые отношения нектона и нектобентоса в Дальневосточных морях. Владивосток: Изд-во ТИНРО-центр, 484 с.
Чучукало В.И., Лапко В.В., Кузнецова Н.А. и др. 1999. Питание донных рыб на шельфе и материковом склоне северной части Охотского моря летом 1997 г. // Изв. ТИНРО. Т. 126. С. 24–57.
Шейко Б.А., Федоров В.В. 2000. Класс Cephalaspidomorphi – Миноги. Класс Chondrichthyes – Хрящевые рыбы. Класс Holocephali – Цельноголовые. Класс Osteichthyes – Костные рыбы // Каталог позвоночных животных Камчатки и сопредельных морских акваторий. Петропавловск-Камчатский: Камчат. печат. двор. С. 7–69.
Шмидт П.Ю. 1950. Рыбы Охотского моря. М.; Л.: Изд-во АН СССР, 370 с.
Яржомбек А.А. 2016. Образ жизни и поведение промысловых рыб. М.: Изд-во ВНИРО, 200 с.
Masuda H., Amaoka K., Araga C. et al. 1984. The fishes of the Japanese Archipelago. V. 1. Tokyo: Tokai Univ. Press, 437 p.
Mecklenburg C.W., Mecklenburg T.A., Thorsteinson L.K. 2002. Fishes of Alaska. Bethesda: Am. Fish. Soc, 1037 p.
Ormseth O.A., TenBrink T.T. 2010. Gulf of Alaska sculpins // NPFMC Gulf of Alaska SAFE. Anchorage: North Pacific Fishery Management Council. P. 777–796.
Spies I., Ormseth O.A., TenBrink T.T. 2012. Bering Sea and Aleutian Islands sculpin // NPFMC Bering Sea and Aleutian Islands SAFE. Anchorage: North Pacific Fishery Management Council. P. 1735–1769.
TenBrink T.T., Buckley T.W. 2012. Resource partitioning among Myoxocephalus sculpins, and their predator–prey relationships with Chionoecetes crabs in the eastern Bering Sea // Mar. Ecol. Prog. Ser. V. 464. P. 221–235. https://doi.org/10.3354/meps09878
Tokranov A.M., Orlov A.M. 2013. Feeding pattern of the great sculpin Myoxocephalus polyacanthocephalus (Cottidae) and its position in the trophic system of near-Kamchatka waters // J. Ichthyol. V. 53. № 11. P. 969–981. https://doi.org/10.1134/S0032945213110088
Дополнительные материалы отсутствуют.
Инструменты
Вопросы ихтиологии


