Известия РАН. Серия физическая, 2020, T. 84, № 9, стр. 1282-1285
Исследование влияния изотермического отжига на параметры металлооксидных пленок CuO, изготовленных спрей-пиролизом и золь-гель методом
В. Е. Полковников 1, *, Д. С. Пермяков 1, С. И. Рембеза 1, Т. Г. Меньшикова 1
1 Федеральное государственное бюджетное образовательное учреждение высшего образования
“Воронежский государственный технический университет”
Воронеж, Россия
* E-mail: polkovnikov.vova.net@yandex.ru
Поступила в редакцию 10.04.2020
После доработки 29.04.2020
Принята к публикации 27.05.2020
Аннотация
Представлены две технологии изготовления пленок оксида меди(II): спрей-пиролиз и золь-гель метод. На примере полученной пленки оксида меди рассмотрен процесс изменения удельного сопротивления пленок при разной температуре в зависимости от времени отжига. Определен фазовый состав, степень кристаллизации и электросопротивление пленки оксида меди.
Полупроводниковые пленки оксида меди(II) p-типа имеют выдающиеся газочувствительные, электропроводящие и оптические свойства [1]. Данный полупроводниковый материал можно получить различными методами: золь-гель, термовакуумным напылением, ВЧ-магнетронным распылением и другими Низкая себестоимость производства и обработки, нетоксичность, а также его электрические и оптические свойства позволяют считать CuO перспективным материалом для использования в преобразователях солнечной энергии и в других изделиях электроники [2–5]. Спрей-пиролиз [6] и золь-гель метод позволяют получить СuO на доступном технологическом оборудовании и с воспроизводимыми электрофизическими свойствами. В методе спрей-пиролиза используются водные растворы солей металлов, которые под давлением сжатого воздуха разбрызгиваются через сопло в виде аэрозоля и осаждаются на нагретую подложку [7]. Температурой подложки определяется возможность кристаллизации пленки в процессе нанесения. Спрей-пиролиз достаточно прост, обладает высокими скоростями нанесения пленки, позволяет изготавливать образцы большой площади. Золь-гель метод позволяет получать металлоксидные пленки из раствора солей металлов. Нанесение пленки на подложку при комнатной температуре осуществляется в основном центрифугированием или окунанием [8]. Преимущества золь-гель метода заключаются в низкотемпературности процессов и в возможности нанесения пленки на любые материалы, в том числе и на пластмассы, однако, синтезированные пленки при этом обладают в основном аморфной структурой, высоким электросопротивлением и термической нестабильностью. Для использования пленок CuO в полупроводниковых приборах необходимо исследовать и оптимизировать режимы термического отжига, приводящего к кристаллизации и стабилизации электрических параметров пленок.
Цель данной работы – отработать технологические режимы спрей-пиролиза и золь-гель метода для изготовления пленок CuO и исследовать влияние метода получения и времени изотермического отжига при температурах 400, 450 и 500°С на особенности кристаллизации и электрические свойства пленок СuO.
Для синтеза пленки CuO методом спрей-пиролиза был приготовлен раствор из хлорида меди (CuCl2 ⋅ 2H2O) объемом 200 мл, в качестве растворителя использовали дистиллированную воду. Раствор бирюзового цвета с молярным содержанием меди 0.1 моль/л перемешивали с помощью магнитной мешалки IKA RH basic 2 при комнатной температуре в течение 10 минут. Распыление раствора производили с помощью аэрографа OPHIR AC004A. Параметры нанесения были выбраны следующие: давление компрессора 1.5 бар, расстояние от источника аэрозоля до подложки 80 см, расход раствора 7 мл/мин. Полученный раствор наносили на нагретые до 300°С предметные стекла для микропрепаратов (ГОСТ 9284-75) размером 26 × 76 × 1 мм, температуру подложки измеряли с помощью пирометра HoldPeak hp-1500. Для поддержания температурного режима процесса нанесения через каждые 6 мин делали паузу длительностью 4 мин. Таким образом было сформировано 5 слоев.
Для создания пленки CuO золь-гель методом, использовали раствор на основе ацетата меди (Cu(CH3COO)2 · H2O), изопропилового спирта (C3H8O) и диэтиламина ((CH3CH2)2NH). Ацетат меди растворяли в изопропиловом спирте в концентрации 0.1 моль/л. Раствор перемешивали на магнитной мешалке 1 ч при комнатной температуре. Для стабилизации раствора использовали диэтиламин, который добавляли покапельно (0.1 мл/мин) при непрекращающемся перемешивании до молярной концентрации 0.01 моль/л. После добавления диэтиламина раствор дополнительно перемешивали в течение 30 мин. В качестве подложек использовали квадратные предметные стекла 26 × 26 × 1 мм, которые были очищены дистиллированной водой и изопропиловым спиртом в ультразвуковой ванне. Пленку наносили центрифугированием при 1500 об./мин в течении 75 с. Всего было нанечено 8 слоев с сушкой между слоями по 10 мин при 250°С. Толщину пленок измеряли с помощью интерференционного микроскопа МИИ-4. Фазовый состав определяли с помощью рентгеновского спектрометра Bruker DIFFRAC EVA3.0 с использованием базы данных ICDD PDF2012.
Для контроля изменения поверхностного сопротивления пленок CuO от температуры и времени отжига, применяли метод измерения сопротивления непосредственно в процессе отжига. Для этого на поверхность исследуемого образца помещали графитовые прижимные контакты. Затем с помощью пишущего мультиметра AM-1109 записывали изменения сопротивления пленки от времени отжига на воздухе. Отжиг образцов сопровождается не только изменением их сопротивления, но и кристаллизацией пленок.
Тип проводимости синтезированных пленок контролировали c помощью термозонда по знаку термоэлектродвижущей силы. Он был определен как дырочный (p-тип). Полученные пленки имеют толщину 1.5 мкм для технологии спрей-пиролиза и 0.440 мкм для золь-гель метода, соответственно. Рентгеновские спектры рис. 1 показали наличие рентгеноаморфного гало в районе 2Θ (20°–24°), по видимому, от стеклянной подложки, и наличие рефлексов, соответствующих моноклинной фазе CuO. Для спрей-пиролиза по положению и количеству рентгенографических пиков можно предположить, что пленка оксида меди сразу после нанесения на подложку при температуре 300°С частично кристаллизована. При этом непосредственно после нанесения пленки на горячую подложку наблюдаются пики 2Θ (31.7°, 35.5° и 38.8°) соответствующие рефлексам от плоскостей (1, 1, 0), (–1, 1, 1) и (1, 1, 1) оксида CuO с моноклинной решеткой типа тенорита. После дополнительного отжига пленки при 500°С в течение 2 ч интенсивность пиков от плоскостей (–1, 1, 1) и (1, 1, 1) увеличилась, и появились новые рефлексы от плоскостей (–2, 0, 2), (0, 2, 0) и (2, 0, 2). Дифракционных максимумов, соответствующих другим соединениям, выявлено не было.
Рис. 1.
Рентгеновские спектры синтезируемых пленок CuO после отжига при разных температурах. Внизу – пленка CuO, изготовленная золь-гель методом с сушкой при 250°С. Вверху – пленка CuO, изготовленная спрей-пиролизом на горячей подложке (T = 300°С).
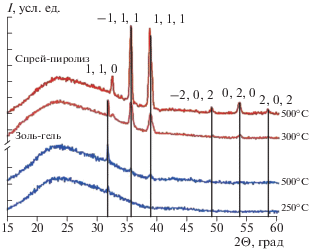
Для пленок, полученных золь-гель методом и прошедших стадию сушки при 250°С, наблюдается единственный слабый рефлекс, при 2Θ (31.7°) соответствующий плоскости CuO (1, 1, 0). В результате отжига пленок в течение 2 ч при 500°С происходит их частичная кристаллизация, и проявляются слабые дополнительные рефлексы от плоскостей CuO: (1, 1, 0) 2Θ (31.7°), (–1, 1, 1) 2Θ (35.5°), (1, 1, 1) 2Θ (38.8°).
Из сравнения рентгенограмм термообработанных образцов, изготовленных спрей-пиролизом и с помощью золь-гель технологий следует, что пленки с частичной кристаллизацией в процессе синтеза (спрей-пиролиз) при температуре отжига 500°С кристаллизуются более полно, чем исходно-аморфные пленки (золь-гель метод).
Процессы кристаллизации пленок CuO сопровождаются изменением их сопротивления. Были определены зависимости изменения поверхностного сопротивления от температуры и времени отжига (рис. 2). Как видно из рис. 2, повышение температуры отжига ускоряет кристаллизацию и стабилизацию сопротивления. При 400°С стабилизация сопротивления идет намного медленнее, чем при 500°С. Это справедливо как для золь-гель метода, так и для спрей-пиролиза. Удельное сопротивление пленки непосредственно после синтеза составляет для спрей-пиролиза 270 Ом ∙ см, а для золь-гель метода 320 Ом ∙ см. Полная стабилизация сопротивления пленок CuO, изготовленных по спрей-пиролиз технологии происходит спустя 33 мин при 500°С, через 80 мин при 450°С и спустя 108 мин при 400°С. Для пленок, изготовленных золь-гель методом, стабилизация сопротивления наступает спустя 28 мин при 500°С, через 75 мин при 450°С и спустя 97 мин при 400°С. Стабилизация сопротивления, вероятно, связана с завершением кристаллизации пленки. Конечные сопротивления пленок после отжига при исследуемых температурах в течение 2 ч составили 58.3 Ом ∙ см для спрей-пиролиза и 20 Ом ∙ см для золь-гель метода.
Рис. 2.
Изменение относительного сопротивления пленок CuO от времени отжига при температурах 400, 450 и 500°С. Внизу – пленка CuO, изготовленная спрей-пиролизом. Вверху – пленка CuO, изготовленная золь-гель методом.
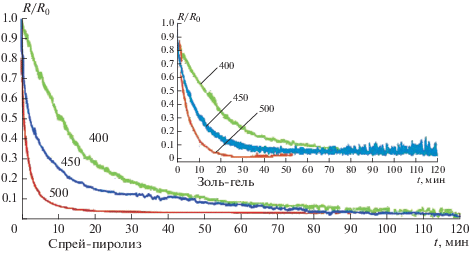
Изменение электросопротивления тонких пленок в процессе их отжига отражает степень упорядочения структуры оксида меди и может служить индикатором процесса кристаллизации пленок CuO.
Параметры процессов кристаллизации можно оценить по величине энергии активации кристаллизации Q [9], которую в нашем случае можно определить из графиков температурных зависимостей времени релаксации τ от температуры T отжига пленок.
где τ – время релаксации процесса, Q – энергия активации кристаллизации, k – постоянная Больцмана.Зависимости логарифма относительного сопротивления от времени отжига при различных температурах удовлетворительно спрямляются, т.е. описываются экспоненциальными зависимостями и позволяют рассчитать времена релаксации процессов τ для температур 400, 450 и 500°С для двух методов синтеза пленок CuO (рис. 3). Для пленок, изготовленных спрей-пиролизом, времена релаксации для разных температур изменяются в пределах от 1000 до 200 с, а для золь-гель метода от 1250 до 300 с. По формуле (1) для трех разных температур отжига были рассчитаны энергии активации процессов кристаллизации [9]. Значения Q составили: для пленок, изготовленных спрей-пиролизом 0.68 эВ, и для пленок, синтезированных золь-гель методом 0.54 эВ. Таким образом, можно заключить, что при синтезе пленок на горячих подложках процесс кристаллизации пленок характеризуется более высоким значением энергии активации, а кристаллизация аморфных пленок (золь-гель методом) происходит с меньшим значением энергии активации процесса.
Рис. 3.
Зависимости изменения поверхностного сопротивления пленок CuO от температуры и времени отжига в логарифмическом масштабе. Внизу: пленка CuO, синтезированная спрей-пиролизом. Вверху: пленка CuO, синтезированная золь-гель методом.
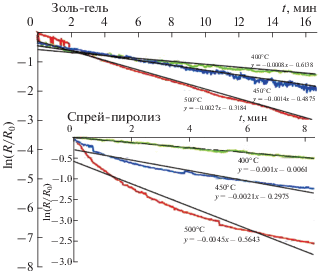
Таким образом, были определены режимы синтеза пленок CuO р-типа проводимости с помощью спрей-пиролиза и золь-гель метода из растворов солей меди. Установлено, что сразу после синтеза пленки имеют аморфную структуру и могут быть кристаллизованы при температурах 400–500°С. После кристаллизации пленок единственной фазой является моноклинная фаза CuO с кристаллической решеткой типа тенорита. В процессе кристаллизации пленок происходит снижение их удельного сопротивления по экспоненциальному закону. Пленка CuO после термической обработки снижает свое сопротивление и увеличивает степень кристаллизации, причем, чем выше температура, тем быстрее происходит стабилизация сопротивления и кристаллизация. Прямыми измерениями электросопротивления пленок CuO в процессе отжига были определены характерные времена релаксации электросопротивления для разных температур отжига и для пленок, синтезированных двумя различными методами. Поскольку величина электросопротивления пленок CuO пропорциональна степени их кристаллизации, то из экспоненциальных зависимостей относительного сопротивления при постоянной температуре, были рассчитаны значения времени релаксации и определены величины энергии активации кристаллизации для двух методов синтеза пленок CuO. Синтезированные пленки CuO после соответствующей термообработки могут быть использованы при разработке электронных устройств и приборов.
Список литературы
Yang Y., Xu D. // Sci. Rep. 2016. V. 6. Art. № 35158.
Dhas R., Dinu A., Christy A.J. et al. // Asian J. Appl. Sci. 2014. V. 7. P. 671.
Shariffudin S.S., Khalid S.S., Sahat N.M. et al. // IOP Conf. Ser. Mater. Sci. Engin. 2015. V. 99. Art. № 012007.
Lim Y.-F., Chua C.S., Lee C.J.J., Chi D. // Phys. Chem. Chem. Phys. 2014. V. 16. P. 25928.
Meshram S.P., Adhyapak P.V., Mulik U.P., Amalnerkar D.P. // Chem. Engin. J. 2012. V. 158. P. 204.
Chafi F.Z., Bahmad L., Hassanain N. et al. // arXiv: 1807.09697. 2018.
Loredana M., Florentina E.I. // Annals. Oradea Univ. Fasc. Manag. Technol. Engin. 2008. V. 7. P. 17.
Baturay S., Tombak A., Batibay D. et al. // Appl. Surf. Sci. 2019. V. 477. P. 91.
Горелик С.С. Рекристаллизация металлов и сплавов. Москва: Металлургия, 1967.
Дополнительные материалы отсутствуют.
Инструменты
Известия РАН. Серия физическая


