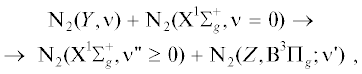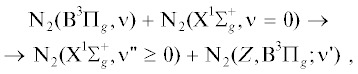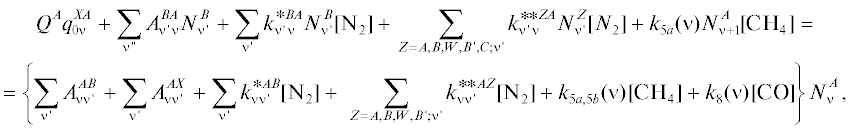Известия РАН. Серия физическая, 2022, T. 86, № 3, стр. 414-422
Моделирование колебательных населенностей метастабильного молекулярного азота в атмосфере титана во время высыпания высокоэнергичных частиц
А. С. Кириллов 1, *, Р. Вернер 2, В. Гинева 2
1 Федеральное государственное бюджетное научное учреждение
Полярный геофизический институт
Апатиты, Россия
2 Институт космических исследований и технологий Болгарской академии наук
Стара Загора, Болгария
* E-mail: kirillov@pgia.ru
Поступила в редакцию 15.10.2021
После доработки 05.11.2021
Принята к публикации 22.11.2021
- EDN: XXHRPI
- DOI: 10.31857/S0367676522030103
Аннотация
Исследована кинетика триплетных состояний молекулярного азота на высотах верхней и средней атмосферы Титана во время высыпания в атмосферу высокоэнергичных электронов и космических лучей. Впервые при расчете концентраций метастабильного молекулярного азота ${{{\text{N}}}_{2}}\left( {{{{\text{A}}}^{3}}\Sigma _{u}^{ + }} \right)$ учитываются столкновительные молекулярные процессы с атмосферными составляющими. Численно показано, что неупругие молекулярные столкновения приводят к преимущественной аккумуляции энергии электронного возбуждения метастабильного азота на нижнем колебательном уровне ν = 0 на высотах средней атмосферы.
ВВЕДЕНИЕ
Молекулярный азот N2 является главным молекулярным газом в атмосферах Титана (спутник Сатурна), Тритона (спутник Нептуна) и Плутона. Вторым по общей концентрации газом в атмосферах упомянутых планет является метан СН4. Взаимодействие высокоэнергичных солнечных ультрафиолетовых фотонов, заряженных частиц из магнитосферы Сатурна, космических лучей с газами атмосферы Титана приводит к образованию потоков вторичных электронов во время процессов ионизации молекул [1]. Вторичные электроны при неупругом взаимодействии с газами N2 и CH4 вызывают диссоциацию и ионизацию молекул данных газов, что приводит к образованию атомов H, C, N и некоторых радикалов, необходимых для синтеза сложных органических молекул. В химических процессах с участием различных атомов и радикалов образуется множество многоатомных газообразных молекул. Образованные молекулы могут превращаться в органические аэрозоли в реакциях синтеза [2–5]. Авторы [5] указали на тот факт, что важность фотолиза и диссоциации CH4 связана с продуктами CH3, CH2, CH, являющимися предшественниками всех других углеводородов, наблюдаемых в экспериментальных наблюдениях. Более того, авторы [5] подчеркнули важную роль электронно-возбужденного молекулярного азота в возбуждении и диссоциации других молекул, но эти процессы до сих пор не учитывались в фотохимических моделях.
В работах [6, 7] электронно-возбужденные молекулы N2 в газовой смеси молекулярного азота и метана N2–CH4 были исследованы как важный агент в химических реакциях и процессах диссоциации. Синтез углеводородов, нитрилов, цианидов и других веществ в смеси N2 и CH4 для условий лабораторного разряда исследован экспериментально и теоретически в работах [8–10]. В этих работах было показано, что электронно-возбужденные молекулы ${{{\text{N}}}_{2}}\left( {{{{\text{A}}}^{3}}\Sigma _{u}^{ + }} \right)$ участвуют в диссоциации молекул CH4 с образованием радикалов CH3 и CH2 в неупругих столкновениях. Химические процессы с участием множества радикалов приводят к образованию углеводородов, нитрилов, цианидов и т.д. Поэтому исследование кинетики триплетных электронно-возбужденных молекул азота очень важно при моделировании химического состава атмосферы Титана, поскольку возбужденные молекулы N2 инициируют образование атомов и радикалов, участвующих в сложном химическом цикле атмосферы.
Кроме того, с уменьшением высоты и ростом давления в атмосфере усиливается роль неупругих молекулярных столкновений в гашении электронно-возбужденных состояний молекул. В недавних работах [11, 12] впервые было показано, что взаимодействие метастабильного молекулярного азота ${{{\text{N}}}_{2}}\left( {{{{\text{A}}}^{3}}\Sigma _{u}^{ + }} \right)$ с молекулами СО играет важную роль в электронном возбуждении молекул угарного газа в верхних атмосферах Титана, Тритона, Плутона. При этом роль данного взаимодействия усиливается с понижением высоты и ростом плотности атмосферы.
В работах [13, 14] теоретически и экспериментально исследовалось взаимодействие метастабильного молекулярного азота ${{{\text{N}}}_{2}}\left( {{{{\text{A}}}^{3}}\Sigma _{u}^{ + }} \right)$ с молекулами углеводородов СН4 (метана), С2Н2 (ацетилена), С2Н4 (этилена) и было показано, что при данных неупругих столкновениях эффективно протекают процессы диссоциации с образованием атомов водорода и химически активных радикалов СН3, С2Н, С2Н3. Поэтому высыпающиеся в атмосферу Титана высокоэнергичные частицы являются источником образования электронно-возбужденных молекул, которые в свою очередь могут инициировать образование различных химически активных составляющих на различных высотах атмосферы Титана.
Главная цель данной работы состоит в моделировании колебательных населенностей триплетных электронно-возбужденных состояний молекулярного азота на высотах верхней и средней атмосферы Титана во время высыпаний высокоэнергичных электронов из магнитосферы Сатурна и космических лучей. Моделирование колебательных населенностей триплетных состояний молекул азота N2 на высотах атмосферы Титана выполнены с учетом вклада как излучательных, так и неупругих столкновительных процессов.
КОНСТАНТЫ ГАШЕНИЯ ЭЛЕКТРОННО-ВОЗБУЖДЕННОГО МОЛЕКУЛЯРНОГО АЗОТА ПРИ СТОЛКНОВЕНИИ С N2, CH4, CO МОЛЕКУЛАМИ
На рис. 1 приведена схема всех колебательных уровней триплетных состояний ${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ B3Πg, W3Δu, ${{{\text{B}}}^{{'3}}}\Sigma _{u}^{ - },$ C3Πu, рассмотренных в данной работе. Образованные во время ионизации высокоэнергичные вторичные электроны эффективно возбуждают различные триплетные состояния молекулярного азота N2 при неупругих столкновениях:
(1)
$\begin{gathered} e + {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{X}}}^{1}}\Sigma _{{\text{g}}}^{ + },\nu = 0) \\ \to \,\,{{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },{{{\text{B}}}^{3}}{{\Pi }_{g}},{{W}^{3}}{{\Delta }_{u}},{{{\text{B}}}^{{'3}}}\Sigma _{u}^{ + },{{C}^{3}}{{\Pi }_{u}},\nu \geqslant 0) + e. \\ \end{gathered} $Рис. 1.
Схема колебательных уровней триплетных состояний ${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ B3Πg, W3Δu, ${{{\text{B}}}^{{'3}}}\Sigma _{u}^{ - },$ C3Πu.

Излучение полос Вегарда–Каплана (VK), первой положительной (1PG) и второй положительной (2PG) систем, полос Ву–Бенеша (WB) и инфракрасного послесвечения (IRA) во время спонтанных излучательных переходов
(2а)
${{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu ) \to {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{X}^{1}}\Sigma _{g}^{ + },\nu {\kern 1pt} ') + h{{\nu }_{{{\text{VK}}}}},$(2б)
${{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{B}}}^{3}}{{\Pi }_{g}},\nu ) \leftrightarrow {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\,\,\nu {\kern 1pt} ') + h{{\nu }_{{{\text{1PG}}}}},$(2в)
${{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{C}}}^{3}}{{\Pi }_{u}},\nu ) \to {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{B}}}^{3}}{{\Pi }_{g}},\nu {\kern 1pt} ') + h{{\nu }_{{{\text{2PG}}}}},$(2г)
${{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{W}}}^{3}}{{\Delta }_{u}},\nu ) \leftrightarrow {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{B}}}^{3}}{{\Pi }_{g}},\nu {\kern 1pt} ') + h{{\nu }_{{{\text{WB}}}}},$(2д)
${{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{B}}}^{{'3}}}\Sigma _{u}^{ - },\nu ) \leftrightarrow {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{B}}}^{3}}{{\Pi }_{g}},\nu {\kern 1pt} ') + h{{\nu }_{{{\text{IRA}}}}}$приводит к тому, что энергия электронного возбуждения перераспределяется между различными колебательными уровнями триплетных электронно-возбужденных состояний молекулы азота. Коэффициенты Эйнштейна для дипольно-разрешенных переходов (2б)–(2д) имеют высокие значения [15], поэтому излучение вышеупомянутых полос молекулярного азота играет важную роль в электронной кинетике N2 и перераспределении энергии возбуждения между триплетными состояниями азота на различных высотах верхней и средней атмосферы Титана.
В работах [16–18] было показано, что внутримолекулярный и межмолекулярный перенос энергии играет очень важную роль в процессах тушения электронного возбуждения молекулярного азота N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ B3Πg, W3Δu, ${{{\text{B}}}^{{'3}}}\Sigma _{u}^{ - },$ C3Πu) при столкновениях с невозбужденными молекулами N2. В этих работах было получено хорошее согласие рассчитанных констант скоростей неупругих процессов с многочисленными экспериментальными данными. Аналитические выражения, основанные на приближениях Ландау–Зинера и Розена–Зинера, были использованы при расчетах коэффициентов скоростей электронного тушения. Было показано, что процессы внутримолекулярного и межмолекулярного переноса энергии важны в тушении триплетных электронно-возбужденных состояний молекулярного азота.
Для условий высокого давления на высотах нижней и средней атмосферы Титана при рассмотрении кинетических процессов необходимо учесть процессы электронного тушения всех триплетных состояний при неупругих молекулярных столкновениях. Поэтому в случае триплетных состояний молекулярного азота мы рассматриваем следующие внутримолекулярные процессы переноса энергии возбуждения:
(3а)
${{{\text{N}}}_{{\text{2}}}}(Y,\nu ) + {{{\text{N}}}_{2}} \to {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{B}}}^{3}}{{\Pi }_{g}},\nu {\kern 1pt} ') + {{{\text{N}}}_{2}},$(3б)
${{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{B}}}^{3}}{{\Pi }_{g}},\nu ) + {{{\text{N}}}_{2}} \to {{{\text{N}}}_{2}}(Y;\nu {\kern 1pt} ') + {{{\text{N}}}_{2}},$Также на высотах нижней и средней атмосферы Титана необходимо учитывать столкновения молекул азота с молекулами метана CH4. В работах [19, 20] были измерены константы скорости тушения N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 1–6) молекулой метана и было показано, что для ненулевых колебательных уровней N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν > 0) происходит колебательная релаксация при неупругих столкновениях с молекулой CH4
(5a)
$\begin{gathered} {{{\text{N}}}_{2}}({{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu = 1 - 6) + {\text{C}}{{{\text{H}}}_{4}} \to \\ \to \,\,{{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}{{\Sigma }_{u}}^{ + },\nu {\kern 1pt} ' = \nu - 1) + {\text{C}}{{{\text{H}}}_{4}}. \\ \end{gathered} $Электронное тушение происходит для нулевого колебательного уровня υ = 0 с последующей диссоциацией молекулы метана CH4 [13, 14]
(5б)
$\begin{gathered} {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu = 0) + {\text{C}}{{{\text{H}}}_{4}} \to \\ \to \,\,{{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{X}}}^{1}}\Sigma _{g}^{ + },\nu {\kern 1pt} ') + {\text{C}}{{{\text{H}}}_{3}} + {\text{H}},\,\,{\text{продукты}}\,\,{\text{реакции}}, \\ \end{gathered} $причем скорость тушения для процесса (5б) измерена в [21].
В работе [22] исследовалось тушение N2(B3Πg, ν = 1–12) молекулами CH4, где было показано, что молекулы метана достаточно эффективны в тушении электронно-возбужденного состояния B3Πg
(6)
$\begin{gathered} {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{B}}}^{3}}{{\Pi }_{g}},\nu ) + {\text{C}}{{{\text{H}}}_{4}} \to \\ \to {\kern 1pt} \,{{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{X}}}^{1}}\Sigma _{g}^{ + },\nu {\kern 1pt} ') + {\text{C}}{{{\text{H}}}_{3}} + {\text{H}}~,\,\,{\text{продукты реакции}}, \\ \end{gathered} $при этом процесс (6) протекает со скоростями, близкими к газокинетическим значениям. Измеренные в [22] константы скоростей тушения N2(B3Πg) при столкновениях (6) находились в диапазоне от 1.6 ∙ 10–10 см3 ⋅ с–1 для ν = 3, 4 до ~5.0 ∙ 10–10 см3 ⋅ с–1 для ν = 11, 12. Поэтому мы используем усредненную константу k6 = 2.8 ∙ · 10–10 см3 ⋅ с–1 для всех двенадцати ν = 1–12 колебательных уровней состояния B3Πg. То же самое значение k7 = 2.8 ∙ 10–10 см3 ⋅ с–1 предлагается и для неупругих столкновений:
(7)
$\begin{gathered} {{{\text{N}}}_{{\text{2}}}}(Y,\nu ) + {\text{C}}{{{\text{H}}}_{4}} \to {\text{N}}_{2}^{*} + {\text{C}}{{{\text{H}}}_{3}} + {\text{H}}, \\ {\text{продукты}}\,\,{\text{реакции}}, \\ \end{gathered} $где Y = W3Δu (ν = 1–21), ${{{\text{B}}}^{{'3}}}\Sigma _{u}^{ - }$ (ν = 0–15), C3Πu (ν = 0–4); а ${\text{N}}_{{\text{2}}}^{*}$ означает электронно-возбужденные и колебательно-возбужденные молекулы азота. Коэффициенты скорости тушения k6 = k7 = = 2.0 ∙ 10–11 см3 ⋅ с–1 процессов (6) и (7) для нулевых колебательных уровней N2(B3Πg, ν = 0) и N2(W3Δu, ν = 0) приняты согласно [23].
В работах [11, 12] была показана очень важная роль неупругих столкновений с молекулами CO в верхней атмосфере Титана, Тритона, Плутона для нижних колебательных уровней состояния ${{{\text{A}}}^{3}}\Sigma _{u}^{ + }.$ Поэтому при расчетах будем учитывать столкновения
с коэффициентами скоростей, рассчитанными в [17]. Также мы пренебрегаем столкновениями с молекулами водорода, поскольку концентрации [H2] намного меньше, чем [CH4] [24, 25] и константы взаимодействия N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + }$) и молекулой H2 принимают очень малые значения [26]. Поэтому мы учитываем только столкновения (8) с молекулами CO.
Все упомянутые процессы тушения триплетного электронно-возбужденного молекулярного азота приведены в табл. 1 с диапазоном констант скоростей взаимодействия. В дополнение к рассмотренным процессам в табл. 1 также указан внутримолекулярный процесс переноса энергии при столкновении с молекулой N2
(9)
$\begin{gathered} {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu = 0{\kern 1pt} - {\kern 1pt} 5) + {{{\text{N}}}_{2}} \to \\ \to \,\,{{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{X}}}^{1}}\Sigma _{g}^{ + },\nu {\kern 1pt} ' = \nu + 25) + {{{\text{N}}}_{2}} \\ \end{gathered} $Таблица 1.
Константы скоростей процессов с участием электронно-возбужденного азота
| Процесс | Диапазон констант скоростей (см3 · с–1) | Ссылки |
|---|---|---|
| N2(A3$\Sigma _{u}^{ + }$, ν = 0 –5) + N2 → N2(X1$\Sigma _{g}^{ + }$, ν' = ν + 25) + N2 | ≤3.7 ∙ 10–16 | [27, 28] |
| N2(A3$\Sigma _{u}^{ + }$, ν ≥ 2) + N2(X1$\Sigma _{g}^{ + }$, ν = 0) → N2(X1$\Sigma _{g}^{ + }$, ν" ≥ 0) + N2(A3$\Sigma _{u}^{ + }$, ν') | 4.1 ∙ 10–15–1.0 ∙ 10–12 | [17] |
| N2(A3$\Sigma _{u}^{ + }$, ν ≥ 7) + N2 → N2(B3Πg, ν') + N2 N2(A3$\Sigma _{u}^{ + }$, ν ≥ 7) + N2(X1$\Sigma _{g}^{ + }$, ν = 0) → N2(X1$\Sigma _{g}^{ + }$, ν" ≥ 0) + + N2(B3Πg,W3Δu,B'3$\Sigma _{u}^{ - }$; ν') |
2.2 ∙ 10–14–3.2 ∙ 10–11 | [16] |
| N2(A3$\Sigma _{u}^{ + }$, ν ≥ 1) + CH4 → N2(A3$\Sigma _{u}^{ + }$, ν' = ν – 1) + CH4 | k5а = 1.2 ∙ 10–12–5.1 ∙ 10–12 | [19, 20] |
| N2(A3$\Sigma _{u}^{ + }$, ν = 0) + CH4 → N2(X1$\Sigma _{g}^{ + }$, ν') + CH3 + H, продукты реакции | k5б = 3.2 ∙ 10–15 | [21] |
| N2(A3$\Sigma _{u}^{ + }$, ν) + CO(X1Σ+, ν = 0) → N2(X1$\Sigma _{g}^{ + }$, ν" ≥ 0) + CO(A3Π, ν') | 1.8 ∙ 10–12–4.9 ∙ 10–11 | [17] |
| N2(B3Πg, ν) + N2 → N2(A3$\Sigma _{u}^{ + }$,W3Δu,B'3$\Sigma _{u}^{ - }$; ν') + N2 N2(B3Πg, ν) + N2(X1$\Sigma _{g}^{ + }$, ν = 0) → N2(X1$\Sigma _{g}^{ + }$, ν" ≥ 0) + + N2(A3$\Sigma _{u}^{ + }$,B3Πg,W3Δu,B'3$\Sigma _{u}^{ - }$; ν') |
1.7 ∙ 10–11–3.6 ∙ 10–10 | [16] |
| N2(B3Πg, ν) + CH4 → N2(X1$\Sigma _{g}^{ + }$, ν') + CH3 + H, продукты реакции | 1.6 ∙ 10–10–5.1 ∙ 10–10 k6 = 2.8 ∙ 10–10, 2.0 ∙ 10–11 |
[22, 23] см. текст |
| N2(W3Δu,B'3$\Sigma _{u}^{ - }$; ν) + N2 → N2(B3Πg, ν') + N2 N2(W3Δu,B'3$\Sigma _{u}^{ - }$, ν) + N2(X1$\Sigma _{g}^{ + }$, ν = 0) → N2(X1$\Sigma _{g}^{ + }$, ν" ≥ 0) + + N2(A3$\Sigma _{u}^{ + }$,B3Πg,W3Δu,B'3$\Sigma _{u}^{ - }$; ν') |
1.3 ∙ 10–11–5.1 ∙ 10–10 | [16] |
| N2(W3Δu,B'3$\Sigma _{u}^{ - }$, ν) + CH4 → N2(X1$\Sigma _{g}^{ + }$, ν') + CH3 + H, продукты реакции | k7 = 2.8 ∙ 10–10, 2.0 ∙ 10–11 | см. текст |
| N2(C3Πu, ν) + N2(X1$\Sigma _{g}^{ + }$, ν = 0) → N2(X1$\Sigma _{g}^{ + }$, ν" ≥ 0) + + N2(A3$\Sigma _{u}^{ + }$,B3Πg,W3Δu,B'3$\Sigma _{u}^{ - }$,C3Πu; ν') | 1.1 ∙ 10–11–6.3 ∙ 10–11 | [18] |
| N2(C3Πu, ν) + CH4 → N2(X1$\Sigma _{g}^{ + }$, ν') + CH3 + H, продукты реакции | k7 = 2.8 ∙ 10–10 | cм. текст |
для которого в [27] были измерены k9 (ν = 0) = = 3.7 ∙ 10–16 см3 ⋅ с–1 и k9 (ν = 1) = 3.4 ∙ 10–16 см3 ⋅ с–1, а для колебательных уровней ν = 2–5 в [28] приведено аналитическое выражение для расчета констант скоростей.
Приведенные в табл. 1 процессы тушения электронно-возбужденных состояний молекулярного азота относятся к ЕЕ (электронно-электронным) или VV (колебательно-колебательным) процессам трансформации энергии возбуждения. Так к VV процессу относится неупругое взаимодействие (5а), при котором наблюдается резонанс энергий колебательной моды ν4 = 1306 см–1 молекулы метана и колебательного кванта состояния ${{{\text{A}}}^{3}}\Sigma _{u}^{ + }$ молекулы N2 [19].
Остальные процессы VV и VT (колебательно-поступательной) релаксации энергии в данной работе не рассматриваются. Качественные особенности VT релаксации хорошо описываются в рамках одномерной модели Ландау–Теллера [29], которая в дальнейшем была обобщена на трехмерный случай в [30]. В дальнейшем в работах профессора Никитина Е.Е. [31–33] также были учтены различные поправки на притяжение сталкивающихся частиц, изменение частоты осциллятора при взаимодействии, квазиклассичность характера относительного движения. Все эти факторы были рассмотрены при расчете констант VT релаксации для столкновений атмосферных газов в [34, 35]. С учетом всех упомянутых поправок в [34, 35] была представлена аналитическая формула зависимости констант VT релаксации от температуры Т
(10)
$k = A{{T}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}\exp \left( { - \frac{B}{{{{T}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}}} + \frac{C}{{{{T}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}}}} + \frac{D}{T}} \right),$Используя результаты [34, 35] и учитывая, что энергия первого колебательного уровня состояния ${{{\text{A}}}^{3}}\Sigma _{u}^{ + }$ составляет |Eν = 1–Eν = 0| = ΔЕ = 1433 см–1, для процесса VT релаксации
(12)
$\begin{gathered} {{{\text{N}}}_{2}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu = 1) + {{{\text{N}}}_{2}} \to \\ \to \,\,\,{{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu = 0) + {{{\text{N}}}_{2}},~ \\ \end{gathered} $получаем константу $k_{{{\text{VT}}}}^{A},$ зависящую от температуры следующим образом
(13)
$k_{{VT}}^{A} = 1.9 \cdot {{10}^{{ - 7}}}{{T}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}\exp \left( { - \frac{{221}}{{{{T}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}}} + \frac{{70}}{{{{T}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}}}} + \frac{{1030}}{T}} \right).$Для комнатной температуры Т = 300 К расчет согласно формуле (13) дает значение $k_{{VT}}^{A}$ = = 8.8 · 10–19 см3 с–1, что значительно меньше констант скоростей, представленных в табл. 1.
Что касается процессов VV релаксации, то тут необходимо рассмотреть эндотермический и экзотермический процессы
(14)
$\begin{gathered} {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu = 1) + {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{X}}}^{1}}\Sigma _{g}^{ + },\nu = 0) \to \\ \to \,\,{{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu = 0) + {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{X}}}^{1}}\Sigma _{g}^{ + },\nu = 1)--897\,\,{\text{с}}{{{\text{м}}}^{{--1}}}, \\ \end{gathered} $(15)
$\begin{gathered} {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu = 2) + {{{\text{N}}}_{2}}({{{\text{X}}}^{1}}\Sigma _{g}^{ + },\nu = 0) \to \\ \to \,\,{{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{A}}}^{3}}\Sigma _{u}^{ + },\nu = 0) + {{{\text{N}}}_{{\text{2}}}}{\text{(}}{{{\text{X}}}^{1}}\Sigma _{g}^{ + },\nu = 1) + 508\,\,{\text{с}}{{{\text{м}}}^{{--1}}}. \\ \end{gathered} $При этом константы VV релаксации можно рассчитывать по аналогичной формуле (10) [31‒35], поскольку для данных процессов не наблюдается квазирезонанса энергии. Отличительной особенностью расчета констант скоростей неупругого взаимодействия в случае VV релаксации является учет факторов колебаний для обеих сталкивающихся молекул. Кроме того, для двухквантового перехода в процессе (15) необходимо учесть фактор $\frac{{{{x}_{e}}}}{2}$ [34, 39], где xe = 0.95 · 10–2 – постоянная ангармонизма для состояния ${{{\text{A}}}^{3}}\Sigma _{u}^{ + }$ [40]. С учетом всего вышеупомянутого получаем аналитические выражения для констант скоростей процессов (14) и (15):
(17)
$k_{{VV,15}}^{A} = 5.6 \cdot {{10}^{{ - 13}}}{{T}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}\exp \left( { - \frac{{111}}{{{{T}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}}} + \frac{{70}}{{{{T}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}}}} + \frac{{365}}{T}} \right).$Для комнатной температуры Т = 300 К расчет согласно формулам (16) и (17) дает значения $k_{{VV,14}}^{A}$ = = 6.0 · 10–20 см3 ⋅ с–1 и $k_{{VV,15}}^{A}$ = 4.1 · 10–18 см3 ⋅ с–1, которые также значительно меньше констант скоростей, представленных в табл. 1. Поэтому рассмотрением VT и VV процессов (12), (14), (15) в данных расчетах можно пренебречь.
КОЛЕБАТЕЛЬНЫЕ НАСЕЛЕННОСТИ МЕТАСТАБИЛЬНОГО МОЛЕКУЛЯРНОГО АЗОТА ${{{\text{N}}}_{2}}\left( {{{{\text{A}}}^{3}}\Sigma _{{\text{u}}}^{ + }} \right)$ НА РАЗЛИЧНЫХ ВЫСОТАХ АТМОСФЕРЫ ТИТАНА
При расчете колебательных населенностей N триплетных состояний ${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ B3Πg, W3Δu, ${{{\text{B}}}^{{'3}}}\Sigma _{u}^{ - },$ C3Πu мы используем следующие уравнения:
(18б)
$\begin{gathered} {{Q}^{B}}q_{{0\nu }}^{{X{\kern 1pt} B}} + \sum\limits_{Z = A,W,B{\kern 1pt} ',C;\nu {\kern 1pt} '} {A_{{\nu {\kern 1pt} '\nu }}^{{ZB}}N_{{\nu {\kern 1pt} '}}^{Z}} + \sum\limits_{Z = A,W,B{\kern 1pt} ';\nu {\kern 1pt} '} {k_{{\nu {\kern 1pt} '\nu }}^{{*Z{\kern 1pt} B}}N_{{\nu {\kern 1pt} '}}^{Z}[{{{\text{N}}}_{2}}]} \,\,\, + \,\,\sum\limits_{Z = A,B,W,B{\kern 1pt} ',C;\nu {\kern 1pt} '} {k_{{\nu {\kern 1pt} '\nu }}^{{**ZB}}N_{{\nu {\kern 1pt} '}}^{Z}[{{{\text{N}}}_{2}}]} = \\ = \left\{ {\sum\limits_{Z = A,W,B{\kern 1pt} ';\nu {\kern 1pt} '} {A_{{\nu \nu {\kern 1pt} '}}^{{BZ}}} } \right. + \,\,\left. {\sum\limits_{Z = A,W,B{\kern 1pt} ';\nu {\kern 1pt} '} {k_{{\nu \nu {\kern 1pt} '}}^{{*BZ}}[{{{\text{N}}}_{2}}] + } \sum\limits_{Z = A,B,W,B{\kern 1pt} ',C;\nu {\kern 1pt} '} {k_{{\nu \nu {\kern 1pt} '}}^{{**BZ}}[{{{\text{N}}}_{2}}]} + {{k}_{6}}(\nu )[{\text{C}}{{{\text{H}}}_{4}}]} \right\}N_{\nu }^{B}, \\ \end{gathered} $(18в)
$\begin{gathered} {{Q}^{Y}}q_{{0\nu }}^{{X{\kern 1pt} Y}} + \sum\limits_{\nu {\kern 1pt} '} {A_{{\nu {\kern 1pt} '\nu }}^{{BY}}N_{{\nu {\kern 1pt} '}}^{B}} + \sum\limits_{\nu {\kern 1pt} '} {{{k}^{{}}}_{{\nu {\kern 1pt} '{\kern 1pt} \nu }}^{{*B{\kern 1pt} Y}}N_{{\nu {\kern 1pt} '}}^{B}[{{{\text{N}}}_{2}}]} + \,\sum\limits_{Z = A,B,W,B{\kern 1pt} ',C;\nu {\kern 1pt} '} {k_{{\nu {\kern 1pt} '\nu }}^{{**ZY}}N_{{\nu {\kern 1pt} '}}^{Z}[{{{\text{N}}}_{2}}]} = \\ = \left\{ {\sum\limits_{\nu {\kern 1pt} '} {A_{{\nu \nu {\kern 1pt} '}}^{{Y{\kern 1pt} B}}} + } \right.\left. {\,\,\sum\limits_{\nu {\kern 1pt} '} {k_{{\nu \nu {\kern 1pt} '}}^{{*YB}}[{{{\text{N}}}_{2}}]\,\,\,\, + } \sum\limits_{Z = A,B,W,B{\kern 1pt} ';\nu {\kern 1pt} '} {{{k}^{{}}}_{{\nu \nu {\kern 1pt} '}}^{{**YZ}}[{{{\text{N}}}_{2}}]} + {{k}_{7}}(\nu )[{\text{C}}{{{\text{H}}}_{4}}]} \right\}N_{{\nu {\kern 1pt} '}}^{Y}, \\ \end{gathered} $(18г)
$\begin{gathered} {{Q}^{C}}q_{{0\nu }}^{{X{\kern 1pt} C}} + \sum\limits_{\nu {\kern 1pt} ' > \nu } {k_{{\nu {\kern 1pt} '\nu }}^{{**CC}}N_{{\nu {\kern 1pt} '}}^{C}[{{{\text{N}}}_{2}}]} = \\ = \left\{ {\sum\limits_{v'} {A_{{\nu \nu {\kern 1pt} '}}^{{CB}}} \,\, + \,\,\sum\limits_{Z = A,B,W,B{\kern 1pt} ';\nu {\kern 1pt} '} {k_{{\nu \nu {\kern 1pt} '}}^{{**CZ}}[{{{\text{N}}}_{2}}]} + \sum\limits_{\nu {\kern 1pt} ' < \nu } {k_{{\nu \nu {\kern 1pt} '}}^{{**C{\kern 1pt} C}}[{{{\text{N}}}_{2}}]} + \,\,2.8 \cdot {{{10}}^{{ - 10}}}[{\text{C}}{{{\text{H}}}_{4}}]} \right\}N_{\nu }^{{C{\kern 1pt} }}, \\ \end{gathered} $В работах [41, 42] анализируются данные ионосферы Титана, полученные с космического летательного аппарата “Кассини” 26 октября 2004 г. и 16 апреля 2005 г. Авторы [41, 42] представили скорости ионообразования в верхней атмосфере Титана во время высыпаний электронов из магнитосферы Сатурна. Воспользуемся данными работ [41, 42] для энергий магнитосферных электронов Е = 30, 200 и 1000 эВ.
Высотные профили рассчитанных скоростей ионообразования в нижней и средней атмосфере Титана во время взаимодействия космических частиц с атмосферными составляющими были представлены в [43]. Авторы [43] рассчитали образование ионов для дифференциальных энергетических спектров космических лучей при параметрах солнечной модуляции 400, 600 и 1000 МВ. Они указали, что гелиоцентрические потенциалы 400 и 1000 МВ воспроизводят солнечную модуляцию в минимуме и максимуме солнечной активности, соответственно. В наших расчетах мы выбрали случай 600 МВ. На рис. 2 приведены скорости ионообразования как за счет магнитосферных электронов в верхней атмосфере, так и за счет космических лучей в нижней и средней атмосфере Титана.
При расчете скоростей образования QA, QB, QY, QC электронно-возбужденных состояний молекулярного азота согласно (10а)–(10г) во время высыпания высокоэнергичных электронов из магнитосферы Сатурна и при вторжении космических лучей воспользуемся методом деградационных спектров электронов в молекулярном азоте N2 [44, 45].
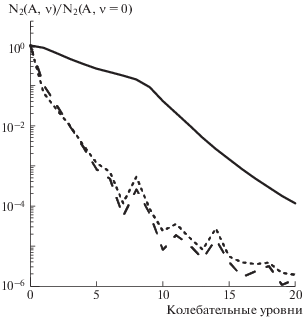
На рис. 3 приведены результаты расчетов относительных концентраций электронно-возбужденных молекул N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0–20)/N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0) на высотах 100, 400 и 1000 км при высыпании высокоэнергичных электронов из магнитосферы Сатурна и вторжении космических лучей. Как показывают результаты расчетов, для всего рассмотренного интервала высот h ≥ 1000 км кривая нормированных концентраций практически не изменяется. Это говорит о том, что излучательные процессы доминируют в кинетике метастабильного молекулярного азота N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + }$) в данном диапазоне высот.
Рис. 3.
Рассчитанные относительные концентрации метастабильного азота N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0–20)/N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0) на высотах 100 (короткие штрихи), 400 (длинные штрихи) и 1000 км (сплошная линия).
Также на рис. 4 проведено сравнение рассчитанных относительных концентраций метастабильного азота N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0–20)/N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0) на высотах 100 и 400 км с результатами расчетов при [CH4] = [CO] = 0 см–3. Как видно из рис. 4, отсутствие учета неупругих взаимодействий молекул азота с молекулами метана и угарного газа приводит к значительным изменениям в результатах расчета на данных высотах. Более того, для высоты 100 км рассчитанные абсолютные концентрации [N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν ≥ 0)] при [CH4] = [CO] = 0 см–3 на порядок превышают значения, рассчитанные при концентрациях молекул метана и угарного газа согласно [24, 25]. Для высоты 1000 км влияние [CH4] и [CO] на результаты расчета концентраций [N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν ≥ 0)] пренебрежимо мало.
Рис. 4.
Рассчитанные относительные концентрации метастабильного азота N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0–20)/N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0) на высотах 100 км (короткие штрихи) и 400 км (длинные штрихи) сравниваются с результатами расчетов относительных концентраций при [CH4] = [CO] = 0 см–3 (точки).
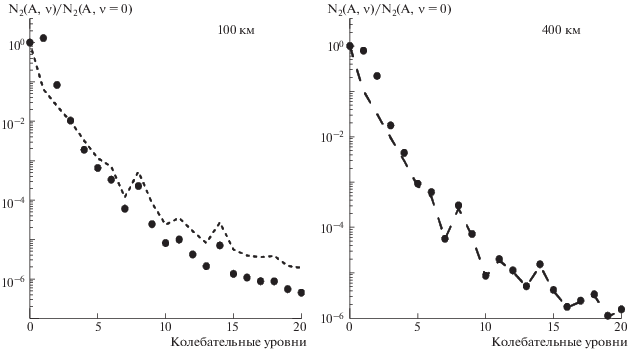
Результаты расчетов показали (см. рис. 3), что для высот средней атмосферы наблюдается значительный рост относительного содержания N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0) по сравнению с другими колебательными уровнями υ > 0. Столь принципиальное различие с верхней атмосферой объясняется значительным вкладом молекулярных столкновительных процессов в кинетику данного ${{{\text{A}}}^{3}}\Sigma _{u}^{ + }$ состояния на нижних высотах. Поэтому в результате неупругих взаимодействий электронное возбуждение большей частью аккумулируется на нижнем колебательном уровне ν = 0 состояния ${{{\text{A}}}^{3}}\Sigma _{u}^{ + }.$
Данный факт аккумуляции энергии на нижнем колебательном уровне ν = 0 метастабильного молекулярного азота может играть значительную роль в химических процессах и образовании радикалов в атмосфере Титана. Как уже говорилось ранее, в работах [19, 20] было показано, что при взаимодействии N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν > 0) с молекулой метана происходит главным образом процесс колебательной релаксации (5а). Связано это с тем, что колебательный квант данного ${{{\text{A}}}^{3}}\Sigma _{u}^{ + }$ состояния находится в хорошем энергетическом резонансе с одной из колебательных мод молекулы СН4. Однако для неупругих столкновений N2(${{{\text{A}}}^{3}}\Sigma _{{\text{u}}}^{ + },$ ν = 0) с молекулой метана эффективно протекает процесс диссоциации СН4 (5б) с образованием радикала СН3 и атомарного водорода [13, 14].
Аналогично при столкновении N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν > 0) с другими составляющими атмосферы Титана может возникнуть резонанс с одной из колебательных мод многоатомной молекулы, что приведет к простой колебательной релаксации при неупругих молекулярных столкновениях. Однако столкновения с N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0) с многоатомными молекулами аналогично процессу (5б) может инициировать процесс диссоциации с образованием химически активных радикалов в атмосфере Титана.
ЗАКЛЮЧЕНИЕ
Выполнено исследование кинетики триплетных состояний молекулярного азота на высотах верхней и средней атмосферы Титана во время высыпания в атмосферу высокоэнергичных электронов из магнитосферы Сатурна и космических лучей. Профили ионообразования в верхней, средней и нижней атмосфере Титана брались согласно [41–43]. Впервые при расчете концентраций метастабильного молекулярного азота N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + }$) учитываются столкновительные молекулярные процессы с атмосферными составляющими N2, СН4, СО. Сравнение относительных концентраций N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0–20)/N2(${{{\text{A}}}^{3}}\Sigma _{u}^{ + },$ ν = 0) для высот верхней и средней атмосферы показало, что неупругие молекулярные столкновения приводят к аккумуляции энергии электронного возбуждения метастабильного азота преимущественно на нижнем колебательном уровне ν = 0 на высотах средней атмосферы. Это может сказаться на процессах образования химически активных радикалов в атмосфере Титана.
Список литературы
Campbell L., Brunger M.J. // Inter. Rev. Phys. Chem. 2016. V. 35. No. 2. P. 297.
Lebonnois S., Bakes E.L.O., McKay C.P. // Icarus. 2002. V. 159. No. 2. P. 505.
Wilson E.H., Atreya S.K. // J. Geophys. Res. Planets. 2004. V. 109. No. 6. Art. No. E06002.
Krasnopolsky V.A. // Planet. Space Sci. 2012. V. 73. P. 318.
Vuitton V., Dutuit O., Smith M., Balucani N. // In: Titan: interior, surface, atmosphere and space environment. Ch. 7. Cambridge Univ. Press, 2014. P. 224.
Szopa C., Cernogora G., Boufendi L. et al. // Planet. Space Sci. 2006. V. 54. No. 4. P. 394.
Torokova L., Watson J., Krcma F. et al. // Contrib. Plasma Phys. 2015. V. 55. No. 6. P. 470.
Pintassilgo C.D., Loureiro J. // Planet. Space Sci. 2009. V. 57. No. 13. P. 1621.
Pintassilgo C.D., Loureiro J. // Adv. Space Res. 2010. V. 46. No. 5. P. 657.
Jauberteau J.L., Jauberteau I. // J. Phys. D. Appl. Phys. 2018. V. 51. No. 31. Art. No. 315201.
Kirillov A.S., Werner R., Guineva V. // Chem. Phys. Lett. 2017. V. 685. P. 95.
Кириллов А.С. // Астрон. вестн. 2020. Т. 54. № 1. С. 33.
Sharipov A.S., Loukhovitski B.I., Starik A.M. // J. Phys. Chem. A. 2016. V. 120. No. 25. P. 4349.
Umemoto H. // J. Chem. Phys. 2007. V. 127. No. 1. Art. No. 014304.
Gilmore F.R., Laher R.R., Espy P.J. // J. Phys. Chem. Ref. Data. 1992. V. 21. No. 5. P.1005.
Kirillov A.S. // Ann. Geophys. 2008. V. 26. No. 5. P. 1159.
Kirillov A.S. // Chem. Phys. Lett. 2016. V. 643. P. 131.
Kirillov A.S. // Chem. Phys. Lett. 2019. V. 715. P. 263.
Thomas J.M., Jeffries J.B., Kaufman F. // Chem. Phys. Lett. 1983. V. 102. № 1. P. 50.
Golde M.F., Ho G.H., Tao W., Thomas J.M. // J. Phys. Chem. 1989. V. 93. No. 3. P. 1112.
Slanger T.G., Wood B.J., Black G. // J. Photochem. 1973. V. 2. No. 1. P. 63.
Piper L.G. // J. Chem. Phys. 1992. V. 97. № 1. P. 270.
Umemoto H. // Phys. Chem. Chem. Phys. 2003. V. 5. No. 24. P. 5392.
Bezard B., Yelle R.V., Nixon C.A. // In: Titan: interior, surface, atmosphere and space environment. Ch. 5. Cambridge Univ Press, 2014. P. 158.
Vuitton V., Yelle R.V., Klippenstein S.J. et al. // Icarus. 2019. V. 324. P. 120.
Herron J.T. // J. Phys. Chem. Ref. Data. 1999. V. 28. No. 5. P. 1453.
Dreyer J.W., Perner D. // J. Chem. Phys. 1973. V. 58. No. 3. P. 1195.
Kirillov A.S. // J. Atm. Sol.-Terr. Phys. 2012. V. 81–82. P. 9.
Ландау Л.Д. Собрание трудов. Т. 1. М.: Наука, 1969. С. 181.
Schwartz R.N., Slawsky Z.I., Herzfeld K.F. // J. Chem. Phys. 1952. V. 20. No. 10. P. 1591.
Никитин Е.Е. Теория элементарных атомно-молекулярных процессов в газах. М.: Химия, 1970. 456 с.
Никитин Е.Е., Осипов А.И. // В кн.: ИНТ. Кинетика и катализ. Т. 4. М.: ВИНИТИ, 1977. 78 с.
Никитин Е.Е., Осипов А.И., Уманский С.Я. // Хим. плазмы. 1989. Т. 15. С. 3.
Кириллов А.С. // Косм. иссл. 1997. Т. 35. № 2. С. 155.
Kirillov A.S. // Ann. Geophys. 1998. V. 16. No. 7. P. 838.
Millikan R.C., White D.R. // J. Chem. Phys. 1963. V. 39. No. 12. P. 3209.
Billing G.D., Fisher E.R. // Chem. Phys. 1979. V. 43. No. 3. P. 395.
Billing G.D. // Chem. Phys. Lett. 1980. V. 76. No. 1. P. 178.
Herman R.C., Shuler K.E. // J. Chem. Phys. 1953. V. 21. No. 2. P. 373.
Радциг А.А., Смирнов Б.М. Справочник по атомной и молекулярной физике. М.: Атомиздат, 1980. 240 с.
Cravens T.E., Robertson I.P., Clark J. et al. // Geophys. Res. Lett. 2005. V. 32. No. 12. Art. No. L12108.
Agren K., Wahlund J.-E., Modolo R. et al. // Ann. Geophys. 2007. V. 25. No. 11. P. 2359.
Molina-Cuberos G.J., López-Moreno J.J., Rodrigo R. et al. // Planet. Space Sci. 1999. V. 47. No. 10–11. P. 1347.
Коновалов В.П., Сон Э.Е. // Хим. плазмы. 1987. Т. 14. С. 194.
Коновалов В.П. // ЖТФ. 1993. Т. 63. № 3. С. 23.
Дополнительные материалы отсутствуют.
Инструменты
Известия РАН. Серия физическая