Химическая физика, 2019, T. 38, № 1, стр. 38-48
Закономерности и механизм формирования алюминидов в системе TiH2–ZrH2–Al в гидридном циклеГ. Н. Мурадян, С. К. Долуханян, А. Г. Алексанян, О. П. Тер-Галстян, Н. Л. Мнацаканян
Г. Н. Мурадян 1, С. К. Долуханян 1, *, А. Г. Алексанян 1, О. П. Тер-Галстян 1, Н. Л. Мнацаканян 1
1 Институт химической физики им. А.Б. Налбандяна Национальной академии наук Армении,
Ереван, Армения
* E-mail: seda@ichph.sci.am
Поступила в редакцию 21.03.2018
После доработки 20.06.2018
Принята к публикации 20.05.2018
Аннотация
Представлены результаты исследования процессов формирования алюминидов в системе Ti–Al–Zr методом гидридного цикла (ГЦ). Установлено влияние соотношений гидридов титана и циркония и порошков алюминия, давления прессования при компактировании реакционной смеси, а также режимов дегидрирования и спекания на характеристики полученных алюминидов (фазовый состав, плотность и абсорбционные свойства). Синтезированы ряд однофазных и двухфазных алюминидов на основе титана и циркония. Показано, что некоторые синтезированные алюминиды без предварительного дробления взаимодействуют с водородом в режиме самораспространяющегося высокотемпературного синтеза с образованием обратимых гидридов. Построен концентрационный треугольник системы Ti–Al–Zr. Метод синтеза алюминидов на основе титана и циркония в ГЦ имеет существенные преимущества перед традиционными: относительно низкие температуры – не более 1000 °C и длительность процесса порядка 30–60 мин; формирование однофазных алюминидов происходит в одну технологическую стадию. Синтез однофазных алюминидов Ti0.25Al0.75, Zr0.25Al0.75, Ti0.05Zr0.2Al0.75 и других происходит при температурах 650–670 °С.
ВВЕДЕНИЕ
Цель работы – исследование процессов формирования алюминидов титана и циркония методом гидридного цикла (ГЦ). Сплавы на основе алюминия имеют ряд характеристик, которые делают их особенно привлекательными в современной технике. Известно, что алюминиевые сплавы из-за чрезвычайно стабильного пассивирующего защитного оксидного слоя очень стойкие к окислению. Алюминиды характеризуются низкой плотностью, высокой прочностью, жаропрочностью и другими качествами. Алюминиевые сплавы значительно более экономичны, чем существующие высокотемпературные сплавы на основе Ni и Ti. Поэтому интерес к сплавам на основе алюминия связан с их многочисленными и важными практическими применениями в качестве конструкционных материалов: в оборонной промышленности; в аэрокосмической, атомной и водородной энергетике; судостроительной, химической, автомобильной и других отраслях транспортного машиностроения, станкостроения, металлообрабатывающей промышленности; радиотехнике, электронике, электротехнике, в медицине (биосовместимые материалы) и т.д.
Существует множество работ, посвященных исследованию методов синтеза и свойств алюминидов. В обзоре Tretyachenko [1], охватывающем 1961–2003 гг. по системе Aluminium–Titanium–Zirconium приведены ссылки на 44 статьи. В связи с возрастанием интереса к алюминидам появилось довольно много новых исследований, посвященных синтезу и исследованию этих материалов.
Наиболее известным способом получения алюминидов являются индукционная и дуговая плавки, которые требуют сложного оборудования (высокотемпературные или дуговые печи) [2–6]. В порошковой металлургии при синтезе алюминидов термообработку реакционной смеси проводят при Т = 850–900 °С в течение более 40 ч [7]. При механохимическом методе их получения при перемешивании в барабанах в течение более 60 ч происходит прилипание реакционной смеси к стенке барабана, что приводит к изменению соотношения компонентов и загрязнению материалами шаров и барабана [8].
Различия в плотностях, температурах плавления и испарения компонентов шихты (например, Al–Ti, Al–Zr и др.) усложняют современные технологии. Плотная оксидная пленка на поверхности частиц металлических порошков препятствует взаимной диффузии компонентов. Способы получения алюминидов этими методами длительные, многостадийные, требуют многократной переплавки, глубокого вакуума и инертной среды при высоких температурах (1600–2500 °C). В последние десятилетия для синтеза алюминидов использовался метод самораспространяющегося высокотемпературного синтеза (СВС). Но для его реализации часто требуется дополнительная активация исходной шихты. В связи с вышеизложенным очевидно, что поиск новых путей синтеза алюминидов заданного состава и структуры является актуальной задачей в современном материаловедении.
В настоящей работе был использован метод гидридного цикла, разработанный в Институте химической физики Национальной академии наук Армении, для синтеза алюминидов тугоплавких металлов. Сущность этого метода заключается в использовании гидридов тугоплавких металлов в качестве исходных материалов для синтеза сплавов либо гидридов и другого металла (Ni, Co, Al и др.). В работах [9–16] детально описаны метод ГЦ и экспериментальные результаты, полученные при синтезе сплавов и интерметаллидов на основе тугоплавких металлов. Метод ГЦ в сочетании с методом СВС позволил разработать эффективные процессы формирования различных бинарных и многокомпонентных сплавов и интерметаллидов, а также синтезировать их гидриды.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Предварительно методом СВС были синтезированы [17] гидрид титана (TiH2, 4.01 вес. % H2) и гидрид циркония (ZrH2, 2 вес. % H2). Полученные гидриды измельчались до фракции <50 мкм и тщательно смешивались с порошком алюминия чистоты 99.7%. Для синтеза гидридов использовались: цирконий чистоты 99.9% (ПЦРК) и титан (ПТМ-1). Порошки TiH2 и ZrH2 столь хрупки, что в процессе приготовления реакционной смеси хTiH2 + yZrH2 + + zAl → TixAlzZry в течение 30–40 мин гидриды продолжали измельчаться до фракции размером менее 10 мкм. Надо отметить, что исходные гидриды имеют наномасштабные размеры частиц кристаллитов менее 50 нм [18].
Реакционная смесь прессовалась в цанговой прессформе в цилиндрические таблетки диаметром d = 22 мм и высотой h = 15–25 мм на гидравлическом прессе (при усилии прессования от 20 000 до 45 000 кГс). Процесс ГЦ проводился в герметичных кварцевых реакторах, снабженных печкой и устройством для контроля вакуума и температуры. Нагрев образца проводился до 1000 °С.
Для аттестации образцов использовались химический, дифференциально-термический (ДТА, дериватограф Q-1500) и рентгенофазовый (РФА, дифрактометры ДРОН-0.5) анализы. Первый анализ (ДТА) проводился при нагреве образца до 1000 °С со скоростью 20 °С/мин. Плотность образцов измерялась гидростатическим методом; рентгеновская плотность рассчитывалась по параметрам кристаллической решетки. Плотность полученных образцов измерялась для таблеток, спрессованных при давлении прессования Р = 30 000 кГс.
В настоящей работе исследовалось влияние соотношений гидридов титана и циркония и порошков алюминия, давления прессования при компактировании реакционной смеси, а также режимов дегидрирования и спекания (температуры и скорости нагрева) на характеристики полученных алюминидов (фазовый состав, плотность и абсорбционные свойства). Ниже приводятся результаты, полученные при исследовании следующих трех составов.
1. Система (0.75 – х)TiH2 – хZrH2–0.25Al (разрез Ti3Al–Zr3Al; 25 ат. % Al)
В работе [4] был исследован псевдобинарный состав Ti0.75 – xAl0.3Zrx, приготовленный дуговой плавкой в атмосфере чистого аргона. Было показано, что гидрирование при комнатной температуре и до 473 К приводит к формированию аморфного гидрида алюминида с соотношением Н/Ме, равным 1.10. В работе [19] рассмотрена стабильность фазы Ti2ZrAl и показаны предпочтительные позиции атомов Zr в Ti3Al. В работе [2] было построено изотермическое сечение тройной системы Al–Ti–Zr при 1073 К путем анализа диффузионных тройных и равновесных сплавов на электронно-зондовом микроанализаторе (determined with electron probe microanalysis EPMA).
Ранее нами при исследовании процессов формирования биметаллических алюминидов Ti3Al и Zr3Al в ГЦ было установлено некоторое различие в механизме их формирования [13, 15]. Исследуемая в настоящей работе система с двумя гидридами переходных металлов состава (0.75 – х)TiH2 – хZrH2 – – 0.25Al более сложная. Ниже приведена реакция формирования алюминидов на основе титана и циркония в режиме ГЦ: (0.75 – х)TiH2 + + хZrH2 + 0.25Al → Ti0.75 – x Al0.25Zrx + H2↑, где 0 ≤ х ≤ 0.75.
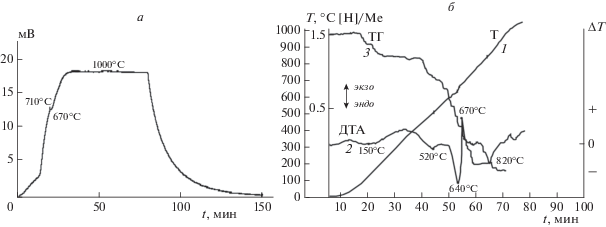
На рис. 1а представлена термограмма ГЦ для состава Ti0.55Al0.25Zr0.2. На всех термограммах ГЦ при нагреве исходной шихты (0.75 – х)TiH2 + + хZrH2 + 0.25Al с ростом температуры наблюдались экзотермические пики при 650–670 °C, свидетельствующие о взаимодействии с алюминием титана и циркония, образованных вследствие диссоциации соответствующих гидридов.
Рис. 1.
а – Термограмма формирования алюминида Ti0.55Al0.25Zr0.2 в ГЦ; б – ДТА-кривые при нагреве шихты 0.55TiH2 + + 0.20ZrH2 + 0.25Al.
В табл. 1 приведены характеристики алюминидов, синтезированных в ГЦ в системе (0.75 – – х)TiH2 – хZrH2–0.25Al. Для сравнения в табл. 1 приведены также характеристики бинарных алюминидов Ti3Al и Zr3Al. По данным РФА продуктами реакции, в зависимости от соотношения содержания гидридов титана и циркония, являются твердые растворы, фазы B2 и (α2)${\text{D}}{{{\text{0}}}_{{19}}}$. При содержании в исходной шихте 15 ат. % TiH2 в продуктах реакции наряду с твердым раствором Al и Ti в Zr появляется фаза B2. С ростом содержания TiH2 фаза B2 растет и становится основной, а наряду с ней появляется α2-фаза (D019). При содержании TiH2 65 ат. % основной становится гексагональная фаза D019 с параметрами кристаллической решетки, близкой к гексагональной фазе алюминида титана – α2-Ti3Al.
Таблица 1.
Характеристики алюминидов в системе (0.75 – х)TiH2 – хZrH2–0.25Al, синтезированных в ГЦ
| Исходные реагенты, ат. % | Фазовый состав, параметры кристаллической решетки, Å | Расчетная формула | Тгор, °С | H2, вес. % | Формула гидрида алюминида, тип кристаллической решетки | Плотность, г/см3 (гидростат.) | ||
|---|---|---|---|---|---|---|---|---|
| TiH2 | Al | ZrH2 | ||||||
| 0 | 25 | 75 | тв. раствор, Al
в ГПУ Zr + Х-фаза; а = 3.242, с = 5.176 |
Zr0.75Al0.25 | 540 | 1.47 | Zr0.75Al0.25H1.07; ВСТ + Х-фаза |
5.864 |
| 15 | 25 | 60 | тв. раств. Al и Ti в Zr; a = 3.234, c = 5.178+ B2-фаза |
Ti0.15Al0.25Zr0.6 | 430 | 1.3 | Ti0.15Zr0.6Al0.25Н0.89 | 5.221 |
| 25 | 25 | 50 | тв. раств. Al и Ti в Zr; а = 3.243, c = 5.175+ B2-фаза |
Ti0.25Zr0.5Al0.25 | 430 | 1.3 | Ti0.25Zr0.5Al0.25Н0.83 | 5.193 |
| 35 | 25 | 40 | B2-фаза; а = 3.384 + + тв. раств. Al и Ti в Zr |
Ti0.35Zr0.4Al0.25 | 360 | 1.32 | Ti0.35Zr0.4Al0.25Н0.79 | 4.61 |
| 45 | 25 | 30 | B2-фаза; а = 3.348+ (α2)D019 | Ti0.45Zr0.3Al0.25 | 330 | 1.57 | Ti0.45Zr0.3Al0.25Н0.87 | 4.429 |
| 55 | 25 | 20 | B2-фаза; а = 3.318+ (α2)D019 | Ti0.55Zr0.2Al0.25 | 310 | 1.32 | Ti0.55Zr0.2Al0.25Н0.67 | 4.199 |
| 65 | 25 | 10 | α2-Ti3Al(D019); а = 5.894, c = 4.629 + B2-фаза; а = 3.307 |
Ti0.65Zr0.1Al0.25 | 300 | 1.28 | Ti0.65Zr0.1Al0.25Н0.59 | 4.134 |
| 75 | 25 | 0 | α2-Ti3Al(D019); a = 5.83, c = 4.647 |
Ti0.75Al0.25 | 500 | 2.27 | Ti0.7Al0.3H1.0 ГЦК |
3.457 |
Для оценки тепловых эффектов, происходящих при нагреве шихты (0.55TiH2 + 0.2ZrH2 + + 0.25Al) до 1000 °C, проводился дифференциально-термический анализ (рис. 1б). На ДТА-кривой 2 (рис. 1б) наблюдаются три заметных эндоэффекта: при 150, 520, 640 ○С, обусловленные разложением исходных гидридов TiH2 и частично гидрида ZrH2. Как видно из рис. 1б, экзотермический пик, наблюдаемый на ДТА-кривой 2 при 670 °С, хорошо совпадает с экзопиком, наблюдаемым на термограмме ГЦ (рис. 1а), что свидетельствует о экзотермической реакции между продуктами разложения гидридов титана и циркония с алюминием. По данным РФА закаленные при температуре 670 °С промежуточные продукты являются сложными алюмогидридами на основе титана и циркония. Четвертый эндоэффект при 820 °С обусловлен разложением промежуточного алюмогидрида. Конечным продуктом реакции (0.55TiH2+ 0.2ZrH2+ + 0.25Al) и в ГЦ, и после ДТА по данным РФА является двухфазный алюминид состава Ti0.55Al0.25Zr0.2 (B2-фаза; $а = {\text{3}}.{\text{318}} + \left( {{{\alpha }_{{\text{2}}}}} \right){\text{D}}{{{\text{0}}}_{{{\text{19}}}}}$). На всех ДТА-кривых при нагреве исходной шихты (0.75 – х)TiH2 + + хZrH2 + 0.25Al (табл. 1) с ростом температуры до 1000 °C наблюдались аналогичные картины, только в зависимости от соотношения TiH2/ZrH2 изменялась глубина экзо- и эндоэффектов.
Для выяснения абсорбционных свойств синтезированных алюминидов к водороду и влияния водорода на фазовый состав полученные компактные таблетки алюминидов без предварительного дробления были сожжены в водороде при РН = 10 атм. В результате прохождения фронта горения (Тг = 300–430 °С) синтезированы гидриды алюминидов (табл. 1) с содержанием водорода (Н/Ме ≥ 1.3–1.65). Все полученные гидриды обратимые: например, Ti0.375Al0.25Zr0.375 + H2 ↔ ↔ Ti0.375Al0.25Zr0.375Н0.99.
2. Система хTiH2–(1 – х)ZrH2–Al (разрез TiAl–ZrAl, 50 ат. % Al)
Ряд тройных сплавов Ti–Al–Zr с различными составами вокруг бинарной γ-TiAl (структура L10) были синтезированы и отожжены при 1273 К в течение 10 ч с последующей закалкой [3]. Почти однофазная γ-фаза была получена в довольно широком диапазоне составов Al50(Ti50 – х – yAlxZry) при 0 ≤ х ≤ 15 и 0 ≤ у ≤ 15. Оба параметра решетки, а и с, возрастают с увеличением концентрации Zr. В работе [20] методом дуговой плавки с последующей гомогенизацией при 1100 °С в течение 100 ч, термообработкой при 800 °С + 600 °С (по 3 ч при каждой температуре) и воздушным охлаждением до 25 °C была получена однофазная γ-фаза алюминида состава 2Zr–50Ti–48Al (ат. %). Установлен предел растворимости Zr в γ-фазе TiAl, составивший ~11 ат. % [21]. Ранее методом ГЦ нами был синтезирован однофазный алюминид γ-TiAl [13], а в работе [15] было показано, что однофазный ZrAl в ГЦ не образуется.
В данной части работы представлены исследования реакции формирования алюминидов титана и циркония в режиме ГЦ следующего состава: хTiH2 + (1 – х)ZrH2 + Al → TixAl Zr1 –x + H2↑, где 0≤ х ≤ 1. В табл. 2 приведены характеристики полученных в ГЦ алюминидов при разных соотношениях исходных компонентов (ряд TixAlZr1 – x), а для сравнения представлены также характеристики бинарных алюминидов TiAl и ZrAl. Был получен ряд двухфазных алюминидов на основе Ti, Al и Zr различных составов наряду с бинарной фазой γ-TiAl (структура L10). Все экзоэффекты, зарегистрированные на термограммах и на ДТА-кривых, находятся в пределах 530–670 °С.
Таблица 2.
Характеристики алюминидов титана и циркония, полученных в ГЦ в сиситеме хTiH2–(1 – х)ZrH2–Al, разрез (TiAl–ZrAl, 50 ат. % Al)
| Исходные реагенты ат. % | Фазовый состав; параметры кристаллической решетки, Å |
Расчетная формула | Тгор, °С (СВС) |
H2, вес. % |
Плотность, г/см3 (гидростат.) |
||
|---|---|---|---|---|---|---|---|
| TiH2 | Al | ZrH2 | |||||
| 0 | 50 | 50 | Al2Zr (гекс.); a = 5.293, c = 8.737 + Zr + ZrAl (следы) | ZrAl | 405 | 0.81 | 4.630 |
| 10 | 50 | 40 | Al2Zr; a = 5.271, c = 8.892 + Zr | Ti0.1Zr0.4Al0.5 | 220 | 0.57 | 4.572 |
| 20 | 50 | 30 | Al2Zr; a = 5.312, c = 8.556+ γ-TiAl (тетрагонал.) | Ti0.2Zr0.3Al0.5 | 125 | 0.48 | 4.342 |
| 25 | 50 | 25 | Al2Zr; a = 5.305, с = 8.755 + γ-TiAl | Ti0.25Zr0.25Al0.5 | 188 | 0.45 | 4.167 |
| 30 | 50 | 20 | Al2Zr; a = 5.299, c = 8.746 + γ-TiAl a = 4.008, c = 4.096 | Ti0.3Zr0.2Al0.5 | 160 | 0.42 | 4.036 |
| 40 | 50 | 10 | γ-TiAl;a = 4.014, c = 4.084 + Al2Zr; a = 5.279, c = 8.746 | Ti0.4Zr0.1Al0.5 | – | – | 3.031 |
| 47 | 47 | 6 | γ-TiAl; a = 4.001, c = 4.077; Al2Zr; a = 5.277, c = 8.738 |
Ti0.47Zr0.06Al0.47 | – | – | 2.886 |
| 50 | 48 | 2 | γ-TiAl; a = 4.003, c = 4.076 + Х-фаза | Ti0.5Zr0.02 Al0.48 | – | – | 2.805 |
| 50 | 50 | 0 | γ-TiAl; a = 3.981, c = 4.051 | TiAl | – | – | 2.75 |
3. Система х(TiH2)–(1 – х)(ZrH2)–3Al (разрез TiAl3–ZrAl3, 75 ат. % Al)
Триалюминиды металлов 4 (Ti, Zr, Hf) и 5 групп (V, Nb, Та) элементов кристаллизуются с объемно-центрированной тетрагональной структурой D022 (для Al3Ti), или структурой D023 (для Al3Zr). Известно, что высокотемпературные триалюминиды, используемые в качестве конструкционных материалов, имеют высокую прочность. В первую очередь это Al3Ti, поскольку он является наименее плотным из этого класса. Однако низкосимметричная тетрагональная структура делает эти фазы по своей природе хрупкими. Структуры D022 и D023 тесно связаны с кубической структурой L12. Сегодня усилия сосредоточены на легировании этих бинарных интерметаллидов для перевода их к структурам L12 более высокой симметрии в надежде на то, что увеличение числа независимых систем скольжения улучшит ударную вязкость. Например, Al3Ti (D022) может быть преобразована в кубическую структуру L12 при легировании переходными элементами четвертого периода, такими как Cr, Mn, Fe, Co, Ni, Cu, Zn, либо элементами 4 группы – Ti, Zr, Hf [5–7]. Распространенным способом получения триалюминидов титана и циркония является дуговая плавка [5], в результате которой с возрастанием температуры от 1408 до 1607 °C в основном формируются фазы TiAl3–ZrAl3. Согласно [5, 6], в тройных системах Al–Ti–Zr, в зависимости от состава и условий получения, формируются алюминиды Al3(TixZr1 – x) либо с ГЦК-решеткой типа L12, либо с тетрагональной структурой (D022 или D023). Было установлено существование ограниченных твердых растворов соединений на основе TiAl3 и ZrAl3 (в разрезе TiAl3–ZrAl3) [6]. Алюминиды титана и циркония получают также посредствам реакции растворения металлов в расплаве алюминия при температуре ниже 800 °С [7, 22]. Структура типа D022 (TiAl3) растворяет до 2 ат. % Zr, в то время как структура типа D023 (ZrAl3) существует в широком диапазоне составов: от чистого ZrAl3 до ≈15 ат. % Ti [5, 22].
В работах [13, 15] методом ГЦ нами были синтезированы однофазные TiAl3 и ZrAl3. В данной части работы представлены исследования реакции формирования триалюминидов титана и циркония в режиме ГЦ:
Формулы и характеристики синтезированных триалюминидов представлены в табл. 3, для сравнения там же приведены характеристики бинарных алюминидов ZrAl3 и TiAl3. Как видно из таблицы, в режиме ГЦ были получены однофазные и двухфазные триалюминиды. Было показано, что изменение параметров процесса ГЦ, усилия прессования от 20 000 до 45 000 кГс, температуры процесса от 900 до 1000 °C и скорости нагрева от 20 до 40 °C/мин существенного влияния на фазовый состав синтезированных триалюминидов не оказывают. Аналогичные результаты были получены при синтезе ZrAl3, TiAl3, NbAl3, TiхNb1 – хAl3.
Таблица 3.
Характеристики синтезированных триалюминидов в системе х(TiH2)–(1 – х) (ZrH2)–3Al (разрез TiAl3–ZrAl3)
| Исходные реагенты, ат. % | Фазовый состав; кристаллическая решетка; параметры, Å; с/а |
Формула | Плотность, г/см3 | |||
|---|---|---|---|---|---|---|
| TiH2 | ZrH2 | Al | гидростат. | рентген. | ||
| 0 | 25 | 75 | ZrAl3 тетрагональный – $D_{{4m}}^{{17}}$ – I4/mmm; ВСТ (D023); a = 4.015, c = 17.318; 4.313 | Zr0.25Al0.75 | 3.863 | 4.09 |
| 5 | 20 | 75 | Тетрагональный, на основе ZrAl3; a = 3.992, c = 17.189; 4.306 |
Ti0.05Zr0.2Al0.75 | 3.075 | 3.617 |
| 10 | 15 | 75 | Тетрагональный, на основе ZrAl3; a = 3.979, c = 17.211; 4.325 |
Ti0.1Zr0.15Al0.75 | 2.939 | 3.444 |
| 12.5 | 12.5 | 75 | Тетрагональный, на основе ZrAl3; a = 3.953, c = 17.063; 4.316 |
Ti0.125Zr0.125Al0.75 | 2.729 | 3.368 |
| 15 | 10 | 75 | Тетрагональный, на основе ZrAl3 и следы TiAl3; a = 3.95, c = 16.947; 4.29 |
Ti0.15Zr0.1Al0.75 | 2.603 | 3.351 |
| 20 | 5 | 75 | TiAl3 тетрагональный; a = 3.852, c = 8.633; 2.241; ZrAl3 тетрагональный; a = 3.937, c = 16.849; 4.279 |
Ti0.2Zr0.05Al0.75 | 2.617 | – |
| 25 | 0 | 75 | TiAl3 тетрагональный – I4/mmm(139), BCT (D022); a = 3.856, c = 8.648; 2.242 |
Ti0.25Al0.75 | 2.564 | 3.326 |
С повышением температуры на термограммах при 660–670°С наблюдались экзоэффекты. Подобные экзоэффекты были зарегистрированы для всех изученных составов данной системы и для раннее изученных бинарных триалюминидов TiAl3, NbAl3 и ZrAl3 [6–8].
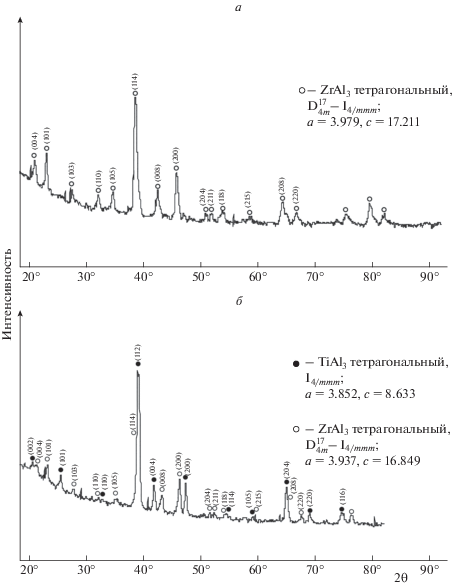
На рис. 2 представлены дифракционные картины однофазного (а – Ti0.1Zr0.15Al0.75) и двухфазного (б – Ti0.2Zr0.05Al0.75) алюминидов. При содержании TiH2 в шихте 1–15 ат. % (строки 1–4 табл. 3) образуются однофазные триалюминиды с тетрагональной кристаллической структурой D023 (близкой к структуре ZrAl3, рис. 2а). При содержании TiH2 15 ат. % (строка 4 табл. 3) на дифракционных картинах появляются следы фазы TiAl3. Когда концентрация TiH2 достигает 20 ат. % (строки 5 и 6 табл. 3), образуется двухфазный алюминид Ti0.2Zr0.05Al0.75, содержащий фазы TiAl3 (D022) и ZrAl3(D023) (рис. 6 б). Эти данные, представленные в табл. 3 (строки 5 и 6), хорошо согласуются с заключением авторов работы [5] об ограниченной взаимной растворимости алюминидов TiAl3 и ZrAl3.
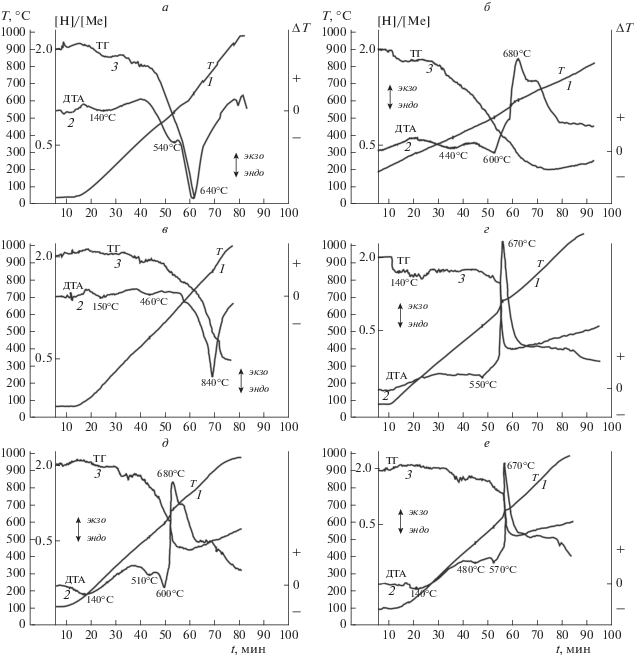
На рис. 3 представлены ДТА-кривые, зарегистрированные для триалюминидов и для раннее полученных гидридов Ti и Zr [13, 15]: a) TiH2; б) TiH2 + 3Al; в) ZrH2; г) ZrH2 + 3Al; д) 0.8TiH2 + + 0.2ZrH2 + 3Al; е) 0.2TiH2 + 0.8ZrH2 + 3Al. На ДТА-кривых при разложении гидрида титана наблюдались два эндоэффекта: при 540 и 640 °C (рис. 3а); на ДТА-кривой для смеси TiH2 + 3Al, кроме двух энодоэффектов, характерных при диссоциации TiH2, появляется экзоэффект при 680 °С, обусловленный взаимодействием освободившегося Ti с Al (рис. 3б). На ДТА-кривой при диссоциации гидрида циркония было зарегистрировано три эндоэффекта: при 150, 460 и 840 °C (рис. 3в). На ДТА-кривой для смеси ZrH2 + 3Al наблюдаются: один эндоэффект от разложения ZrH2 при 550 °C до ГЦК ZrH1.5 и последующий экзоэффект при 670 °C, свидетельствующий о взаимодействии ZrH1.5 с Al, приводящем к формированию триалюминида циркония (рис. 3г). Экзоэффекты, зарегистрированные на ДТА-кривых 2 для смесей 0.8TiH2 + 0.2ZrH2 + 3Al (рис. 3д) и 0.2TiH2 + + 0.8ZrH2 + 3Al (рис. 3е), совпадают с температурами начала экзоэффектов, наблюдаемых на термограммах ГЦ. Результаты закалки промежуточных продуктов реакций как в ГЦ, так и при ДТА и температуре 670 °C с последующим фазовым анализом подтвердили формирование триалюминидов.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В табл. 4 приведены значения тепловых эффектов, сопровождающих формирование бинарных и тройных алюминидов на основе титана и циркония как в ГЦ, так и при термическом анализе (ДТА).
Таблица 4.
Температуры эндо- и экзоэффектов, наблюдаемые при формировании алюминидов в ГЦ и при ДТА-анализе
| Тепловые эффекты | Ме(М')3Al | |||
|---|---|---|---|---|
| α2-Ti3Al, Ti0.75Al0.25 | Zr3Al (Zr0.75Al0.25) |
Ti0.55Al0.25Zr0.2 | Ti0.25Al0.25Zr0.5 | |
| Температуры начала экзоэффектов в °С из термограмм ГЦ | ||||
| Экзоэффект | 660 | 670 | 670 | 660 |
| Температуры тепловых эффектов из ДТА-кривых | ||||
| Экзоэффект | 670 | 630 | 670 | 650 |
| Эндоэффект | 480, 600 | 150, 550, 790 | 150, 520, 640, 820 | 150, 480, 570, 780 |
| Тепловые эффекты | Ме(М')Al | |||
| γ-TiAl | ZrAl | Ti0.4Zr0.1Al0.5 | Ti0.45Zr0.05Al0.5 | |
| Температуры начала экзоэффектов в °С из термограмм ГЦ | ||||
| Экзоэффект | 650 | 650 | 670 | 660 |
| Температуры тепловых эффектов из ДТА-кривых в °С | ||||
| Экзоэффект | 670 | 670 | 670 | 680 |
| Эндоэффект | 530, 630 | 150, 520, 800 | 150, 500, 600, 740 | 150, 510, 620, 730 |
| Тепловые эффекты | Ме(М')Al3 | |||
| TiAl3 | ZrAl3 | Ti0.2Zr0.05Al0.75 | Ti0.05Zr0.2Al0.75 | |
| Температуры начала экзоэффектов в °С из термограмм ГЦ | ||||
| Экзоэффект | 650 | 650 | 670 | 660 |
| Температуры тепловых эффектов из ДТА-кривых в °С | ||||
| Экзоэффект | 680 | 670 | 680 | 670 |
| Эндоэффект | 440, 600 | 550 | 140, 510, 600, 720 | 140,480, 570, 780 |
Анализируя данные табл. 4, можно с очевидностью сказать, что при любом содержании алюминия (25, 50 и 75 ат. %) формирование бинарных и многокомпонентных алюминидов в ГЦ и при ДТА-анализе начинается экзотермической реакцией при Т = 650–670 °С. Можно предположить, что вначале на поверхности зерен металлов формируется богатый алюминием слой (типа МеAl3), поэтому температура экзоэффектов для всех составов по алюминию (25, 50, 75 ат. %) всегда находится в переделах Т = 650–670 °С. В дальнейшем при повышении температуры нагрева до 1000 °С и выдержке при этой температуре 30–60 мин, для составов с содержанием 25 и 50 ат. % Al происходит гомогенизация (или диффузия алюминия в глубь зерна), приводящая к формированию той или иной фазы. А для богатых алюминием образцов (75 ат. % Al) формирование триалюминидов (TiAl3, ZrAl3, Ti0.2Zr0.05Al0.75, Ti0.05Zr0.2Al0.75) происходит при 650–670 °С (т.е. температурах экзоэффектов), что подтверждается РФА-анализом закаленных продуктов ГЦ и ДТА.
Исходя из результатов проведенных исследований, мы можем описать следующий механизм формирования алюминидов на основе титана и циркония. В ГЦ в процессе нагрева шихты хTiH2 + + yZrH2 + zAl → TixAlzZry при Т = 600–1000 °С исходные гидриды разлагаются, разрушаются связи Me–H связи, что приводит к сильной активации титана и циркония и мгновенному экзотермическому взаимодействию их с алюминием, минуя стадию плавления алюминия. На термограммах всех изученных составов эндоэффектов, связанных с разложением, исходных гидридов не наблюдалось, хотя, безусловно, они имели место. Следов плавления на синтезированных образцах также не наблюдалось. Таким образом, формирование всех исследованных в настоящей работе алюминидных фаз титана и циркония протекает по твердофазному механизму. Аналогичные примеры твердофазного механизма формирования сплавов и интерметаллидов на основе тугоплавких металлов, минуя стадию плавления исходных реагентов, нами было показано в предыдущих работах [9–16].
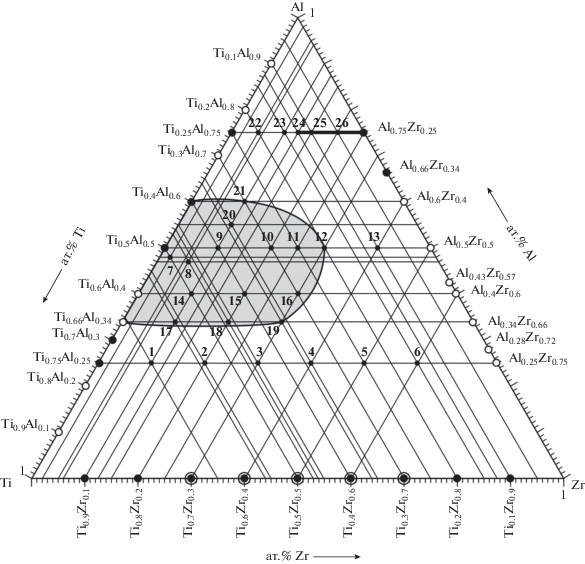
На основании результатов, полученных при изучении процессов формирования алюминидов титана и циркония нижеприведенных систем, построен концентрационный треугольник системы Ti–Al–Zr (рис. 4), на сторонах которого нанесены составы алюминидов титана (Ti–Al) [13], алюминидов циркония (Zr–Al) [15] и ранее исследованных сплавов на основе Ti–Zr, синтезированных методом ГЦ [9]. Внутри треугольника показаны расположения однофазных и двух-, трехфазных алюминидов на основе титана и циркония.
На разрезе Ti3Al–Zr3Al (25 ат. % Al) показан фазовый состав следующих алюминидов по точкам (рис. 4): 1 – Ti0.65Al0.25Zr0.1(D019 + B2); 2 – Ti0.55Al0.25Zr0.2(B2 + D019); 3 – Ti0.45Al0.25Zr0.3(B2 + + D019); 4 – Ti0.35Al0.25Zr0.4(B2 + тв. раств. Al и Ti в Zr); 5 – Ti0.25Al0.25Zr0.5 (тв. раств. Al и Ti в Zr + B2); 6 – Ti0.15Al0.25Zr0.6 (тв. раств. Al и Ti в Zr + B2).
На разрезе TiAl–ZrAl (50 ат. % Al) показан фазовый состав следующих алюминидов по точкам (рис. 4): 7 – Ti0.5Al0.48Zr0.02(γ-TiAl + Х-фаза); 8 – Ti0.47Al0.47Zr0.06(γ-TiAl + Al2Zr); 9 – Ti0.4Al0.5Zr0.1(γ-TiAl + Al2Zr); 10 – Ti0.3Al0.5Zr0.2(Al2Zr + γ-TiAl); 11 – Ti0.25Al0.5Zr0.25(Al2Zr + γ-TiAl); 12 – Ti0.2Al0.5Zr0.3(Al2Zr + γ-TiAl); 13 – Ti0.1Al0.5Zr0.4; 14 – Ti0.5Al0.4Zr0.1(γ-TiAl + ZrAl2); 15 – Ti0.4Al0.4Zr0.2(γ-TiAl + ZrAl2); 16 – Ti0.3Al0.4Zr0.3 (ZrAl2 + γ-TiAl); 17 – Ti0.56Al0.34Zr0.1(γ-TiAl + + ZrAl2); 18 – Ti0.46Al0.34Zr0.2(γ-TiAl + ZrAl2); 19 – Ti0.36Al0.34Zr0.3(γ-TiAl + ZrAl2); 20 – Ti0.35Al0.55Zr0.1(γ-TiAl + ZrAl2); 21 – Ti0.3Al0.6Zr0.1(γ-TiAl + ZrAl2).
В зависимости от состава исходной шихты формируются фазы γ-TiAl и гексагональный ZrAl2 в различных соотношениях. Внутри концентрационного треугольника выделена область двухфазных алюминидов различных составов вокруг бинарной фазы γ-TiAl (структура L10).
На разрезе TiAl3–ZrAl3 (75 ат. % Al) показаны следующие однофазные и двухфазные триалюминиды (табл. 3, рис. 4): 22 – Ti0.2Al0.75Zr0.05(TiAl3 + + ZrAl3); 23 – Ti0.15Al0.75Zr0.1(ZrAl3 + следы TiAl3); 24 – Ti0.125Al0.75Zr0.125(ZrAl3); 25 – Ti0.1Al0.75Zr0.15(ZrAl3); 26 – Ti0.05Al0.75Zr0.2(ZrAl3).
ЗАКЛЮЧЕНИЕ
1. Синтезированы ряд однофазных и двухфазных алюминидов на основе титана и циркония (табл. 1–3): тв. раств. Ti и Al в ГПУ Zr; B2- и (α2)D019-фазы; ряд сплавов на основе Ti, Al и Zr различных составов вокруг бинарной фазы γ-TiAl (L10); однофазные триалюминиды с тетрагональной структурой на основе ZrAl3 (Ti0.05Zr0.2Al0.75, Ti0.1Zr0.15Al0.75, Ti0.125Zr0.125Al0.75).
2. Показано, что на формирование алюминидов в режиме ГЦ наиболее существенное влияние оказывают соотношение исходных компонентов шихты, температура и скорость нагрева исходной шихты.
3. При синтезе алюминидов в системе TiH2–ZrH2–Al в режиме ГЦ происходит сильная активация металлов за счет разрушения связи Ме–Н и их очистка от окисной пленки. “Открытые связи”, очищенная поверхность активированных порошков титана и циркония, наномасштабные размеры частиц кристаллитов (20–80 нм) используемых порошков создают благоприятные условия для реализации твердофазного диффузионного механизма формирования алюминидов, минуя стадию плавления исходных компонентов.
4. Показано, что некоторые синтезированные алюминиды без предварительного дробления взаимодействуют с водородом в режиме СВС с образованием обратимых гидридов.
5. Построен концентрационный треугольник системы Ti–Al–Zr, внутри которого показаны расположения тройных алюминидных фаз для 26 составов, содержащих фазы B2 + D019, γ-TiAl и др.
6. По сравнению с существующими методами синтез алюминидов на основе титана и циркония в ГЦ имеет существенные преимущества: относительно низкие температуры (~1000 °C) и длительность процесса (30–60 мин), формирование однофазных алюминидов происходит в одну технологическую стадию. Синтез алюминидов Ti0.25Al0.75, Zr0.25Al0.75, Ti0.2Zr0.05Al0.75, Ti0.05Zr0.2Al0.75 и других составов происходит при сравнительно низких температурах (650–670 °С).
Список литературы
Tretyachenko L. // Light Metal Systems. Al–Ti–Zr (Aluminium – Titanium – Zirconium) / Eds. Effenberg G., Ilyenko S.V. 11A4: Landolt-Börnstein – Group IV Physical Chemistry. Heidelberg: Springer-Verlag GmbH, 2005. P. 54.
Kai-li Lu, Feng Yang, Zhi-yun Xie et al. // Trans. Nonferrous Met. Soc. China. 2016. V. 26. P. 3052.
Tanda D., Tanabe T., Tamura R. et al. // Mater. Sci. & Engin. 2004. V. 387. P. 991.
Yoshonobu Miyajima, Kazuhiro Ishikawa, Kiyoshi Aoki // Mater. Transaction. 2002. V. 43. № 5. P. 1085.
Knipling K.E., Dunand D.C., Seidman D.N. // Acta Mater. 2008. V. 56. № 6. P. 1182.
Karpets M.V., Milman Yu.V., Barabash O.M. et al. // Intermetallics. 2003. V.11. P. 241.
Dezellus O., Gardiola B., Andrieux J. // J. Phase Equilibria and Difusion – ASM Intern. 2014. V. 35. № 2. P. 120.
Fan G.J., Song X.P., Quan M.X. et al. // Mater. Sci. and Eng., A. 1997. № 231. P. 111.
Долуханян С.К., Алексанян А.Г., Тер-Галстян О.П. и др. // Хим. физика. 2007. Т. 26. № 11. С. 36.
Hakobyan H.G., Aleksanyan A.G., Dolukhanyan S.K. et al. // Intern. J. SHS. 2010. V.19. № 1. P. 49.
Aleksanyan A.G., Dolukhanyan S.K., Shekhtman V.Sh. et al. // J. Alloys Compd. 2011.V. 509. P. 786.
Aleksanyan A.G., Dolukhanyan S.K., Shekhtman V.Sh. et al. // Intern. J. Hydrogen Energy. 2012.V. 37. P. 14234.
Dolukhanyan S.K., Aleksanyan A.G., TerGalstyan O.P. et al. // Intern. J. Self-Propag. High-Temp Synth. 2014. V. 23. № 2. P. 78.
Долуханян С.К., Тер-Галстян О.П., Алексанян А.Г. и др. // Хим. физика. 2015. Т. 34. № 9. С. 1.
Мурадян Г.Н. // Арм. хим. журн. 2016. Т. 69. № 4. С. 416.
Долуханян С.К., Тер-Галстян О.П., Алексанян А.Г. и др. // Хим. физика. 2017. Т. 36. № 4. С. 1.
Dolukhanyan S.K. // Self-Propagating High-Temperature Synthesis of Materials / Eds. Borisov A.A., De Luca L., Merzhanov A.G. Combustion Science and Technology Book Series, V. 5. P. 219. N.Y.: Taylor & Francis, 2002.
Shekhtman V.Sh., Dolukhanyan S.K., Aleksanyan A.G. et al. // Intern. J. Hydrogen Energy. 2001. V. 26. P. 435.
Ravi C., Asokamani R. // Bull. Mater. Sci. 2003. V. 26. № 1. P. 97.
Chen X.F., Reviere R.D., Oliver B.F. et al. // Scripta. Metal. Mater. 1992. V. 27. P. 45.
Kainuma R., Fujita Y., Mitsui H. et al. // Intermetallics. 2000. V. 8. P. 855.
Попова Э.А., Шубин А.Б., Котенков П.В. и др. // Металлы. 2012. Т. 3. С. 3.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика