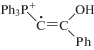Химическая физика, 2019, T. 38, № 12, стр. 19-26
Радикальные интермедиаты в реакциях смешанных фосфониево-иодониевых илидов
Т. Д. Некипелова 1, *, М. В. Мотякин 1, 2, В. В. Каспаров 1, Е. Н. Дегтярев 1, 2, И. И. Левина 1, И. Д. Потапов 1, 3, Т. А. Подругина 3
1 Институт биохимической физики им. Н.М. Эмануэля Российской академии наук
Москва, Россия
2 Федеральный исследовательский центр химической физики им. Н.Н. Семёнова
Российской академии наук
Москва, Россия
3 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
* E-mail: nekip@sky.chph.ras.ru
Поступила в редакцию 05.06.2019
После доработки 05.06.2019
Принята к публикации 20.06.2019
Аннотация
Методом магнитно-резонансной спектроскопии выполнено исследование активных интермедиатов, возникающих при фотолизе фосфониево-иодониевых илидов, и в их реакции с ацетиленами. С использованием стабильного нитроксильного радикала установлен радикальный механизм распада илида и инициирования взаимодействия илидов с ацетиленами. Впервые зарегистрированы радикальные продукты этих реакций и определены их магнитно-резонансные параметры. Сделано предположение о химическом строении активных интермедиатов исследованных реакций.
ВВЕДЕНИЕ
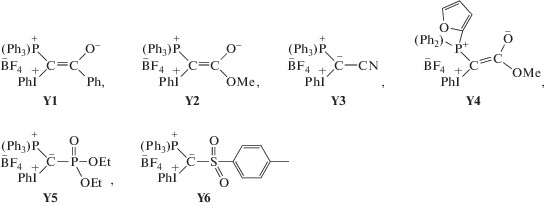
В настоящее время смешанные фосфониево-иодониевые илиды, общая формула которых представлена ниже, исследуются с целью синтеза на их основе новых гетероциклических соединений [1–7]:
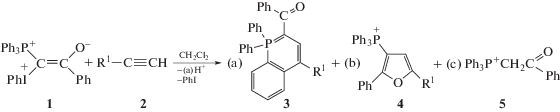
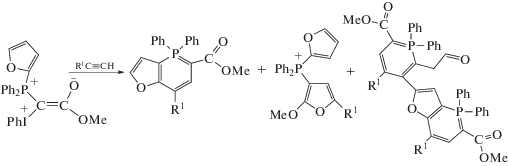
где R1 – Ph или пятичленный ароматический гетероцикл, а R2 = CO(Ph), CO(OMe), CO(OEt), CN, PO(OEt)2, S(O)2(п-MeC6H4).В последнее время открыты две новые реакции смешанных фосфониево-иодониевых илидов с соединениями, содержащими тройную связь (С≡N и С≡С), в результате которых образуются замещенные оксазолы (с нитрилами), фурановые производные и фосфорсодержащие гетероциклические соединения с ацетиленами. Реакция между илидами 1 и ацетиленами 2 является общей для фосфониево-иодониевых илидов различного строения [4–9] (Схема 1 ), а образующиеся гетероциклы являются перспективными функциональными материалами. Схема 1 приведена для бензоильного илида Y1, коэффициенты a, b и c характеризуют относительные выходы продуктов (a + b + c = = 0.7–1.0). В этой и последующих схемах противоион (BF4)– опущен для простоты, поскольку продуктов, образующихся с его участием, не было обнаружено.
Схема 1
Фенилиодониевая группа в составе смешанных илидов определяет их способность к разложению под действием света с образованием активных ионных и ион-радикальных интермедиатов, как это наблюдали для диарилиодониевых солей [10]. Недавно при фотолизе бензоильного илида Y1 (R1 = Ph, R2 = CO(Ph)) и его смесей с ацетиленами были зарегистрированы свободно-радикальные интермедиаты с временами жизни от нескольких минут до нескольких десятков минут [11]. Установлено, что регистрируемые методом ЭПР радикалы в смесях Y1–ацетилен образуются из короткоживущих радикальных предшественников. При этом для смеси илида Y1 с фенилацетиленом (ФА) радикальный продукт образуется только при облучении светом, а в случае 4-метоксифенилацетилена (МФА), 9-этинилфенантрена (9ЭФ) и 1-децина образование радикалов наблюдали сразу после смешения реагентов. В связи с этим возникает вопрос о роли процессов с участием радикалов, поскольку регистрируемые радикалы могут быть побочными продуктами реакции и не участвовать в образовании конечных целевых гетероциклических соединений. Чтобы получить ответ на этот вопрос, методами ЭПР и 31P ЯМР были проведены исследования кинетического процесса расходования илида Y1 и образования продуктов реакции в присутствии стабильного нитроксильного радикала 2,2,4,4-тетраметил-3-гидроксипиперидил-1-оксила (TEMPOL) для смеси Y1–МФА. Нитроксильные радикалы широко известны не только как зонды для определения локальной подвижности и организации различных молекулярных систем [12, 13], но и как эффективные акцепторы С-радикалов и в качестве таковых используются для ингибирования цепных радикальных реакций. Методом ЭПР при 77 K были зарегистрированы первичные радикалы, образующиеся при фотолизе илидов различного строения, а также радикалы, образующиеся в смесях илидов с ацетиленами при комнатной температуре. Результаты этого исследования представлены в данном сообщении.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Илиды Y1–Y6 синтезировали согласно методикам, предложенным в работах [1, 7, 9] и тщательно отмывали эфиром от кислоты (HBF4), которая используется в их синтезе:
Хлористый метилен (эталонный, “Компонент- Реактив”, Россия), не содержащий стабилизатора и HCl, использовали без дополнительной очистки. TEMPOL (компания “Sigma-Aldrich”) очищали перекристаллизацией из циклогексана. Спектры ЭПР Х-диапазона были записаны на спектрометре Bruker EMX (Германия). Микроволновая мощность во избежание эффектов насыщения была не более 2 мВт. При записи спектров амплитуда модуляции, равная 100 кГц, всегда была существенно меньше наименьшей ширины резонансной линии. Для определения магнитно-резонансных параметров ЭПР-линий и моделирования спектров использовали программы WinEPR и SimFonia.
Облучение растворов илидов в дихлометане CH2Cl2 в случае жидких растворов при комнатной температуре проводили в резонаторе ЭПР-спектрометра полным светом ртутной лампы или с использованием фильтра с пропусканием в области 360–480 нм в кварцевых (для полного УФ-спектра) или в стеклянных ампулах (при использовании фильтра). Для регистрации первичных радикалов растворы илидов замораживали при 77 K, облучали определенное время полным светом ртутной лампы или с использованием фильтра с пропусканием в области 360–480 нм и затем снимали спектры ЭПР. Спектры 31P ЯМР регистрировали на спектрометре AVANCE 500 (“Bruker”, Германия) в реакционной смеси в CH2Cl2 при непрерывном мониторинге (128 прохождений на спектр, ~2 мин).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Ингибирование реакции распада илида Y1 и его реакции с 4-метоксифенилацетиленом
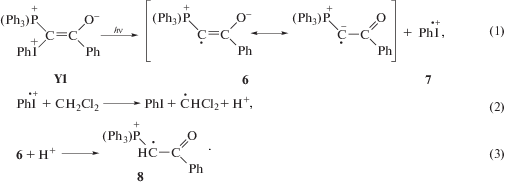
Зафиксировать расходование TEMPOL (0.001 M) при фотолизе илида Y1 (0.05 M) (λ ≥ 365 нм) в резонаторе ЭПР-спектрометра не представлялось возможным ввиду его очень быстрого расходования. По этой же причине оказалось невозможным определить период индукции расходования илида методом 31P ЯМР. Это означает, что скорость расходования TEMPOL выше 1.7 ∙ 10–5 М ∙ с–1. В этих условиях илид расходуется примерно за 1 ч, генерируя два радикала в одном акте распада (Схема 2 , реакция (1)). Это означает, что скорость расходования стабильного радикала сопоставима со скоростью распада Y1 (0.05/3600 = 1.4 ∙ 10–5 М ∙ с–1), т.е. илид расходуется преимущественно при распаде на радикалы, а не в цепной реакции.
Схема 2
Ранее было показано, что Y1 медленно распадается в темноте, давая те же продукты, что и при фотолизе [14]. Время полного расходования зависит от остаточного количества кислоты HBF4, используемой в синтезе. Порция Y1, исследуемая в данной работе, полностью расходуется в растворе CH2Cl2 в темноте за 24 ч. Для проверки радикального характера темновой реакции методом ЭПР было исследовано расходование TEMPOL (0.001 M) в растворе Y1 (0.05 M) в CH2Cl2 без облучения. Скорость расходования TEMPOL в этом случае составляла 4.2 ∙ 10–7 М ∙ с–1, что сопоставимо со скоростью расходования илида (~5.8 ∙ 10–7 М ∙ с–1). Таким образом, распад илида происходит с образованием радикальных интермедиатов. Если илид Y1 и TEMPOL взяты в одинаковых концентрациях (~0.05 M), илид расходуется в течение 3 сут, при этом в спектре 31P ЯМР регистрируется два продукта: фосфониевая соль 5 (72%) и продукт с сигналом около 29 м.д. (28%). Поскольку этот продукт регистрируется методом 31P ЯМР, то, очевидно, он содержит атом фосфора и является продуктом взаимодействия радикалов, образующихся из илида, с нитроксильным радикалом.
Система илид Y1–МФА является очень удобной для исследования взаимодействия илидов с ацетиленами, поскольку она не требует облучения; реакция начинается с небольшим периодом индукции после смешения реагентов ([Y1] = 0.05 M, [МФА] = 0.15 M). Целевые гетероциклы λ5-фосфинолин 3 и фурановое производное 4 образуются в соизмеримых концентрациях (Схема 1 , рис. 1, кривые 1–3), но если продукт 4 образуется за время расходования илида, то образование λ5-фосфинолина 3 продолжается еще в течение 1 ч из нескольких интермедиатов.
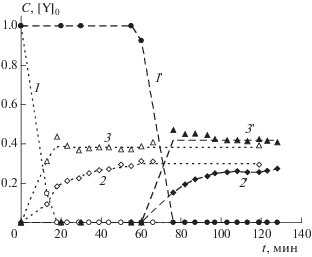
Рис. 1.
Кинетические кривые расходования илида Y1 (1, 1') и образования λ5-фосфинолина 3 (2, 2') и фуранового производного 4 (3, 3') в смеси илид Y1 (0.05 M) + + МФА (0.15 М) в отсутствие (1, 2, 3) и в присутствии добавки TEMPOL (1 ∙ 10–3 М) (1', 2', 3'); растворитель CH2Cl2, 24 °С.
При добавлении TEMPOL ([TEMPOL] = = 0.001 М) к смеси Y1–МФА методом 31P ЯМР регистрировали период индукции (60 мин), близкий к периоду расходования ингибитора в илиде без ацетилена (рис. 1, кривые 1'–3 '), после которого следует быстрое расходование Y1 в течение 20 мин, при этом образование продуктов происходит, как и в случае отсутствия ингибитора. Детальный механизм образования продуктов 3–5 будет обсужден в последующих публикациях. Для смеси, содержащей TEMPOL, изменения во времени в спектрах ЭПР согласуются с данными 31P ЯМР. В периоде индукции концентрация TEMPOL падает, а после его полного израсходования образуется новый радикальный продукт (рис. 2) со спектром, подобным спектру ион-радикала, который наблюдали ранее в смеси Y1–МФА [11].
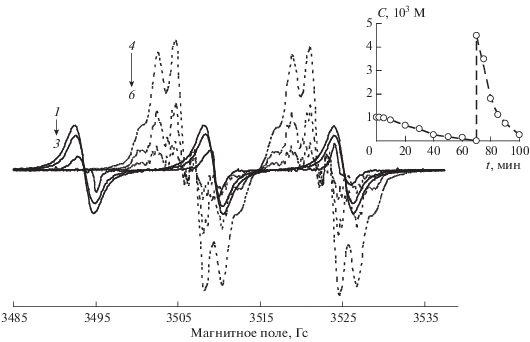
Рис. 2.
Изменение сигнала ЭПР во времени в смеси илид Y1 (0.05 M) + МФА (0.15 М) + TEMPOL (1 ∙ 10–3 М), время регистрации, мин: (1) 2, (2) 20, (3) 60, (4) 70, (5) 80, (6) 90. Вставка: кинетические кривые гибели сигнала радикала TEMPOL и образования сигнала нового радикального продукта реакции, растворитель CH2Cl2, 24 °С.
Полученные результаты свидетельствуют о том, что исследуемая реакция илида с ацетиленами инициируется радикалами, образующимися при распаде илида, или в реакции переноса электрона между илидом и МФА. Эти результаты также показывают, что основные продукты, λ5-фосфинолин 3, фурановое производное 4 и фосфониевая соль 5, образуются в параллельных реакциях первичных радикалов с МФА и растворителем.
Регистрация первичных радикалов и их превращений при фотолизе илидов при 77 K
Ранее в работе [11] было показано, что спектры ЭПР, наблюдаемые при облучении растворов илида Y1 в CH2Cl2 при комнатной температуре, являются вторичными продуктами фотолиза. Был предложен механизм их образования (Схема 2 ), который базируется на известном механизме фотораспада диарилиодониевых солей [10], и предположено, что фотогенерированный радикал 6 (реакция (1)) при взаимодействии с H+, образовавшимся из растворителя в реакции (2), дает катион-радикал 8 (реакция (3)), который регистрируется методом ЭПР. В результате реакции катион-радикала 8 с растворителем образуется фосфониевая соль 5, основной продукт фотолиза илидов.
Первичные радикалы 6 и 7 являются короткоживущими и не регистрируются методом ЭПР при комнатной температуре в реакционной среде, поэтому были проведены эксперименты по регистрации спектров ЭПР при фотолизе растворов илидов Y1, Y3, Y4 в CH2Cl2 при 77 K. Облучение растворов илидов в CH2Cl2 полным светом ртутной лампы (λ > 190 нм) в течение 4–8 мин приводит к возникновению в них радикалов (рис. 3). Cпектры ЭПР (рис. 3) являются суперпозицией двух сигналов. Первый сигнал – хорошо разрешенный дуплет с константой сверхтонкого взаимодействия (СТВ) аН = 505.8 ± 0.3 Гс и g-фактором g = 2.0020 ± 0.0001 (на рис. 3 отмечен штриховой линией). Подобные магнитно-резонансные параметры наблюдали для атомов водорода, стабилизированных в жестких матрицах [15]. Отметим, что данный дублет был получен также при УФ-облучении чистого растворителя, что позволяет с уверенностью отнести этот сигнал к атомарному водороду, полученному в результате фотодиссоциации С–Н-связи в молекуле растворителя. Второй сигнал – не так хорошо разрешен, однако его можно симулировать дублетом. В табл. 1 указаны расчетные константы СТВ и g-факторы для радикалов, образующихся при фотолизе исследованных илидов. Полученные значения констант СТВ и g‑факторов по своим величинам близки к магнитно-резонансным параметрам катион-радикалов фосфилалкиленов [16–19]: величина, аР, константы СТВ на фосфоре в этих радикалах варьируется в диапазоне 11–41 Гс. Также, согласно квантовохимическому расчету [11], неспаренный электрон в подобных радикалах локализуется преимущественно на углероде, так что все другие константы малы и маскируются огибающей линией, что мы и наблюдаем экспериментально. Таким образом, второй сигнал мы относим к катион-радикалу 6, образовавшемуся в результате фотохимического распада илидов (Схема 2 ).
Рис. 3.
Спектры ЭПР растворов илидов в CH2Cl2, облученных УФ-светом в течение 8 мин при 77 К: 1 – илид Y4, 2 – илид Y3, 3 – илид Y1. Магнитно-резонансные параметры ЭПР-сигналов представлены в табл. 1. Штриховой линией отмечены резонансные линии атома водорода.
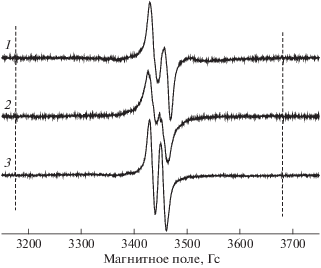
Таблица 1.
Константы СТВ и значения g-факторов для радикалов, образующихся при фотолизе растворов илидов в CH2Cl2 при 77 K
| Илид | Константа СТВ аР, Гс | g-фактор |
|---|---|---|
| Y1 | 21 ± 1 | 2.0030 ± 0.0001 |
| Y3 | 22 ± 1 | 2.0030 ± 0.0001 |
| Y4 | 23 ± 1 | 2.0032 ± 0.0001 |
При облучении видимым светом с длиной волны λ > 360 нм в растворах илидов в CH2Cl2 при 77 K регистрируются те же сигналы ЭПР, что и при УФ-облучении, однако их интенсивность намного слабее. Для получения интенсивных сигналов ЭПР требуется большее по сравнению с УФ время облучения.
Увеличение температуры до 293 K приводит к гибели радикалов в растворах илидов Y3 и Y4, в то время как в растворе илида Y1 в течение 30–40 мин наблюдается хорошо разрешенный сигнал ЭПР (рис. 4). Удовлетворительная симуляция спектра ЭПР данного радикала была получена в предположении расщеплений на ядре фосфора 31Р с константой СТВ ~ 23.66 Гс, на одном протоне с константой ~1.25 Гс, на трех протонах с константой СТВ ~ 4.47 Гс и на двух – с константой СТВ ~ 1.6 Гс (рис. 4). Стабильность этого радикала, по-видимому, обусловлена более эффективным экранированием реакционного центра дополнительным фенильным кольцом в илидном фрагменте молекулы. Сопоставление этого спектра со спектром катион-радикала 8, зарегистрированного при фотолизе Y1 в жидкой фазе (см. рис. 1 в работе [11]), демонстрирует, с одной стороны, близость параметров СТВ, которые относятся к взаимодействию неспаренного электрона с атомом фосфора и протонами фенильного кольца бензоильной группы, с другой стороны – показывает наличие взаимодействия с удаленным протоном с константой СТВ ~1.25 Гс, вместо 16.4 Гс для протона при радикальном центре для радикала 8 (Схема 2 ). Мы полагаем, что в данном случае радикал образуется из протонированной формы илида [14] и имеет следующее строение:
Рис. 4.
Спектр ЭПР (1) раствора илида Y1 в CH2Cl2, зарегистрированный при комнатной температуре после УФ-облучения при 77 К, и расчетный спектр (2) с константами СТВ, представленными в тексте.

Отметим, что все симуляции спектров ЭПР являются оценочными, поскольку раствор илида в CH2Cl2 представляет собой достаточно сложную микрогетерогенную систему [20], а зарегистрированные спектры ЭПР могут представлять собой суперпозицию нескольких спектров от разных, но близких по строению, радикалов.
Радикалы в смесях различных илидов с ацетиленами
Ранее на примере илида Y1 методом ЭПР при комнатной температуре в растворах CH2Cl2 было показано образование относительно стабильных радикальных интермедиатов в смесях этого илида с ацетиленами [11]. C целью установить радикальный характер реакций с ацетиленами для других илидов в настоящей работе было продолжено исследование радикальных продуктов, образующихся в условиях реакции, на примере илидов Y2–Y6. Результаты этого исследования представлены в табл. 2 и 3.
Таблица 2.
Константы СТВ, полученные при симуляции ЭПР-спектров илидов и их смесей с ацетиленами в растворе CH2Cl2*
| Илид | Ацетилен | Условия образования |
Константа СТВ, Гс |
|---|---|---|---|
| Y2 | – | λ ≥ 290 нм | 23.86 (1P), 17.56 (1H), 4.48 (2H), 1.60 (3H) |
| ФА | λ ≥ 380 нм | 19.74 (1P), дублет, быстро гибнет | |
| МФА | λ ≥ 380 нм | 18.03 (1P), 2.9 (1H), 2.37 (1H), 1.5 (1H) | |
| 9ЭФ | Без облучения | 19.99 (1P), 3.18 (1H), 2.08 (1H), 2.06 (1H), 1.89 (1H) | |
| Y3 | – | Радикал не регистрируется | – |
| ФА | λ ≥ 380 нм | 18.85 (1P) | |
| МФА | Без облучения | 15.27 (1P) | |
| 9ЭФ | Без облучения | 14.68 (1P) | |
| Y5 | – | λ ≥ 380 нм | 28.89 (2P), 4.9 (3H) |
| ФА | λ ≥ 380 нм | 16.16 (2Р) | |
| МФА | λ ≥ 380 нм | 18.31 (1P), 12.02 (1P), 2.26 (5H) | |
| 9ЭФ | Без облучения | 20.43 (1P), 13.21 (1P), 2.82 (1H), 2.15 (1H), 2.08 (1H), 1.54 (1H) | |
| Y6 | – | λ ≥ 290 нм | Дублет 30.9 (1P) образуется в течение 2 мин из более сложного спектра |
| ФА | λ ≥ 380 нм | 18.05 (1P), сигнал слабый | |
| МФА | λ ≥ 380 нм | 16.88 (1P), 2.52 (2H), 1.98 (2H), 1.90 (5H) | |
| 9ЭФ | Без облучения | 18.96 (1P), 2.98 (1H), 2.61 (1H), 2.31 (1H), 1.68 (1H) |
Таблица 3.
Константы СТВ, полученные при симуляции ЭПР-спектров смесей илида Y4 с ацетиленами*, **
| Ацетилен | Константы СТВ, Гс |
|---|---|
| ФА (первичный) | 21.27 (1), 3.90 (1), 2.09 (3) |
| ФА (через 30 мин) | 9.50 (2), 2.40 (4) |
| МФА (первичный) | 19.74 (1), 3.09 (1), 2.14 (1), 1.69 (1) |
| МФА (через 60 мин) | 9.87 (2), 1.99 (4) |
| 9ЭФ (первичный) | 20.45 (1), 2.55 (1), 1.98 (1) |
| 9ЭФ (через 21 мин) | 10.46 (2), 2.02 (1), 2.43 (1) |
Для илидов Y1 и Y5 образование радикалов в отсутствие ацетиленов происходит при облучении видимым светом с длиной волны λ ≥ 380 нм, для илидов Y2 и Y6 – при облучении УФ-светом с длиной волны λ ≥ 290 нм, а для илидов Y3 и Y4 образования радикалов в этих условиях не наблюдали. Это коррелируется с полученным результатом о быстрой гибели первичных радикалов из илидов Y3 и Y4, фотогенерированных при 77 K, при нагревании раствора до комнатной температуры. В присутствии ацетиленов радикалы образуются для всех исследуемых илидов при облучении видимым светом или в некоторых случаях без облучения (табл. 2). Чем ниже потенциал ионизации ацетилена и выше сродство к электрону илида, тем легче образуются радикалы. Форма спектра ЭПР, как и ранее для илида Y1, определяется наличием атома фосфора и структурой ацетилена, что указывает на то, что регистрируемые радикалы являются продуктами взаимодействия первичных радикалов 6 с ацетиленами. При этом следует подчеркнуть, что кроме сильного расщепления на ядре 31P, все остальные константы СТВ, полученные при моделировании, являются оценочными вследствие отмеченных ранее причин. Константы СТВ для 31P для радикалов, образующихся из илидов, выше, чем для их смесей с ацетиленами, что свидетельствует о перераспределении электронной плотности неспаренного электрона на остаток ацетилена. Следует отметить некоторые особенности образования радикалов для разных илидов и ацетиленов. Для всех илидов наблюдаемый радикал в смеси с ФА имеет наименьшую концентрацию и практически неразрешенную тонкую структуру кроме СТВ на 31P. Для илида Y3 спектры ЭПР радикалов, образующихся в смесях с ацетиленами, также слабо разрешены, что может быть связано со слабой растворимостью этого илида и микрогетерогенностью полученного раствора. Интересно отметить, что для илида Y5, содержащего два атома фосфора, спектр ЭПР для самого илида моделируется с достаточно высокой константой СТВ aP = 28.9 Гс для обоих атомов Р, а в случае радикалов, образовавшихся в смеси с ацетиленами, наблюдаются две константы СТВ (18–20 Гс и 12–13 Гс), которые могут быть отнесены к атомам фосфора, что свидетельствует о большей удаленности одного из ядер P от радикального центра.
Результаты, полученные для илида Y4 с фурильным заместителем при атоме фосфора, выделены в табл. 3, поскольку для этого илида спектры радикалов претерпевают превращения в процессе наблюдения. Первоначально наблюдаемые спектры представляют сложные дублеты с константой СТВ на ядре 31P 20–21 Гс. Затем эти радикалы постепенно в течение 20–60 мин превращаются в сложные триплеты с константой СТВ 9–10 Гс. Для этого илида, наряду с образованием соединений аналогичных 3 и 4 (Схема 1 ), известно образование продуктов, содержащих два атома фосфора за счет раскрытия фуранового кольца (Схема 3 ) [9]. Вероятно, наблюдаемые радикалы являются предшественниками этих продуктов.
Схема 3
ЗАКЛЮЧЕНИЕ
Таким образом, с использованием стабильного нитроксильного радикала однозначно установлен радикальный характер инициирования реакции смешанных фосфониево-иодониевых илидов с ацетиленами. Впервые зарегистрированы первичные радикалы, образующиеся при фотолизе илидов, и вторичные ион-радикальные интермедиаты, образующиеся в смесях илидов с ацетиленами. Показано, что эти радикальные интермедиаты образуются при взаимодействии всех исследованных фосфониево-иодониевых илидов с различными ацетиленами. Полученные результаты позволяют сделать вывод об универсальном характере взаимодействия смешанных фосфониево-иодониевых илидов с терминальными ацетиленами и об участии ион-радикальных интермедиатов в образовании целевых гетероциклических соединений.
Спектральные измерения методами ЭПР и 31P ЯМР спектроскопии проведены в Центре коллективного пользования ИБХФ РАН “Новые материалы и технологии”. Работа выполнена в рамках госзадания, тема № 1201253303.
Список литературы
Матвеева Е.Д., Подругина Т.А., Гришин Ю.К. и др. // ЖOрХ. 2003. Т. 39. № 4. С. 572.
Матвеева Е.Д., Подругина Т.А., Гришин Ю.К. и др. // Там же. 2007. Т. 43. № 2. С. 209.
Матвеева Е.Д., Подругина Т.А., Павлова А.С. и др. // Изв. АН. Сер. хим. 2008. № 2. С. 391.
Матвеева Е.Д., Подругина Т.А., Павлова А.С. и др. // Там же. № 10. С. 2195.
Matveeva E.D., Podrugina T.A., Pavlova A.S. et al. // Eur. J. Org. Chem. 2009. № 14. P. 2323.
Matveeva E.D., Podrugina T.A., Pavlova A.S. et al. // J. Org. Chem. 2009.V. 74. P. 9428.
Matveeva E.D., Podrugina T.A., Taranova M.A. et al. // J. Org. Chem. 2011. V. 76. P. 566.
Nekipelova T.D., Kuzmin V.A., Matveeva E.D. et al. // J. Phys. Org. Chem. 2013. V. 26. P. 137.
Matveeva E.D., Vinogradov D.S., Podrugina T.A., Nekipelova T.D. et al. // Eur. J. Org. Chem. 2015. P. 7324.
Dektar J.L., Hacker N.P. // J. Org. Chem. 1990. V. 55. P. 639.
Некипелова Т.Д., Каспаров В.В., Коварский А.Л., Воробьев А.Х., Подругина Т.А. и др. // Докл. АН. 2017. Т. 474. № 6. С. 707.
Karpova S.G., Olkhov A.A., Bakirov A.V. et al. // Russian J. Physical Chemistry B. 2018. V. 12. № 1. P. 142.
Ol’khov A.A., Tertyshnaya Yu.V., Chizhov A.S. et al. // Russian J. Physical Chemistry B. 2018. V. 12. № 2. P. 293.
Некипелова Т.Д., Подругина Т.А., Виноградов Д.С., Демьянов П.И., Кузьмин В.А. // Кинетика и катализ. 2019. Т. 60. С. 45.
Stolla S., Ozarowski A., Britt R.D. et al. // J. Magn. Reson. 2010. V. 207. P. 158.
Buck H.M., Huizer A.H., Oldenburg S.J., Schipper P. // Recl. Trav. Chim. Pays–Bas. 1970. V. 89. P. 1085.
Lyons A.R., Symons M.C.R. // J. Chem. Soc., Faraday Trans. II. 1972. V. 68. P. 622.
Wienk M.M., Janssen R.A.J. // J. Amer. Chem. Soc. 1997. V. 119. P. 5398.
Левин Я.А., Воркунова Е.И. Гомолитическая химия фосфора. М: Наука, 1978.
Levina I.I., Klimovich O.N., Bormotov D.S., Vinogradov D.S., Kononikhin A.S., Dement’eva O.V., Senchikhin I.N., Podrugina T.A., Nikolaev E.N., Kuzmin V.A., Nekipelova T.D. // J. Phys. Org. Chem. 2018. V. 31. № 7. P. e3844; https://doi.org/10.1002/poc.3844
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика


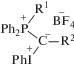 ,
,