Химическая физика, 2019, T. 38, № 2, стр. 16-23
Исследование механизма химических превращений при горении смесей термитного типа MoO3/TiO2/Al/Si
В. А. Горшков 1, *, П. А. Милосердов 1, Н. В. Сачкова 1
1 Институт структурной макрокинетики и проблем материаловедения им. А.Г. Мержанова
Российской академии наук
Черноголовка, Россия
* E-mail: gorsh@ism.ac.ru
Поступила в редакцию 21.02.2018
После доработки 20.06.2018
Принята к публикации 23.05.2018
Аннотация
Проведено исследование механизма химического превращения исходных компонентов в волне горения смесей термитного типа MoO3/TiO2/Al/Si при синтезе литых дисилицида молибдена (MoSi2) и бинарных силицидов молибдена–титана (MoTi)Si2. Синтезы проводили в СВС-реакторе при начальном давлении аргона Р0 = 5 МПa. Экспериментально изучено влияние соотношения исходных реагентов и геометрических факторов на закономерности синтеза этих материалов. Определены интервалы соотношений компонентов, при которых можно синтезировать силициды молибдена и титана с заданными составами. Проведены эксперименты по остановке фронта горения. Показано, что химическое превращение компонентов исходных смесей MoO3/TiO2/Al/Si в волне горения протекает стадийно, а химические реакции можно рассматривать как химически сопряженные процессы. Полученные результаты являются научной основой для создания перспективной литой силицидной керамики, имеющей высокие эксплуатационные свойства.
ВВЕДЕНИЕ
В последнее время широкое распространение получили исследования по созданию керамических материалов с повышенными эксплуатационными свойствами на основе двойных силицидов молибдена, вольфрама, ниобия, титана и др. [1–5 ]. Большое внимание в этих работах уделяется изучению состава и свойств таких материалов, а также разработке новых способов их получения. Из наиболее перспективных методов получения литой силицидной керамики на основе силицидов переходных металлов является самораспространяющийся высокотемпературный синтез (СВС), который практически не требует энергозатрат [6–8 ]. Одним из направлений этого метода является СВС-металлургия. В основе процесса лежат высокоэкзотермические реакции термитного типа с температурами горения выше температур плавления конечных продуктов, получаемых во время синтеза в жидкофазном состоянии [9–11 ]. Эти процессы являются высокоэнергетическими и протекают в атмосферных условиях в нестационарном режиме горения с большим (более 50%) диспергированием (разбросом) реакционной массы и конечных продуктов. Для перевода процесса горения в стационарный режим и уменьшения диспергирования синтезы организуют в СВС-реакторах при начальном избыточном давлении газовой среды (Ar, N) Р0 = 5 МПа. В последнее время в этом направлении выполнен цикл работ, связанный с интересами практики к литой силицидной керамике. В рамках этих исследований было показано, что методом СВС-металлургии можно получать литые композиционные материалы в системах Mo–W–Si, Mo–Nb–Si и Mo–Ti–Si в широких диапазонах соотношений между силицидами [12–16 ] . Из проведенных исследований следует, что наиболее важными параметрами синтеза, влияющими на все стадии процесса, являются: давление газа в реакторе, соотношение реагентов исходных смесей, размер частиц компонентов, а также масштабный (масса смеси) и геометрический факторы (объем реакционной формы, отношение ее диаметра и высоты). Эти параметры оказывают существенное влияние на закономерности горения, процесс фазоразделения, полноту химического превращения, а также формирование состава и микроструктуры литых конечных продуктов. Для организации процесса высокотемпературного синтеза в оптимальных условиях необходимо понимание механизма химических превращений, происходящих в волне горения смесей термитного типа.
В данной работе проведено исследование механизма химического превращения исходных компонентов в волне горения смесей термитного типа MoO3/TiO2/Al/Si при синтезе литых дисилицида молибдена (MoSi2) и бинарных силицидов молибдена–титана (MoTi)Si2. Для этого в экспериментах изучено влияние масштабного и геометрического факторов на закономерности синтеза этих материалов, проведены эксперименты по остановке фронта горения.
МЕТОДИКИ ИССЛЕДОВАНИЯ
В работе осуществляли термодинамический расчет адиабатической температуры горения по программе “Thermo” [17] и проводили экспериментальные исследования. В экспериментах использовали смеси порошков оксидов молибдена(VI) и титана(IV) марки “ЧДА” с алюминием марки АСД-1 и кремнием марки КР0. При изучении процессов горения, диспергирования, фазоразделения, формирования фазового и химического составов, а также и микроструктуры конечных продуктов шихты сжигали в кварцевых стаканчиках диаметром от 10 до 25 мм, высотой 50 мм. Массу исходных смесей варьировали от 15 до 30 г. Синтезы проводили в СВС-реакторах объемом 3 л в атмосфере аргона при начальном давлении 5 МПа.
Для расчета составов исходных смесей использовали следующие химические схемы и их сочетание:
В экспериментах проводили видеосъемку, определяли среднюю линейную скорость горения (U0), потерю массы при синтезе (ηd) за счет диспергирования вещества из реакционной формы и полноту выхода целевого продукта в слиток (ηing) по следующим формулам: U0 = h/tc, где h – высота слоя исходной смеси, tc – время горения смеси, ηd = (М0 – М1)/М0 ⋅ 100%, где М0 – начальная масса смеси, а М1 – конечная масса, а ηing = Мexp/Мcalc ⋅ ⋅ 100%, где Мexp – масса слитка MoSi2 в эксперименте, а Мcalc – масса MoSi2, расcчитаная из схемы химического превращения. Конечные продукты исследовали визуально, а микроструктуру и состав целевых продуктов изучали на автоэмиссионном сканирующем электронном микроскопе сверхвысокого разрешения Zeiss Ultra plus на базе Ultra 55, Германия (Zeiss Ultra plus Field Emission Scanning Electron Microscope).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
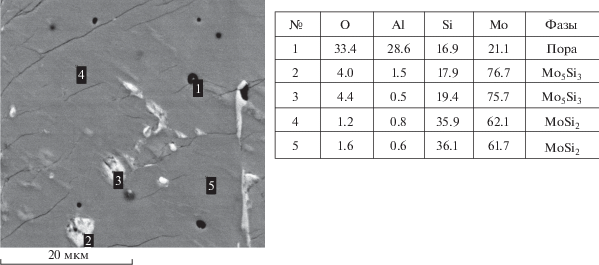
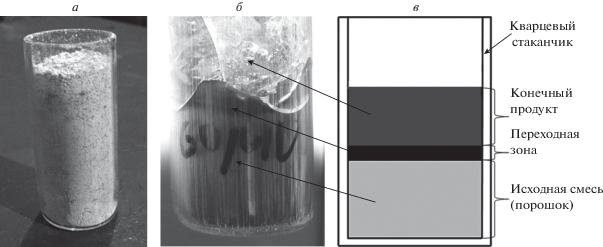
Эксперименты показали, что при начальном давлении газа Р0 = 0.1 МПа горение смеси MoO3/2Al/2Si происходит с практически полным разбросом реакционной массы. С увеличением Р0 выход целевых элементов в металлический слой (ηing) растет и при Р0 = 5 МПа, достигает 96% и дальше не меняется. Выброс вещества из реакционной формы при этом, наоборот, уменьшается, и при Р0 = 5 МПа достигает минимального значения 4%, после чего не меняется. Поэтому все эксперименты проводили при начальном давлении 5 МПа. Осуществить горение смесей MoO3/3.5Si и 3TiO2/4Al/6Si не удалось, несмотря на высокую расчетную температуру горения. В исследованиях по влиянию соотношения Y/X между MoO3/2Al/2Si и MoO3/3.5Si смесями на закономерности синтеза обнаружено (рис. 1), что с увеличением содержания Y/X величины скорости горения (U0) и полноты выхода целевого продукта (ηing) вначале медленно уменьшаются, а затем, при Y/X выше 0.6 наблюдается их резкое падение. Потеря массы (ηd) при этом меняется незначительно от 4 до 2%. На рис. 2 представлены микроструктура и элементный состав силицидного продукта, полученного в интервале изменения Y/X 0.2–0.6. Из анализа микроструктуры, расчета содержания элементов (рис. 2) и диаграммы состояния следует, что материал состоит в основном из фазы, соответствующей дисилициду молибдена (№ 4 и № 5). В нем также присутствует фаза, соответствующая силициду молибдена Mo5Si3 (№ 2 и № 3). Аналогичные зависимости скорости горения (U), полноты выхода целевого продукта в слиток (ηing) и потери массы при синтезе (ηd) наблюдаются при изменении в исходной смеси соотношения Z/X между MoO3/2Al/2Si и 3TiO2/4Al/6Si. Кривые зависимостей U0, ηing и ηd от соотношения Z/X представлены на рис. 3. Из представленного графика видно, что с увеличением Z/X происходит уменьшение U и ηing, а ηd практически не меняется. На рис. 4 представлены микроструктура и элементный состав силицидного продукта, полученного в интервале изменения Z/X от 0 до 0.2. Из анализа микроструктуры, расчета содержания элементов и фазовой диаграммы следует, что материал состоит в основном из фазы, соответствующей растворам силицида титана и молибдена (№№ 1–3). В нем также присутствует фаза, соответствующая дисилициду титана. Визуальные наблюдения и видеосъемка процесса горения в прозрачных кварцевых стаканчиках под давлением 5 МПа показали, что фронт горения данных смесей плоский и распространяется с постоянной скоростью для соотношений Y/X в интервале 0.2–0.6, и Z/X – 0 до 0.2. Конечные продукты в этих интервалах соотношений получаются в жидкофазном состоянии, и из-за различных удельных весов [18–20] под действием гравитации происходит сепарация силицидной и оксидной фаз. В результате после охлаждения и кристаллизации конечные продукты состоят из двух легко отделяемых друг от друга слитков: внизу – целевой продукт (Mо–Ti)Si2, а вверху – оксид Al2O3–SiO2. В дальнейших экспериментах с целью изучения механизма химических превращений в волне “жидкофазного” горения проводили остановку фронта горения. Для этого были выбраны исходные смеси с соотношением Y/X 0.8/0.2 и Z/X = 0.25/0.75. Смеси помещали в кварцевые стаканчики высотой 50 мм. В опытах уменьшали диаметр стаканчиков, а высота была постоянной. В результате удалось осуществить остановку фронта в смеси Y/X состава 0.8/0.2 при критическом диаметре $d_{{cr}}^{{(1)}}$ = 10 мм, а для смеси Z/X состава 0.25/0.75 – при критическом диаметре $d_{{cr}}^{{(2)}}$. = 15 мм (рис. 5). Полученные “реакционные ячейки” (зоны между исходной смесью и конечными продуктами) были проанализированы методом локального рентгеноспектрального анализа. Исследования образцов показали, что в нижней части формы находится непрореагировавшая смесь в верхней – литой оксидный продукт, а между ними – переходная зона. Из анализа микроструктуры и локального состава ее структурных составляющих (рис. 6) следует, что переходная зона представляет собой керметный слой. В этом слое матрица сформирована из оксидного раствора (Al–Si–O, № 2), в которой распределены частицы силицидного продукта (Mo-Si, № 4 и № 5), остатки исходных реагентов (Si, № 3) и (MoO, № 6) и промежуточные продукты (Al–O–Si, № 2 и Si–O, № 1). Из полученных результатов следует, что жидкофазное химическое превращение исходной смеси MoO3/Al/Si в волне горения протекает стадийно и представляет набор возможных реакций, протекающих в процессе химического взаимодействия в волне горения:
(1)
${\text{Mo}}{{{\text{O}}}_{3}} + 2{\text{Al}} \to {\text{A}}{{{\text{l}}}_{2}}{{{\text{O}}}_{3}} + {\text{Mo}},$(2)
$2{\text{Mo}}{{{\text{O}}}_{3}} + 3{\text{Si}} \to 3{\text{Si}}{{{\text{O}}}_{2}} + 2{\text{Mo}},$(3)
${\text{Mo}}{{{\text{O}}}_{3}} + {\text{A}}{{{\text{l}}}_{2}}{{{\text{O}}}_{3}} + {\text{Si}}{{{\text{O}}}_{2}} \to {\text{Mo}}{{{\text{O}}}_{3}} - {\text{A}}{{{\text{l}}}_{2}}{{{\text{O}}}_{3}} - {\text{ Si}}{{{\text{O}}}_{2}},$(6)
$\begin{gathered} {\text{Mo}} - {\text{Al}} + {\text{Mo}}{{{\text{O}}}_{3}} - {\text{ A}}{{{\text{l}}}_{2}}{{{\text{O}}}_{3}} - {\text{ Si}}{{{\text{O}}}_{2}} \to \\ \to {\text{Mo}} - {\text{Si}} + {\text{A}}{{{\text{l}}}_{2}}{{{\text{O}}}_{3}} - {\text{ Si}}{{{\text{O}}}_{2}}. \\ \end{gathered} $Рис. 1.
Влияние соотношения исходных смесей Y/X на скорость горения (U), выход целевого продукта (ηing) и глубину разброса (ηd).
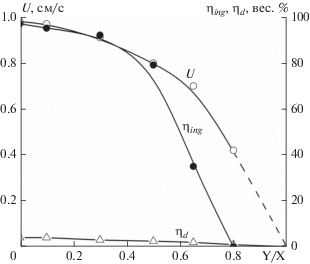
Рис. 3.
Влияние соотношения исходных смесей Z/X на скорость горения (U), выход целевого продукта (ηing) и глубину разброса (ηd).
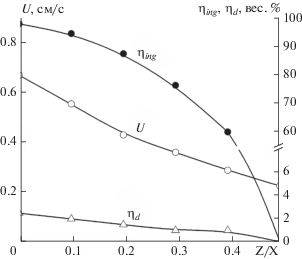
Рис. 4.
Микроструктура и элементный состав целевого продукта, полученного при соотношении смесей Z/X состава 0/1.
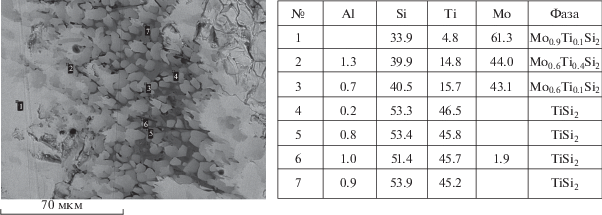
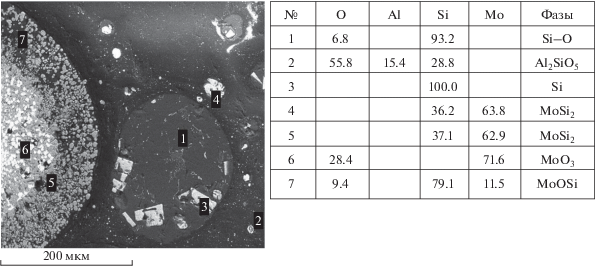
Рис. 6.
Реакционная ячейка, полученная при горении шихты с соотношением смесей Y/X 0.8/0.2 при dcr = 10 мм.
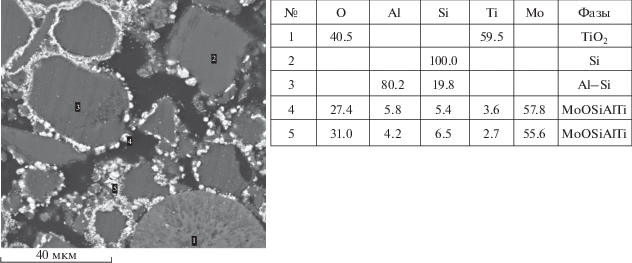
Анализ микроструктуры и локального состава “реакционной ячейки” второго образца для системы MoO3/TiO2/Al/Si (рис. 7) показал, что в этом случае наблюдается аналогичная картина, как и для системы MoO3/Al/Si. В этом слое матрица сформирована из оксидного раствора MoOSiAlTi (№ 4 и № 5), в которой распределены частицы TiО (№ 1), Si (№ 2) и Al–Si (№ 3).
Рис. 7.
Реакционная ячейка, полученная при горении шихты с соотношением смесей Z/X состава 0.25/0.75 при dcr = 15 мм.
Из полученных результатов следует, что жидкофазное химическое превращение исходной смеси MoO3/TiO2/Al/Si в волне горения также протекает стадийно и представляет набор возможных реакций, протекающих в процессе химического взаимодействия в волне горения:
Вначале на границе расплавов оксида молибдена с алюминием и кремнием протекают восстановительные процессы (1')–(3'). Образуются промежуточные оксидные (4') и металлические (5') растворы. После формирования матричного раствора Mo–Ti–Al–Si–Ox, (вследствие диффузионного растворения) протекает реакция (6').
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
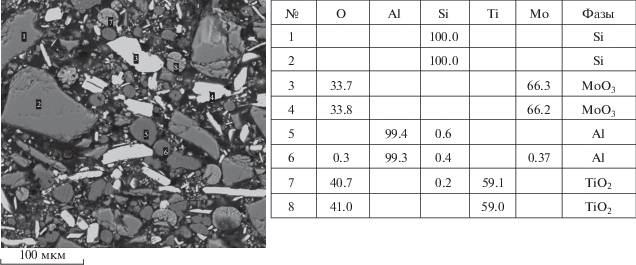
Из анализа результатов проведенного исследования и предыдущих работ [13–16 ] по синтезу литых силицидов молибдена и титана при горении систем термитного типа: MoO3/Al/Si и MoO3/TiO2/Al/Si следует, что основными параметрами, влияющими на все стадии синтеза, являются: давление газовой среды в реакторе, геометрический (масштабный) фактор, соотношение и размер частиц исходных реагентов. Эксперименты показали, что шихты, состоящие из различных сочетаний “горячей” (MoO3/2Al/2Si) и “холодных” (MoO3/3.5Si, 3TiO2/4Al/6Si) смесей горят в широком интервале соотношений реагентов. Эти реакции (X + Y и X + Z) можно рассматривать как химически сопряженные процессы. Термин “сопряженные реакции” используется “…для обозначения такой системы двух протекающих в одной среде реакций, из которых одна зависит в своем течении от другой” [21]. Следует отметить, что “чисто” химическое сопряжение осуществляется в изотермических условиях, когда перенос химической энергии от реакции, дающей эту энергию, к реакции, ее акцептирующую, возможен только при наличии общего промежуточного продукта. Применительно к СВС идея организации сопряженных процессов принадлежит акад. А.Г. Мержанову. Он дал следующее определение сопряженных СВС-процессов: это процессы, в которых основная слабоэкзотермическая реакция (акцептор тепла) протекает одновременно с другой сильноэкзотермической (донор тепла) [21, 22]. В проведенных опытах были выявлены интервалы соотношений компонентов, при которых можно синтезировать силициды молибдена и титана с заданными составами. Для исследования механизма химического превращения были выбраны наиболее “холодные” составы, горение которых проходило вблизи предела горения. На этих составах при постоянной высоте образцов уменьшали их диаметры. В результате возрастали теплопотери и при критических значениях диаметров: для смеси Y/X состава 0.8/0.2 ($d_{{cr}}^{{(1)}}$ = 10 мм), а для смеси Z/X состава 0.25/0.75 ($d_{{cr}}^{{(2)}}$ = 15 мм) получили остановку фронта горения. Из рис. 5б, в видно, что между исходной смесью и литыми конечными продуктами находится промежуточная зона (зона реакции). По-видимому, в этой зоне происходит основное выделение тепла, плавление и перемешивание исходных реагентов, промежуточных и конечных продуктов химических реакций. Из анализа “реакционных ячеек” (рис. 6 и 7) следует, что реакции в этой зоне протекают стадийно. Основной (ведущей) реакцией является восстановление MoO3 алюминием (1), (1'). Оксид молибдена(VI) и Al являются наиболее легкоплавким и из всех компонентов исходной смеси (табл. 1) и расплавляются в зоне прогрева первыми, образуя жидкую среду. Плотность среды при этом меняется и, из-за различных удельных весов исходных реагентов и конечных продуктов, происходит движение среды. Частички алюминия покрыты тонкой тугоплавкой пленкой, которая из-за гидродинамических и термических напряжений разрушается, и Al вступает в окислительно-восстановительную реакцию с оксидом металла [9, 23, 24]. Кремний по сравнению с алюминием более инертный, он имеет температуру плавления почти в 2 раза выше температуры плавления алюминия (табл. 1), а его частицы в несколько раз крупнее частиц Al (рис. 8). В результате конкуренцию в окислительно-восстановительных реакциях выигрывает алюминий и успевает полностью прореагировать в зоне реакции. Это подтверждается тем, что в зоне реакции алюминий в свободном виде не обнаружен, а присутствует только в виде конечного продукта (оксида алюминия) или промежуточных продуктов (оксидных и металлических растворов). В дальнейшем происходит формирование матричных растворов MoO3–Al2O3–SiO2 и Mo–Ti–Al–Si–Ox, после чего, вследствие диффузионного растворения, протекает реакция (6), (6') с образованием конечных продуктов. Анализ результатов исследования химических превращений в волне “жидкофазного” горения показал, что в ней происходят окислительно-восстановительные реакции, ведущую роль в которых играет реакция восстановления оксида молибдена алюминием. При этом кремний также принимает участие в этих реакциях, и все превращения в волне горения можно рассматривать как химически сопряженные процессы. Само же превращение исходных реагентов в конечные продукты происходит стадийно с образованием промежуточных продуктов. Для получения целевых силицидных материалов с заданным составом и микроструктурой необходимо варьировать соотношение реагентов в определенных интервалах, а также использовать порошок кремния с избытком по отношению к стехиометрическому значению и с более крупными частицами ($d_{r}^{{{\text{Si}}}} \gg d_{r}^{{{\text{Al}}}}$), чем у порошка алюминия.
ЗАКЛЮЧЕНИЕ
Из проведенных исследований следует, что наиболее важными параметрами синтеза, влияющими на все стадии процесса, являются: давление газа в реакторе, соотношение реагентов исходных смесей, а также геометрический фактор (объем реакционной формы, отношение ее диаметра и высоты). Определены интервалы соотношений компонентов, при которых синтезированы силициды молибдена и титана с заданными составами. Проведены эксперименты по остановке фронта горения. Изучены микроструктуры и локальный состав полученной “реакционной ячейки” методом локального микроструктурного анализа. Показано, что химическое превращение компонентов исходных смесей MoO3/TiO2/Al/Si в волне горения протекает стадийно, а химические реакции, используемые при проведении синтеза, можно рассматривать как химически сопряженные процессы. Полученные знания являются научной основой для создания перспективной литой силицидной керамики, имеющей высокие эксплуатационные свойства.
Для выполнения исследований было использованно оборудование распределенного центра коллективного пользования ИСМАН.
Список литературы
Zhang H., Chen P., Yan J., Tang S. // Int. J. Refract. Met. Hard Mater. 2004. V. 22. P. 271.
Tantry S.P., Ramasesha S.K., Lee J.-S., Yano T., Ramamurty U. // J. Amer. Ceram. Soc. 2004. V. 87. Issue 4. P. 626.
Qiang H., Chaoli M., Xinqing Z., Huibin X. // Chin. J. Aeronautics. 2008. V. 21. P. 448.
Matsuura K., Ohmi T., Kudoh M., Hasegawa T. // Metall. Mater. Trans. A. 2000. V. 31. Issue 3. P. 747.
Титов Д.Д., Каргин Ю.Ф., Лысенков А.С., Попова Н.А., Горшков В.А. // Материаловедение. 2012. № 7. С. 45.
Merzhanov A.G. SHS on the Pathway to Industrialization. Chernogolovka: ISMAN. 2001.
Merzhanov A.G. // J. Mater. Chem. 2004. V. 14. Issue 12. P. 1779.
Levashov E.A., Mukasyan A.S., Rogachev A.S., Shtansky D.V. // Intern. Mater. Rev. 2017. V. 62. Issue 4. P. 203.
Юхвид В.И. // Изв. вузов. Цв. метуллургия. 2006. № 5. С. 62.
Yukhvid V.I. // Proc. “SHS of materials”. New-York: Taylor and Francis Inc., 2002. P. 238.
Левашов А.Е., Рогачев А.С., Юхвид В.И., Боровинская И.П. Физико-химические и технологические основы самораспространяющегося высокотемпературного синтеза. М.: БИНОМ, 1999.
Горшков В.А., Самборук А.А., Юхвид В.И. // Хим. физика. 2009. Т. 28. № 10. С. 48.
Горшков В.А., Юхвид В.И., Милосердов П.А., Сачкова Н.В. // Неорган. материалы. 2011. Т. 47. № 4. С. 429.
Gorshkov V.A., Yukhvid V.I., Miloserdov P.A., Sachkova N.V., Kovalev D.Yu. // Intern. J. Self-Propag. High-Temp Synth. 2011. V. 20. № 2. P. 100.
Милосердов П.А., Горшков В.А., Юхвид В.И., Сачкова Н.В. // Перспективные материалы. 2013. № 6. С. 69.
Gorshkov V.A., Miloserdov P.A., Sachkova N.V., Kovalev I.D. // Intern. J. Self-Propag. High-Temp Synth. 2014. V. 23. № 1. P. 36.
Shiryaev A. // Ibid 1995. V.4. № 4. P. 351.
Волков А.И., Жарский И.М. Большой химический справочник. Минск: Современная школа, 2005.
Химическая энциклопедия / Под ред.: Кнунянц И.Л. и др. Т. 3. М.: Советская энциклопедия, 1992.
Рипан Р., Четяну И. Неорганическая химия. Химия металлов. Пер. с румынск. Т. 2. М.: Мир, 1972.
Мержанов А.Г. // Докл. РАН. 2010. Т. 434. № 4. С. 489.
Мержанов А.Г. // Вестн. АН СССР. 1979. № 8. С. 10.
Лякишев Н.П., Плинер Ю.Л., Игнатенко Г.Ф., Лаппо С.И. Алюминотермия. М.: Металлургия, 1978.
Юхвид В.И. Самораспространяющейся высокотемпературный синтез: теория и практика. Черноголовка: Территория, 2001. С. 252.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика