Химическая физика, 2019, T. 38, № 5, стр. 17-22
Особенности формирования и стабилизации наночастиц металлов Au, Ag, Ru, Rh и биметаллов в обратномицеллярных растворах
К. Ф. Чернышова 1, *, А. А. Ревина 1
1 Институт физической химии и электрохимии им. А.Н. Фрумкина Российской академии наук
Москва, Россия
* E-mail: karish@list.ru
Поступила в редакцию 21.09.2018
После доработки 19.11.2018
Принята к публикации 21.11.2018
Аннотация
В настоящей работе представлены результаты исследования оптических свойств наноразмерных частиц серебра, золота, родия, рутения, полученных в обратномицеллярных растворах (ОМР) при использовании реакции химического восстановления ионов Men+ в присутствии молекулярного кислорода и восстановителя флавоноида – кверцетина. Методом “молекулярной сборки” были получены наночастицы металлов и биметаллов: Au/Ag, Au/Ru и Au/Rh. Методом UV–VIS-спектрофотометрии исследованы спектральные характеристики монометаллических и биметаллических наночастиц и изучена кинетика их формирования в ОМР.
ВВЕДЕНИЕ
В настоящее время большой интерес вызывает разработка методов направленного синтеза гетероядерных металлических наноразмерных кластеров. Одним из наиболее перспективных направлений является создание новых функциональных материалов на основе биметаллических наночастиц благородных металлов. Биметаллические наночастицы представляют интерес благодаря уникальным электрическим [1], химическим [2], каталитическим [3] и оптическим свойствам [4], которые определяются формой, размером, составом и структурой наночастиц (НЧ).
Синтез полиметаллических наночастиц может происходить как путем агрегации различных атомов и ионов металлов, что приводит к формированию упорядоченной структуры “сплава” [5], так и последовательной агрегацией разных атомов, приводящей к образованию кластеров со структурой типа “core–shell” (ядро–оболочка) [6].
Настоящая работа посвящена синтезу и изучению физико-химических свойств НЧ металлов и полиметалических НЧ бинарных сплавов, полученных методом химического восстановления ионов металлов в обратных мицеллах [7]. Основное преимущество данного метода заключается в том, что образование наночастиц осуществляется в полярном ядре мицеллы, в самоорганизующей среде, способствующей формированию наноструктурных агрегатов. В то же время оболочка мицеллы создает определенные ограничения для роста этих агрегатов, позволяя получать стабильные частицы наноразмеров [8, 9]. Главная особенность метода химического синтеза состоит в том, что в нем в качестве восстановителя используется природное биологически активное соединение из группы флавоноидов – кверцетин (Qr) [10, 11].
В работе рассмотрены основные особенности формирования монометаллических наночастиц Au, Ag, Rh, Ru и биметаллических золотосодержащих наночастиц Au/Ag, Au/Rh, Au/Ru.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали:
• 0.3 М AgNO3 компании “Реахим”;
• 0.048 М HAuCl4 компании “Реахим”;
• 0.04 M RhCl3 ⋅ 4H2O;
• 0.04 M RuOHCl3;
• бис-(2-этилгексил)-сульфосукцинат натрия (АОТ) фирмы “Acros Organics”;
• 3,3',4',5,7-пентагидроксифлавон (С15H10O7) фирмы “Merk” – кверцетин (Qr);
• изооктан (“Компонент-Реактив”);
• миллипоровская вода, удельное сопротивление – 17.8 МОм/см.
Для синтеза наночастиц использовали обратномицеллярные растворы (ОМР) 0.15 М АОТ/изооктан, содержащие 150 мкМ Qr, в которые вводили необходимое количество водных растворов солей в соответствии со значением степени гидратации ω (ω = [H2O]/[AOT]). Синтез НЧ проводился при температуре 21–23 °С в аэробных условиях. Согласно ранее полученным экспериментальным результатам [12], НЧ металлов при химическом синтезе достигали своих окончательных размеров и концентрации в течение двух недель. При изучении кинетики формирования НЧ измерение спектров оптического поглощения (ОП) растворов начиналось через одну минуту после введения в ОМР ионов металлов.
Для измерения спектров оптического поглощения использовали UV–VIS-спектрофотометр Hitachi U-3010 в диапазоне длин волн от 190 до 900 нм, кварцевые кюветы с длиной оптического пути 1 и 10 мм. В качестве раствора сравнения был выбран 0.15 М раствор АОТ в изооктане. Спектры оптического поглощения ОМР регистрировались при комнатной температуре.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Главной особенностью наночастиц металлов является наличие так называемого поверхностного плазмонного резонанса, который представляет собой коллективные колебания поверхностных электронов. Параметры электронного плазмонного резонанса – интенсивность, полуширина полосы и положение в спектре – зависят от материала частицы, ее размера, формы, структуры, состава и влияния окружающей среды. При этом интенсивность как поглощения, так и рассеяния в максимуме полосы чрезвычайно велика, так что полосы плазмонного резонанса могут служить весьма эффективными датчиками в исследованиях наночастиц и окружающей их среды.
Оптические свойства коллоидных систем и их зависимость от размеров и формы частиц традиционно изучались на золях серебра и золота [13–15]. Серебро и золото в коллоидной форме в воде обнаруживают узкие и отчетливые полосы поглощения в ультрафиолетовой и видимой областях. Электроны в них существуют в свободном состоянии в форме электронного газа [16].
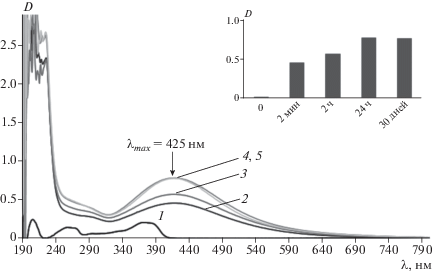
Спектрофотометрический анализ проб ОМР наночастиц серебра (ω = 5.0), отобранных в процессе синтеза, показал, что уже на первом этапе в спектре появляется полоса поглощения вблизи λ ~ 425 нм (рис. 1), отвечающая за присутствие в растворе металлических наночастиц серебра [17]. Последующее увеличение интенсивности поглощения в максимуме полосы во времени связано с продолжением процесса восстановления ионов и увеличением числа наночастиц. После остановки роста ОП можно говорить о стабильности НЧ (вставка на рис. 1)в течение некоторого времени.
Рис. 1.
Спектры ОП кверцетина (1) и ОМР наночастиц Ag (ω = 5.0) сразу после введения водного раствора 0.3 M AgNO3 в раствор 150 мкМ Qr/0.15 М АОТ/изооктан (2) и через 2 ч (3), 24 ч (4), 30 дней (5). На вставке D = f(Δt) при λmax = 425 нм.
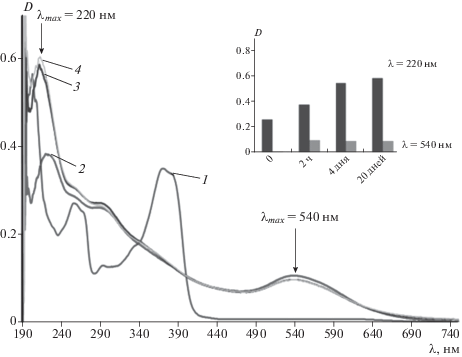
Cпектры ОП наночастиц золота (ω = 5.0), полученные химическим методом восстановления и зарегистрированные в разные промежутки времени, представлены на рис. 2. Спектр 1 – спектр ОП исходного раствора 150 мкМ Qr/0.15 М АОТ/изооктан, состоящий из двух полос (λ1 ~ 265 нм и λ2 ~ 374 нм). При первом измерении, сразу после введения раствора соли в раствор АОТ/изооктан спектр 2 имеет полосу, характерную для НЧ золота (λmax = 540 нм). Важно обратить внимание на ОП при длине волны 220 нм: этот максимум мы можем отнести к НЧ золота более мелкого размера. На вставке к рис. 2 показана зависимость оптической плотности D = f(Δt) при λmax = 220 и 535 нм. Можно сделать вывод, что полученные НЧ золота стабильны во времени.
Рис. 2.
Спектры ОП кверцетина (1) и ОМР наночастиц Au (ω = 5.0) сразу после введения водного раствора 0.048 M HAuCl4 в раствор 150 мкМ Qr/0.15 М Qr/АОТ/изооктан (2) и через 4 дня (3), 20 дней (4). На вставке D = f(Δt) при λmax = 220 и 540 нм.
Ультрадисперсные частицы родия и рутения проявляют уникальные каталитические свойства. Поэтому физикохимия наночастиц этих металлов привлекает особо пристальное внимание исследователей [18–20]. На рис. 3 представлена кинетика формирования НЧ родия (ω = 5.0) при концентрации ионов в водном пуле ОМ [Rh3+]w.p = 0.65 мМ. Спектр 1 – спектр ОП 150 мкМ исходного раствора Qr/0.15 М АОТ/изооктан состоит из двух полос: λmax = 256 и 373 нм. При первом измерении (спектр 2) можно видеть наложение полосы поглощения Qr (λmax = 373 нм) и увеличение интенсивности полосы поглощения в УФ-области с появлением полосы с λmax = 237 нм. Важно обратить внимание на то, что со временем происходит уменьшение полосы поглощения Qr (λmax = 373 нм) и одновременное увеличение ОП в области 410–500 нм. Возможно, это связано с промежуточным образованием металлокомплекса Qr c Rh [21].
Рис. 3.
Спектры ОП кверцетина (1) и ОМР наночастиц Rh (ω = 5.0) сразу после введения водного раствора 0.04 M RhCl3 в раствор 150 мкМ Qr/0.15 М АОТ/изооктан (2) и через 4 дня (3), 12 дней (4), 19 дней (5). На вставке – D = f(Δt) при λmax = 237 и 374 нм.
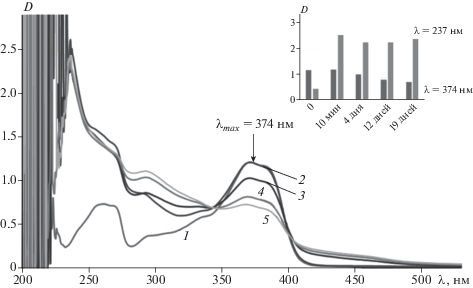
Падение ОП кверцетина (λmax = 373 нм) и его рост при λmax = 237 нм говорят об образовании НЧ родия (вставка на рис. 3). Далее происходит незначительное снижение ОП при λmax ~ 237 нм, что говорит о стабильности полученных НЧ родия в ОМР.
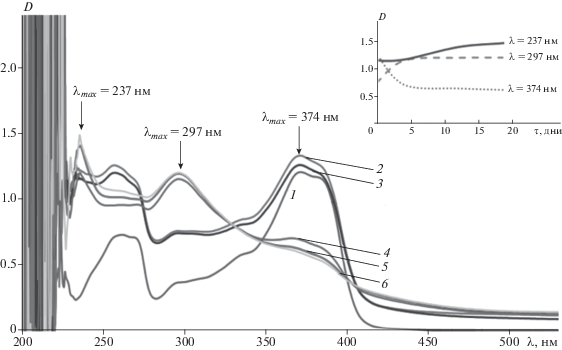
Кинетика формирования наночастиц Ru отличается от кинетики образования полученных ранее наночастиц Ag, Au и Rh. На рис. 4 представлена картина образования НЧ рутения в ОМР (ω = 5.0) в течение 19 дней. Спектр 1 (150 мкМ Qr/0.15 М АОТ/изооктан) спустя 30 мин после введения соли в раствор значительно увеличивается при λmax = 256 и 374 нм. Далее происходит снижение ОП характерных полос Qr при λmax = 256 и 373 нм и формирование полос НЧ рутения с λmax = 237 и 397 нм. На вставке к рис. 4 представлена зависимость D времени при λmax = 237, 297 и 374 нм. Снижение ОП полосы кверцетина (λmax = 373 нм), а также увеличение ОП при λmax = 237 и 297 нм в течение четырех дней и последующие незначительные изменения ОП в течение 19 дней говорят о стабильности полученных наночастиц (вставка к рис. 4).
Рис. 4.
Спектры ОП кверцетина (1) и ОМР наночастиц Ru (ω = 5.0) сразу после введения водного раствора 0.04 M RuOHCl3 в раствор 150 мкМ Qr/0.15 М АОТ/изооктан (2), и через 30 мин (3), 4 дня (4), 12 дней (5), 19 дней (6). На вставке D = f(Δt) при λmax = 237, 297 и 374 нм.
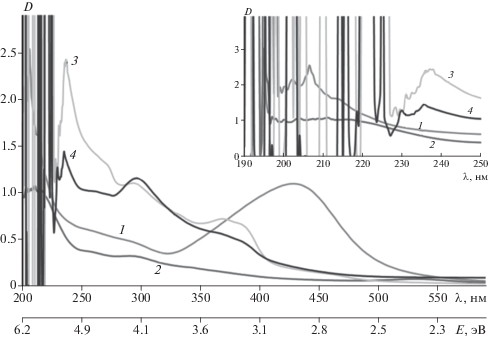
На рис. 5 представлены UV–VIS-спектры сравнения ОП. Поглощение ОМР наночастиц серебра имеет максимум при 420 нм (спектр 1). Спектр НЧ золота (спектр 2) представляет собой монотонно спадающее в длинноволновую область поглощение c максимумом малой интенсивности при длине волны 540 нм, полосу с максимумом при 220 нм и плечом при 300 нм. Наночастицы родия и рутения (спектры 4 и 5) имеют схожие спектры ОП: плечо при длине волны 374 нм и максимумы при 240 и 300 нм. Особое внимание следует уделить УФ-области спектра (вставка на рис. 5): в области длин волн от 190 до 230 нм можно видеть несколько неразрешенных максимумов для НЧ рутения и родия. Возможно, это связано с более мелким размером наночастиц и высокими значениями энергии (шкала энергий, эВ) полученных НЧ.
Рис. 5.
Сравнение спектров ОП обратномицеллярных растворов стабильных НЧ с коэффициентом солюбилизации ω = 5.0: 1 – НЧ Ag, 2 – НЧ Au, 3 – НЧ Rh, 4 – НЧ Ru. На вставке – спектры ОП ОМР стабильных НЧ в области от 190 до 250 нм.
Спектры ОП стабильных металлических НЧ золота и биметаллических НЧ Au/Ag, Au/Ru, Au/Rh (ω = 5.0 для всех образцов) представлены на рис. 6. Можно видеть, что характер спектров оптического поглощения ОМР металлических и биметаллических наночастиц различен.
Рис. 6.
Сравнение спектров ОП обратномицеллярных растворов стабильных НЧ с ω = 5.0: 1 – НЧ Au, 2 – НЧ Au/Ag, 3 – НЧ Au/Ru, 4 – НЧ Au/Rh. На вставке – спектры ОП ОМР наночастиц в области от 200 до 250 нм.
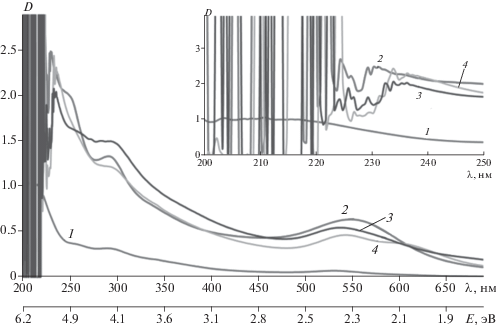
Как было показано ранее, при образовании металлических оболочек вокруг НЧ золота происходит смещение пика плазмонного резонанса в синюю область [22]. Как видно из спектров, в зависимости от рода добавки металла смещение пика плазмонного резонанса происходит в сторону больших длин волн. Положения пиков плазмонного резонанса ОМР наночастиц Au, Au/Ag, Au/Ru, Au/Rh показаны в табл. 1. Пики ОМР биметаллических НЧ Au/Ag, Au/Rh сместились в красную область, при этом спектр ОМР наночастиц Au/Rh имеет два максимума поглощения (548 и 608 нм), а пик электронного плазмонного резонанса НЧ Au/Ru не изменился. Важно отметить, что интенсивность ОП биметаллических наночастиц значительно выше по сравнению с интенсивностью ОП моночастиц.
ЗАКЛЮЧЕНИЕ
В настоящей работе “методом молекулярной сборки” были синтезированы в обратномицеллярных растворах НЧ золота, серебра, родия и рутения. Также были получены биметаллические НЧ типа “сплав”: Au/Ag, Au/Ru, Au/Rh. При измерении кинетики формирования биметаллических наночастиц было обнаружено, что НЧ стабильны и достигают своих окончательных концентраций через пять дней. Обнаружено существенное различие кинетики формирования монометаллических НЧ золота и серебра и биметаллических НЧ Au/Ag, Au/Ru, Au/Rh. Спектры электронного плазмонного резонанса биметаллических НЧ Au/Ag, Au/Ru, Au/Rh в отличие от монометаллических НЧ золота (при одинаковом соотношении содержания металла в растворе) имеют более интенсивные полосы поглощения в области длин волн 500–650 нм.
Список литературы
Кучерик А.О., Кутровская С.В., Осипов А.В. и др. // Изв. ЮФУ. Технич. науки. 2015. № 9. С. 101.
Шаповал Л.В., Бойцова Т.Б., Горбунова В.В. и др. // Журн. общ. химии. 2011. Т. 11. № 2. С. 190.
Сергеев М.О., Антонов А.Ю., Ревина А.А. и др. // Успехи в химии и хим. технологии. 2012. Т. 26. № 7. С. 33.
Чернышова К.Ф., Ревина А.А. // Конденсированные среды и межфазные границы. 2018. Т. 20. № 2. С. 296; https://doi.org/https://doi.org/10.17308/kcmf.2018.20/521
Туранская С.П., Четыркин А.Д., Дубровин И.В. и др. // Поверхность. 2011. Вып. 3(18). С. 343.
Еременко Н.К., Додонов В.Г., Захаров Ю.А. и др. // Вестн. Кемеровского ГУ. 2014. № 3(59). Т. 3. С. 189.
Ревина А.А. Препарат наноразмерных частиц металлов и способ его получения. Патент РФ № 2312741 // Б. И. 2007. № 35.
Robinson B.H., Khan-Lodhi A.N., Towey T. // Structure and Reactivity in Reverse Micelles / Ed. Pileni M.-P. Amsterdam–N.Y.–Toronto: Elsevier, 1989. P. 199.
Pileni M.P. // Langmuir. 1997. V. 13. P. 3266.
Heijnen C.G.M., Haenen G.R.M.M., Van Acker F.A.A., Van Der W.J.F., Bast A. // Toxicol. in Vitro. 2001. V. 15. № 1. P. 3.
Metodiewa D., Jaiswal A.K., Cenas N., Dickancaite E., Segura-Aguilar J. // Free Radical Biology and Medicine. 1999. V. 26. P. 107.
Чернышова К.Ф., Ревина А.А. // Наукоемкие технологии. 2017. Т. 18. № 1. С. 45.
Дементьева О.В., Мальковский А.В., Рудой В.М. // Коллоид. журн. 2008. Т. 70. № 5. С. 607.
Bohren C.F., Huffman D.R. // Absorption and Scattering of Light by Small Particles. New York: Willey, 1983.
Kerker M. The Scattering of Light and Other Electromagnetic Radiation. New York: Academic Press, 1969. P. 38.
Ершов Б.Г. // Ж. Рос. хим. об-ва им. Д.И. Менделеева. 2001. T. XLV. № 3. С. 20.
Kreibig U., Vollmer M. Optical Properties of Metal Clusters. Berlin: Springer, 1995.
Антонов А.Ю., Боева О.А., Ревина А.А., Нуртдинова К.Ф. // Перспективные материалы. Специальный выпуск (№ 10). 2011. С. 268.
Сергеев М.О., Боева О.А., Жаворонкова К.Н. // Успехи в химии и хим. технологии. 2014. Т. XXVIII. № 6. С. 122.
Shoair A.F., El-Bindary A.A., Abd El-Kader M.K. // J. Mol. Struct. 2017. № 1143. P. 100; https://doi.org/ https://doi.org/10.1016/j.molstruc.2017.03.109
Ревина А.А. // Физикохимия поверхности и защита материалов. 2009. Т. 45. № 1. С. 58.
Kuzmin P.G., Shafeev G.A., Simakin A.V., Voronov V.V. // Phys. Wave Phenomena. 2008. V. 16. № 4. P. 261.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика


