Химическая физика, 2020, T. 39, № 11, стр. 67-72
Сорбенты на основе краун-эфиров для очистки водных растворов от ионов металлов
В. Ф. Громов 1, Г. Н. Герасимов 1, М. И. Иким 1, *, Е. Ю. Спиридонова 1, 2, Л. И. Трахтенберг 1
1 Федеральный исследовательский центр химической физики им. Н.Н. Семёнова
Российской академии наук
Москва, Россия
2 Научно-исследовательский физико-химический институт им. Л.Я. Карпова
Москва, Россия
* E-mail: ikim1104@rambler.ru
Поступила в редакцию 24.01.2020
После доработки 24.01.2020
Принята к публикации 20.02.2020
Аннотация
Рассмотрена сорбция ионов меди и свинца сорбентами на основе эфиров 15-краун-5 и 18-краун-6 и их бензозамещенными аналогами, химически связанными с пористыми минеральными подложками, под действием гамма-излучения. Изучено влияние различных параметров на эффективность сорбции металлов из водных растворов. Показано соответствие между способностью сорбента поглощать ионы металла и размером полости краун-эфира, что обуславливает высокую селективность таких сорбентов. Действительно, сорбенты на основе эфира 18-краун-6 обладают значительно большей сорбционной способностью по отношению к свинцу, а эфир 15-краун-5 более эффективен для сорбции ионов меди. Изучено влияние мощности дозы облучения и времени выдержки сорбента в растворе соли на количество сорбированного металла.
ВВЕДЕНИЕ
Проблема очистки жидких отходов различных производств, приносящих огромный вред окружающей среде и здоровью населения, в последнее время приобрела статус приоритетной в ряде научных дисциплин и является предметом исследования различными научными коллективами. Наиболее опасными считаются отходы радиоактивных, радиохимических и гальванических производств, которые могут содержать тяжелые и радиоактивные металлы (не только в виде солей, но и в виде металлорганических соединений), а также примеси органических соединений. Применяемые в настоящее время методы утилизации жидких отходов, в частности электрохимические методы и методы химического осаждения, очень дороги, трудоемки и не могут быть эффективно использованы для обработки разбавленных растворов радиоактивных веществ, поскольку оставшиеся в растворе радиоактивные элементы даже в очень малых концентрациях могут оказывать серьезное влияние на здоровье человека [1–5].
Эффективный способ извлечения ионов металлов из водных растворов – применение краун-эфиров (КЭ). В этом случае катионы металлов внедряются в полиэфирный цикл КЭ и прочно связываются с ним, поскольку прочность связи катионов с полиэфирным циклом находится в пределах от 20 до 40 кДж/моль. По этому показателю КЭ являются более предпочтительными по сравнению с ионитами, содержащими различные функциональные группы, для которых прочность связи ионов металлов с функциональными группами ионитов составляет 8–12 кДж/моль. В то же время прочность связи ионов металлов с КЭ существенно ниже, чем в системе ионы металлов – хелатные ионообменные смолы, в которых она достигает 60–100 кДж/моль. Это, в свою очередь, обеспечивает более легкую регенерацию сорбента за счет извлечения из него сорбированного металла.
Применение краун-эфиров для извлечения катионов металлов из промышленных стоков описано в ряде работ [6–15]. Предпринимались также попытки создания твердых экстрагирующих систем [8, 9], состоящих из пористых пластин, на поверхность которых наносились краун-эфиры. Однако практическая ценность таких систем была ограничена вследствие вымывания КЭ из системы в процессе эксплуатации. Этого недостатка лишены разработанные нами твердые сорбенты, в которых краун-эфир химически связан с поверхностью твердой подложки [16, 17]. Так, сорбенты, полученные в результате радиационно-химической прививки эфиром 18-краун-6 или 15-краун-5 к поверхности полимерной матрицы, не теряли свою активность в течение длительного времени [17]. При выдерживании таких сорбентов в водном растворе, содержащем соли свинца или меди, соответственно, концентрация катионов в обработанном растворе уменьшалась на несколько порядков величины.
В данной работе изучена радиационно-химическая прививка КЭ к поверхности пористой минеральной пластины и исследован процесс извлечения металлов из водных растворов. Определено влияние природы краун-эфира и металла на сорбционную активность полученных сорбентов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве исходных веществ в процессе синтеза сорбентов в работе использовали коммерческие образцы эфиров 15-краун-5, 18-краун-6 и бензо- и дибензозамещенные этих эфиров, а также пластинки из гранулированного силикагеля, удельная поверхность которого, определенная по методу Брунауэра–Эммута–Тейлора, составляла около 50–60 м2/г. Для получения твердых сорбентов тщательно очищенные керамические пластинки (размером около 1 см2 и толщиной приблизительно 1 мм) помещали в раствор КЭ в тетрагидрофуране и эту суспензию подвергали воздействию γ-излучения от источника 60Со при различной мощности дозы (вплоть до 100 рад/с). Суммарная доза облучения составляла около 30 Мрад. По окончании облучения пластинки нагревали при пониженном давлении в течение определенного времени при температуре 150 °С для удаления растворителя.
Для оценки сорбционной активности полученных таким образом сорбентов их выдерживали в течение определенного времени в водном растворе соли металла. Содержание металлов в исследуемых растворах до и после воздействия сорбентов определяли методом рентгено-флуоресцентного анализа на рентгеновском спектрометре СРС-75 [18, 19]. В качестве источника первичного рентгеновского излучения применяли трубку с анодом из родия. Режимы работы трубки: V = 43 кВ, I = 35 мА. Для “монохроматизации” излучения рентгеновской трубки использовалась вторичная мишень из циркония. Анализ растворов, содержащих более 10–3–10–5 г/мл металла, проводили с использованием жидкостной кюветы с рабочими окнами из лавсановой пленки толщиной 10 мкм. Объем кюветы составлял 0.5 мл. При меньшей концентрации ионов металлов исследуемый раствор (50 мкл) наносили на тонкую лавсановую пленку (толщиной 10–20 мкм), натянутую на алюминиевое кольцо, и сушили при комнатной температуре в течение нескольких часов. В результате исследуемая проба представляла собой тонкослойный осадок диаметром около 5 мм, расположенный на поверхности лавсановой пленки в центре кольца.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Известно, что КЭ обладают высокой селективностью по отношению к катионам металлов и способны образовывать с ними стабильные комплексы. Для практического применения краун-эфиров в процессе извлечения ионов металлов необходимо обеспечить их связывание с соответствующей подложкой, обладающей высокой пористостью. Предварительные испытания показали, что исследованные нами подложки даже без нанесения на них КЭ обладают определенной сорбционной активностью и способны извлекать присутствующие в водном растворе катионы металлов, в частности медь. Однако сорбционная эффективность этих подложек недостаточно велика, что обуславливает необходимость нанесения на подложку специальных сорбирующих добавок, к числу которых, в первую очередь, относятся краун-эфиры. Пористую подложку выбирали таким образом, чтобы диаметр пор был несколько больше размера молекул краун-эфира. С учетом длин связей и валентных углов, а также ван-дер-ваальсовских радиусов атомов максимальный размер самой крупной молекулы КЭ, используемой в данной работе, а именно молекулы дибензо-18-краун-6-эфира составляет около 15 Ǻ. Поэтому в качестве пористой подложки для получения сорбентов использовали силикагель с диаметром пор около 40 Ǻ. В этом случае молекулы КЭ проникают в поры подложки и осаждаются на их поверхности. При этом из-за относительно малого размера пор формирование кристаллов КЭ в таких порах затруднено, так что краун-эфир присутствует в системе в молекулярной форме или в виде малых молекулярных кластеров. Это должно существенно облегчать взаимодействие КЭ с катионами металлов.
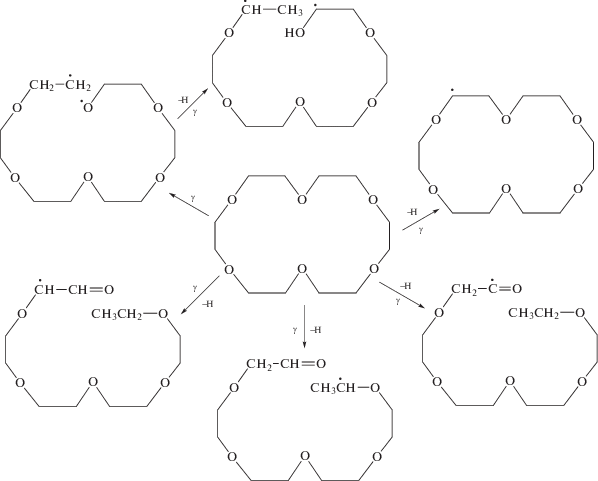
В данной работе для получения твердых сорбентов использовали радиационно-химическую прививку ряда краун-эфиров к поверхности гранулированного силикагеля. Гамма-облучение КЭ сопровождается его радиолизом и приводит к образованию свободных радикалов различной структуры (см. рис. 1). При взаимодействии этих радикалов с радикалами, возникающими при радиолизе подложки, происходит образование химической связи краун-эфира с подложкой. На образование такой связи указывают полученные нами данные ИК-спектроскопии (рис. 2): в спектре пластины из пористого силикагеля, облученной в присутствии эфира 18-краун-6, присутствуют новые полосы поглощения в области 3000 см–1, характеризующие молекулу этого КЭ.
Рис. 2.
ИК-спектр эфира 18-краун-6 (1) и стеклянной пластинки, к которой радиационно-химическим методом присоединен этот эфир (2).
Радиолиз краун-эфиров сопровождается одновременным образованием различных радикалов (рис. 1). Однако эффективными для извлечения ионов металлов из солевых растворов являются лишь сорбенты, получаемые при взаимодействии подложки с радикалами, образующимися при радиолизе КЭ в результате отрыва атома водорода от метиленовой группы КЭ и содержащими замкнутый полиэфирный цикл. На образование таких радикалов указывают данные ЭПР-спектроскопии. Действительно, анализ спектров ЭПР продуктов радиолиза показал, что среди этих продуктов присутствуют радикалы –O–CH–CH2–, образующиеся в результате реакции отрыва H-атома от молекулы КЭ, не приводящей к расщеплению полиэфирного кольца. Доля таких радикалов в продуктах радиолиза зависит от природы краун-эфира. Так, при радиолизе эфира 18-краун-6 или 15-краун-5 доля радикалов с замкнутым полиэфирным циклом составляет 10–11%. В то же время при радиолизе замещенных КЭ, таких, например, как бензо- или дибензозамещенные краун-эфиры, образование свободных радикалов может происходить за счет отрыва атома водорода не только от полиэфирного цикла, но и от бензильной группы. В результате содержание в продуктах радиолиза таких замещенных КЭ свободных радикалов с замкнутым полиэфирным циклом, существенно возрастает.
Используемые в данной работе исходные пористые подложки из силикагеля способны экстрагировать из водного раствора небольшое количество катионов металла. Гамма-облучение таких подложек в отсутствие краун-эфиров сопровождается незначительным уменьшением эффективности сорбции. В то же время облучение подложек в присутствии эфира 18-краун-6 или 15-краун-5 приводит к увеличению количества сорбированного металла на 1.5–2 порядка. Сорбционная емкость катиона металла, привитого к поверхности минеральной подложки краун-эфира, существенно зависит от природы извлекаемого из раствора металла. Так, после контакта с водным раствором хлорной меди (при концентрации соли в растворе 10–3 моль/л) интенсивность сигнала меди в РФ-спектре изменяется от 989 до 8113 отн. ед. при анализе соответственно исходной пластинки и пластинки с привитым 18-краун-6-эфиром. В еще большей степени радиационная прививка этого же сорбента влияет на сорбцию из водного раствора ионов свинца. Действительно, интенсивность сигнала свинца в рентгенофазовом спектре возрастает приблизительно в 30 раз при использовании в качестве сорбента пористой пластинки из силикагеля, к которой был привит 18-краун-6-эфир. Обратная картина наблюдается при использовании сорбентов на основе эфира 15-краун-5: в этом случае сорбент более эффективно поглощает катионы меди, чем катионы свинца. Этот результат свидетельствует о высокой селективности сорбентов на основе КЭ. Действительно, благодаря своей структуре используемый в этих опытах сорбент на основе 18-краун-6-эфира более эффективно захватывает катион свинца, диаметр которого (2.40 Å) в гораздо большей степени соответствует размеру полости этого КЭ (2.60 Å), чем катион меди (1.44 Å). В то же время, как следует из приведенных в табл. 1 данных, размер полости сорбента на основе 15-краун-5-эфира (1.70 Å) в большей степени соответствует размеру катиона меди (1.44 Å).
Таблица 1.
Соотношение размера сорбируемого катиона металла и диаметра полости краун-эфира
| Ион | Диаметр иона, Å | Краун-эфир | Диаметр полости, Å |
|---|---|---|---|
| Zn2+ | 1.48 | 15-краун-5 | 1.7–2.2 |
| Cu2+ | 1.44 | 15-краун-5 | 1.7–2.2 |
| Au+ | 2.74 | 18-краун-6 | 2.6–3.2 |
| Cd2+ | 1.94 | 15-краун-5 | 1.7–2.2 |
| Hg+ | 1.52 | 15-краун-5 | 1.7–2.2 |
| Hg2+ | 2.20 | 15-краун-5 18-краун-6 |
1.7–2.2 2.6–3.2 |
| Pb2+ | 2.40 | 18-краун-6 | 2.6–3.2 |
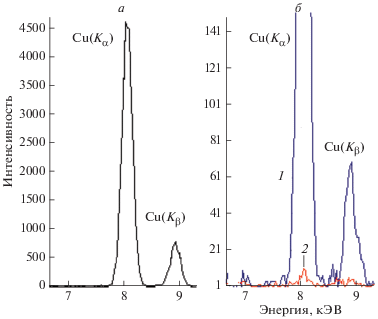
Концентрация катионов металлов, оставшихся в растворе после его обработки краун-эфирами, в значительной степени зависит от времени контакта с КЭ. На рис. 3 и 4 приведены рентгеновские спектры образцов, полученных после высушивания растворов, содержащих 10–3 г/мл катионов свинца и меди, до и после их контакта с эфирами 18-краун-6 и 15-краун-5 соответственно. Видно, что при контакте с сорбентами в течение 2 ч концентрация меди в растворе уменьшается приблизительно в 10 раз, а концентрация свинца – в 100 раз. При контакте растворов с сорбентами в течение 4 ч концентрация катионов меди и свинца уменьшается приблизительно на три порядка по сравнению с их концентрациями в исходных растворах.
Рис. 3.
Рентгеновские спектры образцов, полученных после высушивания растворов, содержащих 10–3 г/мл катионов свинца, до (а) и после (б) их контакта с 18-краун-6-эфиром в течение 2 (кривая 1) и 4 ч (кривая 2).
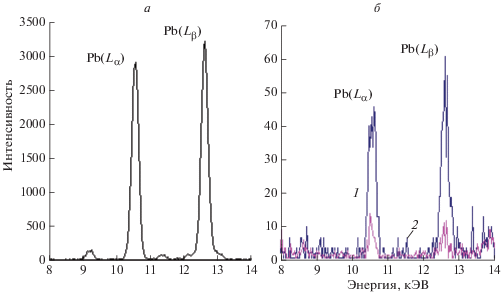
Рис. 4.
Рентгеновские спектры образцов, полученных после высушивания растворов, содержащих 10–3 г/мл катионов меди, до (а) и после (б) их контакта с 15-краун-5-эфиром в течение 2 (кривая 1) и 4 ч (кривая 2).
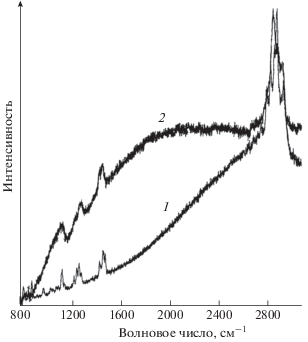
Повышение общей дозы облучения керамических пластинок в растворе КЭ от 1 до 31 Мрад также приводит к значительному увеличению количества КЭ, химически связанного с подложкой, и, как следствие, к росту активности сорбента. Как следует из данных, приведенных на рис. 5, при выдержке сорбента на основе 18-краун-6-эфира в растворе ацетата свинца в течение 90 мин количество сорбированного металла возрастает приблизительно в 3.5 и 5 раз в результате увеличения общей дозы облучения от 1 до 7 и 31 Мрад соответственно.
ЗАКЛЮЧЕНИЕ
Полученные в работе результаты убедительно показывают, что использование различных макроциклических краун-эфиров позволяет получить селективные сорбенты, способные эффективно извлекать катионы металлов из разбавленных водных растворов. Сорбционная активность краун-эфиров определяется соответствием диаметра его полости размеру сорбируемого катиона металла. При сорбции катиона свинца более эффективным является сорбент на основе 18-краун-6-эфира, в то время как для извлечения из раствора катиона меди необходимо использовать 15-краун-5-эфир. При выдерживании сорбентов в водных растворах солей концентрация извлекаемых металлов в таких сорбентах возрастает на несколько порядков величины по сравнению с их концентрацией в растворе.
Работа выполнена за счет субсидии, выделенной ФИЦ ХФ РАН на выполнение государственного задания по теме “Фундаментальные основы создания наноструктурированных систем нового поколения с уникальными эксплуатационными свойствами” (АААА-А18-118012390045-2), а также при финансовой поддержке Российским фондом фундаментальных исследований в рамках научного проекта № 18-29-25038_мк.
Список литературы
Grigor’ev E.I., Trakhtenberg L.I. Radiation-Chemical Processes in Solid State. USA: CRC Press, 1996.
Григорьев Е.И., Трахтенберг Л.И. // Рос. хим. журн. 1998. Т. 42. С. 101.
Wilmarth W.R., Lumetta G.I., Johnson M.E. et al. // Solvent Extr. Ion Exch. 2011. V. 29. № 1. P. 1.
Shou H., Connery K.E., Bartsch R.A. et al. // Ibid. 2013. V. 31. № 7. P. 683.
Burlakova E.B., Goloschapov A.N., Gurevich S.M. et al. // Eur. J. Oncol. 1998. V. 3. № 4. P. 367.
Хираока М. Краун-соединения. Свойства, применение. Пер. с англ. / Под ред. Эмануэля Н.М. М.: Мир, 1986.
Фёгтле Ф., Вебера Э. Химия комплексов “гость–хозяин”. Пер. с англ. М.: Мир, 1988.
Левкин А.В. // Тез. докл. IX Всесоюз. конф. по экстракции М.: Наука, 1991. С. 57.
Абакумов Н.И., Ремез В.П. // Тез. докл. II Всесоюз. конф. по теоретической и прикладной радиационной химии. М.: Наука, 1990. С. 87.
Titova Yu.A., Fedorova O.V., Ovchinnikova I.G. et al. // Macroheterocycles. 2014. V. 7. № 1. P. 23.
Popova N.N., Zhilov V. I., Demin S.V. et al. // J. Inorganic Chem. 2015. V. 60. № 6. P. 754.
Абрамов А.А. // Вестн. МГУ. 2000. Т. 41. № 1. С. 3.
Gokel G.W., Leevy W.M., Weber M.E. // Chem. Rev. 2004. V. 104. № 5. P. 2723.
Tsukanov A.V., Dubonosov A.D., Bren V.A. et al. // Chem. Heterocycl. Compd. 2008. V. 44. № 8. P. 899.
Трахтенберг Л.И., Щукин Е.Р., Громов В.Ф. и др. // Хим. физика. 2006. Т. 25. № 1. С.50
Григорьев Е.И., Нестеров С.В., Трахтенберг Л.И. Сорбент для очистки водных сред от ионов металлов и способ его получения. Патент РФ 2057146 // М., 1996.
Громов В.Ф., Герасимов Г.Н., Иким М.И. и др. // Хим. физика. 2020. Т. 39. № 5. С. 59.
Моровов А.П., Васин М.Г., Виноградов Ю.И. и др. // ВАНТ. Серия: Физика ядерных реакторов. Спец. Выпуск ТИЯС-XI. 1997. С. 18.
Vasin M.G., Ignatyev Yu.V., Lakhtikov A.E. et al. // X‑ray Spectrometry. 2007. V. 36. P. 270.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика