Химическая физика, 2020, T. 39, № 12, стр. 10-16
Структура и свойства кластеров золота с замещающими и присоединенными тиоловыми группами
Ю. А. Дьяков 1, *, В. Г. Яржемский 2, М. Г. Голубков 1
1 Федеральный исследовательский центр химической физики им. Н.Н. Семёнова
Российской академии наук
Москва, Россия
2 Институт общей и неорганической химии им. Н.С. Курнакова Российской академии наук
Москва, Россия
* E-mail: yuri_dyakov@mail.ru
Поступила в редакцию 07.05.2020
После доработки 07.05.2020
Принята к публикации 20.05.2020
Аннотация
Для кластеров Aun с определенным количеством атомов золота (с так называемыми “магическими числами” n = 18, 20, 32, 42, 72) ранее теоретически и экспериментально были получены симметричные полые структуры. Теоретический анализ электронного строения этих структур показал, что кластеры с данным количеством атомов переходных металлов образуют один общий псевдоатом с полностью заполненной внешней электронной оболочкой. В то же время экспериментальные данные указывают на то, что нанокластеры золота с лигандами, присоединенными к металлическому ядру тиоловыми терминальными группами, имеют объемную (не полую) структуру. В настоящей работе теоретически исследована структура кластеров и энергия присоединения группы SH к клеточным и объемным структурам Aun, при этом число атомов золота n варьировалось вблизи значений 18 и 32. Установлено, что присоединение нескольких групп SH к структурам Aun переводит их из клеточных в объемные.
1. ВВЕДЕНИЕ
Наночастицы золота обладают широким набором функциональных свойств, с которыми связывают перспективы их применения в катализе [1, 2] и в наноэлектронике, например в качестве центров самоорганизации функциональных слоев с тиоловой терминальной группой [3, 4]. Кластеры ${\text{A}}{{{\text{u}}}_{n}}{\text{ (}}n < {\text{100)}}$ являются идеальными флуоресцентными метками в биологии и в исследованиях окружающей среды [5, 6]. Согласно теоретическим расчетам небольшие энергетически стабильные кластеры Aun имеют плоскую форму [7, 8]. Небольшие отступления от этого правила были получены теоретически для Au6 [7] и Au8 [9]. Наиболее стабильные кластеры Aun при $n \leqslant 12$ являются плоскими [10, 11], а при n > 14 начинается переход к объемным структурам.
Расчеты и исследования методом фотоэлектронной спектроскопии позволили установить, что кластеры ${\text{Au}}_{n}^{ - }$ (n = 21–25) имеют структуры из соединенных плоскостей и полых трубок [12]. Кластеры Au32, Au42 и Au72 имеют клеточную структуру симметрии Ih, в то время как у кластеров Au20 и Au18 структура напоминает полый тетраэдр [13]. Эти значения близки к длине связи в металлическом золоте (2.88 Å). Симметричные клеточные структуры, как правило, имеют число электронов N = 2(k + 1)2, где k – целое положительное число, бóльшее единицы [13, 14], что соответствует заполненной внешней атомной электронной оболочке.
Основными структурными единицами в кластерах золота являются треугольники Au3 и тетраэдры Au4 [15]. Заполненная электронная оболочка кластера может быть получена также путем замены атома Au на d-элемент с другим числом электронов. Например, теоретически был предсказан 18-электронный икосаэдрический кластер WAu12 [16], а позже кластеры Au12W и Au12Mo были обнаружены экспериментально [17]. Такая 18-электронная конфигурация соответствует заполненной атомной оболочке $3{{s}^{2}}3{{p}^{6}}3{{d}^{{10}}}$ или икосаэдрической оболочке $a_{g}^{2}t_{{1u}}^{6}g_{g}^{{10}}$. Заполненная 18-электронная оболочка может быть получена также путем замены W на Ta, Hf, Re или Os при одновременном изменении заряда кластера [18–20]. Исследовались также свойства биметаллических частиц на основе золота [21–23] и взаимодействие кластеров золота с графитом [24, 25].
Многие функциональные лиганды [26] и самоорганизующиеся монослои [4] присоединены к кластерам золота тиоловой терминальной группой. Поэтому исследование взаимодействий кластеров золота с данной группой представляет собой актуальную задачу.
Экспериментально полученные структуры кластеров AunLx (где L обозначает акцепторный лиганд) имеют симметричное ядро, окруженное менее симметричной оболочкой, непосредственно взаимодействующей с лигандами [2, 27–29]. Например, нанокластер ${{\left[ {{\text{A}}{{{\text{u}}}_{{38}}}{{{\text{L}}}_{{20}}}{{{\left( {P{{h}_{3}}P} \right)}}_{4}}} \right]}^{{2 + }}}$ имеет гранецентрированное кубическое ядро Au34 [2].
Кластер Au102L44 состоит из центрального ядра Au49, двух аксиальных групп Au20 и одной экваториальной группы Au13 [27]. Ядро Au15 кластера Au23L6 представляет собой центрированный кубооктаэдр с двумя атомами на противоположных гранях [28]. Кластер Au68L32 [29] состоит из центрированного кубооктаэдра, окруженного оболочкой Au24.
Таким образом, наблюдается различие структур золотых кластеров и аналогичных кластеров с присоединенными тиоловыми лигандами. Наиболее стабильные кластеры Aun имеют полую клеточную структуру, в то время как кластеры Aun c лигандами имеют симметричное объемное ядро, окруженное менее симметричной оболочкой, к которой и присоединяюся лигады. Для понимания функциональных свойств более крупных наночастиц переходных металлов, особенно окруженных различными химически активными биополимерными оболочками, требуется изучение электронного строения и структуры данных кластеров.
В настоящей работе теоретически исследованы нейтральные 18-электронные кластеры, состоящие из атомов золота, в которых один атом золота заменялся на тиоловую группу SH, либо, наоборот, к 18- или 32-электронному металлическому ядру присоединялись дополнительные тиоловые группы. Установлены особенности электронного строения полученных структур и исследованы особенности взаимодействия данных металлических кластеров с тиоловыми функциональными группами.
2. МЕТОДИКА РАСЧЕТОВ
Расчеты проводились с использованием квантовохимического метода функционала плотности B3LYP с псевдорелятивистским базисом lanl2dz для 5d-элементов (в данном случае золота) и базисом 6-31G(d) для других химических элементов. Структура кластера оптимизировалась до нахождения локального минимума энергии. При этом проверялось отсутствие мнимых частот в спектре внутримолекулярных колебаний. В дальнейшем анализировались значения энергии в этих локальных минимумах, а также общая структура полученных кластеров и длины межатомных связей. Квантовохимические расчеты выполнены с помощью пакета программ GAUSSIAN 09 [30]. Энергия ΔE присоединения групп SH к кластеру золота оценивалась по формуле
где x – число присоединяемых SH-групп.3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для исследования процессов, происходящих в энергетически стабильных полых симметричных кластерах золота при присоединении к ним лигандов, а также при удалении одного атома золота или его замещении другим атомом, в качестве исходных металлических кластеров использовались объемные структуры Au18 и Au32. В качестве лигандов были взяты функциональные группы SH. В реальных молекулах, изучаемых в экспериментах, вместо атома водорода обычно присутствуют различные линейные биополимерные фрагменты.
Кластеры Au18 имеют две основные полые симметричные структуры: наиболее энергетически выгодную конусообразную (в данной работе на всех рисунках и в табл. 1 обозначена как Au18-1) и квазиоктаэдрическую, имеющую энергию на 19.6 ккал/моль выше основной (обозначена как Au18-2). Энергии на всех рисунках для кластеров как с замещенными атомами золота, так и с присоединенными SH-группами приведены относительно наименьшего по энергии кластера с данной химической формулой. В табл. 1 приведены длины связей Au–SH и энергии присоединения тиоловой группы к кластеру Au18 и замещения одного атома золота на тиоловую группу в пересчете на одну группу SH. В случае реакции присоединения энергии отсчитываются от кластера Au18-1. Замещение одного атома золота фактически эквивалентно присоединению тиоловой группы к кластеру Au17. В данном случае в качестве структуры Au17 с минимальной энергией мы использовали конфигурацию, приведенную в работе [31] с геометрией и энергией, пересчитанной нами с помощью метода B3LYP/Lanl2dz.
Таблица 1.
Длины связей R(Au–SH) и средние значения энергий ΔESH присоединения SH-групп к клеточным кластерам Au18 и Au32 в пересчете на одну SH-группу
| Кластер | Химическая формула | ΔESH, эВ | R(Au–SH), Å |
|---|---|---|---|
| Au18-1 – SH-1 | Au17(SH) | 0.380 | 2.49, 2.48* |
| Au18-1 – SH-2 | Au17(SH) | 0.113 | 2.45, 2.50 |
| Au18-2 – SH-1 | Au17(SH) | 0.250 | 2.50, 2.50 |
| Au18-2 – SH-2 | Au17(SH) | 0.143 | 2.49, 2.50 |
| Au18-1 + 2SH-1 | Au18(SH)2 | 0.467 | 2.49, 2.51; 2.49, 2.51** |
| Au18-1 + 2SH-2 | Au18(SH)2 | 0.443 | 2.51, 2.40; 2.51, 2.40 |
| Au18-1 + 2SH-3 | Au18(SH)2 | 0.206 | 2.45, 2.46; 2.50, 2.53 |
| Au18-1 + 2SH-4 | Au18(SH)2 | 0.365 | 2.47, 2.49; 2.45, 2.45 |
| Au18-2 + 2SH-1 | Au18(SH)2 | 0.301 | 2.40, 2.49; 2.41, 2.50 |
| Au18-2 + 2SH-2 | Au18(SH)2 | 0.103 | 2.43, 2.48; 2.49, 2.51 |
| Au18-2 + 2SH-3 | Au18(SH)2 | 0.532 | 2.41, 2.49; 2.39, 2.46 |
| Au18-2 + 2SH-4 | Au18(SH)2 | 0.186 | 2.48, 2.48; 2.43, 2.49 |
| Au32 + 2SH | Au32 (SH)2 | 0.310 | 2.49, 2.50 |
| Au32 + 4SH | Au32 (SH)4 | 0.201 | 2.49, 2.51; 2.49, 2.51; 2.49, 2.51 |
| Au32 + 6SH | Au32 (SH)6 | 0.219 | 2.49, 2.52; 2.49, 2.54; 2.51, 2.52; 2.47, 2.48; 2.46, 2.49; 2.45, 2.50 |
| Au32 + 8SH | Au32 (SH)8 | 0.227 | 2.49, 2.51; 2.42, 2.51; 2.44, 2.48; 2.44, 2.48; 2.45, 2.49; 2.44, 2.51; 2.43, 2.50; 2.45, 2.47 |
| Au32 + 10SH | Au32 (SH)10 | 0.536 | 2.40, 2.49; 2.48, 2.49; 2.41, 2.46; 2.40, 2.48; 2.40, 2.48; 2.45, 2.46; 2.45, 2.50; 2.46, 2.51; 2.41, 2.48; 2.40, 2.47 |
На рис. 1 показаны результаты замещения одного атома золота в кластерах Au18-1 и Au18-2 на одну тиоловую группу, а также удаления одного атома золота с одновременным добавлением электрона для того, чтобы сохранить 18-электронную внешнюю электронную оболочку кластера в соответствии с теорией “магических чисел” электронов. Хорошо видно, что при замещении атома золота, находящегося в вершинах октаэдра и конуса и имеющего наименьшее число связей с соседними атомами, структура кластера меняется незначительно, тогда как при замещении атомов, находящихся на гранях, происходит существенное изменение геометрии. Это связано с тем, что тиоловая группа может образовать ковалентные связи только с двумя атомами золота, тогда как атом золота в кластере образует от четырех до шести связей.
Рис. 1.
Структура кластеров Au18, в которых один атом золота заменен на SH-группу, а также структура отрицательно заряженного кластера ${\text{Au}}_{{17}}^{ - }$, полученного из Au18-1 путем удаления одного атома золота с вершины “конуса”. Кластеры Au18-1 – SH-1 и Au18-1 – SH-2 получены из структуры Au18-1, а кластеры Au18 – 2-SH-1 и Au18-2 – SH-2 – из структуры Au18-2. Жирные цифры под изображениями структур обозначают энергии (в ккал/моль) данных кластеров относительно энергетически самого выгодного кластера с данной химической формулой.

В случае удаления одного атома золота с вершины конуса с одновременным добавлением одного электрона структура остается полой и симметричной, но конфигурация атомов меняется. Это говорит о том, что даже при сохранении числа электронов на внешней электронной оболочке неизменным данная операция меняет структуру кластера.
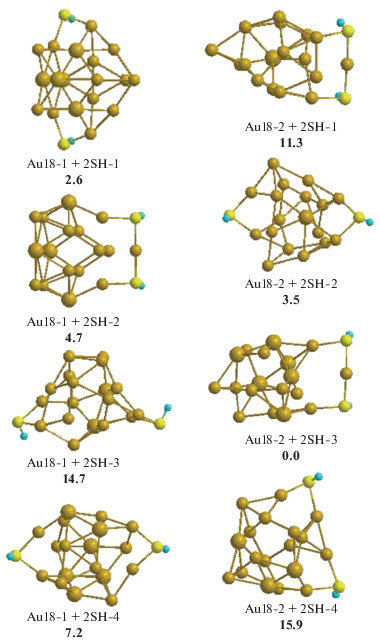
На рис. 2 приведены несколько структур Au18 с двумя присоединенными тиоловыми группами. Видно, что при симметричном присоединении к вершинам кластера Au18-1 структура остается полой и симметричной, тогда как остальные кластеры полностью потеряли свою симметричную форму и стали объемными. При этом хорошо видно, что тиоловая группа образует с атомами золота два вида связей – так называемые “мостики” и “скрепки” (струкуры Au18-1 + SH-2, Au18-2 + SH-1 и Au18-2 + + SH-3), описанные ранее в работе [32]. “Скрепки” представляют собой линейные структуры типа SH–Au–SH и отличаются короткими длинами связей Au–SH, что видно из табл. 1.
Рис. 2.
Структура кластеров Au18, к которым присоединены по две SH-группы. Кластеры Au18-1 + 2SH-1 и Au18-1 + + 2SH-2 получены из структуры Au18-1, а кластеры Au18-2 + 2SH-1 и Au18-2 + 2SH-2 – из структуры Au18-2. Жирные цифры под изображениями структур имеют тот же смысл, что и на рис. 1.
На рис. 3 приведены кластеры Au32(SH)n, где n = 2, 4, 6, 8 и 10. Видно, что с увеличением числа присоединенных SH-групп структура кластера полностью разрушается и образуется центральное квазикристаллическое ядро, к которому хаотично присоединены фрагменты с тиоловыми группами, как было экспериментально обнаружено ранее в различных кластерах золота [32]. При этом энергия присоединения SH-группы при разрушении симметричной клеточной структуры с увеличением количества присоединяемых тиоловых групп сначала падает, однако при образовании центрального квазикристаллического ядра снова увеличивается.
4. ЗАКЛЮЧЕНИЕ
Анализ результатов, полученных при замещении атома золота в клеточных (полых и, как правило, симметричных) кластерах тиоловой группой либо при присоединении такой группы к кластеру, говорит о том, что одновременно имеют место два разнонаправленных процесса. Первый проявляется в перераспределении электронной плотности между SH-группой и кластером, что в случае, если число атомов золота близко к “магическому числу” (см. ссылки, приведенные выше), может привести к стабилизации клеточной структуры, а это было бы невозможно при реально имеющемся в кластере числе атомов. С другой стороны, атом серы тиоловой группы может образовывать не больше двух валентных связей с соседними атомами, тогда как атомы золота могут иметь до шести ковалентных связей с соседними атомами. В результате внедрение или добавление тиоловой группы нарушает исходную структуру, что приводит либо к нарушению симметрии, либо к полному схлопыванию исходной полой клеточной структуры в объемную. Однако этот процесс сильно зависит от конкретного положения, в которое была помещена SH-группа.
В результате можно сделать однозначный вывод: фактор уменьшения возможного количества ковалентных связей атома серы по сравнению с их количеством у атомов золота является определяющим. В естественных условиях, т.е. при присоединении к полым (а тем более симметричным) кластерам золота множества лигандов, симметричные и псевдосимметричные клеточные структуры разрушаются, что делает невозможным существование в биологически активных средах таких конструкций. В естественных условиях исходная структура распадается на центральное объемное ядро и множество боковых фрагментов, как было обнаружено в недавних экспериментально-теоретических исследованиях [32]. Боковые фрагменты в большей части имеют форму тиоловых “мостиков” и линейных “скрепок” вида SH–Au–SH с прочными межатомными связями. Количество таких “мостиков” и “скрепок” растет с увеличением отношения тиоловых групп к числу атомов золота. Количество “скрепок” можно оценить по относительной доле коротких (порядка 2.4 Å) связей в общем количестве связей S–Au.
Работа выполнена в рамках государственного задания ИОНХ РАН в области фундаментальных научных исследований.
Список литературы
Pakrieva E., Kolobova E., Kotolevich Y. et al. // Nanomaterials. 2020. V. 10. № 5. P. 880.
Wan X.K., Wang J.Q., Nan Z.A. et al. // Sci. Adv. 2017. V. 3. № 10. e1701823.
Yarzhemsky V.G., Battocchio C. // Russ. J. Inorg. Chem. 2011. V. 56. № 14. P. 2147.
Battocchio C., Fratoddi I., Venditti I. et al. // Chem. Phys. 2011. V. 379. P. 92.
Cui M., Zhao Y., Song Q. // Trend. Anal. Chem. 2014. V. 57. P. 73.
Kaur N., Aditya R.N., Singh A. et al. // Nanoscale Res. Lett. 2018. V. 13. 302.
Xiong X.G., Xu W.H., Li J. et al. // Intern J. Mass Spectr. 2013. V. 354–355. P. 15.
Яржемский В.Г. Норов Ю.В., Мурашов С.В. и др. // Неорган. материалы. 2010. Т. 46. № 9. С. 1034.
Serapian S.A., Bearpark M.J., Bresme F. // Nanoscale. 2013. V 5. № 14. P. 6445.
Häkkinen H., Yoon B., Landman U. et al. // J. Phys. Chem. A. 2003. V. 107. № 32. P. 6168.
Mukhamedzyanova D.F., Ratmanova N.K., Pichugina D.A. et al. // J. Phys. Chem. C. 2012. V. 116. P. 11507.
Khetrapal N.S., Bulusu S.S., Zeng X.C. // J. Phys. Chem. A. 2017. V. 121. № 12. P. 2466.
Karttunen A, Linnolahti M, Pakkanen T.A. et al. // Chem. Commun. 2008. № 4. P. 465.
Fernández E.M., Soler J.M., Balbás L.C. // Phys. Rev. B. 2006. V. 73. 235433.
Xu W.W., Zhu B., Zeng X.C. et al. // Nature Commun. 2016. V. 7. 13574.
Pyykko P, Runeberg N. // Angew. Chem. Intern. Ed. 2002. V. 41. № 12. P. 2174.
Li X., Kiran B., Li J., et al. // Ibid. 2002. V. 41. № 24. P. 4786.
Яржемский В.Г., Изотов А.Д., Казарян М.А. и др. // Докл. АН. 2015. Т. 462. № 1. С.55.
Яржемский В.Г., Казарян М.А., Дьяков Ю.А. и др. // ЖНХ. 2017. Т. 62. № 1. С. 69.
Яржемский В.Г., Дьяков Ю.А., Изотов А.Д. и др. // ЖНХ. 2019. Т. 64. № 10. С. 1057.
Чернышова К.Ф., Ревина А.А. // Хим. физика. 2019. Т. 38. № 5. С. 17.
Дохликова Н.В., Гришин М.В., Сарвадий С.Ю. и др. // Хим. физика. 2019. Т. 38. № 6. С. 77.
Гатин А.К., Гришин М.В., Сарвадий С.Ю. и др. // Хим. физика. 2018. № 3. С. 48.
Гатин А.К., Гришин М.В., Колченко Н.Н. и др. // Хим. физика. 2017. Т. 36. № 3. С. 81.
Гришин М.В., Гатин А.К., Дохликова Н.В. и др. // Хим. физика. 2019. Т. 38. № 1. С. 3.
Пичугина Д.А., Кузьменко Н.Е., Шестаков А.Ф. // Успехи химии. 2015. Т. 84. № 11. С. 1114.
Jadzinsky P.D., Calero G., Ackerson C.J. et al. // Science. 2007. V 318. P. 430.
Das A., Li T., Nobusada K. et al. // J. Amer. Chem. Soc. 2013. V. 135. P. 18264.
Azubel M., Koivisto J., Malola S. et al. // Science. 2014. V. 345. № 6199. P. 909.
Frisch M.J., Trucks G.W., Schlegel H.B., Scuseria G.E., Robb M.A., Cheeseman J.R., Scalmani G., Barone V., Petersson G.A., Nakatsuji H., Li X., Caricato M., Marenich A.V., Bloino J., Janesko B.G., Gomperts R., Mennucci B., Hratchian H.P., Ortiz J.V., Izmaylov, A.F., Sonnenberg J.L., Williams-Young D., Ding F., Lipparini F., Egidi F., Goings J., Peng B., Petrone A., Henderson T., Ranasinghe D., Zakrzewski V.G., Gao J., Rega N., Zheng G., Liang W., Hada M., Ehara M., Toyota K., Fukuda R., Hasegawa J., Ishida M., Nakajima T., Honda Y., Kitao O., Nakai H., Vreven T., Throssell K., Montgomery J.A.,Jr., Peralta J.E., Ogliaro F., Bearpark M.J., Heyd J.J., Brothers E.N., Kudin K.N., Staroverov V.N., Keith T.A., Kobayashi R., Normand J., Raghavachari K., Rendell A.P., Burant J.C., Iyengar S.S., Tomasi J., Cossi M., Millam J.M., Klene M., Adamo C., Cammi R., Ochterski J.W., Martin R.L., Morokuma K., Farkas O., Foresman J.B., Fox D.J., Gaussian, Inc., Wallingford CT. Gaussian 09. Rev. A. 02. Wallingford CT: Gaussian, Inc., 2009.
Yan L., Cheng L., Yang J. // J. Phys. Chem. C. 2015. V. 119. P. 23274.
Xu W.W., Zeng X.C., Gao Y. // Nanoscale. 2018. V. 10. P. 9476.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика



