Химическая физика, 2020, T. 39, № 8, стр. 64-70
Распределение серы в продуктах газификации автомобильных покрышек
В. М. Кислов 1, *, Ю. Ю. Цветкова 1, С. В. Глазов 1, М. В. Цветков 1, Е. Н. Пилипенко 1, М. В. Салганская 1, 2
1 Институт проблем химической физики Российской академии наук
Черноголовка, Россия
2 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
* E-mail: vmkislov@icp.ac.ru
Поступила в редакцию 09.01.2020
После доработки 09.01.2020
Принята к публикации 20.02.2020
Аннотация
Проведено исследование газификации изношенных шин в режиме фильтрационного горения с использованием как химически инертных, так и способных поглощать серу кальцийсодержащих добавок. Установлено, что при газификации составов с инертной добавкой в золу, смолу и газообразные продукты переходит соответственно 28%, 29% и 43% серы, содержащейся в исходном материале. Введение в качестве добавки крошки мрамора увеличивает долю серы, переходящей в золу, в 1.5 раза и снижает выход пиролизных смол по сравнению с инертной добавкой. В этом случае распределение серы между твердыми, жидкими и газообразными продуктами газификации выглядит следующим образом: 40%, 26% и 34% соответственно.
ВВЕДЕНИЕ
Сера – один из проблемных загрязнителей, образующихся в процессах горения, поскольку она входит в состав многих твердых топлив, а также горючих техногенных отходов. Одними из таких распространенных крупномасштабных серосодержащих техногенных отходов являются использованные автомобильные покрышки.
В России ежегодное количество изымаемых из обращения шин оценивают приблизительно в 50 млн шт. Учитывая устойчивый рост автомобильного парка в России, следует ожидать и соответствующего увеличения количества изношенных покрышек. Подавляющая часть использованных автомобильных шин в России традиционно оказывается на полигонах для захоронения мусора и различных стихийных свалках, и лишь небольшое количество поступает в переработку. Накопление миллионов изношенных автомобильных шин представляет значительную экологическую проблему. Автомобильные покрышки, а также материалы, из которых они изготовлены, относятся к IV классу опасности (малоопасные) и не представляют серьезной угрозы для здоровья человека, но они представляют весьма существенную пожарную опасность. При сгорании этих материалов на открытом воздухе из-за недостатка окислителя, поступающего в режиме естественной диффузии, в атмосферу выбрасываются продукты неполного сгорания. Помимо сажи в окружающую среду попадают бензопирен, диоксины, фураны, полиароматические углеводороды, полихлорированные бифенилы и другие вещества, имеющие высокие классы опасности (I и II).
Благодаря высокой калорийности резины и ее неспособности впитывать влагу одним из привлекательных способов утилизации покрышек является их сжигание с утилизацией выделяющегося тепла при условии обеспечения экологической чистоты выбросов. Использование старых автомобильных шин в качестве топлива далеко не новое решение: в США еще в 2001 году таким способом утилизировали 41% всех вышедших из употребления шин, а в Германии – 50% [1]. Применяемые современные технологии позволяют снизить содержание сажи, диоксинов и других вредных полиароматических углеводородов в продуктах сгорания до минимальных значений [2], однако они не могут решить проблемы, связанные с наличием в резине серы, которая так или иначе присутствует в выбросах.
Основными газообразными серосодержащими продуктами при сжигании автомобильных шин являются сероводород (H2S) и диоксид серы (SO2) [3]. Для предотвращения негативного влияния соединений серы на окружающую среду разработаны различные способы десульфурации дымовых газов [4, 5]. Основным способом очистки дымовых газов является поглощение серосодержащих соединений различными сорбентами. Исходя из физико-химической сути протекающих процессов, методы очистки обычно делят на жидкофазные (мокрые), смешанные (полусухие) и газофазные (сухие) [6–8]. Однако все эти методы высокозатратны, поэтому до настоящего времени ведутся работы по совершенствованию имеющихся и разработке новых методов десульфурации.
Проведенные ранее работы по утилизации и энергетическому использованию бытовых отходов в режиме фильтрационного горения показали, что одна из существенных проблем горения резиновых изделий – выделение большого количества (до 50 мас.%) жидких продуктов пиролиза, которые могут накапливаться и препятствовать равномерной фильтрации газового потока [9]. Одним из способов решения этой проблемы, успешно примененным нами ранее для сжигания таких проблемных отходов, как вязкие углеводородные жидкости, является использование кускового твердого материала, слой которого образует пористый каркас из частиц, обеспечивающий равномерную газопроницаемость среды при фильтрационном горении [10].
Для создания пористого каркаса может быть использован как полностью химически инертный, так и активный материал (реагент, катализатор). При газификации в фильтрационном режиме пористый каркас выполняет также роль теплоносителя, способствующего рекуперации тепла от продуктов к исходным реагентам. В этом случае противоток твердой фазы и газа предоставляет принципиальную возможность нейтрализовать кислые газы посредством добавки в перерабатываемый материал щелочных или щелочноземельных сорбентов [11, 12]. Образующиеся в результате нейтрализации серосодержащих газов соединения должны оставаться в твердых продуктах сгорания и не должны представлять экологической опасности.
Цели настоящей работы – изучение распределения соединений серы при газификации автомобильных покрышек в фильтрационном режиме и исследование возможности нейтрализации серы путем добавок кальцийсодержащих сорбентов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Используемые материалы
В качестве образца была использована автомобильная покрышка марки NEXEN ROADIAN 541 235/75 R16, изготовленная в декабре 2011 года. Для проведения экспериментов в небольшом лабораторном реакторе с покрышки предварительно был снят металлокорд и она была разрезана на квадратные кусочки размером ~10 мм. Элементный состав материала шин следующий: С – 83.6%, H – 7.5%, S – 1.6%, N – 0.32%, O (по разнице) – 2.1%, зола – 4.9%. Химический состав золы шин после выгорания органической части и углерода в пересчете на оксиды таков: SiO2 – 3.92%, Al2O3 – 1.30%, CaO – 29.02%, MgO – 1.75%, SO3 – 36.90%, TiO2 – 5.20%, ZnO – 21.41%, остальное – 0.49%.
В качестве твердого материала, который выполняет роль пористого каркаса и теплоносителя, использовали технический сапфир (Al2O3) с размером частиц 7–10 мм либо крошку мрамора (размер частиц – 3–5 мм). Анализ химического состава используемого мрамора показал присутствие в нем карбоната кальция (CaCO3) практически без посторонних примесей. Для приготовления поглощающего раствора барботажных колб использовали Na2CO3 (ГОСТ 83-79, ХЧ).
Методика химических анализов
Количественный элементный анализ шин, твердых и жидких продуктов, полученных при пиролизе шин, и образцов шин, прошедших термическую обработку в электропечи, проводили методом сжигания в потоке кислорода на элементном CHNS/O-анализаторе “Vario MICRO cube”.
Химический состав зольного остатка, а также мрамора, используемого в экспериментах, получали посредством анализа на сканирующем автоэмиссионном электронном микроскопе Zeiss LEO SUPRA 25. Зольный остаток шин предварительно готовили по ГОСТ Р 55661-2013.
Анализ газообразных продуктов осуществляли с помощью хроматографа Хроматэк Кристалл-5000.2. Серу в газообразных продуктах определяли по разности из массового баланса.
Окисление образцов в печи
Эксперименты по сгоранию частиц автомобильных покрышек проводили в лабораторной электропечи SNOL 6.7/1300. Образцы массой 6–7 г одновременно размещали внутри печи на четырех кварцевых лодочках. Режим нагрева состоял из четырех этапов: 1) нагрев в течение 6 мин от комнатной температуры до 500 °С; 2) нагрев в течение 9 мин от 500 до 700 °С; 3) нагрев в течение 2 мин от 700 до 800 °С; 4) выдержка в течение 2 мин при 800 °С. После каждого этапа один образец вынимали из печи и остужали на воздухе. Выбранный режим нагрева в печи был близок к условиям нагрева частиц шин в экспериментах по газификации.
Методика термодинамических расчетов
Для выявления присутствия возможных соединений серы в газообразных и твердых продуктах газификации, а также оценки воздействия кальцийсодержащих сорбентов на состав продуктов был проведен термодинамический анализ химической системы с помощью программы расчета равновесного состояния многокомпонентных гетерогенных систем [13]. В расчетах полагали, что исходная система состоит из следующих элементов: С + Н + + О + Ca + S + Zn.
Исходя из данных элементного анализа автомобильных шин для описания состава принимали следующую брутто-формулу: С14Н15S0.1Zn0.026. В условиях волны фильтрационного горения материал сначала подвергается нагреву в условиях восстановительной среды, а затем попадает в окислительную среду. Будем рассматривать в первую очередь случай недостатка кислорода, поскольку именно такие условия реализуются в зоне пиролиза и горения шин в реакторе. Кроме того, случай избытка кислорода достаточно подробно описан в работе [14]. Следовательно, в случае использования химически инертного теплоносителя рассматриваемая система принимает вид C14H15Ca0.05S0.1Zn0.026O10. А в случае экспериментов с мрамором в качестве теплоносителя кальций присутствует в большом избытке по отношению к количеству серы, поэтому рассматриваемая система принимает вид C14H15Ca0.5S0.1Zn0.026O10. Расчет термодинамических равновесий в продуктах сгорания проводили для атмосферного давления, варьируя температурный интервал от 0 до 1400 °С с шагом 20 °С.
Методика проведения экспериментов по газификации
Эксперименты по газификации в фильтрационном режиме проводили в вертикальном цилиндрическом реакторе периодического действия, выполненном из кварцевого стекла, с внутренним диаметром 46 мм и длиной 800 мм (рис. 1). Перед экспериментом нижнюю часть реактора заполняли твердым негорючим материалом, выполняющим роль подложки. Далее реактор загружали исследуемой смесью, состоящей из кусочков шин и твердого теплоносителя, который обеспечивает наличие пористого каркаса. В проведенных сериях экспериментов соотношение масс шин и теплоносителя было 1 : 1 (50 мас.% шин и 50% теплоносителя).
Рис. 1.
Принципиальная схема экспериментальной установки: 1 – реактор, 2 – электроспираль, 3 – ротаметр, 4 – вентиль подачи воздуха в реактор, 5 – водяной холодильник, 6 – колба для сбора смол, 7 – термометр, 8 – барботажные колбы, 9 – дожигатель горючих газов, 10 – вентиль подачи воздуха в дожигатель, 11 – электроспираль дожигателя, 12 – отбор проб газообразных продуктов.
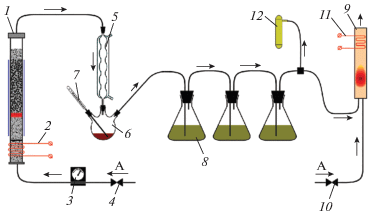
После прогрева электроспиралью 2 нижней части реактора (см. рис. 1) в него начинали подавать воздух, что приводило к формированию волны фильтрационного горения, которая обеспечивала газификацию шин. Продукты газификации, выходящие из верхней части реактора, содержали жидкие (пиролизные смолы) и газообразные продукты. Они последовательно направлялись в водяной холодильник 5, в котором смолы частично оседали на стенках и стекали в трехгорлую колбу 6. Далее для поглощения кислых газов продукты газификации проходили через три соединенные последовательно барботажные колбы 8, заполненные 10%-ным раствором Na2CO3. Пиролизные смолы, присутствующие в газообразных продуктах, практически полностью оседали в первых двух барботажных колбах. Газообразные продукты, прошедшие через колбы, направлялись в дожигатель 9, в котором проводили смешение с дополнительным потоком воздуха и сжигание оставшихся горючих компонентов.
В ходе эксперимента для анализа состава газообразных продуктов периодически отбирали пробы с помощью проточных стеклянных ампул 12 (рис. 1). Местом отбора проб была магистраль между выходом из барботажных колб и дожигателем. После эксперимента содержимое колбы для сбора смол и трех барботажных колб взвешивали, разделяли на фракции с помощью отстаивания в делительных воронках и проводили элементный анализ каждой из полученных фракций.
При использовании в качестве теплоносителя частиц сапфира зольный остаток взвешивали, затем отделяли золу от частиц сапфира и анализировали. При использовании крошки мрамора в качестве теплоносителя на анализ отправляли не только частицы золы, но и размолотые в ступке частицы мрамора.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Результаты термодинамического анализа системы
Оценка возможных фазовых и химических равновесных состояний химической системы был выполнен с помощью программы расчета равновесного состояния многокомпонентных гетерогенных систем [13]. На рис. 2а представлены зависимости мольной доли серосодержащих соединений от температуры в восстановительных условиях, полученные в результате термодинамических расчетов системы C14H15Ca0.05S0.1Zn0.026O10, которая соответствует газификации шин с использованием сапфира в качестве теплоносителя. В восстановительной среде до температуры 560 °С сера в первую очередь взаимодействует с водородом с образованием сероводорода (кривая 1 на рис. 2а), а оставшаяся часть серы реагирует с цинком с образованием сульфида цинка (кривая 3). При температурах 560–620 °С сера из газовой фазы (сероводород) частично переходит в твердую фазу сульфида кальция (кривая 2). При температурах более 800 °С сера из сульфида цинка переходит в форму сероводорода. Кроме того, в продуктах присутствует небольшое количество серооксида углерода (кривая 4).
Рис. 2.
Расчетные зависимости мольной доли (φ) серосодержащих соединений от температуры (Т) для системы C14H15Ca0.05S0.1Zn0.026O10 (а) и для системы C14H15Ca0.5S0.1Zn0.026O10 (б): 1 – сероводород (г.), 2 – сульфид кальция (тв.), 3 – сульфид цинка (тв.), 4 – серооксид углерода (г.).
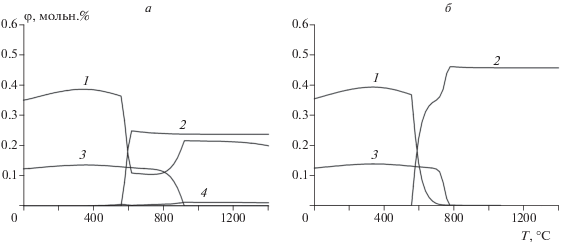
На рис. 2б представлены аналогичные зависимости для системы C14H15Ca0.5S0.1Zn0.026O10, которая соответствует газификации шин в случае использования крошки мрамора. До температуры 560 °С, как и в вышеописанном случае, основные серосодержащие продукты – это сероводород (кривая 1 на рис. 2б) и сульфид цинка (кривая 3). При температурах 560–740 °С сера из газовой фазы постепенно переходит в твердую фазу сульфида кальция (кривая 2). Выше 740 °С сера в рассматриваемой системе остается только в виде твердой фазы ZnS и CaS. А при температурах более 780 °С сера из сульфида цинка полностью переходит в сульфид кальция. Серооксида углерода в этом случае не образуется. В составе окислительной среды вплоть до 1200 °С будет преобладать твердый сульфат кальция, после чего с повышением температуры резко увеличивается скорость его разложения и сера переходит в газовую фазу в форме SO2 [14].
В условиях газификации в режиме фильтрационного горения происходит непрерывная фильтрация газа через слой загруженного в реактор материала. Вместе с потоком газа из высокотемпературной зоны реактора будет уноситься сероводород, смещая равновесия в сторону образования сероводорода согласно правилу Ле Шателье. В связи с неоднородностью состава и относительно медленно протекающими химическими реакциями в условиях экспериментов термодинамическое равновесие, как правило, не успевает установиться. В связи с этим фактические концентрации образующихся веществ могут значительно отличаться от рассчитанных, а результаты этого расчета могут быть использованы только для определения направлений химических процессов.
Результаты экспериментов
Эксперименты показали, что вид используемого теплоносителя (пористого твердого каркаса) влияет на выход образующихся смол: при использовании частиц сапфира выход смол составлял ~45%, а при использовании крошки мрамора – ~40 мас.%. По-видимому, это происходит из-за каталитического влияния карбоната кальция на разложение жидких продуктов пиролиза. Средний элементный состав жидких продуктов пиролиза следующий: С – 85.8%, H – 11.1%, S – 1.05%, N – 0.28%, O (по разнице) – 1.7%. Он был близок к элементному составу органической части исходных шин, за исключением содержания водорода, которое в жидких продуктах оказалось выше. От вида теплоносителя состав жидких продуктов тоже почти не зависел, за исключением несколько меньшего количества азота (0.26%) при использовании мрамора по сравнению с сапфиром (0.35%).
В процессе экспериментов состав газообразных продуктов был непостоянным и довольно сильно колебался. Усредненный состав газа при использовании сапфира в качестве теплоносителя был следующий: N2 – 68–70 об.%, CO2 – 12–14%, CO – 11–14%, H2 – 0.7–1.5%, метан – 0.2–0.4%, этилен – 0.2–0.4%. При использовании мрамора содержание CO2 было несколько выше: 15–19 об.%, а азота – ниже (64–67%). Состав горючих компонентов газа был таким же. Теплота сгорания газообразных продуктов составляла примерно 2 МДж/м3.
Температура горения также различалась для разных видов теплоносителя незначительно. Максимальная температура вблизи стенки реактора составляла 850 °С, в центре реактора температура достигала 1150 °С. На рис. 3 приведены типичные показания термопар в центре (1) и у стенки реактора (2) при газификации автомобильных покрышек с использованием мрамора в качестве теплоносителя. Скачки в показаниях термопар связаны с периодическим обрушением материала в реакторе по мере выгорания горючих компонентов загрузки.
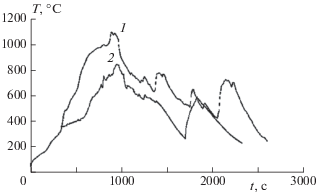
Рис. 3.
Показания термопар в центре (1) и у стенки реактора (2) при газификации автомобильных покрышек в смеси с мраморной крошкой.
На рис. 4 показаны температурный режим окисления частиц покрышки в электропечи и соответствующие этим условиям изменения их массы и элементного состава, отнесенные, соответственно, к массе исходного образца. Как видно из этого рисунка, по мере увеличения температуры и времени процесса частицы покрышки окисляются и масса ее твердого остатка уменьшается. Относительное содержание углерода, водорода и серы при этом снижается. Наиболее резкое снижение происходит на первом этапе окисления: масса образца составляет всего 37.5% от исходной, относительная доля углерода в твердом остатке снижается до 37%, а водорода и серы – до 6.5% и 54% соответственно. При дальнейшем окислении углерод и водород сгорают практически полностью, но даже в этих образцах остается значительное количество серы, которое составляет примерно 21% от ее исходного содержания. Этот результат хорошо согласуется с данными по составу золы шин, представленными выше.
Рис. 4.
Температурный режим окисления частиц покрышки в электропечи (1) и соответствующие относительное изменение общей массы (2) и покомпонентно доли водорода (3), углерода (4) и серы (5).
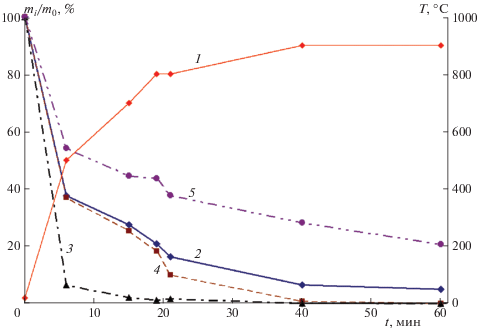
Обнаружена корреляция между степенью выгорания материала и долей серы, остающейся в твердых продуктах сгорания (от ее исходного содержания в материале). Корреляция сохраняется как для частиц, прокаливавшихся в печке, так и для твердых продуктов, образующихся в экспериментах по газификации, в которых остаточное содержание углерода в зольном остатке колебалось в пределах от 5 до ~10 мас.% из-за нестабильности процесса газификации. При максимальном недогорании углерода (10%) доля серы в твердых продуктах сгорания составляла примерно 28 мас.% от ее исходного содержания в материале. После дополнительной прокалки зольного остатка и практически полного выгорания органической части и углерода в золе оставалось около 21% серы от ее исходного содержания, что согласуется как с результатами окисления образцов шин в печке, так и с данными по составу золы используемых шин.
В экспериментах по газификации при использовании мрамора в качестве теплоносителя доля серы (от ее исходного количества), перешедшая в зольный остаток, составляла примерно 40%, что в 1.5 раза больше, чем при использовании инертного в химическом отношении сапфира (примерно 28%). Общее распределение серы между продуктами газификации приведено в табл. 1.
По всей видимости, мраморная крошка, выбранная нами в качестве активного теплоносителя (материала каркаса), по причине невысокой пористости частиц – не самый лучший сорбент кислых газов. Использование более активного щелочного сорбента, например оксида или гидроксида кальция, возможно, позволит увеличить долю серы, переходящей в твердые продукты.
ЗАКЛЮЧЕНИЕ
Эксперименты по газификации автомобильных покрышек в смеси с твердым теплоносителем (50/50) в режиме фильтрационного горения показали, что процесс протекает неравномерно, но устойчиво. Температура и состав газообразных продуктов газификации изменяются мало. При этом зольный остаток содержит 5–10% остаточного углерода, что свидетельствует о неполном сгорании материала шин.
При использовании сапфира в качестве инертного теплоносителя массовая доля серы, перешедшей в зольный остаток, составляет примерно 28%. В смолу и газообразные продукты переходит соответственно 29% и 43% серы. После прокалки зольного остатка до полного окисления углерода массовая доля серы, оставшейся в нем, составляет примерно 21%. Последнее обстоятельство свидетельствует о том, что значительная часть всей серы химически связывается с минеральными компонентами золы.
Добавка кальцийсодержащих сорбентов в газифицируемый материал приводит к некоторому перераспределению соединений серы. В частности, использование в качестве теплоносителя мрамора вместо сапфира позволяет частично связать соединения серы, в результате чего доля серы, переходящей в зольный остаток, увеличивается до 40% в первую очередь за счет снижения ее доли, уходящей в газообразные продукты, до 34%. Снижение доли серы, уходящей с пиролизными смолами, не так заметно. Кроме того, использование мрамора приводит к некоторому снижению общего выхода пиролизных смол с 45 до 40% от массы исходного материала шин.
Определение элементного состава горючих материалов, образующихся продуктов горения, состава мрамора и минеральной части золы выполнены сотрудниками АЦКП ИПХФ РАН ст. инженером Г.В. Гусевой и с. н. с., к. ф.-м. н. Н.Н. Дрёмовой.
Исследование выполнено при финансовой поддержке госзаданием № 0089-2019-0018 и Программы фундаментальных исследований Президиума РАН № 15.
Список литературы
Gieré R., Smith K., Blackford M. // Fuel. 2006. V. 85. № 16. P. 2278; https://doi.org/10.1016/j.fuel.2005.11.024
Манелис Г.Б., Глазов С.В., Салганский Е.А., Лемперт Д.Б. // Успехи химии. 2012. Т. 81. № 9. С. 855; https://doi.org/10.1070/RC2012v081n09ABEH004279
Juma M., Koreňová Z., Markoš J., Annus J., Jelemenský Ľ. // Pet. Coal. 2006. V. 48. № 1. P. 15.
Srivastava R.K., Jozewicz W. // J. Air Waste Manag. Assoc. 2001. V. 51. № 12. P. 1676; https://doi.org/10.1080/10473289.2001.10464387
Ahn J., Okerlund R., Fry, A. Eddings E.G. // Intern. J. Greenh. Gas Con. 2011. V. 5. P. S127; https://doi.org/10.1016/j.ijggc.2011.05.009
Gupta A.K., Ibrahim S., Shoaibi A.Al. // Prog. Energ. Combust. 2016. V. 54. P. 65; https://doi.org/10.1016/j.pecs.2015.11.001
Cordoba P. // Fuel. 2015. V. 144. P. 274; https://doi.org/10.1016/j.fuel.2014.12.065
Stanger R., Wall T. // Prog. Energ. Combust. 2011. V. 37. P. 69.
Salgansky E.A., Kislov V.M., Glazov S.V., Salganskaya M.V. // J. Combust. V. 2016. Article ID 9637082; https://doi.org/10.1155/2016/9637082
Зайченко А.Ю., Глазов С.В., Салганский Е.А. и др. // Теорет. основы хим. технологии. 2017. Т. 51. № 5. С. 525; https://doi.org/10.7868/S0040357117050153
Цветков М.В., Полианчик Е.В., Зайченко А.Ю. // Теорет. основы хим. технологии. 2018. V. 52. № 5. P. 573.
Цветков М.В., Полианчик Е.В., Зайченко А.Ю., Цветкова Ю.Ю., Подлесный Д.Н. // Химия твердого топлива. 2018. № 2. С. 31; https://doi.org/10.7868/S0023117718020068
Трусов Б.Г. // Инж. журнал: наука и инновации. 2012. № 1. С. 21; https://doi.org/10.18698/2308-6033-2012-1-31
Jia X., Wang Q., Cen K., Chen L. // Fuel. 2016. V. 163. P. 157; https://doi.org/10.1016/j.fuel.2015.09.054
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика


