Химическая физика, 2021, T. 40, № 1, стр. 69-72
Влияние УФ-облучения на протекание некаталитического окисления дибензотиофена в дибензотиофенсульфоне кислородом воздуха
В. Н. Корчак 1, *, М. Я. Быховский 1, А. Н. Романов 1, О. Н. Сильченкова 1
1 Федеральный исследовательский центр химической физики им. Н.Н. Семёнова
Российской академии наук
Москва, Россия
* E-mail: korchak@polymer.chph.ras.ru
Поступила в редакцию 21.08.2020
После доработки 21.08.2020
Принята к публикации 20.10.2020
Аннотация
Окисление дибензотиофена (ДБТ) используется в качестве модельной реакции при исследовании процесса каталитического окислительного десульфирования дизельного топлива. Метод окислительного десульфирования включает стадию окисления соединений тиофенового ряда, содержащихся в топливе, в соответствующие тиофенсульфоны с последующей их экстракцией из реакционной смеси с помощью полярной жидкости. В настоящей работе проведено исследование реакции окисления ДБТ в ДБТ-сульфон в растворе октана кислородом воздуха в присутствии бензальдегида при комнатной температуре и облучении реакционной смеси ультрафиолетом (УФ). Показано, что в этом случае конверсия ДБТ в 97–98% может быть достигнута без использования катализатора. Установлено также, что УФ-облучение реакционной смеси можно проводить периодически (импульсами продолжительностью 1 мин), что позволяет избежать нагрева реакционной смеси в ходе реакции.
ВВЕДЕНИЕ
Фотоиндуцированное окисление находит широкое применение в процессах деградации органических примесей [1], деструкции полимеров [2], а также окислительной десульфуризации (ОДС) серосодержащих органических соединений [3]. Метод (ОДС) широко применяется для глубокой очистки моторных топлив от серосодержащих соединений и, в частности, от дибензотиофена (ДБТ) и его производных. В качестве катализаторов используют, как правило, соединения на основе гетерополикислот и солей на их основе, а в качестве окислителей – пероксид водорода [4–10], органические гидропероксиды и перкислоты [11]. Несмотря на то, что окисление ДБТ протекает достаточно быстро, селективно и в мягких условиях, использование перекисных соединений нежелательно из-за их высокой взрывоопасности. В связи с этим было предложено использовать кислород воздуха для получения перекисных соединений из подходящего субстрата непосредственно при проведении окисления ДБТ [12–14]. Авторы указанных работ показали, что подходящим субстратом для получения перекисных соединений являются альдегиды. Образующиеся при взаимодействии альдегидов с кислородом перкислоты окисляют ДБТ до ДБТ-сульфона, а сами переходят в соответствующие кислоты.
Реакцию окисления ДБТ проводят в присутствии катализатора. Ранее нами было показано [15], что при использовании ацетата кобальта в качестве катализатора, а бензальдегида в качестве субстрата для получения перкислоты конверсия ДБТ достигает 97–99% в течение 90–100 мин при комнатной температуре. Без катализатора при комнатной температуре реакция окисления протекает крайне медленно – за 100 мин конверсия ДБТ достигает лишь 35–38%. Использование катализатора, однако, требует дополнительных стадий: приготовления катализатора, контроля активности, удаления отработанного катализатора из реакционной смеси.
Альтернативным способом проведения реакции окисления ДБТ может стать реакция фотохимического окисления ДБТ в ДБТ-сульфон. В литературе имеется сообщение [3] о некаталитическом окислении ДБТ при облучении реакционной смеси УФ-светом с использованием трет-бутилгидропероксида в качестве окислителя. В работе [16] сообщается об окислении ДБТ кислородом воздуха с использованием альдегидов в качестве переносчиков кислорода при УФ-облучении реакционной смеси. Опыты проводились при 30 °С, что требовало наличия специального термостата для поддержания постоянной температуры.
Настоящее сообщение посвящено выяснению возможности проведения некаталитического фотохимического окисления ДБТ системой бензальдегид – кислород воздуха при комнатной температуре в условиях непрерывного облучения, а также в импульсном режиме, чтобы исключить разогрев реакционной смеси.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В кварцевую колбу объемом 50 мл загружали 11 мл октана, 4.9 ммоль бензальдегида и при перемешивании добавляли в реакционную смесь 44 мг (0.24 ммоль) ДБТ. Концентрация серы в исходной смеси составляла 1000 ppm. После загрузки исходной смеси начинали продувку воздуха через реактор со скоростью 20 мл/мин. В опытах с окислением реакционную смесь облучали в течение 1 мин с периодом, равным 10 мин, до достижения конверсии в 97–98%. При этом продолжительность экспериментов составляла 170–180 мин. Для облучения использовали ртутную лампу низкого давления (длина волны – 253.6 нм). При проведении эксперимента периодически отбирали пробы (1 мкл) для хроматографического анализа и определяли концентрацию ДБТ в реакционной смеси. Анализ проводили с использованием хроматографа КРИСТАЛЛ 2000М на капиллярной колонке с фазой ZB-1 и пламенного ионизационного детектора. Температуры колонки, испарителя и детектора составляли 200, 300 и 260 °С соответственно.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
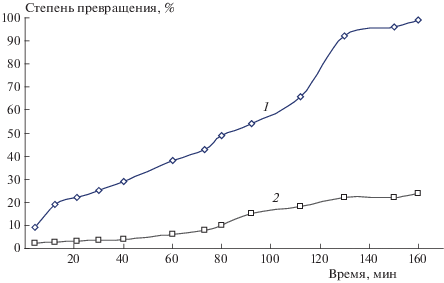
Нами была изучена зависимость степени превращения ДБТ в ДБТ-сульфон в октане от времени при температуре 23 °С при окислении кислородом воздуха в присутствии бензальдегида. Эксперименты проводились как без облучения, так и в режиме облучения реакционной смеси УФ-светом. Полученные результаты, представленные на рис. 1, показывают, что облучение сильно ускоряет окисление ДБТ. Так, из приведенных данных видно, что без облучения УФ-светом скорость окисления при комнатной температуре (23 °С) мала – степень превращения ДБТ за 60 мин составляет всего 5%, а за 160 мин не превышает 25% (рис. 1, кривая 1). При облучении реакционной смеси УФ-светом конверсия ДБТ в 97–98% достигается за 160 мин (рис. 1, кривая 2). Увеличение скорости достижения максимальной конверсии ДБТ сопоставимо с результатами, полученными нами ранее при использовании ацетата кобальта в качестве катализатора [15].
Рис. 1.
Зависимость конверсии ДБТ от времени с освещением УФ (1) и без освещения (2) при температуре 23 °С.
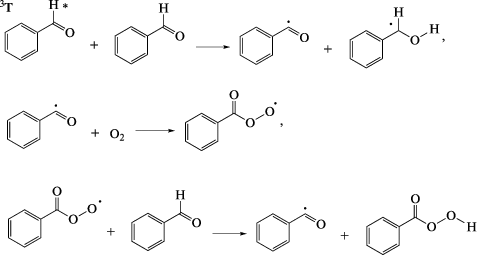
При проведении экспериментов с облучением реакционной смеси УФ-светом было установлено, что облучение разогревает ее примерно на 8–10 °С за 90 мин. Поскольку существует сильная зависимость конверсии ДБТ от температуры [15], то подобный разогрев реакционной смеси препятствует однозначной трактовке полученных результатов. Чтобы избежать такого разогрева, нами был предложен периодический режим облучения. В течение периода, составляющего 10 мин, облучение длится 1 мин, а 9 мин реакция протекает без облучения. В таком периодическом режиме облучение не вызывало увеличения температуры реагирующей смеси и реакция окисления ДБТ протекала изотермически. Из рис. 1 видно (кривая 2), что реакция протекает плавно во всем диапазоне измерений и периодические длительные отключения УФ не сказываются на характере кривой. Это можно объяснить тем, что во время облучения в реакционной смеси накапливается большое количество пербензойной кислоты, достаточное для проведения окисления ДБТ в период отсутствия облучения. Это согласуется с полученными нами ранее данными [15], согласно которым пербензойная кислота, накопленная предварительно, окисляет ДБТ при отсутствии других источников кислорода.
Пербензойная кислота в исследуемой реакционной смеси образуется, по-видимому, в результате фотоинициируемой цепной реакции [17, 18]. Под действием ультрафиолетового излучения молекула бензальдегида переходит в синглетное возбужденное состояние, которое в результате внутренней конверсии быстро релаксирует в возбужденный триплет (3T). Будучи, по сути, бирадикалом, триплетно-возбужденный бензальдегид инициирует цепную реакцию:
Ранее [17, 18] было показано, что в ходе такой цепной реакции квантовый выход образования пербензойной кислоты (на один поглощенный квант УФ-излучения) может достигать нескольких молекул, что свидетельствует о высокой энергоэффективности предложенного некаталитического импульсного способа фотоинициированного окисления ДБТ в ДБТ-сульфон кислородом воздуха в присутствии бензальдегида.
ЗАКЛЮЧЕНИЕ
Проведена реакция окисления ДБТ в ДБТ-сульфон кислородом воздуха в присутствии бензальдегида с использованием облучения реакционной смеси ультрафиолетом при комнатной температуре (23 °С) в периодическом режиме. Показано, что при использовании периодического (импульсами продолжительностью 1 мин) режима облучения удается избежать нагрева реакционной смеси и достичь конверсии ДБТ, составляющей 97–98%, без использования катализатора. Установлено также, что УФ-облучение может быть использовано как в непрерывном, так и в периодическом режиме для проведения фотоокисления ДБТ в ДБТ-сульфон кислородом воздуха в присутствии бензальдегида, что повышает эффективность данного метода как альтернативного энергосберегающего способа окислительного десульфирования моторного топлива, особенно в условиях дефицита солнечного света.
Список литературы
Свиридова Т.В., Садовская Л.Ю., Кокорин А.И. и др. // Хим. физика. 2017. Т. 36. № 4. С. 81.
Тертышная Ю.В., Подзорова М.В. // Хим. физика. 2020. Т. 39. № 1. С. 57.
Yokochi A., Hebert E., Parker J. et al. // Preprints of Symposia-Amer. Chem. Soc. Division of Fuel Chemistry. 2008. V. 53. № 1. P. 415.
Xue-Min Yan, Ping Mei, Jiaheng Lei et al. // J. Mol. Catal. A: Chem. 2009. № 304. P. 52.
Kollins F.M., Lucy A.R., Sharp C. // J. Mol. Catal. 1997. № 117. P. 397.
Mei H., Mei B.W., Yen T.F. // Fuel. 2003. V. 83. P. 405.
Huang D., Wang Y.J., Cui Y.C. et al. // Microporus Mesoporus Mat. 2008. № 116. P. 378.
De Filippis P., Scarsella M. // Energy & Fuels. 2003. № 17. P. 1452.
Lina Yang, Jian Li, Xingdong Yuan et al. // J. Mol. Catal. A: Chem. 2007. № 262. P. 114.
Mohsen M. Mostafa, Mohamed El saied, Asmaa S. Morshedy // J. Environ. Manage. 2019. V. 250. P. 1.
Ismagilov Z., Yashnic S., Kerzhentsev M. et al. // Catal. Rev. – Sci. Eng. 2011. V. 53. № 3. P. 199.
Rao T.V., Sain B., Kafola S. et al. // Energy & Fuels. 2007. № 21. P. 3420.
Murata S., Murata K., Kidena K. et al. // Ibid. 2004. № 18. P. 118.
Dumont V., Oliviero L., Mauge F. et al. // Catal. Today. 2008. № 130. P. 195.
Быховский М.Я., Вэнг Р., Сильченкова О.Н., Тюленин Ю.П., Корчак В.Н. // Технол. нефти и газа. 2014. № 1. С. 48.
Wenshuai Zhu, Chao Wang, Hongping Li et al. // Green Chem. 2015. V. 17. P. 2464.
Bäckström H.L.J., Riiner Ü. // Acta Chem. Scand. 1966. V. 20. P. 630.
Luňak St., Vepřek-Šiška J. // React. Kinet. Catal. Lett. 1981. V. 16. № 4. P. 305.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика