Химическая физика, 2021, T. 40, № 12, стр. 29-38
Численное моделирование термической конверсии продуктов газификации полипропилена
А. М. Тереза 1, *, Г. Л. Агафонов 1, Э. К. Андержанов 1, А. С. Бетев 1, С. П. Медведев 1, С. В. Хомик 1, Г. Н. Мохин 1
1 Федеральный исследовательский центр Химической физики им. Н.Н. Семёнова
Российской академии наук
Москва, Россия
* E-mail: tereza@chph.ras.ru
Поступила в редакцию 14.03.2021
После доработки 25.03.2021
Принята к публикации 20.04.2021
Аннотация
Проведено численное моделирование термической конверсии (ТК) продуктов газификации полипропилена в диапазоне температуры от 700 до 1400 К. За начальные составы исследуемых смесей были приняты экспериментальные данные, представленные в литературе. Расчеты показали, что различные детальные кинетические механизмы (ДКМ) одинаково описывают характер ТК, но значительно различаются по временнóму интервалу протекания основной фазы изучаемого процесса. Показано, что с повышением температуры продуктов газификации полипропилена наблюдается выход метана, водорода и ароматических соединений С6+ с одновременной убылью углеводородов С2+ исходных смесей. Обнаружено, что процесс ТК сопровождается выделением тепла, которое с ростом начальной температуры изучаемого процесса ослабевает, что объясняется увеличением роли эндотермической реакции диссоциации С3Н6. Установлено, что различные ДКМ предсказывают различающиеся составы вторичных продуктов ТК в виде ароматических углеводородов С6+. Показано, что достоверность расчетов повышается с учетом в ДКМ углеводородов С4+.
ВВЕДЕНИЕ
Полипропилен наряду с полиэтиленом является одним из основных видов пластика, нашедшим широкое применение во многих сферах жизнедеятельности человека [1–3]. Утилизация использованного пластика, широко представленного в различных бытовых, коммунальных и технологических отходах, требует комплексного подхода, направленного на рациональное снижение материальных и энергетических затрат [4–8]. Не менее важную роль играют экологические аспекты процессов переработки пластика. В этой связи в последнее время большой интерес представляет пиролиз полипропилена, в результате которого происходит его разделение на твердую, жидкую и газовую фазы [4, 9–13]. Последняя формируется в безокислительном процессе, что позволяет избежать образования токсичных окислов и получить газовые смеси, содержащие ценные с точки зрения дальнейшего их использования компоненты [6, 10, 14–17]. Установлено, что в своем большинстве основными газообразными продуктами пиролиза различных отходов химической промышленности, пластика и переработки биомассы в технологическом окне температур от 500 до 800 К является смесь углеводородов не выше С3, в совокупности с молекулярным водородом [8, 18, 19]. Доля углеводородов С4+ при этом составляет не более 10 мас.% в отходах, содержащих как пластик, так и каучук [8, 18]. При этом состав газовой фазы продуктов пиролиза углеводородов С0–С3 практически всегда един для всех отходов и представлен следующими химическими соединениями: Н2, СН4, С2Н4, С2Н6, С3Н6 и С3Н8. Различие в долях С0–С3 определяется только исходным составом перерабатываемых отходов [8, 10, 15, 18]. Подобная ситуация с образованием той же линейки углеводородов С0–С3 наблюдается и при пиролизе углеводородного горючего, используемого в качестве авиационного топлива [20–22]. Данный факт объясняется единством процесса разрыва химических связей и каналов химических превращений, происходящих при повышении температуры [23]. Все перечисленные компоненты газообразных продуктов пиролиза углеводородов С0–С3 представляют собой ценное химическое сырье. Дальнейшее разделение С0–С3, их переработка и конверсия представляют несомненный интерес [24–31]. Однако развитие использования газообразных продуктов пиролиза полипропилена осложнено рядом причин. В первую очередь к ним относятся различия в технологиях и физико-химических условиях, при которых проводится утилизация его отходов, а также необходимость учета особенностей структуры полипропилена и присутствия в его составе добавочных включений, состоящих не только из атомов углерода и водорода. В результате на выходе из промышленных установок образуются газообразные продукты пиролиза, различающееся как по составу, так и в пропорциях компонентов [2, 25, 26, 32–35]. Дальнейшая их раздельная переработка требует больших материальных затрат [2, 25, 26, 35].
Пиролиз и газификация, как составляющие общей технологии термической конверсии (ТК) полипропилена обладают большим потенциалом для решения поставленных проблем химической переработки отходов полипропилена с экологической и экономической точек зрения [2]. Обе эти технологии способны превращать пластиковое сырье при высокой температуре в полезные продукты. Чтобы осуществить конструкторские работы по созданию промышленных установок переработки газообразных продуктов пиролиза (ГПП) пластика, необходимы надежные знания о кинетике процессов, определяющей их ТК. Численное моделирование данного процесса является важным инструментом в ее изучении [33]. В настоящее время накоплен большой экспериментальный материал по выходу самих ГПП полипропилена [2, 8, 12, 26, 36]. Однако процесс дальнейшей термической конверсии этих смесей является малоизученным. Основной проблемой численного моделирования ГПП полипропилена является большая вариативность детальных кинетических механизмов (ДКМ), которые конструируются блочным образом на основе описания пиролиза отдельных углеводородов [37–39]. Поэтому возникает необходимость адаптации каждого ДКМ под конкретные физико-химические условия пиролиза углеводородов [40, 41]. Применительно к термической конверсии ГПП полипропилена численное моделирование было проведено в работе [42]. При этом была рассмотрена смесь ГПП полипропилена С0–С3 без участия углеводородов С4+. Такой подход используется достаточно часто при расчетах горения и пиролиза различных углеводородных топлив и энергетических смесевых систем [43–46], что обусловлено потребностями упрощения сложных газодинамических расчетов [47]. Эффект, оказываемый на результаты расчетов при включении в рассмотрение углеводородов С4+ при таком численном моделировании, требует отдельного изучения.
Целью настоящей работы было изучение термической конверсии ГПП полипропилена с более полным учетом всех компонентов газовой фазы, регистрируемых на выходе из пиролитической установки, посредством численного моделирования. Получение подобных результатов представляет не только научный интерес, но и позволяет определять пути и направления развития технологий, способствующих совершенствованию процесса утилизации разнообразных отходов с позиций их эффективного и рационального использования.
ЧИСЛЕННОЕ МОДЕЛИРОВАНИЕ
Расчеты проводились с использованием программного пакета CHEMKIN III [48]. Расчетный интервал времени не превышал 1 ч. Гетерогенные процессы, теплообмен с внешней средой и межфазовые переходы не учитывались. В качестве начальных использовались экспериментальные данные из работы [36], в которой измерялся выход газовой фазы из газогенератора, где термически разлагались гранулы чистого полипропилена. Начальный состав ГПП полипропилена представлен в табл. 1 в виде двух смесей. Согласно [36], состав смесей № 1 и № 2 определялся хроматографическим методом анализа на выходе из газогенератора, в котором поддерживалась постоянная температура. Процесс термического разложения полипропилена в газогенераторе проходил в диапазонах температуры 950–1100 К и давления 1.1–1.6 атм. Температура в зоне отбора проб составляла для смеси № 1 около 850 К, а для смеси № 2 – 960 К. Углеводороды С4 в работе [36] были идентифицированы в основном как изобутен (i-C4H8), а небольшая фракция С5 – как 2-метилбутен-1 (i-C5H10). Из табл. 1 видно, что при более высокой температуре в зоне отбора проб доля молекулярного водорода в смеси ГПП значительно вырастет, а доля углеводородов С4+ уменьшается. Также почти в два раза падают доли этана, пропена и пропана, доля этилена слабо возрастает, а доля метана увеличивается почти в два раза. При условии, что температура в газогенераторе в обоих случаях получения смесей №№ 1, 2 была одинакова [36], факт значительного изменения с ростом температуры мольных долей углеводородов на выходе показывает, что уже на пути от газогенератора до зоны отбора проб происходит термическая конверсия ГПП полипропилена.
Таблица 1.
Исходный состав газообразных продуктов полимеризации полипропилена (мольн.%)
| Номер смеси | Н2 | СН4 | С2H4 | С2Н6 | С3Н6 | С3Н8 | i-C4H8 | i-C5H10 |
|---|---|---|---|---|---|---|---|---|
| 1 | 5.3 | 22.6 | 12.3 | 14.3 | 32.8 | 3.2 | 8.9 | 0.6 |
| 2 | 23.7 | 31.6 | 15.0 | 8.0 | 15.7 | 1.4 | 4.5 | 0.1 |
С использованием единого начального состава смесей №№ 1, 2, представленных в табл. 1, проводился расчет для заданного значения начальной температуры Т0 при начальном давлении 1 атм и постоянном объеме (V = const). Посредством варьирования значения начальной температуры, изучалось ее влияние на состав продуктов ТК компонентов смесей №№ 1, 2 и характер протекающих процессов.
Критерием для выбора ДКМ было наличие в них блоков реакций с участием углеводородов i-C4H8 и i-C5H10. Кроме того, учитывалась полнота ДКМ в отношении на присутствия углеводородов С5+, и особенно ароматических соединений С6+, поскольку с ростом температуры в экспериментах отмечен рост их концентраций [49]. Была важна также применимость ДКМ к относительно низкотемпературной области пиролиза и окисления углеводородов (Т0 < 1000 K) [40]. Наиболее полно этим критериям соответствуют последние версии следующих исследовательских объединений: CRECK Modeling Group [37] (версия 1412), HAL [38] и LLNL+NUIG [39] (версия nbch-mech-062920 developed).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
На рис. 1–3 представлены временны́е профили концентрации компонентов [Xi] смесей № 1 и № 2 в процессе ТК при начальной температуре Т0 = 1000 К, рассчитанные по ДКМ из работ [37–39]. Для большей наглядности концентрации [C3Н8] и [i-C5Н10] показаны в увеличенном масштабе, как это указано в подписи к рис. 1. Расчеты по всем трем ДКМ показывают рост концентрации метана и водорода при убыли мольной доли остальных углеводородов С2+. При этом, если для смеси № 1 все три ДКМ предсказывают S-образный вид кривой роста [Н2], то для смеси № 2 первоначально наблюдается небольшая убыль водорода.
Рис. 1.
Временны́е зависимости изменения температуры и концентрации исходных компонентов в процессе ТК смесей № 1 (а) и № 2 (б). Линии соответствуют расчетам по ДКМ из [37] при Т0 = 1000 К, Р0 = 1 атм: 1 – [Н2], 2 – [CН4], 3 – [C2Н4], 4 – [C2Н6], 5 – [C3Н6], 6 – [C3Н8], 7 – [i-C4Н8], 8 – [i-C5Н10], ⚫ – температура. Изменение масштаба для смеси № 1: [i-C5Н10] × 10; для смеси № 2: [C3Н8] × 10, [i-C5Н10] × 100.

Концентрация этилена на начальном участке ТК растет, а затем, достигая максимума, спадает почти до нулевых значений. Такая тенденция в поведении профилей концентрации С2Н4 характерна для всех трех ДКМ и для обеих смесей. Концентрация метана после достижения максимума также начинает медленно понижаться, оставаясь, однако, выше своего начального значения. Концентрация всех остальных углеводородов С2+ убывает сразу с начала ТК. Детальный кинетический механизм из [37] предсказывает очень быстрый распад i-C5Н10 для обеих смесей, в то время, как по ДКМ из [38] концентрация [i-C5Н10] спадает до нуля значительно медленнее, а по ДКМ из [39] вообще заметно плавнее. Концентрации этана, пропена, пропана и изобутена снижаются практически монотонно в расчетах по всем трем ДКМ, достигая своих нулевых значений в моменты времени, близкие к достижению максимума [С2Н4].
Расчеты по всем трем ДКМ демонстрируют рост температуры в обеих смесях с достижением максимума и ее медленный спад затем до значений, превышающих Т0. Только в случае ДКМ из [38] кривая температуры растет постоянно, фактически симбатно с ростом кривой концентрации метана, повторяя по форме профиль [CН4] (рис. 2). Расчеты по ДКМ из [37] и [39] демонстрируют сначала небольшое понижение температуры для смеси № 1, а затем ускоряющийся S-образный рост ее профиля (рис. 1а и рис. 3а). В случае смеси № 2 расчеты по ДКМ из [37] и [39] (рис. 1б и рис. 3б) демонстрируют профили температуры, полученные для смеси № 1 и представленные на рис. 2.
Согласно расчетам по ДКМ из [42], учитывающему только относительно легкие углеводороды C0–C3, концентрация водорода падает, а концентрация этилена растет в процессе ТК полипропилена до квазистационарного уровня. Этот же ДКМ демонстрирует падение температуры в процессе ТК. В случае учета реакций с участием С4+ концентрация С2H4, после достижения максимума падает до уровня 1–2% от своего первоначального значения, а понижение концентрации H2 и температуры, если и происходит, то незначительно, и в процессе развития процесса конверсии смесей №№ 1, 2 концентрация водорода и тепловыделение увеличиваются (рис. 1–3). Такое расхождение с данными работы [42] в поведении зависимостей температуры и концентраций водорода и этилена указывает на важность учета реакций с участием углеводородов С4+ при численном моделировании термической конверсии ГПП полипропилена.
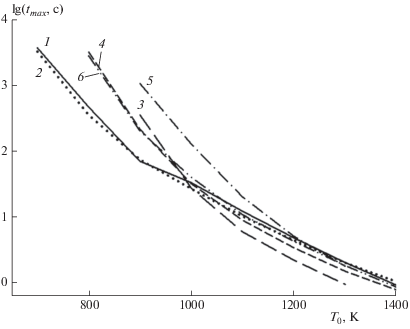
Сравнение рис. 1–3 показывает, что расчеты по всем трем ДКМ [37–39] показывают не только формирование максимумов роста температуры и концентрации метана и этилена, но и близкие значения времени их достижения. Для обеих смесей достижение этих максимумов определяет формирование квазистационарных уровней температуры и концентраций водорода и метана с одновременной убылью до практически нулевых значений концентраций всех остальных углеводородов смесей №№ 1, 2. Концентрация этилена хотя и достигает максимума для обеих смесей согласно расчетам с использованием всех ДКМ [37–39], но затем убывает до значения 1–2% от своей первоначального уровня. Такой вид профилей температуры и концентраций исходных компонентов позволяет рассматривать время достижения максимумов температуры (tmax) и концентрации метана в качестве характерного времени протекания активной фазы ТК смесей №№ 1, 2. На рис. 4 представлена температурная зависимость tmax(Т0), рассчитанная по каждому из ДКМ [37–39]. Видно, что для обеих смесей ДКМ из [37] дает одинаковое значение tmax(Т0). По ДКМ из [39] при T0 < 1000 K tmax(Т0) для смеси № 1 в 4–5 раз больше, чем для смеси № 2, а с повышением температуры эти значения сближаются и при T0 > 1200 K становятся фактически равными. Для ДКМ из [38] tmax(Т0) для смесей №№ 1, 2 при T0 < 1000 K приблизительно равны, но с ростом температуры ТК для смеси № 1 проходит немного быстрее. Следует заметить, что при T0 < 1000 K наблюдаются наибольшие расхождения в значениях tmax(Т0), рассчитанных по ДКМ из работ [37–39]. Так, для смеси № 1 время ТК при T0 < 900 К по ДКМ из [39] более чем на порядок больше, чем по ДКМ [37]. Рисунок 4 показывает, что с ростом начальной температуры все три ДКМ предсказывают все более близкие значения tmax(Т0). Также с увеличением T0 уменьшается влияние состава смеси на tmax(Т0).
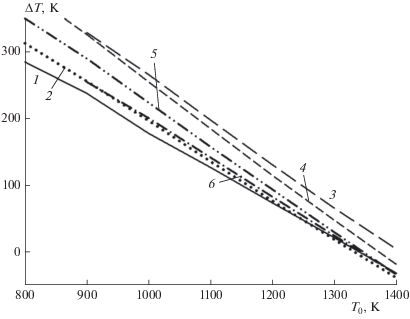
Поскольку термическая конверсия ГПП требует затрат энергии, то целесообразно проанализировать тепловые эффекты, связанные с этим процессом. Рисунки 1–3 демонстрируют рост температуры, что позволяет рассмотреть еще один характерный параметр ТК смесей №№ 1, 2, а именно, максимальный тепловой эффект, определяемый как ΔТ = Т(tmax) – T0. На рис. 5 представлены температурные зависимости ΔТ для смесей №№ 1, 2, рассчитанные по ДКМ из работ [37–39]. Видно, что с увеличением температуры тепловыделение при термической конверсии смесей №№ 1, 2 падает, и в области температур выше 1300 K процесс становится фактически термонейтральным. Несмотря на то, что составы смесей различаются, расчеты показывают одинаковый для них тепловой эффект в рамках каждого ДКМ. Наибольшее тепловыделение показывают расчеты по ДКМ из [38], а наименьшее – по ДКМ из [37]. С ростом температуры различие в расчетах ΔТ по ДКМ из работ [37–39] уменьшается, и при T0 > 1300 К оно не превышает 40 K.
Из рис. 1а и 3а видно, что на начальном этапе ТК наблюдается падение температуры смесей. С ростом T0 такое уменьшение температуры демонстрируют расчеты по всем трем ДКМ. Анализ показывает, что на начальной стадии ТК с ростом T0 увеличивается роль эндотермической реакции диссоциации С3Н6. На рис. 6 представлена температурная зависимость параметра ΔТс = Т(tс) – T0, где tс – времени, в который температура смесей №№ 1, 2 наиболее низкая. Расчеты по всем трем ДКМ показывают, что с увеличением Т0 усиливается и охлаждение этих смесей в начальной фазе ТК. Согласно рис. 6, наименьшее изменение ΔТспредсказывает ДКМ из [38]. По ДКМ из [37] и [39] смеси охлаждаются значительно сильнее и при T0 = 1400 К ΔТс составляет около 100 K. Если по ДКМ из [38] ΔТс одинаково для обеих смесей, то по ДКМ из [37] и [39] смесь № 1 охлаждается на 20–30 K больше, чем смесь № 2. Как следствие, охлаждение смеси № 1 в начальной фазе ТК по ДКМ из [37] и [39] наблюдается при значениях T0 ниже 1100 К. Увеличение абсолютного значения ΔТс с ростом Т0 приводит к тому, что суммарный эффект тепловыделения понижается (рис. 5). Следует заметить, что колебания температуры играют важную роль не только в скорости роста количества атомов в молекулах, но и в скорости их фрагментации [50]. С ростом Т0 выше 1400 К в расчетах необходимо учитывать конденсацию атомов углерода с образованием частиц сажи [51], что будет сопровождаться дополнительным выделением тепла. Тепловой эффект при температурах выше 1400 К с учетом конденсированной фазы углерода будет уже в целом термонейтральным [50]. В данном исследовании такие процессы не учитывались, поскольку при температурах ниже 1400 К сажеобразование незначительно [51].
Из анализа рис. 1–3 видно, что количество атомов углерода в увеличивающемся количестве метана значительно меньше, чем в углеводородах С2+, содержание которых убывает. Расчеты по всем трем ДКМ показали, что в процессе ТК образуется целый ряд вторичных продуктов, которые представляют собой ароматические углеводороды, преимущественно С6+. При этом, в каждом из ДКМ [37–39] предсказывается свой ряд таких углеводородов. В табл. 2 представлены основные вторичные продукты ТК смесей №№ 1, 2. Единым продуктом ТК для всех ДКМ является только бензол (С6Н6). Кроме него по ДКМ из [37] образуется коранулен (C20H10), диметилбензантрацен (C20H16) и трифенилэтилен (C20H16), по ДКМ из [38] − бициклопропил-1,1 (C6H10) и нафталин (C10H8), а по ДКМ из [39] – толуол (С7Н8), нафталин (C10H8) и фенантрен (C14H10). Такой разброс по продуктам ТК смесей №№ 1, 2, демонстрируемый в расчетах с применением различных ДКМ позволяет сделать только качественное утверждение, что наряду с ростом концентрации метана и водорода образуются ароматические соединения С6+. Наличие С6Н6 во вторичных продуктах термической конверсии ГПП полипропилена согласуется с экспериментальными данными по регистрации этого углеводорода при пиролизе различных отходов [49, 52–54]. В этих же работах указывается на появление толуола, что соответствует расчетам по ДКМ из [39]. С ростом температуры ДКМ из [38] предсказывает появление ацетилена. Такой результат вполне ожидаем, если учесть, что увеличение температуры приводит к разложению бензола с образованием ацетилена в качестве одного из продуктов его пиролиза [40].
Таблица 2.
| Вторичный продукт | [37] | [38] | [39] |
|---|---|---|---|
| Бензол C6H6 | + | + | + |
| Толуол С7Н8 | + | ||
| Бициклопропил-1,1 (1,1-Bicyclopropyl C6H10) | + | ||
| Инден (Indene C9H8) | + | ||
| Нафталин (Naphthalene C10H8) | + | + | |
| Бифенил (Biphenyl C12H10) | + | ||
| Фенантрен (Phenanthrene C14H10) | + | ||
| Коранулен (Corannulene C20H10) | + | ||
| Диметилбензантрацен (Dimethylbenzanthracene C20H16) | + | ||
| Трифенилэтилен (Triphenylethylene C20H16) | + |
ЗАКЛЮЧЕНИЕ
Проведенное численное моделирование термической конверсии ГПП полипропилена показало, что используемые в работе ДКМ качественно одинаково описывают изучаемый процесс по профилям как концентраций углеводородных компонентов исходных смесей, так и температуры. Однако временные масштабы процесса ТК для разных ДКМ сильно различаются. Установлено, что характер кинетики термической конверсии малочувствителен к изменению состава исходных смесей. Все расчеты демонстрируют рост концентрации СН4 и Н2 и одновременную убыль остальных углеводородов С2+ исходных смесей ГПП полипропилена. Рост концентрации метана характеризуется достижением максимума, в то время как концентрация водорода асимптотически приближается к своему стационарному уровню. Температура смеси достигает своего максимума в момент окончания активной фазы ТК, когда наблюдается резкое уменьшение количества углеводородов С2+ в исходной смеси.
Обнаружено, что включение углеводородов С4+ в ДКМ вносит существенный вклад в характер термической конверсии ГПП полипропилена. С ростом начальной температуры ТК тепловой эффект процесса уменьшается вследствие роста влияния на ранней стадии эндотермической реакции диссоциации пропена. В процессе ТК из присутствующих углеводородов С2+ образуется целый ряд ароматических углеводородов С6+, чем и объясняется убыль первых. При этом в расчетах по различным ДКМ наблюдаются различия в составе и концентрациях этих вторичных продуктов термической конверсии ГПП полипропилена.
Работа выполнена в рамках Программы фундаментальных исследований Российской академии наук на 2013–2021 гг. по теме ФИЦ ХФ РАН № 49.23 (регистрационный номер ЦИТИС АААА-А18-118031590088-8).
Список литературы
La Mantia F.P. Polymer Sci. Technology Series / Ed. Karger-Kocsis J. V. 2. Dordrecht: Springer, 1999. P. 701; https://doi.org/10.1007/978-94-011-4421-6_95
Bora R.R., Wang R., You F. // ACS Sustainable Chem. Eng. 2020. V. 8. № 43. P. 16350; https://doi.org/10.1021/acssuschemeng.0c06311
Canopoli L., Coulon F., Wagland S.T. // Sci. Total Environ. 2020. V. 698. Paper № 134125; https://doi.org/10.1016/j.scitotenv.2019.134125
Wilkins E.S., Wilkins M.G. // J. Environ. Sci. Health, Part A. 1985. V. 20. № 2. P.149; https://doi.org/10.1080/10934528509375217
Kaminsky W. // J. Physique IV. 1993. V. 3. P. 1543.
Shudo T., Nagano T., Kobayashi M. // Intern. J. Automotive Technol. 2003. V. 4. № 1. P. 1.
Zhang G.-H., Zhua J.-F., Okuwaki A. // Resources, Conservation and Recycling. 2007. V. 50. № 3. P. 231.
Czajczyn’ska D., Anguilano L., Ghazal H. et al. // Therm. Sci. Engineer. Progress. 2017. V. 3. P. 171.
Bridgwater A.V. // Resource Recovery and Conservation. 1980. V. 5. P. 99.
Conesa J.A., Font R., Fullana A. et al. // J. Anal. Appl. Pyrolysis. 2009. V. 84. P. 95.
Chen D., Yin L., Wang H., He P. // Waste Management. 2014. V. 34. P. 2466.
Abbas-Abadi M.S., Haghighi M.N., Yeganeh H., McDonald A.G. // J. Anal. Appl. Pyrolysis. 2014. V. 109. P. 272.
Saptoadi H., Rohmat T. A., Sutoyo // AIP Conf. Proceed. 2016. V. 1737. Paper 030006; https://doi.org/10.1063/1.4949286
Cho M.-H., Jung S.-H., Kim J.-S. // Energy Fuels. 2010. V. 24. P. 1389.
Soler A., Conesa J.A., Iniguez M.E., Ortuno N. // Sci. Total Environ. 2018. V. 622–623. P.1258.
Цветков М.В., Кислов В.М., Салганский Е.А. // ЖПХ. 2019. Т. 92. Вып. 11. С. 1363.
Xu Z., Xiao X., Fang P. et al. // Sustainability. 2020. V. 12. P. 464; https://doi.org/10.3390/su12020464
Williams P.T. // Waste Management. 2013. V. 33. P. 1714.
Zeaiter J. // Fuel. 2014. V. 133. P. 276.
Huang H., Sobel D.R., Spadaccini L.J. // Proc. AIAA/ASME/SAE/ASEE. Indianapolis, Indiana: AIAA, 2002. Paper № 2002-3871.
Fan X.J., Zhong F.Q., Yu G., Li J.G. // J. Propulsion Power. 2009. V. 25. № 6. P. 1226.
Ruan B., Meng H., Yang V. // Intern. J. Heat Mass Transfer. 2014. V. 69. P. 455.
Ямпольский Ю.П. Элементарные реакции и механизм пиролиза углеводородов. М.: Химия, 1990. С. 216.
Conesa J.A., Ortuño N., Palmer D. // Sci. Reports. 2020. V. 10. P. 6750; https://doi.org/10.1038/s41598-020-63807-w
Tangri N., Wilson M. Waste gasification and pyrolysis: High risk, low yield processes for waste management. A technology risk analysis. Report: no-burn.org/gasification-pyrolysis-risk-analysis. US: GAIA, 2017.
Xue Y. Ph. D. Theses. Capstones, US: Iowa State University, 2017. № 16242; https://lib.dr.iastate.edu/etd/16242
Салганский Е.А., Полианчик Е.В., Манелис Г.Б. // Физика горения и взрыва. 2013. Т. 49. № 1. С. 45.
Veksha A., Giannis A., Chang V.W.-C. // J. Anal. Appl. Pyrolysis. 2017. V. 124. P. 16.
Al-Salem S.M., Antelava A., Constantinou A. et al // J. Environ. Manage. 2017. V. 197. P. 177.
Кислов В.М., Жолудев А.Ф., Кислов М.Б., Салганский Е.А. // ЖПХ. 2019. Т. 92. Вып. 1. С. 61.
Кислов В.М., Цветкова Ю.Ю., Глазов С.В. и др. // Хим. физика. 2020. Т. 39. № 8. С. 64.
Westerhout R.W.J., Waanders J., Kuipers J.A.M., Van Swaaij W.P.M. // Indust. Eng. Chem. Res. 1997. V. 36. P. 1955.
Buah W.K., Cunliffe A.M., Williams P.T. // Process Saf. Environ. Prot. 2007. V. 85 (B5). P. 450.
Cho M.-H., Jung S.-H., Kim J.-S. // Energy Fuels. 2010. V. 24. P. 1389.
Chen D., Yin L., Wang H., He P. // Waste Manage. (Oxford). 2014. V. 34. P. 2466.
Фролов С.М., Звегинцев В.И., Аксёнов В.С. и др. // Горение и взрыв. 2018. Т. 11. № 4. С. 44.
Ranzi E., Frassoldati A., Grana R. et al. // Prog. Energy Combust. Sci. 2012. V. 38. № 4. P. 468; http://creckmodeling.chem.polimi.it/
Schönborn A., Le M.D., Fournet R. et al. // Combust. and Flame. 2019. V. 205. P. 466.
Pitz W.J., Liang J., Kukkadapu G. et al. // Intern. J. Chem. Kinet. 2020. V. 53. Issue 3. P. 465; https://doi.org/10.1002/kin.21457
Tereza A., Agafonov G., Anderzhanov E. et al. // High Temp. Mater. Processes. 2019. V. 23. P. 291; https://doi.org/10.1615/HighTempMatProc.2019033024
Xu Z., Xiao X., Fang P. et al. // Sustainability. 2020. V. 12. P. 464; https://doi.org/10.3390/su12020464
Тереза А.М., Агафонов Г.Л., Андержанов Э.К. и др. // Хим. физика. 2020. Т. 39. № 8. С. 58.
Edwards T. // Combust. Sci. Tech. 2006. V. 178. № 1–3. P. 307.
Kick T., Herbst J., Kathrotia T. et al. // Energy. 2012. V. 43. P. 111; https://doi.org/10.1016/j.energy.2012.01.035
Zhong B.-J., Peng H.-S. // J. Propul. Power. 2019. V. 35. № 3. P. 1.
Yang S., Jia M. // Front. Mech. Eng. 2019. V. 5. P. 21; https://doi.org/10.3389/fmech.2019.00021
Nikitin V.F., Mikhalchenko E.V., Kushnirenko A.G. // Proc. AIP Conf. 2020. V. 2304. Paper № 020017; https://doi.org/10.1063/5.0034720
Kee R.J., Rupley F.M., Meeks E., Miller J.A. CHEMKIN III Tech. Report № SAND96-8216. Livermor, CA: Sandia National Laboratories, 1996.
Gaurh P., Pramanik H. // Waste Manage. (Oxford). 2018. V. 77. P. 114.
Wang H. // Proc. Combust. Inst. 2011. V. 33. P. 41.
Агафонов Г.Л., Билера И.В., Власов П.А. и др. // Хим. физика. 2016. Т. 35. № 8. С. 21.
Kiran N., Ekinci E., Snape C.E. // Resources, Conservation and Recycling. 2000. V. 29. P. 273.
Nishino J., Itoh M., Fujiyoshi H., Uemichi Y. // Fuel. 2008. V. 87. P. 3681.
Ramirez-Canon A., Munoz-Camelo Y.F., Singh P. // Environments. 2018. V. 5. P. 72.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика