Химическая физика, 2021, T. 40, № 4, стр. 63-67
Особенности химического превращения взрывчатых веществ и других конденсированных сред в ударно-волновых процессах
В. С. Трофимов 1, *, В. А. Веретенников 1, Е. В. Петров 1
1 Институт структурной макрокинетики и проблем материаловедения им. А.Г. Мержанова
Российской академии наук
Черноголовка, Россия
* E-mail: pnkv@list.ru
Поступила в редакцию 01.10.2020
После доработки 01.10.2020
Принята к публикации 20.10.2020
Аннотация
Настоящая статья приурочена к юбилею нобелевского лауреата, акад. Николая Николаевича Семёнова. В данной работе авторы попытались ознакомить ученых, работающих в области физики взрыва и ударных волн, с анализом данных, полученных в работах, не привлекших достаточного внимания специалистов. Результаты анализа приводят к более глубокому осмыслению механизма химического превращения взрывчатых веществ и других конденсированных сред в ударно-волновых процессах.
ВВЕДЕНИЕ
В своем научном творчестве Н.Н. Семёнов стоял на позициях, кратко выраженных известным афоризмом Л. Больцмана: “Нет ничего практичнее хорошей теории”. Именно поэтому он придавал исключительное значение теоретическому осмыслению эмпирических данных, получаемых научными сотрудниками возглавляемого им Института химической физики АН СССР. И даже в тех случаях, когда этих данных было вполне достаточно для решения конкретных задач, он призывал ученых стремиться установить коренную природу наблюдаемых явлений. В 1955 г. для исследований ударно-волновых процессов в реагирующих конденсированных средах Н.Н. Семёнов создал группу молодых сотрудников под руководством своего ученика, перспективного ученого А.Н. Дремина, который только что с успехом окончил аспирантуру.
В начале 60-х годов А.Н. Дремин выдвинул предположение, что реакция разложения конденсированного взрывчатого вещества (ВВ) совершается частично в ударном фронте детонационной волны. Старшие коллеги тогда его не поддержали, так как это предположение не соответствовало теории детонации Я.Б. Зельдовича, которая предполагала, что во фронте детонационной волны газ только ударно сжимается и разогревается, а реакция взрывного превращения начинается после некоторого периода индукции. Тогда А.Н. Дремин с сотр. начали систематическое исследование структуры детонационных волн в конденсированных взрывчатых веществах. Они провели уникальные трудоемкие эксперименты [1, 2] по ударному инициированию плоского одномерного ударно-волнового процесса в литом тротиле (ТНТ). Позже в работе [3] экспериментально установлено, что реакция разложения конденсированного ВВ действительно частично происходит в ударном фронте детонационной волны. Кроме того, в работе [4] показано, что непосредственно в ударном скачке, например в акриламиде, происходит даже реакция полимеризации.
Анализ полученных в этих работах результатов проведен в работе [5] (см. ниже). Но уже предварительно можно сделать вывод, что физико-химическое превращение в ВВ и других конденсированных реагирующих средах непосредственно в ударных скачках, скорее всего – обычное явление.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
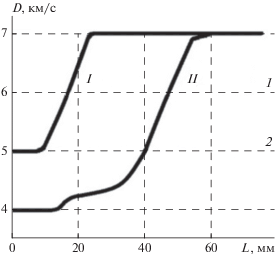
Обратимся к приведенным на рис. 1 данным работ [1, 2]. Здесь D и L – соответственно скорость ударного скачка и его путь в заряде ТНТ. Кривая I взята из работы [1], а кривая II – из [2]. Легко видеть, что в обоих сценариях эволюции инициирующих ударных волн в самоподдерживающуюся детонацию имеют место периоды их распространения с постоянной скоростью. В рамках привычных для “термохимии взрывчатых веществ” терминов эти периоды можно условно назвать “периодами индукции”.
Полагая, что зависимость скорости реакции от температуры соответствует закону Аррениуса, путем подбора предэкспоненциального множителя и энергии активации можно приближенно воспроизвести в расчетах форму каждой из кривых на рис. 1 в отдельности. Однако этого не удается сделать для обеих кривых с помощью одной и той же зависимости скорости реакции от температуры. Отсюда следует, что скорость реакции ВВ определяется не только текущим термодинамическим состоянием реагирующей среды, как утверждается в курсах физической химии для безударных процессов [6], но еще и каким-то иным фактором.
Из сопоставления точек пересечения с одной и той же прямой постоянной скорости (штриховые линии 1 и 2 на рис. 1) кривых I и II следует, что таким фактором может быть только скорость деформации реагирующей среды. Поэтому возможную зависимость скорости реакции от скорости деформации реагирующей среды необходимо всегда иметь в виду при анализе и расчете ударно-волновых процессов в конденсированных реагирующих средах. Как известно, в обычных (не ударно-волновых) процессах влияние скорости деформации среды на скорость реакции не проявляется, поскольку в этих случаях скорости деформации реагирующих сред слишком малы.
В процессе детального анализа экспериментальных данных [1, 2] пришлось существенно уточнить понятие теплоты реакции ВВ. Остановимся на этом подробнее.
Среди исследователей взрывчатых веществ существует представление о том, что каждое ВВ при заданном начальном состоянии можно охарактеризовать определенной энергией Et, являющейся мерой теплового движения и механических напряжений в среде, и химической энергией Q(α), где α – символ, обозначающий не физическую величину, а полный текущий набор химических компонентов среды: α = (α1, α2, α3…αn). Поэтому в работах по ВВ часто встречаются выражения вида: E(X, Y, α) = Et(X, Y, α) + Q(α), где E – удельная внутренняя энергия, Et – мера теплового движения и механических напряжений среды, аргументы X, Y – представляют собой пару независимых параметров (P, V), (P, T) или (V, T). Здесь и ниже P – давление, V – удельный объем, T – температура.
Однако для разделения внутренней энергии среды на две части нужен критерий, позволяющий однозначно разделить меру движения валентных электронов между энергией механических напряжений и энергией химических связей. Поскольку сегодня такой критерий неизвестен, лучше отказаться от разделения внутренней энергии конденсированной среды на части, как от лишнего усложнения теории ВВ.
Поэтому будем рассматривать внутреннюю энергию реагирующей среды как единое целое. Так ее рассматривают в современных руководствах по термодинамике, в частности в известном курсе теоретической физики Л.Д. Ландау и Е.М. Лифшица [7, 8].
В дальнейшем будем рассматривать только среды с положительным коэффициентом теплового расширения. Как известно, определить теплоту реакции действительно можно только применительно к заранее выбранному начальному состоянию ВВ. Отметим параметры такого состояния индексом “0” – E0, P0, V0, T0, α0 и обозначим его точкой с координатами P0, V0 на плоскости P–V (рис. 2).
Рис. 2.
К определению тепловых эффектов реакции. Изотермы продуктов реакции α: А – при T = T0; B – при T = 0 К.
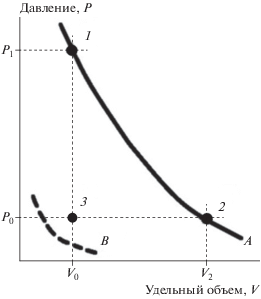
Рассмотрим одно и то же химическое превращение ВВ α0 → α, протекающее в трех разных условиях при постоянных параметрах: V и T; P и T; P и V. Конечный состав α не обязательно равновесный. Соответствующие конечные состояния продуктов реакции обозначим на плоскости P–V точками 1, 2 и 3 (рис. 2). Точки 1 и 2 находятся на изотерме T = T0 продуктов реакции, а точка 3 совпадает с точкой P0, V0. Представим аналитические определения трех тепловых эффектов реакции ВВ α0 → α (рис. 2).
Используемая в физической химии [6] теплота реакции при постоянном объеме (и постоянной температуре) определяется выражением
(1)
$\begin{gathered} {{Q}_{V}} = {{Q}_{{VT}}} = E\left( {{{P}_{0}},{{V}_{0}},{{\alpha }_{0}}} \right) - E\left( {{{P}_{1}},{{V}_{0}},\alpha } \right) = \\ = E\left( {{{V}_{0}},{{T}_{0}},{{\alpha }_{0}}} \right) - E\left( {{{V}_{0}},{{T}_{0}},\alpha } \right), \\ \end{gathered} $а используемая в физической химии [6] теплота реакции при постоянном давлении (и постоянной температуре) –
(2)
$\begin{gathered} {{Q}_{P}} = {{Q}_{{PT}}} = {{E}_{0}} - E\left( {{{P}_{0}},{{V}_{2}},\alpha } \right) - {{P}_{0}}\left( {{{V}_{2}} - {{V}_{0}}} \right) = \\ = {{E}_{0}} - E\left( {{{P}_{0}},{{T}_{0}},\alpha } \right) - {{P}_{0}}\left( {{{V}_{2}} - {{V}_{0}}} \right). \\ \end{gathered} $Введенная в научную терминологию [9] теплота реакции при постоянных давлении и объеме есть
(3)
${{Q}_{{PV}}} = E\left( {{{P}_{0}},{{V}_{0}},{{\alpha }_{0}}} \right) - E\left( {{{P}_{0}},{{V}_{0}},\alpha } \right).$Теплота QPV, наконец, получила свое законное место в третьем издании монографии “Физика взрыва” [10]. Заметим, что последнее выражение (3) имеет смысл только в том случае, когда нулевая изотерма продукта реакции α на плоскости P–V проходит ниже точки начального состояния (далее – начальной точки) P0, V0 по давлению (штриховая кривая на рис. 2). Если же нулевая изотерма продукта реакции α на плоскости P–V проходит выше начальной точки P0, V0 по давлению, например при P0 = 0, то у продукта реакции нет реального термодинамического состояния P0, V0, α. В этом случае для удобства анализа формы термодинамических кривых на плоскости P–V есть смысл ввести формальное состояние продукта реакции:
(3a)
$E\left( {{{P}_{0}},{{V}_{0}},\alpha } \right) = {{E}_{m}}\left( {{{P}_{m}},{{V}_{0}},\alpha } \right) - \frac{{{{V}_{0}}\left( {{{P}_{m}} - {{P}_{0}}} \right)}}{{{{{{\Gamma }}}_{m}}}},$где Em, Pm и Гm – соответственно удельная внутренняя энергия, давление и коэффициент Грюнайзена на нулевой изотерме продукта реакции при V = V0. Ясно, что в реальных процессах формальное состояние продукта реакции не участвует.
Как известно [10], в калориметрических бомбах определяется еще одна характеристика – калориметрическая теплота реакции Qcal. Из анализа процессов в таких бомбах следует аналитическое определение теплоты Qcal и ее связь с QPT:
(4)
$\begin{gathered} {{Q}_{{cal}}} = ~E\left( {{{P}_{0}},{{V}_{0}},{{\alpha }_{0}}} \right) - E\left( {{{P}_{0}},{{V}_{2}},\alpha } \right) = \\ = E\left( {{{P}_{0}},{{T}_{0}},{{\alpha }_{0}}} \right) - E\left( {{{P}_{0}},{{T}_{0}},\alpha } \right), \\ \end{gathered} $Как известно, последнее выражение применяется в исследованиях по термохимии взрывчатых веществ для расчета QP по Qcal [10].
Во многих работах, посвященных детонации ВВ, теплота Qcal из выражения (4) часто обозначается как QV и отождествляется с теплотой реакции при постоянном объеме QVT, определяемом в (1), а выражение (5) трактуется как соотношение между QP и QV (см., например, в [10], стр. 126). Это – ошибка.
Действительно, согласно выражениям (1) и (4), из равенства Qcal = QVT следует, что в точках 1 и 2 изотермы Т = T0 продукт реакции имеет одну и ту же удельную внутреннюю энергию E(V0, T0, α) = E(P0, T0, α) (рис. 2). Но это возможно, если только на всей изотерме Т = T0 между точками 1 и 2 продукт реакции удовлетворяет уравнению идеального газа Менделеева–Клапейрона, так как только у идеального газа внутренняя энергия на каждой изотерме имеет постоянное значение [7]. Но в окрестности точки 1 продукт реакции сжат до плотности конденсированного ВВ и, согласно классической работе [11], должен рассматриваться как твердое тело, т.е. заведомо не является идеальным газом.
Определим роль каждой теплоты реакции в физических процессах. Начнем с теплоты QPV в ударно-волновых процессах. Рассмотрим уравнение закона сохранения энергии в ударном скачке или в детонационной волне, представленное выражением
Перепишем это выражение в следующем виде:
(6)
$\begin{gathered} E\left( {P,V,\alpha } \right) - E\left( {{{P}_{0}},{{V}_{0}},\alpha } \right) = \\ = \frac{{\left( {P + {{P}_{0}}} \right)\left( {{{V}_{0}} - V} \right)}}{2} + {{Q}_{{PV}}}, \\ \end{gathered} $где в левой части уравнения сделана замена E(P0,V0, α0) на E(P0,V0, α). Пока речь идет только о математических соотношениях, неважно, является ли термодинамическое состояние продукта реакции реальным или формальным.
Легко заметить, что при QPV > 0 выражение (6) представляет собой уравнение кривой P(V), которая на плоскости P–V расположена выше начальной точки P0, V0 по давлению. Это – детонационная адиабата.
При QPV = 0 выражение (6) представляет собой уравнение кривой P(V), которая на плоскости P–V проходит через начальную точку P0, V0. Это – ударная адиабата. Как правило, в данном случае в ударном скачке реакция обычно отсутствует. Однако заметим, что законы термодинамики и в этом случае допускают реакцию в ударном скачке, так как в принципе не исключено существование реакций, при которых P и V одновременно остаются постоянными.
При QPV < 0 выражение (6) представляет собой уравнение кривой P(V), которая на плоскости P–V проходит ниже начальной точки P0, V0 по давлению. Это – ударная адиабата с эндотермическим (по теплоте QPV) превращением среды в ударном скачке.
Как показывает анализ, вид кривой P(V), описываемый уравнением (6) на плоскости P–V, в области реальных термодинамических состояний определяет характер наблюдаемого ударно-волнового процесса независимо от того, является ли данная среда взрывчатым веществом. На это впервые обратил внимание Н.М. Кузнецов в работе [12] и ввел в научную терминологию понятия: “безгазовая детонация”, при которой конденсированная среда превращается в конденсированный продукт реакции, а также “малогазовая детонация”, при которой только часть продукта реакции является газом, количество которого значительно меньше по сравнению с целиком газообразными продуктами реакции штатных ВВ.
В работе [11] показано, что внутри детонационных волн штатных ВВ реагирующая среда принципиально не отличается от твердого тела. Поэтому, казалось бы, можно предполагать, что детонационные волны в безгазовых и малогазовых средах не должны принципиально отличаться от детонационных волн в штатных ВВ. Однако опыт показывает, что данное предположение не выполняется.
Так, в работе [13] малогазовая детонация порошкообразной смеси Zn + S инициируется электрической искрой в одном конце закрытого стального реактора. Энергии этой искры недостаточно для создания заметной ударной волны. Тем не менее к противоположной стороне реактора приходит сильная волна, амплитуда которой по порядку величины равна амплитуде детонационных волн штатных ВВ. Поэтому в свете классической работы [11] можно утверждать, что самоускоряющаяся детонационная волна в смеси Zn + S и детонационные волны в штатных ВВ по своей внутренней структуре не должны принципиально различаться – в обоих случаях в детонационных волнах реагирует твердая среда.
Однако в отличие от штатных ВВ самоускоряющаяся детонационная волна в смеси Zn + S является крайне неустойчивой. При указанном инициировании она проходит только в тех реакторах, в стенке которых нет никаких отверстий и нет препятствий, перекрывающих даже незначительную часть поперечного сечения реактора. Отсюда следует, что, вопреки строгой математической теории детонации конденсированных ВВ [8], поток продукта реакции, отгороженный от детонационной волны звуковой поверхностью, все-таки влияет на процессы, протекающие внутри детонационной волны.
В заключение рассмотрим роль трех тепловых эффектов QVT, QPT и QPV в ламинарном движении реагирующей конденсированной среды между ударными скачками в ударно-волновых процессах. Удобно рассмотреть более общий случай, когда между частями среды существует теплообмен.
Будем исходить из закона сохранения энергии, представленного выражением
где q – удельная теплота, поступающая в данный элемент среды извне.
Рассматривая E как функцию P, V и α, согласно выражению (7), можно записать
(8)
$\frac{{dE}}{{dt}} = {{\left( {\frac{{\partial E}}{{\partial P}}} \right)}_{{V\alpha }}}\frac{{dP}}{{dt}} + {{\left( {\frac{{\partial E}}{{\partial V}}} \right)}_{{P\alpha }}}\frac{{dV}}{{dt}} + {{\left( {\frac{{\partial E}}{{\partial t}}} \right)}_{{PV}}}.$Здесь для краткости введено обозначение
(9)
$\left( {\frac{{\partial Z}}{{\partial t}}} \right) = \mathop \sum \limits_{i = 1}^n \left( {\frac{{\partial Z}}{{\partial {{\alpha }_{i}}}}} \right)\frac{{d{{\alpha }_{i}}}}{{dt}},$(10)
$\frac{{d{{Q}_{{PV}}}}}{{dt}} = - {{\left( {\frac{{\partial E}}{{\partial t}}} \right)}_{{PV}}}.$Используя термодинамическое тождество
(11)
${{\left( {\frac{{\partial P}}{{\partial V}}} \right)}_{{S\alpha }}} = - \frac{{{{{\left( {\frac{{\partial E}}{{\partial V}}} \right)}}_{{P\alpha }}} + P}}{{{{{\left( {\frac{{\partial E}}{{\partial P}}} \right)}}_{{V\alpha }}}}}$(13)
$\frac{{dP}}{{dt}} = {{\left( {\frac{{\partial P}}{{\partial V}}} \right)}_{{S\alpha }}}\frac{{dV}}{{dt}} + \frac{Г}{V}\left( {\frac{{d{{Q}_{{PV}}}}}{{dt}} + \frac{{dq}}{{dt}}} \right).$Рассматривая в выражении (7) E как функцию V, T и α, с учетом уравнения (9) можно записать
(14)
$\frac{{dE}}{{dt}} = {{\left( {\frac{{\partial E}}{{\partial V}}} \right)}_{{T\alpha }}}\frac{{dV}}{{dt}} + {{\left( {\frac{{\partial E}}{{\partial T}}} \right)}_{{V\alpha }}}\frac{{dT}}{{dt}} + {{\left( {\frac{{\partial E}}{{\partial t}}} \right)}_{{VT}}}.$Применяя определения удельной теплоемкости среды при постоянном объеме
и теплоты реакции при постоянных V и T(16)
$\frac{{d{{Q}_{{VT}}}}}{{dt}} = - {{\left( {\frac{{\partial E}}{{\partial t}}} \right)}_{{VT}}},$(17)
${{\left( {\frac{{\partial T}}{{\partial V}}} \right)}_{{S\alpha }}} = - \frac{1}{{{{C}_{V}}}}\left( {{{{\left( {\frac{{\partial E}}{{\partial V}}} \right)}}_{{T\alpha }}} + P} \right),$(18)
$\frac{{dT}}{{dt}} = {{\left( {\frac{{\partial T}}{{\partial V}}} \right)}_{{S\alpha }}}\frac{{dV}}{{dt}} + \frac{1}{{{{C}_{V}}}}\left( {\frac{{d{{Q}_{{VT}}}}}{{dt}} + \frac{{dq}}{{dt}}} \right).$Рассматривая E и V как функции P, T и α, с учетом (9) можно записать:
(19)
$\frac{{dE}}{{dt}} = {{\left( {\frac{{\partial E}}{{\partial P}}} \right)}_{{T\alpha }}}\frac{{dP}}{{dt}} + {{\left( {\frac{{\partial E}}{{\partial T}}} \right)}_{{P\alpha }}}\frac{{dT}}{{dt}} + {{\left( {\frac{{\partial E}}{{\partial t}}} \right)}_{{PT}}},$(20)
$\frac{{dV}}{{dt}} = {{\left( {\frac{{\partial V}}{{\partial P}}} \right)}_{{T\alpha }}}\frac{{dP}}{{dt}} + {{\left( {\frac{{\partial V}}{{\partial T}}} \right)}_{{P\alpha }}}\frac{{dT}}{{dt}} + {{\left( {\frac{{\partial V}}{{\partial t}}} \right)}_{{PT}}}.$Применяя определения теплоты реакции при постоянных P и T
(21)
$\frac{{d{{Q}_{{PT}}}}}{{dt}} = - {{\left( {\frac{{\partial E}}{{\partial t}}} \right)}_{{PT}}} - P{{\left( {\frac{{\partial V}}{{\partial t}}} \right)}_{{PT}}}$и теплоемкости среды при постоянном давлении
(22)
${{C}_{P}} = {{\left( {\frac{{\partial E}}{{\partial T}}} \right)}_{{P\alpha }}} + P{{\left( {\frac{{\partial V}}{{\partial T}}} \right)}_{{P\alpha }}},$а также тождество
(23)
${{\left( {\frac{{\partial T}}{{\partial P}}} \right)}_{{S\alpha }}} = - \left( {{{{\left( {\frac{{\partial E}}{{\partial P}}} \right)}}_{{T\alpha }}} + P{{{\left( {\frac{{\partial V}}{{\partial P}}} \right)}}_{{T\alpha }}}} \right),$из уравнений (19), (20) получаем
(24)
$\frac{{dT}}{{dt}} = {{\left( {\frac{{\partial T}}{{\partial P}}} \right)}_{{S\alpha }}}\frac{{dP}}{{dt}} + \frac{1}{{{{C}_{P}}}}\left( {\frac{{d{{Q}_{{PT}}}}}{{dt}} + \frac{{dq}}{{dt}}} \right).$Заметим, что в каждое из выражений (13), (18) и (24) значения удельной теплоты q входят одинаково c тепловыми эффектами реакции QVT, QPT и QPV . Отсюда следует, что из этих трех тепловых эффектов реакции нельзя выделить главный.
ВЫВОДЫ
Таким образом, в результате испытаний взрывчатых веществ получены принципиально новые данные о химических превращениях конденсированных сред в ударно-волновых процессах.
1. Установлено, что скорость химической реакции при ударно-волновом процессе в конденсированных средах зависит не только от текущего термодинамического состояния среды P, V, α, но и от скорости ее текущей деформации dV/dt.
2. Установлено, что, вопреки строгой математической теории детонации [8], возмущения из продуктов реакции проникают через звуковую поверхность внутрь детонационной волны.
3. Показано, что при анализе и расчете ударно-волновых процессов в конденсированных средах необходимо иметь в виду не один, а минимум три разных тепловых эффекта реакции, а именно: QVT, QPT и QPV .
Примером того, что разные тепловые эффекты реакции у одной и той же среды могут существенно различаться, является железоалюминиевый термит [14], у которого QPT > 0, а QPV ≤ 0.
Список литературы
Дремин А.Н., Колдунов С.А., Шведов К.К. // ЖПМТФ. 1963. № 6. С. 131.
Дремин А.Н., Колдунов С.А. // Взрывное дело. № 63/20. М.: Недра, 1967. С. 37.
Трофимов В.С., Трофимова Г.П. // Физика горения и взрыва. 1980. № 2. С. 92.
Веретенников В.А., Дремин А.Н., Михайлов А.Н. // Там же. 1966. № 3. С. 95.
Trofimov V.S., Veretennikov V.A., Petrov E.V. // Advances in Pulsed and Continuous Detonation / Ed. Frolov S.M. M.: Torus press, 2019. P. 54.
Зимон А.Д. Физическая химия: Учебник для вузов. М.: Агар, 2006.
Ландау Л.Д., Лифшиц Е.М. Теоретическая физика в 10 томах. Т. 5. Ч. 1. М.: Физматлит, 2002.
Ландау Л.Д., Лифшиц Е.М. Там же. Т. 6. М.: Физматлит, 2001.
Дремин А.Н., Савров С.Д., Трофимов В.С., Шведов К.К. Детонационные волны в конденсированных средах. М.: Наука, 1970.
Андреев С.Г., Бабкин А.В., Баум Ф.А. и др. Физика взрыва. Т. 1. М.: Физматлит, 2002.
Ландау Л.Д., Станюкович К.П. // ДАН СССР. 1945. Т. 46. С. 399.
Кузнецов Н.М. // ЖЭТФ. 1966. Т. 49. № 5. С. 1526.
Trofimov V.S., Petrov E.V. // Intern. J. Self-Propag. High-Temp. Synth. 2014. V. 23. № 4. P. 187.
Зефиров Н.С., Кулов Н.Н. Хим. энцикл. Т. 4. М.: Большая Российская энциклопедия, 1995.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика