Химическая физика, 2021, T. 40, № 8, стр. 19-25
Нейтрализация соединений серы при фильтрационном горении бурых углей с минеральными добавками
В. М. Кислов 1, *, Ю. Ю. Цветкова 1, М. В. Цветков 1, Е. Н. Пилипенко 1, М. В. Салганская 1, 2
1 Институт проблем химической физики Российской академии наук
Черноголовка, Россия
2 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
* E-mail: vmkislov@icp.ac.ru
Поступила в редакцию 12.11.2020
После доработки 09.12.2020
Принята к публикации 21.12.2020
Аннотация
Исследована газификация сернистого бурого угля с добавлением до 50 мас.% минеральной компоненты. В качестве минеральной компоненты использовали фарфоровые кольца Рашига, играющие роль химически инертного теплоносителя или частицы мрамора, которые дополнительно к этому реагируют с серосодержащими соединениями. Определены теплоты сгорания газообразных продуктов и содержание серы в зольном остатке в зависимости от вида и доли добавки, введенной в газифицируемый материал. С помощью рентгенофазового анализа показано, что в твердом остатке горения соединения серы находятся в виде сульфида и сульфата кальция. Установлено, что добавка 50 мас.% мрамора ведет к увеличению доли серы в зольном остатке в ~3 раза – до 37% от исходного содержания серы. Добавление 50 мас.% инертного наполнителя в шихту повышает температурный режим фильтрационного горения (с 1270 до 1400 °С), в результате чего соединения серы переходят из твердой фазы в газовую фазу.
ВВЕДЕНИЕ
Сера содержится во всех видах твердых топлив, таких как каменные и бурые угли, горючие сланцы, а также и в некоторых видах торфа. Но если содержание серы в торфе обычно не превышает 1.2%, то в углях оно может составлять до 10%, а в некоторых видах сланцев – до 12–14% [1, 2].
Содержащаяся в топливе в относительно небольшом количестве (до 1.5%) сера является нежелательной, а при больших количествах – вредной частью топлива. При термической переработке твердых топлив сера выделяется в виде газообразных соединений (в восстановительной атмосфере преимущественно в виде H2S и COS, а в окислительной – SO2), загрязняя и отравляя окружающую среду, и вызывая коррозию металлических конструкций, соприкасающихся с газообразными продуктами сгорания [3]. Именно поэтому при выборе путей использования тех или иных твердых топлив решающим фактором нередко оказывается содержание в них серы [4].
Угли Подмосковного бассейна главным образом относятся к бурым углям марки Б2 и характеризуются высоким содержанием серы – до 10%, т.е. относятся к сернистым (2.5–4.0% серы) и высокосерным (более 4.0% серы) топливам. Угли этой группы отличаются преобладанием сульфидной серы: главным образом в виде пирита (FeS2), халькопирита (CuFeS2) и марказита (полисульфида железа, FeS2); также в них в заметном количестве присутствуют сероорганические соединения [5]. При пиролизе угля может быть получено до 10–12% жидких продуктов и 15–20% газа. Зольность углей колеблется в пределах от 20 до 35%, характерной чертой их является высокое содержание оксидов алюминия и железа. Теплота сгорания сухих углей по бассейну колеблется от 11 до 17 МДж/кг [6].
Отчасти проблему выбросов вредных газов помогают решить использующиеся на промышленных предприятиях различные системы газоочистки, в том числе от соединений серы, однако они довольно дороги и громоздки [7]. В связи с этим в настоящее время идет поиск более простых и дешевых способов нейтрализации кислых газов. Существуют различные способы газификации твердых топлив [8]; одним из них является исследуемый в ИПХФ РАН способ, в котором в перерабатываемый материал добавляют кальцийсодержащие сорбенты для нейтрализации кислых газов непосредственно при газификации топлива [9]. Так, например, было показано, что добавка кальцийсодержащих сорбентов в шихту позволяет улавливать до 80% содержащихся в ней соединений хлора [10, 11]. Образующиеся при этом хлориды щелочных и щелочноземельных металлов остаются в зольном остатке и экологической опасности не представляют. Цель работы – экспериментальное исследование закономерностей поглощения серосодержащих газов кальцийсодержащими сорбентами при фильтрационном горении углей Подмосковного угольного бассейна.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве топлива был выбран сернистый бурый уголь Подмосковного бассейна – тульский уголь Кимовского разреза. В качестве твердой добавки в одной серии экспериментов использовали химически инертные фарфоровые кольца Рашига, фракция 5–10 мм. В другой серии экспериментов использовали частицы мрамора, фракция 3–7 мм. Анализ химического состава мрамора показал, что он состоит из CaCO3 и не имеет посторонних включений. Выбор мрамора в качестве поглощающей добавки обусловлен тем, что согласно результатам работ [10, 11] он является наименее реакционноспособным по сравнению с другими широко распространенными видами кальцийсодержащих поглотителей кислых газов, поэтому полученные результаты независимо от масштаба используемой нами экспериментальной установки позволят получить оценку нижнего предела эффективности поглощения серосодержащих газов и избежать необоснованного завышения оценки эффективности поглощения серы данным способом.
Элементный анализ угля, жидких продуктов и твердого остатка горения проводили методом сжигания в потоке кислорода на CHNS/O элементном анализаторе Vario MICRO cube, Elementar. Химический состав зольного остатка, а также мрамора, используемого в экспериментах, получали посредством анализа на сканирующем автоэмиссионном электронном микроскопе Zeiss LEO SUPRA 25, Carl Zeiss (табл. 1). Предварительно проведен технический анализ тульского угля по: ГОСТ Р 52911–2013 “Топливо твердое минеральное. Определение общей влаги”, ГОСТ Р 55661–2013 “Топливо твердое минеральное. Определение зольности”, ГОСТ Р 55660–2013 “Топливо твердое минеральное. Определение выхода летучих веществ”. Для определения кристаллических фаз золу анализировали на настольном рентгеновском порошковом дифрактометре Aeris, Malvern PANalytical с рентгеновской трубкой с Cu(Kα)-излучением и размером шага 0.012° в диапазоне 2θ = 5°–85°. Для идентификации фаз использовали электронную базу данных ICDD – PDF-4+.
Таблица 1.
Элементный анализ угля и его золы
| Материал | Элементный состав, % | Содержание золы, % | Теплота сгорания Q, МДж/кг | ||||
|---|---|---|---|---|---|---|---|
| C | H | O | N | S | |||
| Уголь | 42.57 | 3.82 | 23.13 | 0.78 | 2.70 | 27.00 | 13.0 |
| Твердый остаток | 0.14 | 0.08 | – | 0 | 1.18 | 98.60 | – |
Анализ газообразных продуктов выполнен с помощью хроматографа Кристалл-5000.2, Хроматэк. Содержание серы в газообразных продуктах определяли из массового баланса по разности. Влажность угля составила 8%, выход летучих продуктов – 27%, выход кокса – 38%, зольность – 27%. Минеральная часть золы угля, полученной по ГОСТ Р55661–2013, в пересчете на оксиды содержит: 46.0% А12O3, 32.3% SiO2, 2.1% СаО, 18.8% Fe2O3, содержание прочих компонентов в сумме составляло 0.8%.
Процессы в газификаторе шахтного типа
В реакторе фильтрационного горения реализуется несколько характерных зон [12]. В верхней части реактора находится зона сушки и нагревания (20–200 °C). В этой зоне исходная шихта постепенно нагревается потоком восходящего продукт-газа, который в свою очередь охлаждается. Ниже располагается зона пиролиза (200–800 °C), в которой органическая часть топлива, нагреваемая потоком газа, подвергается пиролизу, образуя кокс, газообразные и жидкие продукты пиролиза. Еще ниже располагается зона горения (800–1200 °C), где сгорает кокс и потребляется кислород из восходящего потока воздуха. В этой зоне водяной пар реагирует с коксом, образуя монооксид углерода и водород. В нижней части реактора находится зона охлаждения золы, где зольный остаток охлаждается, отдавая тепло восходящей паровоздушной смеси [13].
Основная идея метода поглощения серосодержащих газов заключается в добавлении щелочного сорбента к шихте, загружаемой в противоточный реактор-газификатор. В верхних слоях шихты поглощение серосодержащих газов идет в соответствии со следующими реакциями (на примере карбоната кальция):
Организация зон в реакторе создает благоприятные условия для нейтрализации соединений серы. В верхней зоне температура невысока и создаются условия, когда пары воды и сероводород или диоксид серы конденсируются на холодной поверхности свежезагруженных частиц шихты. Образующиеся кислоты (сероводородная и сернистая) могут при этом нейтрализоваться минеральными компонентами шихты, в том числе специально добавленными щелочными сорбентами. В зонах пиролиза и сушки поток газа фильтруется через шихту, обеспечивая взаимодействие потока газа с поверхностью сорбента.
Органическая сера в восстановительной зоне пиролиза превращается в сероводород (H2S) и сероокись углерода (COS). Пиритная сера (дисульфид железа) в восстановительной зоне пиролиза при температуре 400 °C превращается в сульфид железа с выделением сероводорода, а при температурах выше 500 °C сульфид железа может восстанавливаться до металлического железа [14]:
В окислительной зоне горения сера из оставшегося сульфида железа при температурах выше 550 °C полностью превращается в оксид серы(IV) [15]:
Образующийся при нейтрализации H2S сульфид кальция при прохождении фронта горения частично окисляется в оксид и сульфат кальция, причем количество образующегося оксида и сульфата кальция зависит от температуры горения [16]:
Сульфит кальция окисляется в сульфат кальция:
Сульфат кальция при повышении температуры выше 1200 °C начинает разлагаться на оксид кальция и диоксид серы:
В зоне охлаждения происходит остывание зольного остатка, а при паровоздушной газификации оксид кальция переходит в гидроксид кальция:
Сульфат кальция, сульфид кальция, оксид кальция, гидроксид кальция и непрореагировавший карбонат кальция выгружаются вместе с золой из нижней части реактора.
Описание установки
Эксперименты по исследованию нейтрализации серосодержащих газов с помощью добавок кальцийсодержащих сорбентов проводили в лабораторном вертикальном кварцевом реакторе периодического действия с внутренним диаметром 45 мм (рис. 1).
Рис. 1.
Принципиальная схема экспериментальной установки: 1 – реактор, 2 – смолоотделитель, 3 – двугорлая колба, 4 – водяной хододильник, 5 – трехгорлая колба, 6 – барботажная колба с 10%-ным водным раствором Na2CO3, 7 – газовая горелка, 8 – теплоотражающий экран, 9 и 10 – электроспирали, 11 – трубка подачи воздуха, 12 – термопары.
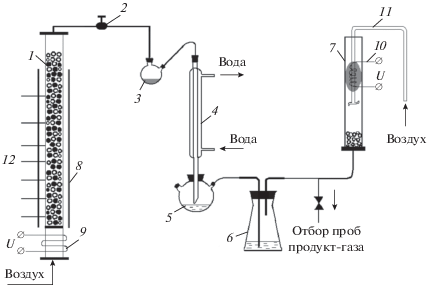
Загрузку газифицируемого материала осуществляли небольшими порциями послойно: вначале загружали порцию угля, затем – порцию негорючего материала, в результате чего в реактор было загружено 8–10 чередующихся слоев угля и негорючего материала. Насыпная плотность частиц тульского угля составляет 585 ± 15 кг/м3, колец Рашига – 880 ± 20 кг/м3 и частиц мрамора – 1070 ± ± 20 кг/м3. Насыпная плотность смесей угля и негорючего компонента практически линейно зависит от массовой доли добавки.
Экспериментальная установка состояла из реактора 1, в который загружали исследуемую шихту. На выходе реактора устанавливали смолоотделитель 2, принцип действия которого подробно описан в работе [17]. На выходе из смолоотделителя находилась двугорлая колба 3, в которой преимущественно осаждались жидкие продукты пиролиза.
Выходящая из колбы 3 парогазовая смесь поступает в водяной холодильник 4, на стенках которого оседают остатки смолы и капли воды, стекающие в приемную колбу 5. Далее по потоку находится барботажная колба 6 с 10%-ным водным раствором Na2CO3 для поглощения содержащихся в газовом потоке сернистых соединений.
После прогрева нижней части реактора 1 с помощью электроспирали 9 в него начинали подавать воздух, что приводило к формированию волны горения, распространяющейся снизу вверх. Удельный расход воздуха в реактор во время эксперимента поддерживали постоянным – 550 м3/(ч ⋅ м2). Полученный продукт-газ сжигали в газовой горелке 7, для чего в нее подавали дополнительное количество воздуха. Отбор проб газообразных продуктов осуществляли на участке магистрали между барботажной колбой и горелкой.
В большинстве экспериментов температуру измеряли у стенки реактора с помощью хромель-алюмелевых термопар, в экспериментах с добавкой инертного теплоносителя также с помощью платинородий-платиновых термопар проводили измерение температуры по оси реактора. В ходе экспериментов периодически осуществляли отбор проб газообразных продуктов в проточные стеклянные ампулы.
При использовании в качестве твердой добавки инертного теплоносителя фарфоровые кольца после сгорания отделяли от золы угля, после чего золу взвешивали и анализировали. При использовании в качестве твердой добавки частиц мрамора анализировали размолотые в ступке вместе частицы извести и золы.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Помимо высокого содержания серы проблемой исследуемого нами угля также является его достаточно высокая зольность (27%) и относительно невысокое содержание в нем углерода (43%), что не позволяет нам достаточно широко варьировать количество вводимой добавки без существенного ухудшения параметров газификации. При послойной загрузке в установившемся режиме даже при добавке 50% негорючей компоненты процесс идет стабильно, его параметры (массовая скорость горения по газифицируемому углю и состав газообразных продуктов) в ходе эксперимента почти не меняются.
При использовании инертного теплоносителя температура горения по оси реактора растет с 1270 (для угля без добавок) до 1400 °С (для добавки 50% инертного материала), что связано с аккумулированием тепла фарфоровыми кольцами (рис. 2). Но из-за теплопотерь через стенки реактора температура горения на стенках реактора оставалась практически постоянной и составляла всего 910 °С [18]. Несмотря на то, что измеренные температуры горения были ниже, чем указанный в литературе диапазон температур плавления золы данного угля (1450–1500 °С) [6], при разгрузке наблюдали оплавление заметной части образующегося зольного остатка. По-видимому, это объясняется локальными перегревами и неоднородным составом золы.
Рис. 2.
Зависимости температуры горения (Т, °С) угля от содержания твердых добавок (ω, мас.%). 1 – с инертным теплоносителем (по оси реактора), 2 – с инертным теплоносителем (у стенки реактора), 3 – с мрамором (у стенки реактора).
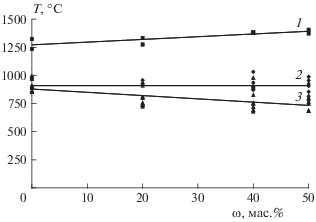
При использовании в качестве добавки частиц мрамора температуру горения измеряли только у стенки реактора. Температура горения снижалась с 910 до 750 °С с увеличением содержания добавки мрамора от 0 до 50 мас.%, что, очевидно, связано с затратами энергии на разложение карбоната кальция до оксида кальция и диоксида углерода. Плавления золы во всех случаях, когда в газифицируемый уголь добавляли мрамор, не происходило. Массовая скорость горения угля во всех экспериментах линейно снижалась при увеличении доли негорючего материала с 0.142 (уголь без добавок) до 0.130 г/с (уголь с добавкой 50% негорючей компоненты).
С увеличением содержания обоих видов негорючей добавки доля горючих компонентов (CO и H2) в продукт-газе снижается, а негорючих (CO2) – увеличивается (рис. 3). Это видно при добавлении к газифицируемому углю мрамора. Если при добавлении фарфоровых колец Рашига теплота сгорания газообразных продуктов снижается с 3.6 до 2.8 МДж/м3, то для составов с мрамором – до 2.2 МДж/м3. Следует отметить, что если при газификации составов с инертным теплоносителем изменение соотношения CO/CO2 приводит к сокращению объема образующихся газообразных продуктов примерно на 5%, то при газификации составов с мрамором за счет дополнительного объема углекислого газа, образующегося при разложении карбоната кальция, выход газообразных продуктов практически не меняется.
Рис. 3.
Зависимости содержания газообразных продуктов (Ni, об.%) от содержания твердых добавок (ω, мас.%) (сплошные линии и заполненные точки – инертный теплоноситель, штриховые линии и незаполненные точки – мрамор, 1 и 2 – H2, 3 и 4 – CO2, 5 и 6 – CO).
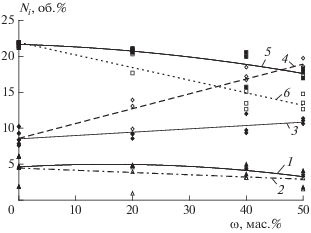
При сжигании бурого угля без минеральных добавок доля серы в золе составляет 12% от начального содержания серы в угле. Это объясняется наличием в золе исходного угля небольшого количества кальция (2.1% в пересчете на CaO) в форме карбоната кальция, который реагирует с сероводородом с образованием сульфида кальция или с диоксидом серы и кислородом с образованием сульфата кальция; последний при температурах эксперимента (910–1270 °С) практически не разлагается. Высокое содержание железа в угле (18.8% в пересчете на Fe2O3) не оказывает влияния на поглощение серы из серосодержащего продукт-газа, так как при температурах выше 600 °С сульфаты железа неустойчивы [19].
Добавление к твердым продуктам сгорания, полученным при сжигании смеси тульского угля с мрамором в массовом соотношении 1 : 1, разбавленной соляной кислоты привело к выделению сероводорода. Это показывает, что одним из соединений серы в золе является сульфид кальция.
Добавка инертного теплоносителя приводит к снижению долей углерода и серы, переходящих из угля в твердые продукты сгорания (рис. 4). По-видимому, это происходит из-за того, что небольшое увеличение температуры и некоторое снижение скорости горения (т.е. зольный остаток находился несколько дольше при более высокой температуре) способствует более полному выгоранию углерода, окислению сульфида кальция и частичному разложению сульфата кальция [20]. Остаточное количество серы в твердых продуктах сгорания составляет 2%.
Рис. 4.
Зависимости долей углерода и серы (Y[i], %), переходящих в твердые продукты сгорания (в расчете на 1 кг угля), от содержания введенной твердой добавки (ω, мас.%): 1 – [C] и 2 – [S] для колец Ришага, 3 – [S] для мрамора.
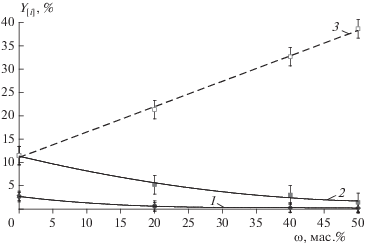
Добавка мрамора приводит к увеличению доли серы в твердых продуктах сгорания с 12 до 37%. По-видимому, небольшое снижение температуры, вызванное частичным разложением CaCO3, оказалось достаточным для предотвращения или снижения степени разложения сульфата кальция и выгорания сульфида кальция. Глубину выгорания углерода для смесей угля с мрамором не анализировали.
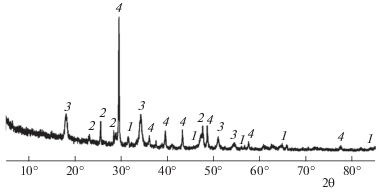
Рентгенофазовый анализ полученной золы (рис. 5) показал наличие сульфата, сульфида, карбоната и гидроксида кальция. Сульфита кальция (CaSO3) обнаружено не было, что согласуется с литературными данными [21].
Рис. 5.
Рентгенофазовый анализ золы, полученной при сжигании смеси тульского угля с мрамором (массовое соотношение 1 : 1): 1 – CaS, 2 – CaSO4, 3 – Ca(OH)2, 4 – CaСO3.
Пиролиз в нагревательной печи угля без добавок при температурных режимах, близких к условиям начала горения угля в эксперименте (800–900 °C), показал, что в жидкие и газообразные продукты пиролиза переходит примерно 30–40% серы, содержащейся в угле. Сера в газообразных продуктах пиролиза преимущественно находится в виде H2S с небольшим количеством сероокиси углерода (COS). В жидкие продукты пиролиза переходит примерно 10% серы, формы которой мы не определяли из-за их многообразия и сложности химического анализа. Таким образом, при пиролизе примерно 20–30% содержащейся в угле серы переходит в H2S и COS. Остающиеся в коксе примерно 60–70% исходной серы после пребывания в зоне горения переходят в золу (примерно 12%) и в газообразные продукты в виде SO2 (примерно 48–58%).
Выход смолы в обеих сериях экспериментов составлял примерно 8% от массы угля, что согласуется с ранее полученными данными [17]. Состав смолы практически не зависел от вида и количества добавки. Элементный состав смолы: C – 74.5–75.5%, H – 6.8–8.4%, O – 10.7–13.3%, N – 0.8–1.2%, S – 2.9–4.6%.
ВЫВОДЫ
1. Добавление к газифицируемому углю химически инертного наполнителя приводит к повышению температуры газификации и, следовательно, снижению содержания серы в золе с 12% от ее исходного содержания в угле (без добавок) до 2% (при 50 мас.% добавки) из-за разложения сульфата кальция и выгорания сульфида кальция.
2. Рентгенофазовый анализ золы, полученной при сжигании смеси тульского угля с мрамором в массовом соотношении 1 : 1, показал наличие сульфата, сульфида, карбоната и гидроксида кальция.
3. Добавка 50 мас.% мрамора ведет к увеличению доли серы, остающейся в зольном остатке с 12 до 37%. Доля серы, переходящая в пиролизную смолу, при этих условиях мало зависит от вида и количества добавки и составляет примерно 10%; доля серы, переходящей в газообразные продукты, соответственно снижается с 78 до 53%.
4. Нейтрализация и удержание серы в твердых продуктах сгорания, равное 37% от исходного содержания серы в угле при добавке 50% мрамора, не является предельным. Увеличивать количество добавляемого мрамора выше 40–50 мас.% нецелесообразно из-за сильного снижения теплоты сгорания газообразных продуктов и КПД газификации. Более перспективным представляется поиск добавки с большей площадью поверхности и/или высокой активностью (например, карбонат натрия или гидроксид кальция).
Определение элементного состава горючих материалов, образующихся продуктов горения, состава мрамора и минеральной части золы выполнены сотрудниками АЦКП ИПХФ РАН ст. инженером Г.В. Гусевой и с. н. с., к. ф.-м. н. Н.Н. Дрёмовой. Рентгенофазовый анализ и расшифровка рентгенограмм выполнена в лаборатории структурной химии в. н. с., к. х. н. Д.В. Корчагиным.
Исследование выполнено при финансовой поддержке государственным заданием № 0089-2019-0018 (регистрационный номер АААА-А19-119022690098-3).
Список литературы
Abad A., de Las Obras-Loscertales M., García-Labiano F. et al. // Chem. Eng. J. 2017. V. 310. P. 226; https://doi.org/10.1016/j.cej.2016.10.113
Maaten B., Loo L., Konist A. et al. // J. Anal. Appl. Pyrolysis. 2017. V. 128. P. 405; https://doi.org/10.1016/j.jaap.2017.09.007
Pinto F., André R.N., Franco C. et al. // Fuel. 2010. V. 89. № 11. P. 3340; https://doi.org/10.1016/j.fuel.2010.03.017
Stanger R., Wall T. // Prog. Energy Combust. Sci. 2011. V. 37. № 1. P. 69; https://doi.org/10.1016/j.pecs.2010.04.001
Потапенко В.А., Кузнецов Ю.Н., Гавришин С.С. // Горная промышленность. 2012. № 4. С. 104.
Комплексная переработка углей и повышение эффективности их использования. Кат.-справ. / Под общ. ред. Щадова В.М. М.: НТК “Трек”, 2007.
Meng X., De Jong W., Pal R. et al. // Fuel Process. Technol. 2010. V. 91. № 8. P. 964; https://doi.org/10.1016/j.fuproc.2010.02.005
Кришеник П.М., Костин С.В., Озерковская Н.И., Шкадинский К.Г. // Хим. физика. 2019. Т. 38. № 2. С. 45; https://doi.org/10.1134/S0207401X19020092
Кислов В.М., Цветкова Ю.Ю., Глазов С.В. и др. // Хим. физика. 2020. Т. 39. № 8. С. 64; https://doi.org/10.31857/S0207401X20080038
Цветков М.В., Зайченко А.Ю., Жирнов А.А. // Теорет. основы хим. технологии. 2013. Т. 47. № 5. С. 589; https://doi.org/10.7868/S0040357113040179
Салганская М.В., Глазов С.В., Салганский Е.А. и др. // Хим. физика. 2008. Т. 27. № 1. С. 20.
Цветков М.В., Полианчик Е.В., Зайченко А.Ю. // Теорет. основы хим. технологии. 2018. Т. 52. № 5. С. 573.
Манелис Г.Б., Полианчик Е.В. // Альтернативная энергетика и экология. 2008. № 2(58). С. 123.
Chen H.K., Li B.Q., Yang J.I. et al. // Fuel. 1998. V. 77. № 6. C. 487; https://doi.org/10.1016/S0016-2361(97)00275-5
Yang F., Lai Y., Song Y. // Process Saf. Environ. Prot. 2019. V. 129. P. 163; https://doi.org/10.1016/j.psep.2019.06.023
Song Z., Zhang M., Ma C. // Fuel Process. Technol. 2007. V. 88. № 6. P. 569; https://doi.org/10.1016/j.fuproc.2007.01.014
Salgansky E.A., Kislov V.M., Glazov S.V., Salganskaya M.V. // J. Combust. (Egypt). 2016. Article ID 9637082; https://doi.org/10.1155/2016/9637082
Колесникова Ю.Ю., Кислов В.М., Салганский Е.А. // Хим. физика. 2016. Т. 35. № 9. С. 53; https://doi.org/10.7868/S0207401X16090041
Gallagher P.K., Johnson D.W., Schrey F. // J. Amer. Ceram. Soc. 1970. V. 53. № 12. P. 666; https://doi.org/10.1111/j.1151-2916.1970.tb12038.x
Jia X., Wang Q., Cen K. et al. // Fuel. 2016. V. 163. P. 157; https://doi.org/10.1016/j.fuel.2015.09.054
Davies N.H., Laughlin K.M., Hayhurst A.N. // Proc. 25th Sympos. (Intern.) on Combust. Pittsburgh: The Combust. Inst., 1994. P. 211; https://doi.org/10.1016/S0082-0784(06)80646-6
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика


