Химическая физика, 2022, T. 41, № 3, стр. 81-84
Автоволновой синтез литого алюминида железа Fe2Al5 из смеси термитного типа
С. Л. Силяков 1, *, М. Ю. Ширяева 1, А. Ф. Беликова 1, Н. Ю. Хоменко 1, Т. И. Игнатьева 1, В. И. Юхвид 1
1 Институт структурной макрокинетики и проблем материаловедения им. А.Г. Мержанова
Российской академии наук
Черноголовка, Россия
* E-mail: ssl@ism.ac.ru
Поступила в редакцию 29.07.2021
После доработки 09.08.2021
Принята к публикации 20.08.2021
- EDN: QLOVYZ
- DOI: 10.31857/S0207401X22030128
Аннотация
В представленной работе показана возможность получения литого алюминида железа Fe2Al5 в режиме автоволнового синтеза из смеси термитного типа при атмосферном давлении в среде воздуха. В исследовании показано, что смеси Fe2O3–αAl горят в широком диапазоне соотношений реагентов, а температура их горения позволяет осуществлять гравитационную сепарацию продуктов горения и получать алюминиды железа в литом виде. Проведено исследование химического и фазового составов, микроструктуры, а также микротвердости синтезированного алюминида железа.
ВВЕДЕНИЕ
Алюминиды железа и их сплавы обладают набором разнообразных важнейших химических и физичеcких свойств. К отличительным признакам таких материалов относятся высокая коррозионностойкость, жаропрочность и жаростойкость при высоких показателях микротвердости. Теми же свойствами обладают покрытия из алюминидов железа [1, 2].
Среди разных способов получения алюминидов железа и покрытий на их основе в режиме горения наибольшее значение имеет автоволновой синтез. Изначально однофазные алюминиды железа в режиме горения были синтезированы из элементов при взаимодействии смеси порошков железа и алюминия. В результате были получены следующие фазовые составы: Fe2Al5, FeAl3. Конечные продукты горения в системе Fe–Al из других исходных смесей имели сложный многофазный состав [3]. Проведенные в работе [4] исследования показали, что синтез алюминидов железа возможен также в условиях горения двухслойных тонких пленок Fe/Al. Процесс горения возможно осуществить при начальной температуре 200–300 °C и толщине пленок 30–100 нм.
Интересным подходом к получению алюминидов железа является совместное использование твердофазной механоактивации и синтеза интерметаллидов из механоактивированной смеси в режиме объемного горения или теплового взрыва [5–7]. В этом случае предварительная активация, т.е. механическая обработка смесей порошков железа и алюминия в высокоэнергетичной мельнице, обеспечивает частичное химическое превращение. Окончательное химическое превращение, а также формирование химического и фазового составов, а также микроструктуры наступает на стадии горения и последующих процессов.
Наибольшие успехи в синтезе литых алюминидов железа были достигнуты при использовании одного из направлений технологического горения [8–11]. Синтез основан на использовании алюмотермической реакции восстановления оксида железа(II) с избыточным содержанием алюминия (выше стехиометрического). Методика позволяет синтезировать однофазные алюминиды железа Fe3Al, FeAl в литом виде. Следует отметить, что смеси FeO c Al не позволяют синтезировать Fe2Al5 вследствие недостаточного теплового эффекта реакции.
В настоящей статье приведены результаты исследований синтеза литого однофазного алюминида железа Fe2Al5 в режиме горения из смеси термитного типа Fe2O3/Al. К настоящему времени синтезированный алюминид железа нашел свое применение в качестве упрочняющей модифицирующей дисперсной добавки термодиффузионного борированного слоя, получаемого при индукционной наплавке [12, 13].
МЕТОДИКА ЭКСПЕРИМЕНТА
В качестве компонентов исходных экзотермических смесей термитного типа использовали порошки оксида железа(III) марки “Ч” и порошок алюминия марки АСД-1. Перед смешением компоненты исходной смеси высушивали. Синтез осуществляли при атмосферном давлении в среде воздуха. Во всех экспериментах сжигание экзотермической смеси осуществляли в графитовых стаканах с внутренним диаметром 40 мм и высотой 100 мм. Экзотермические смеси массой 100 г помещали в стаканы при плотности засыпки 1.3 г/см3. Воспламенение осуществлялось с помощью вольфрамовой спирали.
В экспериментах фиксировали относительную потерю массы (η1) экзотермической смеси Fe2O3/Al при ее горении и относительную полноту выхода литых интерметаллидов железа в слиток (η2), которые рассчитывали по формулам
В экспериментах проводили видеосъемку. В ходе экспериментов определяли концентрационный предел и скорость горения (u). Последнюю рассчитывали как среднюю линейную скорость горения между четырьмя базовыми точками по формуле ui = Hi/ti, где Hi – высота слоя экзотермической смеси Fe2O3/Al, ti – время горения слоя экзотермической смеси.
Рентгенофазовый анализ проводили на дифрактометре ДРОН-3 с графитовым монохроматором на вторичном пучке (излучение Fe(Kα)). Регистрация дифрактограмм велась в режиме пошагового сканирования в интервале углов 2θ = 30°–90° с шагом 0.02° и экспозицией 4 с.
Определение содержания алюминия в литых алюминидах железа выполнено методами классического химического анализа. Металлографическое исследование микроструктуры проводили на микроскопе Axiovert 200 MAT фирмы “Carl Zeiss” (Germany), микротвердость измеряли на микротвердомере “ПМТ 3”. Структуру полученных образцов выявляли с помощью химического травления.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
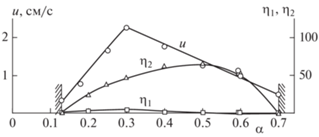
Горение экзотермической смеси термитного типа Fe2O3/Al при атмосферном давлении в среде воздуха идет без значительного диспергирования и выброса вещества, величины которых не превышают 10.5 мас.% (рис. 1). По мере разбавления оксида железа(III) алюминием, кривые скорости горения, относительного выхода алюминидов железа в слиток, а также относительной потери массы при горении экзотермической смеси Fe2O3/Al проходят через максимум. При горении зафиксированы два концентрационных предела распространения горения. Как при α < 0.125, так и при α > 0.7 процесс самораспространяющегося горения железоалюминиевого термита прекращается. Анализ закономерностей фазоразделения в системе Fe2O3/Al показал, что относительная полнота выхода литых интерметаллидов железа в слиток зависит от степени разбавления смеси алюминием (рис. 1).
Рис. 1.
Влияние относительной доли алюминия (α) в смеси Fe2O3/Al на скорость горения (u), относительную потерю массы при горении исходной смеси (η1) и относительный выход металлической фазы в слиток (η2).
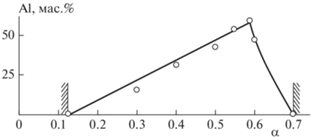
Область синтеза литых алюминидов железа ограничена интервалом значений 0.15 < α < 0.6. По данным химического анализа количество алюминия в литых интерметаллидах в этом интервале может меняться в диапазоне 0.1 < α < 59.9 мас.%, рис. 2. Содержание алюминия в слитке изменяется, практически линейно до α = 0.58. Далее из-за падения температуры горения исследуемой экзотермической смеси доля алюминия резко убывает. При α = 0.54 синтезируется материал с содержанием алюминия, равным 54.5 мас.%.
Рис. 2.
Влияние относительной массовой доли алюминия (α) в смеси Fe2O3/Al на содержание алюминия в литом слитке алюминида железа.
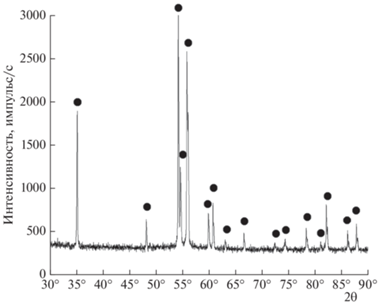
Рентгенофазовый анализ синтезированного материала (α = 0.54) показал (рис. 3), что получен однофазный продукт Fe2Al5 (пространственная группа – Cmcm). Рефлексы на рентгенограмме узкие, что свидетельствует о совершенстве кристаллической структуры Fe2Al5. Параметры элементарной ячейки Fe2Al5 близки к соответствующим значениям параметров базы дифракционных данных (см. табл. 1).
Таблица 1.
Значения пораметров элементарной ячейки синтезированного алюминида железа Fe2Al5
| Источник | Параметры решетки, Å | ||
|---|---|---|---|
| a | b | c | |
| Эксперимент | 7.6564 | 6.4094 | 4.2188 |
| ICDD PDF2* | 7.6486 | 6.4131 | 4.2165 |
* International Centre for Diffraction Data (CARD #000-47-14351); http://www.icdd.com/.
Металлографический анализ синтезированного алюминида показал, что его микроструктура представляет собой совокупность крупных зерен (рис. 4). Микротвердость алюминида Fe2Al5 равна 74.5–78.5 МПа.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Химическую схему синтеза литого алюминида Fe2Al5 можно записать следующем выражением:
Процесс синтеза включает в себя три основные последовательные стадии. На первой стадии протекают горение смеси и химическое превращение Fe2ОЗ и А1 в двухфазный расплав конечных продуктов (автоволновой синтез). На второй стадии происходит гравитационная сепарация продуктов горения – металлической и оксидной фаз. На этой стадии образуются два слоя: верхний – литой оксид алюминия, нижний – литой интерметаллид Fe2Al5. На третьей стадии расплав охлаждается и формируется фазовый состав кристаллической структуры металлического и оксидного слоев.
Возможность синтезировать литой однофазный алюминид железа Fe2Al5 появляется при замене окислителя оксида железа(II) на оксид железа(III) [8–11]. Достигается это за счет повышения температуры при протекании экзотермической окислительно-восстановительной реакции в режиме горения.
Такое повышение температуры обеспечивает расширение области синтеза литых интерметаллидов, приводит к значительному сдвигу концентрационного предела горения до α = 0.7, увеличению массового содержания алюминия в литых алюминидах железа за счет появившейся возможности повышения относительной доли алюминия (α) в исходной смеси (рис. 1, 2). В экспериментах с увеличением α, кривая скорости горения проходит через максимум. На участке роста скорости горения (0.125 < u < 0.3) преобладающее значение имеет возрастание температуры горения смеси Fe2O3/Al за счет повышения теплового эффекта реакции восстановления. Дальнейшее введение алюминия приводит к снижению температуры, а вместе с тем и скорости горения. В этом случае введение избыточного количества алюминия в смесь (выше стехиометрического) можно рассматривать как разбавление термитной смеси инертной добавкой.
Содержание связанного алюминия в зависимости от величины α с 0.125 до 0.58 в литом продукте изменяется практически линейно (рис. 2). Далее при α > 0.58 снижение температуры горения приводит к резкому падению содержания алюминия в литых продуктах.
Анализ полученных значений микротвердости синтезированного алюминида железа Fe2Al5 позволяет констатировать, что они имеют малый разброс и соответствуют табличным значениям [14].
ВЫВОДЫ
1. Проведенные исследования показали, что использование оксида железа(III) в составе железоалюминиевого термита обеспечивает синтез литого однофазного алюминида железа Fe2Al5 за счет повышения энергетики исходной смеси.
2. Наиболее значимым параметром процесса синтеза после температуры горения, влияющим на основные закономерности процесса, фазовый и химический составы алюминидов железа, является доля алюминия в составе исходной экзотермической смеси.
3. Полученные результаты могут послужить научной базой для создания технологического процесса синтеза литого алюминида железа Fe2Al5.
Список литературы
Металловедение алюминия и его сплавов. Справочное руководство / Под ред. Фридляндер И.Н. М.: Металлургия, 1971.
Макеев Д.Н. // Вестн. СГТУ. 2012. № 3(67). С. 92.
Итин В.И., Наибородченко Ю.С. Высокотемпературный синтез интерметаллических соединений. Томск: Изд-во Томского ун-та, 1989.
Мягков В.Г., Жигалов B.C., Быкова Л.Е., Мальцев В.К. // ЖТФ. 1998. Т. 68. № 10. С. 58.
Киселева Т.Ю., Григорьев Т.Ф., Гостев Д.В. и др. // Вестн. МГУ, Сер. 3. Физика, астрономия. 2008. № 1. С. 56.
Наибороденко Ю.С., Касацкий Н.Г., Сергеева Е.Г., Лепакова О.К. // Химия в интересах устойчивого развития. 2002. 10. С. 199.
Ильющенко А.Ф., Лецко А.И., Талако Т.Л., Дьячкова Л.Н., Парницкий Н.М. // Порошковая металлургия. Республ. межвед. сб. науч. тр. Минск: Высш. шк., 2018. С. 25.
Горшков В.А., Саков И.И., Юхвид В.И. // Физика горения и взрыва. 1994. № 5. С. 15.
Горшков В.А., Саков И.И., Юхвид В.И., Комратов Г.Н. // Порошковая металлургия. 1995. № 11/12. С. 15.
Симонян А.В., Горшков В.А., Юхвид В.И. // Литейное производство. 1997. № 8. С. 21.
Simonyan A.V., Ponomarev V.I., Yukhvid V.I. // J. SHS. 1999. V. 8. № 1. P. 88.
Ишков А.В., Иванайский В.В., Кривочуров Н.Т., Аулов В.Ф. Способ наплавки алюминида железа на стальную поверхность. Патент RU 2 693988 C1 // Оффициальный бюллетень Федеральной службы по интеллектуальной собственности “Изобретения. Полезные модели”. 2019. № 19.
Aulov V.F., Rozhkov Yu.N., Silyakov S.L., Yukhvid V.I. // J. SHS. 2020. V. 29. № 3. P. 184; https://doi.org/10.3103/S1061386220030024
Самсонов Г.В., Виницкий И.М. Тугоплавкие соединения. М.: Металлургия, 1976.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика