Химия твердого топлива, 2019, № 5, стр. 68-72
КИНЕТИКА ГИДРОГЕНИЗАЦИИ ТЯЖЕЛОГО И ТВЕРДОГО УГЛЕВОДОРОДНОГО СЫРЬЯ
Н. Ж. Балпанова 1, *, А. М. Гюльмалиев 2, Ю. Н. Панкин 3, Д. Е. Айтбекова 1, **, Ф. Ма 4, К. Су 4, Д. А. Кайкенов 1, Г. Г. Байкенова 5, А. С. Борсынбаев 1, М. И. Байкенов 1, 6, ***
1 Карагандинский государственный университет имени академика Е.А. Букетова
100028 Караганда, Республика Казахстан
2 ФГБУН Институт нефтехимического синтеза имени А.В. Топчиева РАН
11999 Москва, Россия
3 АО“Казахтелеком”
100000 Караганда, Республика Казахстан
4 Синьцзянский университет
830046 Урумчи, СУАР, Китайская Народная Республика
5 Карагандинский экономический университет Казпотребсоюза
100009 Караганда, Республика Казахстан
6 Южно-Уральский государственный университет
454080 Челябинск, Россия
* E-mail: nazerke_90@mail.ru
** E-mail: darzhan91@mail.ru
*** E-mail: murzabek_b@mail.ru
Поступила в редакцию 10.04.2019
После доработки 22.04.2019
Принята к публикации 03.06.2019
Аннотация
Приведены экспериментальные результаты кинетики гидрогенизации широкой фракции 230–300°С каменноугольной смолы в присутствии нанокатализатора Fe3O4. Рассчитаны константы скорости и суммарные константы скорости, энергия активации. Установлено, что лимитирующей стадией превращения широкой фракции 230–300°С каменноугольной смолы в продукты реакции является стадия превращения преасфальтенов в асфальтены. Процесс превращения широкой фракции 230–300°С в продукты проходит в кинетической области гетерогенного процесса.
Одним из важнейших направлений при подготовке процесса переработки твердого и тяжелого углеводородного сырья является гидрогенизация. Исследование кинетики гидрогенизационного превращения органической массы угля необходимо при моделировании и определении оптимальных технологических параметров процессов в зависимости от условия их проведения. Однако при этом возникают трудности, одна из которых – идентификация большого количества индивидуальных соединений, поэтому на практике их приходится группировать по некоторым условным физико-химическим свойствам [1].
Для снижения общего давления водорода в процессе гидрогенизации необходимо разработать надежный метод технологического расчета реактора, для чего необходимо знать величины констант скорости основных реакций, энергии активации и другие параметры, которые определяются формальной кинетикой гидрогенизации широкой фракции 230–300°C каменноугольной смолы.
Известны различные методы расчета кинетических параметров гидрогенизации угля, каменноугольной смолы и высоковязкой нефти [1–3].
Цель исследования – установление кинетических параметров гидрогенизации широкой фракции 230–300°C каменноугольной смолы и разработка кинетической модели процесса в автоклавных условиях. Эта задача решалась путем обработки экспериментальных данных с использованием метода “тяжелого шарика”.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве объекта исследования была использована широкая фракция с температурой кипения 230–300°С, которую отбирали из каменноугольной смолы дистилляционной разгонкой. Каменноугольная смола была получена в процессе коксования угля на предприятии АО “Шубарколькомир”.
Элементный состав широкой фракции каменноугольной смолы (%): С 81.11; Н 9.63; О 8.32; N 0.70; S 0.24. Атомное отношение Н/С – 1.43. Выход широкой фракции с температурой кипения 230–300°C из каменноугольной смолы составляет 42.7%.
Эксперименты по гидрогенизации широкой фракции 230–300°С каменноугольной смолы проводили в реакторе высокого давления с внутренней мешалкой емкостью 0.05 л при начальном давлении водорода 3.0 МПа.
Предварительно перемешанные исходные вещества (широкая фракция каменноугольной смолы, нанокатализатор) помещали в автоклав (массовое содержание нанокатализатора составляет 1.0% на исходную фракцию), закрывали, продували водородом и давали избыточное давление водорода. Затем автоклав нагревали (скорость нагрева составляла 10°С/мин) до необходимой температуры и выдерживали в течение заданного времени, после чего охлаждали до комнатной температуры. Автоклав открывали через 24 ч, и продукты гидрогенизации тщательно промывали бензолом.
Смесь полиароматических углеводородов в гидрогенизате определяли с помощью хромато-масс-спектрометрического (ХМС) анализа. Количественное содержание смол, асфальтенов и масел в гидрогенизате, полученные в процессе гидрогенизации широкой фракции 230–300°С каменноугольной смолы определяли по стандартной методике [4]. Масла, смолы и асфальтены выделяли из гидрогенизата по методу [2].
ХМС-анализ полиароматических углеводородов проводили на газовом хроматографе фирмы Agilent Technologies 7890A с масс-спектрометрическим детектором 5975С. Для анализа использовалась подвижная фаза SE марки А, хромотографическая колонка НР = 5НS, длина которой 30 м, толщина 0.25 мм, толщина адсорбента внутри капилляра 0.25 мкм. Температура колонки изменялась равномерно от 60 до 300°C в течение времени; гелий подавался со скоростью 8 мл/с.
Образец вводили в колонку автосемплером 7683В объемом 1 мкл. После разделения в колонке исследуемый образец поступал в ионизационную камеру масс-спектрометра. В камере, по мере поступления, молекулы разбиваются на осколки электронным ударом энергией 70 эВ, при температуре 250°C. Осколки, вытянутые из ионизационной камеры электростатическим полем, поступали в квадрупольный конденсатор, с помощью которого получали масс-спектры компонентов исследуемого образца.
Хроматограммы и масс-спектры обрабатывали с помощью программы MSDChemStationE02.00.493. Для идентификации веществ по масс-спектрам использовали базу данных масс-спектров NIST-8.
Метод получения наночастиц железа Fe2O3 впервые был опубликован в [5], затем он был унифицирован для процессов переработки твердого и тяжелого углеводородного сырья [6].
Смесь хлорида железа FeCl3 · 6H2O (“х. ч.”) (2.7 г, 10 ммоль) с олеатом натрия С17Н33СОONa (9.1 г, 30 ммоль) добавляли в приготовленную смесь, состоящую из гексана (35 мл), этанола (20 мл) и воды (15 мл), затем раствор нагревали в течение 4 ч при температуре 70°С и перемешивали. Верхний органический слой отделили от водной части, промыли 3 раза водой и получили красно-бурый водный раствор, состоящий из олеата железа. Смесь олеата железа (9 г, 10 ммоль), олеиновой кислоты С17Н33СОOH (1.4 г) и 1-октадецена (50 г), перемешивая, нагревали до температуры 100°С и выдерживали под вакуумом в течение 30 мин. Полученный раствор перемешивали и постепенно нагревали до 320°С, затем в течение 3 ч выдерживали в атмосфере инертного газа азота. Твердый раствор, содержащий наночастицы Fe3O4, охлаждали до комнатной температуры, добавляли избыточное количество этанола, 3 раза отмывали этанолом и подвергали центрифугированию. Полученные наночастицы железа Fe3O4 высушивали при температуре 60°С для дальнейшего использования в каталитических реакциях.
Расчеты значений кинетических констант скорости гидрогенизации широкой фракции с температурой кипения 230–300°С из каменноугольной смолы проводили методом “тяжелого шарика” [7–11].
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Выходы компонентов в гидрогенизате в зависимости от времени (от 20 до 60 мин) и температуры (от 380 до 420°С) в процессе гидрогенизации широкой фракции 230–300°С каменноугольной смолы в присутствии нанокатализатора Fe3O4 представлены на рис. 1.
Рис. 1.
Зависимость выхода продуктов от времени и температуры в процессе гидрогенизации широкой фракции 230–300°С каменноугольной смолы. Продукты реакции: фракция 230–300°С (а), смолы (б), асфальтены (в), масла (г), смесь ПАУ (д), твердые продукты (е). Расчетные значения выходов: 1 – при 380°С, 2 – при 400°С, 3 – при 420°С.
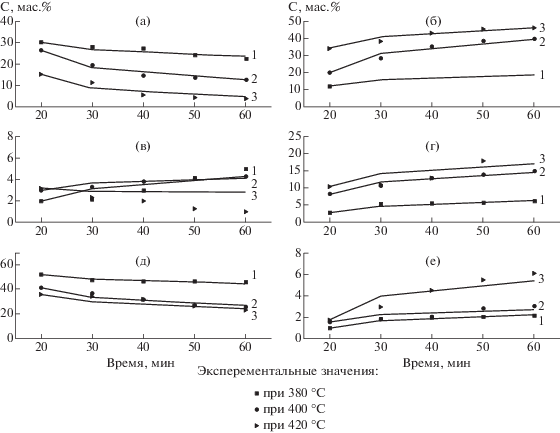
При изучении влияния времени и температуры на результаты гидрогенизации широкой фракции 230–300°С каменноугольной смолы под начальным давлением водорода 3.0 МПа было установлено, что стадия превращения фракции 230–300°С в различные компоненты возрастает с увеличением температуры и продолжительности опыта. Смеси ПАУ в широкой фракции 230–300°С реакционно-способные (рис. 1). Об этом свидетельствуют сравнительно глубокие превращения органических веществ во фракции 230–300°С в начальный период времени и при температуре 420°С. Наблюдается возрастание выхода масел с 10.4 до 20.1% и смол с 33.9 до 46% и уменьшение выхода смеси ПАУ с 35.8 до 23.2% и асфальтенов с 3.2 до 1% с увеличением времени при температуре 420°С. Наблюдается возрастание выхода масел с 6.1 до 20.1% и преасфальтенов с 18.7 до 46% и уменьшение выхода смеси ПАУ с 46 до 23.2% и асфальтенов с 5 до 1% с повышением температуры с 380 до 420°С.
Полученные результаты свидетельствуют об активности нанокатализатора Fe3O4 в заданном интервале времени и температуры на реакции гидрирования и гидрогенолиза смеси ПАУ в широкой фракции 230–300°С ПКС. Следует отметить, что нанокатализатор Fe3O4 в процессе гидрогенизации широкой фракции 230–300°С проявил наибольшую активность в реакциях гидрирования и гидрогенолиза.
На основе приведенных экспериментальных данных предложена схема гидрогенизации широкой фракции 230–300°С ПКС в присутствии нанокатализатора Fe3O4 (рис. 2).
Рис. 2.
Схема гидрогенизации широкой фракции 230–300°С каменноугольной смолы в присутствии нанокатализатора Fe3O4.
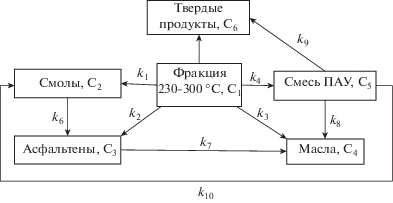
На основе кинетической схемы (рис. 2) была составлена кинетическая модель гидрогенизации широкой фракции 230–300°С каменноугольной смолы, которая представлена в виде системы дифференциальных уравнений:
Начальные условия решения системы дифференциальных уравнений: С1 = 100, С2 = С3 = С4 = = С5 = 0. Расчет системы дифференциальных уравнений проводили с использованием метода “тяжелого шарика”. Рассчитанные константы скорости приведены в табл. 1.
Таблица 1.
Рассчитанные константы скорости гидрогенизации широкой фракции 230–300°С каменноугольной смолы
| Константа скорости, мин–1 | Т, °С | ||
|---|---|---|---|
| 380 | 400 | 420 | |
| k1 | 0.001274 | 0.005316 | 0.005867 |
| k2 | 0.00079 | 0.001349 | 0.00008 |
| k3 | 0.000681 | 0.002357 | 0.004576 |
| k4 | 0.001076 | 0.002396 | 0.004615 |
| k5 | 0.00025 | 0.000741 | 0.004236 |
| k6 | 0.001441 | 0.000012 | 0.000339 |
| k7 | 0.001615 | 0.001857 | 0.007357 |
| k8 | 0.000786 | 0.001636 | 0.001619 |
| k9 | 0.000275 | 0.00018 | 0.000792 |
| k10 | 0.002024 | 0.006678 | 0.005192 |
Анализируя результаты констант скоростей, представленных в табл. 1, получили следующие ряды констант скоростей превращения широкой фракции в продукты гидрогенизации для температур 380°С (1), 400°С (2) и 420°С (3):
(1)
${{k}_{{10}}} > {{k}_{7}} > {{k}_{6}} > {{k}_{1}} > {{k}_{4}} > {{k}_{2}} \approx {{k}_{8}} > {{k}_{3}} > {{k}_{9}} > {{k}_{5}},$(2)
${{k}_{{10}}} > {{k}_{1}} > {{k}_{4}} > {{k}_{3}} > {{k}_{7}} > {{k}_{9}} > {{k}_{8}} > {{k}_{2}} > {{k}_{5}} > {{k}_{6}},$(3)
${{k}_{7}} > {{k}_{1}} > {{k}_{{10}}} > {{k}_{3}} > {{k}_{4}} > {{k}_{5}} > {{k}_{8}} > {{k}_{9}} > {{k}_{6}} > {{k}_{2}}.$Из приведенных данных видно, что лимитирующей скоростью гидрогенизации фракции 230–300°С каменноугольной смолы при 380°С является стадия превращения фракции 230–300°С в твердые продукты, при температуре 400°С лимитирующей стадией является превращение смол в асфальтены, при температуре 420°С – стадия превращения исходной фракции в асфальтены.
На рис. 1 приведены экспериментальные и расчетные выходы продуктов гидрогенизации широкой фракции при 380, 400 и 420°С и показано что с увеличением времени и температуры выход смеси ПАУ значительно уменьшается, а выход масел увеличивается. Эти параметры указывают на то, что процесс гидрогенизации фракции каменноугольной смолы оптимальный.
Выход асфальтенов с увеличением температуры и времени также увеличивается.
Константа скорости превращения смол в асфальтены (табл. 1) k6 уменьшается при увеличении температуры с 380 до 400°С; при 400°С конденсирование смол в асфальтены маловероятно. А при 420°С константа скорости превращения смол в асфальтены повышается, это объясняет тот факт, что увеличение температуры до 420°С приводит к образованию асфальтенов из смол.
Коэффициенты скорости для температур 380, 400 и 420°С процесса гидрогенизации широкой фракции каменноугольной смолы были рассчитаны с использованием уравнения первого порядка:
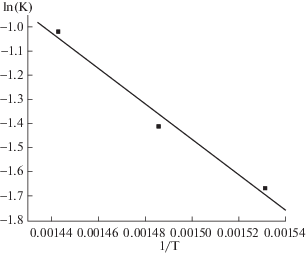
где KΣ – коэффициент скорости, зависящий от степени превращения фракции каменноугольной смолы в продукты реакции, мин–1; C0 – исходная концентрация широкой фракции каменноугольной смолы, доля ед.; C – концентрация непревращенной фракции каменноугольной смолы в интервале времени 20–60 мин, доля ед.; t – продолжительность процесса гидрогенизации, мин.На рис. 3 показана зависимость коэффициента скорости превращения фракции 230–300°С в продукты от обратной температуры и влияние температуры на коэффициент скорости гетерогенного процесса (по величине углового коэффициента можно судить о механизме гетерогенного процесса). Полученная величина энергии активации, равная 60.6 кДж/моль, показывает, что процесс превращения фракции 230–300°С в продукты реакции проходит в кинетической области гетерогенного процесса.
ЗАКЛЮЧЕНИЕ
В ходе проведенных кинетических исследований гидрогенизации широкой фракции 230–300°С каменноугольной смолы в присутствии наноразмерного катализатора Fe3O4 (в интервале температуры от 380 до 420°С и продолжительности времени от 10 до 60 мин) было установлено, что схема превращения широкой фракции 230–300°С каменноугольной смолы имеет пять стадий: смолы, асфальтены, масла, смесь ПАУ и твердые продукты. Рассчитаны константы скорости каждой стадии, суммарная константа скорости превращения широкой фракции в продукты реакции и энергию активации процесса гидрогенизации широкой фракции каменноугольной смолы. Установлено, что лимитирующей стадией процесса является превращение смол в асфальтены. Показано, что с помощью метода “тяжелого шарика” можно рассчитать систему дифференциальных уравнений, описывающих кинетику гидрогенизации широкой фракции каменноугольной смолы с расхождением расчетных и экспериментальных величин не более 2%. На основе кинетики образования продуктов из широкой фракции было установлено, что синтезированный нанокатализатор Fe3O4 в процессе гидрогенизации широкой фракции каменноугольной смолы проявляет наибольшую активность в реакциях образования масел.
Список литературы
Гюльмалиев А.М., Головин Г.С., Гладун Т.Г. Теоретические основы химии угля. М.: Издательство Московского государственного горного университета, 2003. 556 с.
Дмитриев Д.Е., Головко А.К. // Нефтехимия. 2010. Т. 50. № 2. С. 118.
Ма Фэн Юнь, Байкенов М.И., Жубанов К.А. // Вестн. КазНУ. 2009. № 3. С. 92.
Рыбак Б.М. Анализ нефти и нефтепродуктов. М.: Гостехиздат, 1962. 888 с.
Jongham P., Kwangjin A., Yosun H., Je-Geun P., Han-Jin N., Jae-Young K., Jae-Moon H., Taeghwan H. // Nature Materials. 2004. № 3. P. 891.
Yizhao Li, Fengyun Ma, Xintai Su, Chao Sun, Jianchao Liu, Zhiqiang Sun, Yanglong Hou // Catalysis Communications. 2012. № 26. P. 231.
Химмельблау Д. Прикладное нелинейное программирование. М.: Мир, 1975. 535 с.
Гилл Ф., Мюррей У. Численные методы условной оптимизации. М.: Мир, 1977. 296 с.
Бояринов A.И., Кафарова B.B. Методы оптимизации в химической технологии. M.: Химия, 1969. 568 с.
Аоки М. Введение в методы оптимизации: Основы и приложения нелинейного программирования. М.: Наука, 1977. 343 с.
Алексеева Е.В., Кутненко О.А., Плясунов А.В. Численные методы оптимизации. Новосибирск: Новосибирский гос. ун-т., 2008. 128 с. URL. http://www.math.nsc.ru/LBRT/k5/Plyasunov/Posobie3.pdf (дата обращения 10.04.2019).
Дополнительные материалы отсутствуют.
Инструменты
Химия твердого топлива