Химия твердого топлива, 2020, № 5, стр. 3-9
ХАРАКТЕРИСТИКА ГУМИНОВЫХ КИСЛОТ В СИСТЕМЕ ГЕОХИМИЧЕСКИ СОПРЯЖЕННЫХ БОЛОТНЫХ ЛАНДШАФТОВ
А. В. Савельева 1, *, Н. В. Юдина 1, **, Л. И. Инишева 2, ***
1 ФГБУН Институт химии нефти СО РАН
634055 Томск, Россия
2 ФГБОУ ВО Томский государственный педагогический университет
634061 Томск, Россия
* E-mail: anna@ipc.tsc.ru
** E-mail: natal@ipc.tsc.ru
*** E-mail: inisheva@mail.ru
Поступила в редакцию 20.02.2020
После доработки 25.03.2020
Принята к публикации 03.06.2020
Аннотация
Исследованы элементный и структурно-групповой составы и парамагнитные свойства гуминовых кислот торфов, залегающих на разной глубине торфяных залежей различного генезиса. С понижением глубины залегания торфов выделенные гуминовые кислоты характеризуются уменьшением отношения Н/С, количества карбоксильных и метиленовых групп, возрастанием интенсивности сигнала органических парамагнитных центров (ПМЦ), что свидетельствует об усилении структуры ароматического сопряжения. Изменение в гуминовых кислотах торфов по глубине залежи количества ПМЦ находится в прямой зависимости от содержания Fe3+.
ВВЕДЕНИЕ
Состав гуминовых кислот (ГК) определяется средой обитания растений, содержанием минеральных элементов питания, геологическими условиями залегания отложений. Гуминовые вещества представляют собой нерегулярные сополимеры ароматических оксиполикарбоновых кислот, включающие карбоксильные, гидроксильные, метоксильные группы [1–4]. Благодаря такому строению ГК обладают поверхностно-активными свойствами и способностью образовывать водорастворимые комплексы с ионами металлов, что приводит к миграции и перераспределению органических и минеральных соединений в геохимически сопряженных ландшафтах [5, 6].
В работе [7] показано влияние биохимических процессов в деятельном и инертном горизонтах торфяных залежей в бассейне р. Ключ на северо-восточных отрогах Васюганского болота. Соподчиненность ландшафтов в данном речном бассейне способствует миграции водорастворимых веществ внутриболотного стока в сторону трансаккумулятивной части профиля, что, в свою очередь, отражается на формировании химического состава стока веществ и на процессе гумификации.
Развитие Васюганского болота на исследуемой территории начиналось с эвтрофной стадии с господством древесно-травяной растительной ассоциации. В настоящее время большая часть торфяной залежи перешла в олиготрофную стадию развития, мощность верхового торфа на самом высоком ландшафте достигает 120 см. Минеральное ложе болот сложено карбонатными суглинками, что привело к формированию торфов, обогащенных минеральными (в том числе кальцием и железом) соединениями.
Геохимически сопряженные ландшафты представлены по направлению к центру болота следующими биогеоценозами: осоково-сфагновым (торфяная залежь Т1) и сосново-кустарничково-сфагновым (торфяные залежи Т2 и Т3).
Целью данного исследования является характеристика ГК в торфяных залежах геохимически сопряженных ландшафтов в бассейне р. Ключ на северо-восточных отрогах Васюганского болота.
МЕТОДЫ ИССЛЕДОВАНИЯ
Гуминовые вещества выделяли из остатка торфа после удаления водорастворимых и легкогидролизуемых компонентов, обрабатывая его 0.1 н. раствором NаОН при температуре 80°С из расчета 150 мл раствора на 1 г навески. Щелочную экстракцию повторяли трижды при постоянном перемешивании на механической мешалке в течение 2 ч, экстракты объединяли, щелочной раствор обрабатывали 4%-ной НСl для выделения гуминовых кислот.
Содержание железа и кальция в торфах и ГК определяли рентгено-флуоресцентным методом. Элементный состав ГК анализировали на С,Н,N-анализаторе Carlo Erba Strumentazione (модель 1106, Италия).
Регистрацию ИК-спектров ГК проводили на ИК-фурье-спектрометре Nikolet 5700 c Raman модулем (корпорация ThermoElectron, США) в таблетках с KBr при соотношении 1:300 соответственно в интервале значений частоты от 400 до 4000 см–1 c компенсацией сигналов адсорбированной воды. Для количественной оценки интенсивности полос поглощения применен метод базовых линий и относительных оптических плотностей полос поглощения (D) с использованием компьютерной программы [8]. Содержание структурных групп рассчитывали в виде отношения значений оптической плотности в максимуме характеристической полосы поглощения (п.п.) и реперной п.п 1465 см–1.
Методом гель-хроматографического разделения на сефадексе G–75 были получены кривые молекулярно-массового распределения ГК, из которых были рассчитаны средневесовые молекулярные массы. Исходную навеску ГК массой 10 мг растворяли в 2 мл раствора NaOН (0.02 н.) и доводили раствор до 10 мл мочевиной. В качестве элюирующего агента использовали 4 М раствор мочевины, исключающей адсорбцию ГК на геле. Оптическую плотность водных растворов ГК регистрировали на спектрофотометре UNICO spectropotometer 2800 UV/VIS, США при длине волны 465 и 665 нм, при которых не проявляются примеси неспецифических соединений [9].
Содержания парамагнитных центров определяли на приборе EPR spectrometer SE/X-2544 марки Radipan (Польша). В качестве эталона использовали Mg+2 в MgO при атмосферном давлении и комнатной температуре. Эталон не изменяет своих параметров с течением времени и имеет стабильное значение количества ПМЦ [10].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Верховые торфа изучаемых торфяных залежей являются малозольными (2.1–6.0%); переходные и низинные торфа – нормально зольными (до 9.8%). В торфах, залегающих на подстилающих грунтах (Т1 и Т2), зольность достигает 24.5% (табл. 1). Преобладающими минеральными элементами во всех торфах являются железо и кальций, что объясняется повышенным содержанием этих элементов в подстилающих породах, представленных глинами с включением ракушек. Уровни накопления и закономерности распределения соединений железа в торфах зависят от целого ряда факторов, влияющих на условия торфонакопления. Содержание железа варьирует по глубине торфяных залежей в зависимости от зольности торфа. Обогащены соединениями железа придонные слои торфа. Для торфяной залежи Т1 отмечается более высокое содержание железа в приповерхностном слое относительно нижележащего. Низким содержанием железа и кальция характеризуются верховые торфа залежи Т2. Содержание кальция возрастает в торфах залежи Т3. Известно, что кальций – регулятор кислотности почвенной среды, понижает кислотность болотных вод, способствует образованию нерастворимых соединений железа. Образцы торфов заметно различаются между собой по значениям рН и степени разложения в зависимости от генезиса и глубины залегания.
Таблица 1.
Характеристика торфов
| № | Глубина, см | Вид торфа* | рН | R, мас. % | А, мас.% | Содержание, мас. % на торф | ||
|---|---|---|---|---|---|---|---|---|
| ГК | Fe | Ca | ||||||
| Залежь Т1 | ||||||||
| 1 | 0–50 | Сфагновый мочажинный В | 4.0 | 10–15 | 10.9 | 30.5 | 2.0 | 1.4 |
| 2 | 50–100 | Сфагновый мочажинный В | 4.5 | 20 | 6.0 | 33.0 | 1.5 | 2.4 |
| 3 | 100–150 | Осоково-сфагновый П | 5.5 | 35 | 4.7 | 28.0 | 1.2 | 1.1 |
| 4 | 150–200 | Осоковый П | 5.5 | 50–55 | 4.8 | 29.2 | 1.4 | 1.9 |
| 5 | 200–250 | Осоковый Н | 5.5 | 50 | 5.8 | 46.6 | 1.8 | 2.8 |
| 6 | 250–270 | Папоротниковый Н | 5.5 | 50–55 | 24.5 | 45.9 | 2.7 | 4.4 |
| Залежь Т2 | ||||||||
| 7 | 0–50 | Фускум-торф В | 3.5 | 0–5 | 2.7 | 25.1 | 0.9 | 0.5 |
| 8 | 50–75 | Фускум-тофр В | 3.5 | 0–5 | 2.0 | 25.2 | 0.3 | 1.0 |
| 9 | 75–100 | Магелланикум-торф В | 4.0 | 0–5 | 2.1 | 19.8 | 0.6 | 0.9 |
| 10 | 100–150 | Магелланикум-торф В | 4.2 | 10 | 2.3 | 19.0 | 0.6 | 1.0 |
| 11 | 150–200 | Сосново-пушицевый В | 6.0 | 50–55 | 6.0 | 37.1 | 1.2 | 2.4 |
| 12 | 200–250 | Осоковый Н | 6.0 | 50–55 | 4.3 | 25.2 | 1.3 | 2.3 |
| 13 | 250–300 | Осоковый Н | 6.0 | 40–45 | 24.5 | 21.2 | 2.7 | 3.8 |
| Залежь Т3 | ||||||||
| 14 | 0–25 | Сосново-пушицевый В | 2.6 | 45–50 | 5.2 | 27.6 | 1.0 | 2.5 |
| 15 | 25–50 | Древесно-пушицевый П | 3.5 | 45–50 | 6.5 | 22.7 | 1.3 | 3.4 |
| 16 | 50–75 | Древесно-пушицевый П | 5.5 | 55–60 | 8.0 | 23.0 | 1.8 | 4.2 |
| 17 | 75–100 | Древесно-пушицевый П | 5.5 | 55–60 | 9.8 | 39.8 | 2.0 | 4.2 |
Высокая кислотность верховых малоразложившихся сфагновых торфов связана с недостаточной насыщенностью поглощающего комплекса. Степень разложения торфов залежи Т3, представленных сосново-пушицевым и древесно-пушицевым видами, составляет 45–60 мас. %. Торфа залежей Т1 и Т2, залегающие на глубине 150–300 см, также характеризуются высокой степенью разложения 50–55 мас. %.
Содержание ГК в торфах залежи Т1 выше, чем в торфах залежей Т2 и Т3 и составляет 28.0–46.6 мас. %. Это связано с показателями микробиологической активности. Запасы микробной биомассы в залежи Т1 в 4 раза выше, чем в залежи Т2, а соотношение численности актиномицетов и микроорганизмов, использующих минеральные формы азота (КАА – крахмал-аммиачный агар) к численности микроорганизмов, использующих органические формы азота (МПА – мясопептонный агар) КАА/МПА составляет 0.1–0.5, что свидетельствует о преобладании процессов гумификации [7].
В табл. 2 приведены результаты анализа элементного состава выделенных из торфов ГК. Для всех изученных ГК в элементном составе отмечается повышенное содержание углерода, что характерно для торфов Западной Сибири [11]. Атомные отношения Н/С отражают содержание полиненасыщенных фрагментов в ГК [12]. Более низкие значения Н/С наблюдаются для образцов ГК торфов залежи Т1, что свидетельствует о высоком вкладе полиненасыщенных фрагментов в структуру макромолекул. С увеличением глубины залегания торфов в данной залежи независимо от их ботанического состава и степени разложения отношение Н/С в ГК снижается. Для ГК малоразложившихся верховых сфагновых торфов залежи Т2 отмечаются высокие значения отношений Н/С и соответственно низкая степень ароматичности макромолекул.
Таблица 2.
Элементный состав гуминовых кислот
| Номер образца* | ММ1/ММ2, кДа | Элементный состав, % на daf | Атомное отношение | |||||
|---|---|---|---|---|---|---|---|---|
| С | Н | N | О | H/C | O/C | С/N | ||
| Залежь Т1 | ||||||||
| 1 | 29.1/11.0 | 58.2 | 5.7 | 2.0 | 34.0 | 1.18 | 0.43 | 34.0 |
| 2 | 28.8/6.1 | 59.3 | 5.2 | 1.6 | 34.2 | 1.05 | 0.44 | 43.3 |
| 3 | 27.9/5.4 | 58.7 | 4.8 | 1.5 | 34.9 | 0.99 | 0.44 | 45.8 |
| 4 | 11.3/22.5 | 57.9 | 4.7 | 1.8 | 35.0 | 0.98 | 0.45 | 37.6 |
| 5 | 12.0/21.4 | 57.0 | 4.5 | 2.6 | 35.8 | 0.95 | 0.46 | 25.6 |
| 6 | 15.6/31.3 | 56.4 | 4.3 | 2.4 | 36.8 | 0.91 | 0.49 | 27.5 |
| Залежь Т2 | ||||||||
| 7 | 12.6/11/5 | 53.7 | 5.5 | 2.1 | 35.3 | 1.23 | 0.49 | 29.9 |
| 8 | 13.5/10.3 | 54.6 | 6.0 | 2.1 | 33.9 | 1.32 | 0.46 | 30.4 |
| 9 | 11.8/9.4 | 58.5 | 5.8 | 1.9 | 33.8 | 1.19 | 0.43 | 36.0 |
| 10 | 13.3/12.1 | 58.1 | 5.5 | 2.5 | 34.2 | 1.14 | 0.44 | 27.2 |
| 11 | 11.3/24.5 | 59.2 | 4.8 | 1.9 | 34.1 | 0.97 | 0.43 | 36.4 |
| 12 | 10.1/22.0 | 57.4 | 4.8 | 2.4 | 35.6 | 1.00 | 0.46 | 28.0 |
| 13 | 9.3/21.1 | 57.8 | 5.2 | 1.9 | 35.9 | 1.07 | 0.46 | 35.6 |
| Залежь Т3 | ||||||||
| 14 | 15.1/43.5 | 57.7 | 5.5 | 1.8 | 34.9 | 1.14 | 0.45 | 37.2 |
| 15 | 10.1/30.4 | 56.0 | 5.2 | 2.9 | 35.8 | 1.11 | 0.48 | 22.4 |
| 16 | 9.9/23.3 | 56.7 | 5.4 | 2.7 | 35.2 | 1.14 | 0.47 | 24.4 |
| 17 | 9.9/22.3 | 57.8 | 4.7 | 2.4 | 34.9 | 0.97 | 0.45 | 27.9 |
* Номер образца – в соответствии с табл. 1.
Содержание кислорода и отношение О/С варьируют довольно в узких пределах. Кислород входит как в состав каркасной, так и в состав периферийной части макромолекулы. В последнем случае он сконцентрирован преимущественно в углеводных фрагментах [13]. Содержание кислорода в структуре ГК торфов увеличивается с глубиной залежи Т1.
Содержание азота в элементном составе ГК определяется ботаническим составом торфов и расположением на ландшафтном профиле. Наиболее богаты азотом низинные травяные торфа в залежи Т1. В торфах залежи Т2 содержание азота колеблется по глубине залежи в пределах 1.9–2.5 мас. %. Многие исследователи считают, что основные колебания в содержании азота происходят в деятельном торфогенном слое за счет микробиальной деятельности. В ГК древесно-пушицевых торфов залежи Т3 отмечается самое высокое содержание азота.
Фундаментальными свойствами ГК являются нерегулярность строения, нестехиометричность состава и полидисперсность, поэтому ГК характеризуют молекулярно-массовым распределением (ММР), на основании которого рассчитывают молекулярную массу (ММ). Молекулярная масса высокомолекулярной фракции ММ1 и низкомолекулярной фракции ММ2 приведена в табл. 2. Анализ кривых ММР позволил выделить две группы ГК. К первой группе были отнесены ГК древесно-пушицевого, осокового, травяного, папоротникового видов торфа, в ботаническом составе которых преобладают травянистые торфообразователи. Для них характерно преобладание высокомолекулярной фракции. Соотношение ММ1:ММ2 высокомолекулярной и низкомолекулярной фракций составляет примерно 1 : 3 (табл. 2). В области низкомолекулярной фракции наблюдается проявление наибольшей дисперсности. Во вторую группу входят ГК фускум-торфа, магелланикум-торфа, сфагнового мочажинного и осоково-сфагнового видов. Кривые молекулярно-массового распределения второй группы имеют два ярко выраженных максимума. В торфах залежи Т1 высокомолекулярная фракция ГК характеризуется большими значениями ММ, коррелирующими с отношением Н/С. В верховых торфах залежи Т2 обе фракции ГК имеют близкие значения. В залежах Т2 и Т3 отмечается снижение молекулярной массы фракций ГК с глубиной залегания торфов.
Известно, что связь между глубиной залегания и химической структурой ГК более четко проявляется только для образцов торфов с близким ботаническим составом и степенью разложения [14], хотя в ряде работ [15, 16] показано увеличение содержания гуминовых веществ в торфах разного генезиса с глубиной залегания, снижение в них отношения Н/С, карбоксильных групп. Для установления зависимости структурных параметров ГК по глубине залежи рассчитаны спектральные коэффициенты. Степень ароматичности структуры ГК оценивали по отношению значений оптических плотностей характеристических полос поглощения (п.п.) D1610/D1465, распределение метиленовых групп (СН2–) – D2920/D1465, содержание СО- в кислотах – D1720/D1465.
На рис. 1 приведены зависимости структурных параметров ГК в виде отношений оптических плотностей при характеристических п.п. D2920/D1465, D1610/D1465, D1720/D1465 от глубины залегания торфов в залежах Т1, Т2, Т3. В структуре ГК наблюдалось снижение содержания метиленовых групп (D2920/D1465R = 0.80–0.95) и карбоксильных групп (D1720/D1465R = 0.80–0.95) во всех образцах торфов с увеличением глубины их залегания, что может быть связано с протеканием процессов деалкилирования и декарбоксилирования под действием ферментов и микроорганизмов (рис. 1, а, б).
Рис. 1.
Зависимость структурных параметров ГК D2920/D1465 (а), D1610/D1465 (б), D1720/D1465 (в) от глубины залегания торфов в залежах Т1 – 1, Т2 – 2, Т3 – 3.
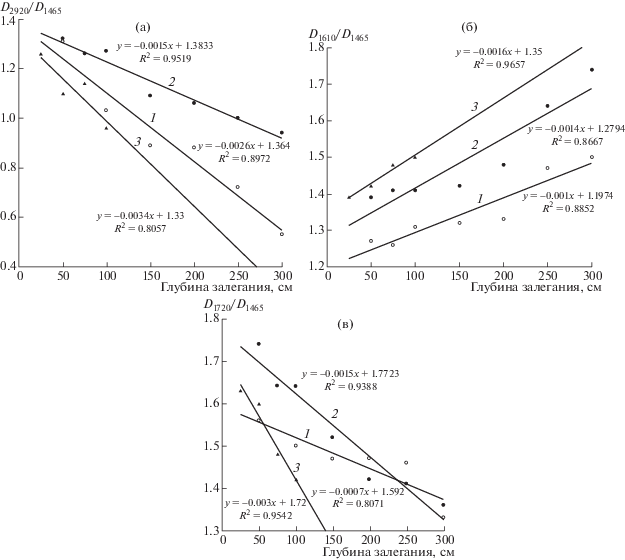
Ароматичность структуры ГК (D1610/D1465), напротив, возрастает с глубиной залегания торфов. Об этом свидетельствуют данные элементного состава ГК, атомные отношения Н/С уменьшаются с глубиной залегания торфов (рис. 1, в; табл. 2).
Присутствие в составе ГК свободных радикалов, обусловливающих парамагнитную активность, многие авторы считают неотъемлемым их свойством, которое непосредственно связано со структурными особенностями [17–20]. Свободные радикалы ГК принимают непосредственное участие в процессе полимеризации как структурные единицы. Уровень парамагнитных центров (ПМЦ) в ГК определяется содержанием ароматических структур и особенностями межмолекулярного взаимодействия. По мнению авторов [18], синергический эффект взаимодействия полисопряженных ароматических систем и водородных связей, формируемых функциональными группами, перекрывает низкое содержание ароматических структур и обеспечивает высокий уровень парамагнетизма. К этому следует добавить возможное влияние внутримолекулярного взаимодействия функциональных групп.
Спектры ПМР для образцов изученных ГК торфов идентичны, в них регистрируется три типа сигналов с g-фактором свободного электрона g ∼ 2.00 и g ∼ 2.11 и g ∼ 4.3, обусловленные присутствием катиона железа [21, 23 ] . Сигнал с g ∼ 4.3 отвечает ионным формам Fe3+, связанным, скорее всего, с карбоксильными группами, значительная часть которых принадлежит ароматическим фрагментам, а сигнал с g ∼ 2.11 принадлежит соединениям Fe3+ с ковалентным характером связи с органическим веществом торфа и минеральным соединениям железа. Ширина сигнала g ∼ 4 составляет 70–100 Гс. Для Fe3+ ковалентной формы отмечено возрастание ширины сигнала до значений 500–550 Гс. Однотипность спектров ЭПР и близкое содержание ПМЦ в ГК (2.7–6.6 ⋅ ⋅ 1017 сп/г) характеризуют их как структуры с подобной системой полисопряжения.
С целью установления роли парамагнитного железа в структуре ГК было проведено выделение ГК различными способами. В первом случае выделяли трехкратной обработкой торфа 0.1 н. раствором NaOH (ГК1), во втором – выделенные ГК1 обрабатывали 4%-ной HCl в течение двух часов на водяной бане – ГК2. В ЭПР-спектрах деминерализованных образцов ГК2 практически исчезает сигнал Fe3+ с g ∼ 4 и снизилась до следовых количеств интенсивность сигнала в ковалентной форме. При этом количество ПМЦ уменьшилось, за исключением ГК2, выделенного из торфа с глубины 250 см. Отмеченная особенность, очевидно, связана с тем, что эти торфа близко расположены к подстилающим грунтам, что существенно влияет на структуру ГК2. Возрастание концентрации ПМЦ в этих образцах, как правило, происходит за счет сорбции непарамагнитных поливалентных ионов металлов, приводящих к более жестким молекулярным структурам, вследствие образования мостиковых связей-сшивок между полисопряженными фрагментами [22].
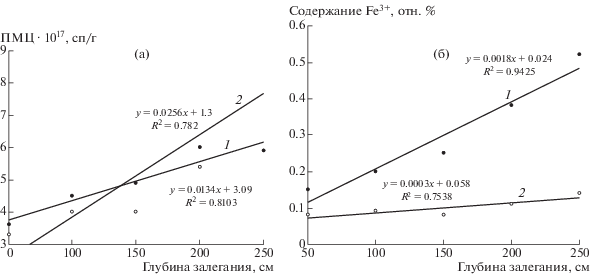
На рис. 2 показано изменение содержания ПМЦ и ионов железа в ГК1 и ГК2 в зависимости от глубины залегания торфов. Сравнительный анализ содержания ПМЦ в ГК1 и ГК2 показал незначительное увеличение с глубиной залегания торфов (рис. 2, а). При этом содержание железа в ГК1 возрастает в 4 раза (рис. 2, б). Снижение концентрации ПМЦ в образцах ГК2 может объясняться гибелью органических радикалов при их взаимодействии с минеральными кислотами.
Рис. 2.
Содержание ПМЦ (а) и ионов железа (б) в ГК1 – 1, ГК2 – 2 торфов в зависимости от глубины залегания в залежи Т2.
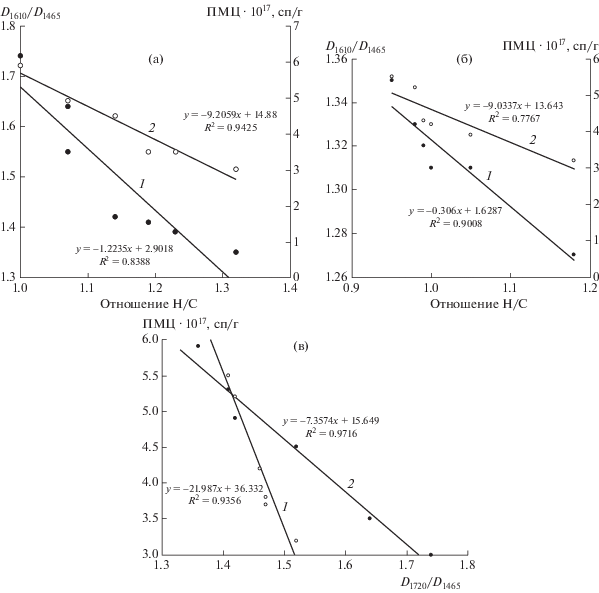
Взаимосвязь параметров, отражающих степень ароматического полисопряжения в структуре ГК торфов залежей Т1 и Т2, приведена на рис. 3, а, б. С увеличением отношения Н/С значения степени ароматичности, оцениваемой отношением спектральных коэффициентов D1610/D1465, и содержание ПМЦ снижаются в структурах ГК. Для ГК торфов залежей Т1 и Т2 характерно снижение содержания ПМЦ с увеличением количества карбоксильных групп (рис. 3, в).
ВЫВОДЫ
Гуминовые кислоты с понижением глубины залегания торфов, независимо от их ботанического состава и степени разложения, характеризуются снижением отношения Н/С, повышением степени ароматичности структуры, уменьшением количества карбоксильных и метиленовых групп, что связано с процессами декарбоксилирования и деалкилирования в анаэробных условиях.
Гуминовые кислоты, выделенные из древесно-травянистых видов торфов с высокой степенью разложения, отличаются от ГК из сфагновых видов более высокой полидисперсностью и преобладанием в молекулярно-массовом распределении низкомолекулярной фракции.
С увеличением глубины залегания торфов интенсивность сигнала органических ПМЦ в ГК незначительно возрастает при одновременном повышении в них содержания Fe3+. Исчезновение сигнала Fe3+ в ЭПР спектрах и снижение его количества в ГК приводит к уменьшению содержания органических ПМЦ.
Содержание ПМЦ в ГК торфов снижается при повышении отношения Н/С, количества карбоксильных групп и уменьшения степени ароматичности, что объясняется усилением структуры ароматического сопряжения.
Список литературы
Piccolo A. // Soil Sci. 2001. V. 166. № 11. P. 810.
Орлов Д.С. Химия почв. М.: Изд-во МГУ, 1992. 259 с.
Sutton R., Sposito G. // Environ. Sci. Technol. 2005. V. 39. № 23. P. 9009.
Sorkina T.A., Polyakov A.Yu., Kulikova N.A. // J. Soils and Sediments. 2014. V. 14. № 2. P. 261.
Monteil Rivera F., Dumonceau G. // J. Anal. Bioanal. Chem. 2002. V. 374. № 6. P. 1105.
Nakashima K., Xing S., Gong Y., Miyajima T. // J. Mol. Struct. 2008. V. 883–884. P. 155. https://doi.org/10.1016/j.molstruc.2007.11.027
Инишева Л.И., Юдина Н.В., Инишев Н.Г., Головченко А.В. // Геохимия. 2005. № 2. С. 197. [Geochemistry International, 2005, vol. 43, no. 2, p. 168.]
Summers R.S., Cornel P.K., Summers R.S., Roberts P.V. // Sci. Total Environ. 1987. V. 62. P. 27.
Орлов Д.С., Гришина Л.А. Практикум по химии гумуса. М.: Изд-во МГУ, 1981. 272 с.
Чуков С.Н. Структурно-функциональные параметры органического вещества почв в условиях антропогенного воздействия. СПб: Наука, 2001. 214 с.
Матухина В.Г., Грирорьева Г.Р., Алтухов В.М. // Геология и геофизика. 1985. № 1. С. 27.
Rice J.A., MacCarthy P. // Org. Geochem.1991. V. 17. № 5. P. 635.
Wershaw R.L., Mikita M.A., Steelink C. // Environ. Sci. Technol. 1981. V. 15. P. 1461.
Марыганова В.В., Бамбалов Н.Н., Стригуцкий В.П., Пармон С.В. // ХТТ. 2013. № 3. С. 19. [Solid Fuel Chemistry, 2013, vol. 47, no. 3, p. 153. https://doi.org/10.3103/S0361521913030051]https://doi.org/10.7868/S0023117713030055
Deport C., Lemee L., Ambles A. // Org. Geochem. 2006. V. 37. № 6. P. 649.
Gondar D., Lopez R., Fiol S., Antelo J.M., Arce F. // Geoderma. 2005. V. 126. № 3–4. P. 367.
Стригуцкий В.П., Бамбалов Н.Н., Прохоров С.Г. // ХТТ. 1996. № 6. С. 29. [SolidFuelChemistry, 1996, vol. 30, no. 6, p. 29.]
Лиштван И.И., Цыганов А.П., Томсон А.Э., Стригуцкий В.П., Соколова Т.В., Пехтерева В.С., Прохоров С.Г., Селянина С.Б., Труфанова М.Ф. // ХТТ. 2017. № 5. С. 34. [Solid Fuel Chemistry, 2017, vol. 51, no 5, p. 296. https://doi.org/10.3103/S0361521917050093]https://doi.org/10.7868/S002311771705005X
Алиев С.А. Азотфиксация и физиологическая активность органического вещества почв. Новосибирск: Наука СО РАН, 1988. 145 с.
Чуков С.Н., Талашкина В.Д., Надпорожская М.А. // Почвоведение. 1995. № 2. С. 169.
Лиштван И.И., Стригуцкий В.П., Якута Ю.Г., Абрамец А.М., Алейникова В.Н., Першай Н.С. // ХТТ. 2017. № 5. С. 39. [Solid Fuel Chemistry, 2017, vol. 51, no. 5, p. 301. DOI: 10.3103/S036152191705010X]https://doi.org/10.7868/S0023117717050061
Цыганов А.Р., Томсон А.Э., Боголицын К.Г., Соколова Т.В., Стригуцкий В.П., Пехтерева В.С., Селянина С.Б., Парфенова Л.Н., Труфанова М.В. // Фундаментальные исследования. 2013. № 4–2. С. 345. http://fundamental-research.ru/ru/article/view?id=31195
Дополнительные материалы отсутствуют.
Инструменты
Химия твердого топлива