Кинетика и катализ, 2020, T. 61, № 3, стр. 385-409
Каталитическая коррозия платиноидных сеток при окислении аммиака воздухом. Коррозия поверхности фронтальной стороны платиноидной сетки в ходе окисления NH3 при 1133 К
А. Н. Саланов a, *, Е. А. Супрун a, А. Н. Серкова a, Н. М. Чеснокова a, Е. Ф. Сутормина a, Л. А. Исупова a, В. Н. Пармон a
a ФГБУН ФИЦ Институт катализа им. Г.К. Борескова СО РАН
630090 Новосибирск, просп. Акад. Лаврентьева, 5, Россия
* E-mail: salanov@catalysis.ru
Поступила в редакцию 17.07.2019
После доработки 30.10.2019
Принята к публикации 18.11.2019
Аннотация
Методами растровой электронной микроскопии и энергодисперсионной рентгеновской спектроскопии исследованы морфология, микроструктура и химический состав поверхности и приповерхностных слоев поликристаллической проволоки промышленной платиноидной сетки с составом Pt (81 мас. %), Pd (15 мас. %), Rh (3.5 мас. %) и Ru (0.5 мас. %). После окисления NH3 воздухом при Т = 1133 К и давлении 3.6 бар в течение 50 ч на фронтальной стороне сетки обнаружен сплошной шероховатый слой из агломератов типа “cauliflowers”, формирующихся в ходе каталитической коррозии. На поверхности фрагментов проволоки размером 100–150 мкм с гладкой микрозернистой структурой зарегистрированы ямки травления нанометрового размера в концентрации 1.0 × 108–6.0 × 108 см–2, которые могут являться центрами коррозии типа “горячие точки” (“hotspots”). Рост ямок травления и формирование кристаллических террас на поверхности зерен обусловлены поверхностной диффузией атомов металла. Сплошной коррозионный слой включает пористые кристаллические агломераты (“cauliflowers”) с линейным размером от 3 до 18 мкм (средний размер около 10 мкм) в концентрации 4.9 × 105 см–2. На поверхности агломератов зарегистрированы поры с диаметром от 0.1 до 1.7 мкм в концентрации 1.3 × 107 см–2. Удельная поверхность платиноидной сетки, рассчитанная из микроскопических изображений с учетом поверхности агломератов и пор, составляет величину около 260 см2/г. В процессе высоко экзотермического окисления NH3 кислородом на поверхности агломератов с низкой концентрацией дефектов и в поровых пустотах шириной 5–15 мкм и глубиной до 10 мкм с повышенной удельной поверхностью и концентрацией дефектов образующиеся на “горячих” участках дна поровых пустот пары летучих оксидов и металлов могут конденсироваться на выше расположенных “холодных” участках поверхности агломератов и монокристаллов. Протекание этих процессов формирует сплошной коррозионный слой из пористых кристаллических агломератов, массивных монокристаллов и глубоких поровых пустот. Образующийся коррозионный слой существенно увеличивает удельную поверхность катализатора, что приводит к росту объемной скорости окисления NH3, ускоряющей коррозионный процесс.
ВВЕДЕНИЕ
Высокотемпературное окисление аммиака кислородом воздуха на платиноидных сетках с преимущественным содержанием платины по сильно экзотермической реакции
Реакция окисления NH3 кислородом воздуха на платиновой черни с образованием оксидов азота была открыта в 1838 г. [3]. В 1906 г. с использованием платиновой фольги весом 50 г было организовано первое промышленное производство HNO3 в количестве около 300 кг в сутки [2]. В 1909 г. для этой же цели были предложены сетки из платиновой проволоки диаметром 0.06 мм [4]. С 1911 г. и по сегодняшний день такие сетки применяют в химической промышленности для производства азотной кислоты. В настоящее время в промышленном окислении NH3 кислородом воздуха используют пакеты, включающие от 3 до 45 сеток диаметром от 3 до 5 м и изготовленные чаще всего из проволоки диаметром 0.06–0.09 мм из сплавов Pt–Rh или Pt–Rh–Pd [2]. Количество применяемых сеток зависит от условий проведения процесса, в основном от величин давления реагентов (1–6 бар), температуры катализатора (1083–1163 К) и концентрации NH3 в воздухе (11–12 об. %). В этих условиях сетки могут работать без замены от 4 до 12 мес. После загрузки сеток в реактор в самом начале процесса (в течение нескольких часов) регистрируется рост активности катализатора, сопровождающийся глубокой структурной перестройкой поверхностного слоя проволоки сеток, которая характеризуется образованием фасеток, кристаллов и крупных агломератов, формирующих поверхностный шероховатый слой. В ходе окисления аммиака при высоких температурах и давлениях регистрируются унос платины в количестве 50–100 мг и более на 1 т произведенной HNO3 и постепенное снижение активности катализатора, а также механическая деградация сеток [1, 2]. Первые изображения шероховатого поверхностного слоя, формирующегося на платиновых сетках в ходе окисления аммиака, приведены в работах [5, 6]. Для описания структурной перестройки поверхности металлического катализатора, инициированной протеканием каталитических реакций окисления Н2 и NH3 на поликристаллических палладии и платине, был использован термин “каталитическая коррозия” [7–9].
На реконструкцию поверхностного слоя Pt, Rh, Pd, Ag, Ir и сплавов Pt–Rh, Pt–Ir, Pd–Ni существенное влияние оказывает состав реакционной смеси, температура и состав катализатора [9–22]. В работах [10, 11] было изучено влияние обработок в О2, N2O, NO и др. образцов Pt, Rh и сплавов Pt–Rh при температурах 973–1473 К на морфологию и унос металлов. Так, в [10] исследовали морфологию поверхности проволок, изготовленных из Pt, Rh и сплава Pt/10–30 мас. % Rh после обработки потоками О2, N2O и NO, направленными перпендикулярно к проволоке, при температурах 1173–1473 К, которые измеряли оптическим пирометром. В таких условиях температура в центре проволоки всегда была выше, чем на концах. После обработки платиновой проволоки в О2 (${{P}_{{{{{\text{O}}}_{{\text{2}}}}}}}$ ≈ 1 бар) в течение 72 ч при 1173 К на поверхности проволоки выявлены межзеренные границы, фасетки, ямки травления и небольшие кристаллы. Ямки травления оказались сосредоточенными в основном в центральной части проволоки, где температура была максимальной (~1173 К), в то время как кристаллы группировались на концах проволоки, где температура была минимальной (≤973 К). Кроме того, было отмечено, что ямки травления располагаются преимущественно в центральной части поверхности зерен, тогда как кристаллы – рядом с межзеренными границами. Количество кристаллов оказалось больше на тыльной относительно газового потока стороне проволоки по сравнению с фронтальной, по-видимому, вследствие неравномерности состава и скорости газового потока, обдувающего платиновую проволоку. Для родийсодержащих сплавов было обнаружено обогащение поверхности родием и появление кристаллов Rh2O3. Влияние реагентов на степень реконструкции поверхности Pt, Rh и сплава Pt/10–30 мас. % Rh располагается в ряду: влажный О2 > N2O > сухой О2 > NO. Повышение температуры проволок до 1473 К существенно ускоряет перестройку поверхности.
В работе [11] был зафиксирован перенос Pt и Rh при обработке чистых металлов и сплавов Pt/5–80 мас. % Rh в различных средах в запаянной кварцевой ампуле диаметром 7 мм и длиной 100 мм из одного конца, находящегося при Т = 1173 К, в другой с Т = 1073 К. За 365 дней для чистой платины перенос составил 193 мкг в О2 и 43, 1 и 3 мкг в воздухе, в парах Н2О и в вакууме соответственно, для чистого родия в этих же условиях – 2, 4, 6 и 2 мкг соответственно. Для сплавов Pt/5–80 мас. % Rh этот показатель возрастал с уменьшением содержания Rh в сплаве и с увеличением парциального давления О2 в газовой фазе. Снижение интенсивности процесса в О2 для Rh может быть обусловлено формированием поверхностного оксида Rh2O3, препятствующего образованию RhO2(газ). Авторы работ [10, 11] связывают обнаруженные в ходе обработки образцов отдельными реагентами (О2, NO, N2O и др.) массоперенос металлов и перестройку поверхности для чистых Pt, Rh и сплавов Pt с различным содержанием Rh с переносом образующихся на “горячих” участках поверхности PtO2(газ) и RhO2(газ) на “холодные” участки поверхности металлов и их сплавов (механизм “Chemical-Vapor-Transport” (CVT)). Однако при окислении NH3 кислородом массоперенос протекает интенсивнее и приводит к более глубокой структурной перестройке поверхности [12–22] по сравнению с обработкой отдельными реагентами [10, 11].
По данным [12–18] в ходе каталитического окисления NH3 кислородом перестройка поверхностного слоя платины (каталитическая коррозия) ускоряется при повышении температуры катализатора. Так, методами измерения электрического сопротивления (R) и растровой электронной микроскопии (РЭМ) [12–15] было установлено, что шероховатость поверхности платиновой проволоки и интенсивность перестройки поверхностного слоя проволоки существенно увеличиваются с ростом температуры проволоки и скорости каталитического окисления NH3. Авторы [12–15] связывают глубокую структурную перестройку платины с сублимацией атомов Pt из “горячего” поверхностного слоя с повышенной сверхравновесной концентрацией адсорбированных атомов Pt в газовую фазу и последующим переносом платины на “холодные” участки поверхности.
В работах [16–18] было рассмотрено влияние температуры катализатора на морфологию поверхности поликристаллических фольги и проволоки Pt при протекании реакции окисления NH3 кислородом. После обработки фольги Pt в смеси NH3/О2 (3.0/4.5 кПа) при 559 К в течение 30 ч было зафиксировано появление гладких фасеток с размером около 0.1 мкм, что указывает на начало реконструкции поверхностного слоя [16, 17]. С ростом температуры от 603 до 647 К реконструкция заметно ускоряется и приводит к формированию упорядоченных рядов из гладких фасеток размером 0.1–0.5 мкм. После обработки катализатора в режиме нагревания–охлаждения в интервале 293–973 К в течение 24 и 240 ч на поверхности были обнаружены объемные кристаллы Pt размером около 2 мкм. По мнению авторов [16, 17] определяющим фактором перестройки поверхности в процессе окисления NH3 является температура катализатора. При Т < 673 К перестройка осуществляется в ходе поверхностной диффузии атомов платины, поскольку в этих условиях летучие оксиды платины практически не образуются. При Т > 673 К перестройка происходит вследствие испарения и реконденсации летучих фрагментов Pt+, PtO+, ${\text{PtO}}_{{\text{2}}}^{ + },$ так как при этих температурах фиксируется появление оксидов платины.
При содержании NH3 в воздухе от 0 до 100 об. % и нагреве платиновой проволоки от 923 до 1673 К размеры фасеток и ямок травления на реконструируемой поверхности сильно зависят от температуры катализатора и состава смеси NH3/воздух [18]. При концентрации 20–30 об. % NH3 в воздухе размер фасеток и ямок травления увеличивался с ростом температуры. При Т ≤ 1173–1273 К на поверхности были обнаружены фасетки и ямки травления размером около 0.5 мкм, тогда как при Т > 1173–1273 К размер фасеток и ямок травления повышался и составлял 1–3 мкм. По мнению авторов [18] в процессе окисления NH3 кислородом перестройка поверхности платины в избытке О2 определяется образованием летучих оксидов платины, а в избытке NH3 – поверхностной диффузией атомов платины.
В работах [19–22] была исследована коррозия состоящих из чистых металлов (Pt, Rh, Pd, Ag, Ir, Au) и сплавов (Pt/5–40 мас. % Rh, Pt/10–20 мас. % Ir и Pd/5 мас. % Ni) отрезков проволоки диаметром 0.2 мм и длиной около 100 мм, соосных с цилиндрическим кварцевым реактором, в ходе окисления NH3. Изучение морфологии поверхности и измерение температуры показало крайне неравномерное распределение возникающей шероховатости и измеряемой оптическим пирометром температуры по длине проволоки при окислении NH3 в течение от 0.5 до 504 ч в потоке, содержащем 17.2 об. % О2, 13.8 об. % NH3 и 69 об. % N2, при температуре около 1173 К в центральной части проволоки. После обработки платиновой проволоки в таких условиях в течение 386 ч на расстоянии 1–2 мм от ее начала (по ходу потока) на поверхности были обнаружены террасы шириной 5–10 мкм с углублениями диаметром 0.1–0.5 мкм [19]. С увеличением расстояния от начала проволоки (≥2 мм) на поверхности появляются вытянутые кристаллические образования типа фасеток высотой около 1 мкм, а на отрезке от 4 до 40 мм – кристаллические агломераты Pt размером 5–20 мкм. При дальнейшем возрастании расстояния от начала проволоки (>40 мм) размеры фасеток и агломератов уменьшаются, и постепенно появляются террасы, близкие к тем, что наблюдались в начале проволоки. В интервале от 4 до 20 мм от начала проволоки ее видимая толщина растет, а в интервале от 20 до 40 мм – уменьшается, далее толщина проволоки не изменяется. Увеличение видимого диаметра проволоки, связанное с ростом размеров фасеток и агломератов на отрезке 4–20 мм, и уменьшение толщины проволоки вследствие понижения размеров фасеток и агломератов на отрезке 20–40 мм совпадают с детектируемым повышением температуры вдоль проволоки от 873 до 1173 К и последующим ее понижением от 1173 до 873 К на этих участках проволоки.
В работе [20] по мере роста содержания Rh в сплавах Pt/5–13 мас. % Rh после окисления NH3 в течение 336 ч было зафиксировано постепенное уменьшение размера пористых кристаллических агломератов (структур типа “cauliflowers”), однако общая картина распределения террас, ямок травления и агломератов по длине проволоки близка к полученной для чистой Pt [19]. При содержании Rh, равном 30 и 40 мас. %, поверхность проволоки перестраивается в меньшей степени, обнаруживаются только углубленные межзеренные границы и фасетки на поверхности зерен. Для чистого Rh картина коррозии близка к полученной для Pt, наблюдаются структуры “cauliflowers” размером 50–60 мкм. В ходе окисления NH3 на чистых Pd, Ag, Ir и сплавах Pt/10–20 мас. % Ir, Pd/5 мас. % Ni протекает глубокая перестройка поверхности с образованием ямок травления, фасеток и структур “cauliflowers”, тогда как на Au-проволоке регистрируется незначительное фасетирование поверхности [21]. Авторы зафиксировали снижение селективности образования NO в ряду: Pd > Pt/10 мас. % Ir > Ag > Pt/20 мас. % Ir > > Pd/5 мас. % Ni > Ir. Нанесение тонкой пленки α-Fe2O3 на поверхность Pt, Rh и сплава Pt/10–30 мас. % Rh уменьшает их активность в окислении NH3 кислородом, однако не препятствует коррозии поверхности катализаторов с образованием структур “cauliflowers” [22].
В работах [19–22] глубокую реконструкцию поверхности чистых металлов Pt, Rh, Pd, Ag, Ir и сплавов Pt/5–40 мас. % Rh, Pt/10–20 мас. % Ir и Pd/5 мас. % Ni в ходе реакции окисления NH3 кислородом связывают с переносом образующихся на “горячих” участках поверхности как летучих оксидов PtO2(газ), RhO2(газ), IrO2(газ), так и атомов Pd(газ), Ag(газ) на “холодные” участки поверхности металлов и их сплавов (CVT-механизм). Авторы работы [20] считают, что для чистых Pt, Rh и сплавов Pt/5–13 мас. % Rh перенос PtO2(газ) и RhO2(газ) по CVT-механизму обусловлен повышенной температурой на локальных поверхностных дефектах “горячих точках” (“hotspots”), формирующихся вследствие протекания сильно экзотермической реакции окисления NH3 кислородом. В непосредственной близости от “hotspots” температура поверхности может быть существенно ниже, что создает локальный температурный градиент, необходимый для переноса металла по CVT-механизму. В области “hotspots” образующиеся PtO2(газ) и RhO2(газ) через газовую фазу переносятся на “холодные” участки поверхности, что приводит к постепенному росту кристаллов. Протекающие процессы травления и роста кристаллов вызывают глубокую структурную перестройку поверхности с образованием структур “cauliflowers”. Авторы [21, 22] полагают, что глубокая перестройка поверхности чистых металлов Pd, Ag, Ir и сплавов Pt/10–20 мас. % Ir и Pd/5 мас. % Ni, а также покрытых α-Fe2O3 в виде тонкой пленки Pt, Rh и сплава Pt/10–30 мас. % Rh происходит в ходе переноса металлов по CVT-механизму, связанному с образованием “hotspots” на поверхности катализаторов вследствие окисления NH3.
Сформировалось несколько качественно различных представлений о механизме каталитической коррозии. Рогинский полагал [7, 8], что массоперенос и последующие структурные изменения на поверхности катализатора связаны с повышенной подвижностью поверхностных атомов металла, обусловленной ослаблением связи адсорбированного атома металла с поверхностью за счет протекания на этом атоме каталитического акта. С другой стороны, Барелко с соавт. [12–15] выдвинул предположение о неравновесной природе процесса перестройки поверхности катализатора в ходе каталитической реакции. Сверхравновесная концентрация адсорбированных атомов металла по сравнению с равновесной для данной температуры возникает вследствие частичного расходования выделяющейся энергии каталитического акта на образования новых адсорбированных атомов металла. Мобильные атомы металла мигрируют по поверхности и сублимируются в газовую фазу, вызывая глубокую структурную перестройку поверхности и перенос платины с одних участков на другие. Массоперенос платины при окислении NH3 связывают также с диффузией атомов платины по поверхности [16–18]. Массоперенос металлов и перестройку поверхности для чистых металлов Pt, Rh, Pd, Ag, Ir и сплавов Pt–Rh, Pt–Ir, Pd–Ni в процессе реакции окисления NH3 кислородом авторы [19–22] объясняют переносом по CVT-механизму образующихся на “горячих” участках поверхности летучих оксидов (PtO2(газ), RhO2(газ) и др.) и металлов (Pd(газ), Ag(газ)) на “холодные” участки поверхности металлов и их сплавов. Такой перенос обусловлен возникновением создающих температурный градиент “hotspots” в области дефектов на поверхности катализаторов вследствие протекания сильно экзотермической реакции окисления NH3 кислородом.
Несмотря на наличие многочисленных публикаций об исследовании каталитической коррозии поликристаллических образцов платины [9, 12–19], а также Rh, Pd, Ag, Ir и сплавов Pt–Rh, Pt–Ir, Pd–Ni [19–22] в ходе каталитической реакции окисления аммиака, роль поверхностных и объемных дефектов, включая дислокации, межзеренные границы и др., в формировании кристаллических агломератов “cauliflowers” изучена явно недостаточно. В литературе отмечалось возможное влияние массопереноса за счет летучих оксидов и металлов (PtO2(газ), RhO2(газ) и др.) и поверхностной диффузии атомов металла на коррозию, в том числе на формирование “cauliflowers”, однако детального исследования влияния этих процессов на формирование агломератов проведено не было. Кроме того, коррозия затрагивает приповерхностные слои катализатора в глубину до нескольких десятков мкм [19–22] и протекает более интенсивно на фронтальной стороне платиноидной сетки (по ходу газового потока) по сравнению с тыльной. Поэтому необходимо учитывать данные для обеих сторон каталитической сетки о конкретном химическом составе и структуре приповерхностных слоев, а также влияние на коррозию процессов, протекающих не только непосредственно на поверхности, но и в объеме катализатора, в частности на поверхности порового пространства, на межзеренных границах и других протяженных объемных дефектах.
В настоящей статье приведены результаты изучения микроструктуры и химического состава поверхности и приповерхностных слоев на фронтальной (по ходу газового потока) стороне платиноидной сетки после окисления NH3 (~10 об. %) воздухом при Т = 1133 К в течение 50 ч. Задачей представленной работы было получение новых микроскопических данных и количественных характеристик коррозионного шероховатого слоя, обнаруживаемого на фронтальной стороне платиноидной сетки, и использование их для анализа протекающих в ходе коррозии процессов на поверхности и в приповерхностных слоях катализатора с целью выявления механизма формирования и роста пористых кристаллических агломератов типа “cauliflowers”.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали вязаные сетки 3 × 82 из проволоки диаметром 82 мкм, измеренным на микроскопических изображениях, полученных в настоящей работе. Сетки произведены Екатеринбургским заводом по обработке цветных металлов согласно СТО 00195200-014-2007. Состав сплава (мас. %/ат. %) согласно ГОСТ 13498-2010: Pt – 81/69.8, Pd – 15/23.7, Rh – 3.5/5.7 и Ru – 0.5/0.8. Содержание возможных примесей Ir, Fe, Au, Pb, Si, Sn, Zn составляет не более 0.11 мас. %, в том числе содержание Ir и Au не должно превышать величину 0.05 мас. %. Согласно ГОСТ 13498-2010 примеси этих элементов могут присутствовать в сплаве как в меньших концентрациях, так и отсутствовать совсем. В настоящей работе методом энергодисперсионной рентгеновской спектроскопии (ЭДС) вышеуказанные примеси не фиксируются. Однако следует отметить, что предел обнаружения элементов для стандартного ЭДС-анализа ~0.1 мас. %, что не позволяет зарегистрировать примеси элементов, которые, возможно, содержатся в сплаве в концентрациях, предусмотренных ГОСТ 13498-2010. Согласно вышеуказанному ГОСТу, плотность (ρ) и температура плавления (Тпл) этого сплава составляют 18.76 г/см3 и 2053–2073 К соответственно. С учетом приведенного значения ρ удельная геометрическая поверхность используемых исходных сеток равна 26.0 см2/г. Для промышленного применения проводят предварительную активацию исходных сеток, включающую электрохимическую очистку поверхности сеток от примесей Fe и др. и осаждение на нее из электролита слоя платины толщиной менее 0.1 мкм [23].
Каталитический процесс окисления аммиака воздухом осуществляли в лабораторном кварцевом реакторе проточного типа с внутренним диаметром 11.2 мм, в который помещали платиноидный пакет толщиной ~1 мм, сформированный из четырех сеток 3 × 82 общим весом 0.61 г. В реакторе пакет фиксировали перпендикулярно газовому потоку между двух сплетенных из проволоки толщиной около 0.2 мм сеток, изготовленных из жаростойкой стали Х23Ю5Т. Условия проведения эксперимента соответствовали работе промышленного агрегата АК-72 [24]: линейная скорость подачи предварительно подогретой в смесителе-подогревателе до 700 К реакционной смеси (~10 об. % NH3 в воздухе) составляла 2.57 м/с, температура в области сеток – 1133 ± 5 К, общее давление – 3.6 бар. Для обеспечения изотермичности работы пакета реактор обогревали снаружи таким образом, чтобы температура внешней стенки реактора была такой же, как и в центре реактора. Температуру измеряли двумя хромель-алюмелевыми термопарами с толщиной проволоки 0.5 мм, расположенными снаружи у внешней стенки реактора и в центральной части реактора на расстоянии 1 мм за пакетом сеток по ходу потока газа. Результаты определения концентрации NH3, NO, NO2 и N2O в отходящей из реактора газовой смеси свидетельствовали о выходе реактора на стационарный режим через 50 ч работы. Степень превращения NH3 составляла около 100%, NH3 на выходе из реактора не обнаружено. При температуре процесса Т = 1133 К и температуре плавления использованного платиноидного сплава Тпл = 2063 К значение Т/Тпл близко к 0.55. В этих условиях подвижность атомов в платиноидной проволоке должна быть существенной, поэтому могут интенсивно протекать процессы рекристаллизации, включающие рост зерен и фасетирование поверхности. Для изучения морфологии и химического состава поверхности проволоки использовали первую сетку по ходу потока газа. Детальное описание реактора и проведения каталитического процесса приведены в работе [24].
Для изучения морфологии поверхностного слоя проволоки применяли растровый электронный микроскоп JSM-6460 LV (“Jeol”, Япония) с вольфрамовым термокатодом при величинах энергии электронов зонда от 1 до 25 кэВ. Формат съемки (2560 × 1920 пикселей в течение 160 с) давал возможность получать в режиме вторичных электронов (ВЭ) микрофотографии высокого качества и регистрировать на поверхности объекты с размерами до 20–40 нм. Микроскоп был укомплектован рентгеновским энергодисперсионным спектрометром INCA Energy-350 (“Oxford Instruments”, Великобритания), позволяющим определять химический состав поверхностного слоя проволоки. Для калибровки спектрометра применяли эталоны, изготовленные из чистых образцов Si и Co. Количественный анализ проводили с применением внутренних стандартов, содержащихся в базе спектрометра. Методы РЭМ и ЭДС, использованные в наших исследованиях, обладают различной эффективной глубиной анализа, меняющейся в интервале от 1 нм до 1 мкм [25]. В работах [26, 27] были оценены линейные размеры областей проникновения электронов зонда (RK–O), эмиссии отраженных электронов (ОЭ) (RОЭ) и рентгеновского излучения (RХ) для чистых металлов Pt, Pd, Rh, Ru и исследуемого платиноидного сплава в ходе взаимодействия электронов зонда с образцом при Е0 = 1–30 кэВ. Для сплава увеличение Е0 от 1 до 30 кэВ приводит к росту величин RK–O и ROЭ в интервалах 5–1620 и 1–308 нм соответственно [27].
Для оценки интенсивности каталитической коррозии, инициированной реакцией окисления NH3, определяли площадь поверхности коррозионного шероховатого слоя, используя микроскопические изображения поверхности. По данным работ [19–22] в ходе каталитической реакции окисления аммиака на чистых металлах Rh, Pd, Ag, Ir и сплавах Pt–Rh, Pt–Ir, Pd–Ni в процессе каталитической коррозии образуются кристаллические агломераты типа “cauliflowers”, которые имеют в основном близкую к сферической форму. Поэтому площадь поверхности агломератов можно рассчитывать как площадь поверхности сферы, которая ограничивает фигуру агломерата, учитывая величину площади видимой поверхности агломерата Si на микрофотографии. Площадь поверхности сферы радиуса R равна 4πR2, где πR2 – площадь большого круга с совпадающими со сферой центром и радиусом. Принимая во внимание, что видимая поверхность агломерата площадью Si может соответствовать площади поверхности большого круга сферы, равной величине $\pi R_{i}^{{\text{2}}},$ площадь сферы, ограничивающей поверхность агломерата с линейным размером $S_{i}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}},$ будет равна 4Si. На микроскопических изображениях “cauliflowers”, приведенных в работах [19–22], обнаруживаются поры различной формы и размера, проникающие глубоко в объем агломератов. Пористая структура увеличивает общую поверхность агломератов. Для оценки величины площади, связанной с внутренними порами в объеме агломератов, регистрируемые на поверхности агломератов поры использовали для вычисления площади поверхности цилиндрических пор, проникающих сквозь агломераты. Поверхность цилиндрической поры рассчитывали, учитывая длину окружности поры Сj и диаметр соответствующего агломерата Di, которые определяли из видимых поверхностей поры Sj и агломерата Si на изображениях. Полученные величины поверхности агломератов и внутренних пор в агломератах позволяли оценить объем, занимаемый агломератами и порами.
Таким образом, результаты исследования методами РЭМ и ЭДС, обладающими эффективной глубиной анализа от 1 нм до 1 мкм, в совокупности с данными оценки геометрических свойств коррозионного шероховатого слоя, дают возможность анализировать процесс формирования пористых кристаллических агломератов на поверхности платиноидных сеток в ходе каталитического окисления NH3.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Настоящая работа по изучению в ходе окисления NH3 воздухом при Т = 1133 К формирования шероховатого слоя, включающего пористые кристаллические агломераты на фронтальной стороне (по ходу газового потока) платиноидной сетки с составом Pt (81 мас. %), Pd (15 мас. %), Rh (3.5 мас. %) и Ru (0.5 мас. %), является продолжением исследований [26, 27]. Эти работы были направлены на изучение влияния воздуха и аммиака на коррозию платиноидной сетки [26], а также реакции окисления NH3 на коррозию тыльной стороны этой сетки [27] при Т = 1133 К. В ходе отжига сеток на воздухе и в аммиаке следы заметной коррозии поверхности проволоки отсутствуют [26]. Были зарегистрированы сетчатая структура поверхности с углеродом на межзеренных границах и рост зерен до размера около 10 мкм. После окисления NH3 воздухом на тыльной стороне сетки зафиксированы области размером 100–200 мкм с различными степенями коррозии (минимальная, средняя и максимальная). В этих областях происходит рост и слияние ямок травления, а также увеличение шероховатости поверхности проволоки в ходе окисления NH3. На фронтальной стороне сетки обнаруживается практически сплошной шероховатый слой из кристаллических агломератов размером около 10 мкм. Настоящая работа выполнена в логике раздельного исследования воздействия отдельных реагентов и каталитической реакции на коррозию в близких условиях. Считаем, что результаты изучения влияния воздуха и аммиака на коррозию платиноидной сетки, а также реакции окисления NH3 на коррозию поверхностного слоя проволоки на тыльной и фронтальной сторонах сетки позволят продвинуться в понимании механизма каталитической коррозии, инициированной реакцией окисления NH3 кислородом.
На рис. 1 приведены микрофотографии платиноидной сетки и поверхности проволоки для фронтальной (а, б, в) и тыльной (г, д, е) сторон одного и того же фрагмента первой по ходу газа сетки после ее использования в процессе окисления NH3 кислородом воздуха при Т = 1133 К в течение 50 ч. Прямоугольниками выделены участки, представленные микрофотографиями с бóльшим увеличением. Из рис. 1а видно, что поверхность проволоки фронтальной стороны сетки покрыта сплошным шероховатым слоем. Этот слой состоит из пористых кристаллических агломератов различной формы и размера, разделенных глубокими пустотами (рис. 1б). Агломераты имеют кристаллическую огранку, сквозные поры и похожи на кристаллические образования типа “cauliflowers”, обнаруженные на платиноидных сетках после их использования в процессе окисления NH3 кислородом в работах [19–22]. Сплошной слой из “cauliflowers” указывает на глубокую каталитическую коррозию платиноидных сеток.
Рис. 1.
Микрофотографии платиноидной сетки и поверхности проволоки на фронтальной (а–в) и тыльной (г–е) сторонах одного и того же фрагмента первой по ходу газа сетки, полученные при Е0 = 25 кэВ в режиме ВЭ и различных увеличениях после окисления NH3 при 1133 К в течение 50 ч. Прямоугольниками выделены участки, представленные микрофотографиями с бóльшим увеличением.
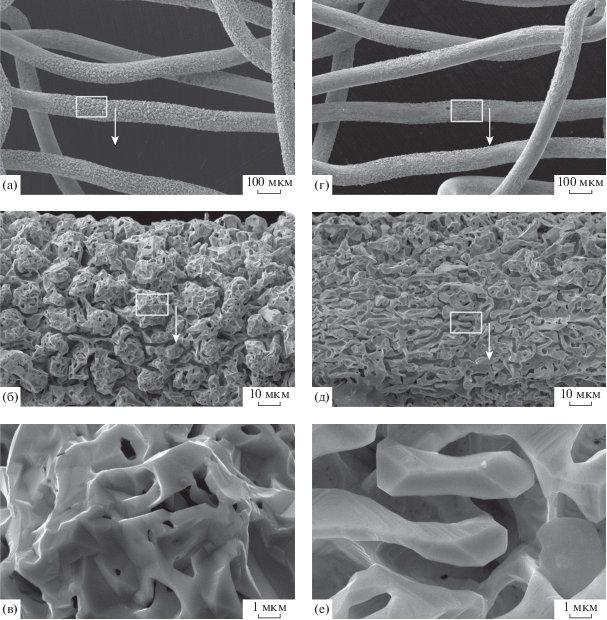
На тыльной по ходу газа стороне сетки (рис. 1г) шероховатость поверхности проволоки существенно меньше по сравнению с таковой для фронтальной стороны этого же участка (рис. 1а). На рис. 1г видны фрагменты проволоки, содержащие области с различной степенью коррозии. На рис. 1д показан участок проволоки, расположенный в центральной части горизонтального фрагмента проволоки на рис. 1г в наиболее прокорродированной области, включающей в основном вытянутые кристаллические образования длиной до 10 мкм и шириной до 1–2 мкм, которые разделены глубокими пустотами шириной 1–2 мкм (рис. 1е). Обнаруженные на тыльной стороне сетки кристаллы имеют существенно меньший размер по сравнению с агломератами на фронтальной стороне (рис. 1б и 1в). Это свидетельствует, что каталитическое окисление NH3 кислородом воздуха приводит к глубокой коррозии поверхностного слоя проволоки на фронтальной стороне платиноидной сетки, тогда как поверхность проволоки на тыльной стороне сетки прокорродирована в значительно меньшей степени. Морфология поверхности проволоки на тыльной стороне платиноидной сетки (рис. 1г) близка к той, что приведена в работе [27]. Реагенты из газового потока поступают вначале на фронтальную и только затем на тыльную сторону сетки, вследствие чего их концентрация и, соответственно, скорость каталитической реакции будут значительно выше на фронтальной стороне. Поэтому окисление аммиака на ней протекает интенсивнее и вызывает более сильную коррозию поверхности проволоки.
Для анализа процесса формирования пористых кристаллических агломератов, инициированного реакцией окисления NH3, исследовали морфологию, микроструктуру и химический состав коррозионного, шероховатого слоя на фронтальной стороне сетки.
Морфология и микроструктура шероховатого слоя на фронтальной стороне платиноидной сетки после окисления NH3 при 1133 К
На рис. 2 представлены микрофотографии приведенного в центральной части изображения на рис. 1а горизонтального фрагмента проволоки (рис. 2г) и отдельных участков этого фрагмента (рис. 2а–2в, 2д–2ж) фронтальной стороны сетки после окисления NH3 при 1133 К в течение 50 ч. Из рис. 2г следует, что поверхность отрезка проволоки длиной около 1 мм преимущественно покрыта сплошным шероховатым слоем из агломератов. С учетом этого слоя диаметр проволоки составляет ~94 мкм. На концах отрезка видны участки проволоки длиной 100–150 мкм и диаметром ~ 84 мкм с относительно гладкой поверхностью. По-видимому, эти участки включают области с пониженной степенью коррозии, аналогичные тем, что были обнаружены на тыльной стороне сетки после окисления NH3 в течение 50 ч [27], и могут формироваться вследствие экранирования газового потока фрагментами проволоки, расположенными перед рассматриваемым отрезком проволоки. На рис. 2а–2в приведены изображения области, обозначенной на рис. 2г левым прямоугольником и расположенной между шероховатым слоем и участком с пониженной степенью коррозии. Обнаруженная четкая граница между этими областями свидетельствует о распространении коррозионного шероховатого слоя в область с пониженной степенью коррозии. На рис. 2д–2ж представлены микрофотографии фрагмента шероховатого слоя, обозначенного на рис. 2г правым прямоугольником в центральной части отрезка проволоки. На изображениях виден сплошной слой из имеющих кристаллическую огранку пористых агломератов, разделенных протяженными пустотами. Вероятно, эти агломераты представляют собой рекристаллизованные зерна, образующиеся в ходе интенсивно протекающих процессов каталитической коррозии и рекристаллизации при 1133 К. Разделяющие зерна пустоты формируются в результате роста и слияния пор, расположенных на межзеренных границах. Такие поры обнаруживаются в областях с пониженной степенью коррозии на рис. 2б и 2в.
Рис. 2.
Микрофотографии поверхности проволоки на фронтальной стороне платиноидной сетки, полученные при Е0 = 25 кэВ в режиме ВЭ и различных увеличениях после окисления NH3 при 1133 К в течение 50 ч. г – Фрагмент проволоки сетки, показанной на рис. 1а. а–в – Микрофотографии участка, отмеченного левым прямоугольником на рис. 2г, на границе между шероховатым слоем и областью с пониженной степенью коррозии. д–ж – Микрофотографии участка, отмеченного правым прямоугольником на рис. 2г, с шероховатым слоем и кристаллическими агломератами. Прямоугольниками выделены участки, представленные микрофотографиями с бóльшим увеличением.

На рис. 3г приведено панорамное изображение области, обозначенной пунктирным прямоугольником на рис. 2а – участок границы длиной ~90 мкм между шероховатым слоем и областью с пониженной степенью коррозии (правая часть изображения) и участок области с наименьшей степенью коррозии (левая часть изображения). Для анализа участков с различной степенью коррозии на рис. 3г имеется горизонтальная шкала (в мкм), условно отсчитывающая расстояние от начала анализируемого фрагмента поверхности. Области, обозначенные большими квадратами и локализованные на расстояниях около 3.2, 40.8 и 69.5 мкм, представлены на рис. 3а, 3б и 3в соответственно. На этих микрофотографиях отчетливо видны темные пятна и кристаллические террасы. Зарегистрированные темные пятна могут быть изображениями ямок травления, формирующихся в ходе миграции атомов металла из дефектных областей поверхности типа “дислокации” и “межзеренные границы”. Миграция атомов металла из дефектов на поверхность ускоряется локальным разогревом отдельных участков поверхности вследствие интенсивного экзотермического окисления молекул NH3 атомами кислорода, внедренными в поверхностные дефекты. Мигрирующие в ходе поверхностной диффузии атомы металла формируют на поверхности зерен кристаллические террасы с низкой концентрацией дефектов [27].
Рис. 3.
Микрофотографии поверхности проволоки на фронтальной стороне платиноидной сетки, полученные при Е0 = 25 кэВ в режиме ВЭ и различных увеличениях после окисления NH3 при 1133 К в течение 50 ч. г – Изображение участка поверхности проволоки в обозначенной пунктирным прямоугольником области на рис. 2а. а–в – Микрофотографии отмеченных на рис. 3г большими квадратами участков областей с различными степенями коррозии. д, е – Средний размер и концентрация ямок травления в областях, обозначенных большими и маленькими квадратами на рис. 3г. ж – Химический состав поверхностного слоя по данным ЭДС на участке, отмеченном большим квадратом на рис. 3г на расстоянии 40.8 мкм.

Размер и концентрацию ямок травления определяли на участках поверхности зерен (~4 × 3 мкм), обозначенных на рис. 3г малыми квадратами. Было обнаружено, что ямки травления распределены неравномерно: в центральной области зерен фиксируется их повышенная концентрация по сравнению с областью, граничащей с межзеренными границами. По-видимому, при температуре реакции расположенные в непосредственной близости от межзеренных границ дислокации мигрируют к этим границам и поглощаются; в результате концентрация ямок травления, связанных с этими дислокациями, уменьшается. Для полной поверхности зерен с площадями 81.8 и 63.5 мкм2, центры которых расположены на расстоянии около 8.5 и 40.8 мкм (рис. 3г), концентрации ямок травления составили значения 8.6 × 108 и 5.1 × 108 см–2 соответственно. В центральной части этих зерен для участков площадью около 13.2 мкм2 концентрации ямок травления были приблизительно в 3 раза выше и равны 2.2 × 109 и 1.6 × 109 см–2 соответственно. Поэтому концентрацию ямок травления на поверхности зерна рассчитывали из значения концентрации на участке площадью около 4 × 3 мкм в центре зерна и с учетом полученной выше поправки.
На рис. 3д и 3е приведены значения среднего размера и концентрации ямок травления для областей, отмеченных квадратами на рис. 3г, в зависимости от расположения участка анализа на фрагменте поверхности со шкалой в нижней части на рис. 3г. В области от 0 до 40 мкм размеры ямок травления и их концентрация изменяются незначительно и составляют величины близкие к 60 нм и 6.0 × 108 см–2 соответственно. На рис. 3г в интервале от 0 до 40 мкм видны зерна с гладкой поверхностью и межзеренные границы, содержащие поры размером ~0.5 мкм. На отрезке от 40 до 50 мкм фиксируются увеличение размера ямок травления до ~80 нм и уменьшение их концентрации до ~1.0 × 108 см–2; на поверхности зерен заметны неровности с размерами 1–2 мкм. В области от 50 до 70 мкм регистрируются существенный рост размеров ямок травления до ~130 нм и незначительное изменение их концентрации; на межзеренных границах видны крупные поры размером 1–2 мкм. Обнаруженные зависимости размера ямок травления и их концентрации от расположения участков анализа на фрагменте поверхности рис. 3г близки к аналогичным зависимостям для областей с минимальной и средней степенями коррозии на тыльной стороне платиноидной сетки [27].
Данные о химическом составе поверхностного слоя на фронтальной стороне сетки в области с пониженной степенью коррозии были получены при измерении концентраций элементов в поверхностном слое методом ЭДС. Анализировали фрагменты поверхности размером около 5 × 5 мкм, обозначенные на рис. 3г квадратами. Были зарегистрированы Pt, Pd, Rh, Ru, С, О и N. При расчете концентраций элементов углерод не учитывали, поскольку он мог находиться в составе поверхностной графитоподобной пленки [26], искажающей величины концентраций элементов при количественном анализе. Измеренные значения концентрации элементов на разных участках анализа различаются несущественно и близки к рассчитанным средним значениям. На рис. 3ж приведены данные о химическом составе поверхностного слоя в области квадрата, расположенного на расстоянии 40.8 мкм на рис. 3г. Измеренные значения содержания элементов составили (ат. %): Pt – 42.3, Pd – 15.1, Rh – 2.7, Ru – 0.7, О – 21.7 и N – 17.5. Аналогичные показатели, полученные ранее в [27] на поверхности проволоки с тыльной стороны платиноидной сетки, были равны (ат. %): Pt – 55.9, Pd – 19.5, Rh – 4.8, Ru – 0, О – 8.7 и N – 11.1. Для сравнения, заявленный заводом-изготовителем состав сплава включает (ат. %): Pt – 69.8, Pd – 23.7, Rh – 5.7, Ru – 0.8. Пониженное содержание Rh и повышенное содержание Ru в поверхностном слое на фронтальной стороне сетки по сравнению с тыльной может быть следствием миграции атомов Rh и Ru в приповерхностных слоях в ходе более интенсивного протекания окисления NH3, приводящего к локальному разогреву отдельных участков поверхности. Кроме того, по-видимому, Ru распределен в объеме крайне неравномерно и поэтому на тыльной стороне сетки не регистрируется вследствие его содержания в некоторых областях на глубине до 1 мкм в количестве на пределе чувствительности метода ЭДС (~0.1 мас. %). Повышенная концентрация кислорода в поверхностном слое проволоки может указывать на образование оксидных (Rh2O3) пленок на поверхности проволоки в ходе окисления NH3 кислородом, а наличие азота (17.5 ат. %) – на формирование поверхностной пленки типа Pt–Nx.
На рис. 3а–3в видны темные нечеткие пятна размером от 60 до 130 нм, которые могут быть обусловлены ямками травления, расположенными в приповерхностных слоях проволоки. Их появление возможно вследствие одновременного роста ямок травления и формирования кристаллических террас на поверхности проволоки. В ходе этих процессов растущие террасы могут закрывать ямки травления. Для того чтобы выяснить, как ямки травления распределены в глубине приповерхностной области проволоки, были сделаны микрофотографии при значениях энергии электронов зонда Е0 в интервале от 1 до 25 кэВ. Изображения получены для поверхности зерна с площадью 63.6 мкм2, обозначенного на фрагменте поверхности рис. 3г большим квадратом, расположенным на расстоянии около 40.8 мкм. Повышение величины Е0 от 1 до 30 кэВ приводит к возрастанию эффективной глубины проникновения электронов зонда в объем образца (RK–O) от 5 до 1620 нм, а эмиссии ОЭ (ROЭ) – от 1 до 308 нм. По мере увеличения значения Е0 изображения приповерхностных слоев претерпевают существенные изменения [27]. При Е0 = 1 кэВ рассчитанная величина RK–O составляет всего 5 нм, а RОЭ – 1 нм, при этом на изображениях не обнаруживаются связанные с ямками травления темные пятна. При Е0 = 5 кэВ величина RK–O возрастает до 80 нм, а RОЭ – до 15 нм, на микрофотографиях появляются четкие межзеренные границы с крупными порами (рис. 4а) и контуры кристаллических террас с поверхностными углублениями (рис. 4б). На поверхности зерна на рис. 4а зафиксировано 10 размытых темных пятен с размером ≤50 нм, обусловленных ямками травления внутри приповерхностного слоя толщиной до 15 нм. При Е0 = 10, 20 и 25 кэВ величина RK–O возрастает до 260, 830 и 1200 нм, а RОЭ – до 50, 158 и 228 нм соответственно, поэтому изображения формируются ВЭ, генерируемыми электронами зонда и эмитируемыми с глубины ≤5 нм, и ОЭ, эмитируемыми с глубины ≤50, ≤158 и ≤228 нм соответственно. На снимках тех же участков, полученных при Е0 = 10 (рис. 4в, 4г), 20 (рис. 4д, 4е) и 25 кэВ (рис. 3б), видны четкие контуры кристаллических террас, а также темные пятна, связанные с присутствием ямок травления внутри приповерхностных слоев на глубинах до 50, 158 и 228 нм соответственно; на изображениях поверхности зерна связанных с этими глубинами анализа, зафиксировано 118 (рис. 4в), 277 (рис. 4д) и 324 (рис. 3б) ямки травления. Таким образом, при Е0 = 1, 5, 10, 20 и 25 кэВ регистрируются микроструктурные особенности как непосредственно на поверхности, так и в слоях толщиной до 5, 15, 50, 158 и 228 нм соответственно.
Рис. 4.
а–е – Микрофотографии поверхности зерна, отмеченного на рис. 3г большим квадратом на расстоянии 40.8 мкм, на фронтальной стороне платиноидной сетки, полученные в режиме ВЭ при Е0 = 5 (а, б), 10 (в, г) и 20 кэВ (д, е) и увеличениях ×10 000 и ×30 000 после окисления NH3 при 1133 К в течение 50 ч. ж – Зависимость концентрации ямок травления от глубины анализа. з – Концентрация ямок травления в приповерхностных слоях толщиной 50 нм в глубину до 250 нм.

На рис. 4ж приведена рассчитанная из данных о количестве ямок травления на зерне площадью 63.6 мкм2 зависимость концентрации ямок травления от глубины анализа (нижняя шкала), связанной с величиной Е0 (верхняя шкала) [25]. Видно, что количество ямок травления постепенно растет с увеличением глубины анализа. При толщине анализируемого слоя ~15 нм их концентрация составляет величину около 1.6 × 107 см–2, а при 250 нм – 5.1 × 108 см–2. Полученное для 250 нм значение оказалось близким к величине, зафиксированной для области с минимальной степенью коррозии на тыльной стороне этой сетки (4.2 × × 108 см–2) [27]. На рис. 4з приведены определенные по кривой на рис. 4ж концентрации ямок травления в приповерхностных слоях толщиной 50 нм в глубину до 250 нм. Видно, что в поверхностном слое их концентрации максимальная – около 1.9 × 108 см–2, а в последующих слоях толщиной 50 нм фиксируется ее постепенное уменьшение до значения 2.9 × 107 см–2 на глубине от 200 до 250 нм.
Кристаллические агломераты на фронтальной стороне платиноидной сетки
На рис. 5 представлены микрофотографии шероховатого слоя и пористых кристаллических агломератов, расположенных в центральной части проволоки на рис. 2г фронтальной стороны сетки после окисления NH3 при 1133 К в течение 50 ч. Из рис. 5а видно, что поверхность проволоки покрыта сплошным шероховатым слоем из кристаллических агломератов. Изображения этих агломератов различной формы и размера с неровной развитой поверхностью, включающей кристаллические грани, углубления и поры, проникающие в объем агломератов, приведены на рис. 5б–5г. Агломераты разделены пустотами шириной 5–15 мкм, распространяющимися в глубину до 10 мкм.
Рис. 5.
а–г, з – Микрофотографии шероховатого слоя и агломератов в центральной части горизонтального отрезка проволоки, показанной на рис. 2г для фронтальной стороны платиноидной сетки, полученные в режиме ВЭ при Е0 = = 25 кэВ и различных увеличениях после окисления NH3 при 1133 К в течение 50 ч. Прямоугольниками выделены участки, представленные микрофотографиями с бóльшим увеличением. д, е – Распределение агломератов и пор по размерам, приведенные на 1 см2 поверхности проволоки и агломератов, полученные на участках (а) и (в) соответственно. ж – Химический состав агломератов по данным метода ЭДС на участке (в).
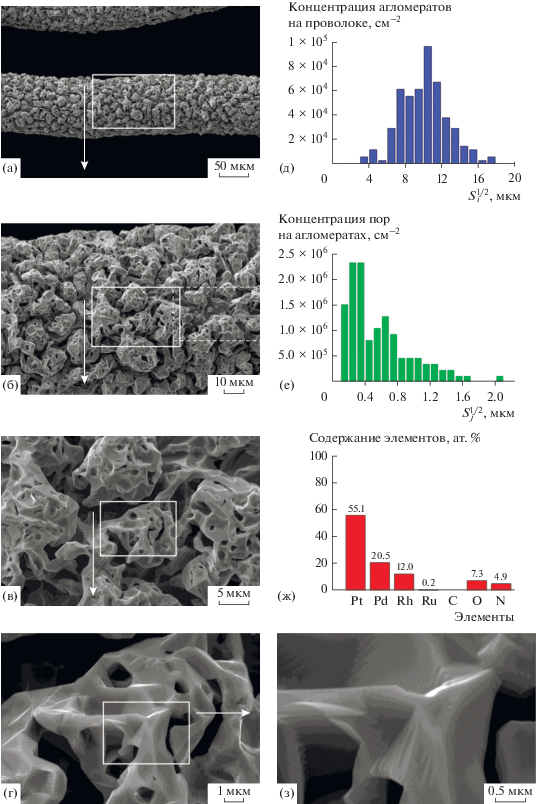
На рис. 5д представлено распределение числа зарегистрированных агломератов в зависимости от их линейного размера для приведенного на рис. 5а фрагмента поверхности проволоки длиной 420 мкм и площадью 3.4 × 104 мкм2, содержащей 169 агломератов. Линейный размер агломерата $S_{i}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}$ определяли из видимой площади агломерата Si на микрофотографии, его значения варьируют от 3 до 18 мкм. Основная часть агломератов имеет размер от 6 до 14 мкм (средний размер ~10 мкм); общее число агломератов на 1 см2 геометрической поверхности проволоки (N) составляет 4.9 × 105. Необходимо отметить, что величины размера и концентрации агломератов, определенные на этом отрезке проволоки, близки к значениям среднего размера (~10 мкм) и концентрации агломератов (6.9 × 105 см–2), рассчитанных на поверхности другого отрезка проволоки длиной 123 мкм. Это свидетельствует о равномерном распределении кристаллических агломератов по поверхности проволоки на фронтальной стороне сетки.
На микрофотографиях рис. 5б–5г на кристаллических гранях агломератов отчетливо видны поры размером около 2 мкм и меньше. При этом на поверхности граней на рис. 5г и 5з не фиксируются темные пятна, связанные с ямками травления в приповерхностном слое агломератов, которые наблюдаются на кристаллических террасах для областей с пониженной степенью коррозии на рис. 3а–3в. Обнаруженные на рис. 5б–5г поры могут формироваться в процессе роста и слияния связанных с дислокациями ямок травления на поверхности и в объеме рекристаллизующихся зерен. На рис. 5е показано распределение числа пор, расположенных на поверхности агломератов, по размерам. Распределение получено с использованием поверхности приведенных на рис. 5в агломератов площадью 8.6 × 102 мкм2, содержащей 113 пор. Линейный размер пор $S_{j}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}$ находили, как и ранее, из видимой площади темного пятна Sj на микрофотографии. Линейный размер пор варьирует от 0.1 до 1.7 мкм. Основная часть пор имеет размер от 0.1 до 1.2 мкм; общее число пор на 1 см2 геометрической поверхности агломератов (N0) составляет 1.3 × 107. На гистограмме распределения пор по размерам (рис. 5е) обнаруживаются два максимума при значениях 0.3 и 0.6 мкм. Это может свидетельствовать о слиянии пор с размером ~0.3 мкм с образованием пор со средним размером ~0.6 мкм. Рост и слияние пор происходят в ходе травления поверхности пор, включающего миграцию атомов металла из дефектов на поверхность пор, диффузию адсорбированных атомов металла по поверхности и испарение в газовую фазу. Эти процессы инициируются реакцией окисления NH3 атомами кислорода, внедренными в дефекты на поверхности пор.
Данные о химическом составе агломератов на фронтальной стороне сетки в области сплошного шероховатого слоя были получены по результатам измерений концентрации элементов в поверхностном слое агломератов методом ЭДС. Анализ проводили в пяти выделенных квадратных фрагментах размером около 5 × 5 мкм, расположенных в центре агломератов на рис. 5в. Были зарегистрированы Pt, Pd, Rh, Ru, С, О и N. При расчете концентраций элементов, как и ранее, углерод не учитывали. Концентрации этих элементов между точками анализа различаются незначительно. На рис. 5ж приведены усредненные данные по химическому составу агломератов. По сравнению с областью пониженной степени коррозии (рис. 3ж) зафиксированные повышенное содержание Rh и пониженное содержание Ru в приповерхностном слое агломератов могут быть следствием миграции атомов Rh и Ru, а также их неравномерного распределения в объеме. Низкая концентрация кислорода и азота в поверхностном слое агломератов может указывать на частичное удаление оксидных (Rh2O3) и нитридных (Pt–Nx) пленок с поверхности агломератов в ходе окисления NH3 кислородом.
На рис. 6а–6в приведены микроскопические изображения кристаллических агломератов, показанных на рис. 5в. Эти агломераты имеют близкую к сферической форму с неровной развитой поверхностью, включающей грани, углубления и поры различной формы и размера. На поверхности агломератов обнаруживаются поры с размером <2 мкм, тогда как между агломератами на поверхности проволоки видны углубления с размером >2 мкм. Это может говорить о более интенсивном протекании процесса травления поверхности проволоки по сравнению с поверхностью агломератов. В пользу такого предположения свидетельствует и наличие продолговатых фрагментов диаметром 3–5 мкм, связывающих агломерат размером ~15 мкм с поверхностью проволоки. Для сравнительной оценки интенсивностей процессов травления и роста агломератов, инициированных реакцией окисления NH3, были рассчитаны площади поверхности агломератов и пор внутри агломератов.
Рис. 6.
а–в – Микрофотографии кристаллических агломератов, показанных на рис. 5в для фронтальной стороны платиноидной сетки, полученные в режиме ВЭ при Е0 = 25 кэВ и различных увеличениях после окисления NH3 при 1133 К в течение 50 ч. г–е – Распределение величин площади поверхности агломератов и внутренних пор и CjNj по размерам (см. подробности в тексте).

На рис. 6г приведено распределение величины площади поверхности агломератов 4SiNi (где 4Si – площадь сферы, ограничивающая поверхность агломерата, Ni – количество агломератов с линейным размером $S_{i}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}},$ приходящихся на 1 см2 геометрической поверхности проволоки) в зависимости от линейного размера агломерата $S_{i}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}},$ полученное с учетом распределения агломератов по линейному размеру (рис. 5д). Максимальное значение площади поверхности агломератов (4.3 × × 107 мкм2) соответствует размеру агломератов ~11 мкм (рис. 6г), а максимальное количество агломератов (7.0 × 104 см–2) приходится на размер ~10 мкм (рис. 5д). Суммирование приведенных на рис. 6г величин площади поверхности 4SiNi агломератов с линейным размером от 3 до 18 мкм дает значение площади для всех агломератов, приходящихся на 1 см2 геометрической поверхности проволоки $\left( {S_{i}^{0}} \right),$ равное 2.2 × 108 мкм2. Следует отметить, что полученная величина близка к площади агломератов, оцененной с учетом концентрации (N = 4.9 × 105 см–2) и среднего линейного размера агломератов (S1/2 = 10 мкм) и составляющей 4SN = 2.0 × 108 мкм2.
На микроскопических изображениях агломератов рис. 1, 2 и 5 и рис. 6а–6в фиксируются поры различной формы и размера, проникающие глубоко в объем агломератов. Для оценки площади этих пор рассчитывали поверхность цилиндров, учитывая длину окружности пор Сj и диаметр соответствующего агломерата Di, которые определяли из видимых поверхностей пор и агломератов на изображениях. Принимая во внимание распределение зарегистрированных пор по линейным размерам (см. рис. 5е), была построена гистограмма распределения величины СjNj (где Nj – количество пор с линейным размером $S_{j}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}},$ приходящееся на 1 мкм2 площади агломерата) в зависимости от линейного размера пор (рис. 6д). На этой гистограмме наблюдаются два максимума, соответствующие наибольшей концентрации пор при значениях $S_{j}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}$ около 0.3 и 0.6 мкм. Кроме того, фиксируются относительно высокие значения СjNj при $S_{j}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}$ > 0.8 мкм. Суммирование приведенных на рис. 6д величин СjNj дает значение 0.27 мкм–1, приходящееся на 1 мкм2 поверхности агломерата. Площадь поверхности внутренних пор для Ni агломератов с площадью Si, линейным размером $S_{i}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}$ и диаметром Di рассчитывали, принимая во внимание полученную величину СjNj = 0.27 мкм–1. На рис. 6е представлено распределение площади поверхности внутренних пор 4SiNiDi0.27 в зависимости от линейного размера агломерата: максимальное значение соответствует линейному размеру агломератов 11 мкм и равно 1.2 × 108 мкм2. Суммирование приведенных на рис. 6е величин 4SiNiDi0.27 дает значение площади всех внутренних пор в объеме кристаллических агломератов (6.6 × 108 мкм2), приходящееся на 1 см2 геометрической поверхности проволоки. Полученное значение близко к площади внутренних пор в агломератах πN0$S_{j}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}$$S_{i}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}$$S_{i}^{0}$ = 4.5 × 108 мкм2, найденной с учетом концентрации и среднего линейного размера пор на поверхности агломератов, а также среднего размера агломератов и поверхности агломератов, приходящейся на 1 см2 геометрической поверхности проволоки (N0 = 1.3 × 107 см–2, $S_{j}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}$ = 0.5 мкм, $S_{i}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}$ = 10 мкм, $S_{i}^{0}$ = 2.2 cм2 соответственно).
Необходимо отметить, что поверхность сферы, ограничивающая агломерат определенного объема, имеет минимальную площадь по сравнению с другими поверхностями, ограничивающими фигуру с данным объемом. На микрофотографиях рис. 1, 2, 5 и рис. 6 видны агломераты с различной формой, отличающейся от сферической. Поэтому оценка с использованием поверхности сферы является нижней границей величины площади поверхности кристаллических агломератов на поверхности проволоки платиноидной сетки. Кроме того, на микрофотографиях рис. 1, 2, 5 и рис. 6 зарегистрированные кристаллические агломераты обнаруживают пористую структуру, увеличивающую их общую площадь поверхности. Оценка площади поверхности внутренней пористой структуры агломератов с учетом сквозных цилиндрических пор может приводить к бóльшим, чем есть на самом деле, величинам, поскольку не рассматривает возможные завышение концентрации пор, пересечение пор в объеме и поры длиной менее диаметра агломерата. Принимая во внимание полученные значения площади поверхности агломератов (2.2 × 108 мкм2) и пористой структуры кристаллических агломератов (6.6 × 108 мкм2), а также величину геометрической поверхности проволоки (1.0 × 108 мкм2), можно считать, что поверхность шероховатого коррозионного слоя проволоки платиноидных сеток после окисления NH3 кислородом воздуха при 1133 К в течение 50 ч, приходящаяся на 1 см2 геометрической поверхности проволоки, составляет величину от 5.0 × 108 до 10.0 × 108 мкм2, что примерно в 5–10 раз превышает геометрическую поверхность исходной проволоки. По данным работы [28] оценка электрохимическим методом поверхности платиноидных сеток с таким же составом, как в нашей работе, свидетельствует об увеличении удельной поверхности от 30 см2/г для исходной сетки до 206 см2/г после ее промышленной эксплуатации в процессе окисления NH3 в течение 330 ч. То есть в течение периода выхода катализатора на оптимальный режим работы удельная поверхность сеток повышается приблизительно в 7 раз. При эксплуатации сетки в течение более 2000 ч ее удельная поверхность постепенно растет и достигает ~400 см2/г.
Поровые пустоты между агломератами на фронтальной стороне платиноидной сетки
В ходе интенсивного травления, инициированного реакцией NH3 с внедренным на дефектах кислородом, ямки травления и поры на межзеренных границах сливаются и образуют сплошные пустоты шириной 5–15 мкм. На рис. 5а–5в видны межзеренные пустоты, распространяющиеся в объем на глубину до 10 мкм относительно внешних поверхностных участков агломератов. Эти пустоты разделяют кристаллические агломераты и формируют поровое пространство в приповерхностном слое. На рис. 7а приведен микроснимок участка поверхности, выделенного на рис. 5б пунктирным прямоугольником и включающего кристаллические агломераты и поровые пустоты между агломератами. На рис. 7б–7е представлены микрофотографии обозначенных на рис. 7а и 7б участков поверхности проволоки внутри порового пространства в приповерхностном слое. На рис. 7в–7е на дне поры видны кристаллические фасетки с темными пятнами размером около 50 нм, которые, по-видимому, связаны с ямками травления. На рис. 7д и 7е на дне поры фиксируется существенно меньше ямок травления, чем на поверхности зерен в области с пониженной степенью коррозии (рис. 3а и 3б), и приблизительно столько же, сколько и в области, граничащей непосредственно с шероховатым слоем (рис. 3в). Вероятно, внутри пор вследствие более интенсивного окисления NH3 температура поверхности значительно выше, чем снаружи, поэтому в ходе травления в порах дислокации и связанные с ними ямки травления мигрируют и исчезают быстрее, чем на поверхности зерен в области с пониженной коррозией. Кроме того, на дне этих пор обнаруживаются углубления, указывающие на распространение поры в объем (рис. 7в и 7г). Из рис. 7а видно, что интенсивно протекающее травление, вызванное реакцией NH3 c атомами кислорода на дефектах в области межзеренных границ, приводит к формированию поровых пустот между кристаллическими агломератами шириной 5–15 мкм и глубиной до 10 мкм.
На рис. 7а в центральной части и в левом нижнем углу микроскопического изображения в области поровых пустот обнаруживаются кристаллы размером 1–2 мкм. На рис. 8а и 8б приведены изображения этих кристаллов, имеющих форму подобную сферической. Кристаллы располагаются на промежуточном расстоянии между поверхностью дна поры и верхними участками агломератов. Поэтому вследствие ограниченной глубины фокуса для растровых электронных микроскопов фокусировка на поверхности кристаллов приводит к нечеткому, размытому изображению поверхности дна поры и агломератов, находящихся, соответственно, ниже и выше относительно кристаллов. На поверхности этих кристаллов обнаруживаются идеальные грани, на которых не фиксируются ни темные пятна, связанные с ямками травления, ни поры, проникающие в объем кристаллов (рис. 8в и 8г). Это свидетельствует о низкой концентрации поверхностных и объемных дефектов в кристаллах, указывающей, вероятно, на формирование этих кристаллов в условиях, приводящих к зарождению и росту монокристаллов с очень низкой концентрацией дефектов. Формирование таких монокристаллов возможно в ходе поглощения бездефектными зародышами кристаллов атомов металла или летучих оксидов металлов из газовой фазы с повышенным давлением паров металлов и оксидов, которое создается в ходе испарения/ сублимации атомов металла и оксидов с поверхности проволоки. Испарение атомов металла и оксидов может существенно ускоряться при формировании сверхравновесного покрытия адсорбированными атомами металла поверхности проволоки в результате миграции атомов металла на поверхность из локально разогретых дефектных областей в ходе высоко экзотермической реакции окисления NH3 атомами кислорода на дефектах.
Рис. 7.
а – Микрофотография участка поверхности проволоки, обозначенного пунктирным прямоугольником на рис. 5б. б–е – Изображения участков порового пространства, показанных прямоугольниками на рис. 7а и 7б. Изображения получены на фронтальной стороне платиноидной сетки в режиме ВЭ при Е0 = 25 кэВ и различных увеличениях после окисления NH3 при 1133 К в течение 50 ч. Прямоугольниками выделены участки, представленные микрофотографиями с бóльшим увеличением.

Рис. 8.
а–г – Микрофотографии кристаллов, показанных в области поровых пустот в центральной части и в левом нижнем углу на изображении рис. 7а. Изображения получены на фронтальной стороне платиноидной сетки в режиме ВЭ при Е0 = 25 кэВ и различных увеличениях после окисления NH3 при 1133 К в течение 50 ч. Прямоугольниками выделены участки, представленные микрофотографиями с бóльшим увеличением.

Поровые пустоты между агломератами имеют повышенную удельную поверхность, приходящуюся на единицу объема, по сравнению с геометрической поверхностью проволоки, поскольку поры в приповерхностном слое включают вертикальные и горизонтальные участки поверхности (относительно поверхности проволоки), содержащие фрагменты фасеток с повышенной концентрацией дефектов, что увеличивает общую поверхность поровых пустот (рис. 7). Кроме того, поверхность поровых пустот, которая является непосредственно поверхностью цельного тела проволоки, может иметь повышенную температуру по сравнению с агломератами. Помимо этого, повышенная температура поверхности пор может быть следствием более эффективного распределения выделяющегося в ходе высоко экзотермической реакции окисления NH3 тепла по объему металлической проволоки, чем между проволокой и агломератами, связанными с ней тонкими фрагментами.
Каталитическая коррозия платиноидных сеток в ходе окислении NH3 кислородом при 1133 К
Активные центры каталитической коррозии. Каталитическую коррозию металлов и сплавов в ходе реакции окисления NH3 кислородом связывают с массопереносом, инициированным повышенной подвижностью поверхностных атомов металла [7, 8], сверхравновесной концентрацией адсорбированных атомов металла [12–15], поверхностной диффузией атомов металла [16–18] и образованием летучих оксидов и паров металлов [19–22]. Массоперенос металлов и перестройку поверхности для чистых Pt, Rh, Pd, Ag, Ir и сплавов Pt–Rh, Pt–Ir, Pd–Ni в процессе реакции окисления NH3 кислородом авторы [19–22] объясняют переносом образующихся на “горячих” участках поверхности летучих оксидов (PtO2(газ), RhO2(газ) и др.) и паров металлов (Pd(газ), Ag(газ)) на “холодные” участки поверхности металлов и их сплавов по CVT-механизму, связанному с образованием создающих температурный градиент “hotspots” в области дефектов на поверхности катализаторов вследствие сильно экзотермической реакции окисления NH3 кислородом. В настоящей работе впервые были получены микроизображения платиноидной проволоки с ямками травления нанометрового размера на поверхности и в приповерхностных слоях после окисления NH3, и с их помощью произведена оценка размера и концентрации ямок травления и расчет их распределения на поверхности и в приповерхностных слоях проволоки на фронтальной стороне сетки. Полученные величины концентрации ямок травления согласуются с приведенными в литературе значениями плотности дислокаций, что свидетельствует о формировании ямок травления на дефектах в ходе реакции окисления NH3. Зафиксированные ямки травления могут являться активными центрами коррозии типа “hotspots”, обсуждаемыми в исследованиях [19–22]. Однако в этих работах не были приведены микроскопические изображения таких центров. Регистрация нанометровых ямок травления (центров коррозии) на поверхности платиноидных сеток в ходе окисления аммиака дает возможность анализировать начальную стадию каталитической коррозии.
На фронтальной стороне платиноидной сетки из Pt, Pd, Rh и Ru (81, 15, 3.5 и 0.5 мас. % соответственно) после окисления NH3 при 1133 К в течение 50 ч на поверхности проволоки обнаруживается в основном сплошной шероховатый слой, включающий пористые кристаллические агломераты, и участки проволоки диаметром ~84 мкм и длиной 100–150 мкм с относительно гладкой поверхностью (рис. 2). На поверхности зерен этих участков зарегистрированы ямки травления размером ~60 нм в концентрации 6.0 × 108 см–2 (рис. 3). На непосредственной границе с шероховатым слоем зафиксированы увеличение их размера до 130 нм и уменьшение концентрации до 1.0 × 108 см–2, что свидетельствует о росте и слиянии ямок травления. В центральной части зерен концентрация ямок травления приблизительно в 3 раза выше, чем в области около межзеренных границ. На тыльной стороне сетки в области минимальной коррозии поверхностная концентрация ямок травления размером ~72 нм составляет 4.2 × 108 см–2 и понижается при переходе в область со средней степенью коррозии до 2.5 × 108 см–2; размер ямок травления при этом увеличивается до ~85 нм [27]. Полученные значения концентрации ямок травления на фронтальной и тыльной сторонах сетки согласуются с типичными величинами плотности дислокаций (107–108 см–2) в отожженных поликристаллических металлах [29].
Зарегистрированные изображения поверхности зерен при значениях энергии электронов зонда в интервале от 1 до 25 кэВ свидетельствуют о постепенном снижении концентрации ямок травления от поверхности в глубину (рис. 4). В поверхностном слое толщиной 50 нм концентрации ямок травления максимальная и составляет около 1.9 × × 108 см–2. В последующих слоях толщиной 50 нм в глубину до 250 нм фиксируется постепенное уменьшение этого показателя до 2.9 × 107 см–2. Повышенная концентрация ямок травления в центральной части зерен по сравнению с участками около межзеренных границ, а также в приповерхностном слое по сравнению с более глубокими слоями, может быть обусловлена миграцией дислокаций к межзеренным границам и к поверхности проволоки в условиях окисления NH3.
На рис. 9 приведены изображения поверхности зерен в области с пониженной степенью коррозии на тыльной (а, б) и фронтальной (в, г) сторонах платиноидной сетки после окисления NH3 при 1133 К в течение 50 ч. На межзеренных границах видны крупные поры размером 250–500 нм, на поверхности зерен обнаруживаются кристаллические террасы высотой около 50 нм и ямки травления размером 100–300 нм. Кроме того, на изображениях зерен фиксируются темные пятна размером около 100 нм, связанные с ямками травления в приповерхностных слоях. Концентрация ямок травления рядом с межзеренными границами существенно ниже, чем в центральной части зерен, по-видимому, вследствие “стока” дислокаций и связанных с ними ямок травления на межзеренные границы.
Рис. 9.
Микрофотографии поверхности зерен на тыльной (а, б) и фронтальной (в, г) сторонах платиноидной сетки, полученные в режиме ВЭ при Е0 = 25 кэВ и увеличениях ×10 000 и ×30 000 после окисления NH3 при 1133 К в течение 50 ч. Прямоугольниками выделены участки, представленные микрофотографиями с бóльшим увеличением.
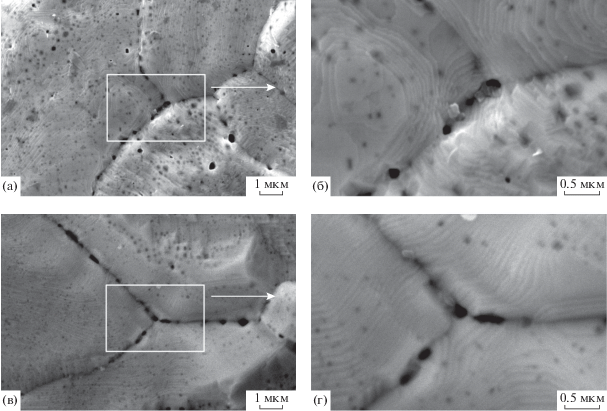
Наблюдаемые ямки травления, расположенные на дислокациях, могут играть роль центров типа “hotspots”, создающих температурный градиент в области дефектов на поверхности катализаторов, который обеспечивает перенос металла с “горячих” участков на “холодные”, вследствие чего происходит коррозия поверхности катализатора [19–22]. В области дефектов возможно интенсивное протекание высоко экзотермической реакции окисления NH3 кислородом, внедренным в приповерхностные слои. По данным работы [27], полученным для платиноидного сплава, при высоких температурах и давлениях О2 атомы Оадс могут внедряться в области дефектов, в том числе в дислокации и межзеренные границы, постепенно проникая в объем. Реакция NH3 с Оадс также будет преимущественно происходить в области дефектов, поскольку локальное покрытие атомами Оадс в ней будет выше, чем на гладкой поверхности, в том числе за счет диффузии атомов Оадс по поверхности и миграции атомов О из объема. Протекание реакции окисления NH3 на дефектах вызывает локальное повышение температуры за счет сильно экзотермической реакции окисления NH3. Рост температуры ускоряет перенос атомов металла от дефектов и их миграцию на поверхность. Этот процесс приводит к появлению и росту ямок травления на поверхности в области дислокаций и межзеренных границ, которые обнаруживаются на микрофотографиях на участках с пониженной степенью коррозии на тыльной и фронтальной сторонах платиноидной сетки (рис. 9, [27]). Мигрирующие на поверхность атомы металла в ходе поверхностной диффузии формируют покрывающие всю поверхность зерен кристаллические террасы с низкой концентрацией дефектов (рис. 9). В ходе этих процессов растущие террасы закрывают ямки травления, поэтому значительная их часть оказывается в приповерхностных слоях. Таким образом, в самом начале коррозионного процесса в областях с пониженной степенью коррозии перестройка поверхностного слоя проволоки в значительной мере обусловлена миграцией на поверхность и поверхностной диффузией атомов металла, тогда как образующиеся летучие оксиды, по-видимому, в основном уносятся газовым потоком за пределы платиноидных сеток.
Поверхность коррозионного шероховатого слоя. По данным РЭМ окисление NH3 кислородом на чистых металлах Pt, Rh, Pd, Ag, Ir и сплавах Pt–Rh, Pt–Pd–Rh–Ru, Pt–Ir, Pd–Ni [9, 12–22, 26, 27] приводит к формированию коррозионного шероховатого слоя, увеличивающего поверхность катализатора. По результатам электрохимических измерений [28] удельная поверхность исходных платиноидных сеток из проволоки диаметром 90 мкм с таким же составом, как и в нашей работе, составляет величину около 30 см2/г. После промышленной эксплуатации в процессе окисления NH3 и выхода катализатора на оптимальный режим работы удельная поверхность сетки через 330 ч возрастает приблизительно в 7 раз до 206 см2/г, а после эксплуатации в течение более 2000 ч увеличивается до ~400 см2/г. По результатам адсорбционных измерений [30] удельная поверхность Pt–Rh-сеток после окисления NH3 в промышленном реакторе повышается в 2–20 раз по сравнению с исходной. В настоящей работе впервые на основании микроскопических изображений агломератов и пор сделана оценка удельной поверхности платиноидной сетки после окисления NH3. Для определения величины поверхности шероховатого слоя были рассчитаны распределения агломератов и пор по размерам, а также произведена оценка внешней поверхности агломератов и внутренних пор с использованием поверхностей сфер и цилиндров. Рассчитанная величина удельной поверхности шероховатого слоя платиноидной сетки, равная 260 см2/г, согласуется со значением этого параметра, полученным электрохимическим методом [28]. Это свидетельствует о возможности определять удельную поверхность шероховатых образцов из микроскопических изображений, что особенно важно для систем с низкими величинами поверхности, для которых применение адсорбционных или электрохимических методов сопровождается определенными трудностями.
После окисления NH3 кислородом воздуха при 1133 К в течение 50 ч на фронтальной стороне сетки поверхность проволоки преимущественно покрыта сплошным шероховатым слоем из пористых кристаллических агломератов с линейным размером от 3 до 18 мкм (средний размер ~10 мкм), разделенных пустотами шириной 5–15 мкм и глубиной до 10 мкм. В области шероховатого слоя вследствие роста агломератов видимый диаметр проволоки увеличивается приблизительно на 10 мкм и составляет ~94 мкм (рис. 2). На поверхности кристаллических граней агломератов регистрируются поры размером менее 2 мкм, проникающие в объем агломератов и обусловленные слиянием ямок травления в ходе окисления NH3. На поверхности агломератов не фиксируются связанные с дислокациями ямки травления, обнаруженные в областях с пониженной степенью коррозии, что указывает на низкую концентрацию дефектов (дислокаций) в приповерхностном слое агломератов (рис. 5). Значительная часть зарегистрированных кристаллических агломератов имеет близкую к сферической форму, поэтому для расчета площади их внешней поверхности использовали поверхность сферы, а площадь поверхности пор в объеме агломератов оценивали по поверхности цилиндров (рис. 6).
С учетом поверхности сфер, ограничивающих агломераты, и распределения агломератов по размерам площадь внешней поверхности агломератов, приходящейся на 1 см2 геометрической поверхности проволоки, составляет 2.2 × 108 мкм2. Пористая структура из цилиндрических пор, пронизывающих насквозь агломераты, существенно увеличивает общую поверхность агломератов. Учитывая распределение пор по размерам и их протяженность, определяемую диаметром агломератов, площадь внутренней поверхности цилиндрических пор, приходящейся на 1 см2 геометрической поверхности проволоки, равна 6.6 × × 108 мкм2. Принимая во внимание полученные оценки величины площади внешней поверхности и внутренней пористой структуры агломератов, а также геометрической поверхности проволоки (1.0 × 108 мкм2), поверхность, приходящаяся на 1 см2 шероховатого коррозионного слоя проволоки платиноидных сеток после окисления NH3 кислородом воздуха при 1133 К в течение 50 ч, может составлять ~1.0 × 109 мкм2. Учитывая удельную геометрическую поверхность исходной проволоки равную 26.0 см2/г, удельная поверхность прокорродированной платиноидной сетки имеет величину 260 см2/г, что согласуется с данными работы [28].
Коррозия вследствие поверхностной диффузии атомов металла или образования летучих оксидов (PtO2(газ), RhO2(газ) и др.)? Коррозия поверхности платины в ходе окисления NH3 может быть обусловлена формированием сверхравновесной концентрации адсорбированных атомов металла [12–15] и диффузией атомов платины по поверхности [16–18]. На металлах Pt, Rh, Pd, Ag, Ir и сплавах Pt–Rh, Pt–Ir, Pd–Ni реакция окисления NH3 кислородом инициирует глубокую коррозию поверхности катализатора, которую связывают с переносом образующихся на “горячих” участках поверхности летучих оксидов (PtO2(газ), RhO2(газ) и др.) и паров металлов (Pd(газ), Ag(газ)) на “холодные” участки [19–22]. В настоящей работе впервые получены микроскопические изображения поверхности в поровых пустотах между кристаллическими агломератами глубиной около 10 мкм на фронтальной стороне платиноидной сетки после окисления NH3. На изображениях видна нанофасетированная поверхность, свидетельствующая о высокой концентрации поверхностных дефектов по сравнению с поверхностью агломератов. Это говорит о том, что окисление NH3 с большей интенсивностью протекает в порах, а не на поверхности агломератов. Учитывая это, мы предлагаем схему роста/формирования агломератов, включающую образование зон с повышенной и пониженной температурами в порах и на агломератах соответственно. Формирование этих зон может приводить к появлению температурного градиента протяженностью ~10 мкм, нормально ориентированного по отношению к поверхности проволоки. Вследствие такого градиента образующиеся на “горячих” участках в поровых пустотах летучие оксиды и пары металлов могут конденсироваться на выше расположенных “холодных” участках поверхности монокристаллов и агломератов. Таким образом постепенно формируются и растут агломераты. В работах [19–22] была рассмотрена подобная схема формирования агломератов, однако, в отличие от них, в нашем исследовании приведены микроскопические данные, подтверждающие перенос металла из пор на агломераты.
Зависимости равновесного давления металлов Pt, Pd и Rh в вакууме, а также PtO2(газ), PdO(газ) и RhO2(газ) в атмосфере О2 (1 бар) от температуры, полученные в работах [31–33], свидетельствуют об изменении величин парциального давления в широком интервале от ~1.0 × 10–15 Па при Т = 400–1000 К до 10–3–103 Па при 2000 К. В атмосфере О2 парциальные давления PtO2(газ) и RhO2(газ) существенно превышают таковые для этих металлов в вакууме. При температуре каталитического окисления NH3 (~1100 К) различие между величинами парциального давления для оксидов (PtO2(газ) и RhO2(газ)) и металлов (Pt и Rh) достигает 10 порядков. Таким образом, в кислородсодержащей среде образующиеся летучие оксиды этих металлов могут осуществлять более значительный массоперенос, приводящий к глубокой коррозии катализатора в ходе окисления NH3 кислородом, чем пары металлов. Данные о химическом составе поверхностного слоя на фронтальной стороне сетки в области с пониженной степенью коррозии (рис. 3ж) и на кристаллических агломератах (рис. 5ж) свидетельствуют о различном составе этих областей. Для области с меньшей степенью коррозии фиксируется пониженное содержание Rh (2.7 ат. %) и повышенное – O (21.7 ат. %) и N (17.5 ат. %) по сравнению с содержанием этих элементов в агломератах (Rh – 12.0 ат. %, O – 7.3 ат. % и N – 4.9 ат. %). Это может говорить о наличие оксидных (Rh2O3) и нитридных (Pt–Nx) пленок на поверхности зерен в области с пониженной степенью коррозии и о разложении этих пленок и накоплении Rh в приповерхностных слоях на агломератах вследствие повышенной температуры на агломератах по сравнению с областью с меньшей коррозией.
Применяемые в составе пакета в промышленном окислении NH3 платиноидные сетки подвергаются коррозии крайне неравномерно. Первая по ходу газа сетка всегда значительно сильнее прокорродирована по сравнению с последующими. По данным работы [28] после промышленного окисления NH3 в течение 2000–4000 ч с использованием пакета из 12 платиноидных сеток удельная поверхность в центральной зоне первой по ходу газового потока сетки составляет ~380 см2/г, тогда как для 3, 5, 7, 9 и 11 сеток – 280, 210, 150, 130 и 110 см2/г соответственно. Уменьшение поверхности сеток в пакете связано с постепенным снижением интенсивности окисления на них NH3. Расчеты технологических параметров окисления NH3 в реакторе [34] показывают расходование около 80% NH3 на первых трех по ходу газа сетках; на последующих четырех сетках окисляется ~18% NH3, а на остальных пяти – всего 2%. Уменьшение интенсивности окисления NH3 на последующих сетках пакета приводит к постепенному снижению температуры на этих сетках. Так, на четвертой сетке она становится на 80°С ниже, чем на первой. Коррозия замедляется, в результате чего поверхность шероховатого слоя увеличивается не так сильно относительно предыдущих сеток. Поступающий газовый поток реагентов захватывает образующиеся на первой сетке летучие оксиды и уносит их к следующим по ходу газа сеткам с пониженной температурой. В случае разложения оксидов на последующих сетках наблюдалось бы формирование развитой коррозионной структуры, однако коррозия на них проявляется в меньшей степени, чем на предыдущих, следовательно, летучие оксиды в основном уносятся за пределы пакета сеток.
На поверхности агломератов не фиксируются связанные с дислокациями ямки травления, зарегистрированные в областях с пониженной степенью коррозии, что указывает на малую концентрацию дефектов (дислокаций) в приповерхностном слое агломератов (рис. 5). На стенках и дне поровых пустот обнаруживаются фасетки и ямки травления размером около 50 нм, свидетельствующие о повышенной концентрации дефектов (рис. 7). Газовый поток с пониженной температурой реагентов (~700 К) по сравнению со средней температурой сеток (~1133 К) прежде всего поступает на поверхность агломератов, на которых окисление NH3 протекает с малой интенсивностью вследствие пониженных концентраций дефектов и температуры реагентов. При этом поток охлаждает агломераты и сам, нагреваясь, поступает с повышенной температурой на поверхность поровых пустот. Из-за бóльших значений концентрации дефектов и температуры на поверхности поровых пустот по сравнению с поверхностью выше расположенных агломератов вследствие сильно экзотермической реакции окисления NH3 в области дефектов на поверхности поровых пустот происходит интенсивная миграция атомов металла из дефектов на поверхность. Адсорбированные атомы диффундируют по поверхности и формируют поверхностный сверхравновесный слой, из которого атомы металла и летучие оксиды испаряются в газовую фазу и создают сверхравновесное давление паров в приграничном слое проволоки в области поровых пустот. По данным работ [12–15] глубокая структурная перестройка поверхности платины в ходе окисления NH3 кислородом связана с сублимацией атомов металла из “горячего” поверхностного слоя с повышенной сверхравновесной концентрацией атомов Pt в газовую фазу и последующим переносом платины на “холодные” участки поверхности. Область поровых пустот шероховатого слоя полностью открыта со стороны газового потока, но при этом ограничена вертикальными стенками, препятствующими уносу испаряющихся атомов металла и летучих оксидов и создающими частично-локально закрытый объем. Поэтому величина сверхравновесного давления паров металла и оксидов в ограниченном объеме поровых пустот может достигать существенных значений, превышающих критические и, соответственно, достаточных для роста и формирования монокристаллов и кристаллических агломератов с очень низкой концентрацией дефектов.
Можно полагать, что в результате интенсивного протекания сильно экзотермической реакции окисления NH3 в области поровых пустот с бóльшими значениями удельной поверхности и концентрации дефектов формируется сплошная область повышенной температуры, охватывающая массивную центральную часть проволоки. Внешняя же поверхность агломератов с малой концентрацией дефектов и охлаждаемая газовым потоком реагентов включает область с пониженной температурой и расположена на расстоянии ~10 мкм от поверхности центральной части проволоки с повышенной температурой. Такое распределение температурных фронтов приводит к появлению температурного градиента, направленного от поверхности агломератов в сторону дна поровых пустот. Вследствие этого образующиеся на “горячих” участках дна поровых пустот летучие оксиды и пары металлов могут конденсироваться на выше расположенных “холодных” участках поверхности монокристаллов и агломератов, формируя грани с пониженным содержанием дефектов. Кроме того, рост температуры в шероховатом слое по сравнению с областью пониженной коррозии приводит к разложению поверхностных пленок Rh2O3 и Pt–Nx и накоплению Rh в приповерхностных слоях агломератов. В областях с повышенной степенью коррозии, в том числе в поровых пустотах шероховатого слоя, массоперенос и перестройка поверхностного слоя проволоки в значительной степени обусловлены разложением и конденсацией на “холодных” участках агломератов и монокристаллов летучих оксидов и паров металлов, образующихся на “горячих” участках, тогда как массоперенос в ходе поверхностной диффузии атомов металла в этих условиях влияет на коррозию в меньшей степени.
ЗАКЛЮЧЕНИЕ
Методами РЭМ и ЭДС проведено исследование морфологии, микроструктуры и химического состава поверхности и приповерхностных слоев проволоки платиноидной сетки, содержащей Pt (81 мас. %), Pd (15 мас. %), Rh (3.5 мас. %) и Ru (0.5 мас. %). После окисления NH3 воздухом при Т = 1133 К и давлении 3.6 бар в течение 50 ч на фронтальной стороне сетки обнаружена глубокая перестройка поверхности проволоки (каталитическая коррозия), приводящая к формированию сплошного шероховатого слоя из агломератов типа “cauliflowers”.
На фронтальной стороне сетки зафиксированы фрагменты проволоки размером 100–150 мкм с гладкой микрозернистой структурой. На этих зернах впервые зарегистрированы ямки травления нанометрового размера и найдены концентрация ямок травления и их распределение по поверхности и в приповерхностных слоях проволоки. Ямки травления размером от 60 до 130 нм в концентрации от 1.0 × 108 до 6.0 × 108 см–2 могут являться центрами коррозии типа “hotspots”, образующимися в ходе высоко экзотермического окисления NH3 на дефектах. Полагаем, что реакция окисления NH3 на ямках травления приводит к локальному росту температуры с появлением температурного градиента, который инициирует миграцию атомов металла на поверхность и поверхностную диффузию адсорбированных атомов металла. Рост ямок травления и формирование кристаллических террас на поверхности зерен в значительной степени обусловлены поверхностной диффузией атомов металла, тогда как образующиеся летучие оксиды, по-видимому, в основном уносятся газовым потоком.
Сплошной коррозионный шероховатый слой на поверхности проволоки в основном состоит из пористых кристаллических агломератов (“cauliflowers”) с линейным размером от 3 до 18 мкм (средний размер ~10 мкм) в концентрации 4.9 × × 105 см–2. На поверхности агломератов зарегистрированы поры с диаметром от 0.1 до 1.7 мкм в концентрации 1.3 × 107 см–2. Впервые, принимая во внимание полученные из микроскопических изображений распределения агломератов и пор по размерам, проведена оценка удельной поверхности шероховатого слоя исследуемой платиноидной сетки. Величины поверхности агломератов и пор в объеме агломератов, рассчитанные с помощью формул для поверхности сфер и цилиндров, составляют 2.2 × 108 и 6.6 × 108 мкм2 на 1 см2 проволоки соответственно. Удельная поверхность платиноидной сетки после окисления NH3 с учетом полученных значений поверхности агломератов и пор равна 260 см2/г.
На основании анализа микроскопических изображений поверхности агломератов и поровых пустот предложена схема формирования кристаллических агломератов. На поверхности агломератов вследствие низкой концентрации дефектов и охлаждения газовым потоком реагентов окисление NH3 протекает с низкой интенсивностью, в результате чего на агломератах может формироваться область, имеющая пониженную температуру. В поровых пустотах шириной 5–15 мкм и глубиной до 10 мкм с повышенной удельной поверхностью и концентрацией дефектов сильно экзотермическое окисление NH3 кислородом происходит интенсивнее, чем на агломератах, поэтому возможно образование зоны с повышенной температурой, охватывающей массивную часть проволоки. В различающихся по температуре областях возникает температурный градиент, направленный от поверхности агломератов в сторону дна поровых пустот. Вследствие этого образующиеся на “горячих” участках дна поровых пустот пары летучих оксидов и металлов могут конденсироваться на выше расположенных “холодных” участках поверхности агломератов и монокристаллов. Протекание этих процессов формирует сплошной коррозионный слой из пористых кристаллических агломератов, массивных монокристаллов и глубоких поровых пустот, который существенно увеличивает удельную поверхность катализатора и приводит к росту объемной скорости окисления NH3, ускоряющей коррозионный процесс. В результате происходит распространение коррозионного слоя на платиноидной проволоке в автокаталитическом режиме.
Список литературы
Satterfield C.N. Heterogeneous Catalysis in Practice. N.Y.: McGraw-Hill Co., 1980. 416 p.
Lloyd L. Handbook of Industrial Catalysis. N.Y.: Springer, 2011. P. 119.
Kuhlmann F. // Justus Leibigs Ann. Chem. 1839. V. 29. № 3. P. 272.
Pat. 271517 DE, 1909.
Parsons C.L. // J. Ind. Eng. Chem. 1919. V. 11. P. 541.
Rideal E.K., Taylor H.S. Catalysis in Theory and Practice. 2nd ed. London: Macmillan & Co Ltd., 1926. P. 176.
Рогинский С.З., Третьяков И.И., Шехтер А.Б. // Журн. физ. химии. 1949. № 10. С. 1152.
Рогинский С.З., Третьяков И.И., Шехтер А.Б. // ДАН СССР. 1953. Т. 91. С. 881.
Garton G., Turkevich J. // J. Chim. Phys. 1954. V. 51. P. 516.
Hannevold L., Nilsen O., Kjekshus A., Fjellvag H. // J. Alloy. Compd. 2005. V. 402. P. 53.
Hannevold L., Nilsen O., Kjekshus A., Fjellvag H. // J. Crystal Growth. 2005. V. 279. P. 206.
Барелко В.В., Володин Ю.Е., Хальзов П.И., Доронин В.Н. // ДАН СССР. 1976. Т. 231. № 5. С. 1143.
Барелко В.В., Хальзов П.И. // Поверхность. 1982. № 6. С. 91.
Lyubovsky M.R., Barelko V.V. // J. Catal. 1994. V. 149. P. 23.
Любовский М.Р., Барелко В.В. // Кинетика и катализ. 1994. Т. 35. № 3. С. 412.
Kraehnert R., Baers M. // Appl. Catal. A. General. 2007. V. 327. P. 73.
Kraehnert R. // Dr. thesis. Der Technischen Universitat Berlin: Berlin, 2005.
McCabe R.W., Pignet T., Schmidt L.D. // J. Catal. 1974. V. 32. P. 114.
Nilsen O., Kjekshus A., Fjellvag H. // Appl. Catal. A. General. 2001. V. 207. P. 43.
Hannevold L., Nilsen O., Kjekshus A., Fjellvag H. // Appl. Catal. A. General. 2005. V. 284. P. 163.
Hannevold L., Nilsen O., Kjekshus A., Fjellvag H. // Appl. Catal. A. General. 2005. V. 284. P. 185.
Hannevold L., Nilsen O., Kjekshus A., Fjellvag H. // Appl. Catal. A. General. 2005. V. 284. P. 177.
Пaт. 1807608 RU. 1995.
Исупова Л.А. // Катализ в промышленности. 2012. № 6. С. 52.
Goldstein J., Newbury D., Joy D., Lyman C., Echlin P., Lifshin E., Sawyer L., Michael J. Scanning Electron Microscopy and X-Ray Microanalysis. N.Y.: Springer. 2003. P. 61.
Саланов А.Н., Супрун Е.А., Серкова А.Н., Сидельникова О.Н., Сутормина Е.Ф., Исупова Л.А., Калинкин А.В., Пармон В.Н. // Кинетика и катализ. 2018. Т. 59. № 1. С. 105.
Саланов А.Н., Супрун Е.А., Серкова А.Н., Кочурова Н.М., Сидельникова О.Н., Сутормина Е.Ф., Исупова Л.А., Калинкин А.В., Пармон В.Н. // Кинетика и катализ. 2018. Т. 59. № 6. С. 756.
Васина С.Я., Бруштейн Е.А., Петрий О.А., Лазаричева И.В., Перов В.М. // Хим. пром-сть. 1992. № 10. С. 30.
Новиков И.И. Дефекты кристаллического строения металлов. Москва: Металлургия, 1975. 208 с.
Bergene E., Tronstad O., Holmen A. // J. Catal. 1996. V. 160. P. 141.
Darling A.S. // Platinum Metals Rev. 1964. V. 8. № 4. P. 134.
Alcock C.B., Hooper G.W. // Procc. Royal Soc. 1960. V. 254. № 1279. P. 551.
Olivei A. // J. Less Common Metals. 1972. V. 29. I. 1. P. 11.
Садыков В.А., Бруштейн Е.А., Исупова Л.А., Телятникова Т.В., Кирчанов А.А., Золотарский И.А., Носков А.С., Кожевникова Н.Г., Кругляков В.Ю., Снегуренко О.И., Гиббадулин Ю.Н., Хазанов А.А. // Хим. промышленность. 1997. № 12. С. 819.
Дополнительные материалы отсутствуют.
Инструменты
Кинетика и катализ


