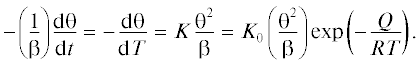Кинетика и катализ, 2022, T. 63, № 4, стр. 526-539
О фундаментальных аспектах решения проблемы “супер” хранения водорода в каталитически синтезированных графитовых нановолокнах
Ю. С. Нечаев a, *, Е. А. Денисов b, А. О. Черетаева c, Н. А. Шурыгина a, Е. К. Костикова d, С. Ю. Давыдов e
a Центральный научно-исследовательский институт черной металлургии им. И.П. Бардина, Научный центр металловедения и физики металлов,
105005 Москва, ул. Радио, 23/9, стр. 2, Россия
b Санкт-Петербургский государственный университет
199034 Санкт-Петербург, Университетская набережная, 7–9, Россия
c Тольяттинский государственный университет, Научно-исследовательский институт прогрессивных технологий
445020 Тольятти, ул. Белорусская, 14, Россия
d Институт прикладных математических исследований, Карельский научный центр Российской академии наук
185910 Петрозаводск, ул. Пушкинская, 11, Россия
e Физико-технический институт им. А.Ф. Иоффе
194021 Санкт-Петербург, ул. Политехническая, 26, Россия
* E-mail: yuri1939@inbox.ru
Поступила в редакцию 10.02.2022
После доработки 24.03.2022
Принята к публикации 24.03.2022
- EDN: KJUSTK
- DOI: 10.31857/S0453881122040098
Аннотация
В настоящей работе рассмотрены некоторые фундаментальные аспекты (основы) решения существующей долгое время (обсуждаемой многими исследователями на протяжении около 25 лет) проблемы “супер” хранения (по терминологии Маеланда (Maeland)) в каталитически синтезированных графитовых нановолокнах (ГНВ) “обратимого” (в количестве порядка 20–30 вес. %) и “необратимого” водорода (в количестве порядка 7–10 вес. %). Проблема была сформулирована в связи с экспериментальными результатами (группа Родригес и Бекера (Rodriguez and Baker)), запатентованными и опубликованными в 1997–2005 гг., которые другие исследователи не могли ни воспроизвести (кроме, в определенной мере, группы Гупты (Gupta) (2000–2006 гг.)), ни раскрыть их физику. Для более глубокого изучения этой актуальной проблемы и выявления ряда фундаментальных (в том числе кинетических и термодинамических) аспектов ее решения нами была модифицирована и использована эффективная методика обработки и анализа спектров термодесорбции водорода, а также связанных с ними термогравиметрических и других данных. Впервые определены (как из термодесорбционных, так и из термогравиметрических данных) характеристики основного десорбционного пика “необратимого” водорода в графитовых нановолокнах, отвечающего кинетическому процессу первого порядка, а именно: температура наибольшей скорости десорбции (Tmax = 914–923 K), энергия активации процесса десорбции (Q ≈ 40 кДж/моль), предэкспоненциальный фактор константы скорости (K0 ≈ 2 × 10–1 c–1), количество выделившегося водорода (~8 вес. %, т.е. атомное отношение H/C ≈ 1). Рассмотрена физика процессов “супер” сорбции “необратимого” и “обратимого” водорода, в т.ч. роль процессов диффузии водорода, сопровождающейся “обратимым” захватом диффузанта определенными сорбционными центрами, а также роль водородного спилловер-эффекта, обеспечивающего локальную атомизацию газообразного H2 при гидрировании графитовых нановолокон, и роль явления Курдюмова по термоупругому равновесию фаз. Показано, что отмеченные выше экстраординарные данные по “супер” хранению водорода в ГНВ не являются ни ошибкой, ни мистификацией, как считает большинство исследователей. Определены необходимые условия для воспроизведения этих экстраординарных результатов другими исследователями. Показано, в частности, что группа Родригес и Бекера способна воспроизвести и “нормальные” результаты (порядка 0.1–4 вес. %) по хранению водорода в ГНВ, получаемые другими исследователями.
1. ВВЕДЕНИЕ
Как известно, одной из актуальных проблем водородной энергетики является проблема компактного и безопасного хранения “обратимого” водорода (т.е. водорода с достаточно быстрой кинетикой его извлечения при рабочих температурах) “на борту” автомобилей с топливными элементами. В этой связи становится весьма актуальной существующая уже длительное время (около 25 лет) проблема “супер” хранения (по терминологии Маеланда [1]) “обратимого” водорода в графитовых нановолокнах (ГНВ), описанная в работах [1–3], в которых, в частности, рассмотрена роль крупнейших корпораций (в т.ч. “Дженерал Моторс” и “Шелл”), и основанная на экстраординарных (никем не воспроизведенных и в должной мере не интерпретированных) результатах [4–12]. Многие исследователи (в т.ч. [13–16]) считают результаты [4–12] по меньшей мере ошибочными, поскольку не смогли ни воспроизвести эти результаты, ни раскрыть их физику.
Цель настоящей работы – вернуть внимание исследователей к решению этой актуальной проблемы, показав, что скорректированные результаты [4–12] не являются ошибкой или мистификацией, определив необходимые условия их воспроизведения другими исследователями, а также рассмотрев физику процессов.
В настоящей работе используется модифицированная (в определенной мере) методология [17–23] для анализа и интерпретации ряда экспериментальных данных, в т.ч. для обработки и анализа термодесорбционных (ТДС) и термогравиметрических (ТГ) спектров из работы [5] для “необратимого” водорода в ГНВ, а также рассматривается физика [2, 17, 18, 24, 25] “супер” хранения водорода в ГНВ, включающая спилловер-эффект [26–30] и явление термоупругого равновесия фаз Г.В. Курдюмова [31, 32].
2. МЕТОДОЛОГИЯ
Разработанная, в частности, для изучения отмеченной выше проблемы [1–3], методика [17–23], наиболее детально описанная в [20], позволяет из спектров ТДС и ТГ [5] для одной скорости нагрева (β) определить, как это сделано в следующем разделе настоящей работы, энергии активации (Q) и предэкспоненциальные множители (K0) констант скорости (K) процессов десорбции, соответствующие десорбционным пикам с разными температурами (Tmax) максимальной скорости десорбции. Следует отметить, что при разработке этой методики (методологии) был принят во внимание и ряд других работ [33–37].
Развитая методология [17–23] дает возможность раскрыть физику десорбционных процессов путем термодинамического анализа полученных характеристик термодесорбционных пиков и сопоставления с соответствующими независимыми экспериментальными и теоретическими данными. Методика [20] содержит несколько стадий реализации, в т.ч использование нескольких критериев достоверности и окончательное уточнение результатов с помощью методов численного моделирования [23].
Первая стадия заключается в аппроксимации исследуемого спектра наименьшим числом симметричных гауссианов. Вторая стадия состоит в определении в приближении реакции первого порядка для каждого из отмеченных выше гауссианов (из температурной зависимости скорости десорбции (–dθ/dt), деленной на β), константы скорости (K(T)) десорбции водорода при различных температурах около Tmax, откуда определяются (при помощи уравнения Аррениуса) значения Q и K0. При этом используется кинетическое уравнение для реакции первого порядка в виде:
где t – время; T – абсолютная температура; R – универсальная газовая постоянная; θ = (C/C0) – относительная средняя концентрация водорода в образце, отвечающая рассматриваемому гауссиану (для данных значений T и t); θ = 1 при t = 0.Соответствующий критерий достоверности (Q*) можно получить из условия максимальной скорости десорбции {d2θ/dT2 = 0} в виде:
где величины Tmax и K(Tmax) могут быть взяты (в удовлетворительном приближении) из полученных выше результатов для рассматриваемого гауссиана.Следующая стадия состоит в определении в приближении реакции второго порядка для каждого из отмеченных выше гауссианов величин Q и K0. При этом используется кинетическое уравнение для реакции второго порядка в виде:
Критерий достоверности (Q*) можно найти из условия {d2θ/dT2 = 0} в виде:
(4)
$Q{\kern 1pt} * \approx \frac{{2RT_{{{\text{max}}}}^{2}{{\theta }}\left( {{{T}_{{{\text{max}}}}}} \right)K\left( {{{T}_{{{\text{max}}}}}} \right)}}{{{\beta }}},$Завершающей стадией является уточнение (и/или подтверждение) полученных выше результатов с помощью численного моделирования [23] десорбционных спектров, с учетом (в смысле определенной фиксации) значений Q* и K(Tmax). Следует отметить, что в этом случае рассматриваемые спектры аппроксимируются не гауссианами, а пиками, соответствующими процессам первого или второго порядка; погрешность (разброс величин) при определении Q и ln K0 в большинстве случаев cоставляет около 15%.
Эффективность этой методологии подтверждается полученными с ее помощью и недавно опубликованными результатами исследований термодесорбции водорода в ряде углеродных наноструктур и графитных материалов [19–22, 25].
3. РЕЗУЛЬТАТЫ ИЗУЧЕНИЯ РЯДА ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ
3.1. Анализ и интерпретация ТДС и ТГ спектров группы Родригес и Бекера для “необратимого” водорода в ГНВ
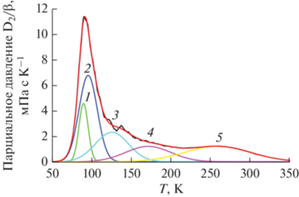
Результаты обработки и анализа (с использованием методики [20]) термодесорбционного (ТДС) спектра для “необратимого” водорода из работы [5] представлены на рис. 1a и в табл. 1. Следует отметить, что суммарное (уточненное) содержание “необратимого” водорода в ГНВ образцах (${{C}_{{{{{\text{H}}}_{2}}\Sigma }}}$ ≈ 11 ± 3 вес. %) определяли из данных [5, 8].
Рис. 1.
Обработка (с использованием методики [20]) термодесорбционных (ТДС) и термогравиметрических (ТГ) данных из работы [5] для “супер” десорбции “необратимого” водорода из ГНВ образцов со структурой типа “елочка” (см. рис. 2 в работе [5]). а – Аппроксимация тремя гауссианами (пики №№ 1–3) ТДС-спектра (β = 0.17 K/с) для образцов, подвергнутых гидрированию в газообразном H2 (при 300 K, 11–4 МПа, 24 ч); красная кривая отвечает сумме трех пиков. б – Аппроксимация тремя гауссианами (пики №№ 1–3) температурной производной ТГ-спектра для образцов, подвергнутых гидрированию в газообразном H2 (при 300 K, 11–4 МПа, 24 ч) и последующему нагреву (β = 0.17 K/с) в He; красная кривая отвечает сумме трех пиков.

Таблица 1.
| Пик № |
Tmax, K |
Порядок реакции |
Q, кДж/моль |
K0, с–1 |
K(Tmax), с–1 |
Q*, кДж/моль |
γ | ${{C}_{{{{{\text{H}}}_{{\text{2}}}}}}}$, вес. % |
H/C |
|---|---|---|---|---|---|---|---|---|---|
| 1 | 914 | 1 | 39 | 1.5 × 10–1 | 9 × 10–4 | 39 | 0.76 | 8.4 | 1.1 |
| 2 | 77.5 | 5.1 × 101 | 2 × 10–3 | 77.5 | |||||
| 2 | 1036 | 1 | 199 | 4.2 × 107 | 4 × 10–3 | 198 | 0.02 | 0.2 | 0.02 |
| 2 | 398 | 8.8 × 1017 | 7 × 10–3 | 396 | |||||
| 3 | 1161 | 1 | 126 | 8.5 × 102 | 2 × 10–3 | 125 | 0.22 | 2.4 | 0.30 |
| 2 | 250 | 7.0 × 108 | 4 × 10–3 | 250 |
Результаты обработки и анализа [20] термогравиметрического (ТГ) спектра из работы [5] приведены на рис. 1б и в табл. 2. Имеются основания (в частности, из рассмотрения кривых (a), (b) и (c) на рис. 7 в [5]) полагать, что пик № 3 на рис. 1б в основном связан с газификацией атомов углерода и/или кислородосодержащих функциональных комплексов (групп). При этом следует принять во внимание, что в работе [5] при нагревании материала в инертной атмосфере при температурах до 1300 K углеводородных продуктов обнаружено не было. Поэтому значение атомного отношения Н/С для пика № 3 (на рис. 1б) может быть пренебрежимо мало, и нет необходимости более точно аппроксимировать этот пик.
Таблица 2.
| Пик № |
Tmax, K |
Порядок реакции | Q, кДж/моль |
K0, с–1 |
K(Tmax), с–1 |
Q*, кДж/моль |
γ | Вес. % | H/C |
|---|---|---|---|---|---|---|---|---|---|
| 1 | 923 | 1 | 43 | 2.9 × 10–1 | 1 × 10–3 | 43 | 0.23 | 8.5 | 1.1 |
| 2 | 87 | 1.7 × 102 | 2 × 10–3 | 87 | |||||
| 2 | 1165 | 1 | 152 | 1.5 × 104 | 2 × 10–3 | 152 | 0.08 | 2.9 | 0.4 |
| 2 | 304 | 2.0 × 1011 | 4 × 10–3 | 303 | |||||
| 3 | 1345 | 1 | 149 | 1.0 × 103 | 2 × 10–3 | 148 | 0.69 | 26 | * |
| 2 | 298 | 1.2 × 109 | 1 × 10–2 | 297 |
С другой стороны, значительный уровень шума для спектра на рис. 1б не мешает определять характеристики основного водородного пика № 1 (рис. 1б) с требуемой (для решения поставленной цели) точностью.
Анализ (с использованием методологии [20]) полученных результатов (табл. 1 и 2) для основного процесса десорбции “необратимого” водорода (пик № 1 на рис. 1а и 1б) из ГНВ образцов [5] показывает, что имеет место процесс (реакция) первого порядка (выражение (1)), которому отвечают следующие характеристики: Tmax = 914–923 K, Q ≈ ≈ 40 кДж/моль, K0 ≈ 2 × 10–1 c–1, ${{C}_{{{{{\text{H}}}_{2}}\Sigma }}}$ ≈ 8 вес. % (т.е. атомное отношение H/C ≈ 1). Десорбционный процесс лимитируется диффузией водорода, сопровождающейся “обратимым” захватом [17, 18, 34–36] диффузанта определенными центрами хемосорбции водорода в ГНВ. Это сопоставимо с диффузионными процессами типа I и II (с энергиями активации QI ≈ 20 кДж/моль и QII ≈ ≈ 120 кДж/моль соответственно), рассмотренными в работах [17, 18] с открытым доступом в Интернете. Полученная энергия активации десорбции (Q ≈ 40 кДж/моль, табл. 1 и 2) является (как и отмеченные выше величины QI и QII) эффективной энергией активации такой диффузии и близка (по абсолютной величине) к энергии связи диффузанта с соответствующими хемосорбционными центрами в углеродном материале [17, 18]. Очевидно, центры локализованы как бы между базовыми углеродными плоскостями в ГНВ [5]; при этом они почти полностью заполнены водородом, т.е. эти базовые углеродные плоскости как бы разделены слоями хемосорбированного водорода (как в многослойном графане [18]).
Характеристический диффузионный размер для рассматриваемого процесса можно оценить (с точностью до порядка величины) при помощи известного [17, 34] выражения L ≈ (D0/K0)1/2. В этом выражении величина предэкспоненциального фактора эффективного коэффициента диффузии водорода (D0) в ГНВ [5] может находиться в интервале соответствующих величин для процессов типа I и II в [17, 18] (т.е. в интервале от D0I ≈ 3 × 10–3 до D0II ≈ 2 × 103 см2/с), что отвечает величине L ≈ (1 × 10–1–1 × 102) см. В полученном интервале возможных значений L находится наиболее приемлемая величина Lобр. ≈ 1 см, отвечающая определенному размеру образца [4, 5] (пучка графитовых нановолокон), приводящая к вполне приемлемому искомому значению D0 ≈ 5 см2/с.
Аналогичным образом [17–23] можно рассмотреть и результаты обработки (табл. 1 и 2) остальных (менее значимых) десорбционных пиков (на рис. 1а и 1б).
3.2. Анализ и интерпретация кинетических данных группы Родригес и Бекера по “супер” сорбции “обратимого” водорода (~30 вес. %) в ГНВ
Как следует из результатов обработки кинетических данных из работы [4] по изменению давления водорода в рабочей камере при “супер” адсорбции “обратимого” водорода (при температуре около 300 K) для трех образцов (№№ 1, 2 и 3) графитовых нановолокон со структурой типа “елочка”, представленных на рис. 2, процесс протекает как реакция первого порядка с константами скорости: K1ads.rev. = 2.7 × 10–5 c–1, K2ads.rev. = 3.8 × × 10–5 c–1 и K3ads.rev = 2.8 × 10–5 c–1 соответственно. Характеристическое время “супер” адсорбции “обратимого” водорода (tads.rev. = 1/Kads.rev) здесь составляло около 9 ч, а время гидрирования образцов – 24 ч.
Рис. 2.
Обработка (в приближении реакции первого порядка) кинетических данных из работы [4] по изменению давления водорода в рабочей камере при “супер” адсорбции “обратимого” водорода (при температуре около 300 K) для трех образцов графитовых нановолокон сo структурой типа “елочка”.

Имеются основания полагать, что процесс лимитируется диффузией водорода на характеристическое расстояние Lобр. ≈ 1 см, отвечающее размеру образца [4, 5] (пучка графитовых нановолокон), и сопровождается “обратимым” захватом [17, 18, 34–36] диффузанта определенными сорбционными центрами в графитовых нановолокнах. Это приводит к приемлемому значению эффективного коэффициента диффузии “обратимого” водорода (Dads.rev ≈ ($L_{{{\text{обр}}{\text{.}}}}^{2}$ × Kads.rev.) ≈ 3 × 10–5 cм2/c), возможному при “обратимом” захвате диффузанта центрами хемосорбции, отвечающими отмеченному выше (в разделе 3.1.) процессу типа I [17], и/или центрами физической сорбции [17, 38] в углеродном наноматериале (см. раздел 5 статьи).
Как показано в работе [4], время “супер” десорбции (при 300 K) преобладающей части “обратимого” водорода из ГНВ-образцов составляло около 10 мин, т.е. характеристическое время десорбции “обратимого” водорода можно принять (с точностью до порядка величины) как tdes.rev = = (1/Kdes.rev) ≈ 6 × 102 с, где Kdes.rev – константа скорости процесса десорбции (в приближении реакции первого порядка). Полагая, что процесс лимитируется диффузией водорода на характеристическое расстояние Lобр. ≈ 1 см, отвечающее размеру образца [4, 5], и сопровождается “обратимым” захватом диффузанта определенными сорбционными центрами в графитовых нановолокнах, получаем приемлемое значение эффективного коэффициента диффузии “обратимого” водорода (Ddes.rev ≈ ($L_{{{\text{обр}}}}^{2}$ × Kdes.rev) ≈ 1.7 × 10–3 cм2/c), возможное при “обратимом” захвате диффузанта центрами физической сорбции [17, 38] в углеродном наноматериале (см. также раздел 5 статьи). В данном случае центры хемосорбции в ГНВ [4, 5], по-видимому, могут иметь предельное заполнение водородом, то есть определенное насыщение, что приводит к прекращению их влияния на диффузию водорода (см. уравнения (11) и (8′) в работе [39] с открытым доступом в Интернете).
3.3. Рассмотрение кинетических данных группы Родригес и Бекера по рентгеновской дифракции
Рентгеноструктурные эксперименты группы Родригес и Бекера показали (см. рис. 12 в [5]), что гидрирование вызывает увеличение межплоскостного расстояния в графитовых нановолокнах от исходного значения a0 = 0.340 нм (перед гидрированием) до значения ahyd = 0.347 нм (после гидрирования продолжительностью 24 ч и удаления “обратимого” водорода). Такое расширение решетки может быть обусловлено “супер” адсорбцией “необратимого” водорода до определенного содержания Сhyd ≈ 8 вес. %, отвечающего десорбционному пику № 1 на рис. 1а (см. раздел 3.1, а также Приложение: Модель полости). При этом можно полагать, что (ahyd. – a0) = χ × Сhyd, где коэффициент пропорциональности χ ≈ 9 × 10–4 нм/вес. %.
Показано (см. рис. 12 в [5]), что десорбционная выдержка (гидрированных образцов) продолжительностью t1 = 24 ч на воздухе при температуре 300 K приводит к значению межплоскостного расстояния a24 = 0.345 нм и соответствующему содержанию “необратимого” водорода С24, а десорбционная выдержка продолжительностью t2 = 48 ч – к значению a48 = 0.342 нм и содержанию водорода С48. В рамках такой модели можно показать, что [(ahyd – a24)/(ahyd – a48)] = [{1 – exp (–24K)}/{1 – ‒ exp (–48K)}], где K (ч–1) – константа скорости десорбционного процесса при 300 K, который рассматривается в приближении реакции первого порядка.
Подстановка экспериментальных значений межплоскостного расстояния приводит к величине [(ahyd – a24)/(ahyd – a48)] = 0.4, которая существенно отличается от предельного (при K → 0) значения lim [{1 – exp (–24K)}/{1 – exp (–48K)}] = 0.5. Следует отметить, что величина [(ahyd – a24)/(ahyd – $a_{{48}}^{*}$)] = 0.5, если использовать возможное (в пределах погрешности измерений) значение межплоскостного расстояния $a_{{48}}^{*}$ = 0.343 нм (вместо a48 = 0.342 нм).
Для оценки константы скорости (при 300 K) рассматриваемого процесса можно использовать выражение K = –(1/t) ln(Ct/Chyd), где время выдержки t равно 24 и 48 ч, а соответствующее содержание водорода Ct составляет C24 = 5.6 вес. % и C48 = 2.2 вес. % (или $С_{{48}}^{*}$ = 3.3 вес. %). Отсюда получаем (с точностью до порядка величины) значение K = Kdes.irrev 300 K ≈ 1.7 × 10–2 ч–1, отвечающее характеристическому времени десорбции ~60 ч.
Такое значение константы скорости десорбции “необратимого” водорода (Kdes.irrev.300K) находится в удовлетворительном соответствии с кинетическими данными группы Родригес и Бекера по изменению распределения пор по размерам в ГНВ образцах, где продолжительность десорбционной выдержки при 300 K составляла 92 ч (см. рис. 11 в [5]).
Вместе с тем следует подчеркнуть, что такое значение константы скорости (Kdes.irrev.300K ≈ 4.6 × × 10–6 с–1) на два порядка превышает величину константы скорости при 300 K, получаемую при использовании характеристик (Q и K0) для десорбционного пика № 1 (рис. 1a и табл. 1).
Анализ показывает, что десорбционный процесс лимитируется диффузией водорода на характеристическое расстояние Lобр. ≈ 1 см, отвечающее размеру образца [5] (пучка графитовых нановолокон), и сопровождается “обратимым” захватом диффузанта определенными сорбционными центрами в графитовых нановолокнах. Это приводит к приемлемому значению эффективного коэффициента диффузии “необратимого” водорода при 300 K (Ddes.irrev 300 K ≈ ($L_{{{\text{обр}}}}^{2}$ × Kdes.irrev 300 K) ≈ ≈ 5 × 10–6 cм2/c), возможному при “обратимом” захвате диффузанта центрами хемосорбции в ГНВ, отвечающими процессу типа I в работе [17], и/или центрами физической сорбции [17, 38] (см. раздел 5 данной статьи).
3.4. Рассмотрение результатов группы Гупты по “супер” сорбции “обратимого” водорода (~17 вес. %) в ГНВ
Полученные группой Гупты данные [10, 11] по многократной “супер” сорбции “обратимого” водорода в графитовых нановолокнах, представленные (в определенной мере) на рис. 3 и 4, можно рассматривать как удовлетворительное воспроизведение данных [5, 8] группы Родригес и Бекера (см. раздел 3.2). Имеет место соответствие (в пределах одного порядка величины) как по количеству “обратимого” водорода (~15 и ~17 вес. % (рис. 3a и 4)), так и по величине характеристического времени его десорбции при 300 K (tdes.rev = = (1/Kdes.rev) ≈ 1 × 103 с, где Kdes.rev – константа скорости процесса десорбции, получаемая из кинетических данных на рис. 3б.
Рис. 3.
Обработка термодинамических и кинетических данных из работы [10] по “супер” сорбции “обратимого” водорода (~15 вес. %) для образцов ГНВ с “пластинчатой” структурой (см. рис. 4), подвергнутых гидрированию (24 ч) в газообразном молекулярном водороде (при давлении 12 МПа и температуре 300 К) и последующему дегидрированию при понижении давления водорода до 0.1 МПа: а – обработка адсорбционных данных в приближении изотермы сорбции типа Генри–Ленгмюра [17]; б – обработка термодесорбционных данных в приближении реакции первого порядка.

Рис. 4.
На микрофотографии графитовых нановолокон [11], подвергнутых гидрированию (24 ч) в газообразном молекулярном водороде при давлении 12 МПа и температуре 300 К до содержания “обратимого” водорода ~17 вес. %, показаны размеры линзообразных нанополостей в одном из нановолокон, необходимые для оценки (см. работы [2, 17, 18, 24]) объема таких нанополостей и плотности локализованного в них “обратимого” водорода, отмеченной (красной точкой) на диаграмме состояния дейтерия на рис. 5a.

Как показано в работах [2, 17, 18, 24, 25], результаты ПЭМ (рис. 4) можно рассматривать как прямое экспериментальное свидетельство (доказательство) многократной “супер” адсорбции “обратимого” водорода (~17 вес. %) в ГНВ [11].
3.5. Физика “супер” хранения “обратимого” водорода в ГНВ
Согласно [2, 17, 18, 24, 25] физика экстраординарных результатов [5, 8, 10, 11] по “супер” хранению “обратимого” водорода (около 20–30 вес. %) в графитовых нановолокнах может быть связана с водородным спилловер-эффектом [26–30], обеспечивающим атомизацию молекулярного водорода и проявляющимся вблизи частиц металлического катализатора в ГНВ-образцах, а также с явлением термоупругого равновесия фаз Г.В. Курдюмова [31, 32]. При этом имеет место термоупругое “мегабарное” сжатие (до твердого состояния, см. диаграммы состояния на рис. 5) молекулярного водорода, локализованного в линзообразных нанополостях (рис. 4) между базовыми углеродными слоями материала, которое происходит за счет энергии ассоциации атомов водорода, проникающих в закрытые нанополости через определенные дефекты в графеновом материале (см. работы [18, 22, 40]). В этой связи следует отметить, что образующиеся в закрытых нанополостях молекулы водорода не могут выйти из них обратно, поскольку дефекты пропускают только атомарный водород, при этом имеет место определенная очистка водорода, используемого для гидрирования ГНВ-образцов.
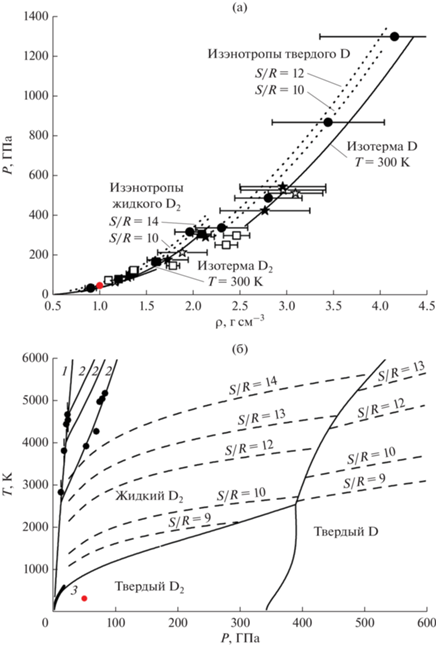
Рис. 5.
Диаграммы состояния дейтерия (из [45]), на которых показаны (красными точками) результаты анализа [2, 17, 18, 24, 25] экспериментальных данных [11]: a – изэнтропы и изотермы (300 K) молекулярного и атомарного дейтерия. Символами показаны экспериментальные данные, кривыми – результаты расчета. Плотность ρ протия увеличена в два раза. Утолщенный отрезок кривой – экспериментальная изотерма (300 K) для твердого молекулярного водорода; б – фазовая диаграмма дейтерия. Ударные адиабаты и изэнтропы для дейтерия по уравнению состояния: 1 и 2 – однократная и двукратная адиабаты; ⚫ – экспериментальные данные; 3 – кривая плавления; утолщенный участок – эксперимент.
4. АНАЛИЗ ДАННЫХ ТДС (РЗЕПКА И ДР.) ДЛЯ “НЕОБРАТИМОГО” ВОДОРОДА В ГНВ
Результаты обработки и анализа ТДС данных [13, 14], которые были получены с консультативным участием Р.Т.К. Бекера [8], представлены на рис. 6 и в табл. 3.
Рис. 6.
Аппроксимация двумя гауссианами термодесорбционного спектра (кинетические кривые “0.08 мас. %” и “0.02 мас. %” из рис. 18 в [13]) для образца № 3 ГНВ с структурой типа “елочка” (табл. 3 в [13]), подвергнутого воздействию газообразного молекулярного водорода при давлении 13 МПа и последующему нагреву от 293 K (β = 0.10 K/с) до остановки и изотермической выдержке при 1173 K.

Таблица 3.
| Пик № |
Tmax, K | Порядок реакции | Q, кДж/моль |
K0, с–1 | K(Tmax), с–1 |
Q*, кДж/моль |
γ | Вес. % | H/C |
|---|---|---|---|---|---|---|---|---|---|
| 1 | 1203 | 1 | 163 | 1.6 × 104 | 1.3 × 10–3 | 162 | 0.96 | 0.08 | 0.010 |
| 2 | 325 | 3.6 × 1011 | 2.7 × 10–3 | 324 | |||||
| 2 | 397 | 1 | 68 | 4.5 × 106 | 5.1 × 10–3 | 67 | 0.04 | 0.02 | 0.002 |
| 2 | 133 | 4.1 × 1015 | 1.0 × 10–3 | 134 |
Характеристики основного десорбционного пика № 1.6 на рис. 6 (Tmax, Q, K0, ${{C}_{{{{{\text{H}}}_{{\text{2}}}}}}}$; табл. 3) сильно отличаются от аналогичных характеристик основного десорбционного пика № 1.1a на рис. 1a (табл. 1), т.е. пик типа № 1.1a отсутствует в ТДС-спектре для ГНВ-образцов [13, 14].
В работе [13], в частности, отмечали (на стр. 8), что Родригес и Бекер [5, 7] считали наличие определенного высокотемпературного десорбционного пика индикатором (атрибутом) материала для “супер” хранения “обратимого” водорода, при этом они [5, 7] связывали этот пик со сравнительно малой частью запасенного водорода, которая могла высвобождаться только при высоких температурах, т.е. с наличием относительно небольшого количества “необратимого” водорода. Очевидно, Родригес и Бекер [5, 7] имели в виду десорбционный пик типа № 1.1a (рис. 1a и табл. 1), но они не определяли его характеристики (Q и K0).
Следует подчеркнуть, что такую десорбцию сравнительно небольшого количества “необратимого” водорода (отвечающего пику типа № 1.1a) из гидрированных ГНВ отмечали и в работах группы Гупты [9–12].
Пик типа № 1.1a отсутствовал в ТДС-спектрах ГНВ в работах [13, 14] (рис. 3), поэтому там не удалось воспроизвести результаты [5, 8, 10, 11] по “супер” хранению “обратимого” водорода в ГНВ.
В работах [13, 14] (с участием Р.Т.К. Бекера [8] в качестве консультанта) воспроизвели самое низкое (из известных, см. рис. 3 в аналитическом обзоре [17]) значение количества адсорбированного графитовыми нановолокнами водорода (около 0.1 вес. %), полученное группой Тиббеттса [16] (из Исследовательского центра корпорации “Дженерал Моторс” (см. [2, 3])).
В этой связи следует также подчеркнуть, что типичные результаты по хранению водорода в ГНВ (см. рис. 3 в [17]), полученные другими исследователями, были воспроизведены группой Родригес и Бекера (см. рис. 5 в [5], где количество водорода составляет ~2 вес. %, а также рис. 4 в [44] с количеством водорода ~3 вес. %).
Как отмечено в [17], для воспроизведения экстраординарных результатов [5, 8, 10, 11] групп Родригес–Бекера и Гупты по “супер” хранению “обратимого” водорода (~20–30 вес. %) необходимо раскрыть использованные ими ноу-хау технологии активационной обработки ГНВ, обеспечивающей появление в ТДС-спектрах пика типа № 1.1a (рис. 1a).
5. АНАЛИЗ ТДС ДАННЫХ (СУДАН И ДР.) ПО ФИЗИЧЕСКОЙ СОРБЦИИ ВОДОРОДА В ОУНТ
Результаты обработки и анализа данных ТДС [46] по физической сорбции водорода в одностенных углеродных нанотрубках (ОУНТ) представлены на рис. 7 и в табл. 4.
Таблица 4.
| Пик № | Tmax, K | Q, кДж/моль |
K0, с–1 | K(Tmax), с–1 |
Q*, кДж/моль |
γ | Вес. % | D/C |
|---|---|---|---|---|---|---|---|---|
| 1 | 90 | 9.2 | 2.1 × 103 | 9.1 × 10–3 | 9.1 | 0.11 | 0.13 | 0.008 |
| 2 | 95 | 5.3 | 3.5 × 100 | 4.6 × 10–3 | 5.2 | 0.33 | 0.40 | 0.024 |
| 3 | 126 | 5.0 | 3.0 × 10–1 | 2.5 × 10–3 | 5.0 | 0.20 | 0.24 | 0.014 |
| 4 | 172 | 6.8 | 2.2 × 10–1 | 1.9 × 10–3 | 6.8 | 0.14 | 0.17 | 0.010 |
| 5 | 259 | 10.7 | 1.8 × 10–1 | 1.3 × 10–3 | 10.7 | 0.21 | 0.25 | 0.015 |
Величины (табл. 4) энергии активации десорбции (Q) и предэкспоненциального фактора константы скорости (K0), полученные для пяти самопроявляющихся десорбционных пиков (рис. 7), очевидно, связаны с известными процессами физической адсорбции водорода углеродными наноструктурами [17, 38], которые можно аппроксимировать как реакции первого порядка. Эти величины использовались в разделах 3.2 и 3.3 при интерпретации обсуждаемых там результатов.
6. ЗАКЛЮЧЕНИЕ
1. Проведенное в настоящей работе изучение (с использованием методологии и результатов [17–25]) ряда кинетических и термодинамических аспектов (основ) решения проблемы “супер” хранения водорода в графитовых нановолокнах (ГНВ) [1–3] показывает, что полученные в работах [5–12] экспериментальные экстраординарные результаты (аккумулирование порядка 20–30 вес. % “обратимого” водорода и порядка 7–10 вес. % “необратимого” водорода) не являются ни ошибкой, ни мистификацией.
2. Продемонстрировано, что физика аккумулирования ~20–30 вес. % “обратимого” водорода высокой плотности, интеркалированного в нанополостях между базовыми углеродными слоями в ГНВ, связана с проявлением спилловер-эффекта и явления Курдюмова по термоупругому равновесию фаз.
3. Проведенное исследование свидетельствует, что существует реальная возможность воспроизведения экстраординарных экспериментальных результатов [5–12], но только при раскрытии использованных в этих работах ноу-хау технологий активирования ГНВ, приводящего к появлению в материале термодесорбционного пика типа № 1 (рис. 1а), отвечающего “необратимому” хемосорбированному водороду (в количестве ~8 вес. %) с определенными кинетическими и термодинамическими характеристиками.
4. В этой связи необходимы дальнейшие экспериментальные и теоретические исследования.
5. Имеются основания ([1–3] и др.) полагать, что в обозримом будущем эти ноу-хау технологии будут использованы одной из крупнейших автомобильных компаний для получения большого конкурентного преимущества.
Список литературы
Maeland A.J. // Int. Sc. J. Alternative Energy Ecology. 2002. V. 1. P. 19.
Nechaev Yu.S., Yurum A., Tekin A., Yavuz N.K., Yürüm Y., Veziroglu T.N. // Am. J. Anal. Chem. 2014. V. 5. № 16. P. 1151.
Nechaev Yu.S., Makotchenko V.G., Shavelkina M.B., Nechaev M.Yu., Veziroglu A. Veziroglu T.N. // Open J. Energy Efficiency. 2017. V. 6. P. 73.
Chambers A., Park C., Baker R.T.K., Rodriguez N.M. // J. Phys. Chem. B. 1998. V. 102. P. 4253.
Park C., Anderson P.E., Chambers A., Tan C.D., Hidalgo R., Rodriguez N.M. // J. Phys. Chem. B. 1999. V. 103. P. 10572.
Rodriguez N.M., Baker R.T.K. Storage of hydrogen in layered nanostructures. U.S. Patent 5653951, 1997.
Rodriguez N.M., Baker R.T.K. Method for introducing hydrogen into layered nanostructures. U.S. Patent 6159538, 2000.
Baker R.T.K. Encyclopedia of Materials: Science and Technology. Amsterdam: Elsevier, 2005. 932 p.
Gupta B.K., Srivastava O.N. // J. Hydr. Energy. 2000. V. 25. P. 825.
Gupta B.K., Srivastava O.N. // J. Hydr. Energy. 2001. V. 26. P. 857.
Gupta B.K., Tiwari R.S., Srivastava O.N. // J. Alloys Comp. 2004. V. 381. P. 301.
Gupta B.K., Srivastava O.N. // International Scientific Journal for Alternative Energy and Ecology. 2006. V. 5. P. 63.
Rzepka M., Bauer E., Reichenauer G., Schliermann T., Bernhardt B., Bohmhammel K., Braue W. // J. Phys. Chem. B. 2005. V. 109. P. 14979.
Reichenauer G., Rzepka M., Bauer E., Schliermann T., Bernhardt B., Bohmhammel K., Braue W. Hydrogen storage capacity of catalytically grown carbon nanofibers. In: Proceedings of Int. Conf. on Carbon. Aberdeen: The Robert Gordon Univ., 2006.
Hirscher M., Becher M., Haluska M., Quintel A., Skakalova V., Choi Y.-M., Fink J. // J. Alloys Comp. 2002. V. 330. P. 654.
Tibbetts G.G., Meisner G.P., Olk C.H. // Carbon. 2001. V. 39. P. 2291.
Нечаев Ю.С. // УФН. 2006. Т. 176. № 6. С. 581. (Nechaev Yu.S. // Physics-Uspekhi. 2006. V. 49. № 6. P. 563.)
Nechaev Yu.S., Veziroglu T.N. // Int. J. Phys. Sci. 2015. V. 10. P. 54.
Nechaev Yu.S., Alexandrova N.M., Shurygina N.A., Cheretaeva A.O., Kostikova E.K., Öchsner A. // J. Nucl. Mater. 2020. V. 535. P. 52162.
Nechaev Yu.S., Alexandrova N.M., Cheretaeva A.O., Kuznetsov V.L., Öchsner A., Kostikova E.K., Zaika Y.V. // Int. J. Hydrogen Energy. 2020. V. 45. № 46. P. 25030.
Нечаев Ю.С., Александрова Н.М., Шурыгина Н.А., Черетаева А.О., Денисов Е.А., Костикова Е.К. // Изв. Акад. наук. Сер. физ. 2021. Т. 85. № 7. С. 910.
Nechaev Yu.S., Denisov E.A., Shurygina N.A., Cheretaeva A.O., Kostikova E.K., Davydov S.Yu., Öchsner A. // J. Carb. Res. C. MDPI. 2022. V. 8. I. 1(6). P. 1.
Zaika Y.V., Kostikova E.K., Nechaev Yu.S. // Tech. Phys. 2021. V. 66. № 2. P. 210.
Nechaev Yu.S., Alexandrova N.M., Shurygina N.A., Cheretaeva A.O. // Fullerenes, Nanotubes and Carbon Nanostructures. 2020. V. 28. P. 233.
Нечаев Ю.С., Денисов Е.А., Шурыгина Н.А., Черетаева А.О., Костикова Е.К., Давыдов С.Ю. // Письма в ЖЭТФ. 2021. Т. 114. № 5–6(9). С. 372.
Yang R.T., Wang Y. // J. Am. Chem. Soc. 2009. V. 131. P. 4224.
Zacharia R., Rather S., Hwang S.W., Nahm K.S. // Chem. Phys. Lett. 2007. V. 434. P. 286.
Zhou C., Wu J., Nie A., Forrey R.C., Tachibana A., Cheng H. // J. Phys. Chem. C. 2007. V. 111, P. 12773.
Zielinski M., Wojcieszak R., Monteverdi S., Mercy M., Bettahar M.M. // Int. J. Hydrogen Energy. 2007. V. 32. P. 1024.
Karim W., Spreafico C., Kleibert A., Gobrecht J., VandeVondele J., Ekinci Y., van Bokhoven J.A. // Nature. 2017. V. 541. P. 68.
Лободюк В.А., Эстрин Э.И. Мартенситные превращения. Москва: Физматлит, 2009. 352 с.
Коваль Ю.Н. // УФН. 2005. Т. 6. № 2. С. 169.
Habenschaden E., Küppers J. // Surf. Sci. 1984. V. 138. L147.
Wei F.-G., Enomoto M., Tsuzaki K. // Comput. Mater. Sci. 2012. V. 51. P. 322.
Legrand E., Oudriss A., Savall C., Bouhattate J., Feaugas X. // Int. J. Hydrogen Energy. 2015. V. 40. P. 2871.
Ebihara K.-I., Kaburaki H., Suzudo T., Takai K. // ISIJ Int. 2009. V. 49. P. 1907.
Zhao X., Outlaw R.A., Wang J.J., Zhu M.Y., Smith G.D., Holloway B.J. // J. Chem. Phys. 2006. V. 124. P. 194704.
Nayyar I., Ginovska B., Karkamkar A., Gennett T., Autrey T. // J. Carbon Res. 2020. V. 6. P. 1.
Нечаев Ю.С. // УФН. 2001. Т. 171. № 11. С. 1251. (Nechaev Yu.S. // Physics-Uspekhi. 2001. V. 44. № 11. P. 1189.)
Hu S., Lozada-Hidalgo M., Wang F.C., Mishchenko A., Schedin F., Nair R.R., Hill E.W., Boukhvalov D.W., Katsnelson M.I., Dryfe R.A.W., Grigorieva I.V., Wu H.A., Geim A.K. // Nature. 2014. V. 516. P. 227.
Давыдов С.Ю., Сабирова Г.И. // Письма в ЖТФ. 2011. Т. 37. № 11. С. 51. (Davydov S.Yu., Sabirova G.I. // Techn. Phys. Lett. 2011. V. 37. P. 515.)
Liu Z., Liu J.Z., Cheng Y., Li Z., Wang L., Zheng Q. // Phys. Rev. B. 2021. V. 85. P. 205418.
Wang W., Dai S., Li X., Yang J., Srolovitz D.J., Zheng Q. // Nature Commun. 2015. V. 6. P. 7853.
Lueking A.D., Yang R.T., Rodriguez N.M., Baker R.T.K. // Langmuir. 2004. V. 20. № 3. P. 714.
Трунин Р.Ф., Урлин В.Д., Медведев А.Б. // УФН. 2010. Т. 180. № 6. С. 605. (Trunin R.F., Urlin V.D., Medvedev A.B. // Physics-Uspekhi. 2010. V. 53. № 6. P. 577.)
Sudan P., Zuettel A., Mauron P., Emmenegger C., Wenger P., Schla L. // Carbon. 2003. V. 41. № 12. P. 2377.
Дополнительные материалы отсутствуют.
Инструменты
Кинетика и катализ