Коллоидный журнал, 2019, T. 81, № 3, стр. 338-343
Стабилизация наночастиц серебра в воде катионным сополимером на основе поли(аминоэтилметакрилата)
А. С. Сеньчукова 1, М. Е. Михайлова 1, А. А. Лезов 1, Е. В. Лебедева 1, А. Н. Подсевальникова 1, Н. В. Цветков 1, *
1 Санкт-Петербургский государственный университет,
кафедра молекулярной биофизики и физики полимеров
199034 Санкт-Петербург, Университетская наб., 7/9, Россия
* E-mail: n.tsvetkov@spbu.ru
Поступила в редакцию 24.11.2018
После доработки 01.12.2018
Принята к публикации 04.12.2018
Аннотация
Продемонстрирована способность катионного сополимера на основе поли(аминоэтилметакрилата) к стабилизации дисперсий серебряных наночастиц в водных средах. Наночастицы получали путем химического восстановления в водном растворе AgNO3 с использованием борогидрида натрия в присутствии катионного статистического тройного сополимера – поли(2-аминоэтилметакрилат-со-N-метил-2-аминоэтилметакрилат-co-N,N-диметил-2-аминоэтилметакрилата). Методом спектрофотометрии показано, что в присутствии сополимера формируются дисперсии серебра, устойчивые в течение продолжительного времени (более полугода). Методами динамического рассеяния света и сканирующей электронной спектроскопии получена согласующаяся информация о размерах стабилизированных наночастиц и их распределении по размерам.
ВВЕДЕНИЕ
Создание и изучение свойств различных материалов с применением нанотехнологического подхода является одним из самых популярных направлений современной науки. [1–3] В первую очередь это связано с уникальностью характеристик наноматериалов, существенно отличающихся от характеристик их “больших” аналогов [4]. Особое место в современных исследованиях занимают металлосодержащие наноматериалы, а именно наночастицы (НЧ) [5, 6], нанокластеры [7] и нанопровода [8], благодаря их экстраординарным электрическим, каталитическим, тепловым и магнитным свойствам [9]. Металлические НЧ используются во многих сферах, таких как биомедицина [10], пищевая [11] и химическая промышленность [12], электроника [13], катализ [14], создание электрохимических датчиков [15] и т.д.
Особое место занимают НЧ благородных металлов, поскольку они обладают выраженными антибактериальными свойствами [16]. Благодаря относительно невысокой стоимости и широким возможностям биотехнологических применений наибольшую популярность приобрели НЧ серебра, которые с успехом используются, в частности, при диагностике и лечении онкологических заболеваний [17, 18].
Очевидно, что многие сферы применения предполагают использование НЧ серебра в растворе. Однако коллоидные растворы серебра неустойчивы из-за большой склонности НЧ к окислению и агрегированию, что приводит к выпадению их из раствора. Для решения этой проблемы используют разнообразные стабилизирующие агенты, такие как поверхностно-активные вещества и полимеры различной архитектуры (линейные, гребнеобразные, разветвленные). Особое место среди полимеров, которые применяются для стабилизации дисперсий металлических НЧ, занимают полиэлектролиты, ввиду того, что они сами могут проявлять противомикробные, противоопухолевые, противовоспалительные и антиоксидантные свойства [19–22] и тем самым усиливать соответствующие свойства НЧ серебра. Химическая структура полиэлектролитов может быть чрезвычайно разнообразной, но по своему типу (заряду цепи) они подразделяются на два больших класса – поликатионы и полианионы. Особо следует отметить катионные полимеры, содержащие аминогруппы, которые, благодаря достаточно легкому синтезу, вариативности свойств, применимости в различных областях, снискали себе заслуженную популярность. Такие полимеры уже эффективно применяются в качестве носителей генов (при создании генных векторов), а также в терапии различных заболеваний [22–25].
Расширить области применения катионных полимеров и тонко настроить их характеристики под конкретную задачу возможно путем сополимеризации мономеров различного химического строения [26, 27].
Одной из проблем, с которой приходится сталкиваться при исследовании и интерпретации свойств сложных супрамолекулярных структур, таких, например, как комплексы полимеров с НЧ, является их значительная полидисперсность. Ее причина кроется, в том числе, в полидисперсности исходных полимерных компонентов. Нивелировать этот негативный фактор позволяет, в частности, контролируемая радикальная полимеризация с обратимой передачей цепи по механизму присоединение–фрагментация (RAFT-полимеризация). Используя этот подход, можно синтезировать полимеры с достаточно узкими молекулярно-массовыми распределениями [28].
Целью настоящей работы является изучение способности катионного сополимера, синтезированного RAFT-полимеризацией [29], стабилизировать дисперсии серебряных НЧ в водных средах и исследование характеристик полученных структур НЧ–полимер.
МЕТОДЫ, МАТЕРИАЛЫ И ПРОЦЕДУРА СИНТЕЗА НАНОЧАСТИЦ
Методы
Абсорбционная спектрофотометрия. Для регистрации наличия НЧ в растворе и наблюдения за динамикой их формирования была использована абсорбционная спектрофотометрия (спектрофотометр UV-1800, Shimadzu Corp., Япония). Спектры поглощения (Abs) измеряли в диапазоне длин волн λ ∈ [190–1100] нм с шагом 1 нм в кварцевых кюветах с длиной оптического пути 1 см.
Динамическое рассеяние света (ДРС). Исследование методом ДРС проводили с помощью установки Photocor Complex (Photocor Instruments Inc., Россия), снабженной коррелятором реального времени (288 каналов, 10 нс), стандартным гониометром (0°–150°) и термостатом (точность поддержания температуры ±0.05°C). В качестве источника света использовали твердотельный одномодовый лазер (λ0 = 654 нм); эксперименты проводили в диапазоне углов рассеяния θ = = 30°–130°. Автокорреляционные функции интенсивности рассеянного света обрабатывали с использованием программы DynaLS, которая дает распределение ρ(τ) интенсивности рассеянного света по временам релаксации τ. Зависимость между 1/τ, где τ отвечает максимуму распределения ρ(τ), и квадратом вектора рассеяния q2 = = [(4πn0/λ0)sin(θ/2)]2 (n0 – показатель преломления раствора) для всех наблюдаемых мод функции распределения представляла собой прямые, проходящие через начало координат. Это указывает на диффузионный характер наблюдаемых процессов: 1/τ = Diq2, где Di – коэффициент поступательной диффузии, соответствующий i-ой моде. Гидродинамические радиусы были рассчитаны по формуле Стокса–Эйнштейна Rhi = = kBT/(6πη0Di), где kB – постоянная Больцмана, T – абсолютная температура.
Сканирующая электронная микроскопия (СЭМ). Изображения стабилизированных НЧ и их агрегатов получали в сканирующем электронном микроскопе Zeiss Merlin (Carl Zeiss, Германия) при ускоряющем напряжении 21 кВ и давлении в камере 50–70 Па; ток электронного пучка составлял 250 пА. Образцы были получены путем высаживания капли коллоидного раствора на кремниевую подложку и высушивания при 45°C в течение 12 ч.
Вискозиметрия и денситометрия. Вискозиметрические измерения проводили в капиллярном вискозиметре LOVIS 2000М (Anton Paar, Австрия) на основе принципа Гепплера. Плотность растворов измеряли с помощью денситометра DMA 5000 M (Anton Paar).
Погрешности результатов, полученных указанными методами молекулярной гидродинамики, не превышали 5%.
Материалы
В качестве стабилизирующего полимера при синтезе НЧ был выбран образец статистического тройного сополимера, поли(2-аминоэтилметакрилат-со-N-метил-2-аминоэтилметакрилат-co-N,N-диметил-2-аминоэтилметакрилата), с молекулярной массой M = 52 200 г/моль [29] (рис. 1).
Рис. 1.
Статистический тройной сополимер поли(2-аминоэтилметакрилат-со-N-метил-2-аминоэтилметакрилат-co-N,N-диметил-2-аминоэтилметакрилат), 〈M0〉 = 143 г/моль. 〈M0〉 – усредненная масса мономерного звена с учетом равного численного содержания разных мономерных звеньев в сополимере.
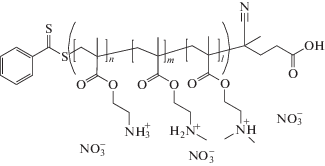
Использовали нитрат серебра, борогидрид натрия и нитрат натрия, поставленные компанией Вектон (Россия).
Серебряные НЧ были синтезированы путем химического восстановления ионов серебра в водных растворах AgNO3 борогидридом натрия в присутствии катионного полимера. Предварительно противоионы Cl– (эти противоионы присутствовали в системе на момент проведения гидродинамических исследований [29]) были заменены на противоионы ${\text{NO}}_{3}^{ - }$ путем диализа водного раствора полимера сначала против концентрированного раствора нитрата натрия, потом против воды. Концентрацию полимера в растворе после диализа определяли по инкременту плотности водного раствора (dp/dc = 0.250) [29]. Молекулярная масса полимера после процедуры диализа подтверждалась путем измерения характеристической вязкости и коэффициента диффузии методом ДРС в 0.2 M растворе NaNO3 с использованием величины гидродинамического инварианта A0, полученной ранее [29].
Процедура синтеза наночастиц
Синтез НЧ проводили путем смешения водных растворов AgNO3 (${{c}_{{{\text{AgN}}{{{\text{O}}}_{3}}}}}$ = 58 ммоль/л) и полимера (cм = 5.6 ммоль/л, cм – концентрация мономерных звеньев в растворе) с последующим добавлением свежеприготовленного раствора NaBH4 (${{c}_{{{\text{NaB}}{{{\text{H}}}_{4}}}}}$ = 264 ммоль/л) в избыточном соотношении NaBH4 : AgNO3 = 9.7 при постоянном перемешивании. Итоговые концентрации и соотношения компонентов в растворе были следующими: cм = 4.9 ммоль/л, ${{c}_{{{\text{AgN}}{{{\text{O}}}_{3}}}}}$ = 0.58 ммоль/л, соотношение число мономерных звеньев полимера: AgNO3 = 8.5.
Синтез наночастиц и последующее хранение коллоидного раствора осуществляли при комнатной температуре (T = 22 ± 3°С).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Спектрофотометрия
За динамикой процесса стабилизации наблюдали методом абсорбционной спектрофотометрии. В ходе реакции восстановления наблюдалось появление пика поверхностного плазмонного резонанса (ППР) свидетельствующего о формировании в растворе НЧ серебра.
На рис. 2а представлены спектры поглощения водного раствора, содержащего сополимер в качестве стабилизирующего агента, в различные моменты времени после добавления раствора борогидрида натрия, а на рис. 2б – временнáя зависимость величины поглощения в максимуме ППР на этих спектрах. Следует отметить, что в отсутствие восстановителя в растворах не наблюдалось образования НЧ в течение двух суток.
Рис. 2.
(а) Спектры поглощения реакционной смеси в различные моменты времени после введения восстановителя; (б) временнáя зависимость оптической плотности в максимуме ППР по измерениям в течение месяца.
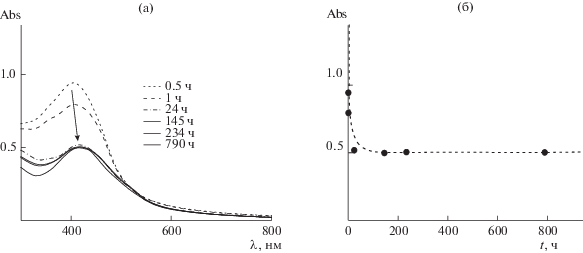
Представленные зависимости иллюстрируют хорошую стабилизирующую способность сополимера в водной среде при указанных концентрациях и соотношениях компонентов (после установления равновесия в течение 1–2 дней система остается стабильной более месяца).
Динамическое рассеяние света
Для исследования размеров стабилизированных сополимером в растворах НЧ (и их агрегатов) был использован метод ДРС. Измерения проводили через 5 месяцев после смешения реагентов (спектры поглощения, измеренные в этот момент, не отличались от измеренных спустя месяц после начала синтеза НЧ), т.е. для равновесного состояния системы (полоса ППР на спектре поглощения имеет максимум при 420 нм).
Результаты измерений иллюстрирует рис. 3а, на котором приведена функция распределения значений нормализованной интенсивности рассеянного света по гидродинамическим радиусам, имеющая бимодальный характер. Зависимости обратного времени релаксации 1/τ от квадрата вектора рассеяния q2 линейны и соответствуют закону 1/τ = Di q2. Это свидетельствует о диффузионном характере наблюдаемых процессов (рис. 3б).
Рис. 3.
(а) Распределение нормализованной интенсивности рассеянного света по гидродинамическим радиусам (θ = 60°) для раствора сополимер–НЧ; (б) зависимости 1/τ от q2, соответствующие модам 1 и 2 на рис. 3а, для дисперсии НЧ, стабилизированной сополимером.
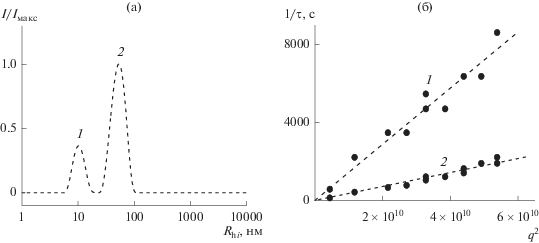
Полученные коэффициенты диффузии и оцененные (по формуле Стокса) гидродинамические радиусы присутствующих в растворе объектов представлены в табл. 1. Также в таблице представлен гидродинамический радиус (Rh) единичных макромолекул исследованного сополимера, определенный ранее [29]. Полученные результаты показывают, что в растворе присутствуют в основном НЧ размером 11.4 нм, но наблюдаются и 56-нм частицы, представляющие собой либо более крупные НЧ, либо агрегаты малых НЧ. Численная доля таких 56-нм объектов невелика (порядка 1%).
Таблица 1.
Характеристики сополимера и синтезированных в его присутствии НЧ серебра
| Параметр | |||||
|---|---|---|---|---|---|
| D1 × 107, см2/с | Rh1, нм | D2 × 108, см2/с | Rh2, нм | Rh*, нм | RСЭМ, нм |
| 2.39 | 11.4 | 5.0 | 56 | 4.9 | 10.5 |
* По результатам работы [29].
Сканирующая электронная микроскопия
Метод ДРС дает информацию о размерах присутствующих в растворе объектов (НЧ, стабилизированных полимером, и их агрегатов). Чтобы получить более детальную информацию о размерах и форме самих НЧ серебра и их агрегатов (без стабилизирующего полимера) была использована СЭМ. Измерения методом СЭМ проводили одновременно с измерениями ДРС, т.е. через 5 месяцев после введения NaBH4.
На рис. 4 в качестве примера представлены микрофотография НЧ и их агрегатов, стабилизированных катионным сополимером (4а) а также гистограмма, отражающая распределение НЧ по радиусам (4б). Гистограмма была построена путем нахождения полувысоты приведенных симметризованных радиальных профилей НЧ по результатам статистической выборки 100 независимых изображений индивидуальных НЧ на нескольких микрофотографиях. Значение радиуса НЧ (RСЭМ), соответствующее максимуму на гистограмме, также представлено в табл. 1.
Рис. 4.
(а) Микрофотография НЧ серебра и их агрегатов, стабилизированных сополимером; (б) гистограмма распределения по размерам единичных НЧ.
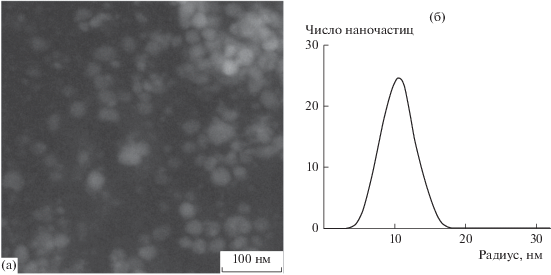
Сопоставление радиуса Rh1, полученного в результате измерений ДРС, и радиуса НЧ серебра RСЭМ, определенного с помощью СЭМ, позволяет оценить количество молекул сополимера, стабилизирующих НЧ. Значения этих радиусов близки: Rh1 = 11.4 нм, RСЭМ = 10.5 нм. Значение Rh1 несколько больше ввиду того, что в методе ДРС детектируются НЧ серебра, стабилизированные полимером, а в методе СЭМ – сами НЧ. Оценка числа молекул сополимера, стабилизирующих одну НЧ Ag, путем нахождения разницы объемов стабилизированной полимером НЧ и самой НЧ металла и деления этой разницы на объем 1 молекулы сополимера (ее гидродинамический радиус Rh приведен в табл. 1) дает значение 2.
Более детально ответить на вопрос о составе частиц в растворе можно, измерив их молярные массы иным независимым методом (например, с помощью аналитического ультрацентрифугирования). Такие исследования планируется провести в дальнейшем.
ЗАКЛЮЧЕНИЕ
Продемонстрирована способность катионного гребнеобразного сополимера, содержащего в мономерных звеньях аминогруппы различного типа, стабилизировать наночастицы серебра в водной среде в течение длительного времени. Этот факт имеет важное практическое значение, поскольку катионные полимеры активно используются в качестве носителей при трансфекции ДНК в клетки, а также в терапии различных заболеваний [22–25]. Создание комплексов катионных полимеров с НЧ может значительно расширить область практического применения таких систем.
Исследование выполнено за счет гранта Российского научного фонда (проект № 16-13-10 148).
Авторы благодарят профессора Ulrich S. Schubert и Anne-K. Trützschler (Jena Center for Soft Matter (JCSM), Friedrich Schiller University Jena, Jena, Germany) за предоставление образца катионного полимера.
Список литературы
Chen G., Zhao Y., Fu G., Duchesne P.N., Gu L., Zheng Y., Weng X., Chen M., Zhang P., Pao C.-W., Lee J.-F., Zheng N. // Science. 2014. V. 344. P. 495.
Reeßing F., Szymanski W. // Curr. Opin. Biotechnol. 2019. V. 58. P. 9.
Huanca D.R., Salcedo W.J. // J. Alloys Compd. 2019. V. 777. P. 554.
Wu B., Zheng N. // Nano Today. 2013. V. 8. P. 168.
Qin L., Zeng G., Lai C., Huang D., Xu P., Zhang C., Cheng M., Liu X., Liu S., Li B., Yi H. // Coord. Chem. Rev. 2018. V. 359. P. 1.
Khampieng T., Wongkittithavorn S., Chaiarwut S., Ekabutr P., Pavasant P., Supaphol P. // J. Drug Deliv. Sci. Technol. 2018. V. 44. P. 91.
Han X., Han M., Ma L., Qu F., Kong R.-M., Qu F. // Talanta. 2019. V. 194. P. 55.
Yin J., Wei B., Li Y., Li Y., Xi P. // J. Energy Chem. 2019. V. 34. P. 1.
White R.J., Luque R., Budarin V.L., Clark J.H., MacQuarrie D.J. // Chem. Soc. Rev. 2009. V. 38. P. 481.
Kaviya S., Santhanalakshmi J., Viswanathan B. // J. Nanotechnol. 2011. 152970.
Xie Y., Chen T., Guo Y., Cheng Y., Qian H., Yao W. // Food Chem. 2019. V. 270. P. 173.
El-Faham A., Atta A.M., Osman S.M., Ezzat A.O., El-Saeed A.M., Al Othman Z.A., Al-Lohedan H.A. // Prog. Org. Coat. 2018. V. 123. P. 209.
Klein D.L., McEuen P.L., Katari J.E.B., Roth R., Alivisatos A.P. // Appl. Phys. Lett. 1996. V. 68. P. 2574.
Murinzi T.W., Clement T.A., Chitsa V., Mehlana G. // J. Solid State Chem. 2018. V. 268. P. 198.
Zhang T., Chen Y., Huang W., Wang Y., Hu X. // Sens. Actuators. B. 2018. V. 276. P. 362.
Patil M.P., Kim G.-D. // Colloids Surf. B. 2018. V. 172. P. 487.
Baruwati B., Polshettiwar V., Varma R.S. // Green Chem. 2009. V. 11. P. 926.
Bilal M., Rasheed T., Iqbal H.M.N., Hu H., Wang W., Zhang X. // Int. J. Biol. Macromol. 2017. V. 103. P. 554.
Samal S.K., Dash M., Van Vlierberghe S., Kaplan D.L., Chiellini E., Van Blitterswijk C., Moroni L., Dubruel P. // Chem. Soc. Rev. 2012. V. 41. P. 7147.
Chen Y., Zhu Q., Cui X., Tang W., Yang H., Yuan Y., Hu A. // Chem. Eur. J. 2014. V. 20. P. 12477.
Kenawy E.-R., Worley S.D., Broughton R. // Biomacromolecules. 2007. V. 8. P. 1359.
Ramamoorth M., Narvekar A. // J. Clin. Diagn. Res. 2015. V. 9. № 1. P. GE01.
Kabanov A.V., Astafyeva I.V., Chikindas M.L., Rosenblat G.F., Kiselev V.I., Severin E.S., Kabanov V.A. // Biopolymers. 1991. V. 31. P. 1437.
Shi B., Zheng M., Tao W., Chung R., Jin D., Ghaffari D., Farokhzad O.C. // Biomacromolecules. 2017. V. 18. P. 2231.
De Cock L.J., De Koker S., De Geest B.G., Grooten J., Vervaet C., Remon J.P., Sukhorukov G.B., Antipina M.N. // Angew. Chem. Int. Ed. 2010. V. 49. P. 6954.
Hemp S.T., Smith A.E., Bryson J.M., Allen M.H., Long T.E. // Biomacromolecules. 2012. V. 13. P. 2439.
Ahmed M., Narain R. // Prog. Polym. Sci. 2013. V. 38. P. 767.
Lokitz B.S., Lowe A.B., McCormick C.L. // ACS. Symp. Ser. 2006. V. 937. P. 95.
Perevyazko I., Trützschler A., Gubarev A., Lebedeva E., Traeger A., Tsvetkov N., Schubert U.S. // Eur. Polym. J. 2017. V. 97. P. 347.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал


