Коллоидный журнал, 2019, T. 81, № 3, стр. 360-366
Определение размера наночастиц металлов, синтезированных в обратных мицеллах, методом эксклюзионной хроматографии
А. Д. Шафигулина 1, А. А. Ревина 1, Н. П. Платонова 1, С. А. Боровикова 1, *, А. К. Буряк 1
1 Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119071 Москва, Ленинский проспект, 31, Россия
* E-mail: Borovikova7@mail.ru
Поступила в редакцию 10.04.2018
После доработки 24.11.2018
Принята к публикации 03.12.2018
Аннотация
Методом эксклюзионной хроматографии определены размеры наночастиц палладия и серебра, синтезированных радиационно-химическим методом в мицеллярных растворах поверхностно-активного вещества АОТ при различных значениях степени гидратации ω0 = [H2O]/[AOT]. Размеры наночастиц серебра находятся в диапазоне от 1.5 до 5.3 нм, а наночастиц палладия – от 1.5 до 3 нм. Проведено сравнение полученных результатов с данными атомно-силовой микроскопии. Показано, что в случае наночастиц, синтезированных в мицеллярных растворах, их размер необходимо корректировать с учетом вклада толщины мицеллярной оболочки.
ВВЕДЕНИЕ
Интерес к изучению наноразмерных объектов, в частности, наночастиц (НЧ) различной природы постоянно растет. Это связано с возникновением аномальных свойств материалов при их переходе в наноразмерное состояние. В настоящее время в целях создания высокоэффективных композиционных материалов активно ведутся исследования, посвященные получению и изучению физико-химических свойств разнообразных наноматериалов.
Одним из перспективных методов получения НЧ является синтез в нанореакторах на основе обратных микроэмульсий типа “вода в масле” или в обратных мицеллах. Использование данного метода синтеза позволяет получать стабильные НЧ с узким распределением по размерам, что является существенным преимуществом, так как физико-химические свойства НЧ сильно зависят от их размеров. Кроме того, такие НЧ хорошо адсорбируются на поверхностях различных носителей, что имеет важное значение при получении нанокомпозитных материалов.
Как известно, оптические, каталитические и другие свойства НЧ металлов во многом определяются их размерами, т.к. даже при небольшом изменении размеров меняется соотношение числа поверхностных и объемных атомов в НЧ [1]. Поэтому очень важно контролировать размер НЧ при синтезе и последующем хранении. В работе для решения этой задачи был применен метод эксклюзионной хроматографии (ЭХ).
Эксклюзионная (ситовая) хроматография – жидкостная хроматография, при которой неподвижной фазой служит пористое тело или гель (гель-проникающая хроматография) и разделение смеси веществ происходит в результате различия в размерах молекул веществ и (или) в их форме и способности проникать в поры неподвижной фазы [2]. Использование ЭХ позволяет определять распределение частиц, в том числе обратных мицелл, по размерам и, при соответствующей калибровке, размеры мицелл [3–6].
Одна из первых работ по ЭХ наноразмерных объектов была посвящена исследованию данным методом НЧ сульфида кадмия в водной среде [4]. В этой работе авторами по двум образцам НЧ с известными размерами была построена градуировочная зависимость “время выхода–размер”. Затем был проведен хроматографический анализ двух неизвестных образцов НЧ CdS с достаточно высокой степенью полидисперсности. Исходя из хроматографических данных, был определен средний размер НЧ сульфида кадмия, а также найдено их распределение по размерам.
В работе [7] методом ЭХ исследованы НЧ серебра и золота, полученные методом обратно-мицеллярного синтеза в неполярных растворителях. Для детектирования НЧ выбиралась длина волны, при которой дисперсии частиц разных размеров имели одинаковое поглощение, а для подтверждения правильности градуировки сравнивали размеры НЧ, полученные для различных фракций на выходе из хроматографа, с расчетными размерами и данными просвечивающей электронной микроскопии.
В работе [3] методом ЭХ исследовали обратно-мицеллярные растворы металлических НЧ. По данным градуировки полистирольных стандартов и гидродинамическому радиусу для них в условиях эксперимента был рассчитан диаметр НЧ в нескольких отобранных фракциях и сопоставлен с результатами атомно-силовой микроскопии (АСМ). Данные разных методов хорошо согласовывались, на основании чего был сделан вывод о достоверности произведенной градуировки.
Принципиально важным является вопрос о соотношении размеров мицеллы и образовавшейся в ней НЧ металла. Поскольку синтез протекает внутри мицеллы путем восстановления ионов металла, находящихся в водном пуле мицеллы, очевидно, что размер НЧ должен быть меньше, чем размер мицеллы. Для определения размера НЧ металла традиционно проводится пересчет, основанный на исключении размера мицеллярной оболочки из измеренного методом ЭХ размера мицеллы, содержащей НЧ. Ограничением такого подхода является различие в размерах синтезированных в мицеллах НЧ и полости внутри мицеллы. Такое ограничение может быть снято путем введения поправочного коэффициента, полученного из данных АСМ после удаления с НЧ мицеллярной оболочки. Однако преимуществом ЭХ является возможность ее применения для исследования НЧ непосредственно в обратно-мицеллярном растворе, что позволяет контролировать процесс синтеза НЧ. Кроме того, ЭХ может быть использована и для препаративного выделения НЧ требуемого размера.
В качестве объектов исследования были выбраны НЧ двух металлов − палладия и серебра, имеющие наиболее широкое применение в различных областях науки и техники. Палладий является одним из металлов, часто используемых в катализе [8–10]. Это связано как со специфическими свойствами палладия, который проявляет активность во многих процессах, так и с развитием платинозамещающих каталитических технологий [11]. Особый интерес также представляют НЧ серебра, так как с развитием нанотехнологий они находят все более разнообразное применение. Так, в обзорах [12, 13] рассмотрены работы, посвященные исследованию антибактериальных (а также антивиральных и антигрибковых) свойств НЧ Ag, а также их использованию для обработки и функционализации различных материалов при создании медицинского оборудования, упаковочных материалов, одежды.
В настоящей работе методом ЭХ исследованы размеры НЧ палладия и серебра, получаемых в обратно-мицеллярных растворах c различным отношением молярных концентраций воды и ПАВ (ω0). Варьирование значения ω0 сказывается на условиях протекания синтеза НЧ, что может влиять на их размеры и стабильность. Представляло интерес оценить влияние условий синтеза на размеры НЧ двух разных металлов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Наноразмерные частицы Pd и Ag были получены радиационно-химическим восстановлением ионов Me z+ из растворов комплексных солей в обратно-мицеллярной системе Me z+ + [H2O]/[AOT]/изооктан [14–17]. АОТ – мицеллообразующее ПАВ (бис(2-этилгексил)сульфосукцинат натрия). НЧ Pd были синтезированы в мицеллярных растворах c различным соотношением молярных концентраций воды и ПАВ ω0 = [H2O]/[AOT] в органической фазе (1.5, 3, 5), а НЧ Ag – в обратно-мицеллярных растворах с ω0 = 2, 4, 8.
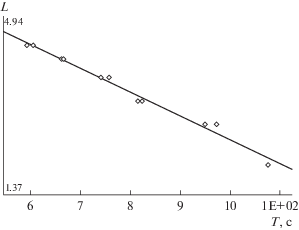
Эксклюзионное разделение НЧ металлов проводили на хроматографе Waters, оснащенном насосом Knauer WellChrom K-120, колонкой Waters UltraStyragel с размером пор 100 нм и спектрофотометрическим детектором Kratos (λ = 254, 300, 420 нм). В качестве подвижной фазы использовали тетрагидрофуран (для градиентной ВЭЖХ, Panreac), скорость потока составляла 0.65 см3/мин. Для определения размеров НЧ была проведена предварительная градуировка колонки Waters UltraStyragel (рис. 1) по полистирольным стандартам (ПСС) известной молекулярной массы (от 580 до 22 000 Да). Данные о временах удерживания использованных ПСС суммированы в табл. 1.
Таблица 1.
Времена удерживания полистирольных стандартов
| Молекулярная масса полистирола, Да | Время удерживания, мин |
|---|---|
| 22 000 | 10.0 |
| 11 600 | 11.1 |
| 5050 | 12.5 |
| 1700 | 13.7 |
| 580 | 16.0 |
Уравнение градуировочной зависимости имеет вид
где L – десятичный логарифм молекулярной массы ПСС, T – время его удерживания (с); среднеквадратичное отклонение составляет 2.7%, погрешность определения массы − 3.4%.Пересчет размеров ПСС в размеры НЧ проводился по эмпирической формуле (2) [18], выведенной для обратно-мицеллярных растворов НЧ:
где Mw – средневесовая молекулярная масса ПСС (Да), определенная по градуировочному графику, d – диаметр (Å) частицы (условно сферической) ПСС, имеющего соответствующую молекулярную массу.ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Определение размеров НЧ палладия
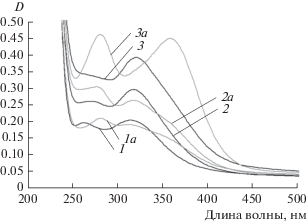
На рис. 2 представлены характерные спектры мицеллярных растворов НЧ палладия со значениями ω0 = 1.5, 3, 5, измеренные на одних и тех же стадиях их эволюции (спустя 1 и 30 сут после проведения синтеза). Видно, что спектры являются сложными и характеризуются максимумами оптического поглощения на длинах волн 258 и 320 нм.
Рис. 2.
Влияние размера водного пула обратных мицелл на спектры оптического поглощения образующихся в них НЧ палладия. Значения ω0: 1 − 1.5, 2 − 3, 3 − 5. Все спектры измерены на одной стадии эволюции НЧ – спустя 1 сут после синтеза. Спектры с индексом “а” измерены через 30 сут.
Известно, однако, что НЧ Pd в водной среде в присутствии полиакрилата характеризуются спектром, плавно нарастающим в УФ-область, с максимумом поглощения при 220 нм [1, 19, 20]. Мы полагаем, что в условиях восстановления радиационно-химическим методом в мицеллярных растворах поверхностно-активного вещества АОТ образуются НЧ Pd, имеющие несколько иной спектр поглощения, анализ которого показал, что преимущественно эти частицы поглощают в области 250–350 нм. Таким образом, для детектирования НЧ палладия были выбраны длины волн 258 и 300 нм.
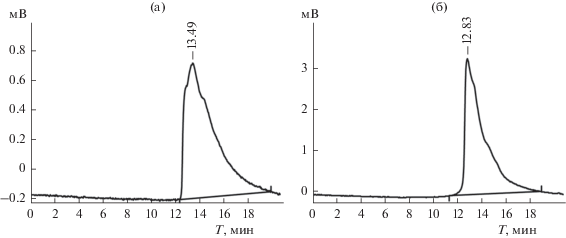
На рис. 3а приведена хроматограмма обратно-мицеллярного раствора НЧ Pd (ω0 = 3) при детектировании на длине волны 258 нм. Эта длина волны информативна относительно и НЧ палладия, и ПАВ (АОТ). Поэтому хроматографический профиль для образца − сложный. При длине волны 300 нм на хроматограмме раствора АОТ в изооктане, не содержащего НЧ Pd, интенсивность сигнала снижается практически до нуля, а на хроматограмме обратно-мицеллярного раствора НЧ Pd сигнал сохраняется, поэтому мы полагаем, что при 300 нм мы детектируем только НЧ палладия. На рис. 3б приведена хроматограмма обратно-мицеллярного раствора НЧ Pd (ω0 = 3) при детектировании на длине волны 300 нм.
Рис. 3.
Хроматограммы НЧ палладия, синтезированных при ω0 = 3; скорость потока элюента (тетрагидрофуран) – 650 мкл/мин, колонка Waters UltraStyragel 103 Å, детектирование на длине волны 258 нм (а) и 300 нм (б).
По данным градуировки по ПСС и значениям их гидродинамического радиуса в условиях эксперимента был рассчитан диаметр НЧ палладия, полученных в обратно-мицеллярных растворах с различным мольным соотношением воды и АОТ. Времена выхода пиков и соответствующие им вычисленные диаметры НЧ приведены в табл. 2.
Таблица 2.
Данные о размерах НЧ Pd по результатам ЭХ и АСМ
| ω0 | Время выхода пика из колонки, мин |
Средний размер НЧ по данным ЭХ, нм | Средний размер НЧ по данным АСМ, нм |
|---|---|---|---|
| 1.5 | 13.5 | 1.5 | 1.3 |
| 3 | 12.9 | 2.0 | 1.7 |
| 5 | 12.0 | 2.8 | 2.6 |
После подтверждения градуировки были построены распределения по размерам для НЧ палладия, синтезированных в обратно-мицеллярных растворах с разным мольным соотношением ω = = Н2О/АОТ, по хроматографическим данным с детектированием на длине волны 300 нм. На рис. 4 приведены средневесовое и среднечисловое распределения НЧ палладия по размерам в мицеллярном растворе с ω0 = 3, рассчитанные по данным ЭX.
Рис. 4.
Средневесовое (1) и среднечисловое (2) распределения по размеру (молекулярной массе) НЧ Pd, синтезированных при ω0 = 3, по данным ЭХ.
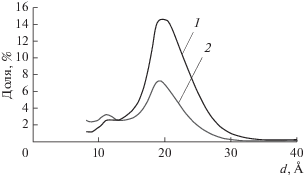
Таким образом, средний диаметр синтезируемых в обратно-мицеллярном растворе (ω0 = 3) НЧ палладия составляет 2 нм. Исходя из представленных данных, можно утверждать, что условия синтеза влияют на распределение частиц Pd по размерам и их средний размер, но частицы минимальных и максимальных размеров присутствуют во всех образцах.
Поскольку одним из основных методов определения размеров НЧ на сегодняшний день считается АСМ, нами проведено сравнение данных двух методов − ЭX и АСМ [21].
Использование АСМ для измерения размеров НЧ Pd, синтезированных в обратно-мицеллярных растворах, потребовало разработки специальной методики удаления с поверхности слюды после нанесения пробы мицеллярного раствора, содержащего НЧ, примесей АОТ и следов углеводорода, которые мешают визуализации частиц. Отметим, что точно определить диаметр НЧ по их латеральным размерам невозможно вследствие известного эффекта уширения, обусловленного конечным радиусом кривизны зонда. Поэтому размеры НЧ оценивали из данных об их высоте. Результаты измерений методом АСМ показывают, что увеличение размера водного пула обратных мицелл в соответствии с выбранным значением коэффициента солюбилизации ω0 приводит к увеличению размеров НЧ, при этом средний диаметр частиц совпадает с полученным методом ЭХ (табл. 2).
Определение размеров наночастиц серебра
Спектры оптического поглощения обратно-мицеллярных растворов НЧ серебра (ω0 = 2, 4, 8), синтезированных радиационно-химическим методом, приведены на рис. 5. Коллоидный раствор с ω0 = 2, имеет две характерных полосы поглощения: в УФ-области (≈250 нм) и в видимой области (419 нм). Для раствора с ω0 = 8 также наблюдаются две характерные полосы поглощения (≈295 и 420 нм).
Рис. 5.
Спектры оптического поглощения обратно-мицеллярных растворов НЧ Ag при значениях ω0 = 2 (1) и 8 (2).
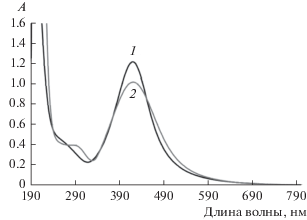
Интенсивность полосы поглощения в видимой области для обратно-мицеллярного раствора НЧ Ag с ω0 = 2 выше, несмотря на то, что в исходном (до облучения) растворе с ω0 = 8 содержание соли серебра было выше. Это может быть связано с тем, что синтез НЧ в растворе с ω0 = 2 прошел с наибольшей степенью превращения ионов Ag+ в НЧ, а также с возможной агрегацией частиц в обратно-мицеллярном растворе с ω0 = 8.
Исходя из полученных данных, при исследовании обратно-мицеллярных растворов НЧ Ag методом ЭХ детектирование НЧ проводили на длине волны 420 нм.
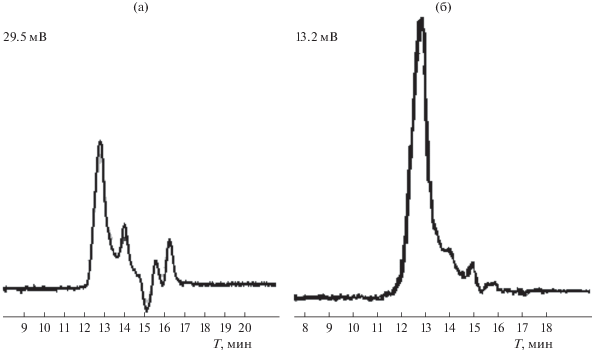
На рис. 6 приведены эксклюзионные хроматограммы обратно-мицеллярных растворов НЧ Ag со значениями ω0 = 2 и 8. Соответствующие значения размера частиц в исследованных растворах представлены в табл. 3.
Таблица 3.
Диапазоны размеров частиц, детектируемых в исследованных обратно-мицеллярных растворах НЧ Ag методом ЭХ
| ω0 | Общий диапазон размеров, нм | Размер в максимуме распределения, нм |
|---|---|---|
| 2 | 1.6–3.6 | 2.6 |
| 4 | 1.6–3.6 | 3.0 |
| 8 | 1.9–3.7 | 3.5 |
Для сравнения аналогичный эксперимент был проведен для раствора “пустых” обратных мицелл АОТ, содержащих только воду, без ионов или НЧ серебра. Детектирование для данного образца проводилось на длине волны 254 нм, так как она соответствует максимальному поглощению молекул АОТ [3]. Соответствующее распределение детектируемых частиц по размерам приведено на рис. 7.
Рис. 7.
Распределение по размерам частиц детектируемых в обратно-мицеллярном растворе “пустых” мицелл АОТ (λ = 254 нм); I – область остаточных адсорбционных взаимодействий, II – область эксклюзионного механизма разделения.
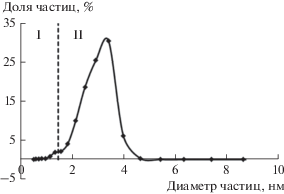
На всех приведенных распределениях присутствуют частицы с размерами ≤1.5 нм. Учитывая то, что согласно литературным данным [22] длина молекулы АОТ составляет примерно 1 нм, размер НЧ в стабилизирующей оболочке из молекул АОТ не может быть таким небольшим даже в хроматографических условиях. Скорее всего, детектирование таких ультрамалых частиц связано с наличием остаточных адсорбционных взаимодействий частиц либо их мицеллярной оболочки с неподвижной фазой колонки. В случае обратно-мицеллярных растворов НЧ Ag интенсивность сигнала детектируемых частиц в этой адсорбционной области выше, чем для раствора “пустых” мицелл, следовательно, мицеллы, содержащие НЧ Ag, сильнее взаимодействуют с материалом неподвижной фазы колонки. Граница между областями адсорбционного (I) и эксклюзионного (II) механизмов разделения не является фиксированной, так как неизвестно, каким образом реализуется переход между этими механизмами.
Таким образом, из приведенных данных следует, что “пустые” мицеллы в растворе состава вода/АОТ/изооктан и частицы, детектируемые в обратно-мицеллярных растворах НЧ, имеют схожую структуру, т.е. детектируемые частицы представляют собой мицеллы, содержащие НЧ металла.
ЗАКЛЮЧЕНИЕ
Методом эксклюзионной хроматографии определены размеры НЧ Ag и Pd, синтезированных радиационно-химическим методом в обратно-мицеллярных растворах АОТ. Показано, что размеры НЧ Ag находятся в диапазоне 1.6–5.3 нм и изменяются обратимо в небольших пределах, что свидетельствует об их высокой стабильности. Размеры НЧ Pd составили от 1.5 до 3.0 нм.
Анализ полученных результатов показывает, что увеличение размера водного пула обратных мицелл в соответствии с выбранным значением коэффициента солюбилизации ω0 приводит к росту размеров НЧ. При этом средний диаметр частиц совпадает с полученным по данным АСМ [21], что позволяет считать ЭХ перспективным и достоверным методом измерения размеров НЧ различных металлов.
Работа выполнена при финансовой поддержке Программы фундаментальных исследований Президиума РАН № 36 на 2018 г.
Список литературы
Ершов Б.Г. // Рос. хим. журн. 2001. Т. 45. № 3. С. 20.
Хроматография. Основные понятия. Терминология. Под ред. Даванкова В.А. М.: Сборники научно-нормативной терминологии. 1997. Вып. 14.
Пономарев К.В., Ларионов О.Г., Шафигулина А.Д., Буланова А.В. // Сорбционные и хроматографические процессы. 2012. Т. 12. Вып. 3. С. 325.
Fischer C.-H., Weller H., Katsikas L., Henglein A. // Langmuir. 1989. V. 5. P. 429.
Fisher Ch.-H., Giersig M. // Langmuir. 1992. V. 8. P. 1475.
Siebrands T., Giersig M., Mulvaney P., Fischer Ch.-H. // Langmuir. 1993. V. 9. P. 2297.
Wilcoxon J.P., Martin J.E., Provencio P. // J. Chem. Phys. 2001. V. 115. P. 998.
Розенберг Ж.И., Берлин А.В. // Рос. хим. журн. 2006. Т. 50. № 4. С. 4.
Лисицын А.С., Пармон В.И., Дуплякин В.К., Лихолобов В.А. // Рос. хим. журн. 2006. Т. 50. № 4. С. 140.
Качевский С.А., Голубина Е.В., Локтева Е.С., Лунин В.В. // Журн. физ. химии. 2007. Т. 81. С. 998.
Стахеев А.Ю., Машковский И.С., Баева Г.Н., Телегина Н.С. // Рос. хим. журн. 2009. Т. 53. № 2. С. 68.
Tran Q.H., Nguyen V.Q., Le A.-T. // Adv. Nat. Sci.: Nanosci. Nanotechnol. 2013. V. 4. 033001.
Lee J., Kim K.-J., Sung W.S., Kim J.G., Lee D.G. // Silver Nanoparticles / Ed. by Perez D.P. Vukovar, Croatia: IntechOpen, 2010. P. 295.
Докучаев А.Г., Мясоедова Т.Г., Ревина А.А. // Химия высоких энергий. 1977. Т. 31. С. 353.
Егорова Е.М., Ревина А.А. // Коллоид. журн. 2002. Т. 64. С. 334.
Ревина А.А. Патент РФ № 2322327. // Б. И. 2008. № 11.
Кезиков А.Н., Ревина А.А., Брянцева Н.В., Магомедбеков Э.П. // Успехи в химии и химической технологии. 2003. Т. 17. № 10. С. 69.
Yau W.W., Kirkland J.J., Bly D.D. Modern Size-Exclusion Liquid Chromatography. Practice of Gel Permeation and Gel Filtration Chromatography. New York: Wiley, 1979.
Ершов Б.Г., Троицкий Д.А. // Журн. физ. химии. 1995. Т. 69. С. 2179.
Ершов Б.Г. // Изв. АН. Сер. хим. 1996. С. 313.
Ревина А.А., Белякова Л.Д., Паркаева С.А., Суворова О.В., Сергеев М.О., Золотаревский В.И. // Физикохимия поверхности и защита материалов. 2010. Т. 46. С. 648.
Abel S., Sterpone F., Bandyopadhyay S., Marchi M. // J. Phys. Chem. B. 2004. V. 108. P. 19 458.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал