Коллоидный журнал, 2019, T. 81, № 5, стр. 650-659
Верификация ячеечной (гетерогенной) модели ионообменной мембраны и ее сравнение с гомогенной моделью
А. Н. Филиппов 1, *, С. А. Шкирская 2
1 РГУ нефти и газа (НИУ) имени И.М. Губкина
119991 Москва,
Ленинский проспект, 65, корп. 1, Россия
2 Кубанский государственный университет
350040 Краснодар,
ул. Ставропольская, 149, Россия
* E-mail: filippov.a@gubkin.ru
Поступила в редакцию 20.04.2019
После доработки 29.04.2019
Принята к публикации 30.04.2019
Аннотация
С использованием подхода Онзагера к неравновесным изотермическим процессам и ячеечного метода впервые получена алгебраическая формула для определения электроосмотической проницаемости ионообменной мембраны при заданной постоянной плотности тока. Ячеечная модель верифицирована с привлечением экспериментальных данных по электропроводности и электроосмотической проницаемости водного раствора соляной кислоты через исходную и модифицированную нанотрубками галлуазита и наночастицами платины и железа катионообменную мембрану МФ-4СК при заданных плотности тока и концентрации. Получено хорошее совпадение теоретических и экспериментальных данных, определены физико-химические параметры модели. Проведено сравнение результатов расчетов по ячеечной и гомогенной моделям тонкопористой мембраны. Показано их соответствие для всех трех образцов сульфокатионитовой мембраны МФ-4СК.
ВВЕДЕНИЕ
Электроосмотическая проницаемость (ЭОП) ионообменных мембран (ИОМ) является важным фактором, который существенно влияет на их использование, например, в топливных элементах. Чрезмерная потеря воды такой мембраной приводит к ее разрушению и возможному перегреву самого топливного элемента. Поэтому для эффективной работы ИОМ в топливных элементах необходимо и желательно еще до проведения эксперимента знать, каким образом их ЭОП будет изменяться при варьировании влагосодержания и концентрации фонового электролита, а также геометрических и физико-химических характеристик зерен ионита. Однако существующие теории для расчета ЭОП не полностью отвечают на поставленные вопросы. Это мотивировало нас построить замкнутую ячеечную модель ИОМ, учитывающую перенос воды или другого растворителя в гидратных/сольватных оболочках ионов. Ранее ячеечная модель показала свою высокую эффективность при расчете гидродинамической проницаемости мембран, обладающих двухуровневой пористостью [1, 2], что убедило нас попытаться использовать ее и применительно к расчету электроосмотической проницаемости ИОМ [3], рассматриваемых как совокупности заряженных пористых частиц сферической формы. Имеющиеся в настоящее время формулы для расчета электрической проводимости ИОМ [4–6] тоже не в полной мере описывают все имеющиеся экспериментальные результаты. В связи с этим нами был применен тот же ячеечный метод и для расчета удельной электропроводности (ЭП) ИОМ. Полученные при этом результаты играют важную роль в процессе изучения и прогнозирования свойств ИОМ, модифицированных неорганическими наночастицами и нанотрубками, поскольку в ряде случаев на практике обнаруживается экстремальная зависимость транспортных, механических и структурных свойств гибридных композитов от содержания нанодисперсных включений [7].
Таким образом, в рамках ячеечной модели ИОМ можно моделировать упорядоченным массивом заряженных пористых шаров, погруженных в жидкие сферические оболочки – ячейки. На основе термодинамики необратимых процессов (подход Онзагера) ранее была поставлена и решена краевая задача для системы уравнений Стокса, Бринкмана, Нернста–Планка–Пуассона [2], описывающих поток бинарного несимметричного электролита через единичную ячейку радиуса b, в центре которой находится пористая сферическая частица радиуса a, имеющая постоянную плотность фиксированного пространственного заряда (обменную емкость). Значение b выбирается таким образом, чтобы отношение объема частиц к объему ячейки равнялось объемной доле гелевой (ионитовой) фазы. На границе жидкой оболочки мы использовали условие Кувабары (отсутствие завихренности жидкого потока), как наиболее адекватно описывающее электрокинетические явления, а на границе между пористой частицей и раствором электролита – условия непрерывности скорости, радиальной компоненты потоков ионов и полного тензора напряжений. С использованием метода, разработанного Хаппелем и Бреннером, результаты решения краевой задачи для ячейки были применены к расчету электропроводности и электроосмотической проницаемости [3] заряженной мембраны в зависимости от доли гелевой проводящей фазы, геометрических и физико-химических характеристик зерна ионита и концентрации бинарного электролита.
В данной работе мы применили разработанную ячеечную модель к определению характеристик полученных нами ранее катионообменных мембран МФ-4СК в исходном состоянии, а также модифицированных нанотрубками галлуазита, функционализированными наночастицами Pt или Fe [6], в водных растворах HCl разной концентрации. Верификация модели выполнена на основании экспериментальных данных, полученных при изучении электроосмотической проницаемости и электропроводности исследуемых мембран.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Для исследования неравновесных изотермических процессов в качестве термодинамических сил выбираем градиенты давления, электрического потенциала и концентрации: ${{\Phi }_{1}} = \nabla p$ ≈ ${{ \approx \left( {{{p}_{{20}}}{\kern 1pt} {\kern 1pt} - {\kern 1pt} {\kern 1pt} {{p}_{{10}}}} \right)} \mathord{\left/ {\vphantom {{ \approx \left( {{{p}_{{20}}}{\kern 1pt} {\kern 1pt} - {\kern 1pt} {\kern 1pt} {{p}_{{10}}}} \right)} h}} \right. \kern-0em} h}{\kern 1pt} ,$ ${{{{\Phi }_{2}} = \nabla {\varphi } \approx \left( {{{{\varphi }}_{{20}}} - {{{\varphi }}_{{10}}}} \right)} \mathord{\left/ {\vphantom {{{{\Phi }_{2}} = \nabla {\varphi } \approx \left( {{{{\varphi }}_{{20}}} - {{{\varphi }}_{{10}}}} \right)} h}} \right. \kern-0em} h}{\kern 1pt} ,$ ${{\Phi }_{3}} = \nabla C \approx $ ${{ \approx \left( {{{C}_{{20}}} - {{C}_{{10}}}} \right)} \mathord{\left/ {\vphantom {{ \approx \left( {{{C}_{{20}}} - {{C}_{{10}}}} \right)} h}} \right. \kern-0em} h}.$ Здесь h – толщина мембраны, а индексы “1” и “2” указывают на левую и правую стороны мембраны, находящейся в измерительной ячейке, заполненной раствором электролита.
Термодинамические силы независимо задаются в эксперименте. В качестве зависимых термодинамических параметров выберем плотности потоков: $U$ – растворителя (например, воды), $I$ – подвижных зарядов (плотность электрического тока), $J$ – растворенного вещества (плотность диффузионного потока электролита). Тогда феноменологические транспортные уравнения могут быть записаны в следующем виде [8]:
(1)
$\left\{ \begin{gathered} U = - \left( {{{L}_{{11}}}\nabla p + {{L}_{{12}}}\nabla {\varphi } + {{L}_{{13}}}\nabla C} \right) \hfill \\ I = - \left( {{{L}_{{21}}}\nabla p + {{L}_{{22}}}\nabla {\varphi } + {{L}_{{23}}}\nabla C} \right) \hfill \\ J = - \left( {{{L}_{{31}}}\nabla p + {{L}_{{32}}}\nabla {\varphi } + {{L}_{{33}}}\nabla C} \right). \hfill \\ \end{gathered} \right.$Механизм переноса растворителя (воды) может быть различным и зависеть как от гидрофильных свойств ИОМ, так и от степени гидратации переносимых ионов. Количественной характеристикой электротранспорта воды в мембранных системах, обычно измеряемой в эксперименте, является ЭОП ${{D}_{{\text{I}}}}$ при постоянной плотности тока – отношение объема перенесенной жидкости ΔV к количеству электричества, пропущенного через единицу площади S мембраны в единицу времени:
где I – плотность тока, τ – время пропускания тока. Другая количественная характеристика электропереноса воды – это число переноса воды tw (моль Н2О/F), которое представляет собой число молей воды ${{\Delta V} \mathord{\left/ {\vphantom {{\Delta V} {{{\upsilon }_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}}}} \right. \kern-0em} {{{\upsilon }_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}}},$ переносимых с 1 г-экв ионов (F = 96 485 Кл/моль):(3)
${{t}_{{\text{w}}}} = \frac{{F\Delta V}}{{{{\upsilon }_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}SI\tau }} = \frac{F}{{{{\upsilon }_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}}}{{D}_{{\text{I}}}},$Установим связь между ${{D}_{{\text{I}}}}$ и кинетическими коэффициентами L12, L22. Поделив первое из соотношений (1) на второе при условиях $\nabla p = \nabla C = 0,$ $I = {\text{const,}}$ получим
Сравнивая (2) и (4), заключаем, что $U = {{\Delta V} \mathord{\left/ {\vphantom {{\Delta V} {S\tau }}} \right. \kern-0em} {S\tau }},$ как и должно быть. Выражения для коэффициентов L12 и L22 были получены в общем случае неидеальной мембраны в работе [3] и являются довольно громоздкими. Приведем их здесь лишь для предельного случая идеально селективной катионообменной мембраны и 1 : 1-электролита:(5)
${{L}_{{12}}} = 3\frac{{F{{D}_{ + }}}}{{RT}}\frac{{\left( {1 + \frac{{{{m}_{0}}}}{{3 - {{m}_{0}}}}\frac{{{{D}_{{{\text{m}} + }}}}}{{{{D}_{ + }}}}} \right)\frac{{{{C}_{0}}}}{{\bar {\rho }}}}}{{{{m}_{0}}{\kern 1pt} \left( {\frac{{{{D}_{{{\text{m}} + }}}}}{{{{D}_{ + }}}}\frac{{{{{\bar {\rho }}}_{0}}}}{{\bar {\rho }}} + {\text{1}}} \right) + \left( {\left( {3 - {{m}_{0}}} \right)\frac{{{{{\bar {\rho }}}_{0}}}}{{\bar {\rho }}} - {{m}_{0}}} \right){\kern 1pt} \frac{{{{C}_{0}}}}{{\bar {\rho }}}}}{\kern 1pt} ,$(6)
$\begin{gathered} {{L}_{{22}}} = {{C}_{0}}{{D}_{ + }}\frac{{{{F}^{2}}}}{{RT}}\left( {\frac{{2{{m}_{0}}}}{{3 - {{m}_{0}}}}\left( {1 + \frac{{{{D}_{ - }}}}{{{{D}_{ + }}}}} \right){{ + }^{{^{{^{{^{{^{{^{{^{{^{{^{{^{{^{{^{{^{{^{{}}}}}}}}}}}}}}}}}}}}}}}}}}}}}} \right. \\ + \,\,\left. {\frac{{\frac{{9\left( {1 - {{m}_{0}}} \right)}}{{3 - {{m}_{0}}}}\left( {\frac{{{{D}_{{{\text{m}} + }}}}}{{{{D}_{ + }}}} + \frac{{\bar {\rho }}}{{{{{\bar {\rho }}}_{0}}}}} \right)\bar {\rho }}}{{{{m}_{0}}\bar {\rho }\left( {\frac{{{{D}_{{{\text{m}} + }}}}}{{{{D}_{ + }}}} + \frac{{\bar {\rho }}}{{{{{\bar {\rho }}}_{0}}}}} \right) + \left( {3 - {{m}_{0}}\left( {1 + \frac{{\bar {\rho }}}{{{{{\bar {\rho }}}_{0}}}}} \right)} \right){{C}_{0}}}}} \right). \\ \end{gathered} $(7)
${{D}_{{\text{I}}}} = \frac{3}{{F{{{\bar {\rho }}}_{0}}}}\frac{{3 - {{m}_{0}}\left( {1 - \frac{{{{D}_{{{\text{m}} + }}}}}{{{{D}_{ + }}}}} \right)}}{{\left( {\frac{{{{D}_{{{\text{m}} + }}}}}{{{{D}_{ + }}}} + \frac{{\bar {\rho }}}{{{{{\bar {\rho }}}_{0}}}}} \right)\left( {9\left( {1 - {{m}_{0}}} \right) + 2m_{0}^{2}\left( {1 + \frac{{{{D}_{ - }}}}{{{{D}_{ + }}}}} \right)} \right) + 2{{m}_{0}}\left( {1 + \frac{{{{D}_{ - }}}}{{{{D}_{ + }}}}} \right)\left( {\frac{{3 - {{m}_{0}}}}{{\bar {\rho }}} - \frac{{{{m}_{0}}}}{{{{{\bar {\rho }}}_{0}}}}} \right){{C}_{0}}}}.$Несмотря на приближенность формул (5)–(7), они хорошо работают для реальных (неидеальных) мембран, в чем убедимся ниже. Видно, что зависимость (7) электроосмотической проницаемости ${{D}_{{\text{I}}}}$ от концентрации раствора 1 : 1-электролита является гиперболической и монотонно убывающей до нуля с ростом ${{C}_{0}}.$ Отметим, что обратная величина ${1 \mathord{\left/ {\vphantom {1 {{{D}_{{\text{I}}}}}}} \right. \kern-0em} {{{D}_{{\text{I}}}}}}$ линейным образом зависит от концентрации электролита, что может быть эффективно использовано при экспресс-анализе экспериментальных зависимостей обратных чисел переноса воды от концентрации:
(7a)
$\begin{gathered} \frac{1}{{{{t}_{{\text{w}}}}}} = \frac{{{{{\bar {\rho }}}_{0}}{{\upsilon }_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}}}{3}\left( {\left( {\frac{{{{D}_{{{\text{m}} + }}}}}{{{{D}_{ + }}}} + \frac{{\bar {\rho }}}{{{{{\bar {\rho }}}_{0}}}}} \right)\frac{{9\left( {1 - {{m}_{0}}} \right) + 2m_{0}^{2}\left( {1 + \frac{{{{D}_{ - }}}}{{{{D}_{ + }}}}} \right)}}{{3 - {{m}_{0}}\left( {1 - \frac{{{{D}_{{{\text{m}} + }}}}}{{{{D}_{ + }}}}} \right)}}} \right. + \\ + \,\,\left. {2{{m}_{0}}\left( {1 + \frac{{{{D}_{ - }}}}{{{{D}_{ + }}}}} \right)\frac{{3 - {{m}_{0}}\left( {1 + \frac{{\bar {\rho }}}{{{{{\bar {\rho }}}_{0}}}}} \right)}}{{3 - {{m}_{0}}\left( {1 - \frac{{{{D}_{{{\text{m}} + }}}}}{{{{D}_{ + }}}}} \right)}}\frac{{{{C}_{0}}}}{{\bar {\rho }}}} \right). \\ \end{gathered} $ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
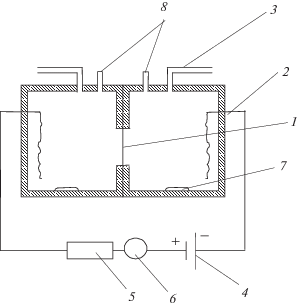
Электроосмотическую проницаемость мембран DI при постоянной плотности тока и число переноса воды tw определяли объемным методом [9] в двухкамерной ячейке с поляризующими хлорсеребряными электродами (рис. 1). Ячейка состоит из двух полукамер I и II емкостью 100 см3 каждая, изготовленных из оргстекла. Камеры снабжены горизонтально расположенными измерительными капиллярами 3 и воронками 8 для заполнения ячейки рабочим раствором. В камерах находятся поляризующие хлорсеребряные электроды 2, изготовленные из серебряной пластины, покрытой слоем хлорида серебра. Герметичность установки обеспечивают тонкие резиновые прокладки, между которыми зажимается ИОМ 1, представляющая собой диск диаметром 3.3 см с рабочей площадью S = 1.778 см2. Ячейка проверялась на герметичность после каждой сборки и заполнения раствором путем выдерживания без наложения внешнего электрического поля в течение 15–20 мин. При заполнении ячейки раствором особое внимание уделялось удалению пузырьков воздуха, образующихся на стенках камер, поскольку они могут внести ошибку в измерения изменений объема жидкости во время эксперимента. Для устранения концентрационной поляризации растворы в ячейке перемешивали с помощью магнитных мешалок 7. После сборки ячейки и заполнения ее раствором от выпрямителя 4 подавали постоянный ток, измеряемый миллиамперметром 6, и через каждые 2–3 мин в зависимости от плотности тока регистрировали перемещение менисков жидкости в измерительных капиллярах.
Рис. 1.
Схема установки для измерения электроосмотической проницаемости мембран объемным методом: 1 – исследуемая мембрана, 2 – хлорсеребряные электроды, 3 – измерительные капилляры, 4 – источник постоянного тока, 5 – магазин сопротивлений, 6 – миллиамперметр, 7 – магнитные мешалки, 8 – воронки для заполнения ячейки рабочим раствором.
Изменения объема раствора в камерах ячейки, полученные в квазистационарном состоянии при заданной плотности тока, использовали для расчета электроосмотической проницаемости DI и числа переноса воды tw в соответствии с уравнениями (2) и (3). Необходимо отметить, что время достижения квазистационарного состояния, характеризуемого равенством по абсолютной величине убыли объема жидкости в одном капилляре и прироста ее объема в другом капилляре, составляло 15–60 мин. Результаты воспроизводили несколько раз. Для того чтобы на электродах кроме основных процессов осаждения и растворения серебра не протекали побочные реакции с образованием газообразных продуктов, которые могут привести к искажению измеряемых объемов, после каждого выполненного эксперимента производили переполюсовку поляризующих хлорсеребряных электродов. В случае частичной потери хлорсеребряными электродами обратимости, сопровождающейся выделением на них газообразных продуктов, их регенерацию проводили согласно методике, описанной в работе [10].
Удельная электропроводность мембран κ (См/м), которая очевидно совпадает с кинетическим коэффициентом L22, была рассчитана из данных по сопротивлению образцов, измеренному ртутно-контактным методом [11] на частоте переменного тока 50–500 кГц. Частота тока, обеспечивающая равенство мнимой составляющей импеданса ячейки нулю, подбиралась индивидуально для каждого образца и каждой концентрации равновесного раствора. Статическую обменную емкость мембран измеряли методом смещения равновесия с избытком титранта.
ВЕРИФИКАЦИЯ МОДЕЛИ
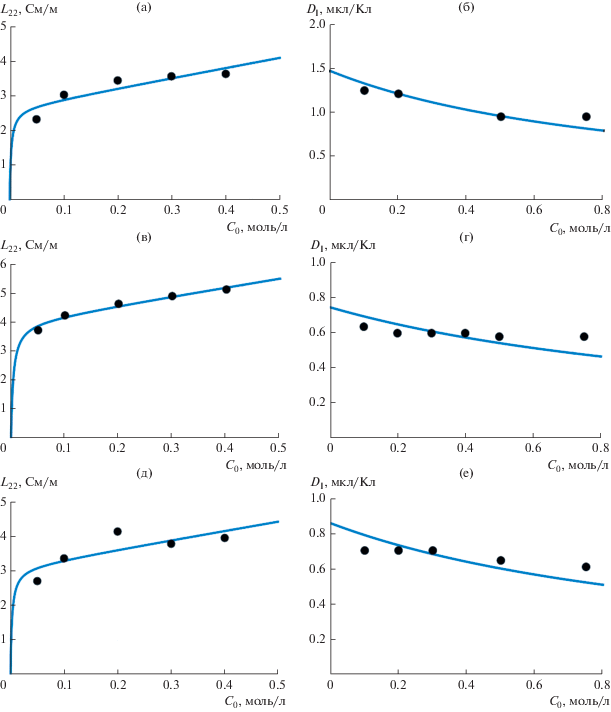
Определение параметров ячеечной модели проводили в два этапа. На первом, предварительном этапе с использованием формул (6) и (7) для идеально селективной катионитовой мембраны $\left( {{{\gamma }_{{\text{m}}}} = \infty } \right)$ и на основании экспериментальных зависимостей ${{D}_{{\text{I}}}}\left( {{{C}_{0}}} \right)$ и $\kappa = {{L}_{{22}}}\left( {{{C}_{0}}} \right)$ находили неизвестные параметры $\left( {{{D}_{{{\text{m + }}}}},{{m}_{0}},{{{\bar {\rho }}}_{0}}} \right),$ минимизируя ошибку отклонения специально построенной целевой функции $f\left( {{{C}_{0}}} \right)$ от ее экспериментальных значений при разных концентрациях электролита,
(8)
$\begin{gathered} f\left( {{{С }_{0}}} \right) = {{D}_{{\text{I}}}}\left( {{{С }_{0}}} \right)H\left( {{{C}_{{\text{1}}}} - {{C}_{0}}} \right) + \\ + \,\,{{L}_{{22}}}\left( {{{С }_{0}} + {{C}_{{\text{1}}}}} \right)H\left( {{{C}_{0}} - {{C}_{{\text{1}}}}} \right)H\left( {{{C}_{2}} - {{C}_{0}}} \right). \\ \end{gathered} $Таблица 1.
Данные оптимизации по приближенным формулам (для идеальной катионообменной мембраны)/ точным формулам
| Мембрана | Dm+, мкм2/с | Dm–, мкм2/с | m0, % | ${{\gamma }_{{\text{m}}}}$ | $\bar {\rho },$ моль/дм3 | ${{\bar {\rho }}_{0}},$ моль/дм3 | kD, Å2 |
|---|---|---|---|---|---|---|---|
| МФ-4СК | 586/586 | –/0 | 9.6/9.3 | $\infty $/3.1 | 1.08 | 106/106 | 3.64/3.64 |
| МФ-4СК/(Hall + Pt) | 838/836 | –/0 | 10.1/9.5 | $\infty $/2.3 | 1.22 | 158/158 | 2.45/2.46 |
| МФ-4СК/(Hall + Fe) | 674/671 | –/0 | 8.9/8.7 | $\infty $/4.1 | 1.16 | 167/161 | 2.32/2.41 |
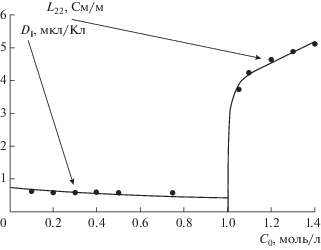
Рис. 2.
Сравнение экспериментальных значений и теоретических кривых для ЭОП и ЭП после проведения процесса сопряженной оптимизации для мембраны МФ-4СК/(Hall + Pt). Для участка электропроводности значения концентрации нужно уменьшить на 1 моль/л.
На втором этапе оптимизировали ту же целевую функцию (8), но для функций ${{L}_{{22}}}\left( {{{C}_{0}}} \right)$ и ${{D}_{{\text{I}}}}\left( {{{C}_{0}}} \right) = {{{{L}_{{12}}}\left( {{{C}_{0}}} \right)} \mathord{\left/ {\vphantom {{{{L}_{{12}}}\left( {{{C}_{0}}} \right)} {{{L}_{{22}}}\left( {{{C}_{0}}} \right)}}} \right. \kern-0em} {{{L}_{{22}}}\left( {{{C}_{0}}} \right)}}$ использовали их точные выражения в случае неидеальной мембраны [3]. При этом количество параметров увеличивалось до 5 (добавлялись коэффициент диффузии коиона Dm– и коэффициент равновесного распределения γm), а значения параметров ${{D}_{{{\text{m + }}}}},$ ${{m}_{0}},$ ${{\bar {\rho }}_{0}},$ найденные на первом этапе, использовали в качестве начальных приближений для второго этапа. Результаты приведены в табл. 1 (знаменатели дробей). Видно, что параметр ${{\gamma }_{{\text{m}}}}$ составляет несколько единиц для всех мембран, что говорит о пониженной концентрации ионов в зернах ионита по сравнению с окружающим их равновесным раствором электролита. При этом коэффициент диффузии коиона оказался на несколько порядков меньше коэффициента диффузии противоиона, поэтому мы положили его в табл. 1 равным нулю. Остальные параметры не сильно изменились по сравнению с идеальным случаем. Макроскопическая пористость для обоих этапов оптимизации находится в пределах 9–10% и слабо различается для всех мембран.
В процессе оптимизации была осуществлена проверка единственности набора определяющих параметров. Необходимость такой проверки связана с большим количеством параметров – 5, требующихся для описания экспериментов с помощью ячеечной модели. С этой целью были проведены два дополнительных оптимизирующих расчета, результаты которых представлены в табл. 2.
Таблица 2.
Данные первой/второй оптимизаций с использованием точных формул
| Мембрана | Dm+, мкм2/с | Dm–, Dm, мкм2/с | m0, % | ${{\gamma }_{{\text{m}}}}$ | $\bar {\rho },$ моль/дм3 | ${{\bar {\rho }}_{0}},$ моль/дм3 | kD, Å2 |
|---|---|---|---|---|---|---|---|
| МФ-4СК | 586/575 | $\frac{{58,\,\,106}}{{0,\,\,0}}$ | 9.6/2.6 | 135/0.51 | 1.08 | 107/104 | 3.64/3.73 |
| МФ-4СК/(Hall + Pt) | 838/814 | $\frac{{66,\,\,122}}{{0,\,\,0}}$ | 10.0/5.0 | 70/0.68 | 1.22 | 158/155 | 2.45/2.50 |
| МФ-4СК/(Hall + Fe) | 673/668 | $\frac{{65,\,\,119}}{{0,\,\,0}}$ | 8.9/5.4 | 558/0.83 | 1.16 | 167/164 | 2.32/2.36 |
Цель первой оптимизации – исключить нулевые значения коэффициента диффузии аниона Dm–, наблюдавшиеся при расчетах по формулам для неидеально селективной мембраны (см. знаменатели дробей в табл. 1). Эта цель была достигнута за счет увеличения коэффициента равновесного распределения ${{\gamma }_{{\text{m}}}},$ который стал достигать несколько десятков (для мембраны с платиной) и даже сотен (для мембраны с железом) единиц. Казалось бы, здесь имеется противоречие с природой ионообменных мембран, так как в этом случае ранее в рамках гомогенной модели было установлено, что ${{\gamma }_{{\text{m}}}} < 1$ [5, 6], поскольку наблюдается положительная сорбция ионов в матрице мембраны. Однако это противоречие устраняется, как только мы принимаем во внимание, что коэффициент ${{\gamma }_{{\text{m}}}}$ для зерна катионита (в ячеечной модели) и для мембраны в целом (гомогенная модель) – это разные величины: концентрация подвижных ионов электролита в зернах катионита существенно ниже, чем в окружающем их равновесном растворе (отрицательная сорбция, ${{\gamma }_{{\text{m}}}} \gg 1$). Действительно, оценим гидродинамическую проницаемость зерен катионита по найденным значениям характерной обменной емкости с использованием формулы связи ${{k}_{{\text{D}}}} = {{{{{\mu }}^{^\circ }}{{D}_{ + }}} \mathord{\left/ {\vphantom {{{{{\mu }}^{^\circ }}{{D}_{ + }}} {\left( {{{{\bar {\rho }}}_{0}}RT} \right)}}} \right. \kern-0em} {\left( {{{{\bar {\rho }}}_{0}}RT} \right)}}$ (последний столбец табл. 1 и 2). На основании полученных значений ${{k}_{{\text{D}}}}$ можно оценить так называемый радиус Бринкмана в зерне ионита ${{R}_{{\text{b}}}} = \sqrt {{{k}_{{\text{D}}}}} ,$ т.е. характерную глубину, на которую течение проникает внутрь пористой частицы при ее контакте с движущейся чистой жидкостью (в остальной части пористого зерна жидкость покоится). Этот радиус, равный 1.5 Å, является наименьшим у мембраны с наночастицами железа, следом идет мембрана с платиной – 1.6 Å и, наконец, чистая мембрана – 1.9 Å. Стоксов радиус протона составляет 0.253 Å, радиус аниона гидроксила – 0.443 Å, аниона хлора – 1.20 Å [12]. В то же время радиус иона кислорода – 1.32 Å, а радиус молекулы воды – 3.1 Å. Сравнивая приведенные значения с радиусом Бринкмана, заключаем, что ни анион хлора, ни анион кислорода, ни, тем более, целиком молекула воды не смогут пройти через зерна катионита. Пройти могут лишь протоны и ионы гидроксила “поодиночке”, если произойдет диссоциация молекул воды, для осуществления которой требуются высокие локальные напряженности электрического поля. Стало быть, перенос воды и ионов электролита может происходить в основном по макропорам между зернами ионита. Отметим попутно, что значения ${{k}_{{\text{D}}}}$ для трех рассмотренных модификаций мембраны МФ-4СК в 2–3 раза выше, чем у родственного полимера – политриметилсилилпропина [13], имеющего примерно такую же макроскопическую пористость (11–13%).
Целью второй из дополнительных оптимизаций было сохранить значения ${{\gamma }_{{\text{m}}}} < 1,$ т.е. “навязать” зернам катионита положительную сорбцию ионов. Однако, как видно в табл. 2 (знаменатели дробей), это приводит к обнулению коэффициента диффузии коиона в зерне ионита (что неправдоподобно) и сильно заниженным (2–6%) значениям макропористости m0. Между тем, метод контактной эталонной порометрии дает для макроскопической пористости мембран МФ-4СК, отлитых с использованием диметилформамида, значения 9–11% [11]. Следовательно, наиболее физическим приемлемым является набор параметров, полученный при первой дополнительной оптимизации (данные в числителях дробей табл. 2). Отметим, что при этом коэффициент диффузии молекулы HCl уменьшается со значения D = 3352 мкм2/с в разбавленном растворе до 106–122 мкм2/с в зернах катионита, т.е. в 27–32 раз. На рис. 3 показано удовлетворительное соответствие экспериментальных данных об удельной электропроводности и ЭОП для всех исследованных мембран теоретическим расчетам, выполненным в ходе первой дополнительной оптимизации (числители дробей в табл. 2). При этом нетрудно заметить, что для всех трех случаев оптимизации значения основных параметров системы Dm+, m0 и ${{\bar {\rho }}_{0}},$ а также связанного с ними ${{k}_{{\text{D}}}}$ практически неизменны. Сильно изменяются коэффициент диффузии Dm– коиона в зерне катионита (геле) и коэффициент равновесного распределения ${{\gamma }_{{\text{m}}}}$ молекул электролита в нем же. Последнее обстоятельство означает, что для определения единственно возможного набора из пяти параметров (m0, ${{\bar {\rho }}_{0}},$ Dm+, Dm–, ${{\gamma }_{{\text{m}}}}$) ячеечной модели хотя бы один из двух последних параметров должен находиться в независимом эксперименте. Поскольку величину Dm– измерить практически невозможно, то это может быть параметр ${{\gamma }_{{\text{m}}}},$ определяемый в экспериментах по обменной сорбции, как это было сделано в работе [14].
РАСЧЕТ ПАРАМЕТРОВ ПО ГОМОГЕННОЙ МОДЕЛИ ТОНКОПОРИСТОЙ МЕМБРАНЫ
Выражение для удельной электропроводности по гомогенной модели впервые было опубликовано в нашей работе [15] (без вывода), а в работе [5] оно впервые применено к обработке экспериментальных данных для мембран МФ-4СК, поверхность которых была модифицирована нанотрубками галлуазита (Hall):
(9)
$\begin{gathered} \kappa = \frac{{{{F}^{2}}}}{{RT}}\bar {\rho }{{D}_{{\text{m}}}}\left( {1 + {{\nu }_{{\text{m}}}}} \right) \times \\ \times \,\,\frac{{\left( {1 + {{\nu }_{{\text{m}}}}} \right)\sqrt {1 + {{{\left( {{{2{{C}_{0}}} \mathord{\left/ {\vphantom {{2{{C}_{0}}} {\bar {\rho }{{\gamma }_{{\text{m}}}}}}} \right. \kern-0em} {\bar {\rho }{{\gamma }_{{\text{m}}}}}}} \right)}}^{2}}} + \left( {1 - {{\nu }_{{\text{m}}}}} \right)}}{{4{{\nu }_{{\text{m}}}}}}. \\ \end{gathered} $В работе [6], как уже отмечалось выше, была представлена новая методика нахождения физико-химических параметров гомогенной модели, основанная на одновременном использовании экспериментальных данных по диффузионной проницаемости,
(10)
$\begin{gathered} P = \frac{1}{2}{{D}_{{\text{m}}}}\frac{\rho }{{{{C}_{0}}}}\left( {\sqrt {1 + {{{\left( {\frac{{2{{C}_{0}}}}{{\bar {\rho }{{\gamma }_{{\text{m}}}}}}} \right)}}^{2}}} - 1 - \frac{{1 - {{\nu }_{{\text{m}}}}}}{{1 + {{\nu }_{{\text{m}}}}}}} \right. \times \\ \times \,\,\ln \left. {\left( {\frac{1}{2}\left( {\left( {1 + {{\nu }_{{\text{m}}}}} \right)\sqrt {1 + {{{\left( {\frac{{2{{C}_{0}}}}{{\bar {\rho }{{\gamma }_{{\text{m}}}}}}} \right)}}^{2}}} + 1 - {{\nu }_{{\text{m}}}}} \right)} \right)} \right), \\ \end{gathered} $В работе [6] для описания экспериментальных данных, полученных для однослойной мембраны МФ-4СК и двух ее образцов, модифицированных галлуазитом и наночастицами платины или железа, использовался пошаговый алгоритм, основанный на попеременном использовании формул (9) и (10) и разных пар из общего набора трех параметров ${{D}_{{\text{m}}}},$ ${{\nu }_{{\text{m}}}},$ ${{\gamma }_{{\text{m}}}}.$ Данный алгоритм, хотя и приводит к нахождению оптимальных (или близких к ним) значений указанных физико-химических параметров, является неудобным в силу большого объема ручного труда и времени. Поэтому мы предлагаем другой (автоматический) алгоритм определения параметров модели, основанный на следующей идее. Минимизация отклонений теоретических и экспериментальных значений проводится сразу по обеим зависимостям $P\left( {{{С }_{0}}} \right)$ и $\kappa \left( {{{С }_{0}}} \right)$ с использованием специально составленной целевой функции
(11)
$\begin{gathered} g\left( {{{С }_{0}}} \right) = P\left( {{{С }_{0}}} \right)H\left( {{{C}_{1}} - {{C}_{0}}} \right) + \\ + \,\,\kappa \left( {{{С }_{0}} + {{C}_{1}}} \right)H\left( {{{C}_{0}} - {{C}_{1}}} \right)H\left( {{{C}_{2}} - {{C}_{0}}} \right), \\ \end{gathered} $Таблица 3.
Физико-химические параметры мембран МФ-4СК, полученные в результате применения гомогенной модели
| Мембрана | Dm+, мкм2/с | Dm–, мкм2/с | m0= Dm+/D+, % | ${{\gamma }_{{\text{m}}}}$ | $\bar {\rho },$ моль/дм3 | ${{\nu }_{{\text{m}}}}$ | Dm, мкм2/с |
|---|---|---|---|---|---|---|---|
| МФ-4СК | 660 | 14.3 | 6.9 | 0.443 | 1.08 | 0.022 | 28.0 |
| МФ-4СК/(Hall + Pt) | 840 | 6.8 | 8.7 | 0.426 | 1.22 | 0.008 | 13.5 |
| МФ-4СК/(Hall + Fe) | 667 | 8.0 | 7.0 | 0.377 | 1.16 | 0.012 | 15.8 |
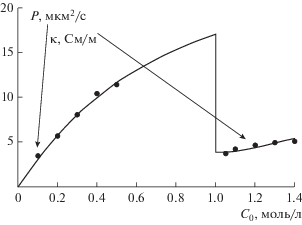
Рис. 4.
Экспериментальные (точки) и теоретические (кривые) зависимости диффузионной проницаемости и удельной электропроводности от концентрации для мембраны МФ-4СК/(Hall + Pt). Вертикальная прямая разделяет участки $P\left( {{{С }_{0}}} \right)$ и $\kappa \left( {{{С }_{0}}} \right)$ (для участка электропроводности значения концентрации нужно уменьшить на 1 моль/л).
Отметим, что качество оптимизации можно регулировать, нормируя функции $P\left( {{{С }_{0}}} \right)$ и $\kappa \left( {{{С }_{0}}} \right),$ входящие в (11), и соответствующие массивы экспериментальных данных, на их максимальные значения. Преимущество предложенного нами сопряженного подхода к определению физико-химических параметров мембранной системы по сравнению с многоступенчатым, представленным в работе [6], состоит в том, что возрастает точность определения параметров. Это позволяет уверенно находить не только коэффициент диффузии противоиона, но и коэффициент диффузии коиона, который значительно меньше (на один-два порядка) по величине. Еще одно преимущество заключается в устойчивости работы новой численной процедуры при изменении данных начального приближения для искомых параметров. Устойчивость достигается за счет более жесткой конструкции сочленяющей формулы (11).
СРАВНЕНИЕ ГОМОГЕННОЙ МОДЕЛИ ТОНКОПОРИСТОЙ МЕМБРАНЫ И ЯЧЕЕЧНОЙ МОДЕЛИ И ОБСУЖДЕНИЕ ПРОБЛЕМЫ ПЕРЕНОСА ВОДЫ
Представляет безусловный интерес сравнить найденные параметры гомогенной и гетерогенной (ячеечной) моделей для одного и того же набора из трех мембран МФ-4СК, который имеется у нас в распоряжении. Для начала установим связь между электропроводностью $\kappa \left( {{{С }_{0}}} \right)$ гомогенной модели и электрокинетическим коэффициентом ${{L}_{{22}}}\left( {{{С }_{0}}} \right)$ ячеечной. Для этого в точном выражении для ${{L}_{{22}}}\left( {{{С }_{0}}} \right)$ (формула (32) в работе [3]) перейдем к пределу при ${{m}_{0}} \to 0,$ означающему отсутствие макроскопической пористости, как это формально предполагается в гомогенной модели мембраны:
(12)
$\begin{gathered} {{\kappa }^{0}} \equiv \mathop {\lim }\limits_{{{m}_{0}} \to 0} {{L}_{{22}}} = \frac{{{{F}^{2}}}}{{2RT}}\left[ {{{{\left( {{{D}_{{{\text{m + }}}}} + {{D}_{{{\text{m}} - }}}} \right)}}^{{^{{}}}}}} \right. \times \\ \times \,\,\left. {\sqrt {{{{\bar {\rho }}}^{2}} + {{{\left( {{{2{{C}_{0}}} \mathord{\left/ {\vphantom {{2{{C}_{0}}} {{{\gamma }_{{\text{m}}}}}}} \right. \kern-0em} {{{\gamma }_{{\text{m}}}}}}} \right)}}^{2}}} + \bar {\rho }\left( {{{D}_{{{\text{m + }}}}} - {{D}_{{{\text{m}} - }}}} \right)} \right] + \frac{{{{k}_{{\text{D}}}}}}{{{{\mu }^{^\circ }}}}{{F}^{2}}{{{\bar {\rho }}}^{2}}. \\ \end{gathered} $Следует отметить, что транспорт воды через ИОМ изучается довольно интенсивно разными исследователями. Например, в работе [16] предпринята попытка описать собственные эксперименты авторов по обратному электродиализу водных растворов NaCl с помощью термодинамики необратимых процессов и связать пермселективность ИОМ с числами переноса соли и воды и моляльностью растворов по обе стороны мембраны. В [17] также экспериментально исследовался осмотический и электроосмотический перенос воды при электродиализе через специально приготовленные с помощью армирующей сетки полимерные катионо- и анионообменные мембраны. Авторы показали, что применение такой сетки внутри мембран может уменьшить осмотический перенос воды как из-за уменьшения площади поверхности, так и, возможно, из-за меньшего набухания мембраны. В недавней работе [18] на основе применения капиллярной модели ИОМ была дана оценка числам свободного переноса воды через нее с использованием теории двойного электрического слоя (ДЭС) Штерна и физико-химических и структурных характеристик мембраны. Однако в области малых концентраций раствора электролита (когда влияние ДЭС наиболее существенно) наблюдается лишь качественное совпадение результатов, а количественное – только при концентрациях, превосходящих 1 моль/л. В то же время при определении характеристик мембран используется как раз область концентраций электролита 0.01–1 моль/л. В предлагаемой нами ячеечной модели, где ДЭС эффективно заменяются скачками электрического потенциала и концентрации, граница применимости полученных формул определяется соотношением толщины ДЭС и “радиуса Бринкмана” – ширины зоны активной фильтрации раствора электролита. Оценки показывают, что полученные результаты в высокой степени достоверны при равновесной концентрации электролита, большей 0.05 моль/л.
ЗАКЛЮЧЕНИЕ
В данной работе проведена проверка адекватности ячеечной модели применительно к исходной гомогенной сульфокатионитовой мембране МФ-4СК и модифицированной нанотрубками галлуазита и наночастицами металлов. Представлен новый сопряженный алгоритм определения физико-химических параметров ячеечной модели на основании данных по удельной электропроводности системы и ее электроосмотической проницаемости.
Впервые предложены точные расчетные формулы для определения электроосмотической проницаемости мембраны при постоянной плотности тока на основании известных модельных физико-химических и геометрических параметров, для определения которых предложен эффективный метод сопряженной оптимизации с использованием экспериментальных данных по электропроводности и электроосмотической проницаемости. Результаты расчетов удовлетворительно согласуются с имеющимися экспериментальными результатами. Выдвинута гипотеза о том, что гомогенная модель тонкопористой мембраны больше соответствует гомогенной по структуре катионообменной мембране МФ-4СК. Ячеечная (гетерогенная) модель мембраны в большей степени должна подходить к описанию свойств гетерогенных мембран, что предполагается проверить в одной из следующих работ авторов.
Возможность вычисления электроосмотического потока воды по алгебраическим формулам с использованием параметров, имеющих ясный физический смысл, важна не только в электромембранных процессах, но и при расчетах так называемых электроосмотических насосов в микрофлюидике [19], а также при анализе условий сохранения необходимого количества влаги в пищевых продуктах при их длительном хранении [20] и, наоборот, минимизации переноса жидкости через бетоны [21]. В этой связи предложенная в данной работе ячеечная модель будет крайне полезной в упомянутых практических случаях, а также в других ситуациях, связанных с регулированием влагосодержания в пористой среде под действием внешнего электрического поля.
Список литературы
Deo S., Filippov A., Tiwari A., Vasin S., Starov V. // Adv. Colloid Interface Sci. 2011. V. 164. P. 21.
Филиппов А.Н. // Коллоид. журн. 2018. Т. 80. С. 745.
Филиппов А.Н. // Коллоид. журн. 2018. Т. 80. С. 758.
Заболоцкий В.И., Никоненко В.В. Перенос ионов в мембранах. М.: Наука, 1996.
Filippov A., Afonin D., Kononenko N., Shkirskaya S. // AIP Conf. Proc. “AMiTaNS’15”. 2015. V. 1684. P. 030004.
Filippov A., Afonin D., Kononenko N., Lvov Y., Vinokurov V. // Colloids Surf. A. 2017. V. 521. P. 251.
Filippov A., Petrova, D., Falina I., Kononenko N., Ivanov E., Lvov Y., Vinokurov V. // Polymers. 2018. V. 10. Article no. 366.
De Groot S., Mazur P. Non-Equilibrium Thermodynamics. Amsterdam: North-Holland, 1962.
Березина Н.П., Шкирская С.А., Сычёва А.А.-Р., Криштопа М.В. // Коллоид. журн. 2008. Т. 70. С. 437.
Гнусин Н.П., Березина Н.П., Демина О.А. // Журн. прикл. химии. 1986. Т. 59. С. 679.
Petrova D.A., Filippov A.N., Kononenko N.A., Shkirskaya S.A., Timchenko M.O., Ivanov E.V., Vinokurov V.A., Lvov Yu.M. // J. Membr. Sci. 2019. V. 582. P. 172.
Мелвин-Хьюз Э.А. Физическая химия. Т. 2. М.: Изд-во иностр. лит-ры, 1962.
Филиппов А.Н., Иванов В.И., Юшкин А.А., Волков В.В., Богданова Ю.Г., Должикова В.Д. // Мембраны и мембранные технологии. 2015. Т. 5. С. 103.
Filippov A.N., Safronova E.Yu., Yaroslavtsev A.B. // J. Membr. Sci. 2014. V. 471. P. 110.
Filippov A., Kononenko N., Afonin D. // Conference Proceedings “Ion Transport in Organic and Inorganic Membranes”, Sochi, 25–30 May 2015. P. 85.
Zlotorowicz A., Strand R.V., Burheim O.S., Wilhelmsen O., Kjelstrup S. // J. Membr. Sci. 2017. V. 523. P. 402.
Porada S., van Egmond W.J., Post J.W., Saakes M., Hamelers H.V.M. // J. Membr. Sci. 2018. V. 552. P. 22.
Фалина И.В., Демина О.А., Заболоцкий В.И. // Коллоид. журн. 2017. Т. 79. С. 792.
Li L., Wang X., Pu Q., Liu S. // Anal. Chim. Acta. 2019. V. 1060. P. 1.
Qiu L., Zhang M., Tang J., Adhikari B., Cao P. // Food Res. Int. 2019. V. 116. P. 90.
Nybo E., Maier R.S., Lauchnor E.G., Seymour J.D., Codd S.L. // Cement Concrete Res. 2019. V. 116. P. 11.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал