Коллоидный журнал, 2019, T. 81, № 5, стр. 660-666
Влияние структурно-энергетических характеристик микропористой структуры углеродных адсорбентов на адсорбцию водорода
А. А. Фомкин 1, *, А. А. Прибылов 1, А. Г. Ткачев 2, Н. Р. Меметов 2, А. В. Мележик 2, А. Е. Кучерова 2, И. Н. Шубин 2, А. Л. Пулин 1, А. В. Школин 1, И. Е. Меньщиков 1, С. А. Жедулов 1, К. О. Мурдмаа 1, С. Д. Артамонова 1
1 Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119071 Москва,
Ленинский проспект, 31, Россия
2 Тамбовский государственный технический университет
392000 Тамбов,
ул. Ленинградская, 1, Россия
* E-mail: fomkinaa@mail.ru
Поступила в редакцию 14.03.2019
После доработки 30.03.2019
Принята к публикации 06.04.2019
Аннотация
Синтезирован новый углеродный микропористый адсорбент МПУ-007 с большим удельным объемом микропор, достигающим 1.44 см3/г. Изучена адсорбция на нем водорода при температуре 303, 313, 323 и 333 К и давлении до 15 МПа. Максимальная величина адсорбции составляет 12 ммоль/г (2.4 мас. %) при 15 МПа и 303 К. Полученные данные сопоставлены с результатами проведенных ранее исследований адсорбции водорода на ряде микропористых углеродных адсорбентов с увеличивающимся удельным объемом микропор. Показано, что дифференциальные мольные изостерические теплоты адсорбции водорода уменьшаются от 10 до 4 кДж/моль с ростом заполнения микропор.
ВВЕДЕНИЕ
Водород широко используется во многих отраслях промышленности – в технологии переработки нефти, производства аммиака, метанола, в металлургии [1]. В последние десятилетия проводятся интенсивные исследования по использованию водорода в качестве энергетического газа, теплоносителя, аккумулятора энергии, источника энергии для разного рода потребителей. Еще в 80-е годы ХХ века были разработаны двигатели на водородном топливе. Использование водорода, как высокоэнергетического газа с практически неограниченной сырьевой базой, в двигателях внутреннего сгорания оправдано, прежде всего, тем, что его высокая теплота сгорания (примерно 120 МДж/кг) превышает более чем в 4 раза теплоту сгорания бензина (около 25 МДж/кг). При сгорании водорода образуется практически только вода, что делает водородные энергетические установки наиболее экологически чистыми.
При всех его достоинствах водород в газообразном состоянии обладает низкой температурой сжижения (его температура кипения Тb = 20.38 K), низкой плотностью при атмосферном давлении и, следовательно, низкой объемной энергией. Возможность широкого применения водорода в качестве экологически чистого источника энергии зависит от решения проблем эффективного его хранения и транспортировки. Определенные сложности при использовании водорода создает его высокая взрыво- и пожароопасность [2]. Поэтому разработка эффективных и безопасных систем хранения водорода является актуальной проблемой.
Наиболее распространенными являются методы хранения водорода в газообразном состоянии при повышенном давлении или в сжиженном состоянии [1]. Хранение сжиженного водорода при 20.38 К хотя и обеспечивает его высокую плотность, равную11 695 м3/м3 [1], но нуждается в использовании специального высокотехнологичного оборудования. Система хранения всегда должна быть открыта для самопроизвольного истечения испаряющегося водорода, что создает дополнительные проблемы обеспечения пожаро- и взрывобезопасности, а также приводит к потерям газа при хранении. Кроме того, система регазификации водорода, требует значительных энергозатрат [3]. Согласно литературным данным перспективными также являются абсорбционные и адсорбционные методы хранения [4–17].
Новое направление использования аккумуляторов водорода в беспилотных летательных аппаратах с электрохимическими топливными элементами требует высоких удельных показателей аккумулирования водорода [18]. Физическая адсорбция H2 в микропористых материалах рассматривается в качестве перспективной технологии при создании высокоемких, экономичных и взрывобезопасных аккумуляторов водорода [19]. Адсорбированный водород находится в силовом поле, создаваемом перекрывающимися полями противоположных стенок микропор, диаметр (ширина) которых соизмерим с размерами сорбируемых молекул. В микропорах, вследствие суперпозиции силовых полей, адсорбция происходит по механизму объемного заполнения [20, 21]. При этом энергия адсорбции определяется не только взаимодействием молекул водорода с поверхностью, но и взаимодействием его адсорбированных молекул между собой с образованием адсорбционных ассоциатов.
Взрывоопасность систем “микропористый адсорбент–водород” исключается из-за высокой степени диспергирования газа микропористой структурой адсорбента, за счет этого становится недостижимой взрывоопасная концентрация водорода.
Адсорбция водорода на существующих промышленных углеродных адсорбентах составляет примерно 1.5 мас. % при температуре T = 293 К и давлении P до 10 МПа. При T = 77 К и P ≈ 5 МПа она может достигать 3 мас. % [22]. Максимальное значение адсорбции водорода, равное 6.2 мас. %, получено в работе [23] при T = 77 К и P = 5.1 МПа. В то же время для использования технологии адсорбционного аккумулирования водорода в перспективе требуется достижение величин адсорбции, составляющих примерно 6.5 мас. % при комнатной температуре [24].
При более высоких температурах адсорбция водорода существенно зависит от характеристик пористой структуры, которая должна быть специально оптимизирована. При этом поверхность адсорбента должна иметь высокую энергетическую гетерогенность. В [11] показано, что адсорбция водорода на ряде микропористых углеродных адсорбентов при p, T = const растет с ростом удельного объема микропор. Однако в соответствии с теорией Дубинина объемного заполнения микропор (ТОЗМ) с ростом объема микропор адсорбция проходит через максимум и затем падает из-за уменьшения энергии адсорбции в широких микропорах. Такая закономерность обнаружена, в частности, при исследовании адсорбции на модельных углеродных адсорбентах [25]. С учетом общих закономерностей адсорбции на микропористых адсорбентах, аналогичные зависимости должны прослеживаться и при адсорбции H2 на ряде адсорбентов с увеличивающимся объемом микропор. В связи с этим, исследование зависимости адсорбции водорода на адсорбентах с большим объемом микропор важно и актуально.
Целью данной работы является изучение влияния структурно-энергетических характеристик микропористых углеродных адсорбентов на адсорбцию водорода.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Адсорбент
В работе использовали углеродный адсорбент с условным обозначением МПУ-007, полученный методом химической активации гидроксидом калия при 750°C смеси кукурузного декстрина, этиленгликоля и фенолформальдегидной смолы. После охлаждения реакционную смесь промыли на фильтре до удаления щелочи, затем обработали соляной кислотой для растворения примесей соединений металлов, промыли водой до нейтрального pH, после чего высушили материал при 110°C до постоянной массы.
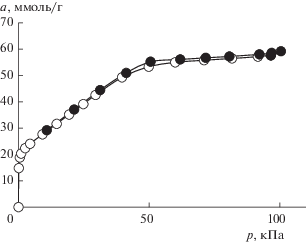
Структурно-энергетические характеристики адсорбента МПУ-007 определяли с использованием изотермы адсорбции азота, измеренной при температуре 77 К (рис. 1) на установке Autosorb iQ (Quantachrome, США).
Как следует из рис. 1, изотерма имеет вид, характерный для адсорбентов с широким распределением пор по размерам − область обратимой адсорбции и узкую область адсорбционного гистерезиса. Резкое изменение хода изотермы при величине адсорбции a = 20 ммоль/г свидетельствует о бимодальном распределении пор по размерам у этого образца активного угля. Для определения параметров микропористой структуры использовали участок изотермы адсорбции, соответствующий интервалу относительных давлений p/ps = 0.01–0.3 [20], и двучленное уравнение адсорбции (1) теории объемного заполнения микропор Дубинина (ТОЗМ) с параметрами, представленными в табл. 1.
(1)
$a = {{a}_{{01}}}\exp \left[ { - {{{\left( {\frac{A}{{E01}}} \right)}}^{{n01}}}} \right] + {{a}_{{02}}}{\text{exp}}\left[ { - {{{\left( {\frac{A}{{E02}}} \right)}}^{{n02}}}} \right].$Таблица 1.
Структурно-энергетические характеристики микропористого углеродного адсорбента МПУ-007, определенные по ТОЗМ
| Удельный объем микропор, W0 = W01 + W02, см3/г | 1.44 |
| Удельный объем микропор первой моды, W01, см3/г | 0.94 |
| Удельный объем микропор второй моды, W02, см3/г | 0.50 |
| Характеристическая энергия адсорбции азота в микропорах первой моды, ${{E}_{{01({{{\text{N}}}_{{\text{2}}}})}}},$ кДж/моль | 5.5 |
| Характеристическая энергия адсорбции азота в микропорах второй моды, ${{E}_{{02({{{\text{N}}}_{{\text{2}}}})}}},$ кДж/моль | 1.2 |
| Характеристическая энергия адсорбции бензола в микропорах первой моды, ${{E}_{{01\left( {{{{\text{С }}}_{6}}{{{\text{Н }}}_{6}}} \right)}}},$ кДж/моль | 15.6 |
| Характеристическая энергия адсорбции бензола в микропорах второй моды, ${{E}_{{02\left( {{{{\text{С }}}_{6}}{{{\text{Н }}}_{6}}} \right)}}},$ кДж/моль | 4.3 |
| Ширина микропор первой моды, Х01, нм | 1.5 |
| Ширина микропор второй моды, Х02, нм | 3.5 |
| Удельная поверхность по азоту, SБЭТ, м2/г | 2520 |
Результаты анализа пористой структуры DFT-методом на установке Autosorb iQ подтверждают наличие бимодального распределения пор по размерам для исследуемого адсорбента.
Регенерацию адсорбента осуществляли при температуре 573 К и давлении, меньшем 0.01 Па.
Водород
В работе использовали газообразный водород особой чистоты. Согласно [1] водород имеет следующие физико-химические характеристики: температура тройной точки ТТ = 13.95 К, температура нормального кипения Тb = 20.38 К, температура критическая Тс = 33.23 К, давление критическое Pc= 13.16 бар, плотность жидкого водорода при температуре кипения ρ = 0.0708 г/см3.
Методика измерения адсорбции
Адсорбцию водорода при давлении вплоть до 15 МПа и температуре 303, 313, 323, 333 К измеряли объемно-весовым методом [27] по изменению массы ампулы с адсорбентом, заполняемой H2. Погрешности измерений по давлению и температуре составили, соответственно, ±0.015 МПа и ±0.3 K, по величине адсорбции ±4 × 10–4 г с доверительной вероятностью 0.95. Абсолютную адсорбцию водорода определяли как полное содержание вещества в микропорах, а объем адсорбента – как сумму объема скелета адсорбента, определенного калибровкой по гелию, и объема микропор.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
С использованием методики [27] получены зависимости адсорбции водорода от давления при температуре 303, 313, 323, 333 К на адсорбенте МПУ 007 (рис. 2).
Рис. 2.
Изотермы абсолютной адсорбции H2 на адсорбенте МПУ-007 при температуре 303 (1), 313 (2), 323 (3) и 333 К (4). Символы – экспериментальные данные, сплошные линии – аппроксимация по ячеечной теории адсорбции Бакаева [33].
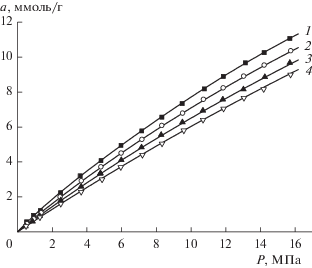
Из экспериментальных данных, представленных на рис. 2, следует, что адсорбция водорода обратима, плавно растет с ростом его давления, не проявляя тенденции к насыщению даже при P = 16 МПа, и уменьшается при повышении температуры. Из уравнения (1) следует, что адсорбция водорода растет с ростом удельного объема микропор. Однако при этом увеличивается их эффективная ширина, что приводит к уменьшению характеристической энергии адсорбции.
Для выяснения зависимости адсорбции водорода на микропористых углеродных адсорбентах от удельного объема микропор мы воспользовались экспериментальными данными [11]. Для сравнения на рис. 3 представлены изотермы адсорбции водорода на микропористых активных углях МПУ-007, ФАС-2008, ФАС-3, АУК и ПАУ-700 при T = 303 К. Наибольшая адсорбция водорода, равная примерно 11 ммоль/г (2.2 мас. %) при 15.7 МПа достигается на адсорбенте МПУ-007, наименьшая, равная 4 ммоль/г (0.8 мас. %), – на адсорбенте ПАУ-700 при том же давлении. В табл. 2 приведены величины адсорбции водорода на этих адсорбентах при давлении 10 МПа и температуре 303 К.
Рис. 3.
Изотермы адсорбции H2 при температуре 303 К на адсорбентах МПУ-007 (1), ФАС-2008 (2), ФАС-3 (3), АУК (4), ПАУ-700 (5).
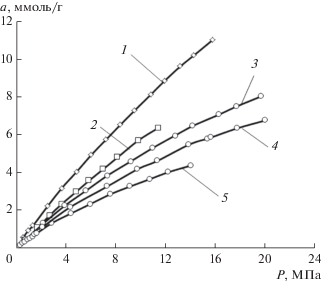
Таблица 2.
Экспериментальные величины адсорбции водорода на микропористых углеродных адсорбентах при давлении 10 МПа и температуре 303 К и рассчитанные по ТОЗМ предельные величины адсорбции насыщенного пара H2 при Тb = 20.38 К
| Адсорбент | ПАУ-700 | АУК | ФАС-3 | ФАС-2008 | МПУ-007 |
|---|---|---|---|---|---|
| Удельный объем микропор, W0, см3/г | 0.46 | 0.51 | 0.71 | 0.96 | 1.44 |
| Эффективная ширина микропор, X0, нм | 0.80 | 0.82 | 1.34 | 1.70 | 0.71 |
| Адсорбция водорода (10 МПа, 303 К, эксперимент), мас. % | 0.66 | 0.84 | 1.0 | 1.16 | 1.48 |
| Предельная величина адсорбции при 20.38 К (ТОЗМ), мас. % | 3.2 | 3.57 | 4.97 | 6.72 | 10.08 |
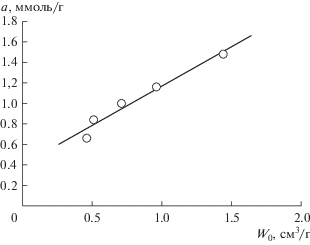
На рис. 4 представлена зависимость адсорбции водорода от удельного объема микропор при 10 МПа и 303 К на микропористых углеродных адсорбентах, различающихся генезисом [11]. Видно, что в изобарных условиях адсорбция растет с увеличением удельного объема микропор W0.
Рис. 4.
Зависимость адсорбции H2 от удельного объема микропор углеродных адсорбентов разного генезиса при давлении 10 МПа и температуре 303 К.
Как следует из табл. 2, адсорбция водорода при Тb = 20.38 К составляет всего лишь 8–20% от ее предельной величины. То есть главную роль в адсорбции водорода играют эффекты взаимодействия его молекул с поверхностью микропор углеродных адсорбентов. Из этого следует важный вывод: увеличение адсорбции водорода наиболее эффективно за счет увеличения энергии его взаимодействия с поверхностью адсорбента, то есть, согласно (1), – за счет увеличения характеристической энергии адсорбции. Это можно осуществить путем модифицирования поверхности с целью создания специфических адсорбционных центров [28].
Изостеры адсорбции
По изотермам адсорбции водорода на микропористом углеродном адсорбенте МПУ-007 построили изостеры адсорбции в координатах ln P–103/T, представленные на рис. 5.
Рис. 5.
Изостеры адсорбции H2 на адсорбенте МПУ-007 при значениях адсорбции a, равных 1.0 (1), 2.0 (2), 3.0 (3), 4.0 (4), 5.0 (5), 6.0 (6), 7.0 (7), 8.0 (8), 9.0 (9), 10.0 (10), 11.0 (11) и 12.0 ммоль/г (12).

Как следует из рис. 5, они в хорошем приближении описываются линейными функциями. Следует отметить, что свойство линейности изостер характерно для адсорбции газов и паров на микропористых адсорбентах [29, 30]. Оно отмечалось и в наших исследованиях [10, 31].
Дифференциальная мольная изостерическая теплота адсорбции
Для расчета дифференциальной мольной изостерической теплоты адсорбции ${{q}_{{{\text{st}}}}}$ использовали общее уравнение [31, 32], учитывающее неидеальность газовой фазы при высоких давлениях (путем введения параметра Z) и неинертность адсорбента при адсорбции, т.е. зависимость V = = V(a, T):
(2)
$\begin{gathered} {{q}_{{{\text{st}}}}} = - RZ{{\left( {\frac{{\partial (\ln P)}}{{\partial \left( {\frac{1}{T}} \right)}}} \right)}_{a}}\left\{ {1 - {{{{{\left( {\frac{{\partial V\left( a \right)}}{{\partial a}}} \right)}}_{T}}} \mathord{\left/ {\vphantom {{{{{\left( {\frac{{\partial V\left( a \right)}}{{\partial a}}} \right)}}_{T}}} {{{V}_{{\text{g}}}}}}} \right. \kern-0em} {{{V}_{{\text{g}}}}}}} \right\} - \\ - \,\,{{\left( {\frac{{\partial P}}{{\partial a}}} \right)}_{T}}\left[ {V\left( {a,T} \right) - T{{{\left( {\frac{{\partial V\left( a \right)}}{{\partial T}}} \right)}}_{a}}} \right], \\ \end{gathered} $В [33] было показано, что деформация адсорбентов при адсорбции в области сверхкритических температур не превосходит 1%, а вклад интенсивностей адсорбционной и термической деформации углеродных адсорбентов пренебрежимо мал. В случае адсорбции водорода на адсорбенте МПУ-007 вклад члена (дP/дa)T составляет менее 2%, поэтому конечное уравнение для расчета теплоты адсорбции имеет вид
(3)
${{q}_{{{\text{st}}}}} = - R{{T}^{2}}{{\left( {\frac{{\partial (\ln P)}}{{\partial \left( T \right)}}} \right)}_{a}}.$На рис. 6 представлены результаты расчета зависимости дифференциальной мольной изостерической теплоты адсорбции водорода от величины адсорбции на адсорбенте МПУ-007.
Рис. 6.
Зависимость дифференциальной мольной изостерической теплоты адсорбции H2 на адсорбенте МПУ-007 от величины адсорбции a при температуре 303 (1), 313 (2), 323 (3) и 333 К (4).
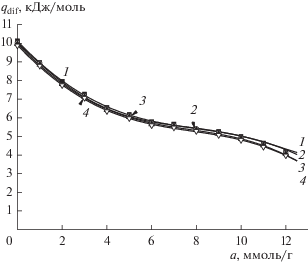
Как следует из рис. 6, теплота адсорбции водорода на адсорбенте МПУ-007 при всех значениях температуры по мере заполнения микропор (от 0 до 12 ммоль/г) уменьшается от 10 до 4 кДж/моль, то есть в 2.5 раза. При этом заполнение микропор достигает всего лишь около 20% от максимального. Такой ход кривых теплоты адсорбции объясняется малой поляризуемостью молекул водорода при широком распределении пор по размерам в изучаемом адсорбенте. По мере заполнения высокоэнергетических адсорбционных центров происходит резкое уменьшение энергии адсорбции. Из данных рис. 4 следует, что дальнейшее увеличение объема микропор углеродных адсорбентов без изменения энергетики поверхности не приведет к существенному увеличению адсорбции водорода. Приведенные в табл. 2 данные свидетельствуют о том, что адсорбенты ФАС-2008 и МПУ-007 имеют высокую потенциальную емкость по водороду, 6.72 и 10.08 мас. %, но обладают недостаточно высокой характеристической энергией адсорбции. Для увеличения адсорбционной активности микропористых углеродных адсорбентов по водороду при условии сохранения большого объема микропор необходимо модифицировать их поверхность введением высокоэнергетических адсорбционных центров.
ЗАКЛЮЧЕНИЕ
1. Синтезирован микропористый углеродный адсорбент МПУ-007 с большим объемом микропор (1.44 см3/г), обладающий бимодальной пористой структурой, перспективный для аккумулирования энергетических газов.
2. Исследована адсорбция водорода на адсорбенте МПУ-007 при давлении до 20 МПа и температуре 303, 313, 323, 333 К. Максимальная величина адсорбции водорода достигает 11 ммоль/г или 2.2 мас. %.
3. На основе полученных данных построены изостеры адсорбции, которые хорошо аппроксимируются линейными зависимостями в координатах ln P−1/T при постоянной величине адсорбции.
4. Рассчитаны зависимости дифференциальной мольной изостерической теплоты адсорбции водорода на микропористом адсорбенте МПУ-007 от величины адсорбции. Теплота адсорбции водорода резко падает по мере заполнения микропор, с 10 до 4 кДж/моль.
5. Из анализа полученных данных следует, что увеличение адсорбции водорода возможно за счет повышения характеристической энергии адсорбции путем введения в структуру адсорбента высокоэнергетических адсорбционных центров.
Список литературы
Гамбург Д.Ю., Семенов В.П., Дубровкин Н.Ф., Смирнова Л.Н. Водород. Свойства, хранение транспортирование, применение. М.: Химия, 1989.
Veziroglu T.N. // Chem. Ind. 1999. V. 53. P. 383.
Пономарев-Степной Н.Н. // Атомная энергия. 2004. Т. 96. С. 411.
Winsche W.E., Hoffmann K.C., Salzano F.J. // Science. 1973. V. 180. P. 1325.
Тарасов Б.П., Лотоцкий М.В., Яртысь В.А. // Рос. хим. журн. 2006. Т. 50. № 6. Р. 34.
Carpetis C., Peschka W. // Int. J. Hydrogen Energy. 1980. V. 5. P. 539.
Chahine R., Bose T.K. // Int. J. Hydrogen Energy. 1994. V. 19. P. 161.
Фомкин А.А., Синицын В.А., Гурьянов В.В. // Коллоид. журн. 2008. Т. 70. С. 408.
Фомкин А.А., Синицын В.А., Гурьянов В.В. // Изв. АН. Сер. хим. 2009. Т. 58. С. 697.
Яковлев В.Ю., Фомкин А.А. // Коллоид. журн. 2009. Т. 71. С. 860.
Фомкин А.А., Прибылов А.А., Мурдмаа К.О., Пулин А.Л., Школин А.В., Меньщиков И.Е., Жедулов С.А. // Физикохимия поверхности и защита материалов. 2019. Т. 55. В печати.
Яковлев В.Ю., Школин А.В., Фомкин А.А., Меньшиков И.Е. // Физикохимия поверхности и защита материалов. 2018. Т. 54. С. 420.
Левин М.А., Исирикян А.А., Фомкин А.А., Серпинский В.В. // Изв. АН СССР. Сер. хим. 1986. С. 2827.
Брек Д. Цеолитовые молекулярные сита. М.: Мир, 1976.
Исаева В.И., Кустов Л.М. // Рос. хим. журн. 2006. Т. 50. № 6. С. 56.
Варшавский И.Л. Энергоаккумулирующие вещества и их использование. Киев: Наукова думка, 1980.
Клямкин С.Н. // Рос. хим. журн. 2006. Т. 50. № 6. С. 49.
Miller A.I. // Nucl. Eng. Int. 2005. V. 50. P. 16.
Богданов А.А. // ЖТФ. 2005. Т. 75. № 9. С. 139.
Дубинин М.М. Адсорбция и пористость. М.: ВАХЗ, 1972.
Фомкин А.А., Синицын В.А. // Физикохимия поверхности и защита материалов. 2008. Т. 44. С. 163.
Chahine R., Bose T.K. // Int. J. Hydrogen Energy. 1994. V. 19. P. 161.
Фомкин А.А., Синицын В.А., Гурьянов В.В. // Коллоид. журн. 2008. Т. 70. С. 408.
Sverdrup G. // Book of Abstracts of VIII World Renewable Energy Congress. Denver, 2004. P. 169.
Меньшиков И.Е., Фомкин А.А., Школин А.В., Яковлев В.Ю., Хозина Е.В. // Изв. АН. Сер. хим. 2018. Т. 67. С. 1814.
Дубинин М.М. // Адсорбция в микропорах / Под ред. Дубинина М.М., Серпинского В.В. М.: Наука, 1983. С. 186.
Прибылов А.А., Калашников С.М., Серпинский В.В. // Изв. АН СССР. Сер. хим. 1990. С. 1233.
Фенелонов В.Б. Пористый углерод. Новосибирск. Изд-во Института катализа СО РАН, 1995.
Авгуль Н.Н., Киселев А.В., Пошкус Д.П. Адсорбция газов и паров на однородных поверхностях. М.: Химия, 1975.
Barrer R.M., Papadopoulos R. // Proc. R. Soc. London. A. 1972. V. 326. P. 315.
Fomkin A.A. // Adsorption. 2005. V. 11. P. 425.
Бакаев В. А. // Изв. АН СССР. Сер. хим. 1971. С. 2648.
Школин А.В., Фомкин А.А. // Коллоид. журн. 2009. Т. 71. С. 116.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал