Коллоидный журнал, 2019, T. 81, № 5, стр. 625-633
Механохимия BI2O3. 2. Механическая активация и термические реакции в энергонасыщенной системе Al + Bi2O3
А. Н. Стрелецкий 1, *, Г. А. Воробьева 1, И. В. Колбанев 1, А. В. Леонов 2, В. Г. Кириленко 1, Л. И. Гришин 3, 4, А. Ю. Долгобородов 1, 3, 4
1 Институт химической физики им. Н.Н. Семенова РАН
119991 Москва, ул. Косыгина, 4, Россия
2 Московский государственный университет им. М.В. Ломоносова,
химический факультет
119991 Москва, Ленинские горы, 1, стр. 3, Россия
3 Национальный исследовательский ядерный университет “МИФИ”
115409 Москва,
Каширское шоссе, 31, Россия
4 Объединенный институт высоких температур РАН
125412 Москва,
ул. Ижорская, 13/19, Россия
* E-mail: str1945@yandex.ru
Поступила в редакцию 10.04.2019
После доработки 28.04.2019
Принята к публикации 29.04.2019
Аннотация
Методами рентгеновской дифракции, синхронного термоанализа и измерения температуры воспламенения при контакте с горячей поверхностью проанализированы закономерности механической активации (МА) и реакционной способности энергонасыщенной системы 15Al + 85Bi2O3 (мас. %). Без МА взаимодействие между компонентами при прогреве в ячейке ДСК не зарегистрировано до 760°C. В результате МА реакция частично протекает непосредственно при помоле, а также при последующем прогреве. При прогреве со скоростью 10 град/мин взаимодействие между компонентами с образованием металлического Bi и аморфного Al2O3 происходит в температурном интервале 350–800°C с максимумами при 520 и 630°C. Ниже 480°C реакция протекает в нанослоях, что следует из положения и формы кривой плавления образовавшегося висмута. Выяснено влияние продолжительности МА на глубину превращения компонентов, кинетику реакции при прогреве в ячейке ДСК, температуру воспламенения при контакте активированного образца с горячей поверхностью и скорость горения смеси. Установлена оптимальная продолжительность МА, при которой температура воспламенения минимальна.
1. ВВЕДЕНИЕ
В первой работе [1] настоящего цикла проанализированы литературные данные о свойствах различных модификаций Bi2O3, возможности использования оксида висмута и соединений на его основе для самых различных приложений, а также особенности дефектной структуры оксида, формирующейся при его механической активации (МА). Настоящая работа посвящена закономерностям образования и свойствам механически активированных энергетических композитов (МАЭК) Al/Bi2O3.
Смесь Al + Bi2O3 реагирует в соответствии с уравнением (1) с высоким тепловым эффектом, равным 506 кал на 1 г смеси.
(1)
$2{\text{Al}} + {\text{B}}{{{\text{i}}}_{2}}{{{\text{O}}}_{3}} \to {\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{3}} + 2{\text{Bi}}{\text{.}}$Существенный интерес к этой системе вызван тем, что среди различных наноразмерных термитных смесей при горении наноразмерных частиц Al + Bi2O3 достигаются наиболее высокие импульс и скорость роста давления [2]. Особенностью этой термитной реакции является выделением газообразного висмута [3, 4], так как температура его кипения ниже температуры термитной реакции. Упомянутые свойства открывает широкие перспективы различных практических применений термита Al/Bi2O3 [2, 5–7]. Для этой системы характерно также отсутствие низших оксидов Bi и низкая температура плавления (около 270°C) металлического Bi. Эти обстоятельства благоприятны для анализа предполагаемой одностадийной кинетики реакции (1) и возможности следить за ней калориметрическими методами по теплоте плавления образующегося висмута.
Известно, что одним из путей снижения температуры воспламенения и увеличения скорости горения в термитных реакциях, а также создания наноразмерного состояния компонентов является МА исходных смесей [8–12]. Основными причинами этих эффектов являются увеличение поверхности контакта между компонентами, создание различных дефектов в их структуре, формирование свежеобразованной неокисленной поверхности металла и другие факторы. В частности, образование дефектной структуры в МоО3 при его МА способствует заметному снижению температуры выделения кислорода из оксида [12]. Температурный диапазон выделения кислорода совпадает с температурами воспламенения термитов на основе МоО3, и можно полагать, что этот процесс вносит существенный вклад в активацию реакции.
Ряд результатов исследования влияния МА на свойства термита Al/Bi2O3 приведен в [8]. В данной работе влияние МА на структуру и реакционную способность термитной композиции Al/Bi2O3 сопоставлено со свойствами активированного Bi2O3. Реакционную способность МАЭК Al/Bi2O3 оценивали несколькими методами. Во-первых, калориметрическим и дифракционным методами контролировали реакцию (1) при медленном прогреве системы в дифференциальном сканирующем калориметре (ДСК) со скоростью 10 град/мин. Во-вторых, изучали влияние продолжительности МА на воспламенение МАЭК при его контакте с горячей поверхностью. Наконец, были проведены первые опыты по измерению влияния активации на скорость горения МАЭК.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали α-Bi2O3 марки “х. ч.” и алюминий марки ПП-2Л. В связи с тем, что в исходном оксиде висмута оказалось значительное количество висмутита Bi2O2CO3, перед проведением экспериментов оксид висмута обычно отжигали на воздухе при 650–670°C. При этом происходит разложение карбоната с выделением CO2 в газовую фазу и формированием α-Bi2O3. Дифракционные данные подтвердили однофазность исходного Bi2O3 после отжига.
Механоактивацию образцов проводили в вибрационной мельнице Аронова в инертной среде. Общая масса загрузки – 12 г (1.8 г Al + 10.2 г Bi2O3). Соотношение компонентов выбрано с небольшим избытком Al по сравнению со стехиометрией (10.8/89.6) реакции (1). Масса шаровой загрузки – 200 г. Для предотвращения взрывного протекания реакции в процессе МА в барабан добавляли 15 мл гексана, а помол проводили циклами по 30 с (с перерывами между циклами по 5 мин).
Дифракционные, адсорбционные, калориметрические, термогравиметрические и масс-спектральные измерения, а также количественный фазовый анализ проводили аналогично [1].
Температуру воспламенения и время задержки воспламенения при контакте МАЭК с горячей поверхностью измеряли на установке, аналогичной приведенной рис. 3 в работе [13]. Навеску исследуемого порошка массой 35 мг помещали в контейнер, вводили в печь, сбрасывали на нагретую поверхность и замеряли время t, через которое композит воспламенится. Нагрев медной воспламеняющей поверхности проводили в муфельной печи ПМ-700, температуру пластины определяли с точностью до 1°C. Максимальная температура пластины – 400°C. Задержку воспламенения измеряли с точностью 0.5 с.
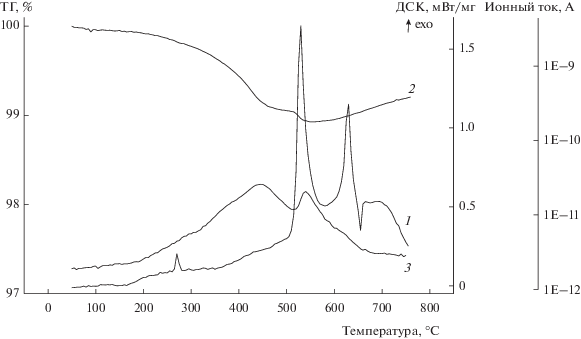
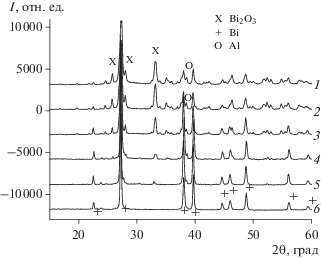
Рис. 1.
Дифрактограммы исходного Bi2O3 (1) и активированных смесей 15Al + 85Bi2O3 (2–5). Продолжительность активации 6 (2), 12 (3) и 15 мин (4, 5).
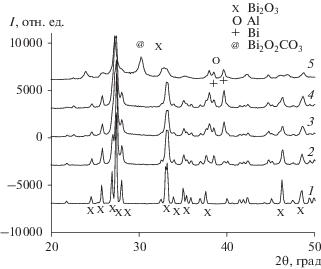
Рис. 2.
Тепловые эффекты при прогреве смеси 15Al + 85Bi2O3 (мас. %) до (1) и после (2, 3) МА; кривая 3 получена при повторном прогреве активированного образца.
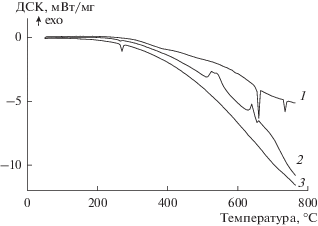
Рис. 3.
Кривые ДСК (1), ТГ (2) и выделения CO2 (3) при прогреве образца 4 из табл. 1 в He. Тепловые эффекты поправлены на базовую линию. Пояснения в тексте.
3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
3.1. Механическая активация
Перечень опытов со смесями 15Al + 85Bi2O3 (мас. %) приведен в табл. 1. Опыты 2–4 выполнены с образцами Bi2O3, предварительно прогретыми при 650°C и не содержащими висмутита, в опыте 5 использовали исходный образец Bi2O3, содержащий Bi2O2CO3.
Таблица 1.
Результаты количественного РФА, размеры L областей когерентного рассеяния и содержание висмута по данным ДСК после МА смеси 15Al + 85Bi2O3 (мас. %) в течение разного времени τ
| № опыта (образца) | τ, мин | Фазовый состав, мас. % | [Bi], мас. % | L, нм | |||||
|---|---|---|---|---|---|---|---|---|---|
| Bi2O3 | Bi | Al | Bi2O2CO3 | Al | Bi2О3 | Bi | |||
| 1 | 0 | 85 | 15 | ||||||
| 2 | 6 | 76.7 | 4.8 | 18.5 | – | 3.2 | 200 | 43 | 89 |
| 3 | 12 | 66.1 | 19.6 | 14.3 | – | 14 | 200 | 31 | 45 |
| 4 | 15 | 62.5 | 21.5 | 16.0 | – | 20 | 120 | 31 | 45 |
| 5 | 15 | 32 | 9 | 10 | 49 | 9 | |||
На рис. 1 приведены дифрактограммы исходного прогретого оксида висмута и четырех смесей Al + Bi2O3 после их МА в течение разного времени. Для исходного образца дифракционным методом наличие карбоната не обнаружено. В результате МА на дифрактограммах кроме линий Al и Bi2O3 появляются линии Bi. Другие фазы не зарегистрированы. Результаты полуколичественного рентгенофазового анализа (РФА) суммированы в табл. 1. Данные РФА носят иллюстративный характер, так как второй продукт реакции (1) – оксид алюминия – является аморфным и при анализе не учитывается. Тем не менее, видно, что с ростом продолжительности активации содержание фазы висмута заметно увеличивается. Таким образом, взаимодействие между компонентами по реакции (1) частично протекает уже в процессе МА смеси.
Как следует из табл. 1 и рис. 1, МА образца 5, в котором присутствует висмутит, не сопровождается разложением карбоната висмута. Интенсивная широкая линия при 2θ ≈ 30°, соответствующая линии висмутита, сохранилась после максимальной продолжительности активации (дифрактограмма 5 на рис. 1), а содержание этой фазы в образце составляет около 50% (табл. 1).
Из рис. 1 следует, что МА смеси сопровождается уширением дифракционных линий. Грубая оценка размеров L областей когерентного рассеяния (ОКР), полученная из данных по количественному фазовому анализу для трех основных фаз приведена в последних столбцах табл. 1. Видно, что размер ОКР для Bi2O3 меньше, чем для Al, увеличение продолжительности активации сопровождается уменьшением значений L, при этом размеры ОКР образующейся фазы висмута близки к размерам ОКР оксида висмута.
Измерения удельной поверхности S дали следующие результаты: для исходного Вi2О3S = 0.1 м2/г, для исходного Al S = 0.43 м2/г, для образцов 2 и 3 (табл. 1) значения S равны 1.5 и 2 м2/г. Таким образом, в процессе МА двухкомпонентной смеси происходит разрушение и уменьшение размеров частиц, однако, по-видимому, размеры частиц композитов больше размеров ОКР.
Насыпная плотность образцов 2 и 3 оказалась равной 2.87 г/см3.
3.2. Химические превращения при медленном прогреве Al/Bi2O3 в ДСК
Влияние МА на ускорение превращения смеси 15Al + 85Bi2O3 по реакции (1) проверяли, прежде всего, путем медленного прогрева (10 град/мин) не активированных и активированных смесей в ячейке ДСК.
Кривая 1 на рис. 2 соответствует тепловым эффектам при прогреве смеси 15Al + 85Bi2O3 до ее МА. На кривой наблюдаются два эндоэффекта, при 650 и 730°C, обусловленные плавлением алюминия и фазовым переходом α-Bi2O3 → δ-Bi2O3 соответственно. На дифрактограмме прогретого образца (первичные данные не приведены) присутствуют фазы Al и Bi2O3 и отсутствует фаза Bi. Таким образом, при прогреве неактивированной смеси компонентов до 760°C реакция (1) не протекает.
Кривая 2 на рис. 2 соответствует прогреву активированного образца 5 (табл. 1). На тепловой кривой наблюдается слабый эндотермический пик плавления металлического висмута при 270°C, который образовался в ходе МА, экзотермические пики, отвечающие реакции оксида висмута с алюминием, с максимумами при 530 и 620°C и эндотермический пик плавления сохранившегося алюминия. При повторном прогреве этого же образца (кривая 3) интенсивность пика плавления висмута резко возрастает, а остальные пики пропадают. Таким образом, можно полагать, что прогрев механически активированной смеси до 760°C приводит к полному протеканию реакции (1).
ДСК-кривая 1 на рис. 3 соответствует разнице кривых первого и второго прогревов образца 4 из табл. 1. При вычитании кривой второго прогрева из кривой первого прогрева появляется формальный экзотермический пик при 270°C из-за того, что к моменту начала повторного прогрева в образце накопилось максимальное количество металлического висмута. Поэтому вблизи температуры плавления висмута формальный экзотермический пик заменен на реальный эндотермический пик, наблюдаемый при первом прогреве. Таким образом, кривая 1 соответствует реально наблюдаемым тепловым эффектам, поправленным на базовую линию. Видно, что превращение протекает в широком температурном диапазоне и имеет два четко выраженных максимума при 520 и 630°C.
Кривая 2 на рис. 3 соответствует данным термогравиметрии (ТГ). Видно, что при температуре выше 300°C масса образца начинает уменьшаться, а при температуре около 520°C кривая изменения массы имеет перегиб, совпадающий по положению с первым интенсивным максимумом на ДСК-кривой. Синхронно с уменьшением массы зафиксировано выделение в газовую фазу CO2 (кривая 3). Кривая выделения газа имеет два максимума, первый при 420°C, а второй совпадает с экзотермическим пиком на ДСК-кривой и перегибом на ТГ-кривой при 520°C. В температурном диапазоне 580–760°C масса образца увеличивается.
В третьем столбце табл. 2 сопоставлены данные ТГ-измерений при низких температурах (до 580°C) для всех образцов. Во всех случаях потеря массы сопровождается выделением CO2. Максимальная потеря массы наблюдается для образца 5 (табл. 1), содержащего висмутит. Выделение CO2 в этом случае обусловлено разложением карбоната. В образцах 2–4 фаза висмутита отсутствует. Выделение CO2 в этих случаях, вероятнее всего, обусловлено окислением накопившихся в смесях следовых количеств углерода следами кислорода в газовой фазе. Углерод в образцах образовался, очевидно, вследствие разложения при МА гексана, в котором проводили помол смеси.
Таблица 2.
Изменение массы (ΔМ) смесей 15Al + 85Bi2O3 (мас. %) при прогреве до разной температуры и относительное содержание Al при 650°C при первом и повторном прогреве образцов, активированных разное время τ. Q – экспериментальная теплота плавления Al, [Al]/[Al]0 – доля Al после прогрева до 650°C относительно его содержания в исходной смеси
| № | τ, мин | Первый прогрев | Второй прогрев, 760°C | ||||||
|---|---|---|---|---|---|---|---|---|---|
| ΔМ, % | Q(Al), кал/г | [Al]/[Al]0, % | ΔМ, % | Q(Al), кал/г | [Al]/[Al]0,% | ||||
| 580°C | 760°C | 900°C | |||||||
| 1 | 0 | – | – | – | 63.17 | 100 | – | – | – |
| 2 | 6 | –0.86 | –0.53 | – | 11.94 | 19 | +0.4 | 11.5 | 18 |
| 3 | 12 | –1.51 | –1.10 | – | 9.78 | 15 | +0.68 | 4.0 | 6.6 |
| 4 | 15 | –1.08 | –0.79 | –2.71 | 4.5 | 7.3 | 0 | 0 | |
| 5 | 15 | –5.2 | –4.34 | –5.6 | 4.1 | 6.6 | 0 | 0 | 0 |
В четвертом столбце табл. 2 сопоставлены данные об изменение массы для всех образцов к температуре 760°C. Видно, что во всех случаях в диапазоне 580–760°C масса образцов увеличивается. Это связано, по-видимому, с окислением сохранившегося в системе алюминия следами кислорода из газовой фазы. Следует напомнить, что алюминий в исходной смеси присутствовал в избытке по сравнению со стехиометрией уравнения (1).
Для образцов 4 и 5 зафиксировано заметное уменьшение массы при температуре 800–900°C (столбец 5 в табл. 2), обусловленное, возможно, разложением остатков оксида висмута.
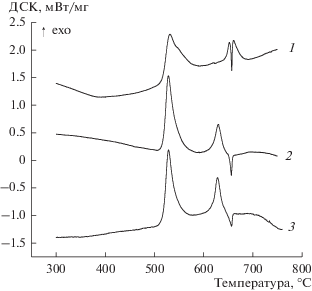
На рис. 4 сопоставлены ДСК-кривые для смесей 15Al + 85Bi2O3, активированных в течение разного времени τ (образцы 2–4 в табл. 1). Видно, что положение первого экзотермического пика при 520°C для всех трех образцов примерно одинаково, а положение второго экзотермического пика сдвигается в область меньших значений температуры при увеличении продолжительности МА. Для смеси, активированной в течение 6 мин, этот второй пик расположен вблизи температуры плавления алюминия, а для смесей после 12 и 15 мин активации он сдвинут в низкотемпературную область на 30°C и хорошо разрешен с пиком плавления алюминия.
Рис. 4.
ДСК-кривые для образцов, активированных в течение (1) 6 мин (образец 2 в табл. 1), (2) 12 мин (образец 3), (3) 15 мин (образец 4).
Количество алюминия, непрореагировавшего к 650°C, оценено из площади пика плавления Al. Величины эндотермических тепловых эффектов плавления алюминия после прогрева смесей 15Al + 85Bi2O3 до 650°C сопоставлены в табл. 2. Для исходной неактивированной смеси (образец 1) реакция при прогреве не произошла, и содержание алюминия Q = 15 мас. %, т.е. оно равно его содержанию в исходной смеси, и [Al]/[Al]0 = 100%. После 6 мин активации (образец 2) доля непрореагировавшего алюминия составляет 19%. По мере роста продолжительности активации доля алюминия, сохранившегося к 650°C, уменьшается, и для образца 5 [Al]/[Al]0 = 6.6%.
В последних двух столбцах табл. 2 приведены данные о содержании алюминия после повторного прогрева тех же образцов. Оказалось, что повторный прогрев практически не изменяет содержание алюминия в образце 2, в то время как в образце 3 количество непрореагировавшего металла уменьшается в два раза, а для образцов 4 и 5 пик плавления алюминия вообще отсутствует. Небольшое увеличение массы при повторном прогреве обусловлено, по-видимому, частичным окислением сохранившегося алюминия следами кислорода в гелии.
Для анализа кинетики термических превращений образцы прогревали до различных промежуточных значений температуры (310, 400, 480, 590, 680, 900°C). Такие значения температуры прогрева выбраны на основании вида термограмм на рис. 3 и рис. 4. Основной массив опытов проводили по следующей схеме: прогрев до одной из перечисленных выше температур, охлаждение и повторный прогрев до 310°C, т.е. чуть выше температуры плавления висмута, а затем измеряли дифрактограммы.
На рис. 5 приведен пример серии дифрактограмм для одной из смесей Al/Bi2O3 после ее прогрева по указанной выше схеме. Видно, как с ростом температуры уменьшается интенсивность линий оксида висмута и алюминия и возрастает интенсивность линии металлического висмута. Реакция протекает в широком температурном диапазоне, от 300 до 700–800°C, и на промежуточных стадиях не зафиксированы частично восстановленные оксиды висмута, т.е. разложение идет нацело по реакции (1), без промежуточных стадий. В силу ряда причин (оксид алюминия аморфен, линии алюминия перекрываются с линиями висмута) количественный РФА проводить нецелесообразно. Полуколичественные данные о кинетике реакции при механической активации и последующем прогреве были получены на основании оценки количества образовавшегося висмута из калориметрических данных.
Рис. 5.
Дифрактограммы образца 4 (табл. 1) после помола (1) и дополнительного прогрева в ДСК до 310 (2), 480 (3), 590 (4), 680 (5), 900°C (6).
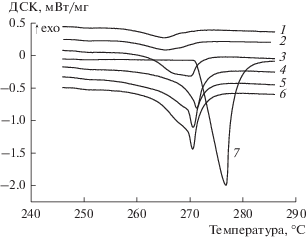
На рис. 6 сопоставлены кривые плавления висмута для образца 3 из табл. 1 после его прогрева до разной температуры. Для эталона висмута (кривая 7) кривая плавления имеет четко выраженный перегиб, а плавление происходит при 271.5°C. Для образца после МА (кривая 1) наблюдается галообразная кривая без четкого перегиба. Теплопоглощение начинается при 257°C. Это различие со стандартной кривой плавления можно трактовать как образование наноразмерных частиц висмута. После прогрева до 400°C (кривая 2) галообразная кривая несколько сдвигается в область высоких температур. После прогрева до 500°C (кривая 3) на кривой плавления появляется вклад от плавления фракции частиц “нормального” висмута. Наконец, на кривых 4–6 этот вклад заметно увеличивается.
Рис. 6.
Кривые плавления висмута в образце 3 (табл. 1) сразу после помола (1) и после дополнительного прогрева до 400 (2), 500 (3), 590 (4), 640 (5), 750°C (6), а также кривая плавления эталона Bi (7).
В табл. 3 приведены результаты анализа ширины дифракционных линий фазы висмута, который образовался в реакции (1) при МА или при последующем прогреве. Данные соответствуют опытам, представленным на рис. 6 для образца 3. Видно, что после МА размеры ОКР висмута составляют около 45 нм. Последующий прогрев приводит к росту размеров ОКР. Сопоставляя данные табл. 3 и рис. 6, можно заключить, что пик плавления “нормального” висмута появляется при размерах ОКР больше 60–80 нм. Кроме того, из данных табл. 3 следует, что размеры ОКР после прогрева до 350°C больше, чем после МА, но до прогрева. Данные РФА подтверждают относительное увеличение концентрации Bi при прогреве до 350°C.
Таблица 3.
Размер L ОКР и величина микродеформаций ε фазы висмута, образовавшегося при МА и последующем прогреве активированного образца до разной температуры T (образец 3 в табл. 1)
| T | 25°C | 350°C | 500°C | 590°C | 640°C | 750°C |
| L, нм | 45 ± 2 | 54 ± 2 | 77 ± 2 | 64 ± 1 | 70 ± 1 | 78 ± 1 |
| ε, % | 0.21 ± 0.01 | 0.15 ± 0.01 | 0.11 ± 0.01 | 0.1 ± 0.01 | 0.13 ± 0.01 | 0.14 ± 0.01 |
Таким образом, в процессе МА и при прогреве до 400°C реакция протекает в областях с размерами 45–55 нм, а затем возникают области продукта со средними размерами больше 70–80 нм. Следует отметить, что вид кривой плавления висмута даже после прогрева до 750°C указывает на существование в образце широкого распределения частиц по размерам с сохранением фракции с размерами около 50 нм.
Полученные результаты не противоречат литературным данным [14–17] о снижении температуры плавления Bi в наноразмерном состоянии.
На рис. 7 приведены кривые накопления продукта реакции (1) – висмута в результате МА и при прогреве активированных в течение разного времени смесей. Из этих данных можно сделать следующие выводы.
Рис. 7.
Кинетика накопления Bi после активации и прогрева до разной температуры. Время МА: 1 – 6, 2 – 12, 3 – 15 мин (образец 4 в табл. 1).
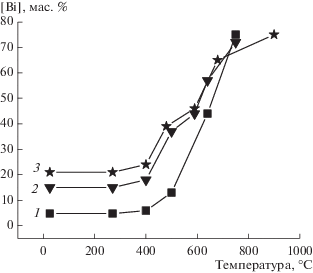
1. Частично реакция протекает при помоле: после 6 мин активации образовалось около 5 мас. % Bi, после 12 мин – 15% Bi, а после 15 мин – 20% Bi.
2. При прогреве реакция начинается уже при температуре 300–400°C, а завершается к 750–900°C.
3. При малой продолжительности МА (6 мин) скорость реакции (1) при низких температурах заметно ниже, чем при бóльших временах активации. Так, например, для образца после 6 мин активации увеличение концентрации висмута в различных диапазонах температуры составляет: Δ6[Bi] (270–400°C) = 1.1%, Δ6[Bi] (400–500°C) = = 7%; в то же время для образца после 12 мин активации Δ12[Bi] (270–400°C) = 3%, Δ12[Bi] (400–500°C) = 19%.
3.3. Воспламенение МАЭК при контакте с горячей подложкой
На рис. 8 приведены данные по временам задержки воспламенения при контакте МАЭК с горячей подложкой. Для смеси со временем активации τ = 12 мин (кривая 2) при температуре подложки 320–350°C воспламенение происходило за время, меньшее 1 с, а при температуре 285°C – через 4 с после контакта. Минимальная температура, при которой воспламенение происходило меньше, чем за 1 с, обозначена нами как T0. Для смеси с τ = 12 мин T0 = 320°C. При снижении температуры подложки ниже некоторого значения T∞ воспламенение МАЭК не происходит. На рис. 8 эти температуры обозначены вертикальными стрелками.
Рис. 8.
Времена задержки t самовоспламенения при контакте активированных смесей 15Al + 85Bi2O3 с подложкой, нагретой до температуры Т. Время МА: 1 – 6, 2 – 12, 3 – 15 мин (образец 5 в табл. 1).
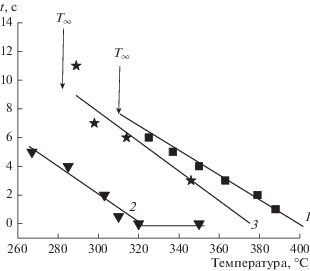
Как следует из данных рис. 8, легче всего воспламеняется образец 3 со временем активации 12 мин. Для него минимальная температура воспламенения, равна 267°C, а при температуре 320°C он воспламеняется мгновенно. Для образца 2 с меньшей продолжительностью активации (τ = 6 мин) аналогичные значения температуры существенно выше (310 и 400°C). Образец 5, подвергнутый активации в течение 15 мин, также воспламеняется хуже, чем образец 2. Следует, однако, отметить, что этот образец содержал значительное количество висмутита. Аналогичную экстремальную зависимость температуры воспламенения от продолжительности активации наблюдали также для системы Al/CuO [12].
Помимо температуры воспламенения для смесей со временем активации 6 и 12 мин была измерена скорость горения зарядов с плотностью 3.0 г/см3 в пластиковых трубках с внутренним диаметром 6.5 мм. Горение инициировали нагревом нихромовой проволоки. Скорость измеряли путем регистрации свечения процесса фотодиодами, на которые по световодам поступало световое излучение продуктов горения. Световоды внедряли внутрь зарядов до половины диаметра, что исключало влияние на регистрацию скорости горения возможных проскоков пламени вдоль стенок трубки. Для смеси Al/Bi2O3 с τ = 6 мин скорость горения на расстоянии 60 мм от точки поджига составила 130 м/с. С увеличением времени активации до 12 мин скорость горения увеличилась до 220 м/с.
4. ЗАКЛЮЧЕНИЕ
Таким образом, в результате механической активации в энергонапряженной аппаратуре термитной смеси Al/Bi2O3 ее реакционная способность резко увеличивается. Реакционную способность проверяли тремя способами: при медленном нагреве (10 град/мин) активированной смеси в ячейке ДСК и при быстром нагреве (~103 град/с) в результате контакта активированного порошка с горячей поверхностью, а также измеряя скорость горения.
В исходной (не активированной) смеси Al/Bi2O3 реакцию между компонентами не удалось провести при температуре ≤800°C при медленном нагреве и при температуре ≤400°C при быстром разогреве. Механическая активация смеси компонентов сопровождается взаимодействием между ними уже в процессе помола и приводит к резкому снижению температуры начала реакции при последующем прогреве. Реакция протекает по одностадийному механизму, в соответствии с уравнением (1), и начинается в наноразмерных областях размером 45–55 нм. Причина влияния МА на реакционную способность может быть связана с уменьшением размеров кристаллитов (ОКР) и перемешиванием компонентов (увеличением поверхности контакта компонентов SC).
При малом времени активации (6 мин) SC, по-видимому, еще недостаточно велика, поэтому глубина превращения при помоле минимальна, а скорость термического превращения в диапазоне 270–500°C существенно ниже, чем для образцов, активированных в течение 12 и 15 мин (рис. 7). Это приводит к тому, что воспламенение при контакте с горячей поверхностью происходит при заметно более высоких температурах. С точки зрения параметров воспламенения наилучшим оказался образец термитной смеси после 12 мин активации. При большей продолжительности активации (τ = 15 мин) воспламенение протекает хуже. Не исключено, что это обусловлено более высокой глубиной реакции при помоле. В первых экспериментах по измерению скорости горения показано, что увеличение продолжительности МА с 6 до 12 мин сопровождается почти двукратным ее возрастанием.
Список литературы
Стрелецкий А.Н., Колбанев И.В., Воробьева Г.А., Леонов А.В., Борунова А.Б., Дубинский А.А. // Коллоид. журн. 2019. В печати.
Puszynski J.A., Bulian C.J., Swiatkiewicz J.J. // J. Propul. Power. 2007. V. 23. P. 698.
Ermoline A., Schoenitz M., Dreizin E.L. // Combust. Flame. 2011. V. 158. P. 1076.
Monk I., Schoenitz M., Dreizin E.L. // J. Energ. Mater. 2017. V. 35. P. 29.
Patel V.K., Kant R., Choudhary A., Painuly M., Bhattacharya S. // Defence Technology. 2019. V. 15. P. 98.
Martirosyan K.S., Wang L., Vicent A., Luss D. // Nanotechnology. 2009. V. 20. 405609.
Ilunga K., del Fabbro O., Yapi L., Focke W.W. // Powder Technol. 2011. V. 205. P. 97.
Dreizin E.L., Schoenitz M. // J. Mater. Sci. 2017. V. 52. P. 11789.
Dreizin E.L. // Prog. Energy Combust. Sci. 2009. V. 35. P. 141.
Baláž P., Achimovičová M., Baláž M., Billik P., Cherkezova-Zheleva Z., Criado J.M., Delogu F., Dutková E., Gaffet E., Gotor F.J., Kumar R., Mitov I., Rojac T., Senna M., Streletskii A., Wieczorek-Ciurowa K. // Chem. Soc. Rev. 2013. V. 42. P. 7571.
Dolgoborodov A.Yu. // Combust. Explos. Shock Waves. 2015. V. 51. P. 86.
Streletskii A.N., Sivak M.V., Dolgoborodov A.Yu. // J. Mater Sci. 2017. V. 52. P. 11810.
Долгобородов А.Ю., Кириленко В.Г., Стрелецкий А.Н., Колбанев И.В., Шевченко А.А., Янковский Б.Д., Ананьев С.Ю., Вальяно Г.Е. // Горение и взрыв. 2018. Т. 11. № 3. С. 106.
Goswami R., Chattopadhyay K. // Appl. Phys. Lett. 1996. V. 69. P. 910.
Kellermann G., Craievich A.F. // Phys. Rev. B. 2002. V. 65. P. 134204.
Goswami R., Chattopadhyay K. // Acta Mater. 2004. V. 52. P. 550.
Petkov V., Selbach S.M., Einarsrud M.-A., Grande T., Shastri S.D. // Phys. Rev. Lett. 2010. V. 105. 185 501.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал


