Коллоидный журнал, 2020, T. 82, № 1, стр. 101-105
Синтез и фотокаталитические свойства коллоидных частиц композита хлорид серебра/серебро
Ф. Х. Уракаев 1, 2, *, Н. В. Хан 1, Ж. С. Шалабаев 1, Б. Б. Татыкаев 1, Р. К. Надиров 1, М. М. Буркитбаев 1
1 Институт геологии и минералогии имени В.С. Соболева СО РАН
630090 Новосибирск, просп. Академика Коптюга, 3, Россия
2 Казахский национальный университет им. аль-Фараби
050040
, Алматы, Казахстан
* E-mail: urakaev@igm.nsc.ru
Поступила в редакцию 04.03.2019
После доработки 13.06.2019
Принята к публикации 26.06.2019
Аннотация
Синтезированы композитные наночастицы AgCl/Ag путем механической активации реакции NH4Cl + AgNO3 + zNH4NO3 = (z + 1)NH4NO3 + AgCl с использованием нецелевого конечного продукта (NH4NO3) в качестве разбавителя, где z = 7.22 – параметр разбавления, с последующим частичным фотовосстановлением AgCl до Ag (Ag+ до Ag0). Методами рентгенофазового анализа, просвечивающей электронной микроскопии и спектрофотометрии поглощения в диапазоне длин волн 200−1000 нм установлено образование нанокристаллов Ag (размером примерно 7 нм) на поверхности 40-нм наночастиц AgCl. Такие композитные частицы AgCl/Ag проявляют высокую каталитическую активность при фоторазложении красителя метиленового синего в водном растворе.
ВВЕДЕНИЕ
Наночастицы (НЧ) серебра [1, 2] и их “композиты” с НЧ галогенидов серебра (AgX/Ag, X = Cl, Br, I) востребованы в различных областях науки и техники [3–6]. В настоящей работе мы остановимся только на композитных НЧ (КНЧ) AgCl/Ag [7–17]. Упомянем, ограничившись недавними публикациями, и о наличии их “гибридов” с другими веществами, находящимися в наноструктурированном состоянии: графитом [18], графеном [5, 19, 20] и g-C3N4 [21], оксидами (TiO2 [22, 23], Cu2O [24], ZnO [25], WO3 [26–28]), двойными оксидами (CaTiO3 [29], LaFeO3 [30], ZnFe2O4 [31]) и MoS2 [32]. Есть композиты и более сложных состава и структуры: Ag/AgCl/Bi6O4(OH)4(NO3)6 · H2O [33] и Ag/AgCl/Bi6O4.46(OH)3.54(NO3)5.54 [34], (CuC10H26N6)3(PW12O40)2/AgCl@Ag [35], Ag/AgCl/ZIF-8 [36], Ag/AgCl/вискоза [6] и пленка хитина–Ag@AgCl [37].
Отметим, что в [1] НЧ серебра и препараты с антибиотиками и другими соединениями на их основе (типа колларгола [2]) предлагается “возродить” в качестве лечебных средств после многолетнего забвения.
Одним из важнейших свойств НЧ серебра и содержащих их веществ является плазмоный резонанс, проявляющийся в ярко выраженном локальном максимуме в спектральной зависимости коэффициента экстинкции [38, 39]. В настоящее время созданию новых типов таких материалов уделяется особое внимание (см., в частности, получение плазмонных КНЧ SiO2@/Ag декорированием in situ поверхности синтезированных мезопористых частиц кремнезема серебром [40]). Методы синтеза и свойства НЧ серебра систематизированы в [1, 2, 39].
Синтез нанокомпозитов AgCl/Ag многообразен. Их получают методами осаждения AgCl [19, 32] или пропитки [34] с одновременным или последующим фотовосстановлением ионов Ag+ до Ag0 [3–6, 8, 18, 21, 22, 26, 27, 29, 30, 35, 37]. Восстановление также проводится полиолами [7, 17, 19, 20, 30, 31, 33, 34, 36], термическим путем [8, 25, 28], с использованием растительного сырья [9–12, 14, 25], дрожжевых клеток [13], грибов [15] и синтезированных бактериями двух типов фермента β-глюкозидазы [16]. Отметим и возможность применения цетилтриметиламмония хлорида [5] и проведения процесса окисления пленок серебра с помощью FeCl3 [23] или CuCl2 [24].
Области применения КНЧ AgCl/Ag и их перечисленных выше “гибридов” весьма разнообразны. В основном они используются в качестве фотокатализаторов для деградации красителей, органических и других загрязняющих веществ. Среди них метиленовый синий [3, 6, 17, 22, 30], метилоранж [4, 8, 23, 24, 27, 33, 37] и родамин B [18, 21, 25–28, 31], 2,4-дихлорфенол [4, 35], нитрофенол [5, 10], фенол [18, 22], бисфенол A [31], тетрациклин [21, 35] и Cr(VI) [21]. Они востребованы и как активное антибактериальное средство [6, 9–12, 14, 15, 34] и при лечении карцином [9, 10], а также используются для получения водорода [29, 35], в качестве рабочих элементов сенсоров [20, 32] и даже стимуляторов всхожести семян [15]. В [13, 16] сообщается о возможности синтеза КНЧ AgCl/Ag в промышленных масштабах для последующих технологических применений.
Ранее мы сообщали о возможности механохимического синтеза НЧ AgCl [41] и AgBr с успешной попыткой получения нанокомпозитного фотокатализатора AgBr/Ag [3]. В настоящей работе этот подход применен для синтеза КНЧ AgCl/Ag, и проведены спектрофотометрические исследования их фотокаталитических свойств в реакции деградации красителя метиленового синего.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез НЧ AgCl, как и в [41], осуществляли методом разбавления нецелевым конечным продуктом (NH4NO3) механически активируемой реакции NH4Cl + AgNO3 + zNH4NO3 = (z + + 1)NH4NO3 + AgCl, где z = 7.22 [41] – коэффициент разбавления. Теоретические и экспериментальные аспекты механохимического способа получения НЧ методом разбавления (или методом МакКормика – его первооткрывателя) детально рассмотрены в обзоре [42]. Этот метод базируется на следующих положениях. Во-первых, целевой продукт (в данном случае AgCl) должен быть термически стабилен или нерастворим, например, в воде; тогда нецелевой продукт должен быть водорастворимым (может быть отмыт водой [3]) или, как в случае NH4NO3, может быть удален путем его термического разложения [41]. Во-вторых, добавление в реакционную смесь NH4Cl + + AgNO3 продукта реакции NH4NO3 будет препятствовать агрегации первоначально образующихся кластеров AgCl или, иначе говоря, будет способствовать стабилизации НЧ AgCl в матрице нецелевого продукта механически активируемой реакции.
Механическую активацию (МА) исходной шихты (навеска m = 10 г) проводили в шаровой планетарной мельнице Pulverissette 6 с использованием фурнитуры из карбида вольфрама (плотность ρ = 14.3 г/см3, твердость по Моосу 9) для исключения натира материала мелющих тел.
Объем барабана составлял 250 мл, число шаров N = 50, их диаметр D = 1 см, вес шаровой загрузки mb = πD3Nρ/6 = 370 г и отношение mb/m = 37. МА осуществляли при частоте вращения водила 420 об./мин в течение 20 мин.
Рентгенофазовый анализ (РФА) образцов проводили на дифрактометре D8 ADVANCE (Bruker, Германия), используя монохроматизированное излучение меди, при напряжении 40 кВ и токе 40 мА; шаг сканирования составлял 2θ = 0.02°, длительность времени измерения на каждом шаге – 1 с.
Просвечивающую электронную микроскопию (ПЭМ) образцов выполняли на приборе JEM 1011 (JEOL, Япония), оснащенном цифровой фотокамерой Morada (OLYMPUS, Япония), при напряжении 100 кВ. Полученные в результате МА образцы (10 мг) помещали в ампулу с гексаном (3 мл), перемешивали и 1 каплю такой суспензии наносили на медные сетки с коллодиевым покрытием.
Спектры поглощения образцов коллоидных растворов измеряли на однолучевом спектрофотометре СФ-56 (Россия) в диапазоне 200−1000 нм; образцом сравнения служила использованная для их приготовления вода. Процедура проведения измерений была следующей. Продукт МА (500 мг) вносили в дистиллированную воду (500 мл) с целью получения коллоидного раствора AgCl [41]. Образец этой дисперсии сразу использовали для быстрой (в течение примерно 1 мин) съемки спектра поглощения. Затем остаток суспензии облучали ксеноновой лампой мощностью 300 Вт в течение 4 ч и измеряли спектр поглощения уже этого образца (было установлено, что 4-х ч достаточно для обнаружения линий серебра по данным РФА, сравните также с [4]).
Из остатка облученной суспензии 10-минутным осаждением на центрифуге Hettich Mikro 220R (5000 об./мин) отделяли целевые КНЧ AgCl/Ag. После 12-часовой сушки при 60°C их образцы исследовали методами РФА и ПЭМ. Таким же способом отделяли НЧ AgCl от продуктов МА и хранили их в темноте.
Фотокаталитическую активность НЧ AgCl и КНЧ AgCl/Ag оценивали по методике [3]. Для этого 40 мг образцов тех или иных частиц вносили в 40 мл водного раствора красителя метиленового синего (10 мг/л). Полученные дисперсии перемешивали в темноте магнитной мешалкой в течение 1 ч. Затем образцы этих дисперсий облучали видимым светом неоновых трубок Sylvania LuxLine FHO T5 с интенсивностью 4 мВт/см, отбирая пробы каждые 20 мин. Облученные образцы сразу центрифугировали (4000 об./мин, 2 мин) для удаления частиц. Измерения оптической плотности A полученных растворов на длине волны 485 нм позволяло определить степень фоторазложения метиленового синего в каждом образце под действием как НЧ AgCl, так и КНЧ AgCl/Ag и проследить за кинетикой этого. Для контроля полученных результатов проводили также опыты по разложению красителя в водном растворе в темноте в присутствии КНЧ AgCl/Ag и при его освещении в отсутствие этих композитных частиц.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
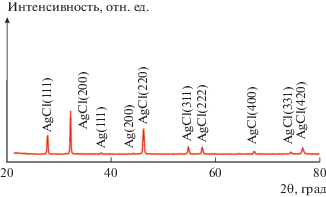
Рентгенофазовый анализ КНЧ AgCl/Ag, полученных облучением НЧ AgCl ксеноновой лампой, показал наличие кубической фазы AgCl (параметр решетки a = 5.5463 Å) и слабых дифракционных пиков серебра при значениях 2θ, равных примерно 38° и 44° (рис. 1). По данным РФА трудно установить состав КНЧ и, как следствие, определить выход реакции фотовосстановления Ag+ до Ag0 при облучении НЧ AgCl ксеноновой лампой. По данным же ПЭМ можно говорить о примерно 3%-ном содержании Ag в КНЧ AgCl/Ag, что находится в пределах ошибки измерений методом РФА.
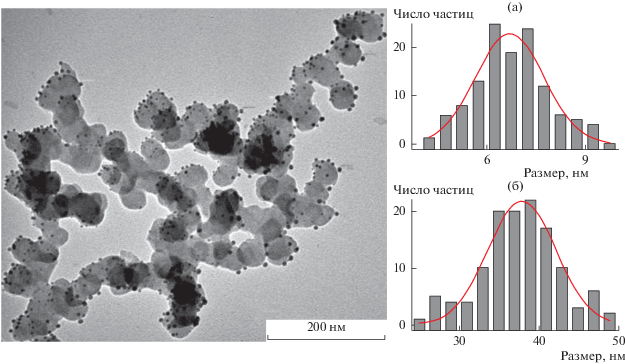
ПЭМ-анализ образца КНЧ AgCl/Ag (рис. 2) показал, что в результате восстановления ионов Ag+ до Ag0 в частицах водной дисперсии AgCl, облучаемой ксеноновой лампой, образуются НЧ Ag со средним диаметром около 7 нм (а), “ассоциированные” (связанные) с поверхностью материнских НЧ AgCl со средним диаметром примерно 40 нм (б). В этой связи уместно сравнить снимок на рис. 2, например, с ПЭМ-снимками в [35], на которых также нет изолированных частиц серебра.
Рис. 2.
ПЭМ-снимок образца КНЧ AgCl/Ag и соответствующие распределения по размерам наночастиц Ag (а) и AgCl (б).
Так как ПЭМ-изображения [41] необлученных МА-образцов AgCl не показали наличия НЧ серебра, можно сделать вывод, что их образование вызвано именно светом ксеноновой лампы.
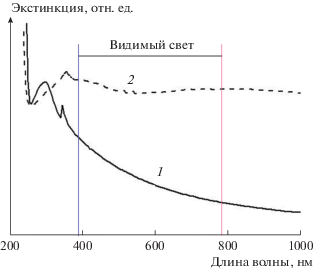
На рис. 3 представлены спектры поглощения НЧ AgCl (1) и КНЧ AgCl/Ag (2) в ультрафиолетовом и видимом диапазонах длин волн. Видно, что максимумы их поглощения находятся в ближней УФ-области спектра. Для НЧ AgCl наблюдаются два максимума поглощения − первый при 299 нм и второй при 346 нм, а для КНЧ AgCl/Ag – только один ярко выраженный максимум при 357 нм.
Максимумы поглощения при 299 и 346 нм (спектр 1) можно приписать, следуя, например, [4], смещенным в длинноволновую область спектра прямым (230 нм) и непрямым (301 нм) экситонным переходам в AgCl. Максимум поглощения КНЧ AgCl/Ag при 357 нм (спектр 2) также сдвинут в сторону более длинных волн относительно его положения (319 нм), зарегистрированного в [4]. С другой стороны, для свободных НЧ серебра [2, 38] максимум поглощения располагается вблизи 400 нм, т.е. при значительно большей длине волны, чем для КНЧ AgCl/Ag (смотрите рис. 3 и, например, данные [4, 17, 35]). Одно из объяснений сдвига максимума поглощения НЧ серебра в составе композитных частиц в сторону коротких волн состоит в их сильной связи с AgCl-матрицей [35]. Более того, говорить о количественном согласии полученных нами спектральных данных с результатами других работ нет особого смысла, поскольку такового согласия не существует и между результатами самих этих работ (смотрите [4–6, 8–10, 12–14, 17, 35]).
Наличие еще двух слабо выраженных максимумов поглощения КНЧ AgCl/Ag в видимой области спектра [4, 17] подробно обсуждается в [17]. В нашем же случае, значения экстинкции для КНЧ для AgCl/Ag, начиная с ее максимального значения при 346 нм, изменяются (уменьшаются) не более чем на 18% вплоть до 1000 нм (рис. 3, спектр 2), в то время как для НЧ AgCl изменение (плавный спад) экстинкции составляет 83% (рис. 3 спектр 1).
В [4, 17] широкие полосы поглощения в видимой области приписыватся плазмонному резонансу (агрегированных) НЧ серебра. Поэтому большое и практически неизменное значение экстинции для КНЧ AgCl/Ag (рис. 3) может свидетельствовать об их потенциальной очень высокой фотокаталитической активности. Отметим, что основное отличие наших КНЧ AgCl/Ag от исследовавшихся другими авторами состоит в наличии остаточных микроискажений решетки AgCl, возникших в результате МА [41].
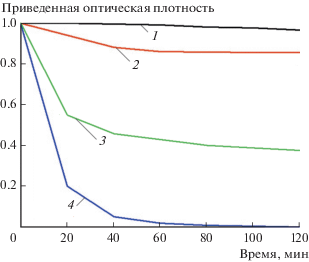
Данные о фотокаталитической активности КНЧ AgCl/Ag и соответствующих контрольных опытов представлены на рис. 4. Видно, что метиленовый синий не подвержен сколько-нибудь существенному разложению в водном растворе при воздействии видимого света неоновых трубок в отсутствие КНЧ AgCl/Ag (кривая 1), т.е. фотоиндуцированное разложение красителя в этом случае не происходит. Незначительное разложение метиленового синего без облучения его раствора видимым светом имеет место в присутствии КНЧ AgCl/Ag (кривая 2). В то же время, наличие КНЧ AgCl/Ag в растворе красителя приводит к его фотодеструкции на 80% уже за первые 20 мин действия видимого света, а за 120 мин достигается полное разложение (кривая 4). Отметим, что и НЧ AgCl также проявляют фотокаталитические свойства (кривая 3), хотя и в заметно меньшей степени, чем КНЧ AgCl/Ag. Укажем также, что скорость разложения красителя под действием КНЧ AgCl/Ag значительно выше, чем в присутствии КНЧ AgBr/Ag [2, 4].
ЗАКЛЮЧЕНИЕ
Разработан двухэтапный метод синтеза композитных наночастиц фотокатализатора AgCl/Ag. На первом этапе механохимической активацией системы NH4Cl–AgNO3–NH4NO3 получены НЧ AgCl со средним размером 40 нм. Затем частичным фотовосстановлением AgCl (ионов Ag+) до атомов Ag0 синтезированы НЧ серебра размером около 7 нм, связанные с материнскими частицами AgCl. КНЧ AgCl/Ag сильно и равномерно поглощают свет в видимой области. Это обеспечивает их высокую каталитическую активность при фоторазложении красителя метиленового синего под действием света неоновых трубок.
Список литературы
Möhler J.S., Sim W., Blaskovich M.A.T., Cooper M.A., Ziora Z.M. // Biotechnol. Adv. 2018. V. 36. P. 1391.
Крутяков Ю.А., Кудринский А.А., Оленин А.Ю., Лисичкин Г.В. // Успехи химии. 2008. Т. 77. С. 242.
Уракаев Ф.Х., Татыкаев Б.Б., Буркитбаев М.М., Бахадур А.М., Уралбеков Б.М. // Коллоид. журн. 2016. Т. 78. С. 501.
Li Q., Chang S., Wu D., Bao S., Zeng C., Nasir M., Tian B., Zhang J. // Res. Chem. Intermed. 2018. V. 44. P. 4651.
Attia Y.A., Mohamed Y.M.A. // Appl. Organomet. Chem. 2019. V. 33. P. e4757.
Rehan M., Khattab T.A., Barohum A., Gätjen L., Wilken R. // Carbohydr. Polym. 2018. V. 197. P. 227.
Chen S., Carey J.L., Whitcomb D.R., Bühlmann P., Penn R.L. // Cryst. Growth Des. 2018. V. 18. P. 324.
Di A., Wang Y., Chen G. // Funct. Mater. Lett. 2018. V. 11. P. 1 850 006.
Chankaew C., Somsri S., Tapala W., Mahatheeranont S., Saenjum C., Rujiwatra A. // Particuology. 2018. V. 40. P. 160.
Konvičková Z., Holišová V., Kolenčík M., Niide T., Kratošová G., Umetsu M., Seidlerová J. // Colloid Polym. Sci. 2018. V. 296. P. 677.
Kota S., Dumpala P., Anantha R.K., Verma M.K., Kandepu S. // Sci. Rep. 2017. V. 7. P. 11566.
Patil M.P., Seo Y.B., Kim G.-D. // Microb. Pathog. 2018. V. 116. P. 84.
Alamri S.A.M., Hashem M., Nafady N.A., Sayed M.A., Alshehri A.M., El-Alshaboury G.A. // J. Microbiol. Biotechnol. 2018. V. 28. P. 917.
Panchal P., Malik R., Paul D.R., Meena P., Tomer V.K., Nehra S.P. // J. Nanosci. Nanotechnol. 2019. V. 19. P. 5249.
Spagnoletti F.N., Spedalieri C., Kronberg F., Giacometti R. // J. Environ. Manage. 2019. V. 231. P. 457.
Araújo J.N., Tofanello A., da Silva V.M., Sato J.A.P., Squina F.M., Nantes I.L., Garcia W. // Int. J. Biol. Macromol. 2017. V. 102. P. 84.
Gaikwad S.H., Koratti A., Mukherjee S.P. // Appl. Surf. Sci. 2019. V. 465. P. 413.
Gou J., Li X., Zhang H., Guo R., Deng X., Cheng X., Xie M., Cheng Q. // J. Ind. Eng. Chem. 2018. V. 59. P. 99.
Wang X., Han Q., Yu N., Wang T., Wang C., Yang R. // Colloids Surf. B. 2018. V. 162. P. 296.
Tang J., Xiong P., Cheng Y., Chen Y., Peng S., Zhu Z.-Q. // Biosens. Bioelectron. 2019. V. 130. P. 125.
Xu H., Chang Y., Shen X., Liu Z., Zhu B., Macharia D.K., Wang Z., Chen Z., Zhang L. // J. Colloid Interface Sci. 2019. V. 543. P. 25.
Tian W., Wu H., Su C., Huang Y., Zhao W., Yang X. // J. Photochem. Photobiol. A. 2018. V. 350. P. 122.
Wang Y., Zhang M., Li J., Yang H., Gao J., He G., Sun Z. // Appl. Surface Sci. 2019. V. 476. P. 84.
Lou S., Wang W., Wang L., Zhou S. // J. Alloy Compd. 2019. V. 781. P. 508.
Cai A., Guo A., Du L., Qi Y., Wang. // Mater. Res. Bull. 2019. V. 103. P. 225.
Chai C., Liu J., Wang Y., Zhang X., Duan D., Fan C., Wang Y. // Appl. Phys. A. 2019. V. 125. P. 96.
Fang H., Cao X., Yu J., Lv X., Yang N., Wang T., Jiang W. // J. Mater. Sci. 2019. V. 54. P. 286.
Senthil R.A., Osman S., Pan J., Sun M., Khan A., Yang V., Sun Y. // Colloids Surf. A. 2019. V. 567. P. 171.
Jiang Z., Pan J., Wang B., Li C. // Appl. Surf. Sci. 2019. V. 436. P. 519.
Gao X., Shang Y., Liu L., Nie W., Fu F. // J. Phys. Chem. Solids. 2019. V. 127. P. 186.
Liu Q., Xu Y., Wang J., Xie M., Wei W., Huang L., Xu H., Song Y., Li H. // Colloids Surf. A. 2018. V. 553. P. 114.
Li Y., Dai H., Feng N., Xie X., Zhang J., Li W. // Mater. Express. 2019. V. 9. P. 59.
Zhao M., Yuan Q., Zhang H., Li C., Wang Y., Wang W. // J. Alloy Compd. 2019. V. 782. P. 1049.
Zhao M., Hou X., Lv L., Li C., Wang Y., Meng A. // Mater. Sci. Eng. C. 2019. V. 98. P. 83.
Chen S., Li F., Li T., Cao W. // J. Colloid Interface Sci. 2019. V. 547. P. 50.
Fan G., Luo J., Guo L., Lin R., Zheng X., Snyder S.A. // Chemosphere. 2018. V. 209. P. 44.
Yi C., Liu J., Meng D., Lv J., Zhang X., Shu Y., Su S., Zhu J. // Composites. B. 2019. V. 160. P. 677.
Каленский А.В., Звеков А.А., Никитин А.П., Ананьева М.В., Адуев Б.П. // Оптика и спектроскопия. 2015. Т. 118. С. 1012.
Siddiqi K.S., Husen A., Rao R.A.K. // J. Nanobiotechnol. 2018. V. 16. P. 14.
Дементьева О.В., Филиппенко М.А., Громан К.Э., Рудой В.М. // Коллоид. журн. 2012. Т. 74. С. 460.
Уракаев Ф.Х., Буркитбаев М.М., Татыкаев Б.Б., Уралбеков Б.М. // Коллоид. журн. 2015. Т. 77. С. 648.
Urakaev F.Kh. // Int. J. Comput. Mater. Sci. Surf. Eng. 2011. V. 4. P. 347.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал